Область техники, к которой относится изобретение
Настоящее изобретение относится к фармацевтической композиции для перорального введения, с улучшенным всасыванием энзалутамида при пероральном введении.
Более конкретно, настоящее изобретение относится к фармацевтической композиции для перорального введения, содержащей энзалутамид и поливиниловый спирт.
Уровень техники
В последних исследованиях по поиску новых лекарственных средств кандидатами на разработку часто становятся лекарства, плохо растворимые в воде. В альтернативных вариантах также существует необходимость в улучшении медицинских возможностей за счет раннего обеспечения терапевтических средств в клинических условиях, и общая технология солюбилизации остается важной проблемой.
Энзалутамид является ингибитором сигнального пути андрогенных рецепторов. Он имеет химическое название 4-{3-[4-циано-3-(трифторметил)фенил]-5,5-диметил-4-оксо-2-сульфанилиденимидазолидин-1-ил}-2-фтор-N-метилбензамид и представлен следующей химической структурной формулой:
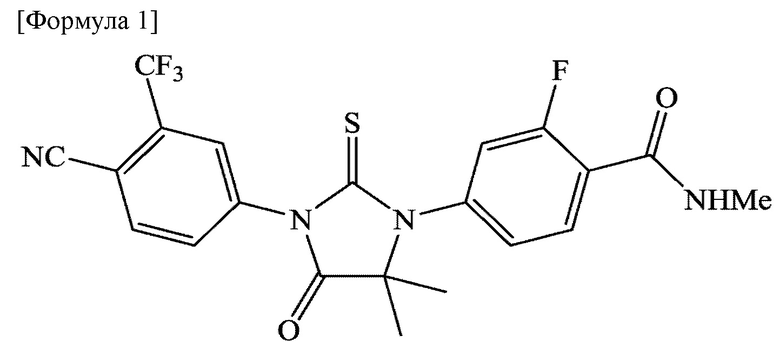
Энзалутамид известен как активный ингредиент для использования в терапевтических агентах для лечения метастатического кастрационно-резистентного рака простаты или тому подобного (Патентная литература 1). Энзалутамид выпускается на рынке в виде мягких капсул («XTANDI» (зарегистрированный товарный знак)), содержащих 40 мг энзалутамида на капсулу и фармацевтические добавки. Согласно инструкции по применению продукта (Непатентная литература 1) взрослым перорально вводят 160 мг один раз в сутки, и при этом указано, что принимают капсулы с продольным размером приблизительно 21 мм и поперечным размером приблизительно 10 мм и в одной дозе принимают четыре капсулы. В частности, одна таблетка приемлемого размера, содержащая предопределенное количество энзалутамида и обладающая целесообразной и хорошей растворимостью и/или стабильностью при растворении и всасыванием при пероральном введении, была бы полезна в качестве подходящей замены этих мягких капсул.
В качестве способов солюбилизации энзалутамида известны способ аморфизации энзалутамида и способ приготовления твердой дисперсии энзалутамида с носителем (Патентная литература 2-4).
Список цитируемой литературы
Патентная литература
Патентная литература 1 - WO 2006/124118
Патентная литература 2 - WO 2014/043208
Патентная литература 3 - WO 2014/041487
Патентная литература 4 - WO 2014/167428
Непатентная литература
Непатентная литература 1 - Инструкция по применению «XTANDI» (зарегистрированный товарный знак), Капсула 40 мг
Сущность изобретения
Техническая задача
Даже в настоящее время разработка составов для улучшения растворимости энзалутамида и повышения его всасывания при пероральном введении независимо от pH является важной технической проблемой для обеспечения эффективности лекарственного средства, и в этом вопросе есть пространство для дальнейших улучшений.
Задачей, решаемой в настоящем изобретении, является создание фармацевтической композиции для перорального применения, в которой независимо от рН улучшены растворимость и/или свойства растворения энзалутамида, и поддерживается состояние пересыщения. Другой целью настоящего изобретения является создание фармацевтической композиции для перорального применения, характеризующейся улучшенным всасыванием при пероральном введении.
Решение задачи
Получая твердую дисперсию с использованием энзалутамида и поливинилового спирта (далее иногда называемого ПВС), можно добиться pH-независимой солюбилизации и/или растворения энзалутамида, и можно поддерживать состояние его пересыщения, и, кроме того, улучшается его биодоступность при пероральном введении в живой организм.
Настоящее изобретение относится к:
[1] фармацевтической композиции для перорального применения, включающей энзалутамид и поливиниловый спирт;
[2] фармацевтической композиции для перорального применения по [1], где поливиниловый спирт имеет степень омыления 30 мол. % или более и 99 мол. % или менее;
[3] фармацевтической композиции для перорального применения по [1] или [2], где поливиниловый спирт имеет степень полимеризации 50 или более, и 600 или менее;
[4] фармацевтической композиции для перорального применения по любому из [1]-[3], содержащей твердую дисперсию, включающую энзалутамид и поливиниловый спирт;
[5] фармацевтической композиции для перорального применения по любому из [1]-[4], дополнительно содержащей вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи;
[6] фармацевтической композиции для перорального применения по [5], где вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, представляет собой поливинилпирролидон и/или сополивидон;
[7] фармацевтической композиции для перорального применения по любому из [1]-[6], дополнительно содержащей со-дезинтегрант;
[8] фармацевтической композиции для перорального применения по [7], в которой со-дезинтегрант представляет собой соединение или два или более соединений, выбранных из группы, состоящей из хлорида калия, хлорида натрия, хлорида магния и дигидрофосфата калия;
[9] фармацевтической композиции для перорального применения по [7] или [8], в которой со-дезинтегрант представляет собой хлорид калия;
[10] фармацевтической композиции для перорального применения по любому из [1]-[9], дополнительно включающей дезинтегрант;
[11] фармацевтической композиции для перорального применения по [10], где дезинтегрант представляет собой соединение, или два или более соединений, выбранных из группы, состоящей из кросповидона и низкозамещенной гидроксипропилцеллюлозы;
[12] фармацевтической композиции для перорального применения по [10] или [11], где дезинтегрант представляет собой кросповидон;
[13] фармацевтической композиции для перорального применения по любому из [1]-[12], где фармацевтическая композиция представляет собой таблетку;
[14] фармацевтической композиции по любому из [1]-[13], где энзалутамид является аморфным;
[15] способу получения фармацевтической композиции для перорального введения, включающей энзалутамид и поливиниловый спирт,
[16] способу получения фармацевтической композиции для перорального применения по [15], включающему этап приготовления твердой дисперсии, содержащей энзалутамид и поливиниловый спирт;
[17] способу получения фармацевтической композиции для перорального применения по [16], в котором твердую дисперсию получают способом экструзии горячего расплава;
[18] способу получения фармацевтической композиции для перорального применения по [16], в котором твердую дисперсию получают способом с применением растворителя; и
[19] использованию вещества, имеющего функциональную группу, способную функционировать в качестве акцептора водородной связи, в производстве фармацевтической композиции для перорального применения, содержащей энзалутамид и поливиниловый спирт.
Выгодные эффекты, обеспечиваемые изобретением
Согласно настоящему изобретению может быть обеспечена фармацевтическая композиция для перорального применения, в которой, независимо от рН, улучшены растворимость и/или свойства растворения энзалутамида, и сохраняется его пересыщение. Кроме того, может быть обеспечена фармацевтическая композиция для перорального применения, в которой увеличены показатели биодоступности и скорости всасывания энзалутамида.
Краткое описание чертежей
Фиг. 1 представляет собой график, показывающий результаты испытания на осаждение в Экспериментальном примере 1.
Фиг. 2 представляет собой график, показывающий результаты испытания на осаждение в Экспериментальном примере 2.
Описание вариантов осуществления изобретения
Используемый в настоящем изобретении термин «для улучшения растворимости» означает, что растворимость, растворенная концентрация или уровень растворения энзалутамида в растворителе увеличиваются. Более конкретно, в одном варианте осуществления, по отношению к тому, что растворимость энзалутамида в воде (20±5°С) составляет 2 мкг/мл, когда её оценивают, например, в тесте на растворение согласно Экспериментальному примеру 3, Экспериментальному примеру 4, Экспериментальному примеру 5, Экспериментальному примеру 8, Экспериментальному примеру 11, Экспериментальному примеру 13, Экспериментальному примеру 15 или Экспериментальному примеру 16, описанным ниже, данный термин определяется как эффект улучшения растворенной концентрации в 5 раз или более, в 10 раз или более в одном варианте осуществления, и в 20 раз или более в другом варианте осуществления.
Используемый в настоящем изобретении термин «для улучшения свойств растворения» означает, что улучшается уровень растворения энзалутамида из фармацевтической композиции. Более конкретно, в одном варианте осуществления, при измерении в тесте растворения согласно Экспериментальному примеру 3, Экспериментальному примеру 4, Экспериментальному примеру 5, Экспериментальному примеру 8, Экспериментальному примеру 11, Экспериментальному примеру 13, Экспериментальному примеру 15 или Экспериментальному примеру 16, описанным ниже, данный термин определяется как уровень растворения через 10 минут после начала испытания составляет 60% или более, а в одном варианте осуществления - 80% или более.
Используемый в настоящей заявке термин «для поддержания пересыщения» означает, что энзалутамид растворен в растворе в количестве, превышающем растворимость энзалутамида. Более конкретно, в одном варианте осуществления, когда фармацевтическую композицию, содержащую энзалутамид, оценивают с помощью теста осаждения согласно Экспериментальному примеру 1 или Экспериментальному примеру 2, описанным ниже, то этот термин определяют как то, что время, в течение которого изменение уровня растворения энзалутамида в фармацевтической композиции находится в пределах 10% по отношению к уровню растворения в начале испытания, составляет 30 минут или более, в одном варианте осуществления - 60 минут или более, и в другом варианте осуществления - 90 минут или более.
Используемый в настоящей заявке термин «для улучшения всасывания при пероральном введении» означает, в одном варианте осуществления, что параметры всасывания при пероральном введении, скорости всасывания или ФК соответствуют или превосходят аналогичные параметры капсулы XTANDI (зарегистрированный товарный знак), которая является продуктом из уровня техники, у испытуемого субъекта, такого как собака, человек или тому подобное. В частности, это означает наличие свойств, соответствующих или превосходящих свойства капсулы XTANDI (зарегистрированный товарный знак) в одной дозе.
Более конкретно, в настоящем изобретении определено, что, например, значения Cmax или AUC у собаки составляют 0,8 или более, предпочтительно 0,9 или более и более предпочтительно 1 или более от соответствующего значения, полученного для капсулы XTANDI (зарегистрированный товарный знак).
Состояние улучшения всасывания при пероральном введении означает, что лекарственное средство в растворе находится в состоянии, при котором лекарство легко всасывается, таком как аморфное состояние или переходные состояния, например, согласно оценке с использованием рентгеновской дифракции, комбинационного рассеяния, инфракрасного поглощения, терагерцевой спектроскопии, или тому подобного.
Используемый в настоящем изобретении термин «твердая дисперсия» означает дисперсию, включающую энзалутамид и поливиниловый спирт, где бόльшая часть энзалутамида существует в бесформенном виде. Используемый здесь термин «бесформенный» означает аморфные или переходные состояния. Бесформенный энзалутамид существует в виде твердого раствора, который гомогенно распределен в поливиниловом спирте. Используемый в настоящей заявке термин «большинство» («бόльшая часть») означает, что при приготовлении дисперсии на кристалл энзалутамида приходится 40% или менее, предпочтительно 20% или менее. В другом варианте осуществления это означает, что количество кристаллов энзалутамида составляет 40% или менее, предпочтительно 20% или менее, и более предпочтительно 10% или менее при измерении методом рентгеновской порошковой дифракции, дифференциальной сканирующей калориметрии (ДСК) или любыми другими стандартными средствами количественного анализа.
Используемый в настоящем изобретении термин «степень омыления» означает величину омыления, определяемую способом измерения, описанным в Японской Фармакопее, семнадцатое издание, или способом измерения, обеспечивающим скоррелированые с ним результаты, и может быть рассчитана по следующему уравнению (1). В связи с этим необходимо, чтобы способ измерения имел коэффициент корреляции 0,5 или более, и 0,6 или более в одном варианте осуществления со способом измерения, описанным в Японской фармакопее, семнадцатое издание.
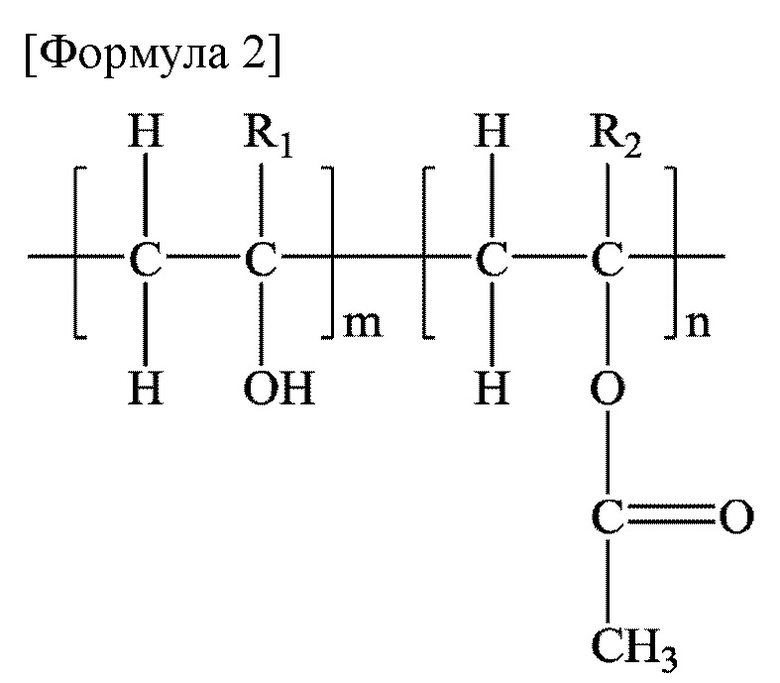
Степень омыления = m/(m + n) × 100 (1)
(m: количество гидроксильных групп; n: количество ацетильных групп)
Используемый в настоящем изобретении термин «степень полимеризации» означает «среднюю степень полимеризации» и определяется как значение, рассчитанное на основе величины вязкости при оценке в соответствии с разделом «Вспомогательные вещества» Японской Фармакопеи, или как значение молекулярной массы, измеренной гель-фильтрацией или аналогичным способом, или значение, измеренное в соответствии с методом измерения, дающим скоррелированные с ними результаты. В альтернативном варианте этот термин определяется как значение, измеренное с помощью (4) Метода измерения средней степени полимеризации в JIS K6726 «Методы исследования поливинилового спирта», или значение, измеренное в соответствии с методом измерения, дающим скоррелирование с ним результаты. В связи с этим необходимо, чтобы метод измерения, скоррелированный с методом измерения значения вязкости при оценке в соответствии с разделом «Вспомогательные вещества» Японской Фармакопеи, или гель-фильтрацией или аналогичными методами, представлял собой метод измерения, имеющий коэффициент корреляции 0,5 или более, и в одном варианте осуществления - 0,6 или более, по отношению к способу измерения значения вязкости при оценке в соответствии с разделом «Вспомогательные вещества» Японской Фармакопеи, или гель-фильтрацией или аналогичным методом. Кроме того, необходимо, чтобы метод измерения, скоррелированный с (4) Методом измерения средней степени полимеризации в JIS K6726 «Методы испытаний для поливинилового спирта», представлял собой метод измерения, имеющий коэффициент корреляции 0,5 или более, и в одном варианте осуществления - 0,6 или более, с (4) Методом измерения средней степени полимеризации в JIS K6726 «Методы испытаний для поливинилового спирта».
Используемый в настоящем изобретении термин «стабильный» означает устойчивость, например, к нагреванию, свету, температуре и/или влажности. Например, после того, как фармацевтической композиции дают отстояться в заданных условиях, это термин определяют как вариант осуществления, где процентное содержание максимального родственного энзалутамиду вещества в фармацевтической композиции не превышает заданного значения, или этот термин определяют как вариант осуществления, где, даже если твердую дисперсию получают нагреванием и плавлением, процентное содержание максимального родственного энзалутамиду вещества, содержащегося в фармацевтической композиции, не превышает заданного значения.
Например, в одном варианте осуществления этот термин означает, что процентное содержание максимального родственного энзалутамиду вещества после хранения при 70°C в течение 9 дней (в герметичном виде) составляет не более 0,5%, и в одном варианте осуществления - не более 0,3%.
В одном варианте осуществления этот термин означает, что процентное содержание максимального родственного энзалутамиду вещества после хранения при 25°C и 60% относительной влажности (в дальнейшем иногда упоминается как 25°C, ОВ 60%) в течение 1 месяца, при 25°C 60% ОВ в течение 3 месяцев, при 25°С, 60% ОВ в течение 6 месяцев, при 40°С и 75% относительной влажности (в дальнейшем иногда обозначается как 40°С, 75% ОВ) в течение 1 месяца, при 40°С, 75% ОВ в течение 3 месяцев или при 40ºС, 75% ОВ в течение 6 месяцев, составляет не более 0,5%, и в одном варианте осуществления - не более 0,3%.
Используемый в настоящем изобретении термин «максимальное родственное вещество» означает наиболее представленное родственное вещество из родственных энзалутамиду веществ. Более конкретно, например, когда количество каждого родственного вещества, содержащегося в фармацевтической композиции, измеряют методом высокоэффективной жидкостной хроматографии (далее - метод ВЭЖХ), то максимальное родственное вещество определяют как родственное вещество, характеризующееся наибольшей площадью пика из полученных родственных веществ.
Термин «количество максимального родственного вещества», используемый в данном изобретении, определяется как процент максимального родственного вещества по отношению к общей площади пиков энзалутамида и его родственных веществ, при измерении площади пика максимального родственного вещества, содержащегося в фармацевтической композиции, методом ВЭЖХ.
Энзалутамид является плохо растворимым в воде лекарственным средством, имеющим растворимость в воде 2 мкг/мл (20±5°С). Можно добиться хорошей растворимости и/или хороших свойств растворения с использованием технологии по настоящему изобретению. Кроме того, с использованием технологии по настоящему изобретению можно добиться хорошего всасывания при пероральном введении.
Доза энзалутамида может быть надлежащим образом определена в зависимости от конкретного случая, принимая во внимание, например, симптомы заболевания, возраст пациента, расу, пол или тому подобное.
Суточная доза составляет, например, приблизительно от 0,001 мг/кг до 100 мг/кг, от 0,01 мг/кг до 100 мг/кг в одном варианте осуществления, от 1 мг/кг до 10 мг/кг в еще одном варианте осуществления, при однократном введении или разделении на две-четыре дозы в сутки. Каждый из указанных нижних пределов и каждый из указанных верхних пределов при желании можно комбинировать произвольным образом.
Содержание энзалутамида составляет, например, от 0,05 мг до 10000 мг, от 0,5 мг до 10000 мг в одном варианте осуществления, от 5 мг до 1000 мг в еще одном варианте осуществления, от 10 мг до 200 мг в еще одном варианте осуществления и от 40 мг до 160 мг в еще одном варианте осуществления на фармацевтическую композицию для перорального применения. Каждый из указанных нижних пределов и каждый из указанных верхних пределов при желании можно комбинировать произвольным образом.
Относительное содержание энзалутамида составляет, например, от 1 мас. % до 75 мас. %, от 2 мас. % до 50 мас. % в одном варианте осуществления, от 2 мас. % до 30 мас. % в еще одном варианте осуществления и от 6,7 мас. % до 50 мас. % в еще одном варианте осуществления по отношению к общей массе фармацевтической композиции для перорального введения. Каждый из указанных нижних пределов и каждый из указанных верхних пределов при желании можно комбинировать произвольным образом.
Поливиниловый спирт, используемый в настоящем изобретении, никак конкретно не ограничивается при условии, что он является фармацевтически приемлемым. Степень омыления поливинилового спирта, используемого в настоящем изобретении, составляет, например, от 30 мол. % до 99 мол. %, предпочтительно от 55 мол. % до 85 мол. %, более предпочтительно от 63 мол. % до 82 мол. %, и еще более предпочтительно от 66 мол. % до 80 мол. %. Каждый из указанных выше нижних и верхних пределов (и каждый из нижних и верхних пределов, описанный в Примерах ниже) при желании можно комбинировать произвольным образом.
Степень полимеризации поливинилового спирта, используемого в настоящем изобретении, никак конкретно не ограничивается при условии, что она является фармацевтически приемлемой.
Более конкретно, степень полимеризации составляет, например, менее 2200, 2 или более и менее 2200 в одном варианте осуществления, 10 или более и менее 2200 в еще одном варианте осуществления, 100 или более и менее 2200 в еще одном варианте осуществления, 2 или более и 600 или менее в еще одном варианте осуществления, 10 или более и 600 или менее в еще одном варианте осуществления, 50 или более и 600 или менее в еще одном варианте осуществления, и 100 или более и 500 или менее в еще одном варианте осуществления. Каждый из указанных выше нижних и верхних пределов (и каждый из нижних и верхних пределов, описанный в Примерах ниже) при желании можно комбинировать произвольным образом.
Каждую степень омыления и каждую степень полимеризации при желании можно комбинировать произвольным образом, и в одном варианте осуществления степень омыления и степень полимеризации поливинилового спирта составляют, соответственно, 63 мол. % или более и 82 мол. % или менее, и 50 или более и 600 или менее.
В связи с этим, поливиниловый спирт улучшает растворимость и/или свойства растворения энзалутамида и поддерживает пересыщение энзалутамида. Кроме того, поливиниловый спирт обладает функцией улучшения всасывания энзалутамида при пероральном введении.
Примеры поливиниловых спиртов, используемых в настоящем изобретении, включают:
GOHSENOL (зарегистрированный товарный знак) EG-03P (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 3,0 до 3,8 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 86,5 до 89,0 мол. %);
GOHSENOL (зарегистрированный товарный знак) KL-05 (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 4,0 до 5,0 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 78,5 до 82,0 мол. %),
GOHSENOL (зарегистрированный товарный знак) KL-03 (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 2,8 до 3,4 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 78,5 до 82,0 мол. %);
GOHSENOL (зарегистрированный товарный знак) KP-08R (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 6,0 до 8,0 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 71,0 до 73,5 мол. %);
GOHSENOL (зарегистрированный товарный знак) NK-05R (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 4,5 до 5,5 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 71,0 до 75,0 мол. %);
GOHSENX (зарегистрированный товарный знак) LL-810 (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 7,0 до 10,0 мПа⋅с (10% раствор в смеси метанол/вода (массовое отношение 1/1)), степень омыления: от 45,0 до 51,0 мол. %);
GOHSENX (зарегистрированный товарный знак) LL-920 (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 9,0 до 13,0 мПа⋅с (10% раствор в смеси метанол/вода (массовое отношение 1/1)), степень омыления: от 30,0 до 38,0 мол. %);
GOHSENX (зарегистрированный товарный знак) LL-940 (Nippon Synthetic Chemical Industry Co., Ltd., вязкость: от 20,0 до 28,0 мПа⋅с (10% раствор в смеси метанол/вода (массовое отношение 1/1)), степень омыления: от 34,0 до 41,0 мол. %);
POVAL (зарегистрированный товарный знак) JR-05 (JAPAN VAM & POVAL CO., LTD., вязкость: от 4,5 до 6,5 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 70,0 до 74,0 мол. %);
POVAL (зарегистрированный товарный знак) JL-05E (JAPAN VAM & POVAL CO., LTD., вязкость: от 4,0 до 6,0 мПа⋅с (4% водный раствор, 20°C), степень омыления: от 80,0 до 84,0 мол. %);
POVAL (зарегистрированный товарный знак) JMR-10M (JAPAN VAM & POVAL CO., LTD., степень полимеризации: от 200 до 280, степень омыления: от 63,0 до 67,0 мол. %);
POVAL (зарегистрированный товарный знак) JMR-10L (JAPAN VAM & POVAL CO., LTD., степень полимеризации: от 200 до 280, степень омыления: от 30,0 до 40,0 мол. %);
поливиниловый спирт (Polysciences, Inc., степень полимеризации: приблизительно 100, степень омыления: 80% мол. %) и тому подобное.
Эти поливиниловые спирты могут быть добавлены по отдельности или в виде комбинации двух или более поливиниловых спиртов, имеющих разные степени омыления и/или степени полимеризации.
Относительное содержание поливинилового спирта никак конкретно не ограничивается при условии, что оно позволяет улучшить растворимость, свойства растворения и/или всасывание энзалутамида при пероральном введении. Относительное содержание поливинилового спирта составляет, например, от 2 мас. % до 90 мас. %, от 5 мас. % до 75 мас. % в одном варианте осуществления, и от 10 мас. % до 20 мас. % в еще одном варианте осуществления по отношению к общей массе фармацевтической композиции для перорального применения. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать. Например, это содержание составляет от 20 мас. % до 1000 мас. %, от 50 мас. % до 500 мас. % в одном варианте осуществления и от 150 мас. % до 350 мас. % в еще одном варианте осуществления по отношению к массе энзалутамида. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать.
Фармацевтическая композиция для перорального применения по настоящему изобретению может представлять собой, например, твердый препарат, такой как таблетки, капсулы, гранулы, порошок, мелкие гранулы или тому подобное, и таблетки в одном варианте осуществления.
Фармацевтическая композиция для перорального применения по настоящему изобретению может содержать твердую дисперсию, включающую энзалутамид и поливиниловый спирт.
В одном варианте осуществления энзалутамид существует в виде аморфного вещества в фармацевтической композиции для перорального применения по настоящему изобретению.
В фармацевтической композиции для перорального применения по настоящему изобретению она может быть составлена путем соответствующего использования различных фармацевтических добавок, если это необходимо, в той степени, в которой могут быть достигнуты необходимые эффекты по настоящему изобретению. Такие фармацевтические добавки никак конкретно не ограничиваются при условии, что они являются фармацевтически приемлемыми и фармакологически приемлемыми. Примеры фармацевтических добавок включают со-дезинтегранты, дезинтегранты, наполнители, корригирующие вещества, шипучие агенты, подсластители, ароматизаторы, лубриканты, буферы, антиоксиданты, сурфактанты, глиданты и тому подобное.
Со-дезинтегрант никак конкретно не ограничивается при условии, что он придает свойство быстрого растворения энзалутамиду в препарате.
Более конкретно, примеры со-дезинтеграторов включают хлорид калия, хлорид натрия, хлорид магния, дигидрофосфат калия, гидрокарбонат натрия, гидрофосфат калия, сульфат калия, сульфат натрия, карбонат натрия, хлорид кальция и тому подобное; и примеры включают хлорид калия в одном варианте осуществления.
Со-дезинтегранты могут быть добавлены по отдельности или в виде комбинации двух или более дезинтегрантов.
Относительное содержание со-дезинтегранта никак конкретно не ограничивается при условии, что оно позволяет достигать свойство быстрого растворения энзалутамида. Относительное содержание со-дезинтегранта составляет от 1 мас. % до 50 мас. %, от 2 мас. % до 40 мас. % в одном варианте осуществления и от 5 мас. % до 30 мас. % в другом варианте осуществления по отношению к общей массе фармацевтической композиции для перорального применения. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать.
Дезинтегрант никак конкретно не ограничивается, при условии, что он придает свойство быстрого растворения энзалутамиду в препарате.
Более конкретно, примеры дезинтегрантов включают кросповидон, гидроксипропилцеллюлозу с низкой степенью замещения, кристаллическую целлюлозу, карбоксиметилцеллюлозу натрия, крахмалгликолят натрия и тому подобное; примеры включают кросповидон, гидроксипропилцеллюлозу с низкой степенью замещения и тому подобное в одном варианте осуществления; и примеры включают кросповидон в одном варианте осуществления.
Примеры кросповидона включают Kollidon CL (название продукта, BASF) и тому подобное.
Дезинтегранты могут быть добавлены по отдельности или в виде комбинации двух или более из них.
Относительное содержание дезинтегранта никак конкретно не ограничивается при условии, что оно позволяет достигать свойств быстрого растворения энзалутамида. Относительное содержание дезинтегранта составляет от 0,5 мас. % до 30 мас. %, от 1 мас. % до 20 мас. % в одном варианте осуществления и от 2 мас. % до 10 мас. % в другом варианте осуществления по отношению к общей массе фармацевтической композиции для перорального применения. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать.
Примеры наполнителей включают лактозу, сахарозу, D-маннит, D-сорбит, крахмал, прежелатинизированный крахмал, декстрин, аравийскую камедь, пуллулан, легкую безводную кремниевую кислоту, синтетический силикат алюминия, метасиликат алюмината магния и тому подобное.
Примеры корригирующих веществ включают лимонную кислоту, винную кислоту, яблочную кислоту и тому подобное.
Примеры шипучих агентов включают бикарбонат натрия и тому подобное.
Примеры подсластителей включают сахарин натрия, дикалий глицирризинат, аспартам, стевию, тауматин и тому подобное.
Примеры ароматизаторов включают лимон, лимон-лайм, апельсин, ментол и тому подобное.
Примеры лубрикантов включают стеарат магния, стеарат кальция, стеариновую кислоту, гидрогенизированное масло и тому подобное.
Примеры буферов включают лимонную кислоту, янтарную кислоту, фумаровую кислоту, винную кислоту, аскорбиновую кислоту и их соли; глутаминовую кислоту, глутамин, глицин, аспарагиновую кислоту, аланин, аргинин и их соли; оксид магния, оксид цинка, гидроксид магния, фосфорную кислоту, борную кислоту, и их соли; и тому подобное.
Примеры антиоксидантов включают аскорбиновую кислоту, дибутилгидрокситолуол, пропилгаллат и тому подобное.
Примеры сурфактантов включают полисорбат 80, лаурилсульфат натрия, полиоксиэтилен гидрогенизированное касторовое масло и тому подобное.
Примеры глидантов включают легкую безводную кремниевую кислоту и тому подобное.
Эти фармацевтические добавки могут быть добавлены соответствующим образом по отдельности или в виде комбинации двух или более из них в соответствующих количествах. Что касается относительных содержаний фармацевтических добавок, каждая фармацевтическая добавка может содержаться в таком количестве, чтобы можно было достичь необходимых эффектов настоящего изобретения.
«Вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи», может быть добавлено дополнительно.
Вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, никак конкретно не ограничивается при условии, что оно представляет собой полимер, который ингибирует водородные связи между молекулами поливинилового спирта, обладает функцией усиления аморфных свойств поливинилового спирта или улучшает стабильность и растворимость энзалутамида. Примеры включают вещества с отрицательно заряженными атомами, такими как фтор, кислород, азот или тому подобное; в одном варианте - осуществления поливинилпирролидон и сополивидон, и в еще одном варианте осуществления - сополивидон.
Примеры сополивидона включают Kollidon VA64 (название продукта, BASF), Kollidon VA64 Fine (название продукта, BASF) и тому подобное.
Примеры поливинилпирролидона включают Kollidon 30 (название продукта, BASF) и тому подобное.
Вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, может быть добавлено в фармацевтическую композицию для перорального применения по настоящему изобретению любым образом в той степени, в которой могут быть достигнуты необходимые эффекты по настоящему изобретению.
Примеры такого варианта осуществления включают вариант осуществления, в котором вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, добавляют к твердой дисперсии, содержащей энзалутамид и поливиниловый спирт.
Вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, может быть добавлено само по себе или в виде комбинации двух или более веществ.
Относительное содержание вещества, имеющего функциональную группу, способную функционировать в качестве акцептора водородной связи, никак конкретно не ограничивается при условии, что это позволяет достичь свойств быстрого растворения энзалутамида и что может быть получена стабильная фармацевтическая композиция. Относительное содержание вещества, имеющего функциональную группу, способную функционировать в качестве акцептора водородной связи, составляет, например, от 1 мас. % до 40 мас. %, от 2 мас. % до 30 мас. % в одном варианте осуществления, от 5 мас. % до 25 мас. % в еще одном варианте осуществления, от 10 мас. % до 20 мас. % в еще одном варианте осуществления и от 6,7 мас. % до 40 мас. % в еще одном варианте осуществления по отношению к общей массе фармацевтической композиции для перорального применения. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать. Относительно массы энзалутамида относительное содержание вещества, имеющего функциональную группу, способную функционировать в качестве акцептора водородной связи, составляет, например, от 1 мас. % до 1000 мас. %, от 50 мас. % до 500 мас. % в одном варианте осуществления и от 100 мас. % до 300 мас. % в еще одном варианте осуществления. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать. Относительно массы поливинилового спирта относительное содержание вещества, имеющего функциональную группу, способную функционировать в качестве акцептора водородной связи, составляет, например, от 10 мас. % до 1000 мас. %, от 20 мас. % до 200 мас. % в одном варианте осуществления, от 30 мас. % до 150 мас. % в еще одном варианте осуществления. Каждый из нижних пределов и каждый из верхних пределов при желании можно произвольным образом комбинировать.
Фармацевтическая композиция для перорального применения по настоящему изобретению может быть изготовлена в соответствии с известными способами, включая, например, аморфизацию энзалутамида, смешивание, гранулирование, формование (таблетирование), нанесение пленочного покрытия и тому подобное.
Способ изготовления фармацевтической композиции для перорального введения по настоящему изобретению будет объяснен ниже.
Этап аморфизации
Примеры способа аморфизации энзалутамида включают способ приготовления твердой дисперсии. Способ приготовления твердой дисперсии энзалутамида и поливинилового спирта никак конкретно не ограничивается, при условии, что он является обычным способом приготовления твердой дисперсии. Примеры таких способов включают способ с использованием растворителя, способ экструзии горячего расплава и тому подобное.
(I) Способ с применением растворителя
Примеры способа с применением растворителя включают способ, в котором после растворения энзалутамида и поливинилового спирта и/или суспендирования в растворителе растворитель удаляют; и тому подобное.
Используемый растворитель никак конкретно не ограничивается при условии, что энзалутамид и поливиниловый спирт могут быть растворены и/или суспендированы в этом растворителе. Более конкретно, примеры растворителей включают метанол, дихлорметан, воду, этанол, ацетон, пропиленгликоль, диметилсульфоксид и тому подобное; и в одном варианте осуществления эти примеры включают метанол и воду. Эти растворители могут быть подходящим образом использованы по отдельности или в виде комбинации двух или более в соответствующих количествах.
Примеры способа удаления растворителя включают распылительную сушку, выпаривание, лиофильную сушку и тому подобное; и в одном варианте осуществления эти примеры включают распылительную сушку.
Примеры этапов приготовления распыляемого раствора, содержащего энзалутамид, который используют при распылительной сушке, включают этапы:
(1) растворение и/или суспендирование поливинилового спирта в воде;
(2) добавление метанола к (1) для приготовления смешанного раствора; и
(3) добавление энзалутамида к смешанному раствору (2) для приготовления раствора для распыления.
Аппарат для распылительной сушки никак конкретно не ограничивается при условии, что энзалутамид может быть превращен в аморфную форму или может быть получена твердая дисперсия энзалутамида и поливинилового спирта. Примеры таких аппаратов включают распылительную сушилку. Условия распылительной сушки никак конкретно не ограничиваются при условии, что может быть получена твердая дисперсия энзалутамида и поливинилового спирта. Температура на выходе распылительной сушилки составляет, например, от 20°С до 80°С.
Способ сушки никак конкретно не ограничивается при условии, что он является обычным способом, в котором может быть осуществлена фармацевтическая сушка. Примеры подходящих устройств включают сушилку с принудительной подачей воздуха, сушилку при пониженном давлении, вакуумную сушилку, сушилку с псевдоожиженным слоем и тому подобное.
(II) Способ экструзии горячего расплава
В способе экструзии горячего расплава энзалутамид и поливиниловый спирт нагревают и плавят, а затем охлаждают.
Температура во время нагревания и плавления может быть соответствующим образом установлена в соответствии с температурой плавления энзалутамида или температурой стеклования поливинилового спирта. Температура составляет, например, от 100°С до 220°С. Температура во время нагревания и плавления может быть подходящим образом установлена с учетом растворимости, свойств растворения, способности к пересыщению и/или стабильности энзалутамида.
Аппарат никак конкретно не ограничивается при условии, что энзалутамид может быть превращен в аморфную форму или может быть получена твердая дисперсия энзалутамида и поливинилового спирта. Примеры таких аппаратов включают двухшнековый экструдер.
В качестве носителя для твердой дисперсии может быть дополнительно добавлено «вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи».
Способ измельчения никак конкретно не ограничивается при условии, что он является обычным способом, в котором может быть осуществлено фармацевтическое измельчение. Примеры устройств включают ударную мельницу (Hosokawa Micron Corporation; мельница тонкого помола), мельницу для сухого и мокрого помола (Powrex Corporation: Comil), ножевую мельницу (Dalton Corporation; Power Mill) и тому подобное.
Этап смешивания
Способ смешивания никак конкретно не ограничивается при условии, что он является обычным способом, в котором каждый компонент может быть смешан фармацевтически и однородно. Примеры устройств включают смеситель V-типа, смеситель ленточного типа, контейнерный смеситель, высокоскоростной смеситель и тому подобное.
Этап гранулирования
Способ гранулирования никак конкретно не ограничивается при условии, что он является обычным способом, в котором гранулирование может быть осуществлено фармацевтически. Примеры устройств включают гранулятор с псевдоожиженным слоем, гранулятор расплава с перемешиванием, гранулятор с высоким сдвиговым усилием, машину для помола (пульверизации) и гранулирования, экструзионный гранулятор, барабанный гранулятор с псевдоожиженным слоем, распылительный гранулятор, сухой гранулятор, двухшнековый экструдер и т.п.; и сухой гранулятор в одном варианте осуществления.
Этап формования (таблетирования)
Способ формования никак конкретно не ограничивается при условии, что он является обычным способом, в котором формование может быть осуществлено фармацевтически. Примеры устройств включают ротационную таблетировочную машину, таблетировочную машину с одним пуансоном, масляный пресс и тому подобное.
На этапе формования, например, может быть использован способ, в котором гранулированный продукт, содержащий твердую дисперсию энзалутамида, или смешанный продукт (смешанный продукт перед компрессионным формованием, в частности смешанный продукт перед таблетированием), приготовленный путем смешивания гранулированного продукта с различными фармацевтическими добавками, такими как лубрикант, подвергают компрессионному формованию для получения таблеток; может быть использован способ прямого таблетирования, при котором твердую дисперсию энзалутамида смешивают с подходящими фармацевтическими добавками, и смесь прессуют для получения таблеток; или тому подобное.
Этап нанесения пленки
Способ нанесения пленочного покрытия никак конкретно не ограничивается при условии, что он является обычным способом, в котором пленочное покрытие может быть осуществлено фармацевтически.
Примеры устройств включают машину для дражирования, машину для нанесения покрытия в псевдоожиженном слое, и тому подобное.
Основные материалы для пленочного покрытия и красящие агенты могут быть соответствующим образом добавлены по отдельности или в виде комбинации двух или более материалов в подходящих количествах.
При необходимости после нанесения пленочного покрытия продукт с покрытием может быть высушен. Способ сушки никак конкретно не ограничивается при условии, что он является обычным способом, в котором сушка может быть осуществленафармацевтически. Примеры устройств включают машину для дражирования, машину для нанесения покрытия в псевдоожиженном слое и тому подобное. Условия сушки никак конкретно не ограничиваются при условии, что условия определяются соответствующим образом в зависимости от стабильности препарата.
Настоящее изобретение включает, в случае фармацевтической композиции для перорального применения, содержащей энзалутамид и поливиниловый спирт, применение вещества, имеющего функциональную группу, способную функционировать в качестве акцептора водородной связи при изготовлении стабильной фармацевтической композиции для перорального применения.
Что касается терминов «энзалутамид», «поливиниловый спирт» и «вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи», которые применяются в контексте использования настоящего изобретения, могут прямо применяться пояснения к соответствующим терминам, приведенные для фармацевтической композиции для перорального применения по настоящему изобретению.
Примеры
Энзалутамид, который использовали в приведенных ниже примерах, был приготовлен в соответствии со способом, описанным в WO 2011/106570.
Далее настоящее изобретение будет дополнительно проиллюстрировано следующими Примерами, Сравнительными Примерами и Экспериментальными Примерами, но никоим образом не ограничено ими.
Экспериментальный Пример 1. Испытание на осаждение
Следующее испытание на осаждение было выполнено, чтобы подтвердить эффект поливиниловых спиртов с различными степенями омыления на улучшение растворимости энзалутамида и поддержание пересыщения. В качестве поливиниловых спиртов использовали POVAL (JMR-10M, JAPAN VAM & POVAL CO., LTD., далее иногда обозначаемый как «А1»), GOHSENOL (NK-05R, Nippon Synthetic Chemical Industry Co., Ltd., далее иногда обозначаемый как «А2»), GOHSENOL (KL-05, Nippon Synthetic Chemical Industry Co., Ltd., далее иногда обозначаемый как «A3»), POVAL (PE-05JPS, JAPAN VAM & POVAL CO., LTD., далее иногда обозначаемый как «B1»), POVAL (JT-05, JAPAN VAM & POVAL CO., LTD., далее иногда обозначаемый как «B2», и GOHSENOL (NL-05, Nippon Synthetic Chemical Industry Co., Ltd., далее иногда обозначаемый как «B3»). Степени омыления и степени полимеризации поливиниловых спиртов, использованных в этом испытании, показаны в Таблице 1. После того, как 200 мг каждого поливинилового спирта предварительно растворяли в 500 мл воды, к этому раствору добавляли 1 мл раствора энзалутамида в ацетоне (содержащего 40 мг эквивалента энзалутамида), с концентрацией, доведенной до 40 мг/мл, и проводили испытание на осаждение в соответствии с испытанием на растворение методом с использованием лопастной мешалки из Японской Фармакопеи, при скорости вращения мешалки 50 об./мин при постоянной температуре 37°С. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 1,579 в 5-мм ячейке за 100%.
Таблица 1
Результаты испытания показаны на Фиг. 1. Каждый тест повторяли три раза, и показаны средние значения. В диапазоне значений омыления (от 66 мол. % до 99 мол. %) поливиниловых спиртов, использованных в Экспериментальном примере 1, когда степень омыления была ниже, растворимость улучшалась, и пересыщение сохранялось. В частности, в диапазоне значений степени омыления от 66 мол. % до 80 мол. % было установлено, что в дополнение к высокому уровню растворения пересыщение также можно поддерживать в высокой степени.
Экспериментальный Пример 2. Испытание на осаждение
Следующее испытание на осаждение было выполнено, чтобы подтвердить влияние поливиниловых спиртов с различными степенями полимеризации на улучшение растворимости энзалутамида и поддержание пересыщения. В качестве поливиниловых спиртов использовали поливиниловый спирт, имеющий степень омыления 80 и степень полимеризации приблизительно 100 (производства Polysciences, Inc., далее иногда сокращенно обозначаемый как «А4»), поливиниловый спирт, имеющий степень омыления 80 и степень полимеризации приблизительно 300 (GOHSENOL, KL-03, Nippon Synthetic Chemical Industry Co., Ltd., далее иногда сокращенно обозначаемый как «A5»), и поливиниловый спирт, имеющий степень омыления 80 и степень полимеризации приблизительно 2200 (GOHSENOL, KH-17, Nippon Synthetic Chemical Industry Co., Ltd., в дальнейшем иногда сокращенно обозначаемый как «B4»). Степени омыления и степени полимеризации поливиниловых спиртов, использованных в испытании, показаны в Таблице 2. После того, как 200 мг каждого поливинилового спирта предварительно растворяли в 500 мл воды, к этому раствору добавляли 1 мл раствора энзалутамида в ацетоне (содержащего 40 мг эквивалента энзалутамида), с концентрацией, доведенной до 40 мг/мл, и проводили испытание на осаждение в соответствии с испытанием на растворение методом с использованием лопастной мешалки из Японской Фармакопеи, при скорости вращения мешалки 50 об./мин при постоянной температуре 37°С. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 1,579 в 5-мм ячейке за 100%.
Таблица 2
Результаты испытания показаны на Фиг. 2. Каждый тест повторяли три раза, и показаны средние значения. На фиг. 2 представлен результат для A3 в Экспериментальном примере 1. В диапазоне значений полимеризации (от 100 до 2200) поливиниловых спиртов, использованных в Экспериментальном примере 2, когда степень полимеризации была ниже, уровень растворения улучшался. В частности, в диапазоне значений полимеризации от 100 до 500 было установлено, что в дополнение к высокому уровню растворения пересыщение также можно поддерживать в высокой степени.
Пример 1
В 40 мл воды 3 г «А2» перемешивали до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 160 мл метанола к раствору «А2», добавляли 1 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (сушилка Niro SD-MicroTM, GEA), чтобы получить фармацевтическую композицию (твердую дисперсию) из Примера 1.
Пример 2
В 280 мл воды перемешивали 10 г «А6» (поливиниловый спирт, полученный очисткой «А5», от компании «Nippon Synthetic Chemical Industry Co., Ltd., для уменьшения количества остаточного растворителя, в дальнейшем иногда сокращенно обозначаемый как «А6») до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 1120 мл метанола к раствору «А6», добавляли 10 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (сушилка Niro SD-MicroTM, GEA), чтобы получить фармацевтическую композицию (твердую дисперсию) из Примера 2. Степень омыления и степень полимеризации «А6», использованные в следующих Примерах, приведены в Таблице 3.
Пример 3
В 2356,8 г воды 120 г «А6» перемешивали до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 7463,2 г метанола к раствору «A6», добавляли 60 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (QSD-0.8-CC, GEA), чтобы получить фармацевтическую композицию (твердую дисперсию) из Примера 3. Методом рентгеновской дифракции было подтверждено, что фармацевтическая композиция (твердая дисперсия) из Примера 3 находилась в аморфном состоянии.
Пример 4
В 2342,4 г воды 180 г «А6» перемешивали до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 7417,7 г метанола к раствору «A6», добавляли 60 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (QSD-0.8-CC, GEA), чтобы получить фармацевтическую композицию (твердую дисперсию) из Примера 4. Методом рентгеновской дифракции было подтверждено, что фармацевтическая композиция (твердая дисперсия) из Примера 4 находилась в аморфном состоянии.
Пример 5
В 3513,6 г воды 270 г GOHSENOL (EG-05P, Nippon Synthetic Chemical Industry Co., Ltd., в дальнейшем иногда сокращенно обозначаемый как «B5») перемешивали при нагревании до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 11126,4 г метанола к раствору «B5», добавляли 90 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (QSD-0.8-CC, GEA), чтобы получить фармацевтическую композицию (твердую дисперсию) из Примера 5. Степень омыления и степень полимеризации «B5», использованные в испытаниях, показаны в Таблице 3.
Таблица 3
Пример 6
В 96 мл воды 3 г «В2» перемешивали при нагревании до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 224 мл метанола к раствору «В2», добавляли 1 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (сушилка Niro SD-MicroTM, GEA) с получением фармацевтической композиции (твердой дисперсии) из Примера 6.
Пример 7
В 175 мл воды 3 г «В3» перемешивали при нагревании до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 325 мл метанола к раствору «B3», добавляли 1 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (сушилка Niro SD-MicroTM, GEA) до получения фармацевтической композиции (твердой дисперсии) из Примера 7.
Экспериментальный Пример 3. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (твердых дисперсий), полученных в Примерах 1-7 (содержащих 80 мг эквивалента энзалутамида). Состав каждой фармацевтической композиции показан в Таблице 4. Для исследования использовали порошок, смешанный с одним и тем же количеством маннита (PEARLITOL 200SD) для каждой фармацевтической композиции (твердой дисперсии). Испытание на растворение проводили с использованием воды (объем тестовой жидкости: 500 мл, температура жидкости: 37°C) в качестве жидкости для испытания на растворение в соответствии с Тестом на растворение, методом с лопастной мешалкой из Японской Фармакопеи, при скорости вращения мешалки 50 об./мин. (250 об./мин в течение периода от 0 до 3 минут с начала испытания и 200 об./мин от 3 до 5 минут). Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 0,6316 в 1-мм ячейке за 100%.
Таблица 4
(Единицы: мг)
Уровни растворения через 10 минут после начала теста растворения (D10мин) показаны в Таблице 5. Высокие уровни растворения, составляющие 60% или более, были получены в фармацевтических композициях (твердых дисперсиях) из Примеров 1-4 с использованием поливинилового спирта, имеющего степень омыления 81 мол. % или менее. Среди фармацевтических композиций (твердых дисперсий) из Примеров 2-4, использующих «А6», чрезвычайно высокие уровни растворения, составляющие 80% или выше, были получены в фармацевтических композициях (твердых дисперсиях), содержащих в два или более раз больше «А6» по сравнению с энзалутамидом. В фармацевтических композициях (твердых дисперсиях) из Примеров 5-7 с использованием поливинилового спирта, имеющего степень омыления 88 мол. % или более, в то время как растворимость энзалутамида в воде (20±5°С) составляет 2 мкг/мл, даже фармацевтическая композиция из Примера 7 показала растворенную концентрацию 15,2 мкг/мл (= 80 мг × 9,5%/ 500 мл), и наблюдался эффект улучшения растворенной концентрации в 7 и более раз. Аналогичным образом, фармацевтические композиции из Примеров 5 и 6, соответственно, показали растворенные концентрации 22,56 мкг/мл (повышение в 11,28 раза) и 41,6 мкг/мл (повышение в 20,8 раза), и наблюдались эффекты улучшения растворенной концентрации в 10 и более раз.
Таблица 5
Пример 8
В 120 мл воды 10 г «А6» перемешивали до растворения. К смешанному раствору, приготовленному путем добавления 480 мл метанола к раствору «А6», добавляли 2 г энзалутамида и перемешивали до растворения для приготовления раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (сушилка Niro SD-MicroTM, GEA) с получением фармацевтической композиции (твердой дисперсии) из Примера 8.
Экспериментальный Пример 4. Испытание на растворение
Было проведено испытание на растворение фармацевтической композиции (твердой дисперсии), полученной в Примере 8 (содержащей 80 мг эквивалента энзалутамида). Состав из Примера 8 показан в Таблице 6. Для испытания использовали порошок, смешанный с одним и тем же количеством маннита (PEARLITOL 200SD) для каждой фармацевтической композиции (твердой дисперсии). Испытание на растворение проводили с использованием 500 мл воды, 500 мл 1-й жидкости для теста на дезинтеграцию из Японской Фармакопеи (JP1) и раствора, приготовленного растворением 895 мг порошка SIF (порошка, имитирующего кишечный сок, Biorelevant.com) в 500 мл 2-й жидкости для теста на дезинтеграцию из Японской Фармакопеи (JP2 + SIF) в качестве трех типов жидкостей для испытания на растворение, в соответствии с тестом на растворение, методикой с лопастной мешалкой из Японской Фармакопеи при скорости вращения мешалки 50 об./мин (250 об./мин в течение периода от 0 до 3 минут с начала испытания и 200 об./мин от 3 до 5 минут) при температуре жидкости 37°C. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 0,6316 в 1-мм ячейке за 100%.
Таблица 6
(Единицы: мг)
Уровень растворения через 10 минут после начала испытания на растворение (D10мин) показан в Таблице 7. Чрезвычайно высокие уровни растворения, составляющие 80% или выше, наблюдались в любой тестируемой жидкости из воды, JP1 и JP2 + SIF. Поскольку фармацевтическая композиция (твердая дисперсия) по настоящему изобретению, которая может быть приготовлена с использованием поливинилового спирта, не зависит от рН, ожидается, что она может быть растворена даже в среде с низким рН, такой как среда в желудке, и что может быть достигнуто быстрое всасывание лекарственного средства.
Таблица 7
Сравнительный пример 1
После смешивания 20 г сополимера поливинилового спирта, акриловой кислоты и метилметакрилата (POVACOAT Type F, Daido Chemical Corporation) с 4 г энзалутамида 22,5 г смеси плавили и перемешивали с использованием экструдера (DSM Xplore Pharma Micro) и измельчали в порошок для получения фармацевтической композиции (твердой дисперсии) из Сравнительного примера 1.
Экспериментальный Пример 5. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (твердых дисперсий), полученных в Примере 4 и Сравнительном Примере 1 (содержащих 160 мг эквивалента энзалутамида). Состав каждой фармацевтической композиции показан в Таблице 8. Для испытания использовали порошок, смешанный с одним и тем же количеством маннита (PEARLITOL 200SD) для каждой фармацевтической композиции (твердой дисперсии). Испытание на растворение проводили с использованием воды (объем жидкости для испытания: 500 мл, температура жидкости: 37°C) в качестве жидкости для теста на растворение в соответствии с Тестом на растворение, методом с лопастной мешалкой из Японской Фармакопеи, при скорости вращения мешалки 50 об./мин. После того, как порошком, смешанным с маннитом, предварительно заполняли шприц, шприцем отбирали 20 мл жидкости для испытания на растворение. Порошок диспергировали встряхиванием, и шприц помещали в тестер растворения, чтобы начать испытание. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 1,2632 в 1-мм ячейке за 100%.
Таблица 8
(Единицы: мг)
Уровни растворения через 10 минут после начала теста на растворимость (D10мин) показаны в Таблице 9. Даже по сравнению с POVACOAT «А6» показал высокий эффект улучшения растворимости. Другими словами, был достигнут высокий эффект улучшения растворимости для выбора поливинилового спирта, имеющего низкую степень омыления.
Таблица 9
Экспериментальный Пример 6. Испытание всасывания при пероральном введении у собак
Суспензии фармацевтических композиций (твердых дисперсий), приготовленных в Примерах 2, 3 и 5, и капсулы XTANDI (зарегистрированный товарный знак) (каждая из которых содержит 160 мг эквивалента энзалутамида) перорально вводили пяти самцам собак породы бигль по отдельности натощак. Состав каждой фармацевтической композиции (твердой дисперсии) показан в Таблице 10. После введения периодически брали кровь и измеряли концентрацию неизмененного энзалутамида в плазме, полученной центрифугированием. Собаки находились в состоянии натощак более 16 часов перед назначенным временем введения. Собак подвергали обработке пентагастрином (внутримышечное введение в ягодицы; за 30 минут до введения и через 30 и 90 минут после введения) для контроля кислотности внутрижелудочного рН, и выполняли испытание.
Таблица 10
(Единицы: мг)
Максимальная концентрация в плазме в неизмененной форме (Cmax), площадь под кривой «концентрация в плазме-время» для неизмененной формы от 0 до 24 часов (AUC) и время достижения максимальной концентрации в плазме для неизмененной формы (Tmax) суспензий фармацевтических композиций (твердые дисперсии) из Примеров 2, 3 и 5 и капсул XTANDI (зарегистрированный товарный знак), а также их соотнесение со значениями для капсул XTANDI (GMR) приведены в Таблице 11. В Примере 5, содержащем «В5», имеющий степень омыления 88 мол. %, в количестве, в 3 раза превышающем количество энзалутамида, и Cmax, и AUC продемонстрировали такое же всасывание, как у капсул XTANDI (зарегистрированный товарный знак). В Примерах 2 и 3, содержащих «А6», имеющий степень омыления 81 мол. %, в количестве в 1 раз и в 2 раза превышающем количество энзалутамида, соответственно, как Cmax, так и AUC показали всасывание выше, чем у капсул XTANDI (зарегистрированный товарный знак), и было достигнуто высокое всасывание. Кроме того, в Примерах 2 и 3 значение Tmax было меньше, чем у капсул XTANDI (зарегистрированный товарный знак), и наблюдалась быстрое всасывание.
Таблица 11
XTANDI
Сравнительный пример 2
После того как 15 г поливинилпирролидона (Kollidon 30, BASF) смешивали с 5 г энзалутамида, 18 г смеси плавили и смешивали с помощью экструдера (DSM Xplore Pharma Micro) и измельчили в порошок для получения фармацевтической композиции (твердой дисперсии) из Сравнительного Примера 2.
Экспериментальный Пример 7. Всасывание при пероральном применении у собак
Суспензии фармацевтических композиций (твердых дисперсий), приготовленных в Примере 4 и Сравнительном Примере 2, и капсулы XTANDI (зарегистрированный товарный знак) (каждая из которых содержит 160 мг эквивалента энзалутамида) вводили перорально четырем самцам собак породы бигль по отдельности натощак. Состав каждой фармацевтической композиции показан в Таблице 12. Испытание проводили в тех же условиях, что и в Экспериментальном примере 6.
Таблица 12
(Единицы: мг)
Максимальная концентрация в плазме в неизмененной форме (Cmax), площадь под кривой «концентрация в плазме-время» для неизмененной формы от 0 до 24 часов (AUC) и время достижения максимальной концентрации в плазме для неизмененной формы (Tmax) суспензии фармацевтических композиций (твердые дисперсии) из Примера 4 и Сравнительного примера 2 и капсул XTANDI (зарегистрированный товарный знак), а также их соотнесение со значениями для капсул XTANDI (GMR) приведены в Таблице 13. В то время как значения Cmax и AUC были ниже, чем у капсул XTANDI (зарегистрированный товарный знак), в Сравнительном примере 2, содержащем поливинилпирролидон (обычно используемый в качестве основного материала для твердой дисперсии), в количестве, в 3 раза превышающем количество энзалутамида, и Cmax, и AUC были выше, чем у капсул XTANDI (зарегистрированный товарный знак), в Примере 4, содержащем «А6» в количестве, в 3 раза превышающем количество энзалутамида, и было достигнуто высокое всасывание. Кроме того, в Примере 4, как и в Примерах 2 и 3, значение Tmax было меньше, чем у капсул XTANDI (зарегистрированный товарный знак), и наблюдалось быстрое всасывание.
Таблица 13
Пример 9
После смешивания 300 г энзалутамида, 900 г «А6» и 300 г поливинилпирролидона (Kollidon 30, BASF) смесь плавили и перемешивали с помощью экструдера (KEX-25, Kurimoto, Ltd.) и измельчали в порошок до получения фармацевтической композиции (твердой дисперсии) из Примера 9. Рентгеновской дифракцией было подтверждено, что твердая дисперсия из Примера 9 находилась в аморфном состоянии.
Пример 10
После смешивания 200 г энзалутамида, 400 г «А6» и 400 г сополивидона (Kollidon VA64, BASF) смесь плавили и перемешивали с использованием экструдера (KEX-25, Kurimoto, Ltd.) и измельчали в порошок до получения фармацевтической композиции (твердой дисперсии) из Примера 10.
Экспериментальный Пример 8. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (твердых дисперсий), полученных в Примерах 9 и 10 (содержащих 160 мг эквивалента энзалутамида). Состав каждой фармацевтической композиции (твердой дисперсии), как показано в Таблице 14. Для испытания использовали порошок, смешанный с одним и тем же количеством маннита (PEARLITOL 200SD) для каждой фармацевтической композиции (твердой дисперсии). Испытание на растворение проводили с использованием воды (объем жидкости для испытания: 500 мл, температура жидкости: 37°C) в качестве жидкости для испытания на растворение в соответствии с тестом на растворение, методом с лопастной мешалкой из Японской Фармакопеи при скорости вращения мешалки 50 об./мин. После того, как порошком, смешанным с маннитом, предварительно заполняли шприц, шприцем отбирали 20 мл жидкости для испытания на растворение. Порошок диспергировали встряхиванием, и шприц помещали в тестер растворения, чтобы начать испытание. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 1,2632 в 1-мм ячейке за 100%.
Таблица 14
(Единицы: мг)
Уровни растворения через 10 минут после начала испытания на растворение (D10мин) показаны в Таблице 15. В обоих Примерах 9 и 10 были получены чрезвычайно высокие уровни растворения, составляющие 80% или выше.
Таблица 15
Экспериментальный Пример 9 Всасывание при пероральном применении у собак
Суспензии фармацевтических композиций (твердых дисперсий), приготовленных в Примерах 9 и 10, и капсулы XTANDI (зарегистрированный товарный знак) (каждая из которых содержит 160 мг эквивалента энзалутамида) вводили перорально пяти самцам собак породы бигль по отдельности натощак. Состав каждой фармацевтической композиции показан в Таблице 14. Испытание проводили в тех же условиях, что и в Экспериментальном примере 6.
Максимальная концентрация в плазме в неизмененной форме (Cmax), площадь под кривой «концентрация в плазме-время» для неизмененной формы от 0 до 24 часов (AUC) и время достижения максимальной концентрации в плазме для неизмененной формы (Tmax) суспензии фармацевтических композиций из Примеров 9 и 10 и капсул XTANDI (зарегистрированный товарный знак) и их соотнесение со соответствующими значениями капсул XTANDI (GMR) приведены в Таблице 16. Cmax в примере 9, а также Cmax и AUC в Примере 10 были выше, чем у капсул XTANDI (зарегистрированный товарный знак), и было получено высокое всасывание. Кроме того, в Примерах 9 и 10 значение Tmax было меньше, чем у капсул XTANDI (зарегистрированный товарный знак), и наблюдалось быстрое всасывание.
Таблица 16
Экспериментальный Пример 10. Измерение количества максимального родственного вещества
Для фармацевтических композиций (твердых дисперсий), полученных в Примерах 9 и 10 (каждая из которых содержит 80 мг эквивалента энзалутамида), количество максимального родственного энзалутамиду вещества измеряли методом ВЭЖХ.
Измерение количества максимального родственного вещества проводили в следующих условиях:
- В качестве колонки для ВЭЖХ использовали Zorbax SB-CN, размер частиц: 5 мкм, 4,6 мм (внутренний диаметр) × 150 мм (производства Agilent), при температуре 30°C.
- В качестве подвижной фазы А использовали 0,05% водный раствор трифторуксусной кислоты.
- В качестве подвижной фазы B использовали 0,05% раствор трифторуксусной кислоты в ацетонитриле.
- В качестве раствора для разбавления образцов использовали смесь ацетонитрил/вода (9:1), так что концентрация энзалутамида составляла 240 мкг/мл.
- Количества родственных веществ измеряли с помощью спектрофотометра с ультрафиолетовым поглощением (длина волны: 260 нм), в соответствии с программой градиента, показанной в Таблице 17 ниже, и путем регулирования скорости потока до 1 мл/мин. Процент площади пика максимального родственного вещества рассчитывали в виде процента от общей площади пика энзалутамида и родственных веществ.
Таблица 17
Результаты Экспериментального примера 10 показаны в Таблице 18.
Таблица 18
Пример 11
В ступку добавляли 1200 мг фармацевтической композиции (твердой дисперсии) из Примера 9, 1446 мг маннита (PEARLITOL 200SD), 720 мг хлорида калия, 180 мг кросповидона (Kollidon CL), 36 мг легкой безводной кремниевой кислоты (Silysia 320TP) и 18 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали с использованием таблеточной машины с одним пуансоном для получения фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 11.
Пример 12
В ступку добавляли 1200 мг фармацевтической композиции из Примера 9, 1446 мг маннита (PEARLITOL 200SD), 720 мг хлорида натрия, 180 мг кросповидона (Kollidon CL), 36 мг легкой безводной кремниевой кислоты (Silysia 320TP), и 18 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали с использованием таблеточной машины с одним пуансоном для получения фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 12.
Пример 13
В ступку добавляли 1200 мг фармацевтической композиции из Примера 9, 1446 мг маннита (PEARLITOL 200SD), 720 мг гексагидрата хлорида магния, 180 мг кросповидона (Kollidon CL), 36 мг легкой безводной кремниевой кислоты (Silysia 320TP) и 18 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали, используя машину для таблетирования с одним пуансоном, с получением фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 13.
Таблица 19
(Единицы: мг)
Экспериментальный Пример 11. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (таблеток, содержащих 40 мг эквивалента энзалутамида), полученных в Примерах с 11 по 13. Испытание на растворение проводили с использованием воды (объем жидкости для испытания: 500 мл, температура жидкости: 37°C) в качестве жидкости для испытания на растворение в соответствии с тестом на растворение, методом с лопастной мешалкой из Японской Фармакопеи, при скорости вращения мешалки 50 об./мин. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 0,3158 в 1-мм ячейке за 100%.
Уровни растворения через 10 минут после начала испытания на растворение (D10мин) показаны в Таблице 20. Высокий уровень растворения, равный 60% или выше, наблюдался в Примере 13 с использованием магния хлорида гексагидрата. Кроме того, чрезвычайно высокие уровни растворения, равные 80% или выше, были получены в Примере 11 с использованием хлорида калия и в Примере 12 с использованием хлорида натрия.
Таблица 20
Экспериментальный Пример 12. Испытание всасывания при пероральном применении у собак.
Фармацевтическую композицию (таблетки, содержащие 160 мг эквивалента энзалутамида (четыре таблетки)), приготовленную в Примере 11, и капсулы XTANDI (зарегистрированный товарный знак) перорально вводили четырем самцам собак породы бигль по отдельности натощак. Испытание проводили в тех же условиях, что и в Экспериментальном примере 6.
Максимальная концентрация в плазме в неизмененном виде (Cmax), площадь под кривой «концентрация в плазме-время» для неизмененной формы от 0 до 24 часов (AUC) и время достижения максимальной концентрации в плазме для неизмененной формы (Tmax) фармацевтической композиции из Примера 11 и капсул XTANDI (зарегистрированный товарный знак), а также их соотнесение со значениями капсул XTANDI (GMR) показаны в Таблице 21. В Примере 11 значения Cmax и AUC были выше, чем у капсул XTANDI (зарегистрированный товарный знак), и было получено высокое всасывание. Кроме того, в Примере 11 значение Tmax было меньше, чем у капсул XTANDI (зарегистрированный товарный знак), и наблюдалось быстрое всасывание.
Таблица 21
Пример 14
В ступку добавляли 4000 мг фармацевтической композиции (твердой дисперсии) из Примера 10, 4820 мг маннита (PEARLITOL 200SD), 2400 мг хлорида калия, 600 мг кросповидона (Kollidon CL), 120 мг легкой безводной кремниевой кислоты (Silysia 320TP) и 60 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали, используя машину для таблетирования с одним пуансоном, с получением фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 14.
Пример 15
В ступку добавляли 2000 мг фармацевтической композиции (твердой дисперсии) из Примера 10, 2410 мг маннита (PEARLITOL 200SD), 1200 мг хлорида натрия, 300 мг кросповидона (Kollidon CL), 60 мг легкой безводной кремниевой кислоты (Silysia 320TP) и 30 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали, используя машину для таблетирования с одним пуансоном, с получением фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 15.
Пример 16
В ступку добавляли 2000 мг фармацевтической композиции (твердой дисперсии) из Примера 10, 2410 мг маннита (PEARLITOL 200SD), 1200 мг дигидрофосфата калия, 300 мг кросповидона (Kollidon CL), 60 мг легкой безводной кремниевой кислоты (Silysia 320TP) и 30 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали, используя машину для таблетирования с одним пуансоном, с получением фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 16.
Таблица 22
(Единицы: мг)
Экспериментальный Пример 13. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (таблеток, содержащих 40 мг эквивалента энзалутамида), полученных в Примерах 14-16. Испытание на растворение проводили с использованием воды (объем жидкости для испытания: 500 мл, температура жидкости: 37°C) в качестве жидкости для испытания на растворение в соответствии с тестом на растворение, методом с лопастной мешалкой из Японской Фармакопеи, при скорости вращения мешалки 50 об./мин. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 0,3158 в 1-мм ячейке за 100%.
Уровни растворения через 10 минут после начала испытания на растворение (D10мин) показаны в Таблице 23. В любом из примеров были получены чрезвычайно высокие уровни растворения, составляющие 80% или выше.
Таблица 23
Экспериментальный пример 14. Испытание всасывания при пероральном применении у собак
Фармацевтическую композицию (таблетки, содержащие 160 мг эквивалента энзалутамида (четыре таблетки)), приготовленную в Примере 14, и капсулы XTANDI (зарегистрированный товарный знак) вводили перорально трем самцам собак породы бигль по отдельности натощак. Испытание проводили в тех же условиях, что и в Экспериментальном примере 6.
Максимальная концентрация в плазме в неизмененной форме (Cmax), площадь под кривой «концентрация в плазме-время» для неизмененной формы от 0 до 24 часов (AUC) и время достижения максимальной концентрации в плазме для неизмененной формы (Tmax) фармацевтической композиции (таблеток) из Примера 14 и капсулы XTANDI (зарегистрированный товарный знак), и их соотнесение со значениями капсул XTANDI (GMR) показаны в Таблице 24. В Примере 14 и Cmax, и AUC показали высокие значения по сравнению с капсулами XTANDI (зарегистрированный товарный знак), и было получено высокое всасывание. Кроме того, в фармацевтической композиции (таблетках) из Примера 14 значение Tmax было меньше, чем у капсул XTANDI (зарегистрированный товарный знак), и наблюдалось быстрое всасывание.
Таблица 24
Пример 17
В ступку добавляли 1200 мг фармацевтической композиции из Примера 9, 1266 мг маннита (PEARLITOL 200SD), 720 мг хлорида калия, 360 мг кросповидона (Kollidon CL), 36 мг легкой безводной кремниевой кислоты (Silysia 320TP), и 18 мг стеарата магния, и смешивали с использованием пестика. Полученный смешанный порошок таблетировали, используя машину для таблетирования с одним пуансоном, для получения фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 17.
Пример 18
В ступку добавляли 1200 мг фармацевтической композиции из Примера 9, 1266 мг маннита (PEARLITOL 200SD), 720 мг хлорида калия, 360 мг низкозамещенной гидроксипропилцеллюлозы (L-HPC, LH-21), 36 мг легкой безводной кремниевой кислоты (Silysia 320TP) и 18 мг стеарата магния, и смешивали с помощью пестика. Полученный смешанный порошок таблетировали, используя машину для таблетирования с одним пуансоном, для получения фармацевтической композиции (таблетки, 600 мг на таблетку) из Примера 18.
Таблица 25
(Единицы: мг)
Экспериментальный Пример 15. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (таблеток, содержащих 40 мг эквивалента энзалутамида), полученных в Примерах 17 и 18. Испытание на растворение проводили с использованием воды (объем жидкости для испытания: 500 мл, температура жидкости: 37°C) в качестве жидкости для испытания на растворение, в соответствии с тестом на растворение по методике с использованием лопастной мешалки из Японской Фармакопеи при скорости вращения мешалки 50 об./мин. Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровни растворения рассчитывали, принимая поглощение 0,3158 в 1-мм ячейке за 100%.
Уровни растворения через 10 минут после начала испытания на растворение (D10min) показаны в Таблице 26. Чрезвычайно высокие уровни растворения, составляющие 80% или выше, наблюдались в фармацевтических композициях (таблетках) из Примера 17 с использованием кросповидона и Примера 18 с использованием низкозамещенной гидроксипропилцеллюлозы.
Таблица 26
Пример 19
В 40 мл воды 3 г «А1» перемешивали до растворения. К смешанному раствору, приготовленному путем дополнительного добавления 160 мл метанола к раствору «А1», добавляли 1 г энзалутамида и перемешивали до растворения с получением раствора для распыления. Раствор для распыления подвергали распылительной сушке с помощью распылительной сушилки (сушилка Niro SD-MicroTM, GEA) с получением фармацевтической композиции (твердой дисперсии) из Примера 19.
Экспериментальный пример 16. Испытание на растворение
Было проведено испытание на растворение фармацевтических композиций (твердых дисперсий), полученных в Примерах 5-7 и 19 (содержащих 80 мг эквивалента энзалутамида). Состав каждой фармацевтической композиции показан в Таблице 27. Для испытания использовали порошок, смешанный с одним и тем же количеством маннита (PEARLITOL 200SD) для каждой фармацевтической композиции (твердой дисперсии). Испытание на растворение проводили с использованием воды (объем жидкости для испытания: 500 мл, температура жидкости: 37°C) в качестве жидкости для испытания на растворение в соответствии с тестом на растворение по методике с использованием лопастной мешалки из Японской Фармакопеи при скорости вращения мешалки 50 об/мин. (250 об./мин в течение периода от 0 до 3 минут с начала теста и 200 об/мин от 3 до 5 минут). Поглощение энзалутамида в ультрафиолетовой области измеряли при 260 нм. Уровень растворения рассчитывали, принимая поглощение 0,6316 в 1-мм ячейке за 100%.
Таблица 27
(Единицы: мг)
Уровни растворения через 10 минут после начала испытания на растворение (D10мин) показаны в Таблице 28. Высокий уровень растворения, равный 100% или выше, был получен в фармацевтической композиции (твердой дисперсии) из Примера 19 с использованием поливинилового спирта, имеющего степень омыления 66 мол. %. В фармацевтической композиции (твердой дисперсии) из Примеров 5-7 с использованием поливинилового спирта, имеющего степень омыления 88 мол. % или более, даже фармацевтическая композиция из Примера 7 показала растворенную концентрацию 15,2 мкг/мл (= 80 мг × 9,5%/ 500 мл), и наблюдался эффект улучшения растворенной концентрации в 7 и более раз по отношению к растворимости энзалутамида в воде.
Таблица 28
Промышленная применимость
В соответствии с настоящим изобретением может быть обеспечена фармацевтическая композиция для перорального применения, в которой улучшены растворимость и/или свойства растворения энзалутамида, поддерживается пересыщение, и улучшено всасывание энзалутамида при пероральном введении.
Хотя настоящее изобретение было описано со ссылкой на конкретные варианты осуществления, возможны различные изменения и модификации, очевидные специалистам в данной области техники, не выходящие за пределы объема прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Лекарственная форма в виде капсулы, содержащая таблетки с диметилфурмаратом | 2019 |
|
RU2742745C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2008 |
|
RU2470637C2 |
| Твёрдая фармацевтическая композиция для изготовления перорального антиретровирусного терапевтического средства | 2020 |
|
RU2760129C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЦЕРЕБРОВАСКУЛЯРНЫХ РАССТРОЙСТВ И СПОСОБЫ ИХ ИЗГОТОВЛЕНИЯ | 2012 |
|
RU2559776C2 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ГИНДАРИНА | 2007 |
|
RU2372912C2 |
| ДЕЗИНТЕГРИРУЮЩИЙ АГЕНТ | 1999 |
|
RU2201215C2 |
| ПЕРОРАЛЬНАЯ КОМПОЗИЦИЯ ТВЕРДОГО РАСТВОРА МАЛОРАСТВОРИМОГО В ВОДЕ АКТИВНОГО ВЕЩЕСТВА | 2003 |
|
RU2314811C2 |
| ФАРМАЦЕВТИЧЕСКАЯ ПРОТИВОДИАБЕТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ЗАМЕЩЕННОГО ТИОФЕНКАРБОКСИЛАТА И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2018 |
|
RU2688235C1 |
| Твёрдая фармацевтическая композиция для изготовления перорального терапевтического средства для профилактики и/или лечения ВИЧ-инфекции | 2021 |
|
RU2759544C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, КОМПОЗИЦИЯ И КОМБИНИРОВАННЫЙ СОСТАВ, СОДЕРЖАЩИЕ АКТИВАТОР ГЛЮКОКИНАЗЫ И АКТИВАТОР РЕЦЕПТОРА PPAR, И СПОСОБ ИХ ПРИГОТОВЛЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2781638C2 |
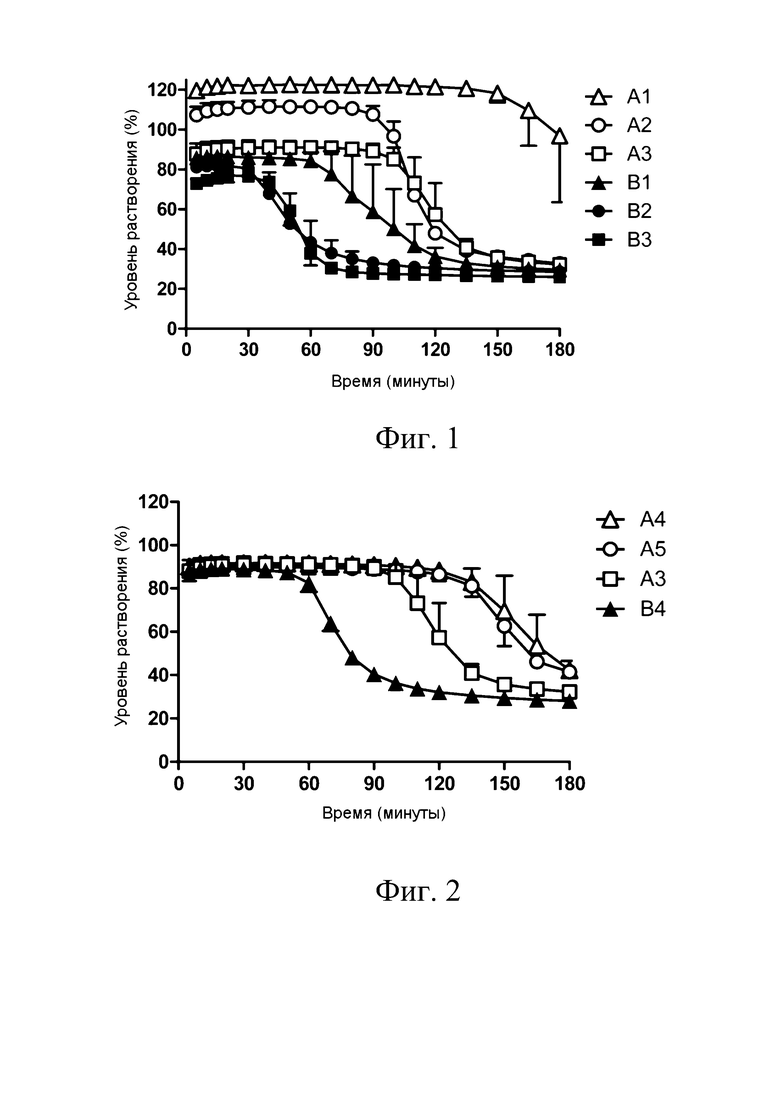
Группа изобретений относится к области фармацевтики, а именно к фармацевтической композиции для перорального введения энзалутамида и способу её получения. Фармацевтическая композиция для перорального введения энзалутамида включает энзалутамид и поливиниловый спирт, где поливиниловый спирт имеет степень омыления от 63 мол.% до 85 мол.%, и степень полимеризации от 100 до 500, где содержание поливинилового спирта составляет от 50 мас.% до 500 мас.% по отношению к массе энзалутамида, и дополнительно включающая хлорид калия, хлорид натрия, или дигидрофосфат калия как со-дезинтегрант. Способ получения вышеуказанной фармацевтической композиции включает этап приготовления твердой дисперсии, содержащей энзалутамид и поливиниловый спирт. Получаемая фармацевтическая композиция обладает улучшенной растворимостью, увеличенными биодоступностью и скоростью всасывания энзалутамида. 2 н. и 9 з.п. ф-лы, 2 ил., 28 табл., 16 пр.
1. Фармацевтическая композиция для перорального введения энзалутамида, включающая энзалутамид и поливиниловый спирт, где поливиниловый спирт имеет степень омыления от 63 мол.% до 85 мол.%, и степень полимеризации от 100 до 500, где содержание поливинилового спирта составляет от 50 мас.% до 500 мас.% по отношению к массе энзалутамида, и дополнительно включающая хлорид калия, хлорид натрия, или дигидрофосфат калия как со-дезинтегрант.
2. Фармацевтическая композиция для перорального введения по п. 1, включающая твердую дисперсию, содержащую указанный энзалутамид и указанный поливиниловый спирт.
3. Фармацевтическая композиция для перорального введения по любому из пп. 1, 2, дополнительно содержащая вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, где вещество, имеющее функциональную группу, способную функционировать в качестве акцептора водородной связи, представляет собой поливинилпирролидон и/или сополивидон.
4. Фармацевтическая композиция для перорального введения по любому из пп. 1-3, дополнительно включающая дезинтегрант.
5. Фармацевтическая композиция для перорального введения по п. 4, в которой дезинтегрант представляет собой соединение или два или более соединений, выбранных из группы, состоящей из кросповидона и низкозамещенной гидроксипропилцеллюлозы.
6. Фармацевтическая композиция для перорального введения по п. 4 или 5, в которой дезинтегрант представляет собой кросповидон.
7. Фармацевтическая композиция для перорального введения по любому из пп. 1-6, представляющая собой таблетку.
8. Фармацевтическая композиция по любому из пп. 1-7, где энзалутамид является аморфным.
9. Способ получения фармацевтической композиции для перорального введения, включающей энзалутамид и поливиниловый спирт, где поливиниловый спирт имеет степень омыления от 63 мол.% до 85 мол.% и степень полимеризации от 100 до 500, где содержание поливинилового спирта составляет от 50 мас.% до 500 мас.% по отношению к массе энзалутамида, и дополнительно включающую хлорид калия, хлорид натрия, дигидрофосфат калия как со-дезинтегрант, причем указанный способ включает этап приготовления твердой дисперсии, содержащей энзалутамид и поливиниловый спирт.
10. Способ получения фармацевтической композиции для перорального введения по п. 9, в котором твердую дисперсию получают методом экструзии горячего расплава.
11. Способ получения фармацевтической композиции для перорального введения по п. 10, в котором твердую дисперсию получают методом с использованием растворителя.
| WO 2014043208 A1, 2014.03.20 | |||
| WO 2016116121 A1, 2016.07.28 | |||
| Handbook of pharmaceutical excipients, Fifth edition, Edited by Raymond C Rowe, Pharmaceutical press and American pharmacists association, 2006, стр | |||
| Телефонная трансляция с катодными лампами | 1920 |
|
SU592A1 |
| СПОСОБ ПОЛУЧЕНИЯ АМОРФИЗОВАННОГО ПОЛИВИНИЛОВОГО СПИРТА | 2001 |
|
RU2205191C1 |
| WO 2015118015 A1, 2015.08.13. | |||
Авторы
Даты
2024-11-21—Публикация
2018-04-27—Подача