ОБЛАСТЬ ТЕХНИКИ
[0001] Способы и композиции для стимуляции донор-специфической толерантности к аллогенным трансплантатам цельных органов у реципиента, получающего аллогенный трансплантат цельного органа от донора.
УРОВЕНЬ ТЕХНИКИ
[0002] Трансплантация органов требует подготовки и взятия цельного органа человека у донора и трансплантации в организм реципиента. Основная проблема при трансплантации цельных органов заключается в том, что реципиент не толерантен к донору. Т-клетки реципиента будут отторгать орган, а В-клетки реципиента будут вырабатывать антитела к органу, в конечном счете вызывая его недостаточность. Краеугольным камнем при трансплантации цельных органов является развитие у реципиента толерантности к трансплантированному человеческому органу. По оценкам, в США ежегодно проводится более 36000 операций по трансплантации органов, и еще больше проводится в Европе и других крупных странах. Также оценивают, что в США более 120000 пациентов находятся в листах ожидания по трансплантации органов. Спрос на здоровые органы значительно превышает предложение подходящих органов. В 2018 году было выявлено около 10000 доноров. См. https://optn.transplant.hrsa.gov.
[0003] Отторжение трансплантата является существенной проблемой при трансплантации цельных органов. Отторжение трансплантата как Т-клетками, так и В-клетками может привести к значительным осложнениям в работе органов или даже к недостаточности трансплантата. Пятилетняя выживаемость трансплантата, например, при трансплантации сердца составляет 77,7%, при трансплантации почки - 78,6%, при трансплантации печени - 72,8%, а при трансплантации легких - 53,4%. Как правило, эта проблема решалась, в частности, путем подбора доноров и реципиентов с одинаковыми антигенами основного комплекса гистосовместимости (МНС) и путем избегания реципиентов с антителами к типам тканей реципиента. Кроме того, улучшилось применение иммуносупрессивных режимов для контроля иммунологического ответа, лежащего в основе отторжения трансплантата. Однако толерантность не была достигнута, и средняя продолжительность выживаемости для многих органов составляет всего 10 лет.
[0004] Сохранение жизнеспособности органов до и во время процедуры имплантации является второй важной задачей. Изъятие, хранение и трансплантация органа может оказать кардинальное влияние на внутреннюю структуру и функцию органа и может значительно повлиять на степень, в которой восстановление нормальной функции органа задерживается или предотвращается после завершения трансплантации.
[0005] Период времени, в течение которого цельные человеческие органы могут эффективно сохраняться, варьируется в зависимости от органа: для почек он составляет от 24 до 36 часов, для поджелудочной железы - от 12 до 18 часов, для печени - от 8 до 12 часов, и для сердца и легких - от 4 до 6 часов. См. https://unos.org/transplantation/matching-organs.
[0006] Повреждение органа происходит в основном в результате ишемии и переохлаждения, но также может быть связано с реперфузией органа ex vivo или во время имплантации.
[0007] Способы сохранения органов, включая перфузию ex vivo, известны в данной области техники и служат для минимизации повреждения органов и обеспечения оптимального выживания и функционирования трансплантата.
[0008] Основные цельные органы, которые были предметом процедур трансплантации, включают почки, печень, сердце и легкие. Трансплантацию этих цельных органов осуществляли с различной степенью успеха. Основная вариативность связана с методами, используемыми для препятствования опосредованному иммунной системой отторжению трансплантата. Опыт показал, что не существует одного иммуносупрессивного препарата или метода, который был бы эффективен во всех ситуациях, связанных с трансплантацией цельных органов. Ограничивающий фактор обычно заключается в токсичности, связанной с каждым отдельным иммуносупрессивным препаратом. Токсичность, связанная с отдельно взятым иммуносупрессивным препаратом, может часто препятствовать нормальному функционированию трансплантированного цельного органа или других органов, таких как почки, которые могут отказывать при использовании ингибиторов кальциневрина для предотвращения отторжения.
[0009] Связанные с токсичностью недостатки известных иммуносупрессивных препаратов, обычно используемых для предотвращения отторжения трансплантата при трансплантации цельных органов, требуют поиска новых способов предотвращения отторжения трансплантатов цельных органов.
[0010] Способность различать собственные и чужеродные антигены имеет решающее значение для иммунного ответа. Это различение приводит к аутотолерантности. Аутоиммунитет развивается при утрате аутотолерантности. В процедурах трансплантации существует неудовлетворенная потребность в индукции толерантности к трансплантатам цельных органов.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0011] Достижение донор-специфической иммунной толерантности остается конечной
иммунологической целью при трансплантации. Большинство современных подходов сосредоточены на контроле периферических зрелых донор-специфических Т-клеток путем обеднения (например, алемтузумаб, тимоглобулин и т.д.) или подавления (например, ингибиторы кальциневрина, базиликсимаб и т.д.) без оказания воздействия на продукцию аллореактивных Т-клеток в тимусе. Тем не менее, даже несмотря на значительный прогресс иммуносупрессивных препаратов и новые иммуномодулирующие режимы толерантность к трансплантатам до сих пор не достигнута.
[0012] Автор настоящего изобретения показал, что толерантность к трансплантатам цельных органов может быть достигнута посредством имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса (называемого также «КТТ» или «RVT-802»), реципиенту с тимэктомией, чтобы сократить период применения посттрансплантационных иммуносупрессивных препаратов для предотвращения отторжения трансплантированного органа. Удаление тимуса реципиента и замена на продукт, полученный из аллогенной культивированной ткани постнатального тимуса, приводит к восстановлению иммунной системы реципиента цельного органа и толерантности реципиента к самому себе, а также к трансплантированному аллогенному цельному органу.
[0013] Индукция толерантности путем хирургического внедрения продукта, полученного из аллогенной культивированной ткани постнатального тимуса, аналогична индукции толерантности с помощью дендритных клеток («ДК») донора при трансплантации гемопоэтических стволовых клеток (Sharabi Y & Sachs DH, 1989, “Mixed chimerism and permanent specific transplantation tolerance induced by a nonlethal preparative regimen," J Exp Med 169(2):493-502; Manilay JO, Pearson DA, Sergio JJ, Swenson KG, & Sykes M, 1998, “Intrathymic deletion of alloreactive T cells in mixed bone marrow chimeras prepared with a nonmyeloablative conditioning regimen,” Transplantation 66(1):96-102.). Серия исследований, проведенных Исследовательским центром биологии трансплантации (TBRC, Бостон, Массачусетс), показала решающую роль тимуса в индукции толерантности (Yamada K, et al., 1997, “Role of the thymus in transplantation tolerance in miniature swine. I. Requirement of the thymus for rapid and stable induction of tolerance to class I-mismatched renal allografts,” J Exp Med 186(4):497-506.) и включала тестирование трансплантации тимуса с индукцией толерантности на модели у крупных животных (Yamada K, et al., 2000, “Thymic transplantation in miniature swine. II. Induction of tolerance by transplantation of composite thymokidneys to thymectomized recipients,” J Immunol 164(6):3079-3086; 5; Yamada K, et al., 2003, “Thymic transplantation in miniature swine: III. Induction of tolerance by transplantation of composite thymokidneys across fully major histocompatibility complex-mismatched barriers,” Transplantation 76(3):530-536; Nobori S, et al., 2006, “Thymic rejuvenation and the induction of tolerance by adult thymic grafts," Proc Natl Acad Sci U S A 103(50):19081-19086. В серии исследований, проведенных этой группой, успешно использовали донора с совпадающим классом II/несовпадающим классом I (тимуса и почки или сердца) в качестве составных тканей тимуса (тимо-почка и тимо-сердце) с 12-дневным курсом циклоспорина («CsA») для индукции толерантности к трансплантату. Исследователи утверждали, что неваскуляризированный тимус не вызывал толерантности в использованной ими модели. Точнее, однако, неваскуляризированный тимус, который не был культивирован, не приживался на длительное время. Как они указали, неудача приживления некультивированного тимуса могла быть связана с ишемическим повреждением помимо аллоиммунитета (Yamada K, et al., 2000). Эту элегантную концепцию создания васкуляризованного тимуса до трансплантации для индукции толерантности было бы трудно реализовать в клинических условиях без использования ксенотрансплантации (В этом разделе цитируется Kwan J et al Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants, которая будет сдана для публикации в 2019 г.).
[0014] Ограничение трансплантации неваскуляризованного тимуса можно преодолеть с помощью системы культивирования, а также обеднения Т-клетками. Экспериментальная трансплантация аллогенного культивированного продукта, полученного из постанатальной ткани тимуса (КТТ), в котором сохранены ЭКТ (эпителиальные клетки тимуса), успешно применялась для лечения педиатрических пациентов с врожденной атимией (Markert ML, Devlin BH, McCarthy EA, 2010, “Thymus transplantation,” Clin Immunol., 135(2): 236-46; Markert ML, et al., 2004, “Postnatal thymus transplantation with immunosuppression as treatment for DiGeorge syndrome,” Blood 104(8):2574-2581; Markert ML, et al., 1999, “Transplantation of thymus tissue in complete DiGeorge syndrome,” N Engl J Med 341(16):1180-1189 27).
[0015] В этом источнике синдром Ди Георга определяется как состояние, при котором в сердце, тимусе и паращитовидной железе присутствуют различные дефекты. Около 1% грудных детей с синдромом Ди Георга имеют атимию и, следовательно, не имеют Т- клеток для борьбы с инфекцией. Говорят, что эти дети имеют полный синдром Ди Георга. Существует 4 подгруппы детей, соответствующих критериям полного синдрома Ди Георга, синдрома делеции 22q11.2, CHARGE, грудных детей от матерей с диабетом и грудных детей без синдромных или генетических дефектов. Во всех четырех группах грудные дети с атимией представляют собой очень маленькую группу, возможно, 1% от общего числа детей, которым поставлен диагноз, такой как диагноз синдрома делеции 22q11.2.
[0016] Тимопоэз был подтвержден биопсией аллотрансплантата и присутствием наивных
Т-клеток реципиента на периферии (Markert ML, 2010,; Markert ML, et al., 2008, “Use of allograft biopsies to assess thymopoiesis after thymus transplantation,” J Immunol 180(9):6354- 6364; Markert ML, et al., 2007, “Review of 54 patients with complete DiGeorge anomaly enrolled in protocols for thymus transplantation: outcome of 44 consecutive transplants,” Blood 109(10):4539-454728). Исследования у детей, получавших лечение с помощью исследуемого КТТ, демонстрируют толерантность к MHC донора по реакциям смешанной культуры лимфоцитов (Chinn IK, Devlin BH, Li YJ, & Markert ML, 2008, “Long-term tolerance to allogeneic thymus transplants in complete DiGeorge anomaly,” Clin Immunol 126(3):277-281). Кроме того, грудные дети с врожденной атимией после трансплантации КТТ могут бороться с такими инфекциями, как вирус Эпштейна-Барр (Markert ML, 2014, Thymus Transplantation. Stiehm’s Immune Deficiences, eds Sullivan KE & Stiehm ER (Academic Press), 1st Ed, стр. 1059-1067; Isakovic K, Smith SB, & Waksman BH, 1965, “Immunologic Tolerance in Thymectomized, Irradiated Rats Grafted with Thymus from Tolerant Donors,” Science 148(3675):1333-1335). Основываясь на этих данных, полученных у людей с врожденной атимией, было определено, что после хирургического внедрения реципиенту продукта, полученного из аллогенной культивированной ткани постнатального тимуса, экспрессирующего MHC донора цельного органа, будет развиваться толерантность как к собственному организму, так и к донору, при одновременной продукции функциональных Т-клеток, которые будут защищать реципиента от инфекций. Тимус и обучение тимоцитов. (В этом разделе цитируется Kwan J et al Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants, которая будет сдана для публикации в 2019 г.)
[0017] Тимус обычно расположен сверху сердца. Тимус обеспечивает необходимое микроокружение для развития Т-клеток и имеет решающее значение для создания и поддержания адаптивной иммунной системы (Boehm T and Takahama Y, 2014, Thymic Development and Selection of T Lymphocytes. Heidelberg: Springer-Verlag). Во время постнатального развития тимус обучает гемопоэтические стволовые клетки, мигрирующие из костного мозга в тимус.Стволовые клетки-предшественники колонизируют тимус, тем самым образуя тимоциты. После этого тимоциты проходят ряд стадий созревания. Об этом свидетельствует экспрессия ряда наблюдаемых маркеров клеточной поверхности, появляющихся на тимоцитах.
[0018] Т-клетки имеют решающее значение для защиты организма от инфекций. Т-клетки, которые развиваются в нормально функционирующем тимусе, вырабатывают разнообразный набор Т-клеточных рецепторов (обычно белков на поверхности клетки), которые позволяют зрелой Т-клетке бороться с широким спектром инфекций. Во время этого процесса обучения развивающиеся Т-клетки инструктируются тимусом не атаковать нормальные белки организма, такие как инсулин или паратиреоидный гормон (которые регулируют уровень глюкозы и кальция в крови). Эти инструкции выполняются под влиянием гена аутоиммунного регулятора («ген AIRE»).
[0019] Вкратце, процесс обучения происходит в нормально функционирующем тимусе. Эпителиальные клетки тимуса («ЭКТ») и дендритные клетки («ДК»), расположенные в тимусе, обучают тимоциты в тимусе, образованные из стволовых клеток костного мозга, не атаковать белки главного комплекса гистосовместимости (МНС) реципиента (антигены), такие как антигены HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA- DQA1, HLA-DPB1, HLA-DPA1. HLA-антигены имеют 2 белка, которые удерживают в бороздке аутопептид. Аутопептид может происходить из белка щитовидной железы или пептида инсулина, или почти любого другого белка, экспрессируемого в организме. Тимоциты, развивающиеся в тимусе, образуют Т-клеточный рецептор (TCR), состоящий из двух белков, которые пересекают мембрану. TCR экспрессируется на клеточной поверхности Т-клеток. Каждая Т-клетка экспрессирует множество копий своего уникального TCR. Если TCR слишком тесно связывается с аутопептидом:MHC на дендритной клетке, дендритные клетки посылают сигнал, в результате чего T-клетка претерпевает апоптоз и погибает.Этот механизм предотвращает развитие аутоиммунитета к собственному организму. ЭКТ может также посылать сигнал тимоцитам о том, что они слишком тесно связываются. Наконец, ДК может захватывать кусочки мембраны из ЭКТ и презентировать аутопептид ЭТК:MHC развивающемуся тимоциту. Если тимоциты связываются слишком тесно, ДК посылает сигнал, в результате чего тимоцит претерпевает апоптоз и погибает.Благодаря этим механизмам Т-клетки, покидающие тимус, не являются аутореактивными. Т-клетки, покидающие тимус, очень разнообразны и могут распознавать инфекции, но они не атакуют белки организма.
[0020] Двумя основными составляющими тимуса являются эпителий и тимоциты, которые вырабатываются в тимусе следующим образом. Клетки, полученные из стволовых клеток костного мозга, общих лимфоидных предшественников («CLP»), мигрируют в тимус.CLP поступают в тимус в ответ на сигналы (хемокины), продуцируемые эпителием и эндотелием тимуса. В тимусе CLP дифференцируются в тимоциты и пролиферируют.Тимоциты вырабатывают уникальный Т-клеточный рецептор («TCR»), который экспрессируется на клеточной поверхности. Тимоциты также начинают экспрессировать молекулы CD3, CD4 и CD8 Т-клеток. Развивается огромное разнообразие Т-клеток, что делает клетки способными реагировать на инфекции в течение всей жизни реципиента. Реакции смешанной культуры лимфоцитов показывают толерантность Т-клеток реципиента у детей, получавших лечение с помощью культивированной ткани тимуса (RVT-802), к MHC донора тимуса.
[0021] Аутореактивные тимоциты реципиента удаляются до выхода из тимуса. Это происходит при взаимодействии реципиента тимоцитов и ДК реципиента, которые мигрируют в тимус.В тимоцитах реципиента, которые слишком тесно связываются с ДК, индуцируется апоптоз в качестве меры защиты организма от аутоиммунных заболеваний. После завершения этого процесса тимоциты покидают тимус.Новые циркулирующие Т-клетки, то есть «наивные» Т-клетки, экспрессируют маркеры CD45RA и CD62L. Проточная цитометрия и спектральное типирование показали развитие разнообразного репертуара Т-клеток. Эти Т-клетки реципиента имеют разнообразные репертуары TCR и пролиферируют нормальным образом в ответ на митогены. Они защищают реципиента от инфекции, не имея аутореактивности. Продукт, полученный из аллогенной культивированной ткани постнатального тимуса.
[0022] Было показано, что продукт, полученный из аллогенной культивированной ткани постнатального тимуса, эффективен для лечения Т-клеточного иммунодефицита (первичного иммунодефицита), возникающего в результате врожденной атимии. Т-клеточный иммунодефицит из-за атимии связан с врожденными нарушениями, которые предотвращают развитие функционального тимуса, такими как полная аномалия Ди Георга (cDGA), связанная с делецией 22q11.2 и синдромом CHARGE (колобома, порок сердца, атрезия хоан, задержка роста или развития, генитальная гипоплазия и аномалии уха или глухота), связанном с мутациями в гене chd7 (геликазный хромодомен ДНК-связывающего белка 7) и у пациентов, лишенных тимуса, с дефицитом белка N1 (FOXN1). Врожденная атимия является редким смертельным заболеванием, и в настоящее время не существует вариантов ее медикаментозного лечения с использованием разрешенных к применению лекарственных препаратов. В отсутствие лечения и какого-либо терапевтического восстановления иммунной системы ребенка первичный иммунодефицит, вызванный врожденной атимией, приводит к летальному исходу, при этом почти все грудные дети умирают в возрасте до двух лет, чаще всего от тяжелых инфекций.
[0023] Продукт, полученный из аллогенной культивированной ткани постнатального тимуса, представляет собой тканеинженерный продукт.На основании сведений, приведенных в этом описании и примерах, ожидается, что КТТ будет эффективен для развития толерантности у реципиента, которому был трансплантирован цельный орган.
[0024] Как более подробно описано в данном описании и примерах, хирургическое введение продукта, полученного из аллогенной культивированной ткани постнатального тимуса (например, «RVT-802»), пациентам, лишенным тимуса, приводит к каскаду событий, приводящих к развитию функциональной иммунной системы. После хирургического введения продукта, полученного из аллогенной культивированной ткани постнатального тимуса (например, RVT-802), реципиенту, Т-клетки обучаются ЭКТ донора и ДК реципиента. ЭКТ донора в сочетании с ДК реципиента обеспечивают толерантность к имплантированной донорской ткани тимуса, которую имплантируют в виде культивированных срезов ткани тимуса. Это та же самая индукция толерантности, что и в нормальном тимусе. ЭКТ реципиента в сочетании с ДК реципиента приводят к аутотолерантности, как описано в данном описании.
[0025] Клинически было показано, что этот сложный процесс приводит к выживаемости >70% у пациентов с врожденной атимией, получивших продукт, полученный из аллогенной культивированной ткани постнатального тимуса (например, RVT-802), благодаря способности реципиента бороться с инфекциями (Markert ML, Devlin BH, Alexieff MJ, Li J, McCarthy EA, Gupton SE, et al., 2007, “Review of 54 patients with complete DiGeorge anomaly enrolled in protocols for thymus transplantation: outcome of 44 consecutive transplants,” Blood, 109(10):4539-47; Markert ML, Devlin BH, McCarthy EA. Thymus transplantation. 2010, Clin.Immunol., 135(2): 236-46). Реципиенты могут бороться с вирусными инфекциями, такими как вирус Эпштейна-Барр, которые были бы смертельными до КТТ. (Chinn IK, Devlin BH, Li YJ, & Markert ML, 2008). Обзор индукции толерантности при трансплантации цельных органов в комбинации с трансплантацией КТТ.
[0026] В соответствии с описанием, фигурами, примерами и формулой изобретения в настоящем описании автор продемонстрировал, что КТТ индуцирует донор-специфическую толерантность на модели трансплантации сердца у крысы. В описанных в настоящем документе экспериментах использовались сопоставимые методы трансплантации КТТ, которые были использованы в клинической практике у субъектов с врожденной атимией, таких как субъекты, страдающие от cDGA. У грудных детей с cDGA практически нет наивных Т-клеток до хирургического внедрения КТТ. После хирургического внедрения КТТ у грудных детей развивались наивные Т-клетки примерно через 6 месяцев после хирургического вмешательства. (Markert ML, et al., 2004, “Postnatal thymus transplantation with immunosuppression as treatment for DiGeorge syndrome,” Blood 104(8):2574-2581; Markert ML, Devlin BH, & McCarthy EA, 2010, “Thymus transplantation,” Clin Immunol 135(2):236-246). Исследования индукции толерантности на крысиной модели были основаны на результатах исследований трансплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса (КТТ), с 1993 по 2017 год у грудных детей, лишенных тимуса, с полной аномалией Ди Георга. В описанных исследованиях были получены благоприятные результаты хирургического введения КТТ у грудных детей с врожденной атимией. Опубликованные результаты показали общую выживаемость 71% (61/86) (медиана 11,7 лет, от 1,2 до 25 лет) при этом заболевании, которое в противном случае является смертельным (Markert, ML, et al., 2010). Биопсия трансплантированной культивированной ткани тимуса продемонстрировала тимопоэз по результатам иммуногистохимического исследования (Markert, ML, et al., 2008). Проточная цитометрия и спектральное типирование показали развитие разнообразного репертуара Т-клеток. Реакции смешанной культуры лимфоцитов показывают толерантность Т-клеток реципиента к донорским антигенпрезентирующим клеткам (Chinn IK, Devlin BH, Li YJ, & Markert ML, 2008).
[0027] Важно отметить, что реципиенты КТТ могут бороться с вирусными инфекциями, такими как вирус Эпштейна-Барр, которые были бы смертельными до КТТ (Markert, ML, 2014, Thymus Transplantation. Stiehm’s Immune Deficiences, eds Sullivan KE & Stiehm ER (Academic Press), 1st Ed, стр. 1059-1067). Основываясь на этих полученных у людей данных, демонстрирующих толерантность к несовпадающим антигенам MHC тимуса, провели оценку трансплантации КТТ на крысиной модели с использованием тех же методов, которые были использованы в клинической практике, на предмет ее способности индуцировать донор-специфическую толерантность на модели трансплантации сердца у крысы. Эти исследования показали, что трансплантация несоответствующих сердец вместе с КТТ донора, экспрессирующим антигены МНС I и II класса сердца донора (с первоначальным обеднением Т-клетками с помощью антител к CD5 и иммуносупрессией с помощью циклоспорина), индуцирует толерантность к антигенам сердца донора, сохраняя при этом аллореактивность по отношению к другим антигенам МНС.
[0028] Настоящее изобретение обосновывает совместную трансплантацию тимуса донора и цельных органов в качестве способа индукции толерантности к трансплантированному цельному органу у реципиента. Группой пациентов, которая получила бы наибольшую пользу от этой процедуры, являются грудные дети, нуждающиеся в трансплантации сердца. Поскольку постнатальная ткань тимуса присутствует у умерших грудных детей и может быть взята из их организма, а тимус реципиента в плановом порядке удаляют у грудных детей, подвергаемых трансплантации сердца, для переноса этого подхода в клинику не требуется никаких дополнительных процедур, кроме трансплантации культивированной ткани тимуса (КТТ).
Обзор получения продукта, полученного из аллогенной культивированной ткани постнатального тимуса
[0029] Продукт, полученный из аллогенной культивированной ткани постнатального тимуса, получают, культивируют и хранят в течение до 21 дня, а в день имплантации помещают в отдельные индивидуальные чашки для транспортировки в операционную, как более подробно описано в настоящем документе.
[0030] КТТ (культивированную ткань тимуса) асептически обрабатывают и культивируют в соответствии с действующими Правилами производства и контроля качества лекарственных средств («cGMP»), например, cGMP, установленными Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США, с получением частично обедненных Т-клетками срезов ткани тимуса. КТТ дифференцируется из нативного тимуса с помощью процесса кондиционирования, подробно описанного ниже. КТТ осуществляет нормальный процесс положительного и отрицательного отбора развивающихся Т-клеток в тимусе после имплантации, позволяя Т-клеткам быть толерантными как к тимусу донора, так и к трансплантату цельного органа донора, а также к тканям реципиента. Кроме того, эти Т-клетки могут распознавать чужеродные антигены в контексте белков основной гистосовместимости (МНС) реципиента для борьбы с инфекцией.
[0031] Способом введения является хирургическая имплантация КТТ способом, описанным ниже. Однократное введение обычно составляет от 1000 до 20000 мм2 площади поверхности КТТ на площадь поверхности тела реципиента («ПТТ») в м2. Площадь поверхности представляет собой сумму всех площадей поверхности всех культивированных срезов ткани. Отдельные срезы КТТ имплантируют за одну хирургическую процедуру введения.
[0032] Хирургическая имплантация продукта, полученного из аллогенной культивированной ткани постнатального тимуса, у пациентов, лишенных тимуса, приводит к каскаду событий, приводящих к развитию функциональной иммунной системы. (Markert ML, 2007; Markert ML, et al., 2010; Markert ML, Devlin BH, McCarthy EA. Chapter 84 Thymic reconstitution. 2013. В: Fleisher TA, Shearer WT, Schroeder HW, Frew AJ, Weyand CM, editors. Clinical Immunology (Fourth Edition). Лондон; стр. 1032-8).
[0033] CLP реципиента из костного мозга мигрируют к донорскому трансплантату тимуса. Донорский трансплантат тимуса обеспечивает микроокружение, в котором тимоциты реципиента вырабатывают широкий репертуар TCR, способных распознавать патогены.
[0034] Миграция ДК реципиента в тимус донора истощает аутореактивные тимоциты реципиента, которые атаковали бы ткани реципиента после того, как новые Т-клетки покинут тимус и поступят в кровообращение. Генетически реципиентные наивные Т-клетки появляются в кровотоке примерно через 5-12 месяцев после введения. Эти Т-клетки реципиента имеют разнообразные репертуары TCR и пролиферируют нормальным образом в ответ на митогены. Они защищают реципиента от инфекции, не имея аутореактивности.
[0035] CLP костного мозга реципиента мигрируют в аллотрансплантат тимуса, где они развиваются в Т-клетки реципиента. Отрицательный отбор по ДК реципиента, которые мигрировали в тимус донора, приводит к толерантности к антигенам МНС реципиента. Иммуногистохимические признаки тимопоэза наблюдаются при биопсии трансплантированной культивированной ткани тимуса, взятой по прошествии примерно 2-3 месяцев после трансплантации. Тимопоэз отражает способность Т-клеток защищаться от инфекций и бороться с ними, а также предотвращать аутоиммунные заболевания.
[0036] Наивные Т-клетки обнаруживаются в кровообращении через 5-12 месяцев после трансплантации, что дает возможность защищаться от инфекций и бороться с ними, а также предотвращать аутоиммунные заболевания.
[0037] Автор изобретения впервые продемонстрировал, что имплантация культивированной ткани тимуса эффективна при лечении первичного иммунодефицита, возникающего в результате врожденной атимии, связанной с такими состояниями, как полная аномалия Ди Георга (cDGA) или дефицит белка FOXN1 (forkhead box protein N1). Автор изобретения обнаружил, что замена дефектной ткани тимуса нормальной тканью тимуса после культивирования (например, КТТ и RVT-802) может также устранить отсутствие толерантности, наблюдаемое у реципиентов трансплантированных цельных органов.
[0038] Доклиническая и клиническая работа, лежащая в основе лечения врожденной атимии путем внедрения культивированной ткани тимуса, привела к осознанию того, что внедрение КТТ (например, RVT-802) у пациентов может способствовать развитию толерантности к трансплантированному цельному органу. В частности, внедрение КТТ будет восстанавливать иммунную систему и индуцировать толерантность к донорскому органу, если субъекта сначала подвергают тимэктомии и иммуносупрессии до имплантации КТТ, экспрессирующего MHC органа донора.
[0039] Измерение экспрессии и распределения определенных маркеров, связанных с клеточными компонентами тимуса, позволяет установить фенотип ex vivo. Условия культивирования, описанные в данном описании и примерах, подтверждают наблюдение тимопоэза in vivo после внедрения КТТ субъекту, лишенному тимуса.
[0040] Важно отметить, что после хирургического внедрения КТТ реципиенту, лишенному тимуса, развитие наивных Т-клеток и присутствие широкого спектра TCR- вариабельных областей дает четкое доказательство того, что культивирование ткани тимуса может способствовать развитию функциональной эндогенной популяции Т-клеток. Кроме того, в ткани тимуса во время культивирования была отмечена экспрессия ключевых регуляторных и структурных генов. Циркулирующие наивные (CD45RA+CD62L+) Т-клетки могут быть впервые обнаружены через 3-5 месяцев после хирургического внедрения КТТ. Эти наблюдения были отмечены при лечении пациентов с полной аномалией Ди Георга (Markert ML, 2010; Markert ML. 2013).
[0041] Доклинические данные, описанные в литературе для имплантации ткани тимуса, согласуются с надежной клинической эффективностью трансплантации аллогенной культивированной ткани постнатального тимуса и обосновывают ее применение у людей. (Markert ML, Watson TJ, Kaplan I, Hale LP, Haynes BF, 1997, “The human thymic microenvironment during organ culture,” Clin Immunol Immunopathol. Jan; 82(1):2 6-36; Hong R, Schulte-Wissermann H, Jarrett-Toth E, Horowitz SD, Manning DD, 1979, “Transplantation of cultured thymic fragments. II. Results in nude mice,” J Exp Med., 149(2): 398-415. Li B, Li J, Hsieh CS, Hale LP, Li YJ, Devlin BH, Markert ML, 2009, “Characterization of cultured thymus tissue used for transplantation with emphasis on promiscuous expression of thyroid tissue- specific genes,” Immunol Res. 2009; 44 (1-3):71-83; Li B, Li J, Devlin BH, Markert ML, 2011, “Thymic microenvironment reconstitution after postnatal human thymus transplantation,” Clin Immunol., Sep; 140(3): 244-59).
[0042] Пациенты с полной аномалией Ди Георга имеют дефекты трех желез, которые развиваются в области шеи несформировавшегося зародыша, сердца, тимуса и паращитовидных желез. Обычно сердце и тимус опускаются в грудь, а паращитовидные железы, которые регулируют уровень кальция, остаются в шее. Лечение субъектов с cDGA с помощью КТТ привело к выживаемости в двухлетнем возрасте, равной 75%, по сравнению с выживаемостью 6% у не проходящих лечение субъектов (неопубликованные данные). Согласно литературным данным дети обычно умирают в течение двух лет при отсутствии лечения. (Markert, et al., 2010). Следует отметить, что имплантация КТТ не влияет на проблемы с сердцем и паращитовидной железой, которые должны решаться отдельно.
[0043] Первый аспект настоящего изобретения относится к хирургическому внедрению аллогенного культивированного продукта, полученного из постанатальной ткани тимуса, реципиенту, для индукции толерантности к трансплантату цельного органа у иммунологически нормального реципиента. Такие способы включают, состоят из или по существу состоят из удаления тимуса у иммунокомпетентного реципиента с последующим обеднением Т-клетками реципиента с помощью индукционного иммуносупрессивного режима, включающего один или более иммуносупрессивных препаратов, таких как одно или более антител и/или один или более ингибиторов кальциневрина. Индукционный иммуносупрессивный режим вводят в терапевтически эффективном количестве для обеднения субъекта зрелыми Т-клетками и/или для подавления отторжения трансплантированного цельного органа Т-клетками реципиента. Получают подходящий цельный орган человека и тимус от умершего донора, и трансплантируют указанный цельный орган реципиенту. В течение некоторого периода времени вводят поддерживающий иммуносупрессивный режим для подавления отторжения трансплантата. Тимус от умершего донора подвергают режиму кондиционирования на период до 21 дня для асептической обработки донорской ткани тимуса в органной среде для тимуса с получением срезов донорской ткани тимуса, частично обедненных Т-клетками, в результате чего образуется продукт, полученный из аллогенной культивированной ткани постнатального тимуса. Частично обедненные Т-клетками срезы донорской ткани тимуса демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер. Затем продукт, полученный из аллогенной культивированной ткани постнатального тимуса, хирургическим путем помещают реципиенту, обычно в четырехглавую мышцу бедра. Продукт, полученный из аллогенной культивированной ткани постнатального тимуса, позволяет реципиенту вырабатывать наивные Т-клетки после имплантации. Все новые развивающиеся Т-клетки являются генетически реципиентными и толерантными как к реципиенту, так и к донору. Дозировка срезов ткани тимуса составляет приблизительно 1000-20000 мм2 площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2. После имплантации продукт, полученный из аллогенной культивированной ткани постнатального тимуса, вызывает у субъекта тимопоэз и толерантность.
[0044] Если рассматривать в качестве примера трансплантат сердца, донором будет умерший донор. Тимус будет удален у донора одновременно с удалением сердца. Трансплантацию сердца проводят немедленно с индукционной иммуносупрессией для уменьшения числа Т-клеток и подавления оставшихся Т-клеток реципиента, предотвращая их атаку на донорское сердце. Тимус донора обрабатывают с образованием продукта, полученного из человеческой аллогенной культивированной ткани постнатального тимуса, который может быть использован для имплантации для индукции толерантности по истечении от по меньшей мере 12 до приблизительно 21 дня кондиционирования. В качестве меры предосторожности примерно половина продукта, полученного из аллогенной культивированной ткани постнатального тимуса, может быть подвергнута криоконсервации после кондиционирования, чтобы в случае возникновения проблемы с последующим отторжением сердца, требующей введения высоких доз стероидов или других иммуносупрессивных препаратов для лечения отторжения, при котором очень высокие дозы стероидов повреждают продукт, полученный из аллогенной культивированной ткани постнатального тимуса, криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, был бы доступен для имплантации после того, как эпизод отторжения будет взят под контроль.
[0045] Важно отметить, что после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса, иммунная толерантность сохраняется даже при наличии инфекций. При других подходах, таких как костимулирующая блокада, вирусные инфекции могут привести к потере толерантности, поскольку примерно треть CD8 Т-клеток обладает аллореактивностью. Когда иммунная система активируется для борьбы с инфекцией, аллореактивные CD8 Т-клетки начинают отторгать трансплантат цельного органа. Напротив, при использовании ткани тимуса, обработанной с получением продукта, полученного из аллогенной культивированной ткани постнатального тимуса, для индукции толерантности, все потенциально аллореактивные Т-клетки, направленные против донора, удаляются посредством процесса отрицательного отбора.
[0046] В одном варианте осуществления донорская ткань тимуса соответствует аллелям HLA в органе донора, отсутствующим у реципиента. Все новые развивающиеся Т-клетки являются генетически реципиентными и толерантными как к реципиенту, так и к донору.
[0047] Во втором аспекте настоящего изобретения предложен способ стимуляции донор-специфической толерантности к аллогенному трансплантату цельного органа, полученному от умершего донора, у реципиента, нуждающегося в трансплантации цельного органа, включающий следующие стадии:
(a) удаление тимуса у реципиента;
(b) применение к указанному реципиенту схемы индукции иммуносупрессии, включающей один или более иммуносупрессивных препаратов, для истощения Т- клеток указанного реципиента и/или для подавления способности Т-клеток указанного реципиента отторгать трансплантированный цельный орган;
(c) обеспечение как подходящего цельного органа человека, так и тимуса от умершего донора;
(d) трансплантацию цельного органа человека реципиенту;
(e) применение к указанному реципиенту схемы поддержания иммуносупрессии;
(f) обеспечение продукта, полученного из аллогенной культивированной ткани постнатального тимуса, где указанный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, получен из подходящей ткани тимуса донора цельного органа; где донорскую ткань тимуса подвергают режиму кондиционирования на период до 21 дня с получением продукта, полученного из аллогенной культивированной ткани постнатального тимуса; дополнительно где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов донорской ткани тимуса; где частично обедненные Т-клетками срезы донорской ткани тимуса демонстрируют области, положительные на цитокератин (CK) (с использованием антитела AE1/AE3), рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер; и
(g) имплантацию продукта, полученного из аллогенной культивированной ткани постнатального тимуса, реципиенту по истечении от 12 до 21 дня режима кондиционирования, где дозировка срезов ткани тимуса составляет приблизительно 1000-20000 мм2 площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у реципиента.
[0048] В одном варианте осуществления предложен способ стимулирования донор-специфической толерантности к аллогенному трансплантату сердца у реципиента, нуждающегося в сердце от умершего донора. Способ включает следующие стадии:
(a) получение подходящего человеческого сердца от умершего донора для трансплантации;
(b) удаление тимуса у умершего донора одновременно с получением сердца для кондиционирования с получением продукта, полученного из аллогенной культивированной ткани постнатального тимуса; где тимус донора соответствует аллелям HLA в трансплантированном органе донора;
(c) применение к указанному реципиенту схемы индукции иммуносупрессии, включающей один или более иммуносупрессивных препаратов, для истощения Т-клеток указанного реципиента и/или для подавления их активности, где один или более иммуносупрессивных препаратов включают глюкокортикоиды, вводимые при индукции анестезии и после реперфузии;
(d) трансплантацию сердца реципиенту;
(e) применение к указанному реципиенту схемы поддержания иммуносупрессии, включающим один или более иммуносупрессивных препаратов, выбранных из группы, состоящей из ингибитора кальциневрина, ингибитора инозинмонофосфат дегидрогеназы и антитимоцитарного глобулина в течение периода времени, достаточного для предотвращения или подавления отторжения трансплантата сердца;
(f) в период с 12 до 21 дня обеспечение аллогенного культивированного продукта, полученного из ткани постнатального тимуса, полученного из донорской ткани тимуса; где донорскую ткань тимуса подвергают режиму кондиционирования на период от приблизительно 12 до приблизительно 21 дня с получением аллогенного культивированного продукта, полученного из ткани постнатального тимуса; дополнительно где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов донорской ткани тимуса; где частично обедненные Т-клетками срезы донорской ткани тимуса демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер;
(g) имплантацию части продукта, полученного из аллогенной культивированной ткани постнатального тимуса, реципиенту, где дозировка срезов ткани тимуса составляет приблизительно 1000-20000 мм2 площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у реципиента; и
(h) криоконсервация части продукта, полученного из аллогенной культивированной ткани постнатального тимуса, для использования у реципиента в случае раннего эпизода отторжения, требующего высоких доз стероидов, которые повредили бы часть продукта, полученного из аллогенной культивированной ткани постнатального тимуса, имплантированную на стадии (g).
[0049] В одном варианте осуществления предложен способ стимулирования донор- специфической толерантности к аллогенному трансплантату сердца у реципиента, нуждающегося в сердце от умершего донора. Способ включает следующие стадии:
(a) получение подходящего цельного человеческого сердца от умершего донора для трансплантации;
(b) удаление тимуса у умершего донора одновременно с получением сердца для кондиционирования с получением продукта, полученного из аллогенной культивированной ткани постнатального тимуса; где тимус донора соответствует аллелям HLA в трансплантированном органе донора;
(c) применение к указанному реципиенту схемы индукции иммуносупрессии, включающей один или более иммуносупрессивных препаратов, для истощения Т-клеток указанного реципиента и/или для подавления их активности, где один или более иммуносупрессивных препаратов включают глюкокортикоиды, вводимые при индукции анестезии и после реперфузии;
(d) хирургическое удаление сердца и тимуса реципиента;
(e) трансплантацию человеческого сердца донора реципиенту;
(f) применение к указанному реципиенту схемы поддержания иммуносупрессии, включающим один или более иммуносупрессивных препаратов, выбранных из группы, состоящей из ингибитора кальциневрина, ингибитора инозинмонофосфат дегидрогеназы и антитимоцитарного глобулина в течение периода времени, достаточного для предотвращения или подавления отторжения трансплантата сердца; где если послеоперационное состояние реципиента слишком нестабильно, чтобы можно было постепенно прекратить введение глюкокортикоидов и безопасно имплантировать реципиенту продукт, полученный из аллогенной культивированной ткани постнатального тимуса, указанный продукт подвергают криоконсервации для последующей имплантации, когда состояние реципиента стабилизируется, где донорскую ткань тимуса подвергают режиму кондиционирования на период от приблизительно 12 до приблизительно 21 дня с получением продукта, полученного из аллогенной культивированной ткани постнатального тимуса; дополнительно где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса органной среде для тимуса с получением частично обедненных Т-клетками срезов донорской ткани тимуса; где частично обедненные Т-клетками срезы донорской ткани тимуса демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер;
(h) имплантацию части продукта, полученного из аллогенной культивированной ткани постнатального тимуса, реципиенту после того, как состояние пациента стабилизируется, где дозировка срезов ткани тимуса составляет приблизительно 1000-20000 мм2 площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у реципиента; и
(i) криоконсервация части продукта, полученного из аллогенной культивированной ткани постнатального тимуса, для использования у реципиента в случае эпизода отторжения, требующего высоких доз стероидов, которые повредили бы часть продукта, полученного из аллогенной культивированной ткани постнатального тимуса, имплантированную на стадии (h).
[0050] В третьем аспекте настоящего изобретения предложен способ стимуляции донор- специфической толерантности к аллогенному трансплантату цельного органа, полученному от живого донора, представляющего собой человека, у реципиента, представляющего собой человека, нуждающегося в трансплантации цельного органа, включающий следующие стадии:
(a) удаление тимуса у реципиента;
(b) лечение реципиента индукционным иммуносупрессивным режимом, включающим один или более иммуносупрессивных препаратов, для обеднения Т-клетками реципиента и/или для подавления отторжения трансплантированного цельного органа Т-клетками реципиента;
(c) обеспечение подходящего цельного органа от живого донора, представляющего собой человека;
(d) трансплантацию указанного цельного органа реципиенту;
(e) применение к указанному реципиенту схемы поддержания иммуносупрессии;
(f) обеспечение криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, хранящегося в банке криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса; где криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, был получен путем обработки ткани тимуса от донора тимуса, экспрессирующего аллели HLA, совпадающие с аллелями HLA у реципиента, которые отсутствуют в трансплантате цельного органа; где донорская ткань тимуса была подвергнута режиму кондиционирования на период до 12 дней; дополнительно где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов ткани тимуса, где срезы ткани тимуса по завершении режима кондиционирования демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер;
(g) размораживание криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса; и
(h) имплантацию размороженного криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, реципиенту, где дозировка криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, составляет приблизительно 1000-20000 мм2 площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у реципиента.
[0051] В четвертом аспекте настоящего изобретения предложен способ стимуляции донор-специфической толерантности к аллогенному трансплантату цельного органа, полученному от умершего донора, представляющего собой человека, у реципиента, представляющего собой человека, нуждающегося в трансплантации цельного органа, включающий следующие стадии:
(a) удаление тимуса у реципиента;
(b) применение к указанному реципиенту схемы индукции иммуносупрессии, включающей один или более иммуносупрессивных препаратов, для истощения Т-клеток указанного реципиента и/или для подавления способности Т-клеток указанного реципиента отторгать трансплантированный цельный орган;
(c) обеспечение подходящего цельного органа от живого донора, представляющего собой человека;
(d) трансплантацию указанного цельного органа реципиенту;
(e) применение к указанному реципиенту схемы поддержания иммуносупрессии;
(f) обеспечение криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, хранящегося в банке криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса; где криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, получен путем обработки ткани тимуса от донора тимуса, экспрессирующего аллели HLA, совпадающие с аллелями HLA у реципиента, которые отсутствуют в трансплантате цельного органа; где донорская ткань тимуса была подвергнута режиму кондиционирования на период до 12 дней; дополнительно где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов ткани тимуса, где срезы ткани тимуса по завершении режима кондиционирования демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер;
(g) размораживание криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса; и
(h) имплантацию размороженного криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, реципиенту, где дозировка криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, составляет приблизительно 1000-20000 мм2 площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у реципиента.
[0052] В одном варианте осуществления со второго по четвертый аспектов настоящего изобретения предложен продукт, полученный из аллогенной культивированной ткани постнатального тимуса, по п. 63 формулы, где тимус в день сбора демонстрирует, что >50% областей являются положительными на кератин, о чем свидетельствует кружевовидный рисунок окрашивания, присутствуют тельца Гассаля, что окрашивание на CK14 обеспечивает кружевовидный рисунок, и что >90% ядер являются интактными.
[0053] Пятый аспект настоящего изобретения относится к продукту, полученному из аллогенной культивированной ткани постнатального тимуса, для имплантации субъекту, подвергаемому трансплантации цельного органа, полученному путем получения подходящей ткани тимуса от донора, где донорскую ткань тимуса подвергают режиму кондиционирования на период до 21 дня; дополнительно где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов донорской ткани тимуса; где срезы донорской ткани тимуса демонстрируют, между 5 и 9 днями после сбора, области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер; извлечение частично обедненных Т-клетками срезов донорской ткани тимуса в качестве продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
[0054] В одном варианте осуществления тимус в день сбора демонстрирует, что >50% областей являются положительными на кератин, о чем свидетельствует кружевовидный рисунок окрашивания, присутствуют тельца Гассаля, что окрашивание на CK14 обеспечивает кружевовидный рисунок, и что>90% ядер являются интактными.
[0055] В одном варианте осуществления пятого аспекта настоящего изобретения продукт, полученный из аллогенной культивированной ткани постнатального тимуса, подвергают криоконсервации.
[0056] В одном варианте осуществления криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, хранят в жидком азоте для будущего использования.
[0057] В еще одном варианте осуществления криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, хранят в банке криоконсервированных тканей.
[0058] В одном варианте осуществления продукт, полученный из аллогенной культивированной ткани постнатального тимуса, получают из подходящей ткани тимуса от донора, содержащего аллели HLA, совпадающие с аллелями HLA у предполагаемого реципиента, отсутствующие в трансплантате цельного органа.
[0059] В одном варианте осуществления аллели HLA представляют собой: HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DRB3, HLA-DRB4, HLA-DRB5, HLA- DQA1, HLA- DPB1, HLA-DPA1.
[0060] Шестым аспектом настоящего изобретения является криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, полученный способом, включающим следующие стадии:
(a) получение подходящей ткани тимуса от донора;
(b) типирование аллелей HLA: HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DRB3, HLA-DRB4, HLA-DRB5, HLA-DQA1, HLA-DPB1, HLA-DPA1;
(c) подвергание ткани тимуса режиму кондиционирования на период до 12 дней; где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных T-клетками срезов донорской ткани тимуса; дополнительно где по завершении режима кондиционирования срезы донорской ткани тимуса демонстрируют, на 5-9 день, области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер;
(d) сбор частично обедненных T-клетками срезов донорской ткани тимуса в качестве продукта, полученного из аллогенной культивированной ткани постнатального тимуса;
(e) криоконсервация продукта, полученного из аллогенной культивированной ткани постнатального тимуса, в жидком азоте; и
(f) хранение криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, в жидком азоте в банке криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
[0061] В одном варианте осуществления тимус в день сбора демонстрирует, что >50% областей являются положительными на кератин, о чем свидетельствует кружевовидный рисунок окрашивания, присутствуют тельца Гассаля, что окрашивание на CK14 обеспечивает кружевовидный рисунок, и что >90% ядер являются интактными.
[0062] В одном варианте осуществления криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, в жидком азоте хранится реципиентом для будущего использования.
[0063] Седьмой аспект настоящего изобретения относится к способу подготовки тимуса донора для трансплантации реципиенту. Такие способы включают, состоят из или по существу состоят из культивирования тимуса донора в течение вплоть до приблизительно 5 дней, вплоть до приблизительно 6 дней, вплоть до приблизительно 7 дней, вплоть до приблизительно 8 дней, вплоть до приблизительно 9 дней, вплоть до приблизительно 10 дней, вплоть до приблизительно 11 дней, вплоть до приблизительно 12 дней, вплоть до приблизительно 13 дней, вплоть до приблизительно 14 дней, вплоть до приблизительно 15 дней, вплоть до приблизительно 16 дней, вплоть до приблизительно 17 дней, вплоть до приблизительно 18 дней, вплоть до приблизительно 19 дней, вплоть до приблизительно 20 дней или вплоть до приблизительно 21 дня, а затем помещение культивированной ткани тимуса в организм реципиента хирургическим путем, как дополнительно описано в настоящем документе. Период культивирования от приблизительно 6 до приблизительно 12 дней обеспечивает хорошую функцию. Для успешной трансплантации криоконсервированной ткани тимуса ткань обычно культивируют в течение от приблизительно 6 до приблизительно 12 дней, а затем подвергают криоконсервации.
[0064] Восьмой аспект настоящего изобретения относится к продукту, полученному из аллогенной культивированной ткани постнатального тимуса (КТТ; RVT-802), для имплантации субъекту, подвергаемому трансплантации цельного органа, изготовленному способом подвергания ткани тимуса от подходящего донора режиму кондиционирования на период до 21 дня; где режим кондиционирования для продукта, полученного из аллогенной культивированной ткани постнатального тимуса, включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов ткани тимуса, где срезы ткани тимуса демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по крайней мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер.
[0065] В одном варианте осуществления восьмого аспекта тимус донора в день сбора демонстрирует, что >50% областей являются положительными на кератин, о чем свидетельствует кружевовидный рисунок окрашивания, присутствуют тельца Гассаля, что окрашивание на CK14 обеспечивает кружевовидный рисунок, и что >90% ядер являются интактными.
[0066] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения тимус реципиента получают хирургическим путем.
[0067] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения тимус реципиента получают с помощью роботизированной хирургии.
[0068] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения тимус реципиента получают с помощью торакоскопической хирургии.
[0069] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения цельный орган представляет собой часть целого органа.
В одном варианте осуществления способ с первого по четвертый аспектов дополнительно включает стадию криоконсервации мононуклеарных клеток периферической крови от умершего донора для будущего использования в реакции смешанной культуры лимфоцитов для демонстрации клеточной толерантности.
[0070] В одном варианте осуществления реакцию смешанной культуры лимфоцитов для демонстрации клеточной толерантности проводят с использованием мононуклеарных клеток периферической крови от реципиента и криоконсервированных мононуклеарных клеток периферической крови от донора после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса, в соответствии с процедурой имплантации КТТ согласно данному описанию.
[0071] В одном варианте осуществления реакцию смешанной культуры лимфоцитов для демонстрации клеточной толерантности проводят с мононуклеарными клетками периферической крови от реципиента и криоконсервированными мононуклеарными клетками периферической крови от донора приблизительно через 6-12 месяцев после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
[0072] В одном варианте осуществления реакцию смешанной культуры лимфоцитов для демонстрации клеточной толерантности проводят с мононуклеарными клетками периферической крови от реципиента иа криоконсервированными мононуклеарными клетками периферической крови от донора после того, как количество наивных Т-клеток достигает 10% от общего количества Т-клеток у реципиента.
В одном варианте осуществления с первого по четвертый аспектов имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз у субъекта в течение 12 месяцев после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
[0073] В одном варианте осуществления с первого по четвертый аспектов развитие толерантности определяют с помощью реакции смешанной культуры лимфоцитов, проводимой с криоконсервированными мононуклеарными клетками периферической крови от умершего донора и наивными Т-клетками от реципиента.
[0074] В одном варианте осуществления с первого по четвертый аспектов гуморальную толерантность определяют по развитию гуморального иммунитета и отсутствию донор-специфических антител.
[0075] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения трансплантат цельного органа представляет собой трансплантат сердца, трансплантат почки, трансплантат печени, трансплантат легкого, трансплантат сердца/легкого, трансплантат поджелудочной железы, трансплантат кишечника, трансплантат желудка, трансплантат брюшной стенки, черепно-лицевой трансплантат, трансплантат волосистой части головы, трансплантат полового члена, трансплантат матки, односторонний или двусторонний трансплантат верхних конечностей, односторонний васкуляризированный композитный аллотрансплантат или их комбинацию.
[0076] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения способ дополнительно включает оценку реципиента на индекс панель- реактивных антител («PRA») HLA I класса или HLA II класса до трансплантации цельного органа.
[0077] В одном варианте осуществления трансплантат цельного органа представляет собой трансплантат сердца.
[0078] В одном варианте осуществления трансплантат цельного органа представляет собой трансплантат сердца ребенка.
[0079] В одном варианте осуществления трансплантат цельного органа представляет собой трансплантат сердца взрослого.
[0080] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения способ дополнительно включает оценку реципиента на индекс панель- реактивных антител («PRA») HLA I класса или HLA II класса до трансплантации цельного органа.
[0081] В одном варианте осуществления у реципиентов с HLA-антителами проводят перекрестную пробу на совместимость с потенциальными донорами.
[0082] В одном варианте осуществления реципиентов с HLA-антителами проводят виртуальную перекрестную пробу на совместимость с потенциальными донорами с помощью UNET.
[0083] В дополнительном варианте осуществления, если зарегистрирован индекс PRA >20% в виртуальной перекрестной пробе на совместимость, способ дополнительно будет включать стадию проведения плазмафереза в операционной во время трансплантации цельного органа реципиенту.
[0084] В дополнительном варианте осуществления, если зарегистрирован индекс PRA>70% в виртуальной перекрестной пробе на совместимость, способ дополнительно будет включать стадию фактического проведения перекрестной пробы на совместимость потенциального донора и проведение плазмафереза в операционной во время трансплантации цельного органа реципиенту. Как правило, трансплантации в этих условиях не проводят из-за плохих показателей успешности.
[0085] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения способ дополнительно включает стадию оценки реципиентов с HLA-антителами путем проведения виртуальной перекрестной пробы на совместимость с помощью UNET.
[0086] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения способ дополнительно включает проведение плазмафереза в операционной во время трансплантации цельного органа реципиенту, если индекс панель-реактивных антител против HLA составляет >20%.
[0087] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения способ дополнительно включает стадию проведения фактической перекрестной пробы на совместимость потенциального донора и проведение плазмафереза в операционной во время трансплантации цельного органа реципиенту, если индекс панель-реактивных антител против HLA составляет >70%.
[0088] В одном варианте осуществления цельный орган является совпадающим по HLA, например, для живых родственных донора и реципиента для трансплантата почки, частичного трансплантата печени и частичного трансплантата кишечника.
[0089] В еще одном варианте осуществления цельный орган является несовпадающим по HLA.
[0090] В одном варианте осуществления цельный орган является совпадающим по HLA. В еще одном варианте осуществления совпадение HLA определяют путем типирования аллелей HLA: HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DRB3, HLA-DRB4, HLA-DRB5, HLA-DQA1, HLA- DPB1, HLA-DPA1 у донора и реципиента.
[0091] В одном варианте осуществления трансплантаты цельных органов совместимы по группе крови.
[0092] В еще одном варианте осуществления цельный орган является несовпадающим по HLA. В одном варианте осуществления несовпадение по HLA определяют путем типирования HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DQA1, HLA-DPB1, HLA-DPA1 у донора и реципиента.
[0093] В одном варианте осуществления культивированные срезы ткани тимуса хирургически имплантируют в четырехглавую мышцу бедра субъекта.
[0094] В одном варианте осуществления культивированные срезы ткани тимуса хирургически имплантируют в организм субъекта в область, отличную от четырехглавой мышцы.
[0095] В одном варианте осуществления часть продукта, полученного из аллогенной культивированной ткани постнатального тимуса, хирургическим путем имплантируют в четырехглавую мышцу бедра реципиента.
[0096] В еще одном варианте осуществления оставшуюся часть продукта, полученного из аллогенной культивированной ткани постнатального тимуса, подвергают криоконсервации в жидком азоте для будущей трансплантации.
[0097] В одном варианте осуществления режим кондиционирования осуществляют в течение периода от приблизительно 12 дней до приблизительно 21 дня.
[0098] В одном варианте осуществления период кондиционирования донорской ткани тимуса составляет от приблизительно 5 дней до приблизительно 21 дня, или приблизительно 5 дней, или приблизительно 6 дней, или приблизительно 7 дней, или приблизительно 8 дней, или приблизительно 9 дней, или приблизительно 10 дней, или приблизительно 11 дней, или приблизительно 12 дней, или приблизительно 13 дней, или приблизительно 14 дней, или приблизительно 15 дней, или приблизительно 16 дней, или приблизительно 17 дней, или приблизительно 18 дней, или приблизительно 19 дней, или приблизительно 20 дней, или приблизительно 21 день.
[0099] Специалисту в данной области будет ясно, что в данной области техники известно множество потенциальных индукционных иммуносупрессивных режимов и поддерживающих иммуносупрессивных режимов, и что специалист в данной области может без труда выбрать подходящий индукционный и поддерживающий иммуносупрессивный препарат.Следующие иллюстративные индукционные иммуносупрессивные режимы и поддерживающие иммуносупрессивные режимы являются примерами практического осуществления способов с первого по четвертый аспектов изобретения и подтверждают возможность осуществления заявленных изобретений.
[00100] В одном варианте осуществления с первого по четвертый аспектов изобретения индукционный иммуносупрессивный режим включает индукционный иммуносупрессивный препарат, выбранный из группы, состоящей из глюкокортикоида, антитимоцитарного глобулина (кроличьего), антитимоцитарного глобулина (лошадиного) и алемтузумаба.
[00101] В еще одном варианте осуществления АТГ представляет собой антитимоцитарный глобулин (кроличий).
[00102] В одном варианте осуществления индукционный иммуносупрессивный режим включает введение глюкокортикоида. В одном варианте осуществления глюкокортикоид включает метилпреднизолон. В еще одном варианте осуществления глюкокортикоид представляет собой метилпреднизолона натрия сукцинат.В дополнительном варианте осуществления метилпреднизолона натрия сукцинат вводят внутривенно в дозе не более 4 мг/кг/сут.
[00103] В одном варианте осуществления индукционный иммуносупрессивный режим включает антитимоцитарный глобулин кроличьего происхождения. В еще одном варианте осуществления антитимоцитарный глобулин кроличьего происхождения вводят внутривенно в дозе приблизительно 1,5 мг/кг.В дополнительном варианте осуществления антитимоцитарный глобулин вводят ежедневно в течение четырех дней. В еще одном варианте осуществления АТГ представляет собой АТГ лошадиного происхождения.
[00104] В одном варианте осуществления индукционный иммуносупрессивный режим включает базиликсимаб. В еще одном варианте осуществления базиликсимаб вводят в дозе 10 мг внутривенно реципиентам с массой тела менее 35 кг.В еще одном варианте осуществления базиликсимаб вводят в дозе 20 мг внутривенно реципиентам с массой тела более 35 кг.
[00105] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения второй иммуносупрессивный режим включает один или более иммуносупрессивных препаратов, выбранных из группы, состоящей из глюкокортикоида, ингибитора кальциневрина, ингибитора инозинмонофосфат дегидрогеназы, азатиоприна и антитимоцитарного глобулина («АТГ»).
[00106] В одном варианте осуществления иммуносупрессивный препарат в составе поддерживающего иммуносупрессивного режима представляет собой антитимоцитарный глобулин (АТГ).
[00107] В одном варианте осуществления АТГ вводят внутривенно в дозе приблизительно 1,5 мг/кг в течение периода от 3 до 14 дней, начиная с введения в операционной.
[00108] В одном варианте осуществления антитимоцитарный глобулин вводят ежедневно в течение 3-14 дней в дозе приблизительно 15 мг/кг/сут путем внутривенного введения.
[00109] В одном варианте осуществления первый иммуносупрессивный режим включает алемтузумаб.
[00110] В еще одном варианте осуществления алемтузумаб вводят в дозе приблизительно 0,25 мг/кг в течение 4 дней внутривенно реципиентам с массой тела менее 35 кг. В еще одном варианте осуществления алемтузумаб вводят в дозе приблизительно от 3 до 20 мг в течение 4 дней внутривенно реципиентам с массой тела более 35 кг.
[00111] В одном варианте осуществления второй иммуносупрессивный режим включает один или более иммуносупрессивных препаратов, выбранных из группы, состоящей из ингибитора кальциневрина и ингибитора инозинмонофосфат дегидрогеназы или азатиоприна.
[00112] В одном варианте осуществления иммуносупрессивный препарат в составе поддерживающего иммуносупрессивного режима представляет собой ингибитор кальциневрина.
В одном варианте осуществления иммуносупрессивный препарат в составе поддерживающего иммуносупрессивного режима представляет собой ингибитор инозинмонофосфат дегидрогеназы.
[00113] В одном варианте осуществления иммуносупрессивный режим включает ингибитор инозинмонофосфат дегидрогеназы, например, мофетила микофенолат.В одном варианте осуществления мофетила микофенолат вводят внутривенно в дозе от приблизительно 15 до приблизительно 25 мг/кг. В одном варианте осуществления мофетила микофенолат вводят внутривенно два-три раза в сутки.
[00114] В еще одном варианте осуществления ингибитор инозинмонофосфат дегидрогеназы представляет собой микофеноловую кислоту. В еще одном варианте осуществления микофеноловую кислоту вводят в дозе от приблизительно 25 до приблизительно 50 мг/кг в 2 или 3 дробных дозах.
[00115] В одном из вариантов осуществления микофеноловую кислоту вводят в дозе для детей, составляющей приблизительно 400 мг/м2/доза дважды в сутки с максимальной дозой 720 мг, или для ППТ от 1,19 до 1,59 м2 - в дозе приблизительно 540 мг дважды в сутки, или для ППТ>1,58 м2 - в дозе приблизительно 720 мг дважды в сутки.
[00116] В одном варианте осуществления мофетила микофенолат вводят в дозе от приблизительно 15 до приблизительно 25 мг/кг/доза дважды в сутки для детей или приблизительно 1500 мг перорально или внутривенно дважды в сутки для взрослых, с корректировкой при WBC>3500.
[00117] В одном варианте осуществления с первого по четвертый аспектов настоящего изобретения второй иммуносупрессивный режим может дополнительно включать глюкокортикоид, выбранный из группы, состоящей из метилпреднизолона, преднизона и преднизолона. В одном варианте осуществления дозу глюкокортикоида поддерживают ниже 4 мг/кг/сут.
[00118] В одном варианте осуществления глюкокортикоид вводят в постепенно снижающейся дозировке, как описано в других местах настоящего описания.
[00119] В еще одном варианте осуществления с первого по четвертый аспектов настоящего изобретения ингибитор кальциневрина представляет собой такролимус.В еще одном варианте осуществления ингибитор кальциневрина представляет собой циклоспорин А.
[00120] В еще одном варианте осуществления с первого по четвертый аспектов настоящего изобретения введение второго иммуносупрессивного режима постепенно прекращают после того, как количество наивных Т-клеток достигает 10% от общего количества Т-клеток. В еще одном варианте осуществления второй иммуносупрессивный режим постепенно прекращают после трансплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[00121] Для более полного понимания принципов, раскрытых в настоящем документе, и их преимуществ приводится следующее далее подробное описание со ссылкой на прилагаемые графические материалы, на которых:
[00122] На фиг.1 схематически показан механизм действия продукта, полученного из аллогенной культивированной ткани постнатального тимуса (например, КТТ, RVT-802), после введения для восстановления иммунитета при врожденной атимии.
[00123] На фиг.2 показана схема этапов восстановления иммунной системы у крысы, как описано в других местах в примере 1, путем удаления тимуса у иммунологически нормальной крысы Lewis, введения антитела для уничтожения Т-клеток крысы-реципиента, имплантации культивированной неонатальной ткани тимуса от крысы-донора крысе-реципиенту, введения иммуносупрессивного препарата в течение приблизительно 4 месяцев и оценки развития Т-клеток у крысы-реципиента. Следует отметить, что все крысы в группе лечения имели более 10% наивных Т-клеток до прекращения введения циклоспорина.
[00124] На фиг.3 показано развитие наивных Т-клеток у двух экспериментальных крыс- реципиентов из примера 1 (растущие линии справа) по сравнению с двумя контрольными крысами, не получившими имплантат из ткани тимуса (толстые линии у исходного уровня).
[00125] На фиг.4 показана схема производственного процесса для сбора тимуса у донора, культивирования тонких срезов донорской ткани тимуса в течение до 21 дня и имплантации культивированной ткани тимуса в четырехглавую мышцу реципиента.
[00126] На фиг.5А показана схема, демонстрирующая получение срезов ткани тимуса для определения характеристик, как обсуждается в разделе
[00520]. Фиг. 5В представляет собой изображение срезов ткани тимуса на целлюлозных фильтрах на хирургических губках в чашке для тканевых культур, которая используется для культивирования тимуса.
[00127] На фиг.6A-H изображено гистологическое исследование срезов ткани тимуса из партии (MFG-056) культивированной ткани тимуса на 5, 9, 12 и 21 день после сбора тимуса от донора. Окрашенные гематоксилином-эозином срезы (левые панели) и их соответствующая реакционная способность с коктейлем антител к цитокератину AE1/AE3 (правые панели; коричневый цвет обозначает положительную реакционную способность) показаны на 5 день (фиг.6А, 6В), 9 день (фиг.6C, 6D), 12 день (фиг.6E, 6F) и 21 день (фиг.6G, 6H) соответственно. Полоски в левом нижнем углу каждой панели соответствуют 100 мкм. Панели с H&E демонстрируют прогрессирование обеднения Т-клетками с течением времени. Фиг. 6E и 6F демонстрируют преимущественно эпителиальные клетки. По мере обеднения тимоцитами с течением времени происходит конденсация эпителия субкапсулярного слоя коры. Аналогичная конденсация происходит в медуллярных областях тимуса. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00128] На фиг.7А и В показана гистология срезов ткани тимуса в 0 день периода анализа в масштабе 5 мм (фиг.9А) и 100 мкм (фиг.7 В), соответственно. Она демонстрирует тимус и тимоциты при низком увеличении (полоска 5 мм) и высоком увеличении (полоска 100 мкм) в 0 день. Этот тимус является нормальным. В это время в корковой и медуллярной области имеется большое количество тимоцитов с темно-синими ядрами, способствующими общему темно-синему виду ткани. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00129] Фиг. 8А и 8В представляют собой изображения с окрашенного H&E предметного стекла, иллюстрирующие гистологию срезов ткани тимуса на 5 день периода анализа в масштабе 5 мм (фиг.8А) и 100 мкм (фиг.8В), соответственно. Прогрессирование обеднения тимоцитами приводит к более эозинофильному (розовому) виду ткани. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00130] Фиг. 9A и B. Окрашивание H&E иллюстрирует гистологию срезов ткани тимуса на 12 день периода анализа в масштабе 5 мм (фиг.9А) и 100 мкм (фиг.9В), соответственно. Можно видеть прогрессирующее обеднение тимоцитами. Более высокое увеличение демонстрирует множество эозинофильных клеточных тел, в которых отсутствуют ядра, которые являются симптомом некротических клеток, претерпевших кариолизис (растворение ядер). Эта степень некроза ожидается в культуре в этот момент времени. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00131] Фиг. 10A и 10B. Окрашивание H&E иллюстрирует гистологию срезов ткани тимуса на 21 день периода анализа в масштабе 5 мм (фиг.10А) и 100 мкм (фиг.10В), соответственно. Необходимо отметить сохранение общей архитектуры ткани, включая на фиг.10B субкапсулярный слой коры, корковую область и медуллярную область, содержащую множество телец Гассаля. Маленькие темные клетки в основном представляют собой некротические тимоциты, еще не претерпевшие кариолизис.Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00132] На фиг.11A-E изображены иллюстративные срезы тимуса, которые были иммуноокрашены коктейлем антител к цитокератину (AE1/AE3). Фиг. 11A. 0 день; фиг.11B. 5 день; фиг.11C. 9 день; фиг.11D. 12 день; и фиг.11E. 21 день. Структура эпителиальной сети тимуса остается неизменной по мере культивирования. Полоска соответствует 400 мкм. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00133] На фиг.12А и 12В показана гистология ткани тимуса на предметных стеклах после воздействия условий принудительной деградации посредством 10-кратной концентрации PBS. На фиг.12А показана корковая область на 9 день после воздействия условий принудительной деградации. На фиг.12В показана корковая область на 21 день после воздействия условий принудительной деградации. На фиг.12А мазок синего цвета представляет собой ДНК, высвобожденную из клеток. Большая часть клеток демонстрирует признаки деградации, хотя могут быть идентифицированы небольшие очаги клеток с интактными ядрами. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00134] На фиг.13 изображены окрашенные H&E гистологические срезы для клинического образца MLM247. Они соответствуют 0 дню культивирования. Полоска соответствует 200 мкм. Срез представляет собой замороженный срез с 0 дня. Поскольку он был заморожен, ткань выглядит иначе, чем погруженная в парафин фиксированная формалином ткань в 0 день. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00135] Фиг. 14. Замороженный срез, окрашенные H&E гистологические срезы для клинического образца MLM219. Этот срез был заморожен, поэтому ткань выглядит иначе, чем погруженная в парафин фиксированная формалином ткань, которая была культивирована и представлена выше. Тем не менее, важные гистологические характеристики обеднения тимоцитами и устойчивой жизнеспособности ЭКТ хорошо представлены. Фото сделано Laura P. Hale, MD, PhD, кафедра патологии, Университет Дьюка.
[00136] Фиг. 15 представляет собой фотографию свежесобранной ткани тимуса.
[00137] Фиг. 16 представляет собой схему, описывающую сбор, культивирование, трансплантацию и биопсию трансплантата КТТ под почечной капсулой крысы, как представлено в примере 5.
[00138] Фиг. 17A-D представляют собой фотографии ткани тимуса, собранной у 3-дневных крыс F1 (LWxDA), которая была разрезана на четыре части, как описано в примере 5 (фиг.17A). Фотография кусочков тимуса, культивированных на стерильных фильтрах из смешанного эфира целлюлозы с органной средой для тимуса в течение 5-7 дней в инкубаторе с CO2 при 37°C, как описано в примере 5 (фиг.17B). Фиг. 17C представляет собой фотографию КТТ, трансплантированного под почечную капсулу крысы LW. Фиг. 17D представляет собой фотографию трансплантата тимуса, собранного через 6 месяцев после трансплантации. Стрелки указывают на КТТ под почечной капсулой.
[00139] Фиг. 18A-D представляют собой фотографии, изображающие гистологическую картину свежей ткани тимуса (верхние рамки) и КТТ (нижние рамки) при 100-кратном увеличении. На фиг.18А показано сравнение медуллярной дифференцировки в окрашенной H&E свежей ткани тимуса (верхняя рамка) и КТТ, культивированного в течение 5 дней (нижняя рамка), как описано в примере 5. На фиг.18B показан типичный кружевовидный рисунок, наблюдаемый в КТТ, культивированном в течение 5 дней (нижняя рамка), при окрашивании на цитокератин по сравнению со свежей тканью тимуса (верхняя рамка), как описано в примере 5. На фиг.18С показана свежая ткань тимуса (верхняя рамка) и КТТ, обедненный Т-клетками (нижняя рамка), при окрашивании на Ki-67. На фиг.18D показана свежая ткань тимуса, окрашенная на CD3 (верхняя рамка), и ткань тимуса в КТТ, культивированная в течение 5 дней и затем окрашенная на CD3 (нижняя рамка). Коричневое пятно, отмеченное в окрашенном на CD3 КТТ (фиг.18D, нижняя рамка), вероятно, относится к некоторому количеству жизнеспособных клеток с остатками мертвых Т-клеток, не вымытых из ткани.
[00140] Фиг. 19A-D представляют собой фотографии, изображающие гистологическую картину свежей ткани тимуса (верхние рамки) и КТТ (нижние рамки) при 600-кратном увеличении. На фиг.19А показано сравнение медуллярной дифференцировки в окрашенной H&E свежей ткани тимуса (верхняя рамка) и КТТ, культивированном в течение 5 дней (нижняя рамка), как описано в примере 5. На фиг.19B показан типичный кружевовидный рисунок, наблюдаемый в КТТ, культивированном в течение 5 дней (нижняя рамка), при окрашивании на цитокератин по сравнению со свежей тканью тимуса (верхняя рамка), как описано в примере 5. На фиг.19С показана свежая ткань тимуса (верхняя рамка) и КТТ, обедненный Т-клетками (нижняя рамка), при окрашивании на Ki-67. На фиг.19D показана свежая ткань тимуса, окрашенная на CD3 (верхняя рамка), и ткань тимуса в КТТ, культивированная в течение 5 дней и затем окрашенная на CD3 (нижняя рамка). Коричневое пятно, отмеченное в окрашенном на CD3 КТТ (фиг.19D, нижняя рамка), вероятно, относится к некоторому количеству жизнеспособных клеток с остатками мертвых Т-клеток, не вымытых из ткани.
[00141] Фиг. 20 представляет собой схему плана эксперимента, описанного в примере 5. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00142] На фиг.21 показаны репопулирующие Т-клетки реципиентного типа, которые видны в нижнем правом квадранте после трансплантации КТТ. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00143] На фиг.22A и B показан трансплантированный тимус, эксплантированный через 8,5 месяцев после трансплантации, демонстрирующий положительное окрашивание на цитокератин (фиг.22A), а также окрашивание Т-клеток, аналогичное нативному тимусу (фиг.22B). Исходное 400-кратное увеличение. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00144] На фиг.23 показаны графики значительного увеличения количества циркулирующих CD4 и CD8 T-клеток по сравнению с контрольными животными без трансплантации КТТ. На ней также показано значительно увеличенное количество наивных CD4 и наивных CD8 Т-клеток в группе, подвергшейся трансплантации культивированной ткани тимуса (ТКТТ), по сравнению с контрольной группой, которая не подвергалась ТКТТ, и значительно увеличенное количество CD4 и CD8 недавних эмигрантов из тимуса (RTE) в группе, подвергшейся трансплантации культивированной ткани тимуса (КТТ), по сравнению с контрольной группой, которая не подвергалась КТТ. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00145] На фиг.24 показано иммуногистохимическое исследование трансплантированного КТТ, эксплантированного на 180 день, демонстрирующее нормальную гистологию тимуса под почечной капсулой (справа на фиг.24А). На фиг.24B показан эксплантированный трансплантат, окрашенный H&E. Показаны окрашивания на жизнеспособные Т-клетки (CD3), пролиферацию Т-клеток (Ki67) и цитокератин (детектированный кроличьим поликлональным антителом). На панели, окрашенной на цитокератин, виден кружевовидный рисунок с образованием тельца Гассаля (стрелка) на ЭКТ. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00146] На фиг.25 показан процент выживаемости крыс LW после тимэктомии и иммуносупрессии с трансплантатами сердца DA с трансплантацией КТТ (закрашенные треугольники, синяя линия) и без трансплантации КТТ (перевернутые треугольники, красные линии) (ТКТТ). Крысы LW с ТКТТ являются толерантными; крысы LW без ТКТТ являются иммунодефицитными и вследствие этого не отторгают сердце DA. Контроль демонстрирует полное отторжение трансплантатов сердца DA у крыс LW, не подвергавшихся каким-либо манипуляциям (незакрашенные квадраты). Контрольные животные LW также не отторгали сердечный трансплантат LW (незакрашенный кружок с горизонтальной линией) (n=9). Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00147] Фиг. 26A и 26B представляют собой фотографии трансплантированных аллотрансплантатов (сердец DA) от животных с трансплантацией КТТ (26A) и без нее (26B), демонстрирующие инфильтрацию мононуклеарными клетками без признаков отторжения, на основании оценки согласно Международному обществу трансплантации легких и сердца (ISHLT), 2004, как изображено на фиг.26C (закрашенные синие квадраты и закрашенные красные треугольники). Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00148] Фиг. 27 представляет собой график выживаемости трансплантата сердца BN в шее в процентах выживаемости животных в зависимости от дней выживания трансплантата у крыс LW с внедренным КТТ (которые были иммунокомпетентны и отторгли аллогенное сердце BN, трансплантированное в шейный отдел) и контрольных животных LW без внедренного КТТ (которые были иммунодефицитными из-за отсутствия тимуса и не могли отторгнуть сердце BN, трансплантированное в шейный отдел) по сравнению с контролем BN (крыса LW отторгает сердце BN, трансплантированное в шейный отдел) и сингенными контролями (крысы LW не отторгают сердца LW, трансплантированные в шейный отдел). Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00149] Фиг. 28A и 28B представляют собой фотографии ткани сердца BN с (фиг.28A) и без (фиг.28B) внедренного КТТ через 11 и 46 дней, соответственно. Эти изображения являются основой для данных на фиг.27 и 29. Сердце в 28А не было отторгнуто из-за толерантности. Сердце в 28B не было отторгнуто из-за иммунодефицита вследствие отсутствия тимуса. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00150] На фиг.29 показана классификация степеней отторжения сердец BN, трансплантированных в шейный отдел. Сингенные сердца LW, помещенные в организм крыс LW (незакрашенные кружки), не были отторгнуты. Сердца BN, помещенные в организм крыс LW (закрашенные кружки), были отторгнуты. Сердца BN, помещенные в организм крыс LW, получивших КТТ, были отторгнуты (закрашенные квадраты). Сердца BN, помещенные в организм крыс LW, не получивших КТТ, были отторгнуты в слабой степени (заштрихованные треугольники) у 2 крыс и не отторгнуты у других трех крыс. Эти данные показывают, что крысы с КТТ были способны в высокой степени отторгать сердца от третьей стороны, даже когда они принимали сердца DA (фиг.26C), поскольку ТКТТ экспрессировал DA. Крысы без КТТ были иммунодефицитными и не отторгали ни сердца DA (фиг.26C), ни сердца BN. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00151] Фиг. 30A и 30B представляют собой фотографии сердец BN, где крысы получали или не получали внедрение КТТ по сравнению с сердцами LW и DA, соответственно. На фиг.30A, после того как введение иммуносупрессивных препаратов прекращали и трансплантировали сердце BN, сердце BN было быстро отторгнуто и вследствие этого имеет очень большой размер из-за всего воспаления. Сердце LW имеет нормальный размер для сердца, перекачивающего кровь через тело. Сердце DA имеет маленький размер, так как оно было помещено в брюшную полость и не должно было перекачивать кровь. На фиг.30B крыса является иммунодефицитной и не может отторгнуть ни сердце BN, ни сердце DA после прекращения введения иммуносупрессивных препаратов. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00152] Фиг. 31A-B представляют собой графики степени отторжения для эксплантированных сердец BN из шейного отдела крыс с внедрением КТТ и без него по сравнению с контролями BN и сингенными контрольными крысами. На фиг.31A показана количественная оценка воспалительных клеток в первичном аллотрансплантате сердца DA в брюшную полость. Сингенный контроль демонстрирует, что крысы LW не отторгают сердца LW. Контроль DA демонстрирует, что крысы LW действительно отторгают сердца DA. Группа с КТТ не отторгает сердце DA из-за толерантности. Группа без КТТ не отторгает сердце DA из-за иммунодефицита вследствие отсутствия тимуса. На фиг. 31B показано количественное определение воспалительных клеток во вторичных аллотрансплантатах сердца BN в шейном отделе. Сингенный контроль демонстрирует, что крысы LW не отторгают сердца LW. Контроль BN демонстрирует, что крысы LW действительно отторгают сердца BN. Группа с КТТ отторгает сердце BN, потому что она является иммунокомпетентной. Группа без КТТ не отторгает сердце BN из-за иммунодефицита вследствие отсутствия тимуса. На фиг.31C показаны крысы с сердцами DA и BN, которые были собраны от реципиентов LW вместе с нативным сердцем LW во время отторжения сердца BN, трансплантированного в шейный отдел. На нижней правой панели показаны Т-клетки (коричневые) в сердце BN, приводящие к его отторжению. На фиг. 31D показана инфильтрация Т-клетками в сердцах LW, DA и BN контрольных животных без внедрения КТТ. Они не демонстрируют инфильтрации Т-клетками, поскольку животные являются иммунодефицитными. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00153] Фиг. 32: Гуморальная толерантность после ТКТТ. На фиг.32А показаны иллюстративные гистограммы для донор-специфического аллоантитела (антитела к DA и антитела к BN) после трансплантации, измеренного с помощью перекрестной пробы на совместимость с Т-клетками. Верхняя левая панель (контроль DA) демонстрирует выработку антитела к DA (жирная линия) у нормальной крысы LW после получения гетеротопического трансплантата сердца DA в брюшную полость. Верхняя средняя панель демонстрирует отсутствие антитела к DA у крыс LW, получивших ТКТТ; это свидетельствует о толерантности. Верхняя правая панель демонстрирует отсутствие ответа от крыс LW без ТКТТ; это отражает иммунодефицит крыс после тимэктомии и обеднения Т-клетками без получения донорского тимуса. На нижней левой панели показано нормальное антитело к BN, образованное нормальной крысой LW, которой трансплантировали сердце BN в шейный отдел. Нижняя средняя панель демонстрирует нормальный ответ крыс LW с ТКТТ против BN после трансплантации сердца BN в шейный отдел, что демонстрирует иммунокомпетентность и способность отторгать трансплантат от третьей стороны. На нижней правой панели показано, что у крыс LW без ТКТТ отсутствует ответ против BN после трансплантации сердца BN в шейный отдел, что свидетельствует о некомпетентности иммунной системы и отсутствии способности отторгать трансплантат от третьей стороны. На фиг.32B показаны уровни антитела к DA после первичной трансплантации сердца DA. Крысы LW с ТКТТ из донора тимуса LWxDA не вырабатывают антитела к DA после трансплантации сердца DA, поскольку они толерантны к DA. Крысы LW без ТКТТ не вырабатывают антитело к DA после трансплантации сердца DA, поскольку они являются иммунодефицитными. На фиг.32C показаны уровни антитела к BN после вторичной трансплантации сердца BN в шейный отдел. Крысы LW с ТКТТ от донора LWxDA вырабатывают антитела к BN, демонстрируя иммунокомпетентность против трансплантата от третьей стороны. Крысы LW без ТКТТ не вырабатывают антител к BN, демонстрируя некомпетентность иммунной системы. Это изображение взято из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00154] Фиг. 33. Криоконсервация культивированной ткани тимуса от примата, не являющегося человеком, после 12 дней культивирования. Верхний ряд представляет собой цитокератин при сборе (A), на 6 день культивирования (B), на 12 день культивирования (C) и после 12 дней культивирования с последующей криоконсервацией в течение 35 дней и размораживанием для фотографии (D). Цитокератин (AE1/AE3) в D имеет сходство с цитокератином в C. Во втором ряду показано окрашивание на CK14 с теми же временными точками. CK14 в H очень схож с показанным в панели G. Третий ряд демонстрирует окрашивание на CD3, которое демонстрирует ожидаемую потерю жизнеспособных Т-клеток с течением времени. Панель L схожа с панелью K в том, что она имеет очень мало Т-клеток. Четвертый ряд демонстрирует окрашивание Ki-67 пролиферирующих Т-клеток. Окрашивание Ki-67 отсутствует к 6 дню, поскольку Т-клетки в основном погибли. На этой фигуре показана способность к криоконсервации тимуса, полученного примата, не являющегося человеком, аналогично тому, как культивированная ткань тимуса будет криоконсервирована для пациентов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[00155] Названия, заголовки и подзаголовки, представленные в настоящем документе, не должны интерпретироваться как ограничивающие различные аспекты раскрытия. Соответственно, термины, определенные ниже, более полно определяются ссылкой на описание в целом. Все источники, цитируемые в настоящем документе, полностью включены посредством ссылки.
[00156] Если не указано иное, научные и технические термины, используемые в настоящем документе, имеют значения, обычно понимаемые специалистами в данной области техники. Кроме того, если из контекста не следует иное, термины в единственном числе включают множественное число, а термины во множественном числе включают единственное число. В данной заявке использование «или» означает «и/или», если не указано иное. В контексте пункта формулы с множественной зависимостью использование «или» означает ссылку на более чем один предшествующий независимый или зависимый пункт формулы только в виде альтернативы.
[00157] Кроме того, следует отметить, что в контексте настоящего описания и прилагаемой формулы изобретения формы единственного числа, а также любое употребление любого слова в единственном числе включают множественное число объекта, если только объект явно и однозначно не ограничен единственным числом. В контексте настоящего документа термин «включать» и его грамматические варианты не имеют ограничительного характера, так что перечисление элементов в списке не исключает других подобных элементов, которыми могут быть заменены перечисленные элементы или которые могут быть добавлены к перечисленным элементам.
[00158] Настоящее изобретение может быть наилучшим образом понято со ссылкой на следующие определения:
[00159] Термин «приблизительно» используется в настоящем документе для обозначения примерно, в районе, порядка или около. При использовании термина «приблизительно» в сочетании с диапазоном численных значений он модифицирует указанный диапазон путем расширения границ в большую и меньшую сторону от приведенных численных значений. В целом, термин «приблизительно» используется в настоящем документе для модификации численного значения в большую или меньшую сторону от указанного значения с отклонением +/-10%. В контексте настоящего документа термин «приблизительно» относится к численному значению, включая, например, целые числа, дроби и процентные доли, независимо от того, указаны ли они в явном виде. Термин «приблизительно» относится к диапазону численных значений (например, +/-5-10% от приведенного диапазона), который специалист в данной области техники посчитает эквивалентным приведенному значению (например, имеющему ту же функцию или результат). Когда такие термины, как «по меньшей мере» и «приблизительно» предшествуют списку численных значений или диапазонов, указанные термины модифицируют все значения или диапазоны, представленные в списке. В некоторых случаях термин «приблизительно» может включать численные значения, округленные до ближайшей значащей цифры.
[00160] В контексте настоящего документа термин «животное» включает, не ограничиваясь перечисленным, людей и позвоночных, отличных от человека, таких как дикие, домашние и сельскохозяйственные животные. Животное также может быть названо «субъектом».
[00161] В контексте настоящего документа термин «биосовместимый» относится к любому материалу, который при имплантации млекопитающему не вызывает у указанного млекопитающего неблагоприятного ответа.
[00162] «Хроническое отторжение трансплантата» обычно происходит у людей по прошествии от нескольких месяцев до нескольких лет после трансплантации, даже при успешной иммуносупрессии острого отторжения. Фиброз является частым фактором хронического отторжения трансплантатов всех видов органов.
[00163] В контексте настоящего документа термины «содержащий» (и любая форма этого термина, такая как «содержать», «содержит» и «содержащийся»), «имеющий» (и любая форма этого термина, такая как «иметь» и «имеет») или «включающий» (и любая форма этого термина, такая как «включает» и «включать»), являются включительными или неограниченными и не исключают дополнительных, не перечисленных элементов или стадий способа. Кроме того, термин, используемый в сочетании с термином «содержащий», также понимается как подходящий для использования в сочетании с термином «состоящий из» или «по существу состоящий из».
[00164] В контексте настоящего документа термин «трансплантат» относится к ткани или органу, которые имплантируют индивидууму, обычно для замены, исправления или иного преодоления дефекта. Ткань или орган может состоять из клеток, которые происходят от одного и того же человека; этот трансплантат называется в настоящем документе следующими взаимозаменяемыми терминами: «аутотрансплантат», «аутологичный трансплантат» и «аутологичный имплантат». Трансплантат от генетически отличной особи того же вида называется в настоящем документе следующими взаимозаменяемыми терминами: «аллотрансплантат», «аллогенный трансплантат» и «аллогенный имплантат». Трансплантат от индивидуума его идентичному близнецу называется в настоящем документе «изотрансплантатом», «сингенным трансплантатом» или «сингенным имплантатом». «Ксенотрансплантат», «ксеногенный трансплантат» или «ксеногенный имплантат» относится к трансплантату от одного индивидуума другому индивидууму, принадлежащему к другому виду.
[00165] В настоящем документе термин «совпадающий по HLA» относится к паре «донор-реципиент», в которой ни один из HLA-антигенов не является несовпадающим для донора и реципиента. HLA-типирование в способах согласно изобретению включает: аллели HLA: HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DQA1, HLA-DPB1, HLA-DPA1.
[00166] В контексте настоящего документа термин «несовпадающий по HLA» относится к соотнесению HLA-антигенов донора и реципиента, как правило, в отношении HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DQA1, HLA-DPB1, HLA-DPA1, где имеет место несовпадение HLA между донором и реципиентом. В некоторых случаях один гаплотип является совпадающим, а другой - несовпадающим. Эта ситуация часто встречается при использовании органов от живых или умерших доноров. Несовпадение HLA в парах донор-реципиент приводит к повышенному риску отторжения трансплантата по сравнению с совпадающими по HLA парами.
[00167] В качестве контекста для приведенных выше определений HLA-антигены соответствуют «человеческим лейкоцитарным антигенам», которые представляют собой белковые молекулы, экспрессирующиеся на поверхности клеток, которые придают этим клеткам уникальную антигенную характеристику. Они также известны как «антигены главного комплекса гистосовместимости». Таким образом, MHC- или HLA-антигены являются молекулами-мишенями, которые распознаются Т-клетками как «свои» или «чужие». Если HLA-антигены получены из того же источника гемопоэтических стволовых клеток, что и иммунные эффекторные клетки, они считаются «своими». Если HLA-антигены получены из другого источника гемопоэтических восстанавливающих клеток, они считаются «чужими».
[00168] Различают два основных класса HLA-антигенов: HLA класса I и HLA класса II. Антигены HLA I класса (A, B и C у людей) делают каждую клетку распознаваемой как «свою». Антигены HLA II класса (DRB1, DPB1, DPA1, DQB1 и DQA1 у людей) участвуют в реакциях между лимфоцитами и антигенпрезентирующими клетками. Оба класса HLA-антигенов вовлечены в качестве мишеней при отторжении трансплантированных органов.
[00169] Гены HLA сгруппированы в кластер в положении 6p21 человеческой хромосомы. Этот кластер генов кодирует шесть классических трансплантационных генов HLA. Сегмент 6p21 также кодирует гены, кодирующие белки, играющие важную роль в регуляции иммунной системы и других фундаментальных молекулярных и клеточных процессов. Полный локус включает приблизительно 3,6 млн п.о. и по меньшей мере 224 генных локуса. В результате кластеризации возникают определенные «гаплотипы» (набор аллелей, присутствующих на одной хромосоме). Гаплотипы, унаследованные от одного из родителей, как правило, наследуются в виде группы. Набор аллелей, унаследованных от каждого из родителей, образует гаплотип, в котором некоторые аллели проявляют тенденцию к ассоциации друг с другом. HLA-типирование используется для идентификации гаплотипов реципиента и помогает в идентификации подходящих совместимых доноров. Некоторые гаплотипы более распространены, чем другие, и они различаются по частоте в разных расовых и этнических группах.
[00170] В контексте настоящего документа выражение «нуждающийся в этом» означает, что субъект был идентифицирован как имеющий потребность в определенном способе или виде лечения. В некоторых вариантах осуществления идентификация может быть осуществлена посредством любого средства диагностики. В любом из способов и видов лечения, описанных в настоящем документе, субъект может представлять собой нуждающегося субъекта.
[00171] В контексте настоящего документа выражение «целое число от X до Y» означает любое целое число, включая граничные значения. Например, фраза «целое число от X до Y» означает 1, 2, 3, 4 или 5.
[00172] В контексте настоящего документа термин «млекопитающее» означает грызуна (т.е. мышь, крысу или морскую свинку), обезьяну, кошку, собаку, корову, лошадь, свинью или человека. В некоторых вариантах осуществления млекопитающее представляет собой человека.
[00173] В контексте настоящего документа термин «орган» относится к цельному васкуляризированному органу, который выполняет определенную функцию или группу функций в организме. Термин «орган» включает, не ограничиваясь перечисленным, сердце, легкое, почку, печень, поджелудочную железу, кожу, матку, кость, хрящ, тонкую или толстую кишку, мочевой пузырь, головной мозг, молочную железу, кровеносные сосуды, пищевод, фаллопиеву трубу, желчный пузырь, яичники, поджелудочную железу, предстательную железу, плаценту, спинной мозг, конечность, включая верхнюю и нижнюю, селезенку, желудок, яички, тимус, щитовидную железу, трахею, мочеточник, мочеиспускательный канал, матку.
[00174] В контексте настоящего документа термины «предотвращать», «предотвращающий» и «предотвращение» относятся к назначению терапии индивидууму, у которого в конечном итоге может проявиться, но пока еще не проявился, по меньшей мере один симптом заболевания, расстройства или состояния, чтобы снизить вероятность того, что у индивидуума разовьется симптом заболевания, расстройства или состояния в течение заданного периода времени. Такое снижение может быть отражено, например, в отсроченном появлении у пациента по меньшей мере одного симптома заболевания, расстройства или состояния.
[00175] В контексте настоящего документа термины «субъект», «индивидуум» или «пациент», используемые взаимозаменяемо, означают любое животное, включая млекопитающих, таких как мыши, крысы, другие грызуны, кролики, собаки, кошки, свиньи, крупный рогатый скот, овцы, лошади или приматы, такие как люди.
[00176] В контексте настоящего документа выражение «терапевтически эффективное количество» означает количество активного соединения или фармацевтического агента, которое вызывает биологический или лекарственный ответ, который необходим исследователю, ветеринару, врачу или другому клиницисту в ткани, системе, животном, индивидууме или человеке. Терапевтический эффект зависит от расстройства, подлежащего лечению, или от желаемого биологического эффекта. Так, терапевтический эффект может представлять собой уменьшение тяжести симптомов, связанных с расстройством, и/или ингибирование (частичное или полное) прогрессирования расстройства, или улучшенное лечение, заживление, предупреждение или устранение расстройства или побочных действий. Количество, необходимое, чтобы вызвать терапевтический ответ, может быть определено на основании возраста, состояния здоровья, размера и пола субъекта. Оптимальные количества также могут быть определены на основе мониторинга ответа субъекта на лечение.
[00177] Термин «ткань» в контексте настоящего документа относится к любому типу тканей человека или животных и включает, не ограничиваясь перечисленным, сосудистую ткань, ткань кожи, печеночную ткань, ткань поджелудочной железы, нервную ткань, мочеполовую ткань, желудочно-кишечную ткань, ткань скелета, включая кости и хрящи, жировую ткань, соединительную ткань, включая сухожилия и связки, амниотическую ткань, хориальную ткань, твердую мозговую оболочку, перикард, мышечную ткань, железистую ткань, ткань лицевой области, глазную ткань.
[00178] «Банк тканей» в контексте настоящего изобретения относится к долговременному хранению криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, который хранится в жидком азоте. Общее руководство по созданию хранилища для продукта, полученного из аллогенной культивированной ткани постнатального тимуса, может быть взято из Руководства для промышленности. Текущая версия надлежащей тканевой практики (CGTP) и дополнительные требования к производителям человеческих клеток, тканей, а также продуктов на основе клеток и тканей (HCT/Ps), доступного по адресу https://www.fda.gov/downloads/BiologicsBloodVaccines/GuidanceComplianceRegulatoryInformation/Guidances/Tissue/UCM285223.pdf.
[00179] «Тканевая инженер(ия) (тканеинженерный)» относится к процессу создания тканей ex vivo для применения при замещении или восстановлении ткани. Тканевая инженерия является примером «регенеративной медицины», которая включает в себя подходы к восстановлению или замещению тканей и органов путем включения клеток, генов или других биологических структурных элементов, наряду с биоконструкционными материалами и технологиями.
[00180] Термин «отторжение трансплантата» охватывает как острое, так и хроническое отторжение трансплантата. «Острое отторжение» представляет собой отторжение иммунной системой реципиента трансплантированной ткани, когда трансплантированная ткань является иммунологически чужеродной. Острое отторжение характеризуется инфильтрацией трансплантированной ткани иммунными клетками реципиента, выполняющими свои эффекторные функции и разрушающими трансплантированную ткань. Острое отторжение характеризуется быстрым началом и обычно происходит у людей в течение нескольких недель после операции по трансплантации. Как правило, острое отторжение может быть ингибировано или подавлено иммуносупрессивными препаратами, такими как рапамицин, циклоспорин A, моноклональное антитело к CD40L и тому подобное.
[00181] В контексте настоящего документа термины «лечить», «получающий лечение» или «применять схему (лечения)» означают как терапевтическое лечение, так и профилактические меры, цель которых состоит в том, чтобы замедлить (уменьшить) нежелательное физиологическое состояние, расстройство или заболевание, или достичь полезных или желательных клинических результатов. Например, полезные или желательные клинические результаты включают, не ограничиваясь перечисленным, облегчение симптомов; уменьшение степени состояния, расстройства или заболевания; стабилизированное (т.е. не ухудшающееся) состояние, расстройство или заболевание; задержка начала или замедление прогрессирования состояния, расстройства или заболевания; улучшение состояния, расстройства или патологического состояния или ремиссия (частичная или полная), определяемая или неопределяемая; улучшение по меньшей мере одного измеримого физического параметра, не обязательно распознаваемого пациентом; или оздоровление или улучшение состояния, расстройства или заболевания.
[00182] Как описано в настоящем документе, любой диапазон концентраций, процентный диапазон, диапазон отношений или целочисленный диапазон следует понимать как включающие значение любого целого числа в пределах указанного диапазона и, когда применимо, его долей (таких как одна десятая и одна сотая целого числа), если не указано иное. Диапазоны являются приблизительными и могут отличаться более чем на целое число.
[00183] Единицы, приставки и символы обозначены в их общепринятой форме согласно Международной системе единиц (система СИ). Численные диапазоны включают границы диапазонов. Измеренные значения считаются приблизительными с учетом значащих цифр и ошибки, связанной с измерением.
[00184] Следует также отметить, что отдельные признаки, описанные в настоящем документе, которые для ясности описаны в контексте отдельных вариантов осуществления, также могут быть представлены в комбинации в одном варианте осуществления. И наоборот, различные признаки изобретения, которые для краткости описаны в контексте одного варианта осуществления, также могут быть представлены по отдельности или в любой подходящей подкомбинации.
Сбор донорской ткани тимуса.
[00185] Донорская ткань тимуса может быть получена во время постнатальных операций на сердце с информированного согласия семьи донора. Удаление части тимуса может быть необходимо для доступа к месту проведения операции. Таким образом, часть тимуса может быть удалена во время операции на сердце при постнатальных операциях на сердце, что обусловлено характером хирургической операции.
[00186] Во время постнатальных операций на сердце часть ткани тимуса во время хирургической операции может быть удалена в отходы. При всех операциях на сердце, независимо от того, проходит ли тимус скрининг на трансплантацию, хирург помещает удаленную ткань тимуса в стерильный контейнер.
[00187] Донорами ткани тимуса для трансплантации ткани тимуса у грудных детей с полным синдромом Ди Георга были грудные дети в возрасте до девяти месяцев. Лекарственное вещество продукта, полученного из аллогенной культивированной ткани постнатального тимуса, изготавливают путем обработки и культивирования удаленной в отходы ткани тимуса, как описано в настоящем документе.
[00188] Согласие на использование тимуса для трансплантации культивированной ткани тимуса может быть получено до или после сбора тимуса. Тем не менее, согласие, позволяющее взять кровь у грудного ребенка до проведения шунтирования, необходимо и всегда должно быть получено до операции. Этот образец крови используют для скрининга донора.
[00189] Удаленную в отходы ткань тимуса помещают в стерильный контейнер. Проводят стандартное тестирование донора и его родной матери в соответствии с рекомендациями FDA для трансплантации тканей. При хирургических операциях, описанных в настоящем документе, не требуется подбор типа ткани, но такой подбор типа ткани может быть осуществлен в определенных ситуациях.
[00190] Ткань может быть обработана немедленно или может храниться в холодильнике в течение ночи для обработки на следующий день. Если ткань тимуса должна будет храниться в течение ночи, ткань асептически добавляют в органную среду для тимуса (среду «TOM», описанную ниже) в количестве, достаточном, чтобы полностью покрыть ткань тимуса в исходном контейнере. Контейнер с тимусом помещают в холодильник до готовности к обработке на следующий день.
Обзор кондиционирования ткани тимуса
[00191] Режим кондиционирования обедняет культивированные срезы ткани тимуса тимоцитами донора. По полученным in vitro данным (иммуногистохимия), период культивирования от 12 до 21 дня сохраняет эпителиальную сеть согласно оценке с использованием антител к цитокератину. Культивирование предпочтительно проводят при 37°C в инкубаторе с 5% CO2.
[00192] Для успешного культивирования ткань тимуса предпочтительно нарезают на срезы и помещают на целлюлозу Millipore® или эквивалентные фильтры и помещают на хирургические губки в чашки для тканевых культур. Среда содержит органную среду для тимуса (TOM), и ее меняют ежедневно.
[00193] При поступлении тимуса проводят его патологическое исследование. Тест на принадлежность должен показать >50% областей, положительных на кератин, имеющих кружевовидный рисунок окрашивания. Тест на активность должен показать тельца Гассаля; он также должен показать окрашивание на CK14 с кружевовидным рисунком. Тест на жизнеспособность должен показать >90% интактных ядер, наблюдаемых в срезах. Выпуск партии ткани производят в день между 5 и 9 днями (включительно) и проводят с помощью патологического исследования. Для принадлежности области на ткани между 5 и 9 днями должны быть положительными на кератин, AE1/AE3. Для активности культивируемая ткань тимуса между 5 и 9 днями должна демонстрировать окрашивание на цитокератин CK14, рассредоточенное по всей ткани, и должно быть идентифицировано по меньшей мере одно тельце Гассаля. Для жизнеспособности культивированная ткань тимуса между 5 и 9 днями должна демонстрировать интактные ядра.
[00194] В одном варианте осуществления срезы ткани тимуса кондиционируют в течение приблизительно 12 дней, после чего криоконсервируют.В еще одном варианте осуществления все срезы ткани тимуса кондиционируют в течение приблизительно 12 дней, затем около половины имплантируют реципиенту, а оставшиеся срезы ткани тимуса криоконсервируют для будущего использования.
[00195] В течение 24 часов после сбора тимус нарезают на тонкие срезы. Срезы выдерживают в культуре в течение 12-21 дня. Этот процесс культивирования, как подробно описано ниже, обедняет срезы жизнеспособными Т-клетками донора и в конечном итоге позволяет хирургически имплантированному срезу ткани восстанавливать иммунную систему субъекта, лишенного тимуса, хотя и на потенциально более низких, но иммунологически эффективных уровнях Т-клеток.
[00196] Процесс культивирования, как описано ниже, значительно модифицирует биологические характеристики донорской ткани тимуса и содержащихся в ней клеток следующим образом, чтобы оптимизировать эффективные терапевтические свойства срезов КТТ.
[00197] Процесс культивирования гарантирует получение определенного состава культивированных клеток/тканей, обладающих необходимыми биологическими характеристиками, способом, подходящим для хирургической имплантации субъекту, чтобы обеспечить восстановление иммунной системы субъекта.
[00198] Процесс культивирования приводит к потере тимоцитов и относительному обогащению эпителиальных клеток тимуса и других стромальных клеток в срезах донорской ткани тимуса.
[00199] Процесс культивирования, кроме того, приводит к обеднению тимоцитами и поддержанию ЭКТ, чтобы обеспечить восстановление иммунной системы реципиента, и обеспечивает развитие толерантности у реципиента к HLA-антигенам в тимусе донора.
[00200] В целом, процесс производства предназначен для обеднения донорской ткани тимуса тимоцитами и для сохранения функциональной архитектуры стромы тимуса (эпителиальных клеток тимуса и фибробластов).
[00201] В одном варианте осуществления обработанная донорская ткань тимуса представляет собой сконструированный продукт ткани тимуса, способный индуцировать толерантность к типам ткани тимуса (HLA-антигенам) у нуждающегося в этом субъекта после хирургической имплантации.
[00202] Для сохранения жизнеспособности нарезанной на срезы ткани тимуса срезы тимуса помещают на целлюлозные фильтры Millipore и помещают в чашки для тканевых культур, содержащие среду, хирургические губки. Культуральную среду в каждой чашке для тканевых культур заменяют ежедневно со дня сбора у донора до дня имплантации (с 12 по 21 день).
[00203] Культивирование донорской ткани тимуса обедняет обработанную таким образом ткань тимоцитами, что сводит к минимуму риск развития реакции «трансплантат против хозяина» («РТПХ»), что может быть весьма проблематичным у пациентов со значительным иммунодефицитом после тимэктомии.
[00204] В течение первых нескольких дней в культуре многие тимоциты «выпадают» из срезов ткани в культуральную среду и отбрасываются при смене среды. Поскольку культивирование продолжается в течение периода культивирования, тимоциты донора продолжают погибать, но их клеточные остатки сохраняются в срезах КТТ.
[00205] Не ограничиваясь какой-либо конкретной теорией, полагают, что наличие этих нежизнеспособных тимоцитов и их остатков, в которых отсутствуют ядра, является важным для предполагаемой функции тканеинженерного продукта, поскольку они помогают сохранить открытые карманы в трехмерной сети эпителиальных клеток тимуса, что необходимо для введения стволовых клеток костного мозга реципиента после обработки. Важность наличия «пространства» для входящих стволовых клеток костного мозга подтверждается опытом с пациентом DIG003 в Markert, 1999 (см. список цитируемых источников ниже). Пациент, описанный в вышеупомянутом источнике, получил очень большую дозу стероидов (40 мг/кг/сут x 3 дня метилпреднизолона) через 35 дней после трансплантации КТТ, что привело к апоптозу тимоцитов и конденсации эпителия. Никаких наивных Т-клеток не развилось, и пациент скончался от инфекции. При вскрытии внедренный тимус представлял собой массу жизнеспособного кубического эпителия без промежутка между эпителиальными клетками для проникновения тимоцитов.
[00206] В течение периода культивирования проводят HLA-типирование, чтобы определить, имеют ли пациент (реципиент) и донорская ткань какие-либо общие аллели HLA. У реципиента проводят тестирование антител к HLA, чтобы определить, есть ли у реципиента какие-либо антитела к HLA-антигенам в тимусе. Если у реципиента есть антитела, нацеленные на MHC донора, потребуется поиск другого тимуса. Донора и мать донора проверяют на наличие инфекции в соответствии с руководящим документом FDA «Руководство для промышленности. Определение приемлемости для доноров человеческих клеток, тканей и продуктов на основе клеток и тканей (HCT/Ps)» и более поздними руководящими документами. Ткань асептически обрабатывают в соответствии со Сводом федеральных нормативных актов (CFR), часть 1271, подраздел D «Текущая версия надлежащей тканевой практики».
[00207] После просмотра документации партии и проведения контроля качества ткань выпускают с производства и предоставляют операционной бригаде для трансплантации, ткань хирургически имплантируют реципиенту, как описано ранее.
[00208] Культивированную ткань тимуса получают способом, более полно описанным ниже и в разделе примеров, приведенном в данном описании.
[00209] Таким образом, процесс культивирования собранной ткани тимуса значительно модифицирует биологические характеристики донорской ткани и содержащихся в ней клеток следующим образом: потеря тимоцитов донора и обогащение эпителиальными клетками тимуса и другими стромальными клетками, а также обеднение тимоцитами донора изменяет физиологические функции ткани (например, секрецию цитокинов и факторов роста), а также ее структурные свойства.
[00210] В течение первых нескольких дней в культуре многие тимоциты «выпадают» из срезов ткани в культуральную среду и отбрасываются при смене среды.
[00211] Манипуляции, производимые в ходе процесса производства, приводят к изменениям общего вида и гистологической картины получаемых клеток, содержащихся в готовом продукте, по сравнению с источником или исходным материалом, полученным от донора.
[00212] Ткань тимуса в течение первых нескольких дней культивирования имеет красный цвет из-за остатков крови на ткани и внутри ткани. См., например, фиг.15.
[00213] Между 5 и 9 днями наблюдается жизнеспособная ткань без заражения крови, которое было выраженным в 1 день.
[00214] В течение оставшихся дней культивирования глубина ткани уменьшается по мере обеднения тимоцитами. Снижение плотности тимоцитов в ткани подтверждено иммуногистохимическим анализом и подробно описано ниже.
[00215] В 0 день после сбора удаленной в отходы ткани тимуса ткань плотно заселяется жизнеспособными тимоцитами, встроенными в строму, которая содержит эпителиальные клетки тимуса и фибробласты. Окрашивание AE1/AE3 и CK14 подтверждает наличие положительных на цитокератин (CK) эпителиальных клеток тимуса, характерных для нормального тимуса. Эпителиальные клетки тимуса образуют кружевовидную трехмерную сеть с чувствительными процессами, окружающую соседние тимоциты.
[00216] В процессе культивирования срезы тимуса культивируют, как описано ниже. Множество тимоцитов вымывается из ткани, особенно в течение первых 3 дней. Это обеднение может быть идентифицировано гистологически уже на второй день по окрашиваниям H&E, которые демонстрируют снижение плотности тимоцитов, особенно в медуллярных областях. Большая часть тимоцитов, оставшихся в ткани, демонстрирует ядерные изменения, соответствующие апоптозу и/или некрозу, или демонстрирует кариолизис (полную потерю ядер). Многие из этих мертвых тимоцитов и их клеточные остатки остаются в тканях тимуса и, как полагают, предотвращают полное схлопывание пространства между эпителиальными клетками.
[00217] Некоторая конденсация эпителия может наблюдаться во внешних областях, таких как субкапсулярный слой коры, где потеря тимоцитов привела к схлопыванию сети эпителиальных клеток. Эти конденсированные эпителиальные клетки субкапсулярного слоя коры могут образовывать линейные группы толщиной в несколько слоев, что может повысить механическую прочность срезов. Часть медуллярного эпителия также может конденсироваться, образуя участки прилегающих эпителиальных клеток.
[00218] Гибель тимоцитов продолжается по мере культивирования, причем остатки некротических тимоцитов удерживаются в ткани. Дальнейшая конденсация медуллярного эпителия и эпителия субкапсулярного слоя коры является минимальной между 7 и 19 днями культивирования.
[00219] Области с эпителиальной архитектурой, подобной нормальной тимусу, все еще можно наблюдать на поздней стадии культивирования для каждого тимуса с использованием окрашивания AE1/AE3. Для тканей, культивируемых в течение более длительного времени, эпителиальная архитектура корковой и медуллярной области все еще может быть легко различима; например, тельца Гассаля остаются в медуллярных областях. Степень обеднения тимоцитами, однако, приводит к существенно отличной общей гистологической картине при окрашивании H&E по сравнению с нормальным тимусом в моменты времени позже 0 дня.
Подробное культивирование ткани тимуса.
[00220] Общая процедура получения продукта, полученного из аллогенной культивированной ткани тимуса, заключается в том, что ткань тимуса для грудных детей с полным синдромом Ди Георга получают в виде удаленной в отходы ткани от грудных детей в возрасте до 9 месяцев, подвергаемых операции на сердце, как описано ранее. Для трансплантации цельного органа удаленный в отходы тимус будет получен от людей в возрасте до 50 лет.Использование ткани тимуса будет зависеть от того, соответствует ли она критериям для использования, изложенным в данном описании.
[00221] Ткань тимуса аспетически обрабатывают и культивируют в условиях cGMP с получением срезов ткани тимуса, частично обедненных Т-клетками.
[00222] Производство культивированной ткани тимуса (КТТ) состоит из следующих основных этапов: получение и обработка поступающей ткани тимуса, нарезание на срезы, культивирование, замены среды, расчет дозы, упаковка и транспортировка тимуса в операционную. Кроме того, поступающую ткань тимуса проверяют на пригодность, а срезы ткани тимуса подвергают тестированию в процессе производства и при выпуске.
[00223] В одном варианте осуществления процесс нарезания на срезы ткани тимуса включает использование стерильных одноразовых ножниц и пинцета для отрезания кусочка ткани тимуса. Оперирующий хирург удаляет капсулу тимуса с помощью пинцета и ножниц и помещает капсулу в крышку чашки для последующей утилизации.
[00224] Кусочек ткани тимуса помещают в одноразовый инструмент для приготовления срезов ткани с помощью пинцета. Верхнюю часть инструмента для приготовления срезов (например, ручного микротома Stadie-Riggs (Thomas Scientific, Суидсборо, Нью-Джерси)) помещают на среднюю часть инструмента для приготовления срезов и закрепляют на месте. Оперирующий хирург пропускает лезвие через кусочек ткани, чтобы отрезать срез. Срезы имеют толщину приблизительно от 0,5 до 1 мм. После разрезания каждого среза верхнюю часть среза удаляют, и срез ткани переносят на предварительно смоченные стерилизованные фильтры Millipore с помощью пинцета. Фильтры предварительно смачивают TOM. Заполняют приблизительно 50-90% пространства фильтра без наложения кусочков ткани.
[00225] Как правило, в процессе производства от ткани отрезают три кусочка в начале нарезания, все из которых имеют размер примерно 3x3 мм. Один отправляют для гистологического исследования, а два сохраняют.Тимоциты свободно поступают в среду при нарезании тимуса на срезы.
[00226] В одном варианте осуществления фильтр и срезы тимуса переносят на желатиновую хирургическую губку, пропитанную TOM, в чашке для тканевых культур. Два фильтра помещают на губку и используют 2 губки на чашку для тканевых культур. Процесс нарезания срезов тимуса повторяют до тех пор, пока не будет подготовлено необходимое количество срезов. Культуральные чашки помечают номером операции, номером чашки и этикеткой со штрихкодом ISBT. Готовые чашки помещают в увлажненный инкубатор при 37°C с 5% CO2.
[00227] Тканеинженерное лекарственное вещество содержит срезы ткани тимуса после того, как они были помещены в культуральную чашку в среду и культивированы в течение 12-21 дня, как описано ниже. Тканеинженерный лекарственный препарат содержит срезы ткани тимуса после переноса в контейнер для лекарственного препарата. Для создания лекарственного препарата из лекарственного вещества не проводится никакая другая обработка; единственной обработкой лекарственного вещества для создания лекарственного препарата является перенос срезов в герметичный контейнер и соответствующая смена среды.
[00228] Культивирование срезов ткани тимуса более конкретно изложено в следующих абзацах.
[00229] В одном варианте осуществления ткань тимуса получают из операционной как удаленную в отходы ткань от грудных детей в возрасте 9 месяцев и подвергаемых операции на сердце. Затем операционная бригада помещает ткань в стерильную чашку для образцов с завинчивающейся крышкой и транспортирует в учреждение GMP при условиях окружающей среды для обработки. Стерильный контейнер для образцов, в который поступает тимус, помечен, включая штрих-код, именем донора и номером медицинской карты. Группа скрининга доноров присваивает тимусу уникальный идентификатор (тимусы нумеруют последовательно) и уникальный номер медицинской карты. Для производства каждая ткань имеет номер операции и уникальную этикетку. Все идентификаторы внесены в «Конфиденциальную форму донора тимуса», которая ведется отдельно от документации партии и является конфиденциальной.
[00230] В одном варианте осуществления система укупорки контейнера с лекарственным веществом может представлять собой чашку для клеточных культур с крышкой. Один срез ткани тимуса помещают на фильтр, и два фильтра помещают на каждую желатиновую губку в органной среде для тимуса в чашке. Четыре среза помещают в каждую чашку для культивирования, и чашки хранят в инкубаторе с ежедневной сменой среды до готовности к выпуску.
[00231] В одном варианте осуществления чашки для культивирования могут быть получены от Corning. Чашки могут быть стерильными, непирогенными чашками для клеточных культур из полистирола от Falcon® размером 100 мм (продукт №353003). Чашки очищают обработкой газоразрядной плазмой в вакууме и стерилизуют гамма- излучением. Размеры чашки составляют 89,43 мм внешнего диаметра на 19,18 мм.
[00232] В иллюстративном варианте осуществления губка Surgifoam® может быть произведена компанией Ethicon, и она соответствует требованиям к рассасывающейся желатиновой губке согласно USP (Фармакопея США). Подходящей губкой является стерильная, нерастворимая в воде, эластичная, рассасывающаяся губка из свиного желатина, предназначенная в качестве кровоостанавливающего средства.
Иллюстративным примером фильтра из смешанного эфира целлюлозы является фильтр, изготовленный Millipore (продукт №SMWP 02500). 25 мм гидрофильная мембрана имеет размер пор 5,0 мкм. Ее изготавливают из биологически инертных смесей ацетата целлюлозы и нитрата целлюлозы. Фильтр стерилизуют окисью этилена перед использованием.
[00233] После выпуска и приема тимуса донора в лабораторию для обработки тимус нарезают на тонкие срезы, которые помещают на стерильные кусочки фильтровальной бумаги, которые помещают на хирургические губки в стерильные чашки для культивирования. Если ткань обрабатывают не сразу, ее хранят в органной среде для тимуса (TOM), как описано ниже, при 2-8°C в течение до 24 часов после сбора у донора до начала обработки. TOM состоит из культуральной среды Хэма F-12, буфера HEPES, L-глутамина и термоинактивированной фетальной бычьей сыворотки (FBS).
[00234] В одном варианте осуществления обработка происходит в помещении бокса биологической безопасности (BSC), соответствующего ISO 5, в производственной чистой комнате, соответствующей ISO 7. Только одна партия ткани тимуса от одного тимуса обрабатывается в BSC в любой момент времени. BSC очищают перед использованием. Тимус проверяют на внешний вид путем визуального осмотра и взвешивают.Затем тимус помещают в 150-миллиметровую чашку для тканевых культивирования в TOM. Капсулу тимуса удаляют стерильным одноразовым пинцетом и ножницами. Кусочки ткани отбирают для тестирования и в качестве архивных образцов. Поступающую ткань тимуса тестируют на принадлежность с помощью гистологического исследования. Пригодность донора также подтверждают.Обработку продолжают до получения результатов гистологического исследования и всех результатов скрининга донора.
[00235] Критерии приемлемости для скрининга доноров таковы, что должны быть соблюдены все требования по пригодности донора. Скрининг доноров необходим в соответствии с разделом 21, частью 1271 CFR для защиты безопасности реципиента трансплантата ткани тимуса. Этот скрининг минимизирует риск передачи заболевания от донора реципиенту.
[00236] С помощью стерильных одноразовых ножниц и пинцета отрезают кусочек ткани. Кусочек ткани помещают в одноразовый инструмент для приготовления срезов ткани с помощью пинцета. Как описано выше, верхнюю часть инструмента для приготовления срезов помещают на среднюю часть инструмента для приготовления срезов и закрепляют на месте. Оперирующий хирург пропускает лезвие через кусочек ткани, чтобы отрезать срез. Срезы имеют толщину приблизительно от 0,5 до 1 мм. После разрезания каждого среза верхнюю часть среза удаляют, и срез ткани переносят на предварительно смоченные стерилизованные фильтры Millipore® с помощью пинцета. Фильтры предварительно смачивают TOM. Заполняют приблизительно 50-90% пространства фильтра без наложения кусочков ткани. Фильтр и срезы тимуса переносят на желатиновую хирургическую губку, пропитанную TOM, в чашке для тканевых культур.
Органная среда для тимуса (TOM)
[00237] Среду изготавливают из ингредиентов, одобренных для применения у людей, с низкой вероятностью аллергических реакций, когда такие реагенты доступны.
[00238] Все реагенты должны отслеживаться таким образом, чтобы все ингредиенты можно было идентифицировать после трансплантации, если возникнут какие-либо проблемы.
[00239] Фетальная бычья сыворотка (FBS) должна быть изготовлена с использованием материала из США из-за проблем с болезнью Крейтцфельдта-Якоба. Информация о каждой партии должна быть отправлена в FDA до использования.
[00240] Хотя нормальные взрослые имеют природные антитела к FBS (антитела к галактозе-альфа-1,3-галактозе (Gal-α-1-3Gal)), которые тестируются как изогемагглютинины IgM, у детей с иммунодефицитом с синдромом Ди Георга эти антитела отсутствуют.4.4. (Parker W, Yu PB, Holzknecht ZE, Lundberg K, Buckley RH, Platt JL., 1997, “Specificity and function of ‘natural’ antibodies in immunodeficient subjects: Clues to B cell lineage and development,” J Clin Immunol. 17: 311-321).
[00241] Среда должна быть проверена на бактериальное, грибковое и микоплазменное загрязнение перед использованием.
[00242] В одном варианте осуществления для приготовления TOM используют следующие материалы:
[00243] HAMS F12, Gibco №11765-054 (или вариант 11765-062), бутылки по 500 мл или эквивалентный источник.
[00244] HEPES, Gibco №15630-080 или эквивалент, 1M раствор, бутылки по 100 мл. Конечная концентрация 25 мМ.
[00245] L-глутамин, Gibco №25030-081 или эквивалентный источник (исходно 200 мМ).
[00246] Фетальная бычья сыворотка, Gibco, №16140 (термоинактивированная) или №10082-147 (термоинактивированная, сертифицированная).
[00247] В одном варианте осуществления FBS, которая является термоинактивированной, может быть использована следующим образом:
[00248] FBS должна быть термоинактивирована при 56°C в течение 30 мин.
[00249] Чтобы снизить вероятность загрязнения среды, среду следует разделить на аликвоты, и аликвоту не следует использовать более одного раза.
[00250] Аликвоты оставшегося FBS можно хранить в замороженном виде (-20°C) в аликвотах по 25 мл для использования в исследованиях.
[00251] В одном варианте осуществления TOM может быть приготовлена следующим образом.
[00252] Разморозить фетальную бычью сыворотку в течение ночи в холодильнике или при температуре 37°C, часто осторожно перемешивая путем вращения сосуда.
[00253] Если используется фетальная бычья сыворотка, не являющаяся термоинактивированной, провести термоинактивацию при 56°C в течение 30 минут.
[00254] Поместить все компоненты среды вместе в 4-литровую колбу, если необходимо приготовить 4 литра за один раз, перемешивать в течение 3-5 минут с помощью якоря мешалки на столике магнитной мешалки на средней скорости (без образования пены).
[00255] Стерилизовать с использованием фильтров на 0,2 мкм.
[00256] В одном варианте осуществления стерилизация препарата TOM может быть осуществлена следующим образом. Налить 1 литр TOM в колбу на один литр. Отмерить 80 мл TOM в одноразовый стерильный цилиндр. Налить 80 мл TOM в аппарат для стерилизующей фильтрации Corning на 150 мл. Подсоединить вакуумный шланг и осуществить стерилизующую фильтрацию в соответствии с указаниями производителя. Вынуть блок фильтра из контейнера и утилизировать. Закрыть колбу для сбора стерильной крышкой (входит в комплект). Пометить номером партии TOM. Протестировать одну аликвоту на наличие бактериальной культуры с анаэробами; грибковую культуру, другое; и микоплазменную культуру. Протестировать одну аликвоту на наличие эндотоксина. Хранить все аликвоты TOM в морозильной камере при -20°C в вертикальном положении.
[00257] Среда TOM может быть выпущена для использования, если: результат на LAL (лизат амебоцитов Limulus) равен или меньше 2 ЕЭ/мл для образцов, разведенных в 20 раз для тестирования, или 1 ЕЭ/мл для образцов, разведенных в 10 раз для тестирования; все результаты культивирования показывают отсутствие роста.
[00258] Для фильтрации и дозирования среды должен применяться BSC.
[00259] Перед выпуском TOM тестируют на стерильность и наличие эндотоксина. TOM не выпускают для культивирования тимуса донора до тех пор, пока не будет соблюден критерий приемлемости 14-дневного теста на стерильность. После приготовления TOM хранится при температуре -20°C до размораживания, после чего ее можно хранить в холодильнике до двух недель.
[00260] В одном варианте осуществления 14-дневный тест на стерильность может, например, проводиться с использованием системы культивирования BacT/ALERT. BacT/ALERT (BioMerieux, Дарем, Северная Каролина) - это коммерчески доступная система культивирования, которая может использоваться для тестирования образцов с использованием автоматической системы детекции микроорганизмов.
[00261] Все находящиеся в процессе производства культуры и культуры лекарственного вещества инкубируют в течение 14 дней или немедленно сообщают, если продукт становится положительным. Для положительных тестов организм(ы) идентифицируют и определяют их чувствительность к антибиотикам. Флаконы с культурами, содержащие среду для аэробного роста, и флаконы, содержащие среду для анаэробного роста, инокулируют образцами, подлежащими тестированию, в 1 день, 7 день и день выпуска. Все флаконы инкубируют в течение 14 дней при 35-37°С.
[00262] FBS может быть получена от бренда GIBCO, Life Technologies. FBS готовят с помощью асептического, утвержденного процесса. FBS отвечает требованиям USDA (Министерства сельского хозяйства США) в отношении происхождения животных со скотобойни, возможности отслеживания и страны происхождения. Всю фетальную кровь собирают от плодов, полученных от здоровых матерей, которые прошли сертифицированный ветеринарный осмотр до и после смерти. Все FBS отслеживаются по дате и месту сбора. FBS, собранная и обработанная в Соединенных Штатах, происходит от одобренных и проверенных USDA предприятий по убою. США признаны USDA свободными от ящура и чумы крупного рогатого скота. Чтобы квалифицировать поставщика, перед применением FBS тестируют на pH, осмоляльность, наличие эндотоксина, тотальный белок и принадлежность.
[00263] Готовые чашки помещают в увлажненный инкубатор при 37°C с 5% CO2. Каждую партию ткани тимуса хранят в отдельном инкубаторе. После помещения срезов тимуса в инкубатор проводят отбор проб частиц и мониторинг персоналом.
[00264] Срезы тимуса культивируют в течение до 21 дня и ежедневно меняют среду во время культивирования. Эти срезы тимуса считаются лекарственным веществом. В течение периода культивирования многие тимоциты вымываются из срезов ткани тимуса или тимоциты претерпевают апоптоз при сохранении стромы тимуса. Все этапы производства проводят с использованием стерильного одноразового оборудования и расходных материалов. Среду отсасывают пипеткой из чашки для культивирования и помещают в один стерильный коллекторный контейнер для тестирования в процессе производства. Десять (10) мл свежей органной среды для тимуса затем аккуратно отмеряют в каждую чашку для культивирования путем ополаскивания срезов ткани. После завершения замены среды из объединенной среды при необходимости отбирают пробы на стерильность и гистологию. Отбор проб частиц и мониторинг персоналом завершают и производят очистку производственной линии.
[00265] Среду меняют ежедневно.
[00266] Срезы культивируют в течение до 21 дня.
[00267] Тестирование в процессе производства проводится для обеспечения понимания процесса и качества продукта, а также для обеспечения безопасности и качества конечного лекарственного препарата.
Тестирование в процессе производства
[00268] Образцы собирают для тестирования на стерильность в процессе производства в 1 день и 7 день. Образцы собирают для тестирования на микоплазму в процессе производства на 7 день. Образцы собирают для гистологического исследования в процессе производства между 5 и 9 днями. Дозу определяют за день до выпуска. Окрашивание по Граму, BacT, тесты на микоплазму и эндотоксин проводят в день выпуска.
[00269] Окрашивание по Граму представляет собой бактериологический лабораторный метод, используемый для разделения видов бактерий на две группы: грамположительные и грамотрицательные. Окрашивание по Граму проводят на объединенной отработанной культуральной среде из чашек для культивирования. В этом способе используется метод окрашивания для определения классификации на основе физических свойств клеточной стенки. Этот способ используется для предварительной морфологической идентификации или для определения наличия значительного количества бактерий в клиническом образце. Окрашивание проводят либо вручную, либо с использованием автоматического прибора для окрашивания. Было продемонстрировано, что два разных метода окрашивания не показали качественных различий, которые могли бы повлиять на результаты культивирования.
[00270] Гистологическое исследование, проводимое на 5-9 день, включает: (1) определение того, что области, положительные на кератин AE1/AE3, рассредоточены по всей ткани в 5-9 дни; (2) микроскопически идентифицировано по меньшей мере 1 тельце Гассаля; (3) окрашивание на CK14 срезов ткани рассредоточено по всей ткани тимуса; и (4) микроскопически наблюдаются интактные ядра.
[00271] Наличие телец Гассаля и интактных ядер, а также успешное окрашивание на CK14 указывают на нормальную здоровую ткань тимуса, которая была культивирована.
[00272] Время культивирования является важным параметром процесса. Как отмечается, культивирование проводят в течение до 21 дня.
[00273] Тестирование образцов тимуса в 5, 9, 12 и 21 дни в культуре проводят для определения, являются ли результаты гистологического исследования, полученные между 5 и 9 днями в культуре, репрезентативными для результатов гистологических исследований, полученных между 12 и 21 днями в культуре. На основании наблюдений, проведенных гистологом для образцов, обсуждаемых в примерах, гистологическая картина срезов ткани на 5 день отражает наблюдения в каждый из более поздних моментов времени (9, 12 и 21 день). Это подтверждает необходимость проведения тестирования при выпуске между 5 и 9 днями.
[00274] Гистологическое исследование любого среза подтверждает заключение о приемлемости всей партии. Релевантные характеристики любого среза тимуса отражают характеристики всего тимуса, подтверждая продолжение использования одного среза ткани для гистологического тестирования.
[00275] Тестирование на принудительную деградацию, указанное, как показано на фиг. 12А и 12В, продемонстрировало, что продукт культивированной ткани тимуса не подвергается легкой деградации и наиболее чувствителен к замораживанию/размораживанию, а также к изменениям осмолярности. Другие условия, протестированные во время тестирования на принудительную деградацию, практически не влияли на продукт культивированной ткани тимуса.
Контроль лекарственного вещества культивированного продукта тимуса
[00276] Критерии приемлемости поступающего продукта ткани тимуса включают тесты, приведенные ниже в таблице 1.
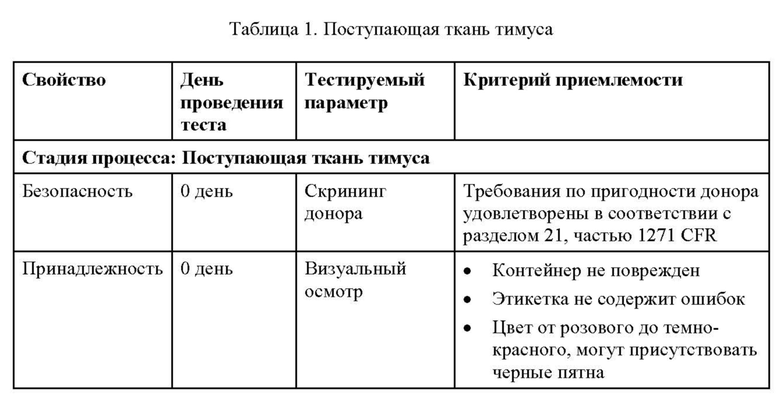
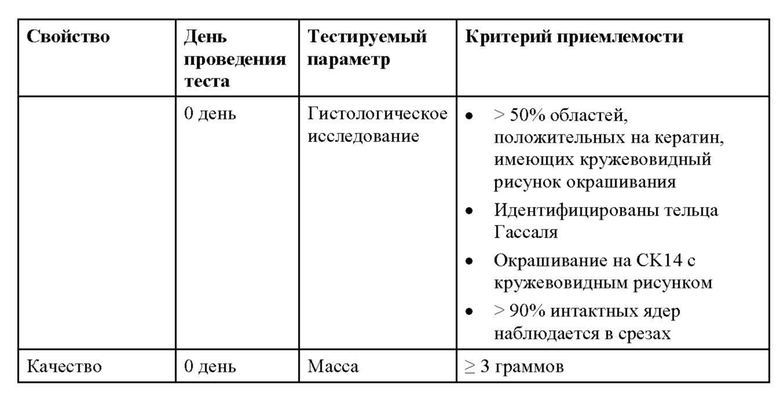
[00277] Сокращения: CK, цитокератин; ЭЕ, эндотоксиновая единица; USP, Фармакопея США. Ткань тимуса обрабатывают до получения всех результатов скрининга донора.
[00278] Как правило, критерий приемлемости для массы равен 3 граммам или более. Это соответствует минимальной массе тимуса, которая является приемлемой для обеспечения достаточного количества материала для правильной дозировки конечного продукта. Критерий приемлемости основан на опыте обработки ткани тимуса.
[00279] Критерии приемлемости для тестирования в процессе производства приведены ниже в таблице 2.
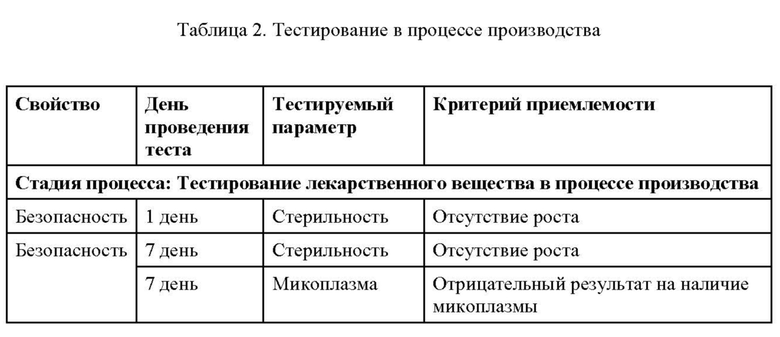

[00280] Критерии приемлемости для тестирования лекарственного вещества из культивированной ткани тимуса приведены ниже в таблице 3.
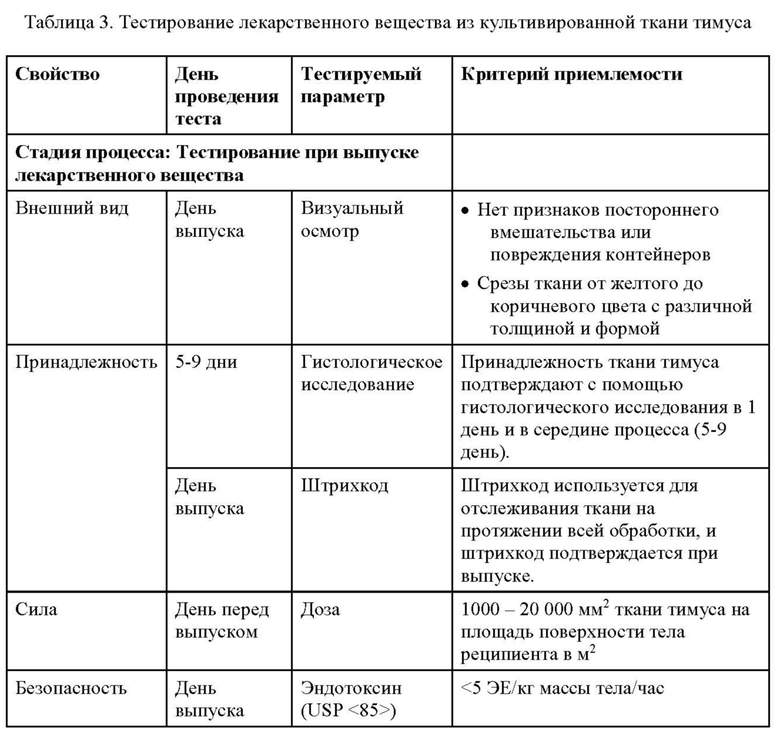
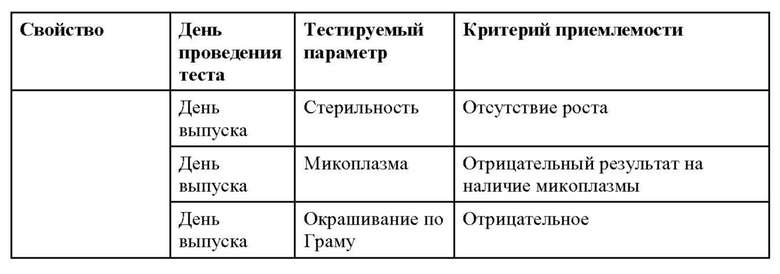
[00281] Критерием приемлемости для принадлежности является подтверждение принадлежности ткани тимуса с помощью гистологического исследования в 1 день и в середине процесса (5-9 день). Штрихкод используется для отслеживания ткани на протяжении всей обработки, и штрихкод подтверждается при выпуске для проверки верной принадлежности продукта.
Гистологическое исследование по иммунохимии
[00282] Метод гистологии является стандартным методом, используемым в больницах для всех типов тканей, как известно специалисту в данной области техники.
[00283] Образцы продукта фиксируют в 10% формалине и перевозят в лабораторию. Контейнеры помечают закодированным идентификатором вместо имени пациента для защиты конфиденциальности пациента вместе с номером медицинской карты. По прибытии в гистологическое отделение образцам присваивается уникальный регистрационный номер гистологического отделения и штрихкод. Все последующие блоки, предметные стекла и документы помечают штрихкодом с этим номером гистологического отделения.
[00284] После того, как образец получен в лаборатории, фиксированную в формалине ткань макроскопически проверяют и готовят письменное общее описание материала, которое станет частью окончательного отчета. Затем фиксированную в формалине ткань обрабатывают и погружают в парафиновый блок по стандартной методике на автоматизированном обрабатывающем устройстве. Из парафинового блока вырезают срезы, и сертифицированные ASCP (Американским обществом клинической патологии) лаборанты-гистологи проводят следующие виды окрашивания:
[00285] Гематоксилин и эозин.
[00286] Иммуногистохимическое исследование на цитокератин с AE1/AE3.
[00287] Иммуногистохимическое исследование на цитокератин 14.
[00288] Иммуногистохимическое исследование на CD3.
[00289] Иммуногистохимическое исследование на Ki-67.
[00290] Во время выполнения вышеупомянутых иммуногистохимических исследований также проверяются и анализируются соответствующие контрольные предметные стекла. Все контрольные предметные стекла и внутренние контроли демонстрируют ожидаемую иммунореактивную картину. Поступающий образец тимуса также служит в качестве контроля для срезов ткани, которые были культивированы в течение 5-9 дней при тестировании образцов в рамках тестирования активности. Поступающий образец тимуса выглядит как типичный образец тимуса, после чего в ходе культивирования в течение 5-9 дней и последующего тестирования в срезах ткани происходят изменения. После 5-9 дней культивирования образец должен демонстрировать области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер.
[00291] Предметные стекла интерпретируются гистологом, сертифицированным в области патологической анатомии, с дополнительным опытом в гистологической оценке ткани тимуса. Окончательный отчет выдается гистологом, и в нем фиксируются результаты.
[00292] Критерии приемлемости для тестирования лекарственного вещества из культивированной ткани тимуса приведены ниже в таблице 4.
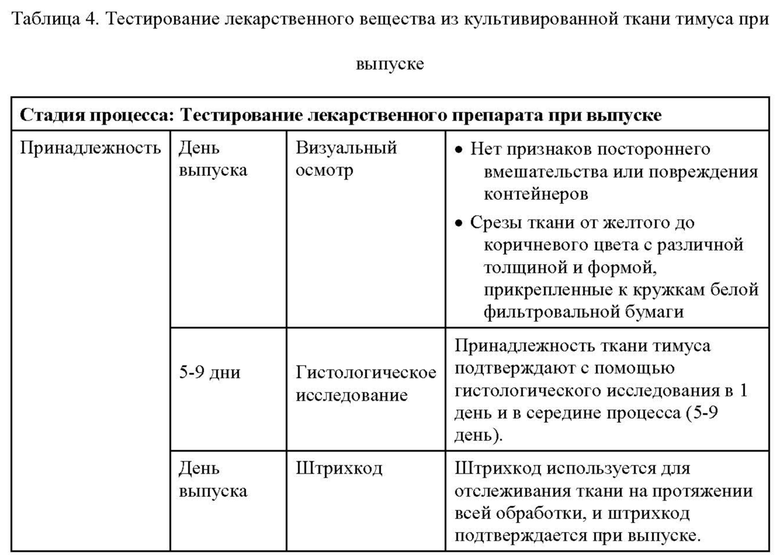
[00293] Культивированная ткань тимуса не должна содержать микроорганизмов. В тесте на стерильность, проводимом в 1 день и 7 день, не должно быть выявлено роста микроорганизмов. При тестировании на 7 день результат в отношении микоплазмы должен быть отрицательным. Тест на стерильность должен показывать отрицательный результат окрашивания по Граму.
[00294] Стерильность продукта поддерживают с использованием соответствующих контролей, включая асептическую технику; использование программы обучения и проверки квалификации лаборантов; использование надлежащих процедур квалификации чистых помещений; применение установленных процедур наполнения средой и использование готового к использованию стерилизованного устройства или устройства, стерилизованного с использованием утвержденных циклов стерилизации.
[00295] Контейнеры с обработанной тканью тимуса визуально осматривают на наличие повреждений. Срезы ткани обычно имеют цвет от желтого до красновато-коричневого с различной толщиной и формой.
[00296] Принадлежность ткани тимуса подтверждают с помощью гистологического исследования в 1 день и в середине процесса (5-9 день).
[00297] Штрихкод используется для отслеживания ткани на протяжении всей обработки, и штрихкод подтверждается при выпуске.
[00298] Дозировка (площадь) составляет 1000-20000 мм2 ткани тимуса на площадь поверхности тела реципиента в м2. Дозу контролируют по площади поверхности срезов, поступающих в операционную, в зависимости от площади поверхности тела пациента.
[00299] Приемлемый диапазон доз определен как 1000-20000 мм2 ткани тимуса на площадь поверхности тела (ППТ) реципиента в м2. Площадь ткани тимуса определяют по фотографии с использованием программного анализа (программное обеспечение для анализа изображений PAX-it). ППТ определяют с использованием роста пациента в см и массы в кг. Для расчета ППТ использую формулу Дюбуа и Дюбуа:
[00300] ППТ=0,007184 × [рост (см)]0,725 × [масса тела (кг)]0,425.
[00301] Культивированную ткань тимуса проверяют на наличие эндотоксина. Стандарт составляет ≤ 5 ЭЕ/кг массы тела/час.
[00302] Тестирование на эндотоксин может быть проведено, например, с использованием системы Endosafe PTS. В картриджах, используемых с Endosafe PTS, используется хромогенный кинетический тест на лизат амебоцитов Limulus (LAL). Каждый картридж содержит точное количество реагента LAL, хромогенного субстрата и контрольного стандартного эндотоксина. Тестируемый образец с помощью пипетки отмеряют в четыре резервуара для образцов. Прибор отбирает и смешивает образец с реагентом LAL в двух каналах (каналы для образцов) и с реагентом LAL и положительным контролем продукта в двух других (каналы с добавкой). Образец инкубируют, а затем объединяют с хромогенным субстратом. После смешивания измеряют оптическую плотность лунок и сравнивают с градуировочной кривой, сохраненной в приборе. Прибор измеряет время реакции в каждом канале. Сохраненную градуировочную кривую, специфичную для каждой партии картриджей, строят с использованием зависимости логарифма времени реакции от логарифма стандартной концентрации эндотоксина. Значения для образца и добавки рассчитывают путем интерполяции по градуировочной кривой с использованием времени реакции. Это тестирование соответствует требованиям Фармакопеи США (USP).
[00303] Тестирование на микоплазму может быть проведено следующим образом. Образец объединенной среды извлекают из планшетов на 7 день и тестируют перед выпуском продукта.
[00304] В случае положительного результата на культуру во время производства партия будет утилизирована и не будет введена. В случае положительного результата на культивирования после введения клинического препарата лечащий врач пациента и спонсор клинического исследования будут относиться к пациенту надлежащим образом. Положительный результат на культуру требует идентификации видов загрязняющего организма и определения его чувствительности к антибиотикам. Лечащий врач назначит антибиотикотерапию для реципиента тимуса, если она показана.
[00305] Препарат проходит аналогичные визуальные осмотры и гистологическое исследование перед применением.
[00306] После культивирования срезов ткани тимуса в течение до 21 дня срезы переносят в контейнеры для лекарственного препарата для транспортировки в операционную. После получения в операционной срезы внедряют в мышцу бедра реципиента.
[00307] Контейнер должен быть целым, без видимых повреждений, и срезы ткани имуса должны иметь вид от желтых до красновато-коричневых срезов ткани с различной толщиной и формой. Срезы ткани визуально осматривают, чтобы подтвердить, что эти критерии приемлемости удовлетворены.
Криоконсервация и размораживание продукта, полученного из аллогенной культивированной ткани постнатального тимуса
[00308] Криоконсервация продукта, полученного из аллогенной культивированной ткани постнатального тимуса, может быть проведена следующим образом.
[00309] Криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, полученный способом, включающим следующие стадии:
[00310] (a) получение подходящей ткани тимуса от донора;
[00311] (b) типирование аллелей HLA: HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DRB3, HLA-DRB4, HLA-DRB5, HLA-DQA1, HLA-DPB1, HLA-DPA1;
[00312] (c) подвергание ткани тимуса режиму кондиционирования на период до 12 дней; где режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных T-клетками срезов донорской ткани тимуса; дополнительно где по завершении режима кондиционирования срезы донорской ткани тимуса демонстрируют, на 5-9 день, области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, наличие по меньшей мере одного тельца Гассаля, окрашивание на CK14, рассредоточенное по всей ткани, и наличие интактных ядер;
[00313] (d) сбор частично обедненных T-клетками срезов донорской ткани тимуса в качестве продукта, полученного из аллогенной культивированной ткани постнатального тимуса;
[00314] (e) криоконсервация продукта, полученного из аллогенной культивированной ткани постнатального тимуса, в жидком азоте; и
[00315] (f) хранение криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, в жидком азоте в банке криоконсервированного продукта, полученного из аллогенной культивированной ткани постнатального тимуса. В одном варианте осуществления криоконсервированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, по п. 66 формулы, где тимус в день сбора демонстрирует, что >50% областей являются положительными на кератин, о чем свидетельствует кружевовидный рисунок окрашивания, присутствуют тельца Гассаля, что окрашивание на CK14 обеспечивает кружевовидный рисунок, и что >90% ядер являются интактными.
[00316] В одном варианте осуществления тимус донора нарезают на срезы и разделяют на две примерно равные части, помещая каждый срез с его целлюлозным фильтром в отдельный криофлакон (пробирки от Nunc). Фильтр складывают пополам, чтобы вставить его в пробирку. Добавляют от приблизительно 1 до приблизительно 1,5 мл среды для замораживания [подвергнутой стерилизующей фильтрации 90% термоинактивированной фетальной бычьей сыворотки (FBS) и 10% диметилсульфоксида (ДМСО)] при комнатной температуре, чтобы она покрывала ткань. На пробирке заменяют стерильную крышку криофлакона. Все пробирки помещают в Cool Cell от Biocision или эквивалентную емкость, находящуюся при комнатной температуре. Любые пустые ячейки в CoolCell должны быть заполнены пробирками с 1 мл среды для заморозки. Пробирки помещают на ночь в морозильную камеру при -80°C. В качестве альтернативы каждую ткань с фильтром помещают в 5 мл флакон для тканей CryoELITE (Wheaton). Помещают от 3 до 5 мл среды для заморозки при комнатной температуре, чтобы она покрыла ткань. Помещают в коробку Styrofoam и ставят на ночь в морозильную камеру при -80°. Затем флаконы переносят в паровую фазу криогенного аппарата на базе жидкого азота. В качестве альтернативы для доведения температуры криофлаконов до температуры жидкого азота можно использовать криогенный аппарат с регулируемой скоростью замораживания.
[00317] Чтобы восстановить ткань, необходимо извлечь криофлакон или флакон для ткани CryoELITE из криогенного аппарата на базе жидкого азота. Необходимо быстро разморозить кусочки тимуса путем вращения флакона на водяной бане при 37°C. Пробирку опрыскивают 70% этанолом, а затем помещают в бокс биологической безопасности (BSC). Ткань тимуса и фильтр удаляют из криофлакона Nunc или из флакона для ткани CryoELITE с помощью пинцета. Ткань и фильтр помещают в коническую пробирку объемом 50 мл, содержащую 20 мл TOM при 4°C. В каждую коническую пробирку объемом 50 мл, содержащую 20 мл ТОМ при 4°C, можно поместить до 5 фильтров. Необходимо немедленно перенести 5 фильтров с тканью в свежую коническую пробирку с 20 мл среды TOM при 4°C и оставить на 15 минут при 4°C. Промывку повторяют 3 раза. Удерживая ткань при 4°C, каждый кусочек переносят в собственный контейнер Starplex на 120 мл с 5 мл TOM при 4°. Все контейнеры доставляют в хирургический блок в термостатированном контейнере с охлаждающим пакетом внутри. Контейнеры Starplex с тканью доставляют в операционную. Ткань на фильтрах переносят в стерильное поле в чашку для тканевых культур с приблизительно 2 мл стерильного физиологического раствора. Операционная медицинская сестра удаляет ткань с фильтровальной бумаги путем соскабливания или вытягивания пинцетом. Операционная медицинская сестра помещает ткань, находящуюся в виде бесформенной стопки, обратно на фильтровальную бумагу. Чашку для тканевых культур с приблизительно 4 фильтрами и тканью переносят в место проведения операции, где хирург может легко получить доступ к ткани. Ткань помещают в четырехглавую мышцу аналогично процедуре с КТТ (RVT- 802). Cryo-CTT схож с КТТ в том, что он частично обеднен Т-клетками, срезы ткани тимуса демонстрируют области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани, срезы содержат по меньшей мере одно тельце Гассаля, окрашивание на CK14 рассредоточено по всей ткани, и присутствуют интактные ядра.
Трансплантация КТТ
[00318] В одном варианте осуществления несоответствующие срезы ткани тимуса от донора культивируют в течение 12-21 дня. В день трансплантации цельного органа обычно назначают стероиды обычно при индукции анестезии. При трансплантации сердца или легкого тимус реципиента хирургическим путем удаляют во время трансплантации цельного органа. При трансплантации других органов тимэктомия может быть выполнена до дня трансплантации или в этот день. Метод тимэктомии будет хирургическим, торакоскопическим или роботизированным. По окончании операции после реперфузии реципиенту дают больше стероидов перед получением конского антитимоцитарного глобулина (например, кроличьего антитимоцитарного глобулина) в течение 3-7 дней для уничтожения большей части остаточных Т-клеток (и NK-клеток) у реципиента, или алемтузумаб в течение 4 дней для уничтожения Т-, В- и NK-клеток. Затем начинают введение иммуносупрессивного препарата (такого как циклоспорин или такролимус) и микофенилата до тех пор, пока не разовьются Т-клетки и не будет выявлено более 10% наивных Т-клеток. Для увеличения числа наивных Т-клеток до этого значения может потребоваться от 6 до 12 месяцев. Культивированную ткань тимуса обрабатывают для тимуса донора цельного органа. Половина КТТ может быть имплантирована в четырехглавую мышцу между 12 и 21 днями. Другая половина тимуса будет подвергнута криоконсервации для будущего использования реципиентом. Иммуносупрессивные режимы будут подавлять любые оставшиеся Т-клетки до тех пор, пока срезами культивированной ткани тимуса, имплантированными реципиенту, не будут высвобождены наивные Т-клетки, и реципиент не будет удовлетворять критериям постепенного прекращения поддерживающего иммуносупрессивного режима (для постепенного прекращения введения иммуносупрессивных препаратов необходимо более 10% наивных Т-клеток).
Протокол тимэктомии
[00319] Пациента доставляют в операционную и помещают под общую анестезию с помощью интубационной трубки.
[00320] Грудь и брюшную полость подготавливают и обкладывают простынями в стерильных условиях.
[00321] Пациент подвергается полной стернотомии через разрез кожи размером около 4 см.
[00322] Осуществляют вход в обе плевральных полости, чтобы гарантировать полную резекцию.
[00323] Диафрагмальные нервы визуализируют с обеих сторон и стараются не ставить их под угрозу.
[00324] Тимус идентифицируют и тщательно отсекают от плеврального листка легкого, проходя с нижних рогов до верхних рогов.
[00325] Проводят полную тимэктомию.
[00326] В средостении достигается гемостаз.
[00327] Размещение плевральной дренажной трубки. Одну плевральную дренажную трубку вставляют всегда (в средостение). Если во время операции осуществляется вход в одну плевральную полость, плевральная дренажная трубка проходит от средостения до этой плевральной полости. Если осуществляется вход в обе плевральных полости, используют вторую плевральную дренажную трубку, аналогичным образом проходящую от средостения до другой плевральной полости.
[00328] Размер дренажа. Для грудных детей возрастом до 2 лет используют дренажи Blake №15. Для детей возрастом от 2 лет используют дренажи Blake №19.
[00329] Закрытие грудины: у новорожденных или грудных детей для закрытия грудины используют швы 0-Ticron. Для возраста приблизительно 1-2 года используют стернальные провода №1. Для возраста приблизительно 2-5 лет используют стернальные провода №4.
[00330] Фасцию, подкожную клетчатку и кожу закрывают с помощью непрерывного рассасывающегося шовного материала.
[00331] На грудину помещают вакуумную повязку для раны.
[00332] Пациента экстубируют в операционной.
[00333] Должен производиться подсчет количества губок, инструмента и игл, которое должно быть правильным в конце операции.
Хирургическая имплантация продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
[00334] Продукт, полученный из аллогенной культивированной ткани постнатального тимуса, должен быть имплантирован в соответствии со следующими инструкциями. Имплантация ткани тимуса в бедро требует здорового ложа мышечной ткани.
Подготовка к процедуре имплантации
[00335] Максимальную и минимальную дозу продукта, полученного из аллогенной культивированной ткани постнатального тимуса, планируемую для трансплантации, следует рассчитывать для каждого отдельного пациента. Предполагаемого реципиента необходимо надлежащим образом идентифицировать до введения.
[00336] В стерильных условиях в вытяжном шкафу с ламинарным потоком срезы ткани на кусочках фильтровальной бумаги, находящихся на хирургических губках в среде, извлекают из чашек для тканевых культур и помещают в стерильные чашки объемом 120 мл с 20 мл среды, упакованные для поддержания стерильности и доставляемые в операционную или упакованные для отправки. Срезы ткани не извлекают из индивидуальных контейнеров до тех пор, пока они не будут готовы к использованию. Необходимо проверить дату и время истечения срока годности продукта.
[00337] Продукт, полученный из аллогенной культивированной ткани постнатального тимуса (срезы ткани) всегда должен обрабатываться с использованием строгой стерильной техники. Необходимо осмотреть каждый контейнер на предмет утечек или признаков повреждения. В случае признаков загрязнения использование запрещено. За пределами стерильного поля необходимо вынуть контейнеры для продукта, полученного из аллогенной культивированной ткани постнатального тимуса, из упаковочной коробки. Необходимо вынуть стойки, содержащие полипропиленовые контейнеры, из наружного пакета. Когда все будет готово, член бригады за пределами стерильного поля, но рядом со стерильным подготовительным столом, откроет каждый контейнер и удалит крышку, по одному контейнеру за раз. Затем каждый открытый контейнер должен удерживается членом бригады за пределами стерильного поля путем протягивания его/ее руки над стерильным полем, не касаясь стерильного поля.
[00338] Член бригады в стерильном поле использует пинцет для изъятия отдельного среза ткани вместе с его фильтровальной бумагой из контейнера и помещения его в стерильную чашку для тканевых культур, содержащую приблизительно 2 мл физиологического раствора без консервантов, на стерильном столе для подготовки. Четыре среза ткани с кусочками фильтровальной бумаги, взятые из четырех контейнеров, помещают в одну стерильную чашку для тканевых культур, которая находится на стерильном поле перед членом бригады в стерильном поле. Используя стерильный пинцет, член бригады в стерильном поле затем отделяет срез ткани от фильтровальной бумаги, используя два пинцета, один из которых удерживает фильтр на месте, в то время как другой тянет ткань или соскабливает ткань в стопку. Ткань, удаленную с каждой фильтровальной бумаги, помещают на эту фильтровальную бумагу в стопку в середину фильтровальной бумаги. Затем стерильную чашку для тканевых культур переносят в стерильное поле. Следующий набор из четырех контейнеров с продуктом, полученным из аллогенной культивированной ткани постнатального тимуса, затем обрабатывают таким же образом, пока хирург имплантирует первые 4 среза. Когда хирург заканчивает имплантацию первых четырех срезов, следующую чашку с 4 кусочками ткани помещают в хирургическое поле, а исходную чашку для тканевых культур возвращают в стерильное поле перед членом стерильной бригады в стерильном поле для загрузки третьего набора четырех срезов ткани. Этот цикл продолжают, пока все желаемые ткани не будут имплантированы. Все кусочки ткани не переносят в начале, чтобы избежать загрязнения воздуха в операционной.
Ход хирургической операции
[00339] Стадия 1. Открытие кожи.
[00340] После индукции общей анестезии сделайте вертикальный разрез кожи (обычно длиной ~5 см) над одним из передних отделов бедра. Примечание: размер разреза и использование одной или обеих ног для процедуры имплантации определяется размером пациента, запланированным количеством трансплантированной ткани и его/ее мышечной массой. Если вся или большая часть ткани может быть имплантирована в одну ногу, то следует использовать только одну ногу.
[00341] Стадия 2. Откройте фасцию, чтобы обнажить мышцы переднего отдела.
[00342] Стадия 3. Раздвигание мышц и имплантация.
[00343] Отделите мышцу с помощью тонзиллярного зажима или подобного инструмента вдоль естественных борозд четырехглавой мышцы. Отдельные кусочки продукта, полученного из аллогенной культивированной ткани постнатального тимуса, должны быть имплантированы без разрезания мышечной ткани. Поместите отдельные срезы ткани в «карманы» на расстоянии около 1 см друг от друга и на глубине около 1 см в четырехглавой мышце вдоль естественных борозд. В зависимости от размера пациента, хирург может поместить приблизительно 6-7 срезов в 6-7 карманов вдоль каждой борозды. Отдельные срезы продукта, полученного из аллогенной культивированной ткани постнатального тимуса, могут быть разрезаны пополам перед имплантацией в зависимости от массы ткани на каждом фильтре. Толстый срез ткани, который полностью покрыл фильтровальную бумагу, следует разрезать пополам для оптимальной васкуляризации каждой ткани. Необходимо имплантировать столько ткани в каждом переднем отделе, сколько требуется для максимальной запланированной дозы.
[00344] Стадия 4. Закрытие мышц.
[00345] Необходимо закрыть мышцу одним швом над участком, где была имплантирована ткань тимуса, чтобы предотвратить повторное открытие мышц и выход трансплантата из мышц. Необходимо убедиться, что имплантированная ткань полностью покрыта мышечной тканью без обнаженной ткани тимуса до закрытия разреза.
[00346] Стадия 5. Необходимо повторить стадии 3-4 для каждого среза продукта, полученного из аллогенной культивированной ткани постнатального тимуса, до максимальной предполагаемой дозы.
[00347] Стадия 6. Закрытие разреза.
[00348] Необходимо подтвердить гемостаз. Закрыть разрез кожи двумя слоями рассасывающихся швов и нанести стандартную повязку, такую как полоски для закрытия ран или клей для склеивания кожи. Необходимо оставить фасцию открытой, чтобы оставить место для отека мышечной лакуны. Для предотвращения загрязнения может быть использована герметичная повязка.
Послеоперационное хирургическое/медицинское лечение.
[00349] При необходимости необходимо использовать мягкие анальгетики. Необходимо осуществлять контроль признаков инфекции или расхождения швов.
[00350] Если донор является живым родственным донором, например, в случае легкого, почки, кишечника или частичной трансплантации печени, часть тимуса этого донора цельного органа может быть достаточной для культивирования и имплантации. Критерии патологии, перечисленные выше для дня сбора и для 5-9 дней, должны быть выполнены.
[00351] Криоконсервированная культивированная ткань тимуса может быть получена от третьего донора. Однако третий донор должен экспрессировать все аллели HLA реципиента, которые не экспрессируются донором цельного органа. Они включают HLA- A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DQA1, HLA-DPB1, HLA-DPA1. Несовпадение аллелей HLA-DP допустимо, если несоответствие является «допустимым». В других аллелях допускается незначительное несовпадение, например, HLA-A*01:02 реципиенту, несущему HLA-A*01:01, другими словами, второе поле (после двоеточия) может отличаться, первое поле (до двоеточия) должно быть идентичным.
Процедуры трансплантации человеческого сердца
[00352] Приемлемость субъекта определяют на основе ряда критериев, в том числе: плохой прогноз от 12 до 24 месяцев без трансплантации сердца, несмотря на максимальную поддерживающую терапию, осуществляемую в настоящее время; врожденное или приобретенное заболевание сердца с отставанием в развитии в соответствии с критериями UNOS; симптомы прогрессирующей сердечной недостаточности на фоне врожденного или приобретенного заболевания сердца, резистентного к медикаментозной терапии; аномальная гемодинамика или увеличение легочного сосудистого сопротивления; неоперабельное структурное заболевание сердца; симптомные аритмии, не поддающиеся медикаментозному лечению или аппаратной терапии, или плохая переносимость физических нагрузок.
[00353] Оценивают ряд абсолютных и относительных противопоказаний к операции по трансплантации сердца, включая, например, обратимую почечную дисфункцию, если субъект не является кандидатом на трансплантацию сердца/почки; необратимое заболевание печени, если субъект не является кандидатом на трансплантацию сердца/печени; необратимую легочную дисфункцию, использование нетрадиционной механической поддержки аппаратом искусственной вентиляции легких (например, аппарата высокочастотной ИВЛ, максимальные значения CMV (управляемой механической вентиляции легких)) или фиксированную легочную гипертензию (TPG (транспульмональный градиент давления)>15), если субъект не является кандидатом на трансплантацию сердечно-легочного комплекса; сахарный диабет при микрососудистых заболеваниях; или активная, неконтролируемая эпилепсия.
[00354] Другие противопоказания могут включать другие заболевания, ограничивающие долгосрочное выживание и реабилитацию после трансплантации сердца; наркотическую зависимость, морбидное ожирение, злокачественные новообразования; активное психическое расстройство; и другие причины, такие как документально подтвержденное медицинское несоответствие.
[00355] Относительные противопоказания включают активные инфекции; когнитивную дисфункцию; неадекватный сосудистый доступ и значительную аллогенную сенсибилизацию.
[00356] Также учитывается контроль гистосовместимости донора и реципиента. Пациентов оценивают на наличие панель-реактивных антител («PRA») на предварительно выработанные HLA-антитела, которые реципиент мог выработать в ответ на «сенсибилизирующее событие», такое как предшествующее переливание крови или обширные хирургические вмешательства с использованием шунтирования/препаратов крови или гомотрансплантатных материалов.
[00357] Проводят оценку истории предварительной сенсибилизации реципиента, например, предыдущих переливаний крови; число, даты; предыдущих хирургических вмешательств; предыдущих беременностей; истории иммунизации и введения ВВИГ (внутривенного иммуноглобулина) (с датами).
[00358] Пациенты с чрезмерно высоким уровнем PRA на HLA I класса или II класса или пациенты, подвергающиеся повторной трансплантации, могут быть кандидатами на стратегии десенсибилизации. Конкретные стратегии будут индивидуализированы для потенциального реципиента и могут включать использование плазмафереза, ВВИГ, ритуксимаба и/или бортезомиба. Существенными антителами являются те, которые остаются после разведения 1:16.
[00359] Предварительно сенсибилизированные пациенты могут потребовать фактической перекрестной пробы на совместимость с потенциальными донорами. Пациенты с наличием HLA-антител в анамнезе будут подвергаться виртуальной перекрестной пробе на совместимость в UNET во время рассмотрения возможности трансплантации.
[00360] Предварительно сенсибилизированные пациенты могут потребовать фактической перекрестной пробы на совместимость с потенциальными донорами на основании следующих общих рекомендаций. Все пациенты с наличием HLA-антител в анамнезе будут подвергаться виртуальной перекрестной пробе на совместимость в UNET во время рассмотрения предложения.
[00361] Если cPRA<20%: виртуальная перекрестная проба на совместимость в UNET, никаких дополнительных мер не требуется; продолжают стандартную ретроспективную перекрестную пробу на совместимость донора и стандартную иммуносупрессию.
[00362] Если cPRA>20%: виртуальная перекрестная проба на совместимость в UNET, реципиент получает плазмаферез в операционной («ОП») во время трансплантации.
[00363] Если cPRA>70%: виртуальная перекрестная проба на совместимость, рассмотрение возможности фактического проведения перекрестной пробы на совместимость потенциального донора, если позволяет время; осуществление плазмафереза в ОП. Рассмотрение возможности размещения катетера для плазмафереза в ОП для продолжения плазмафереза после операции.
[00364] Текущие вмешательства по снижению уровня антител определяются перекрестной совместимостью донора, DSA и клиническим течением заболевания.
[00365] Для всех предварительно сенсибилизированных пациентов кровь будет отправлена для проверки на донор-специфические антитела в течение первых двух недель после трансплантации, и эта процедура повторена в соответствии с клиническими показаниями. Регулярное тестирование на DSA будет проводиться у всех пациентов после трансплантации по меньшей мере каждые 6 месяцев после трансплантации и при необходимости, если возникнут какие-либо опасения, связанные с течением заболевания.
[00366] Как до, так и после трансплантации следуют стандартным протоколам переливания крови.
Осуществление иммуносупрессии
[00367] Осуществляемая иммуносупрессия зависит от подлежащего трансплантации цельного органа.
Трансплантация сердца ребенка
[00368] Все пациенты будут получать индукционную терапию базиликсимабом или
антитимоцитарным глобулином в зависимости от их клинической ситуации и факторов риска. Тип используемой индукционной терапии будет определен до трансплантации (медикаментозная терапия первого режима иммуносупрессии).
[00369] В одном варианте осуществления предшествующая трансплантации/индукционная терапия обычно включает введение:
[00370] Мофетила микофенолата (CellCept®), 25 мг/кг в/в перед операционной.
[00371] Метилпреднизолона, 10 мг/кг в/в при индукции (максимальная доза 500 мг).
[00372] Метилпреднизолона, 10 мг/кг в/в при прекращении пережатия аорты (максимальная доза 500 мг).
[00373] АТГ (антитимоцитарного глобулина), 1,5 мг/кг в/в при прекращении пережатия аорты.
[00374] В качестве альтернативы может быть использован базиликсимаб (Simulect®), дозированный в зависимости от массы тела реципиента.
[00375] <35 кг, 10 мг при прекращении пережатия аорты и 2-я доза через 4 дня.
[00376] >35 кг, 20 мг при прекращении пережатия аорты и 2-я доза через 4 дня.
[00377] В одном варианте осуществления иммуносупрессивная терапия перед трансплантацией для кандидатов на трансплантацию сердца и КТТ может включать:
[00378] Базиликсимаб (Simulect®) - (если нет возможности назначить АТГ).
[00379] Дозировка:
[00380] <35 кг: Начальная доза: 10 мг в/в вводят перед операцией путем анестезии при индукции анестезии (после стабилизации состояния и введения метилпреднизолона).
[00381] Вторая доза: 10 мг в/в вводят через 4 дня после трансплантации; вторую дозу удерживают при возникновении осложнений (включая тяжелые реакции гиперчувствительности или потерю трансплантата)
[00382] >35 кг: Начальная доза: 20 мг в/в вводят перед операцией путем анестезии при индукции анестезии, при достижении стабильного состояния.
[00383] Вторая доза: 20 мг в/в вводят через 4 дня после трансплантации; вторую дозу удерживают при возникновении осложнений (включая тяжелые реакции гиперчувствительности или потерю трансплантата).
[00384] Введение: В/в инфузия в течение 20-30 минут.Период полувыведения у детей 1-11 лет: 9,5 дней, подростков 12-16 лет: 9,1 дня, взрослых: 7,2 дня.
[00385] В одном варианте осуществления антитимоцитарный глобулин (АТГ, кроличьего происхождения, Thymoglobulin®) может быть введен в соответствии со следующей схемой дозирования для субъектов, перенесших трансплантацию сердца:
[00386] 1,5 мг/кг/сут в течение 3-7 дней в зависимости количества лимфоцитов, маркеров и количества тромбоцитов. Первую дозу вводят после реперфузии органа при прекращении пережатия аорты (во время операции).
[00387] Продолжают ежедневное введение на основе вышеуказанных параметров, согласно решению врача, ответственного за трансплантацию.
[00388] Введение: Медленная в/в инфузия в течение 6 часов для первой дозы, последующие дозы могут быть введены в течение 4 часов, в зависимости от переносимости.
[00389] В одном варианте осуществления помимо обычного предоперационного/внутриоперационного введения метилпреднизолона для случаев проведения операции в условиях искусственного кровообращения пациенты могут получить дозу метилпреднизолона (SoluMedrol) 10 мг/кг (максимальная доза 500 мг) в/в посредством анестезии при индукции анестезии перед базиликсимабом, а затем вторую дозу 10 мг/кг (максимум 500 мг) при реперфузии (до АТГ).
Послеоперационная поддерживающая иммуносупрессия (поддерживающий иммуносупрессивный режим)
[00390] В одном варианте осуществления иммуносупрессия после трансплантации
включает:
[00391] АТГ (Thymoglobulin®) 1,5 мг/кг в/в ежедневно, в общей сложности 5-7 доз.
[00392] Удерживать при WBC<2000 или количестве тромбоцитов <50 000.
[00393] 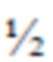 дозы, при WBC, равном 2000-3000, или количестве тромбоцитов, равном 50 000-75 000.
дозы, при WBC, равном 2000-3000, или количестве тромбоцитов, равном 50 000-75 000.
[00394] Микофенолат 15-25 мг/кг в/в или п/о каждые 12 часов.
[00395] Скорректировать при непереносимости со стороны желудочно-кишечного тракта или лейкопении/нейтропении.
[00396] Может заменить азатиоприн при непереносимости со стороны желудочно-кишечного тракта.
[00397] Может заменить микофеноловую кислоту (Myfortic®) при непереносимости со стороны желудочно-кишечного тракта.
[00398] Такролимус следует начинать через 24-48 часов после трансплантации, в зависимости от функции почек и переносимости при пероральном введении.
[00399] Начальная доза составляет ~ 0,05 мг п/о каждые 12 часов и корректируется в зависимости от уровней.
[00400] ~10-15 в течение первых 6 месяцев, 8-12 в течение 6 мес-3 лет, 4-8 в течение >3 лет.
[00401] Может заменить циклоспорин, если требуется в/в лечение или в случае непереносимости такролимуса.
[00402] Метилпреднизолон 5 мг/кг в/в каждые 8 часов x 6 доз (максимальная доза 125 мг).
[00403] Затем 1 мг/кг/доза в/в или п/о каждые 12 часов (максимум 30 мг/доза).
[00404] В течение следующих 2-3 месяцев дозу введение постепенно прекращают на основании результатов биопсии.
[00405] В одном варианте осуществления может быть введен такролимус (FK506, Prograf®). Обычные лекарственные формы включают внутривенные растворы по 0,5 мг/мл и пероральные капсулы по 0,5 мг, 1 мг и 5 мг на капсулу.
[00406] Начальную дозу ~0,05 мг/кг/доза дают каждые 12 часов (максимум 5 мг/доза), когда реципиент получает препарат перорально/через назогастральный зонд/под язык, обычно начиная через ~24 часа после операции, если функция почек приемлема.
[00407] Остаточные уровни такролимуса контролируют ежедневно до достижения терапевтической дозировки. При необходимости частоту введения увеличивают до одного раза в 8 часов, чтобы достичь необходимых остаточных терапевтических уровней. Если лекарственный препарат вводят сублингвально, содержимое капсулы разбрызгивается под языком (может привести к повышению уровней). Пероральные и сублингвальные дозы отсутствуют.Как правило, для сублингвального введения необходимо ввести ~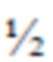 дозы для перорального приема.
дозы для перорального приема.
[00408] Дозирование такролимуса может проводиться на основании уровней в сыворотке цельной крови, измеренных методом масс-спектрометрии, через 10-14 часов (7-9 часов при введении дозы каждые 8 часов) после последней дозы.
[00409] При контроле уровней такролимуса, назначаемых пациенту, учитывают функцию почек и печени, нежелательные реакции, историю инфекции и отторжения. Корректировки дозы не требуются, если уровни составляют +/-1 в пределах желаемого диапазона, если пациент клинически чувствует себя хорошо. В этих случаях решение остается за лечащим врачом, ответственным за трансплантацию.
[00410] В одном варианте осуществления циклоспорин вводят пациентам, неспособным переносить такролимус. Начальная доза: 2 мг/кг/доза внутрь каждые 12 часов. При невозможности достичь терапевтических уровней (особенно у грудных детей и детей младшего возраста) частоту дозирования увеличивают до одного раза в 8 часов.
[00411] В целом дозирование основано на следующих уровнях в сыворотке цельной крови, измеренных методом масс-спектрометрии, через 10-14 часов (7-9 часов при введении дозы каждые 8 часов) после последней дозы.
[00412] При контроле уровней циклоспорина, назначаемых пациенту, учитывают функцию почек и печени, нежелательные реакции, историю инфекции и отторжения. Корректировки дозы не требуются, если уровни составляют +/-10-20 в пределах желаемого диапазона, если пациент клинически чувствует себя хорошо. В этих случаях решение остается за врачом, ответственным за трансплантацию. Необходимо приложить все усилия для документирования целевого уровня циклоспорина для пациента в медицинской карте. В/в доза обычно равна 1/3 пероральной дозы.
[00413] В одном варианте осуществления может быть введен мофетила микофенолат (Cellcept®) (200 мг/мл, 250 мг или 500 мг в виде таблеток):
[00414] Начинают с 30-50 мг/кг/сут в двух дробных дозах (максимальная доза для детей 2 г/сут, для взрослых 3 г/сут).
[00415] В/в доза=п/о доза.
[00416] Терапевтический лекарственный мониторинг не требуется, но может быть проведен в случае наличия опасений относительно токсичности.
[00417] Микофенолат может вызывать подавление функции костного мозга и нейтропению.
[00418] Доза может удерживаться при ANC<500 или WBC<1000; может потребоваться уменьшить дозу при снижении ANC (<1000) или WBC (<3000). На практике дозы 500 мг Cellcept=360 мг Myfortic (микофенолат).
[00419] В одном варианте осуществления вместо мофетила микофенолата может быть введен микофенолат (лекарственные формы Myfortic®, таблетка 180 мг, таблетка 360 мг) в соответствии со следующими параметрами дозировки:
[00420] Начинают введение таблетки с отсроченным высвобождением: 400 мг/м2/доза два раза в сутки; максимальная доза: 720 мг в ОП ППТ 1,19-1,58 м2: 540 мг два раза в сутки, ППТ>1,58 м2: 720 мг два раза в сутки.
[00421] Форма для в/в введения или суспензия недоступны. Если требуется в/в введение или суспензия, то лекарственный препарат заменяют на Cellcept. (500 мг Cellcept=360 мг Myfortic). Микофенолат может вызывать подавление функции костного мозга аналогично мофетила микофенолату.
[00422] В одном варианте осуществления при непереносимости мофетила микофенолата может быть введен азатиоприн следующим образом:
[00423] Начинают с 2-4 мг/кг/сут, один раз в сутки
[00424] Азатиоприн вызывает подавление функции костного мозга, и, возможно, потребуется снизить дозу в зависимости от WBC/ANC. В/в доза равна пероральной дозе.
[00425] В одном варианте осуществления может быть введен стероид в виде метилпреднизолона (Solu-Medrol®), преднизона или преднизолона.
[00426] Внутривенные стероиды начинают вводить во время операции (в качестве индукционной иммуносупрессивной терапии) и продолжают после операции в дозе 5 мг/кг/доза (максимум 125 мг/доза) в/в каждые 8 часов × 6 доз.
[00427] После этого может быть начат пероральный прием стероидов в виде таблеток преднизона или суспензии преднизолона в дозе 3 мг/мл. Внутривенное введение метилпреднизолона продолжают, если реципиент трансплантата не переносит иммуносупрессивный режим при пероральном введении. Можно перейти на пероральную терапию, если реципиент может переносить пероральные лекарственные препараты. Примерные диапазоны дозировки стероидов составляют:
[00428] 0-10 кг, начиная с 2 мг/кг/сут, разделенные на два раза в сутки, постепенно снижая раз в 2 дня, удерживая на уровне 6 мг в день;
[00429] 0-30 кг, начиная с 2 мг/кг/сут, разделенных на два раза в сутки (максимальная разовая доза составляет 30 мг, см. ниже), постепенно снижая на 5 мг/сут каждые два дня, затем удерживая на уровне 10 мг в сутки;
[00430] >30 кг, 30 мг 2 раза в сутки x 4 дозы, 25 мг 2 раза в сутки x 4 дозы, 20 мг 2 раза в сутки x 4 дозы, 15 мг 2 раза в сутки x 4 дозы, 10 мг 2 раза в сутки x 4 дозы, затем начиная введение 15 мг в сутки с дальнейшим постепенным снижением кардиологом, ответственным за трансплантацию.
[00431] В течение первого месяца после трансплантации на основании результатов биопсии продолжают постепенно снижать дозу стероидов. Если развивается отторжение, то введение стероидов начинают заново по усмотрению кардиолога, ответственного за трансплантацию, и продолжают в течение неопределенного времени в зависимости от дальнейших результатов биопсии и клинического статуса пациента.
[00432] Другие лекарственные препараты во втором иммуносупрессивном режиме включают следующие:
[00433] Сиролимус (Rapamune®) (капсулы 0,5 мг, 1 мг, 2 мг): Начинают после постановки диагноза коронарной артериопатии аллотрансплантата или по иным клиническим показаниям, выявленным кардиологом, ответственным за трансплантацию.
[00434] Начальная доза: 1 мг/м2 (максимальная доза: 3 мг) раз в сутки или разделенная на 2 суточных дозы при сложности с достижением адекватного уровня.
[00435] Целевой терапевтический уровень составляет 4-8, в случае приема обоих лекарственных препаратов принимают более низкий уровень такролимуса (тот же диапазон 4-8).
[00436] Остаточный уровень, измеренный через 23-25 часов после последней дозы или через 11-13 часов после последней дозы при дозировке каждые 12 часов.
[00437] Введение микофенолата (Cellcept®, Myfortic®), азатиоприна прекращают в случае начала приема сиролимуса.
[00438] Начинают профилактику с помощью Bactrim: может вызвать причиняющие беспокойство язвы в полости рта и отсроченное заживление ран.
[00439] Правастатин (Pravachol®) - используется у подростков/детей старшего возраста и детей с CAV (коронарной артериопатией трансплантата)
[00440] Начинают введение с 0,2 мг/кг/сут раз в сутки (выпускается в форме таблеток, можно осуществлять введение  ,
,  или до 1-2 таблеток в сутки на ночь).
или до 1-2 таблеток в сутки на ночь).
[00441] Дозу корректируют при изменении массы тела (максимальная доза 20 мг/сут).
[00442] Функциональную пробу печени, CK (креатинкиназу) контролируют каждые 8 недель.
[00443] Введение лекарственного препарата прекращают при появлении болей в суставах или мышцах.
[00444] Ганцикловир в/в - предназначен для профилактики ЦМВ, если реципиент или донор является положительным на IgG к ЦМВ.
[00445] Индукционная терапия: 5 мг/кг в/в каждые 12 часов x 7-14 дней.
[00446] Поддерживающая терапия: 5 мг/кг в/в ежедневно.
[00447] WBC и функцию почек контролируют.
[00448] При переносимости переходят на пероральный валганцикловир.
[00449] Валганцикловир (Valcyte®) - для профилактики ЦМВ у всех реципиентов или доноров, положительных на ЦМВ.
[00450] Таблетки 450 мг или суспензия 50 мг/мл.
[00451] 4 месяца - 16 лет: общая суточная пероральная доза (мг)=[7 x ППТ x клиренс креатинина].
[00452] >16 лет: 900 мг перорально ежедневно.
[00453] Контролируют ЦМВ с помощью ПЦР при каждом посещении.
[00454] Триметоприм-сульфаметоксазол (Bactrim®, Septra®):
[00455] Таблетки одинарной дозировки 80 мг/400 мг, таблетка двойной дозировки 160 мг/800 мг, суспензия 40 мг/200 мг на 5 мл.
[00456] Начинают при одновременном приеме пищи внутрь, перед выпиской для предупреждения плазмоклеточной пневмонии/токсоплазмоза.
[00457] 1 мес - 12 лет: 5-10 мг/кг/сут TMP в дробных дозах дважды в сутки 3 раза в неделю в последовательные дни.
[00458] >12 лет: 80-160 мг TMP перорально ежедневно или 160 мг TMP перорально 3 раза в неделю.
[00459] Осуществляют контроль на предмет лекарственных препаратов, которые могут повышать или понижать уровни такролимуса и циклоспорина, как известно специалисту в данной области техники.
[00460] Также осуществляют контроль на предмет лекарственных препаратов, имеющих синергетическую нефротоксичность с такролимусом и циклоспорином.
Лечение острого отторжения трансплантата
[00461] В одном варианте осуществления субъект получает лечение следующим образом в случае, если имеет место отторжение трансплантата.
[00462] В одном варианте осуществления, если реципиент трансплантата имеет отторжение степени 0, 1R без гемодинамического нарушения: лечение не требуется, и можно рассмотреть возможность постепенного прекращения введения стероидов.
[00463] Если пациент демонстрирует клеточное отторжение степени 2R без гемодинамического нарушения, применяется следующий режим лечения:
[00464] Оптимизируют поддерживающую иммуносупрессию.
[00465] Вводят метилпреднизолон в дозе 15 мг/кг/сут в/в x 3 дня (максимум 1000 мг), возможно введение дробных доз каждые 12 часов или введение один раз каждые 24 часа.
[00466] Биопсию повторяют через 1-2 недели, в случае рефрактерного клеточного отторжения повторяют метилпреднизолон и, необязательно, Thymoglobulin®.
[00467] Если отторжение разрешилось, биопсию повторяют через 1 месяц (через 6 недель после отторжения) и возобновляют ранее определенный протокол биопсии, если отторжение было успешно вылечено.
[00468] В случае рефрактерного клеточного отторжения повторяют метилпреднизолон и рассмотривают возможность введения тимоглобулина.
[00469] Если у пациента присутствует клеточное отторжение степени 2R без гемодинамического нарушения или отторжение более высокой степени.
[00470] Оптимизируют иммуносупрессию на более высоких уровнях (10-15).
[00471] Вводят метилпреднизолон в дозе 15 мг/кг/сут в/в x 3 дня (максимум 1000 мг).
[00472] Вводят Thymoglobulin®.
[00473] Осуществляют плазмаферез, если есть свидетельства или беспокойство по поводу опосредованного антителами отторжения.
[00474] Если у пациента присутствует опосредованное антителами отторжение с гемодинамическим нарушением или без него:
[00475] Вводят метилпреднизолон в дозе 15 мг/кг/сут в/в x 3 дня (максимум 1000 мг).
[00476] Осуществляют плазмаферез x 5 циклов (ежедневно или через день).
[00477] Вводят ВВИГ в дозе 1-2 г/кг в/в ежемесячно х 6 месяцев.
[00478] Свидетельство дисфункции трансплантата или гемодинамического нарушения требует биопсии (когда состояние пациента стабилизируется) для проверки на клеточное отторжение и опосредованное антителами отторжения, включая окрашивание на C4d. Во время ожидания результатов биопсии начинают введение метилпреднизолона (SoluMedrol), рассматривают возможность введения тимоглобулина и плазмафереза.
[00479] Биопсии степени 3R или гемодинамическое нарушение лечат как эпизод отторжения высокой степени тяжести.
[00480] Вводят метилпреднизолон (SoluMedrol) в дозе 15 мг/кг/сут в/в x 3 дня (максимум 1000 мг). Рассматривают возможность инотропной терапии, тимоглобулина; и/или плазмафереза.
[00481] Опосредованное антителами отторжение с гемодинамическим нарушением или без него. Диагноз: идентификация отложения C4d в ткани миокарда с наличием донор- специфических антител в образце сыворотки периферической крови. Рассматривают возможность введения стероидов, АТГ, плазмафереза для лечения опосредованного антителами отторжения.
Осуществления иммуносупрессии почек и поджелудочной железы
[00482] Иллюстративные индукционные иммуносупрессивные режимы и поддерживающие иммуносупрессивные режимы для процедур трансплантации почки и поджелудочной железы представлены ниже. В одном варианте осуществления реципиенты трансплантата получают белатацепт в качестве поддерживающей терапии в качестве части второго иммуносупрессивного режима. Этот протокол обычно используют, когда реципиент является положительным на Ig к вирусу Эпштейна-Барр (EBV), не демонстрирует DSA (донор-специфических аллоантител); независимо от абсолютных или рассчитанных показателей панель-реактивных антител (PRA), трансплантат характеризуется отрицательным результатом перекрестной пробы на совместимость, и реципиент имеет возраст <70 лет с ИМТ≤35. Дополнительные соображения включают в себя способность реципиента переносить индукцию (если он иначе не получил бы тимоглобулин). У реципиента не должно быть идиопатического фокально-сегментарного гломерулосклероза (ФСГС) в анамнезе и предшествующей трансплантации отличного от почки цельного органа. Протокол применим только для трансплантации почки.
[00483] В одном варианте осуществления индукционный иммуносупрессивный режим включает введение 500 мг метилпреднизолона внутривенно во время операции. 30 мг алемтузумаба вводят путем внутривенной инфузии в течение трех часов (через 2 часа после введения стероидов). Вводят 10 мг/кг белатацепта (общая масса тела) (с округлением до ближайших 12,5 мг) после введения предшествующих лекарственных препаратов.
[00484] В одном варианте осуществления поддерживающий иммуносупрессивный режим включает 10 мг/кг TBW белатацепта на 4 день после операции и в конце 2, 4, 8 и 12 недели; затем 5 мг/кг каждый месяц (с округлением до ближайших 12,5 мг). Сиролимус вводят в дозе 2 мг в сутки, при этом первый остаточный уровень измеряют через 2 недели (цель составляет 8-10 нг/мл). Как правило, стероидная поддерживающая терапия не требуется.
[00485] В одном варианте осуществления для почечных трансплантатов с низким риском, где реципиент не является кандидатом на введение белатацепта, индукционный иммуносупрессивный режим может не включать индукционный иммуносупрессивный режим, т.е. индукционный иммуносупрессивный режим является необязательным. Поддерживающий иммуносупрессивный режим может включать 1000 мг микофеноловой кислоты, вводимые каждые 12 часов, и такролимус, вводимый в дозе 0,1 мг/кг/сут, максимум 5 мг каждые 12 часов.
[00486] В одном варианте осуществления, когда реципиент имеет высокий риск и ему противопоказан АТГ, ослаблен, имеет возраст >70 лет и имеет признаки недавней инфекции и недавних противораковых мероприятий, индукционный иммуносупрессивный препарат может включать 20 мг базаликсимаба для начала в операционной и на 4 день после операции (POD). Поддерживающий иммуносупрессивный режим может включать 1000 мг микофеноловой кислоты каждые 12 часов, и такролимус в дозе 0,1 мг/кг/сут, максимум 5 мг каждые 12 часов при снижающихся дозировках стероидов.
[00487] В одном варианте осуществления, включающем трансплантаты почек с высоким риском или трансплантаты почки и поджелудочной железы, рассматриваются следующие параметры. Реципиенты, имеющие историю пика PRA>30, историю донор-специфического антитела (DSA, независимо от абсолютного или рассчитанного PRA), 2-й трансплантат с ранней потерей трансплантата из-за предполагаемой иммунологической причины, 3-й или более трансплантат, педиатрические реципиенты двух почек (взрослые), почка/поджелудочная железа, только поджелудочная железа и при высоком риске DGF (отсроченной функции трансплантата) или высоком риске биопсии. При таком трансплантате индукционный иммуносупрессивный режим (индукционная терапия) может включать тимоглобулин 1,5 мг/кг IBW (с округлением до ближайших 25 мг) x 4 дозы, начинаемый в операционной.
[00488] В одном варианте осуществления, где реципиент имеет нулевой PRA, у него отсутствуют аутоиммунные заболевания и имеется высокий ИМТ, индукционный иммуносупрессивный режим может включать 1,5 мг/кг IBW тимоглобулина (с округлением до ближайших 25 мг) x 4 дозы, начинаемый в операционной. Второй иммуносупрессивный режим (поддерживающая терапия) может включать снижающиеся дозировки стероидов, например, 500 мг в ОП, 240 мг в 1 день после операции, 125 мг во 2 день после операции, 125 мг в 3 день после операции, 90 мг в 4 день после операции, с 1000 мг микофеноловой кислоты каждые 12 часов, начиная с 4 дня после операции, и 0,1 мг/кг/сут такролимуса, максимум 5 мг каждые 12 часов.
[00489] В одном варианте осуществления, где трансплантацию поджелудочной железы проводят после трансплантации почки, индукционный иммуносупрессивный режим может включать тимоглобулин 1,5 мг/кг IBW (с округлением до ближайших 25 мг) x 4 дозы, начинаемый в операционной. Второй иммуносупрессивный режим может включать снижение дозировки стероидов до минимума 5 мг в сутки, введение 1000 мг микофеноловой кислоты каждые 12 часов, начиная с 4 дня после операции, и введение 0,8 мг/кг/сут такролимуса, максимум 4 мг каждые 12 часов.
[00490] Для всех иммуносупрессивных режимов, включающих введение микофеноловой кислоты, начальная доза может быть выбрана на основе оценки факторов пациента и трансплантата.
Осуществление иммуносупрессии при трансплантации сердца взрослого
[00491] В одном варианте осуществления обычно вводят индукционные иммуносупрессивные режимы. Иногда могут быть сделаны исключения, когда считают, что риски индукционной терапии перевешивают преимущества такой терапии (т.е. индукционный иммуносупрессивный режим является необязательным).
[00492] В одном варианте осуществления, когда вводят индукционный иммуносупрессивный режим, режим может включать Simulect® (базиликсимаб): 20 мг в/в вводят в ОП после реперфузии (при прекращении пережатия аорты) и повторяют на 4 день после операции. У пациентов, получающих индукционную иммуносупрессивную терапию, ингибитор кальциневрина (CNI), вводимый в составе второго иммуносупрессивного режима, следует начинать через 48 часов после операции, но его введение может быть начато позже, в зависимости от состояния почек пациента. Стероиды могут быть введены в периоперационном периоде, обычно 500 мг метилпреднизолона внутривенно при индукции общей анестезии и 500 мг в/в перед реперфузией (при прекращении пережатия аорты).
[00493] В одном варианте осуществления поддерживающего иммуносупрессивного режима (послеоперационная поддерживающая иммуносупрессивная терапия) режим может включать стероиды, например, метилпреднизолон, 125 мг в/в, раз в 8 часов × 3 дозы (начиная через 8 часов после реперфузии), за которым следует преднизон: 0,5 мг/кг два раза в сутки, начиная со 2 дня после операции; дозу снижают на 5 мг два раза в сутки каждые 2 дня до 10 мг два раза в сутки (или 20 мг раз в сутки) и поддерживают эту дозу до 30 дней после трансплантации. Второй иммуносупрессивный режим может также включать ингибиторы кальциневрина (CNI), например, такролимус/FK506/Prograf® (предпочтительный препарат): 1 мг внутрь каждые 12 часов. Дозу корректируют до целевого остаточного уровня 10-15 нг/мл. Типичные корректировки дозы производят после 5 доз ингибитора кальциневрина для установления устойчивого состояния. Дневные уровни CNI первоначально отслеживают для оценки токсичности CNI.
[00494] В альтернативном варианте осуществления вводят циклоспорин/CyA/Neoral® в дозе 100 мг (от 1,5 до 5 мг/кг) внутрь каждые 12 часов. Дозу обычно корректируют до целевого остаточного уровня 33 нг/мл. Поддерживающий иммуносупрессивный режим может также включать антипролиферативный препарат, такой как мофетила микофенолат (Cellcept®), от 1000 до 1500 мг перорально, причем дозировку корректируют для поддержания количества лейкоцитов >3000. В качестве альтернативы, антипролиферативный препарат может представлять собой микофенолат (Myfortic®) в дозе 360 мг - 720 мг, вводимый перорально два раза в сутки, причем дозировку корректируют для поддержания количества лейкоцитов>3000. В еще одном варианте осуществления антипролиферативный препарат представляет собой азатиоприн (Imuran®), вводимый перорально в дозе 2 мг/кг в сутки, причем дозу корректируют для поддержания количества лейкоцитов >3000.
[00495] В одном варианте осуществления поддерживающий иммуносупрессивный режим может включать сиролимус (Rapammune®) (TOR-I), вводимый перорально в дозировке 2 мг в сутки. Дозировку обычно корректируют для поддержания остаточного уровня 4-12 мкг/мл.
[00496] В одном варианте осуществления поддерживающий иммуносупрессивный режим может включать снижающуюся дозировку стероидов, например, в 1 месяц дозу снижают до 15,0 мг п/о в сутки; во 2 месяц дозу снижают до 12,5 мг п/о в сутки; на 3 месяц дозу снижают до 10,0 мг п/о в сутки; на 4 месяц дозу снижают до 7,5 мг п/о в сутки; на 5 месяц дозу снижают до 5,0 мг п/о в сутки; на 6 месяц дозу снижают до 2,5 мг п/о в сутки. Снижение дозировки стероидов следует пересмотреть после ≥ степени 1R согласно ISHLT с признаками некроза миоцитов. Снижение дозировки может быть возобновлено после улучшения статуса отторжения по результатам гистологического исследования.
[00497] В одном варианте осуществления поддерживающий иммуносупрессивный режим может включать следующие дополнительные/вспомогательные препараты: метотрексат (MTX), вводимый в дозе от 2,5 до 5 мг два раза в неделю для клеточно-опосредованного отторжения. MTX следует рассматривать для 3 или более последовательных биопсий со степенью >=1R/2 степени или 2 последовательных биопсий со степенью 2R/3A.
Осуществление иммуносупрессии для печени и кишечника у взрослых
[00498] В одном варианте осуществления трансплантация печени без почечной дисфункции может быть выполнена без какого-либо индукционного иммуносупрессивного режима, т.е. такой индукционный иммуносупрессивный режим является необязательным. Поддерживающий иммуносупрессивный режим может включать введение 1 г микофенолата каждые 12 часов и 2-3 мг такролимуса каждые 12 часов вместе при снижающихся дозировках стероидов. Типичная снижающаяся дозировка стероидов представляет собой: 500 мг метилпреднизолона в/в во время операции; 250 мг метилпреднизолона в/в через 6 часов после операции, однократно; 180 мг метилпреднизолона в/в в 1 день после операции, однократно; 90 мг метилпреднизолона в/в во 2 день после операции, однократно; 60 мг метилпреднизолона в/в в 3 день после операции, однократно; 30 мг метилпреднизолона в/в в 4 день после операции, однократно; 20 мг в сутки преднизона п/о в 5-14 дни после операции; снижение на 2,5 мг каждые 2 недели. В одном варианте осуществления снижающаяся дозировка преднизолона может вводиться в виде 20 мг в сутки в течение первых 2 недель; 17,5 мг в сутки в течение 2-4 недели; 15 м в сутки в течение 4-6 недели, 12,5 мг в сутки в течение 6-8 недели; 10 мг в сутки в течение 8-10 недели; 7,5 мг в сутки в течение 10-12 недели; 5 мг в сутки в течение 12-14 недели; 2,5 мг в сутки в течение 14-16 недели. Прекращают на 16 неделе. При определенных обстоятельствах дозу преднизолона постепенно снижают до 5 мг в сутки и удерживают в течение одного года.
[00499] В одном варианте осуществления проводят щадящую для почек трансплантация печени, когда имеет место предоперационная дисфункция, требующая HD или CVVHD/F. В еще одном варианте осуществления проводят щадящую для почек трансплантация печени, когда имеет место послеоперационная почечная дисфункция с уровнями креатинина в сыворотке >2 мг/дл в 0-1 дни после операции.
[00500] В одном варианте осуществления индукционный иммуносупрессивный режим включает 1,5 мг/кг тимоглобулина (с округлением до ближайших 25 мг) каждые 48 часов в течение 4 доз. В одном варианте осуществления дозировку снижают при панцитопении или нейтропении. При количестве лейкоцитов 2-3 или тромбоцитов 30-50 дают  дозы. При WBC<2 или количестве тромбоцитов <30 дозировку удерживают.
дозы. При WBC<2 или количестве тромбоцитов <30 дозировку удерживают.
[00501] В одном варианте осуществления, когда показана премедикация, премедикация может быть введена за 30-60 минут до инфузии АТГ, 650 мг ацетаминофен в/в или перорально, дифенгидрамин 25-50 мг; и метилпреднизолон 40 мг в/в (или можно использовать снижающуюся дозировку, описанную выше).
[00502] В одном варианте осуществления трансплантат представляет собой трансплантат кишечника или трансплантат нескольких внутренних органов, такой как трансплантат печени, кишечника, поджелудочной железы, где реципиент подвергнут высокому иммунологическому риску (PRA>0, имеет предшествующую беременность или трансплантацию изолированного кишечника, или где имеет место низкий иммунологический риск при высоком риске заражения, индукционный иммуносупрессивный режим может включать премедикацию, как описано выше, и также может включать 1,5 мг/кг тимоглобулина (с округлением до ближайших 25 мг) каждые 24 часа в общей сложности до 6 мг/кг и 20 мг базиликсимаба в 0 и 4 дни после операции. Поддерживающий иммуносупрессивный режим может включать снижающуюся дозировку стероидов, как описано выше, и 1 г микофенолата каждые 12 часов и 1 мг такролимуса сублингвально каждые 12 часов (цель 12-16 мг/мл).
[00503] В отдельных вариантах осуществления такролимус вводят в дозировке для достижения целевых уровней 5-8 (печень) или 12-17 (кишечник, печень-кишечник), когда пациент принимает мофетила микофенолат (Cellcept). Цель может быть изменена, если пациент участвует в исследовании лекарственного препарата, имеет отторжение, нарушение функции почек или имеет пожилой возраст.
[00504] В отдельных вариантах осуществления, где вводят мофетила микофенолат (MMF, Cellcept), стандартная дозировка для взрослых составляет 1000 мг каждые 12 часов. Уменьшение дозировки может быть сделано у пациентов с панцитопенией или нейтропенией в соответствии со следующим: WBC 2-3 или тромбоциты 30-50: рассматривают возможность введения  дозы; для WBC<2 или тромбоцитов <30; рассматривают возможность удерживания дозы.
дозы; для WBC<2 или тромбоцитов <30; рассматривают возможность удерживания дозы.
[00505] В отдельных вариантах осуществления, включающих лечение острого отторжения аллотрансплантата печени, может быть назначено следующее лечение: метилпреднизолон 500 мг в/в в сутки в течение 3 доз. Если функциональные пробы печени не улучшаются, могут быть назначены две дополнительные дозы (всего 5 доз по 500 мг в/в в сутки) с повторной биопсией печени, проводимой накануне 3 дня после операции или утром 4 дня после операции.
[00506] В отдельных вариантах осуществления пациенты, получавшие SoluMedrol® или Thymoglobulin®, чей результат на IgG к ЦМВ ранее был отрицательным, должны быть повторно проверены на IgG к ЦМВ в начале лечения.
Осуществлени иммуносупрессии при трансплантации легкого
[00507] В отдельных вариантах осуществления иммуносупрессию при трансплантации легкого осуществляют со следующими индукционным и поддерживающим иммуносупрессивным режимами. Индукционные иммуносупрессивные режимы могут следовать за индукционным иммуносупрессивным режимом, описанным ранее. Поддерживающие иммуносупрессивные режимы могут включать следующее:
[00508] Ингибиторы кальциневрина: такролимус каждые 12 часов с дозировкой, скорректированной для поддержания остаточных уровней такролимуса. См. таблицу 5 ниже.
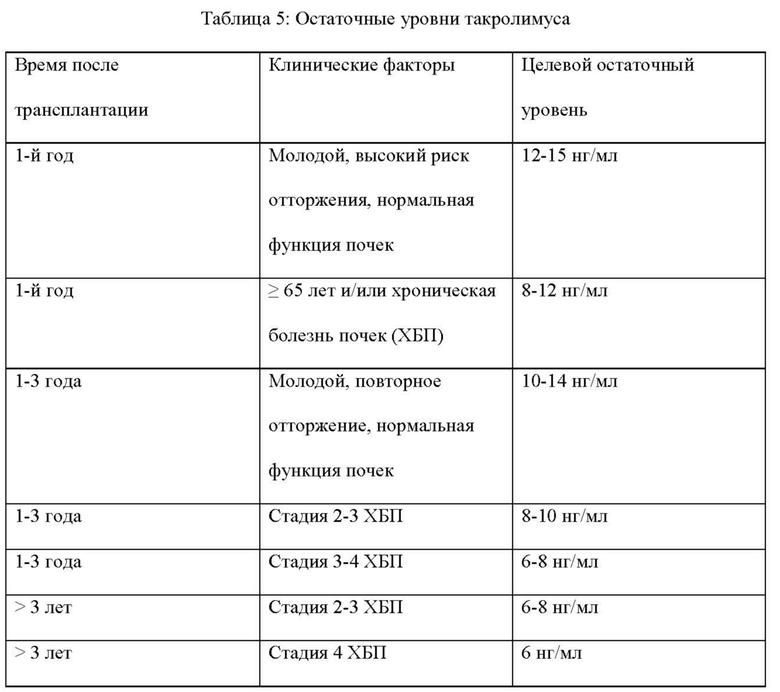

[00509] Циклоспорин вводят каждые 12 часов с дозировкой, скорректированной для поддержания остаточных уровней CyA в соответствии с таблицей 6 ниже.
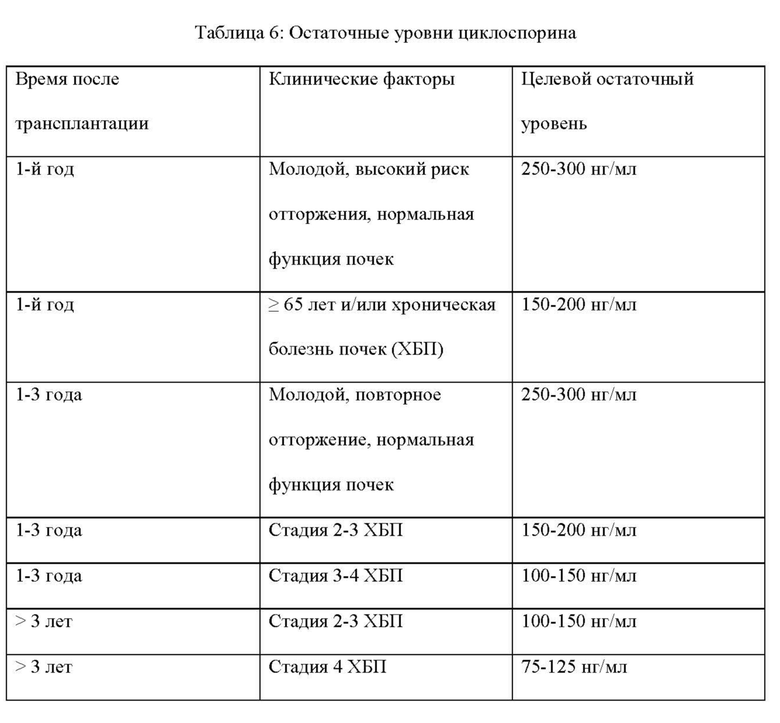

[00510] Снижающаяся дозировка стероидов в течение 0-3 месяцев после трансплантации, 20 мг перорально в сутки; через 3-6 месяцев после трансплантации по 15 мг перорально в сутки; через 6-9 месяцев после трансплантации по 10 мг перорально в сутки; и через более чем 9 месяцев после трансплантации по 5 мг перорально в сутки.
[00511] Может быть введен азатиоприн перорально в дозе 2 мг/кг в сутки. Важно обеспечить нормальные уровни фермента TMPT до начала и следовать результатам функциональных проб печени/общего анализа крови. В случае лейкопении могут быть рассмотрены корректировки дозировки.
[00512] Мофетила микофенолат (Cellcept®) может быть введен в обычной дозе 1000 мг два раза в сутки. Обычная доза для трансплантации сердца и легкого составляет 1500 мг в сутки, перорально. Следует принимать во внимание результаты общего анализа крови и корректировать дозировку в случае лейкопении.
[00513] Сиролимус, как правило, противопоказан в первые 3 месяца после трансплантации из-за проблем с расхождением анастомотических швов. При введении сиролимус обычно вводят по 1 мг в сутки перорально, корректируя эту дозировку на основе остаточных уровней. Например, при введении в качестве третьего препарата или для снижения количества CNI целевой остаточный уровень составляет 4-8 нг/мл; а в качестве альтернативы для CNI остаточный уровень составляет 10-15 нг/мл.
Примеры
[00514] Пример 1: Исследование вариабельности внутри тимуса.
[00515] Была изучена вариабельность внутри тимуса, чтобы определить, можно ли считать результаты гистологического исследования одной части тимуса репрезентативными для результатов гистологического исследования в любой другой части того же тимуса. Результаты этого теста использовали, чтобы определить, сколько образцов должно быть протестировано как во время стандартного тестирования при выпуске, так и для тестирования при валидации процесса.
[00516] Как отмечалось ранее, были установлены гистологические критерии приемлемости, включая оценку: областей, положительных на кератин AE1/AE3, рассредоточенных по всей ткани на 5-9 день; идентификацию по крайней мере 1 тельца Гассаля; окрашивание на CK14, рассредоточенное по всей ткани; и наличие интактных ядер.
[00517] Для этого исследования три тимуса нарезали на срезы направленным образом и отслеживали местоположение срезов в каждом тимусе. Срезы культивировали в 6-луночных планшетах, чтобы обеспечить возможность отслеживания каждого среза. Нарезание на срезы проводили, как показано на фиг. 5A.
[00518] Для каждого тимуса в исследовании срезы были предназначены для анализа в каждый из следующих моментов времени: базовый уровень (0 день), 5 день, 9 день, 12 день и 21 день.
[00519] От 5 до 11 срезов культивировали в каждый момент времени для каждого тимуса. Срезы культивировали в соответствии с методами, описанными выше, с ежедневными сменами среды. Срезы были направлены для окрашивания H&E в лабораторию патологической анатомии и проанализированы на принадлежность, активность и жизнеспособность. Все срезы в этом исследовании соответствовали критериям приемлемости при выпуске для гистологического исследования, как указано выше, а именно: области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани на 5-9 день; идентифицировано по меньшей мере 1 тельце Гассаля; окрашивание на CK14 рассредоточено по всей ткани; и наблюдаются интактные ядра.
[00520] В дополнение к оценке того, соответствует ли каждый срез критериям приемлемости при выпуске, гистологом был проведен более подробный анализ каждого среза с окрашиванием H&E и AE1/AE3. Изображения некоторых из этих предметных стекол для партии культивированной ткани тимуса MFG-056 показаны на фиг. 6A-Н. Были сделаны следующие наблюдения.
[00521] Все срезы, полученные из одного и того же донорского тимуса, соответствовали критериям приемлемости в каждый момент времени. В разных срезах корковые области похожи друг на друга, и медуллярные области похожи друг на друга. Однако наблюдались различия в относительной пропорции корковой и медуллярной областей между срезами.
[00522] Различия, наблюдаемые между различными срезами, полученными из одного и того же тимуса, в зависимости от времени культивирования, были в основном связаны с количеством некроза, главным образом тимоцитов (который увеличивался с увеличением времени культивирования) и количеством остаточных тимоцитов (которое уменьшалось с увеличением времени культивирования).
[00523] На основании этих наблюдений любой срез из тимуса являлся репрезентативным для всего тимуса. Кроме того, гистологическая картина срезов ткани на 5 день отражает наблюдения в каждый из более поздних моментов времени (9, 12 и 21 день).
[00524] Пример 2: Исследование временной динамики целого тимуса.
[00525] Для этого исследования на одну SOP (стандартную рабочую процедуру) пять тимусов были нарезаны на срезы и культивированы. В день нарезания первый, средний и последний срезы подготавливали для иммуногистохимического исследования. Оставшуюся часть каждого тимуса нарезали на срезы и культивировали в 6-луночных планшетах. Каждый тимус был предназначен для одного из следующих моментов времени: базовый уровень (0 день), 5 день, 9 день, 12 день и 21 день. См. фиг. 7, где показан срез тимуса в 0 день, фиг.8, где показан срез на 5 день, фиг.9, где показан срез на 12 день, и фиг.10, где показан срез на 21 день.
[00526] Общее количество срезов от каждого тимуса составляло от 21 до 62 срезов. Срезы культивировали в соответствии с методами, описанными выше, с ежедневными сменами среды. Срезы были направлены для окрашивания H&E в лабораторию патологической анатомии и проанализированы на принадлежность, активность и жизнеспособность. Все срезы в этом исследовании соответствовали критериям приемлемости при выпуске для гистологического исследования, а именно: области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани на 5-9 день; идентифицировано по меньшей мере 1 тельце Гассаля; окрашивание на CK14 рассредоточено по всей ткани; и наблюдаются интактные ядра.
[00527] В дополнение к оценке того, соответствует ли каждый срез критериям приемлемости при выпуске, гистологом был проведен более подробный анализ каждого среза с окрашиванием H&E и AE1/AE3. Были сделаны следующие наблюдения.
[00528] Все срезы, полученные из одного и того же донорского тимуса и протестированные в один и тот же момент времени, аналогичным образом соответствовали критериям приемлемости для этого момента времени с вариациями относительных количеств корковой и медуллярной области, остаточных тимоцитов и/или некроза, как описано выше.
[00529] Отмеченные различия заключались в относительном размере, форме, относительном содержании корковой и медуллярной областей тимуса, степени некроза, конденсации эпителия тимуса и количестве остаточных тимоцитов.
[00530] Кроме того, партии от разных доноров, протестированные в разные моменты времени, также были качественно схожи друг с другом. Наблюдаемые различия были связаны с количеством некроза (который увеличивался с увеличением времени культивирования) и количеством остаточных тимоцитов (которое уменьшалось с увеличением времени культивирования).
[00531] Гистологическое исследование любого среза привело к аналогичному заключению о приемлемости всей партии. На основании этих наблюдений относительные характеристики любого среза из тимуса отражают таковые для всего тимуса. Кроме того, гистологическая картина срезов ткани на 5 день отражает наблюдения в каждый из более поздних моментов времени (9, 12 и 21 день), хотя в более поздние моменты времени наблюдается больший некроз. Фиг. 11 представляет собой хороший пример, демонстрирующей сходство эпителиальной сети, оцененное с помощью антитела AE1/AE3 с 0 дня по 21 день.
[00532] Пример 3: Исследование принудительной деградации ткани тимуса.
[00533] В этом исследовании срезы ткани тимуса обрабатывали с целью получения срезов ткани, которые считались деградировавшими или нежизнеспособными. Для этих экспериментов использовали три тимуса. Из каждого тимуса были взяты контрольные образцы. Были протестированы условия обработки, приведенные в таблице 7.

[00534] Тепловой шок осуществляли, помещая 10-сантиметровую культуральную чашку, содержащую срезы, в пакет со струнным замком и помещая на водяную баню при температуре 55°C. Подставка стояла на опоре и не была погружена. Замораживание/размораживание осуществляли, помещая 10-сантиметровую культуральную чашку в морозильную камеру при -20°C на 4 часа с последующим размораживанием при температуре окружающей среды.
[00535] Образцы тестировали в гистологическом исследования на 5 и 9 дни в культуре. Некоторые образцы также тестировали на 21 день. Все срезы в этом исследовании соответствовали критериям приемлемости при выпуске для гистологического исследования, а именно: области, положительные на кератин AE1/AE3, рассредоточенные по всей ткани на 5-9 день; идентифицировано по меньшей мере 1 тельце Гассаля; окрашивание на CK14 рассредоточено по всей ткани; и наблюдаются интактные ядра.
[00536] В дополнение к оценке того, соответствует ли каждый срез критериям приемлемости при выпуске, гистологом был проведен более подробный анализ каждого среза. Были сделаны следующие наблюдения.
[00537] Образцы, подвергнутые замораживанию/размораживанию или 10-кратной концентрации PBS, показали наибольшую степень некроза, но некоторые клетки все еще оставались неповрежденными и соответствовали гистологическим критериям жизнеспособности. См. фиг. 12, где приведен пример воздействия 10-кратной концентрации PBS.
[00538] Срезы, которые хранили при комнатной температуре, высушивали, инкубировали в физиологическом растворе или 1% ДМСО или подвергали тепловому шоку, показали меньшую степень гистологических изменений.
[00539] Для контрольных образцов гистологом были сделаны следующие наблюдения.
[00540] Тимоциты постепенно теряются по мере культивирования ткани тимуса. Однако мертвые клетки могут сохраняться в культивированном тимусе в течение длительного времени из-за неспособности рекрутировать фагоциты для их удаления. Ядра клеток, претерпевающих апоптотическую гибель, первоначально конденсируются и окрашиваются более темным (синим) красителем гематоксилином. Поскольку энергия этих клеток истощаются, но они не подвергаются фагоцитозу, они теряют целостность их мембран и становятся некротическими. Кариолизис (растворение ядер в некротических клетках) обычно происходит в течение 2-3 дней in vivo, но, по-видимому, происходит медленнее во время культивирования тимуса. Таким образом, нередко наблюдаются большие эозинофильные (розовые) пространства остатков некротических клеток, где ядра тимоцитов претерпели кариолизис.Некоторые мертвые тимоциты сохраняют свои ядра, которые имеют рваные края и измененные характеристики окрашивания по сравнению с таковыми у жизнеспособных клеток.
[00541] По мере обеднения ткани тимоцитами эпителиальные клетки тимуса становятся более заметными. Трехмерная сеть эпителия тимуса (ЭТ) обычно демонстрируется в срезах через легкое и кружевовидное расположение соединенных эпителиальных клеток и/или (на вид) рассредоточенных клеток ЭТ, связи которых не видны в исследуемом срезе. Поскольку тимоциты теряются во время культивирования, трехмерная сеть сокращается. Это приводит к конденсации остаточного эпителия, так что субкапсулярный кортикальный эпителиальный слой становится толще и медуллярные клетки ЭТ становятся более плотно упакованными. Ядра жизнеспособных клеток ЭТ обычно имеют овальную форму, являются более крупными, чем ядра тимоцитов, и имеют четко очерченную ядерную мембрану, выделенную окраской гематоксилином (синим), а также одно или несколько ядрышек. Эти ядра ЭТ обычно выглядят «незакрашенными», что означает, что они не окрашиваются в темный цвет гематоксилином. Это соответствует интерпретации того, что они живы и метаболически активны, поскольку активный хроматин («эухроматин») не может связывать краситель гематоксилин. Присутствие ядрышек, которые являются сайтами синтеза рибосом, во многих клетках ЭТ также подтверждает, что они живы и метаболически активны. Типичная гистологическая картина контрольных срезов с 5, 12 и 21 дня показана на фиг. 8, 9 и 10 соответственно.
[00542] Для условий обработки, включая комнатную температуру, высушивание, 1% ДМСО и тепловой шок, гистолог указал, что внешний вид срезов существенно не отличался от контроля. Что касается образца, подвергшегося тепловому шоку, гистолог отметил, что термическая обработка могла «зафиксировать» клетки путем коагуляции белков, что предотвращает дальнейшую деградацию. Термическую обработку использовали в качестве фиксатора для тканей, в том числе тимуса.
[00543] На фиг.12А и 12В показана гистология ткани тимуса на предметных стеклах после воздействия условий принудительной деградации. На фиг.10 изображена гистологическая картина контрольных срезов ткани тимуса на 21 день.
[00544] Общая гистологическая картина ткани, подвергнутой вынужденной деградации, в эти моменты времени аналогична, но характеризуется меньшим количеством остаточных тимоцитов на 21 день (фиг.12В). Репрезентативные тельца Гассаля в медуллярных областях обозначены стрелками на фиг.12B. Репрезентативные жизнеспособные эпителиальные клетки тимуса обозначены стрелками на фиг.12A и 12B. Кортикальная область, показанная на фиг.12B, почти полностью состоит из некротических лимфоцитов на 21 день. Полоски в левом нижнем углу соответствуют 100 мкм.
[00545] Пример 4: Анализ партии лекарственного вещества ткани тимуса
[00546] Данные анализа партии для 10 партий ткани тимуса приведены ниже в таблице 8.
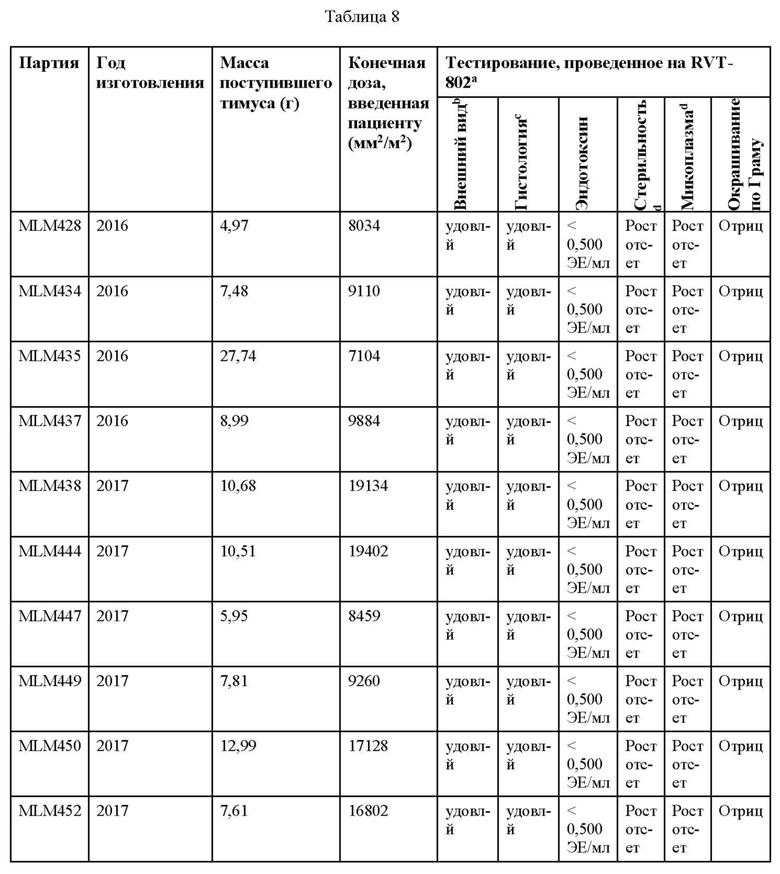
[00547] Условные обозначения:
(a) Эти партии были протестированы в соответствии со спецификацией, действовавшей на момент изготовления. Результаты тестирования лекарственного вещества, представленные в этой таблице, также представляют собой окончательные результаты тестирования лекарственного препарата.
(b) Спецификация для внешнего вида представляла собой отсутствие признаков постороннего вмешательства или повреждения контейнеров
(c) Гистологическое исследование использовали для определения как принадлежности, так и активности. Спецификация для гистологического исследования (проводимого между 5-9 днями) была следующей:
(d) Области, положительные на кератин, рассредоточены по всей ткани.
i. Идентифицировано по меньшей мере 1 тельце Гассаля
ii. Окрашивание на CK14 рассредоточено по всей ткани
iii. Наблюдаются интактные ядра
iv. Образцы для тестирования на стерильность и микоплазму собирали в 1, 7 и 14 дни.
[00548] Данные для 56 клинических тимусов, 8 тимусов, использованных для исследований вариабельности внутри тимуса, вариабельности между тимусами и тестирования временной динамики, и 3 тимусов, которые подверглись принудительной деградации, были использованы для создания текущей контрольной библиотеки. Образцы принудительной деградации в библиотеке (отрицательные контроли) представляли собой образцы, которые подвергались разложению под воздействием замораживания/размораживания или 10-кратной концентрации PBS. Полный набор данных привел к 14 различным кластерам. Все образцы принудительной деградации сгруппированы вместе, а клинические образцы или образцы для определения характеристик не сгруппированы с образцами принудительной деградации.
[00549] Пример 5.
[00550] Общий дизайн эксперимента примера 5 изображен на фиг. 20. Приведено схематическое представление хирургических процедур и программы лечения. Фигуры и большая часть приведенного ниже текста взяты из рукописи, находящейся в стадии подготовки к сдаче для публикации: Kwun J, Li J, Rouse DC, Park J, Farris AB, Turek JW, Knechtle SJ, Kirk AD, Markert ML Cultured Thymus Transplantation Promotes Donor-specific Tolerance to Allogeneic Heart Transplants.
[00551] На схеме дизайна эксперимента изображено восстановление наивных Т-клеток, тимопоэз и донор-специфическая толерантность, индуцированная хирургическим введением КТТ. Все крысы Lewis (LW) были подвергнуты тимэктомии и обеднены Т-клетками с помощью mAb к CD5 до трансплантации сердца и хирургического внедрения КТТ. КТТ от крыс F1 (LWxDA) и сердца от крыс DA пересаживали реципиентам LW с тимэктомией. Циклоспорин (CsA) вводили в течение четырех месяцев после трансплантации с помощью осмотического насоса. Сердце BN от третьей стороны трансплантировали в шею через 2-3 месяца после прекращения введения CsA. С контрольными крысами проводили идентичные манипуляции, за исключением того, что у них не осуществляли хирургическое внедрение КТТ.
[00552] Пример 5 демонстрирует, что КТТ, имплантированный в модели на крысе с некомпетентной иммунной системой, как описано ниже, может индуцировать толерантность к трансплантированному цельному органу. Авторы осуществили трансплантацию совпадающего по гаплотипу F1 (Lewis x Dark Agouti, LWxDA) трансплантата КТТ (культивированного, как описано ниже) с васкуляризованными несоответствующими трансплантатами сердца DA крысам Lewis.
[00553] До трансплантации КТТ реципиентов подвергали тимэктомии и обедняли Т- клетками.
[00554] Циклоспорин вводили в течение 4 месяцев, начиная со дня трансплантации сердца. Контрольная группа не получала трансплантацию КТТ. Через два месяца после прекращения иммуносупрессии у реципиентов, которым трансплантировали КТТ, отмечалась репопуляция наивных CD4 (CD62L+CD45RC+) Т-клеток в периферической крови; у контрольных крыс аналогичное явление не наблюдалось (фиг.23). Даже после развития недавних эмигрантных из тимуса CD4 (CD90+CD45RC+) T-клеток реципиенты, получившие трансплантацию КТТ, не отторгали аллотрансплантаты сердца DA (фиг. 23). Контроли не отторгали трансплантаты DA из-за отсутствия функциональных Т-клеток (фиг.23).
[00555] Для подтверждения донор-специфической неотвечаемости на 180 день после первоначальной трансплантации несоответствующего сердца DA трансплантировали сердце с несовпадающим MHC от Brown Norway (BN). Крысы LW с трансплантатами КТТ F1 (LWxDA) быстро отторгли сердце BN от третьей стороны (среднее время отторжения, 10 дн; n=5) (фиг.27). Контроли не отторгали сердце от третьей стороны (n=5). Реципиенты КТТ были способны продуцировать антитела против донора BN от третьей стороны, но не против донора тимуса DA, демонстрирующего гуморальную донор- специфическую толерантность (фиг. 32A). Иммуногистохимия трансплантированных КТТ при вскрытии показала функциональную ткань тимуса (фиг. 24). Таким образом, ТКТТ F1 (LWxDA) у крыс Lewis приводила к специфической толерантности к аллогенному MHC DA, экспрессируемому в тимусе донора, что приводило к длительной выживаемости трансплантатов сердца DA после отмены всей иммуносупрессии.
[00556] Материалы и методы. Модели на животных
[00557] В этом примере 5 аллогенный КТТ собирали и культивировали от 3-дневных крысят F1 (детенышей Lewis x Dark Agouti (фиг.17A и 17B), как описано ниже, а затем имплантировали подвергнутым тимэктомии крысам Lewis (RT-1l) аналогично лечением грудных детей с бестимусной cDGA, как описано ранее. (Markert, ML, et al., 2008; Market, ML, et al., 2010).
[00558] Крысы Lewis (RT-1l) и BN (RT-1n) были приобретены у Charles River. Крысы DA (RT-1av1) были приобретены у Envigo. F1(LEW/DA; RT-1l/av1) разводили занесенные в протокол сотрудники в основном отделе по разведению животных в Университете Дьюка в объекте обеспечения лабораторных животных. Реципиентам Lewis делали тимэктомию, как описано в Rendell VR, Giamberardino C, Li J, Markert ML, & Brennan TV, 2014, “Complete thymectomy in adult rats with non-invasive endotracheal intubation.” J Vis Exp (94).
[00559] Вкратце, поднижнечелюстные железы и грудиноподъязычная мышца были отделены тупым пинцетом, чтобы обнажить ткань, лежащую над трахеей. В манубрие грудины делали разрез величиной от 1 до 1,5 см. 7-сантиметровый расширитель типа alms использовали для оттягивания манубрия и двух половин грудиноподъязычной мышцы для обнажения тимуса. Тимус захватывали тупым пинцетом и извлекали. Обрезанные концы грудины закрывали одним шелковым швом от 3 до 4-0. На разрез наносили две капли бупивакаина по 2,5 мг/мл, а наружный слой кожи закрывали тремя или четырьмя 9 мм зажимами для ран.
[00560] Всех крыс с тимэктомией содержали на диете, содержащей Septra (PMI Nutrition International, LLC). Для индукции обеднения Т-клетками in vivo внутрибрюшинно вводили 1 мг mAb к CD5 (OX19; BioXCell, NH) в 0, 5 и 10 дни после тимэктомии и осуществляли супрессию с помощью циклоспорина 0,25 мг/кг/сут посредством осмотического насоса с 0 дня (момент трансплантации сердца и ТКТТ) до 4 месяцев в отношении трансплантации сердца. Всех крыс использовали и содержали в соответствии с руководящими принципами и соблюдением требований институционального комитета по этике Университета Дьюка.
Культивирование тимуса in vitro и КТТ
[00561] Тимусы трехдневных новорожденных крысят F1 (LEW/DA) собирали в стерильных условиях, разрезали на четыре части по линии естественного шва и переносили на стерильные нитроцеллюлозные фильтры (MF-Millipore, Millipore Sigma) в чашку для тканевых культур со средой TOM (фиг. 17B). Ткань тимуса культивировали в CO2-инкубаторе с 5% CO2 при 37°C в течение желаемого периода времени (от 5 до 7 дней). Среду меняли ежедневно. Органная среда для тимуса (TOM) состояла из HAMS F12 (Life Technologies) в концентрации 86,5%; Hepes (Life Technologies) в концентрации 25 мМ; L-глутамина (Life Technologies) в концентрации 2 мМ; фетальной бычьей сыворотки (Life Technologies) в концентрации 10%; и пенициллина-стрептомицина (Life Technologies) в 1-кратной концентрации. В день трансплантации кусочки тимуса промывали свежей средой и трансплантировали под почечную капсулу крысы Lewis с одним надежным швом (мононить 10-0). См. фиг. 17C. Все манипуляции проводили в стерильных условиях в боксе биологической безопасности.
Трансплантации сердца в брюшную полость и шейный отдел
[00562] Донорские сердца DA (RT-1av1) с полным несоответствием MHC трансплантировали реципиентам Lewis (RT-1l), подвергнутым тимэктомии. Трансплантацию сердца в брюшную полость проводили с использованием модифицированной техники на основе методов, описанных Schmid C, Binder J, Heemann U, & Tilney NL, 1994,” Successful heterotopic heart transplantation in rat,” Microsurgery 15(4):279-281.
[00563] Вкратце, сердце донора трансплантировали в брюшную полость реципиента после короткого периода холодовой ишемии в растворе Евро-Коллинз. Легочную артерию и аорту донора соединяли с нижней полой веной реципиента и нисходящей частью аорты, присоединяя конец к боковой части, в качестве сосудов притока и оттока для обеспечения кровообращения с использованием непрерывных нерассасывающихся швов мононитью 9/0. Циклоспорин A (CsA) вводили с помощью осмотического насоса (модель 2ML4, Alzet). Реципиенты также получали циклоспорин (CsA) в дозе приблизительно 2,5 мг/кг/сут после трансплантации тимуса с помощью осмотических насосов. CsA был отменен через 4 месяца после трансплантации тимуса, когда количество наивных Т-клеток в тестовой группе превысило 10%. Насос загружали в стерильных условиях и хирургическим путем вставляли подкожно в срединную область спины реципиентов. Осмотический насос заменяли каждый месяц в течение 4 месяцев. Для трансплантации сердца от третьей стороны с полным несоответствием MHC BN (RT-1n) реципиентам Lewis, несущим сердце DA, был использован метод трансплантации васкуляризированного сердца в шейный отдел, описанный Heron, et al. (Heron I., 1971, “A technique for accessory cervical heart transplantation in rabbits and rats,” Acta Pathol Microbiol Scand A 79(4):366-372), модифицированным способом.
[00564] Через 6-7 месяцев в шею трансплантировали сердце BN от третьей стороны. Вкратце, сердце от третьей стороны трансплантировали в правую часть шейного отдела через продольный разрез от челюстной кости до мечевидного отростка. Донорская легочная артерия и наружная яремная вена были соединены концами, а аорта была соединена с правой общей сонной артерией с помощью манжеты. Трансплантаты контролировали путем ежедневной пальпации, а затем подтверждали лапаротомией во время умерщвления. Животных умерщвляли в день отторжения (прекращения биения) или в назначенный момент времени.
Проточный цитометрический анализ и мониторинг DSA
[00565] Периферическая кровь была получена из черепной полой вены и окрашена антителами. Для анализа наивных и недавних эмигрантов из тимуса авторы использовали комбинацию анти-крысиного CD3 APC (BD Biosciences); анти-крысиного CD4 APC-Cy7 (Biolegend); анти-крысиного CD8a V450 (BD); анти-крысиного CD45 PE-Cy7 (BD); анти-крысиного CD45RC - PE (BD); анти-крысиного CD62L FITC (BD); и анти-крысиного CD90 BV 510 (Biolegend). Для оценки процентного содержания T-, B- и NK-клеток авторы использовали комбинацию анти-крысиного TCR FITC (BD); анти-крысиного CD4 APC- Cy7(Biolegend); анти-крысиного CD8a V450 (BD); анти-крысиного CD45 PE-Cy7 (BD); анти-крысиного CD45RA PE (Invitrogen); анти-крысиного NKR-P1A-APC (Invitrogen). Для различения хозяина и донора авторы использовали комбинацию анти-крысиного TCR APC (Biolegend), анти-крысиного CD45 PE-Cy7 (BD); MHC I класса RT1Aa (Santa Cruz Biotechnology). Авторы также использовали вторичное козье антимышиное IgG (Invitrogen) для неконъюгированного MHC I класса RT1Aa. Донор-специфическое аллоантитело (DSA) оценивали путем перекрестной пробы на совместимость из последовательно собранных образцов сыворотки реципиента с донором DA или крысами BN, представляющими собой третью сторону. FITC-конъюгированные полиспецифичные антитела крысиного иммуноглобулина добавляли к образцам и инкубировали после промывки. Т-клетки окрашивали АРС-конъюгированным антителом к CD3. Образцы анализировали на LSR fortessa (Beckman Coulter).
Некропсия
[00566] Трансплантат тимуса и все сердца были оценены при вскрытии через 8 месяцев после ТКТТ, когда тестовая группа отторгла сердце BN, трансплантированное в шейный отдел. Как и предполагалось, полученные из реципиента Т-клетки, не экспрессирующие MHC DA, появились в периферической крови реципиентов трансплантатов тимуса (фиг. 21).
Гистология, иммуногистохимия (IHC) и морфологический анализ
[00567] Все культивированные образцы тимуса и ТКТТ из-под почечной капсулы замораживали в OCT (среде для заморозки тканей; Tissue Tek). Контрольная ткань тимуса была получена от крысят возрастом новорожденных до 5-дневных. Срезы размером от четырех до пяти мм окрашивали на CD3 (поликлональное; Dako), Ki-67 (клон: SP6; Thermo), CK, (поликлональное; Invitrogen). Изображения IHC были получены с использованием микроскопа Olympus Vanox AH-3 цифровой камеры Olympus DP-70. Эксплантированные сердца подвергали последовательному нарезанию на срезы (5 мкм) от уровня середины желудочка до основания. Окрашивание H&E проводили для стандартного обследования и оценки отторжения. Инфильтрирующие трансплантат Т-клетки оценивали с помощью окрашивания поликлональным антителом к CD3 (Dako). Целые препараты трансплантатов сканировали с помощью Aperio ScanScope XT (Aperio Technologies, Inc., Виста, Калифорния).
Статистический анализ
[00568] Экспериментальные результаты анализировали с помощью GraphPad Prism (GraphPad Software 7.0, Сан-Диего, Калифорния). Для различий в выживаемости трансплантата использовали логарифмический ранговый критерий, а для других данных - t-критерий Стьюдента или U-критерий Манна-Уитни. Все данные были представлены как среднее ± стандартное отклонение. P-значения, которые были менее 0,05, считали статистически значимыми.
[00569] Результаты
[00570] Гистологический анализ (фиг. 18C и 18D (100-кратное увеличение) и фиг.19C и 19D (600-кратное увеличение) показал снижение Ki67+, CD3+ клеток в тимусе после культивирования, аналогично изменениям, наблюдаемым после культивирования ткани тимуса, используемой для пациентов (Markert ML, et al., 2008), “Use of allograft biopsies to assess thymopoiesis after thymus transplantation.” J Immunol 180(9):6354-6364). Как и в культивируемом тимусе человека, сеть эпителиальных клеток тимуса (ЭКТ) была сохранена в культивированной ткани тимуса крыс, как определено по окрашиванию на цитокератин (CK) (фиг.18 В (100-кратное увеличение) и фиг. 19В (600-кратное увеличение).
[00571] Как и предполагалось, полученные из реципиента Т-клетки, не экспрессирующие MHC DA, появились в периферической крови реципиентов трансплантатов тимуса (фиг. 21). После трансплантации КТТ в нижнем правом квадранте на фиг. 21 на 26, 55, 97 и 253 дни можно видеть возрастающую репопуляцию Т-клеток реципиентного типа.
Иммуногистохимическое исследование трансплантированной аллогенной ткани тимуса.
[00572] Репопуляция циркулирующих Т-клеток после обеднения Т-клетками и трансплантации тимуса и сердца изображена на фиг. 23. Все животные показали значительное снижение циркулирующих Т-клеток после обеднения Т-клетками. Реципиенты сердечного аллотрансплантата с внедренным КТТ (синяя/пунктирная линия) продемонстрировали постепенную репопуляцию циркулирующих Т-клеток. Животные без внедренного КТТ также продемонстрировали некоторую степень циркулирующих Т-клеток (красная/точечная линия). Тем не менее, у животных с внедренным КТТ были значительно повышены наивные и недавние эмигрантные из тимуса CD4 и CD8 Т-клетки (р<0,01), в то время как контрольные животные не демонстрировали ни циркулирующих наивных, ни недавних эмигрантных из тимуса CD4 и CD8 Т-клеток.
[00573] Трансплантированный тимус, эксплантированный через 8,5 месяцев после трансплантации, продемонстрировал положительное окрашивание на цитокератин (фиг. 22A), а также окрашивание Т-клеток, аналогичное нативному тимусу (фиг. 22B). Исходное 400-кратное увеличение.
[00574] Животны с внедренным КТТ продемонстрировали значительно более высокую репопуляцию наивных (CD62L+CD45RC+) CD4 и CD8 T-клеток, а также недавних эмигрантов из тимуса (RTE) в периферической крови, в то время как контрольные группы без трансплантации тимуса продемонстрировали низкий уровень циркулирующих наивных CD4 и CD8 T-клеток и не продемонстрировали циркулирующих RTE CD4 и CD8 T-клеток (фиг.23). Общее количество циркулирующих CD3 Т-клеток существенно не различалось в группах до трансплантации. Как и ожидалось, реципиенты LW с трансплантатом КТТ показали значительно увеличенные количества циркулирующих CD4 и CD8 T-клеток по сравнению с контрольными животными без трансплантации КТТ (фиг. 23).
[00575] Трансплантированные культивированные ткани тимуса под почечной капсулой на 180 день у реципиента сердечного аллотрансплантата изображены на фиг. 24.
[00576] Гистологическое исследование показало отличающиеся структуры, отдельные от ткани почки (20-кратное исходное увеличение). Трансплантированная культивированная ткань тимуса продемонстрировала нормальную структуру тимуса (H&E), жизнеспособные Т-клетки (CD3), пролиферацию Т-клеток (Ki67) и формирование телец Гассаля (черная стрелка) с кружевовидным рисунком (цитокератин) на эпителиальных клетках, что подтверждает жизнеспособность тимус с тимопоэзом (фиг.24B). Исходное 200-кратное увеличение. (Данные представлены как среднее значение ± стандартное отклонение; n=8-9 животных на группу; t-критерий Стьюдента, *P<0,05; **P<0,01; ***P<0,001, ****P<0,0001; NS, не значимо (p>0,05).
[00577] Кроме того, иммуногистологический анализ трансплантированного КТТ, эксплантированного на 180 день, показал нормальную гистологию тимуса, жизнеспособные Т-клетки (CD3), пролиферацию Т-клеток (Ki67) и кружевовидный рисунок CK с образованием телец Гассаля (стрелка) на ТЕС после хирургического внедрения КТТ (фиг. 24B). Эти наблюдения подтверждают жизнеспособность и функцию (тимопоэз) трансплантированного тимуса у животных, получивших аллогенную трансплантацию сердца.
[00578] Таким образом, крысы, получившие трансплантацию КТТ, продемонстрировали тимопоэз с развитием наивных Т-клеток у реципиентов сердечного аллотрансплантата.
[00579] Ожидалось, что Т-клетки, специфичные к донору DA, не будут развиваться, поскольку Т-клетки развивались в КТТ, экспрессирующем как DA, так и LW.
[00580] Сердце DA оценивали на наличие признаков отторжения. На фиг.25 показаны крысы LW с трансплантатами сердца DA и без какого-либо иммуносупрессивного лечения, отторгнувшие трансплантаты сердца DA в течение 10 дней (контроль DA, незакрашенные квадраты). Однако даже после развития RTE Т-клеток (CD90+CD45RC+) реципиенты LW с хирургически внедренным КТТ не отторгали (отсутствовало прекращение биения) сердечные аллотрансплантаты DA (n=8, закрашенные треугольники). Неожиданно контрольные животные LW без внедренного КТТ также не отторгали сердечный трансплантат DA (n=9, перевернутые закрашенные треугольники). Обе группы продемонстрировали хорошее качество биения в течение всего периода исследования (день 180). Поскольку непрерывное биение трансплантата не обязательно означает отсутствие отторжения, двух крыс-реципиентов умерщвляли через два месяца после прекращения иммуносупрессии (т.е., до трансплантации сердца BN от третьей стороны в шейный отдел), чтобы подтвердить отсутствие отторжения. Эксплантированные сердечные аллотрансплантаты (сердца DA) от обоих животных показали минимальную инфильтрацию мононуклеарными клетками (фиг.26A, с внедренным КТТ; и фиг.26B, без внедренного КТТ), без признаков отторжения по оценке согласно Международному обществу трансплантации легких и сердца (ISHLT), 2004, см. фиг. 26C.
[00581] Кривая выживаемости Каплана-Мейера (фиг. 25) показала значительно более длительную выживаемость трансплантата у животных с КТТ или без него и сингенных контролей (сердце LWсердце в крысу LW) по сравнению с крысами LW с трансплантатами сердца DA без какой-либо иммуносупрессии (контроль DA). Репрезентативные отсканированные изображения эксплантированного трансплантата на 180 день от животных с КТТ и без него показаны на фиг.26А и 26В. Изображения были адаптированы из сканирования целого препарата.
[00582] Оценка согласно ISHLT не показала различий в оценке отторжения между сердечными аллотрансплантатами от реципиентов с КТТ по сравнению с реципиентами без КТТ (n=3-4 на группу) (фиг. 26C). U-критерий Манна-Уитни, *P<0,05; NS, не значимо (р>0,05).
[00583] Основываясь на восстановлении наивных Т-клеток после ТКТТ, авторы полагают, что животные с КТТ потеряли свой донор-специфичный репертуар Т-клеток, в то время как животные без трансплантации тимуса не полностью восстановили свои популяции Т-клеток (общая гипочувствительность).
Аллореактивность в отношении васкуляризованного трансплантата сердца от третьей стороны
[00584] Чтобы подтвердить достижение донор-специфической неотвечаемости (толерантности), в отличие от общей гипочувствительности, в обеих группах животных была проведена дополнительная трансплантация полностью несовпадающего по МНС сердца BN через 6-7 месяцев (180-210 день) после трансплантации сердца DA.
[00585] Крысы LW крысы с внедренным КТТ (закрашенные треугольники. фиг. 27) быстро отторгли (прекращение биения трансплантата) сердце BN от третьей стороны (n=5, медианное время выживания (MST)=10±1,0 дня). Тем не менее, контрольные животные LW без внедренного КТТ не отторгали сердца от третьей стороны (n=6, MST≤38,5±8,9 дня), возможно, из-за отсутствия каких-либо аллореактивных Т-клеток.
[00586] В соответствии с этим отсутствием отторжения сердца от третьей стороны гистологический анализ подтвердил, что у животных с внедренным КТТ (перевернутые закрашенные треугольники, фиг. 27) наблюдалась повышенная инфильтрация мононуклеарными клетками в аллотрансплантате сердца (фиг. 28A), тогда как животные без внедренного КТТ продемонстрировали немодифицированный аллотрансплантат сердца BN (фиг. 28B). Реципиенты с КТТ быстро отторгали сердце BN (MST=10±1,0 дней) (закрашенные квадраты, фиг.29), в то время как реципиенты без КТТ не отторгали сердца BN от третьей стороны (заштрихованные треугольники, фиг. 29). Контроль BN (закрашенные кружки, фиг.29) продемонстрировал отторжение сердец BN крысами LW. Сингенный контроль (незакрашенные кружки, фиг.29) продемонстрировал отсутствие отторжения сердец LW крысами LW. Кривая выживаемости Каплана-Мейера (фиг. 27) показала значительные различия в выживаемости трансплантата. Репрезентативные сканированные изображения эксплантированного трансплантата сердца BN во время отторжения или через 46 дней после трансплантации показаны на фиг. 28А и 28В, соответственно. Трансплантаты сердца BN от животных с внедренным КТТ показали значительную инфильтрацию мононуклеарными клетками (фиг. 28A), в то время как трансплантаты сердца BN от животных без внедренного КТТ не имели признаков отторжения (фиг. 28B). Изображения были адаптированы из сканирования целого препарата.
[00587] Гистологическое исследование (оценка согласно ISHLT) эксплантированных сердец BN от крыс с внедренным КТТ (закрашенные квадраты, фиг.29) показало отторжение степени 3R со значительно увеличенной инфильтрацией воспалительными клетками по сравнению с сингенными контролями или крысами без внедренного КТТ (заштрихованные треугольники, фиг. 29). Оценка согласно ISHLT показала значительно более высокую степень отторжения сердец BN у животных с КТТ по сравнению с сердцами BN у животных без КТТ (n=3-5 на группу). U-критерий Манна-Уитни, *P<0,05; **P<0,01; NS, не значимо (р>0,05).
[00588] Также следует отметить, что сердца BN, трансплантированные в шейный отдел у реципиентов с внедренным КТТ, были значительно увеличены (фиг. 30A), в то время как сердца DA в брюшной полости были меньше, чем нативные сердца (фиг. 30A). Сердца BN от реципиентов без внедренного КТТ не продемонстрировали какого-либо увеличения размера (фиг. 30B) по сравнению с сердцами BN от реципиентов с внедренным КТТ.
Избирательная Т-клеточная инфильтрация в сердцах от третьей стороны, но не в сердцах DA, которые имеют общий MHC DA с КТТ.
[00589] Были использованы два традиционных способа для определения отторжения трансплантата в этой модели трансплантации сердца крысы: измерения сердцебиения/прекращения и система оценки согласно ISHLT для человека. Первый нечувствителен к отторжению низкой степени, а второй нечувствителен к отторжению высокой степени. В результате инфильтрацию воспалительными клетками измеряли в сердцах DA от 3 крыс на 180 день и в сердцах BN во время умерщвления через 7-8 месяцев у 5 крыс. Таким образом, инфильтрацию воспалительными клетками измеряли в сердцах DA от 3 крыс на 180 день и в сердцах BN во время умерщвления через 7-8 месяцев у 5 крыс.
[00590] Крысы, которых лечили обеднением T-клеток, хирургическим внедрением КТТ введением CsA в течение четырех месяцев, не продемонстрировали повышенного уровня инфильтрации воспалительными клетками в сердцах DA после репопуляции T-клеток (фиг. 31A). Контрольные трансплантаты DA (у крыс LW без иммуносупрессии) продемонстрировали значительно увеличенную инфильтрацию трансплантата иммунными клетками в сердце DA по сравнению с инфильтрацией иммунными клетками в сердцах DA у крыс с КТТ или без КТТ. У животных с внедренным КТТ наблюдалась массивная инфильтрация воспалительными клетками в сердечном аллотрансплантате от третьей стороны (сердце BN) (фиг. 31B). Контрольные трансплантаты BN (у крыс LW без иммуносупрессии) и трансплантаты BN от реципиентов с КТТ продемонстрировали значительно повышенную инфильтрацию воспалительными клетками по сравнению с таковыми в трансплантатах BN от животных без КТТ. Крысы, которым не внедряли КТТ, не имели инфильтратов в сердце BN (фиг. 31B, заштрихованные треугольники) из-за некомпетентности их иммунной системы.
[00591] Т-клеточная инфильтрация была оценена с помощью иммуногистохимии и подтвердила селективную инфильтрацию Т-клетками в BN (правые панели, фиг. 31C), но не в DA (средние панели, фиг. 31C) сердцах животных, которым внедряли КТТ, и в отсутствие T-клеточной инфильтрации в обоих сердцах животных без КТТ (фиг. 31D). Аллотрансплантаты сердца у крыс DA и BN собирали с нативным сердцем во время отторжения сердца BN. В целом нативное сердце и сердце DA (196 день после операции) не продемонстрировали резкого увеличения Т-клеток, в то время как сердце BN (14 день после операции) продемонстрировало огромное количество Т-клеток у реципиентов с внедренным КТТ. Изображения были адаптированы из сканирования целого препарата. Было проанализировано в общей сложности 3-5 животных на группу; t-критерий Стьюдента, *P<0,05; **P<0,01; ***P<0,001, ****P<0,0001; NS, не значимо (p>0,05).
[00592] Эти данные подтверждают, что для группы, получившей КТТ, Т-клеточная инфильтрация происходит только в трансплантате BN от третьей стороны, но не в трансплантате, имеющем совпадающий MHC (DA) с трансплантированным тимусом, возможно, из-за отсутствия репертуара Т-клеток (из-за отрицательного отбора) против (сердца DA) донорских антигенов.
Гуморальный ответ против донорских антигенов после трансплантации тимуса
[00593] Проводили оценку ответов на донорские антитела, чтобы определить, была ли аллогенная Т-клеточная неотвечаемость, отмеченная у подвергнутых тимэктомии крыс LW с последующей трансплантацией LWxDA и хирургическим внедрением КТТ, связана с гуморальной толерантностью по отношению к MHC донорского DA. Последовательно собирали образцы сыворотки реципиентов и проводили перекрестную пробу на совместимость с МНПК от крыс DA и BN методом проточной цитометрии. Животные, получившие трансплантаты сердца DA или BN без иммуносупрессии, вырабатывали антитела против своих доноров (соответственно DA или BN). Животные с сингенным сердечным аллотрансплантатом не вырабатывали антитела против MHC DA или BN, как показано на фиг.32A (горизонтально заштрихованные пики в левом столбце, сверху для DA и снизу для BN). Иллюстративные гистограммы для донор-специфического аллоантитела (антитела к DA и антитела к BN) после трансплантации, измеренного с помощью перекрестной пробы на совместимость с Т-клетками методом проточной цитометрии, показаны на фиг. 32A. Реципиенты с КТТ или без него не генерировали никаких антител против антигена DA (верхний ряд, средний и правый столбцы на фиг.32A), в то время как животные с КТТ были способны генерировать антитела против антигена BN (нижний ряд, средняя панель, фиг.32А). Образцы сыворотки от реципиентов трансплантатов сердца DA без иммуносупрессии и от реципиентов LW трансплантатов сердца BN без иммуносупрессии использовали в качестве положительных контролей (контроль DA и контроль BN) для антител к DA (верхний ряд, левая панель, жирная линия) или антител к BN (нижний ряд, левая панель, пунктирная линия), соответственно.
[00594] Интересно, что, подобно гипочувствительности Т-клеток, у животных с ТКТТ или без нее не были обнаружены Ab к DA (фиг. 32B). Ab к BN легко обнаруживались у животных с LWxDA с внедренным КТТ, но не у животных без внедренного КТТ, p<0,01 (фиг. 32C). Животные без КТТ были в основном иммунодефицитными. Животные с КТТ имели специфическую толерантность к DA.
[00595] Таким образом, совместная трансплантация тимуса привела к специфической толерантности к аллогенному MHC DA, экспрессируемому в тимусе донора, и, таким образом, к долгосрочному выживанию трансплантата сердца DA посредством предотвращения развития донор-специфического T-клеточного репертуара к DA, а также предотвращения донор (DA)-специфического гуморального ответа. Иммунокомпетентность была продемонстрирована у этих крыс быстрым отторжением сердец BN от третьей стороны, а также аллоантительным ответом против донорских клеток BN.
[00596] Дальнейшее подтверждение лечения, описанного выше, может быть получено из клинического опыта с пациентом с аномалией Ди Георга.
[00597] Пациент 1 представляет собой ребенка, родившегося с полной аномалией Ди Георга. У него не было Т-клеток при рождении. Основной проблемой для пациента 1 был выраженный гипопаратиреоз, приводивший ко многим госпитализациям по поводу гипокальциемии. Пациенту 1 была проведена трансплантация культивированной ткани тимуса (КТТ) и трансплантация паращитовидной железы от родителя в один и тот же день. В небольшом клиническом исследовании участвовали три других пациента, получившие тимус плюс паращитовидную железу от родителя. Пациент 1 получил две трансплантации в возрасте 4 месяцев. Хотя у пациента 1 не было Т-клеток, пациенту 1 давали антитимоцитарный глобулин кроличьего происхождения для иммуносупрессии до трансплантации согласно протоколу. Никакой другой иммуносупрессии не проводили. У пациента 1 развились наивные Т-клетки и нормальные пролиферативные Т-клеточные ответы на митогены. У всех четырех пациентов, которые получили как тимус, так и паращитовидную железу в ходе исследования, развился нормальный уровень гормона паращитовидной железы. Пациент 1 был единственным субъектом, который смог отказаться от приема препаратов кальция в течение длительного времени (10 лет). Из трех других пациентов один умер в возрасте до одного года из-за проблем с легкими, а два других с полной аномалией Ди Георга вынуждены были вернуться к приему препаратов кальция к возрасту приблизительно одного года. Пациент 1 был единственным субъектом, имевшим отрицательную реакцию смешанной культуры лимфоцитов (MLR) против родителя, выступавшего донором паращитовидной железы, во все моменты времени. Другие три субъекта имели положительные MLR, начиная с их первого анализа.
[00598] Возможное объяснение сохранения пациентом 1 функции паращитовидной железы заключается в том, что донор паращитовидной железы пациента 1 имел аллели HLA II класса, которые соответствовали либо аллелям II класса реципиента (светло-серая заливка на графике ниже), либо аллелям II класса донора тимуса (темно-серая заливка в таблице ниже).
[00599] Стволовые клетки у пациента 1 развивались в тимоциты в тимусе.
[00600] Дентритные клетки от пациента 1 мигрируют в тимус и удаляют Т-клетки, которые тесно связываются с МНС на ДК пациента 1. Имеется толерантность к аллелям в светло-серой заливке. См. таблицу 9.
[00601] Эпителиальные клетки тимуса донора тимуса также удаляют тимоциты, которые тесно связаны с ними (темно-серая заливка). Это является механизмом толерантности к аллелям, залитым темно-серым цветом.
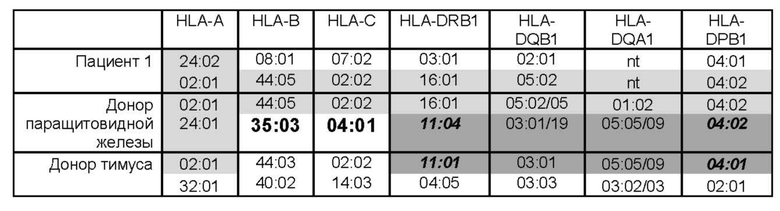
[00602] Следует отметить, что у донора паращитовидной железы имеется один аллель HLA-B и один аллель HLA-C, которые не совпадали ни с реципиентом, ни с донором тимуса. Авторы не поняли, почему паращитовидная железа не была отторгнута. Однако по прошествии 10 лет ребенку была поставлена живая вакцина против кори/эпидемического паротита/краснухи. Функция паращитовидной железы была нарушена за две недели, и пациент 1 вернулся к приему препаратов кальция.
[00603] Авторы пришли к выводу, что живая вакцина активировала CD8 Т-клетки у пациента 1. Одна треть CD8 Т-клеток обладает врожденной аллореактивностью. Аллореактивные CD8 T-клетки реагировали бы на несовпадающие аллели HLA-B и C у донора паращитовидной железы (выделенные жирным шрифтом большого размера аллели HLA-B и HLA-C в таблице).
[00604] Исходя из данных, полученных для этого пациента, ясно, что необходимо совпадение как для класса I, так и для класса II для индукции долгосрочной толерантности. Кроме того, по несоответствиям 2 поля (жирный курсив) в DRB1 и DPB1 между донором паращитовидной железы и донором тимуса можно видеть, что несовпадения 2 поля могут быть допустимыми и позволяют достигать толерантности. В частности, эти несовпадения 2 поля не привели к нарушению функции трансплантата; они были допустимы. Этот ребенок благополучно развивается с хорошим количеством и функцией Т-клеток и нормальными уровнями иммуноглобулина. Пациент 1, однако, остается на препаратах кальция, так как паращитовидная железа от родителя была отторгнута.
[00605] Вышеприведенные варианты осуществления и преимущества являются лишь иллюстративными и не должны рассматриваться как ограничивающие настоящее изобретение. Настоящее изобретение может быть легко применено к другим типам устройств, экспериментов и хирургических процедур. Также описание вариантов осуществления настоящего изобретения предназначено для иллюстрации, а не для ограничения объема формулы изобретения. Многие альтернативы, модификации и варианты будут очевидны для специалистов в данной области техники.
[00606] Необходимо понимать, что хотя изобретение было раскрыто в сочетании с его подробным описанием, вышеизложенное описание предназначено для иллюстрации, но не для ограничения объема изобретения, который определяется объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и модификации находятся в пределах объема нижеследующей формулы изобретения.
[00607] Цитируемые источники, обсуждаемые в заявке, полностью включены посредством ссылки для их назначения, что ясно исходя из контекста заявки.
[00608] Все патенты, патентные заявки и публикации, цитируемые в настоящем документе, настоящим включены посредством ссылки в полном объеме. Раскрытие этих публикаций в полном объеме включено в настоящую заявку посредством ссылки.
[00609] Раскрытие всех без исключения патентов, патентных заявок, публикаций и регистрационных номеров, цитируемых в настоящем документе, полностью включены в настоящий документ посредством ссылки.
[00610] Хотя настоящее изобретение было раскрыто со ссылкой на различные варианты осуществления, очевидно, что другие варианты осуществления и их варианты могут быть разработаны другими специалистами в данной области техники без отклонения от сущности и объема изобретения. Следует считать, что прилагаемая формула изобретения включает все такие варианты осуществления и эквивалентные варианты.
[00611] Вышеизложенное письменное описание считается достаточным, чтобы обеспечить возможность осуществления вариантов его осуществления специалистом в данной области техники. Вышеизложенное описание и примеры подробно описывают отдельные варианты осуществления изобретения и описывают наилучший порядок действий, рассматриваемый авторами. Однако следует иметь в виду, что независимо от того, насколько подробно вышеприведенное может быть описано в тексте, вариант осуществления может быть осуществлен многими способами, и изобретение следует истолковывать в соответствии с прилагаемой формулой изобретения и любыми ее эквивалентами.
[00612] Цитируемые источники:
[00613] Ahonen, P., 1985, “Autoimmune polyendocrinopathy - candidosis - ectodermal dystrophy (APECED): autosomal recessive inheritance,” Clinical Genetics, 27: 535-542Ahonen, P., et al., 1987, “Adrenal and steroidal cell antibodies in patients with autoimmune polyglandular disease type I and risk of adrenocortical and ovarian failure,” J. Clin. Endocrinology and Metabolism, 64: 494-500.
[00614] Ahonen, P., et al., 1987, “Adrenal and steroidal cell antibodies in patients with autoimmune polyglandular disease type I and risk of adrenocortical and ovarian failure,” J. Clin. Endocrinology and Metabolism, 64: 494-500.
[00615] Ahonen, P., et al., 1988, J. Clin. Endocrinology and Metabolism, 66, 1152-1157.
[00616] Ahonen, P., et al., 1990, “Clinical variation of autoimmune polyendocrinopathy- candidiasis-ectodermal dystrophy (APECED) in a series of 68 patients,” New Engl. J. Med. 322: 1829-1836.
[00617] Arulanantham, K., et al., 1979, “Evidence for Defective Immunoregulation in the Syndrome of Familial Candidiasis Endocrinopathy,” New Eng. J. Med. 300:164-168.
[00618] Blizzard, R. M. and Kyle M., 1963, “Studies of the Adrenal Antigens and Antibodies in Addison’s Disease,” J. Clin. Invest. 42: 1653-1660Boehm T, Takahama Y. 2014. Thymic Development and Selection of T Lymphocytes. Heidelberg: Springer-Verlag.
[00619] Boehm T, Takahama Y. 2014. Thymic Development and Selection of T Lymphocytes. Heidelberg: Springer-Verlag.
[00620] CFR Title 21; 1271 Human cells, tissues, and cellular and tissue-based products.
[00621] Chinn I, Devlin B, Li YJ, et al., 2008. “Long-term tolerance to allogeneic thymus transplants in complete DiGeorge anomaly,” Clin Immunol. 126(3): 277-281.
[00622] Heron I., 1971, “A technique for accessory cervical heart transplantation in rabbits and rats,” Acta Pathol Microbiol Scand A 79(4):366-372.
[00623] Hong R, Schulte-Wissermann H, Jarrett-Toth E, Horowitz SD, Manning DD, “Transplantation of cultured thymic fragments. II. Results in nude mice,” J Exp Med. 149(2): 398-415.
[00624] Li B, Li J, Hsieh CS, Hale LP, Li YJ, Devlin BH, Markert ML. 2009 “Characterization of cultured thymus tissue used for transplantation with emphasis on promiscuous expression of thyroid tissue-specific genes,” 2009, Immunol Res. 2009, 44(1-3):71-83.
[00625] Li B, Li J, Devlin BH, Markert ML. 2011, “Thymic microenvironment reconstitution after postnatal human thymus transplantation,” Clin Immunol. Sep; 140(3): 244-59.
[00626] Krohn, K., et al., 1992, “Identification by molecular cloning of an autoantigen associated with Addison's disease as steroid 17α-hydroxylase,” Lancet 339:770-773.
[00627] Markert ML, Kostyu DD, Ward FE, McLaughlin TM, Watson TJ, Buckley RH, Schiff SE, Ungerleider RM, Gaynor JW, Oldham KT, Mahaffey SM, Ballow M, Driscoll DA, Hale LP, Haynes BF. “Successful formation of a chimeric human thymus allograft following transplantation of partially HLA-matched postnatal thymus,” 1997, Journal of Immunology, 158:998-1005.
[00628] Markert ML, Boeck A, Hale LP, Kloster AL, McLaughlin TM, Batchvarova MN, et al., “Transplantation of thymus tissue in complete DiGeorge syndrome,” 1999, N Engl J Med. 341(16): 1180-9.
[00629] Markert ML, et al., 2004, “Postnatal thymus transplantation with immunosuppression as treatment for DiGeorge syndrome,” Blood 104(8):2574-2581.
[00630] Markert ML, Devlin BH, Alexieff MJ, Li J, McCarthy EA, Gupton SE, et al., “Review of 54 patients with complete DiGeorge anomaly enrolled in protocols for thymus transplantation: outcome of 44 consecutive transplants,” 2007, Blood, 109(10): 4539-47.
[00631] Markert ML, et al., 2008), “Use of allograft biopsies to assess thymopoiesis after thymus transplantation.” J Immunol 180(9):6354-6364.
[00632] Markert ML, Devlin BH, McCarthy EA, 2010, “Thymus transplantation,” Clin Immunol., 135(2): 236-46.
[00633] Markert ML, Devlin BH, McCarthy EA. Chapter 84 Thymic reconstitution. 2013. In: Fleisher TA, Shearer WT, Schroeder HW, Frew AJ, Wey and CM, editors. Clinical Immunology (Fourth Edition). Лондон, стр. 1032-8.
[00634] Markert ML. 2014. “Thymus Transplantation,” Stiehm’s Immune Deficiences, eds Sullivan KE & Stiehm ER (Academic Press), 1st Ed, стр. 1059-1067.
[00635] Markert ML, Watson TJ, Kaplan I, Hale LP, Haynes BF, “The human thymic microenvironment during organ culture,” 1997, Clin Immunol Immunopathol., Jan; 82(1): 26-36.
[00636] Neufeld, M. et al., 1981, “Two types of autoimmune Addison's disease associated with different polyglandular autoimmune (PGA) syndromes,” Medicine 60: 355-362.
[00637] Parker W, Yu PB, Holzknecht ZE, Lundberg K, Buckley RH, Platt JL, “Specificity and function of ‘natural’ antibodies in immunodeficient subjects: Clues to B cell lineage and development,” 1997, J Clin Immunol., 17:311-321.
[00638] Perheentupa J., 2002, Endocrinol. Metab. Clin. North Am. 31: 295-320Rota IA and Dhalla F. FOXN1 deficiency nude severe combined immunodeficiency. Orphanet Journal of Rare Diseases. 2017; 12:6.
[00639] Rendell VR, Giamberardino C, Li J, Markert ML, & Brennan TV, 2014, “Complete thymectomy in adult rats with non-invasive endotracheal intubation,” J Vis Exp (94).
[00640] Schmid C, Binder J, Heemann U, & Tilney NL, 1994,” Successful heterotopic heart transplantation in rat,” Microsurgery 15(4):279-281.
[00641] Schoenecker JG, Hauck RK, Mercer MC, Parker W, Lawson J, 2000, “Exposure to topical bovine thrombin during surgery elicits a response against the xenogeneic carbohydrate galactose α1-3Galactose,” J Clin Immunol., 20:434-444.
[00642] Uibo R., et al., 1994, “Autoantibodies to cytochrome P450 enzymes P450scc, P450c17, and P450c21 in autoimmune polyglandular disease types I and II and in isolated Addison's disease,” J. Clin. Endocrinol. Metab. 78: 323-328.
[00643] Zlotogora, J., et al., 1992, “Polyglandular autoimmune syndrome type I among Iranian Jews,” J. Med. Genet, 29, 824-826.
[00644] Сокращения:
[00645] AIRE: ген аутоиммунного регулятора.
[00646] Ab: антитело.
[00647] Ag: антиген.
[00648] APC: антигенпрезентирующая клетка.
[00649] ATG: тимоглобулин.
[00650] 2 р/сут: два раза в сутки
[00651] ИМТ: индекс массы тела
[00652] ППТ: площадь поверхности тела.
[00653] BSC: бокс биологической безопасности.
[00654] cDGA: полная аномалия Ди Георга.
[00655] CFR: Свод федеральных нормативных актов США.
[00656] CK: цитокератин.
[00657] CNI: ингибитор кальциневрина.
[00658] КТТ: продукт, полученный из аллогенной культивированной ткани постнатального тимуса.
[00659] CVVHD/F: непрерывная вено-венозная гемодиафильтрация.
[00660] ДК: дендритная клетка.
[00661] DSA: донор-специфическое антитело.
[00662] DGF: отсроченная функция трансплантата
[00663] EBV: вирус Эпштейна-Барр.
[00664] ЭЕ: эндотоксиновая единица.
[00665] FBS: фетальная бычья сыворотка.
[00666] FDA: Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США.
[00667] ФСГС: фокально-сегментарный гломерулосклероз.
[00668] H&E: гематоксилин и эозин.
[00669] HD: гемодиализ.
[00670] HEPES: N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота.
[00671] HI: HI - термоинактивация.
[00672] в/б: внутрибрюшинный.
[00673] ВИЧ: вирус иммунодефицита человека.
[00674] IBW: идеальная масса тела.
[00675] ИЗСД: инсулинозависимый сахарный диабет.
[00676] ISHLT: Международное общество трансплантации легких и сердца.
[00677] ISO: Международная организация по стандартизации.
[00678] LAL: лизат амебоцитов Limulus.
[00679] mAb: моноклональное антитело.
[00680] MHC: главный комплекс гистосовместимости.
[00681] MST: среднее время выживания.
[00682] МНПК: мононуклеарные клетки периферической крови.
[00683] PBS: натрий-фосфатный буфер.
[00684] POD: день после операции.
[00685] PRA: панель-реактивные антитела.
[00686] с/л: сублингвальный.
[00687] TBW: общая масса тела
[00688] TC: культура ткани.
[00689] Tfh: фолликулярный т-хелпер.
[00690] TOM: органная среда для тимуса.
[00691] USP: Фармакопея США.
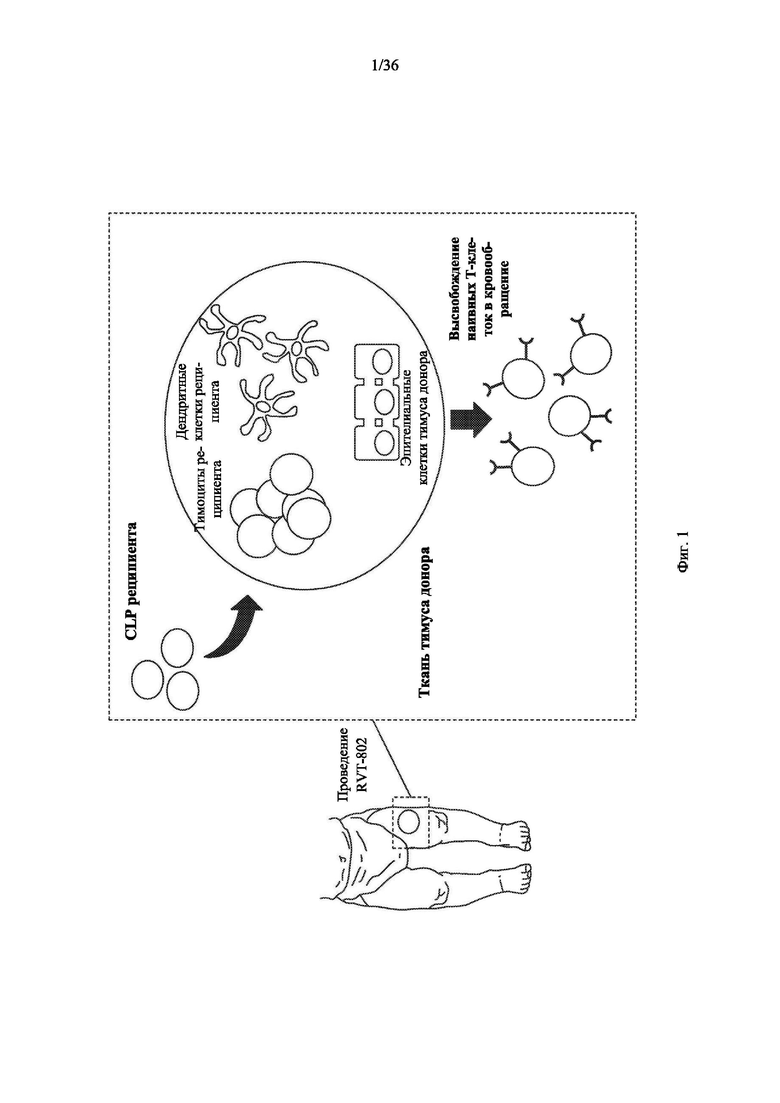
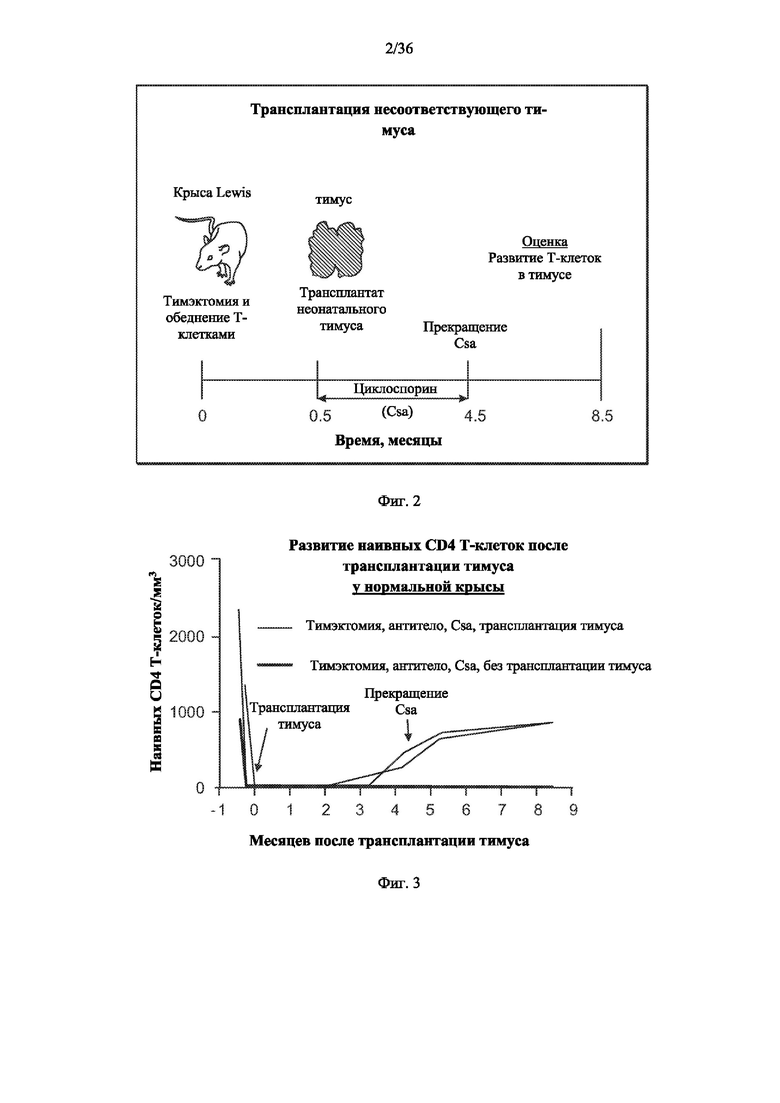
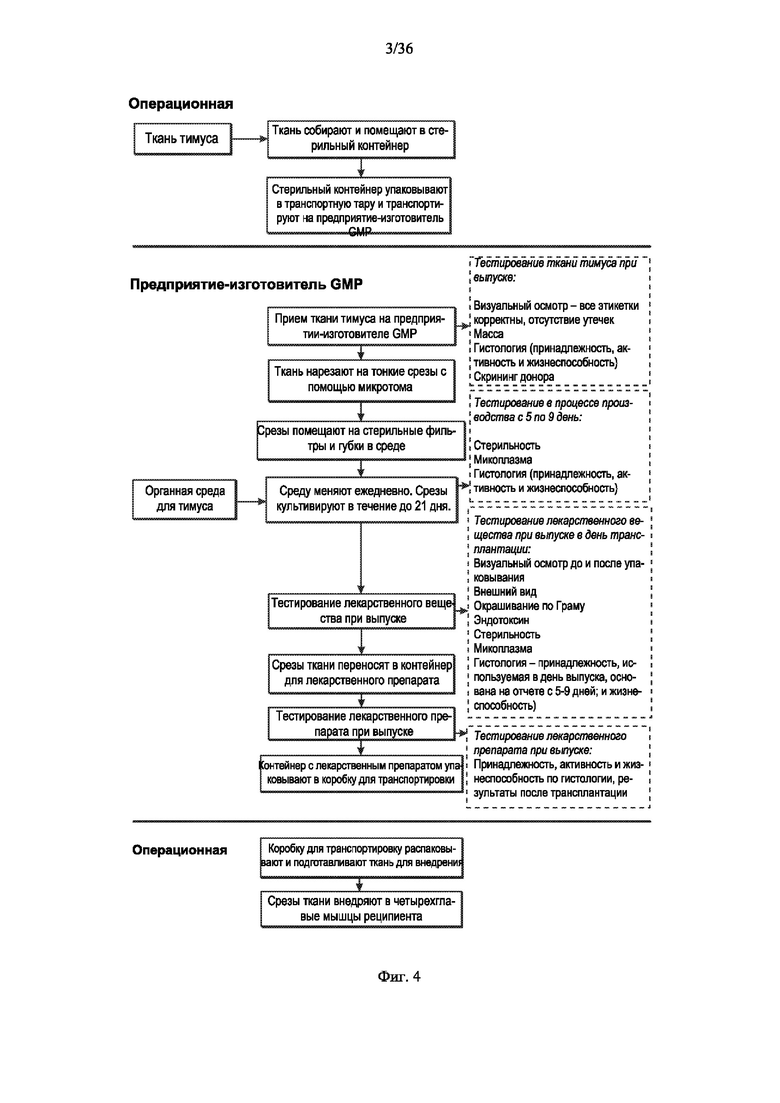
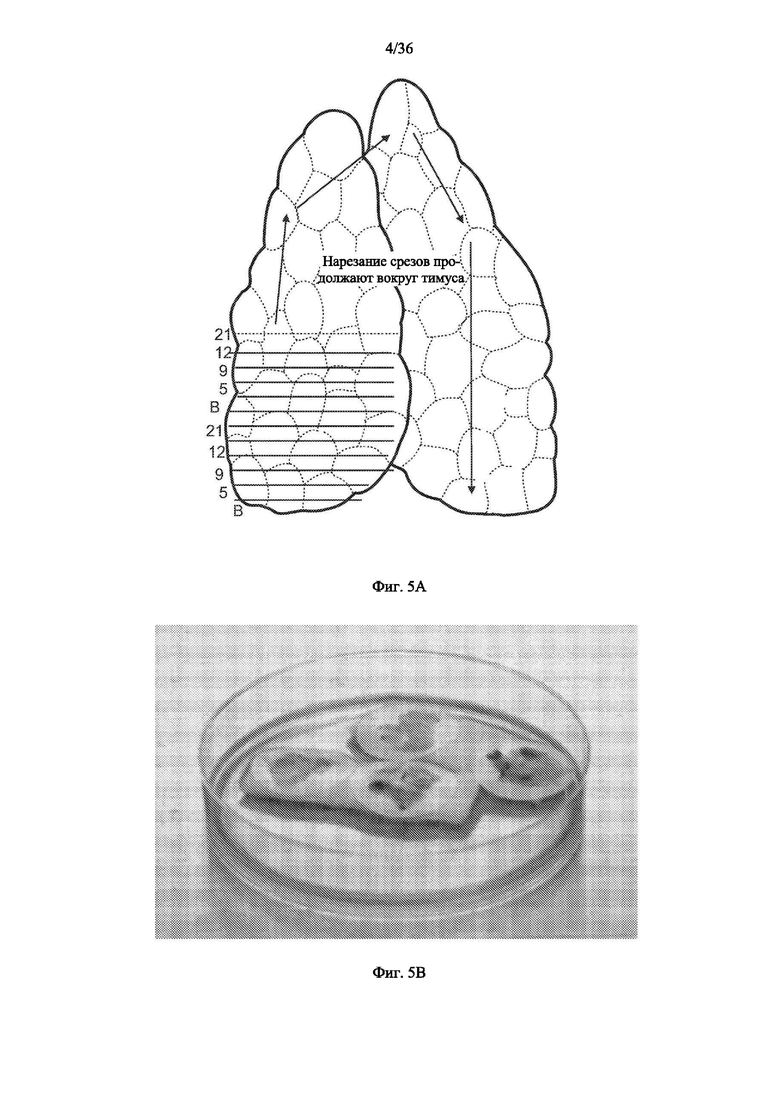
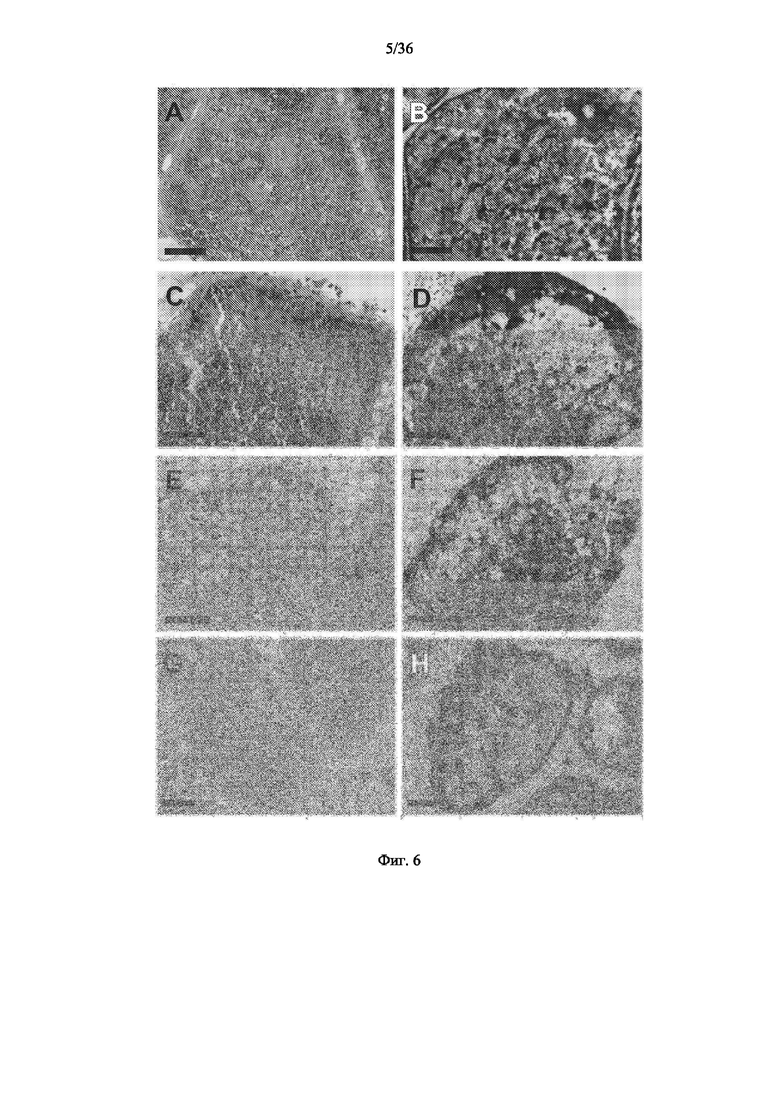
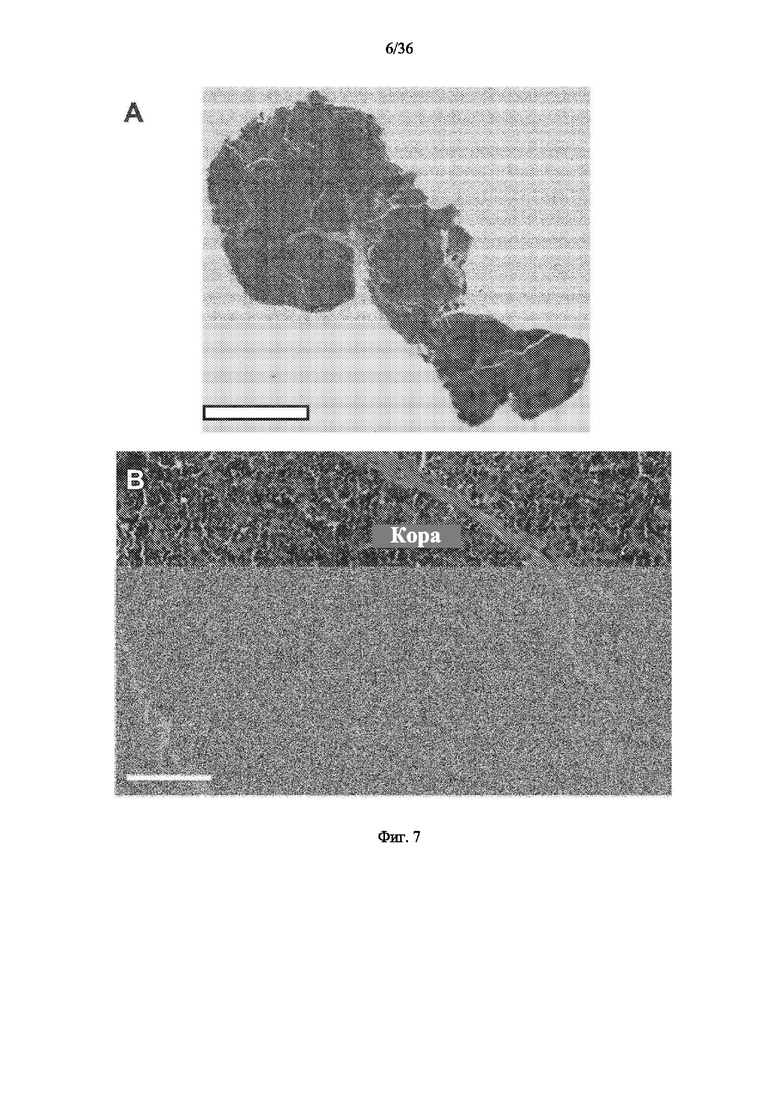
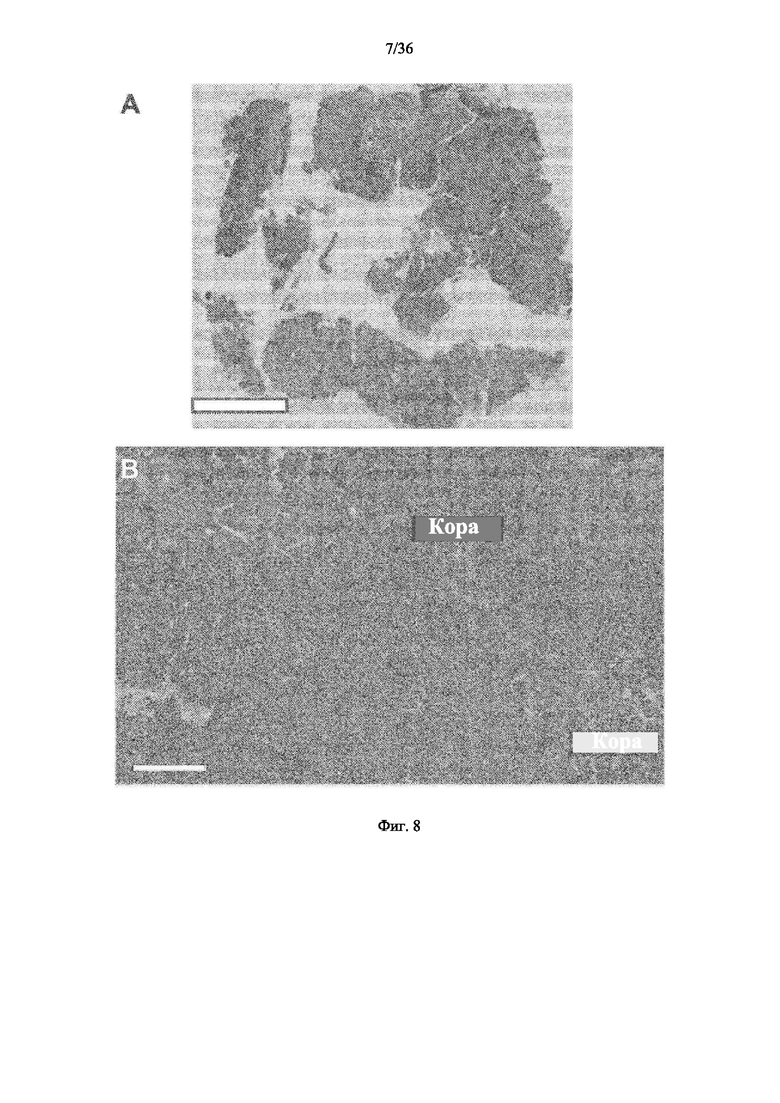




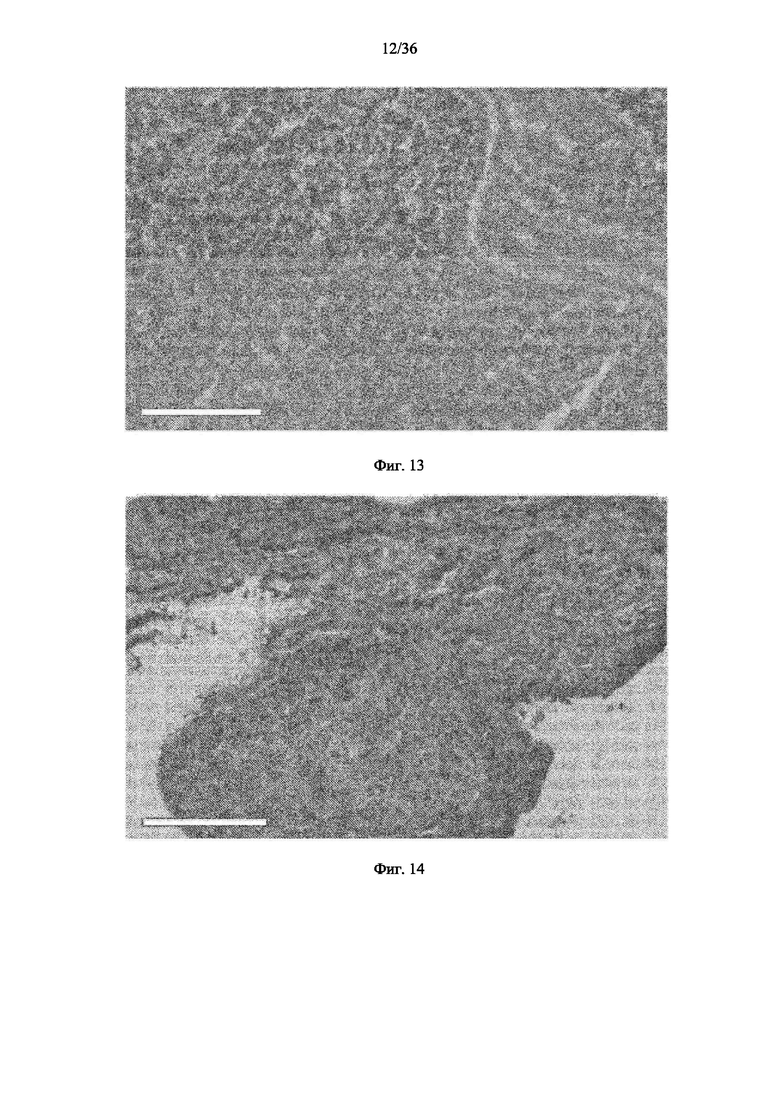
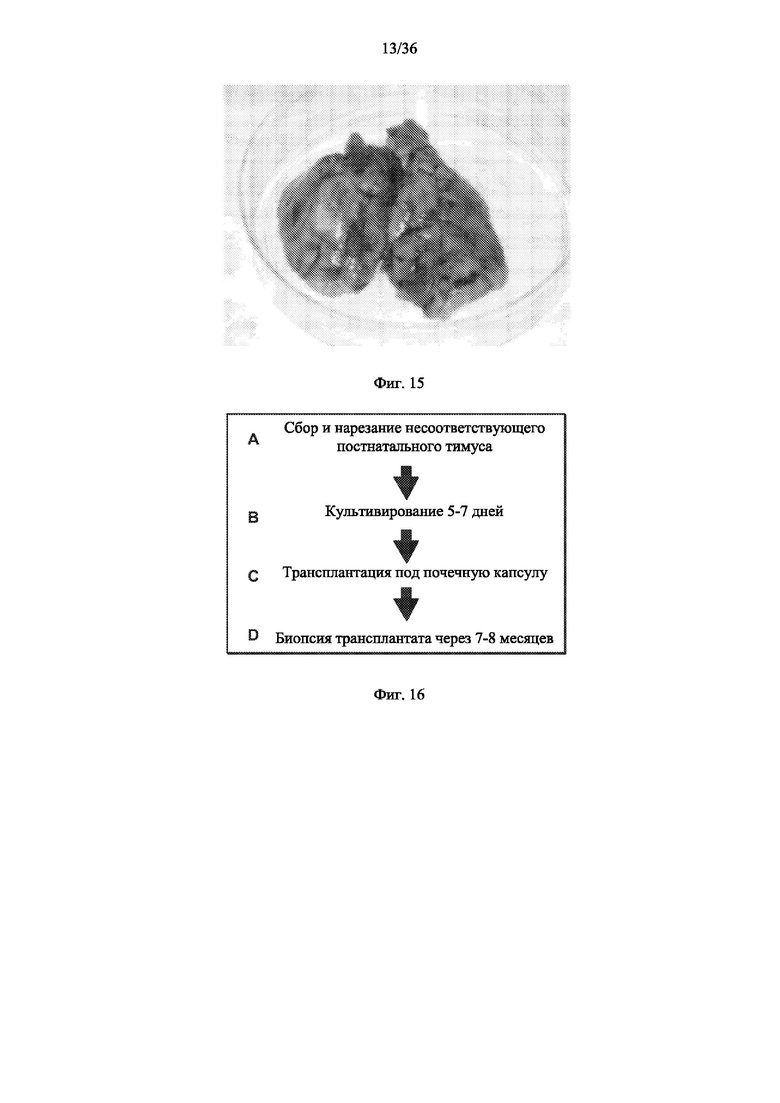
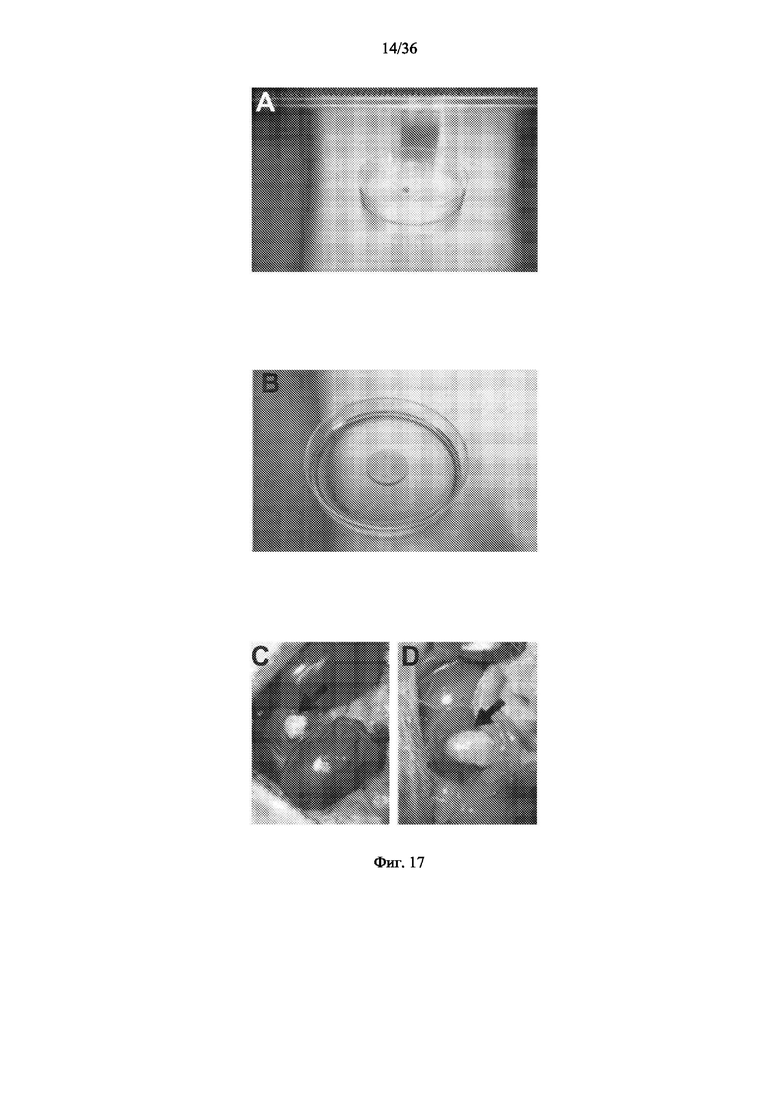

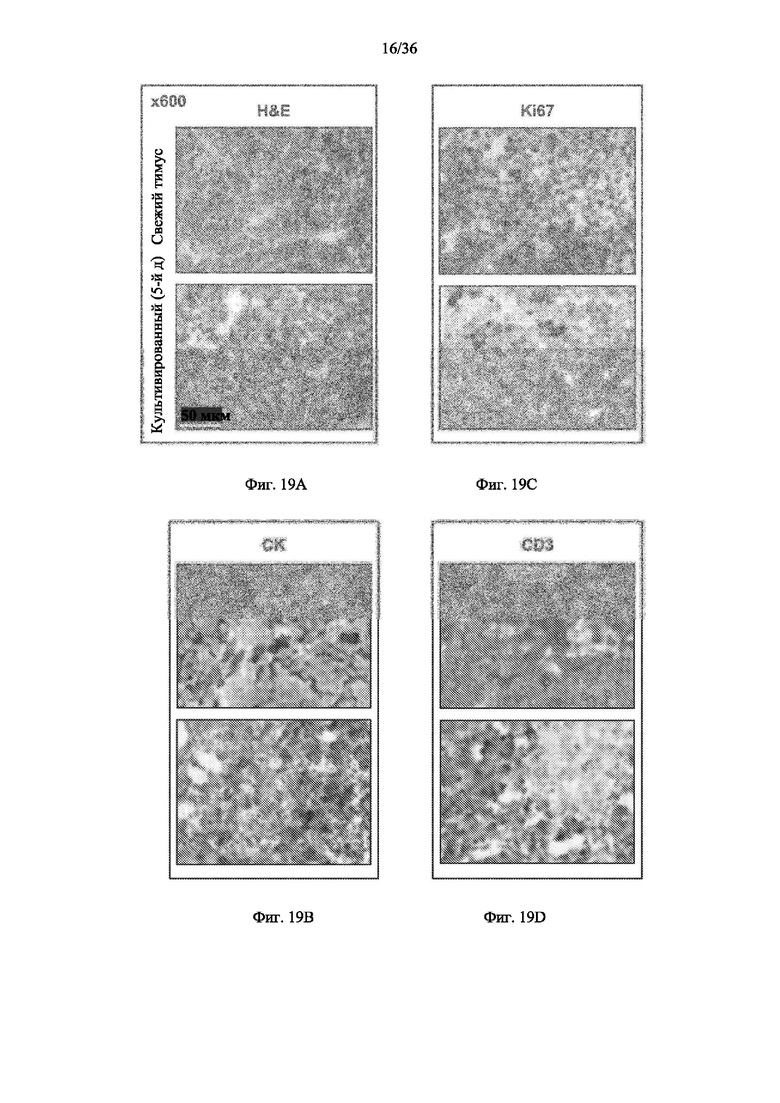
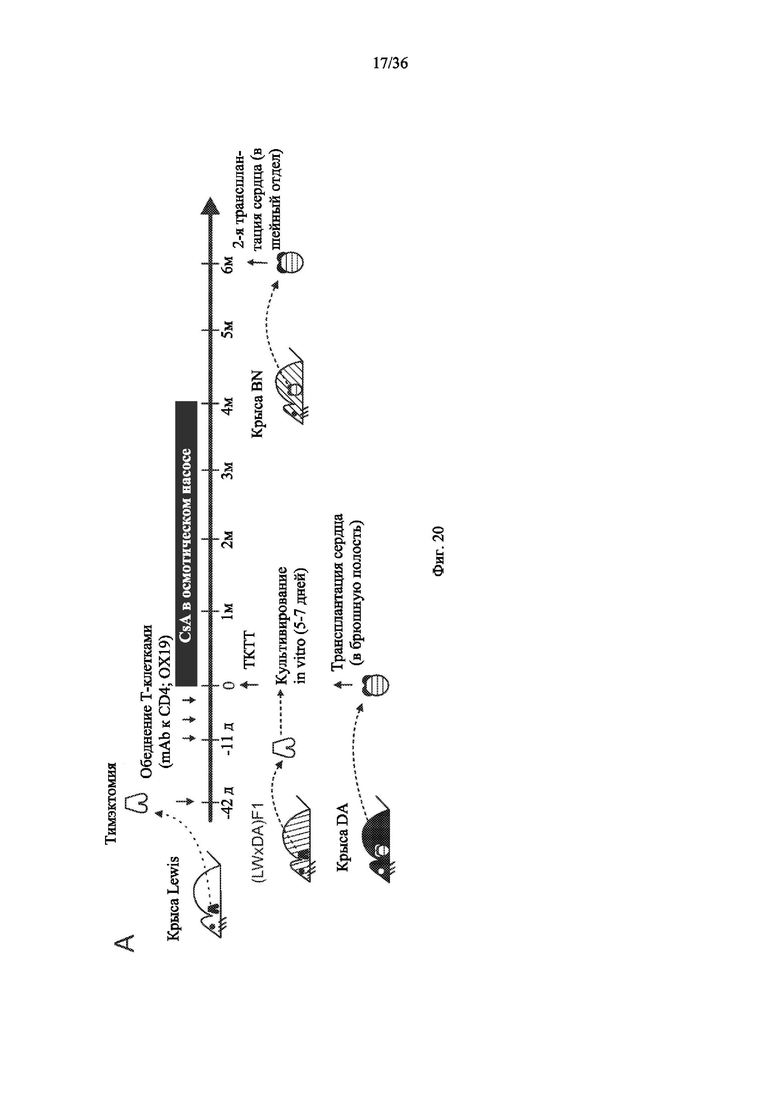
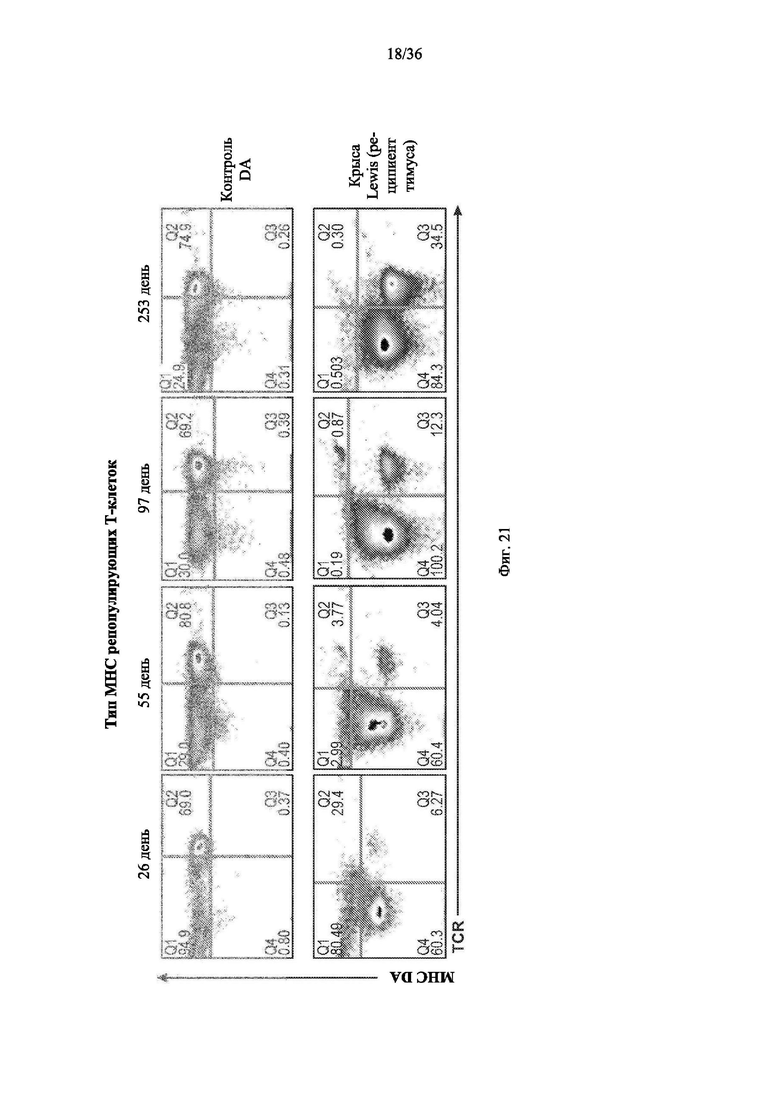
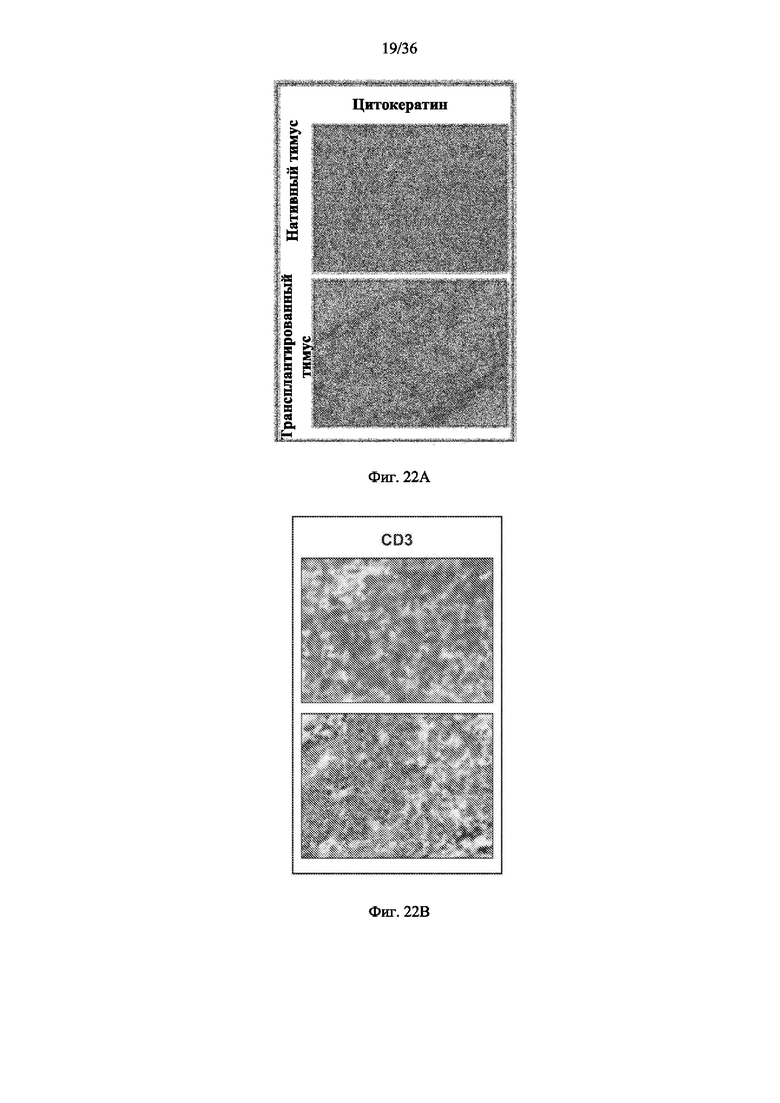
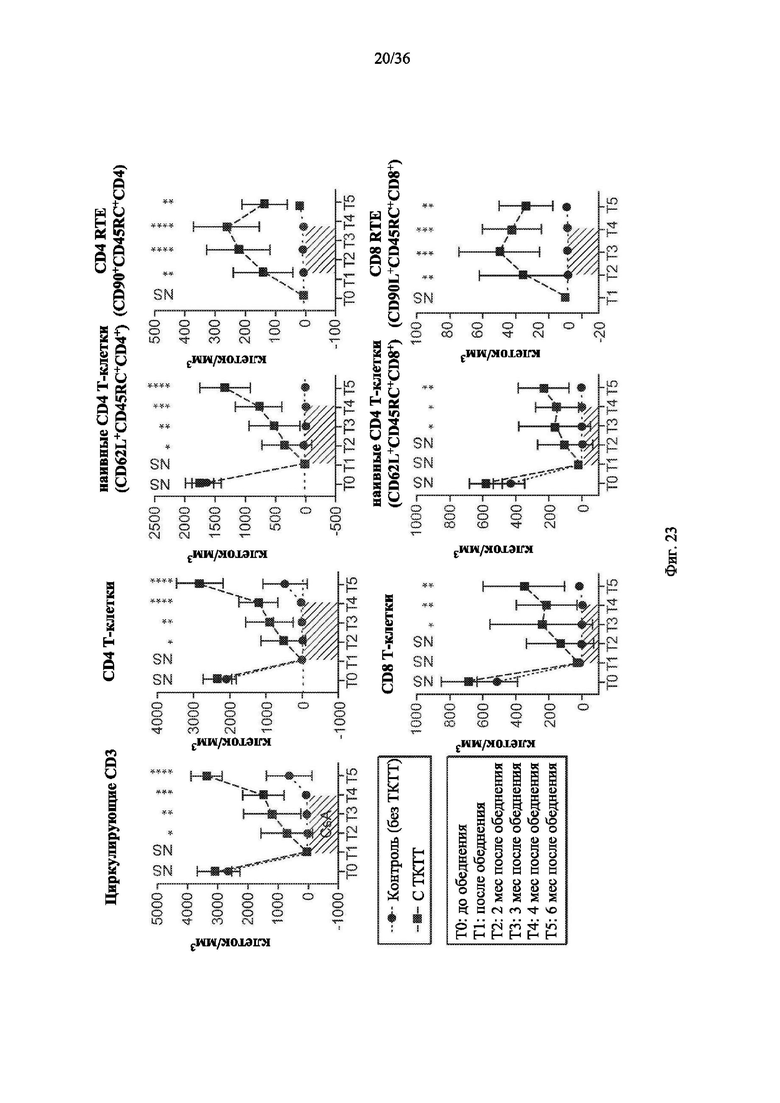
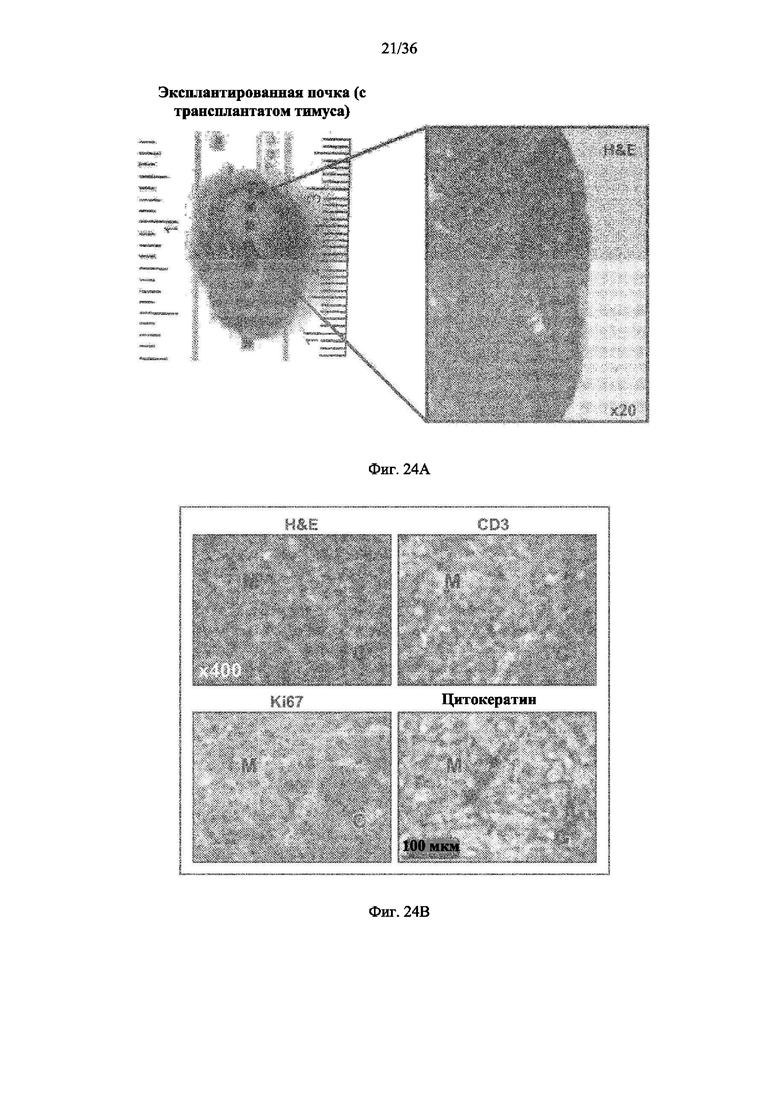
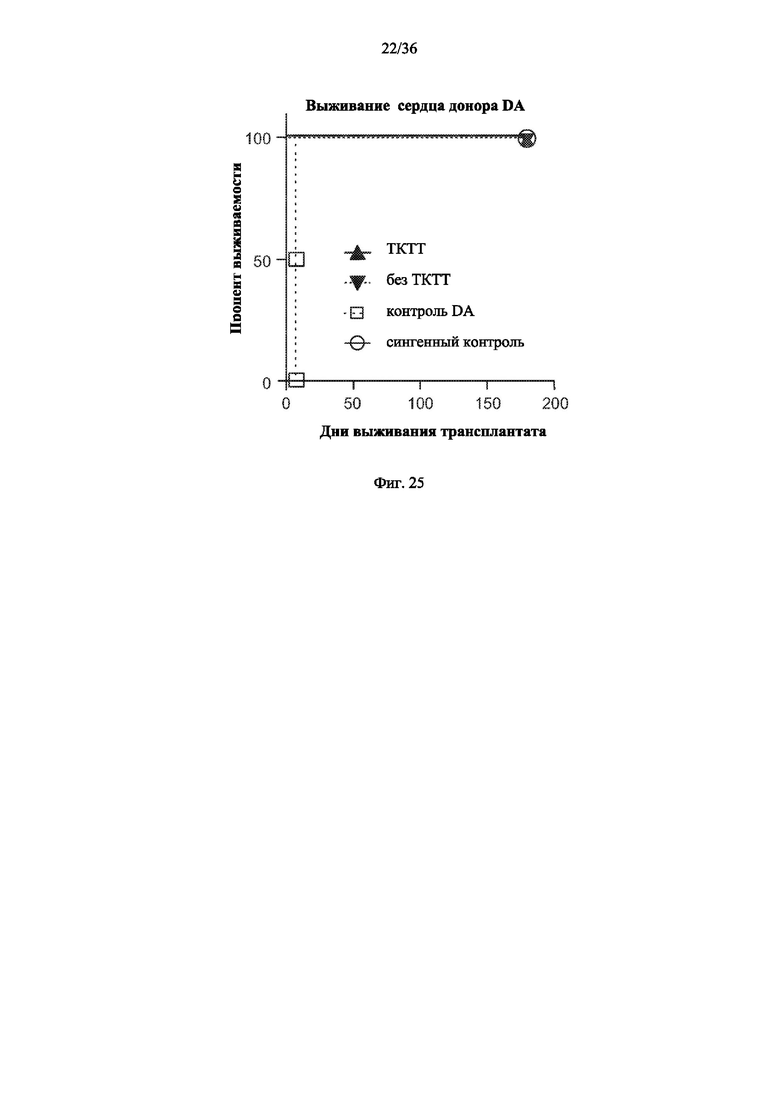
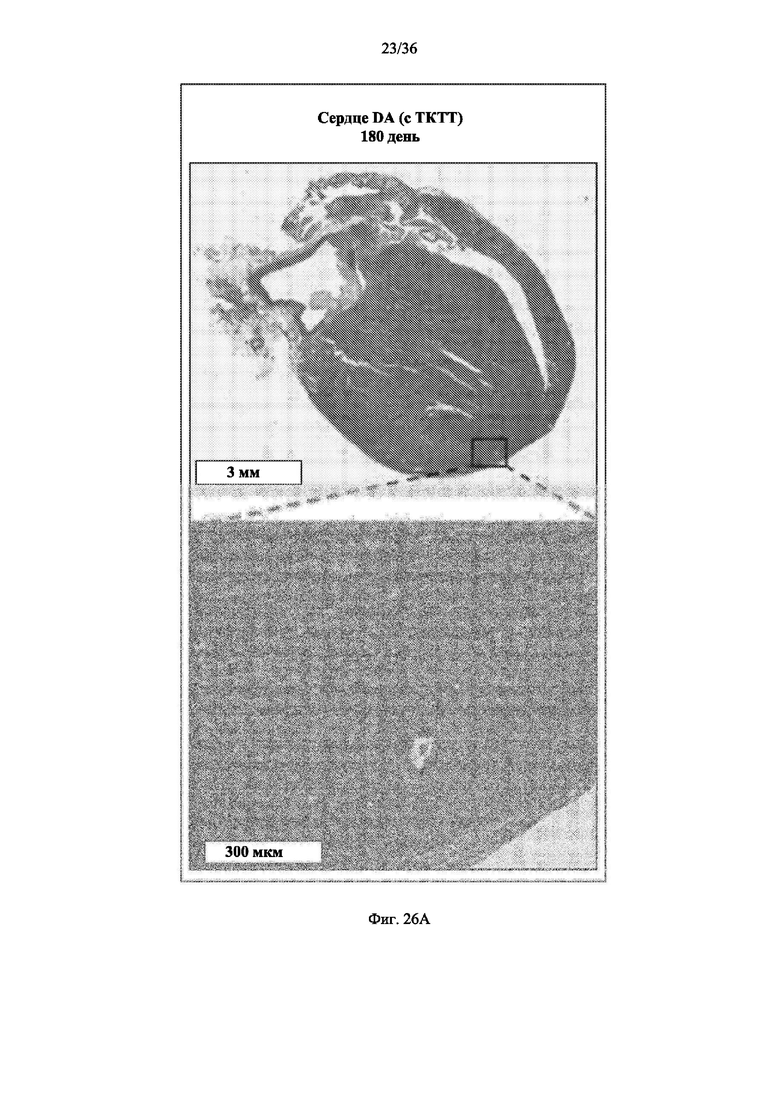

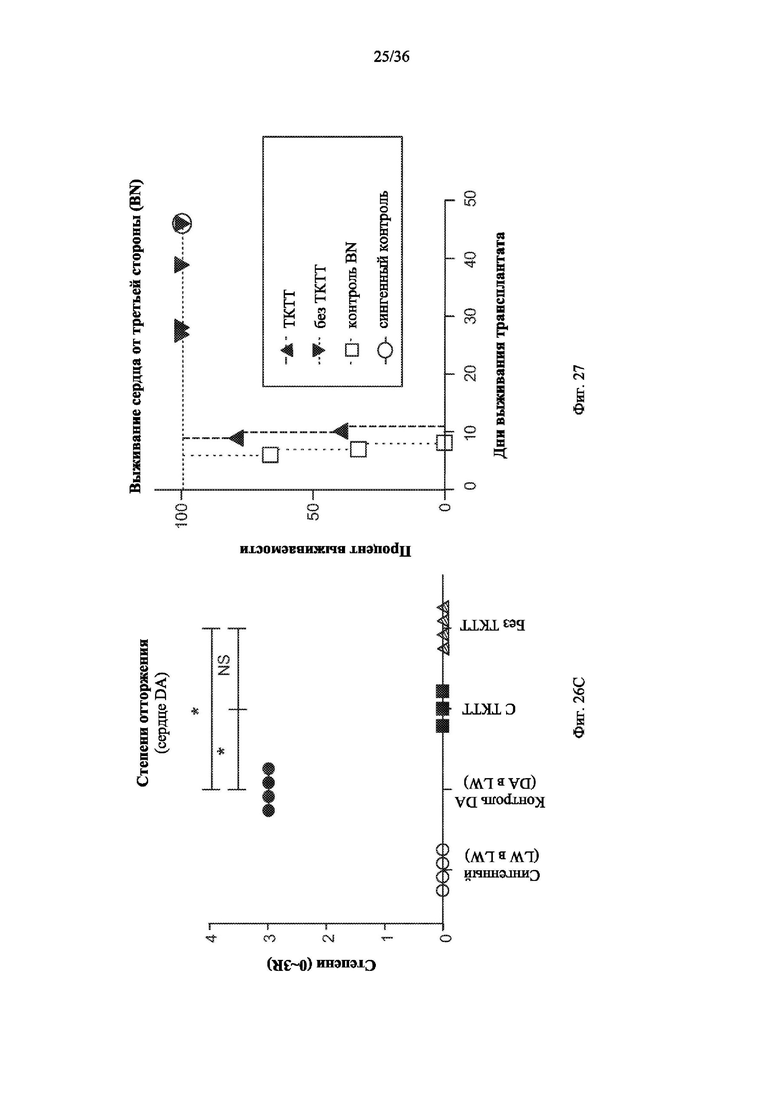
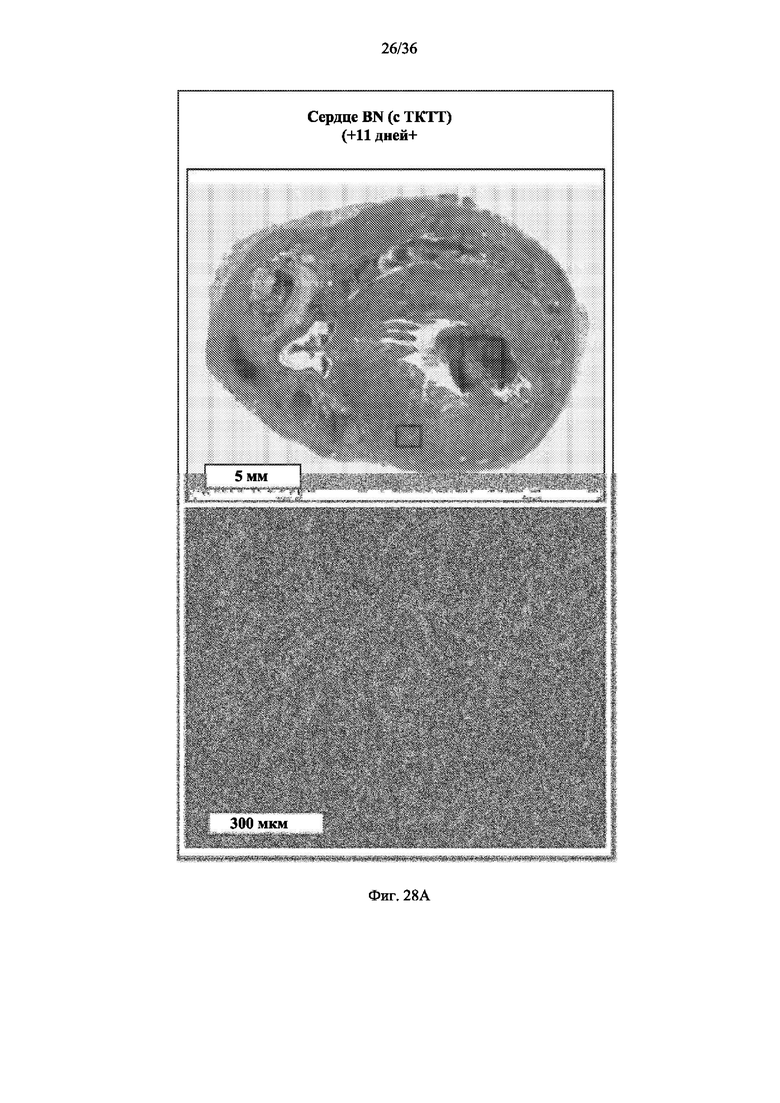
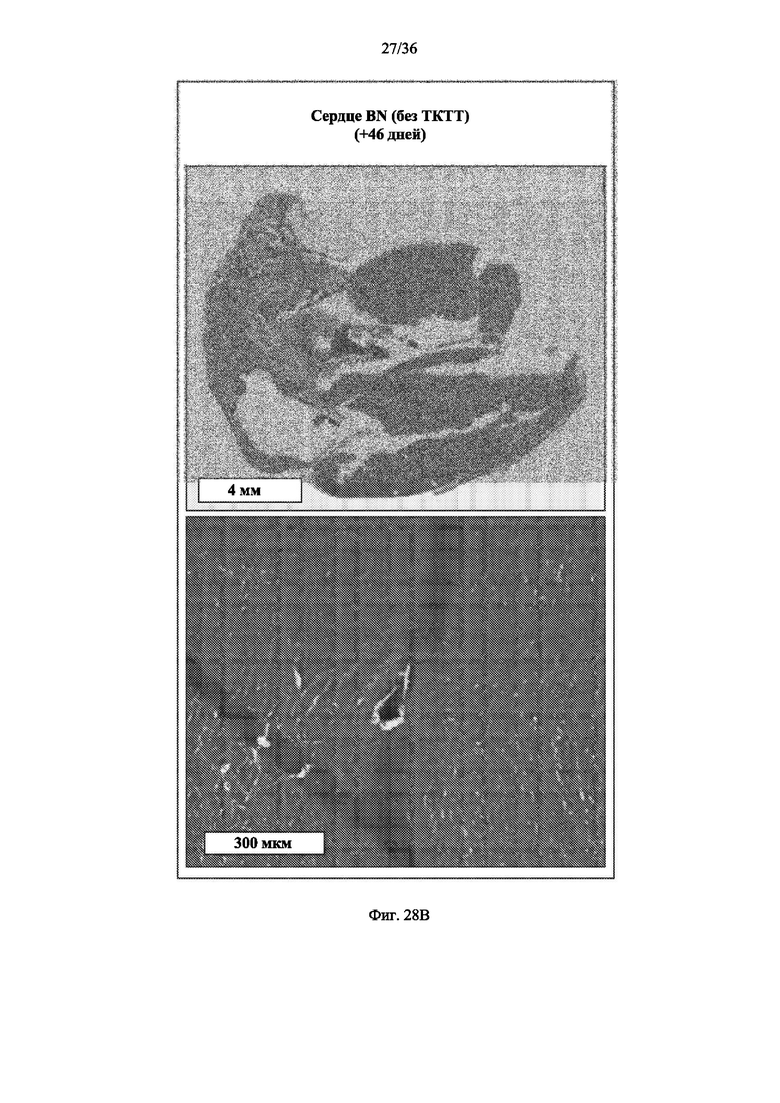
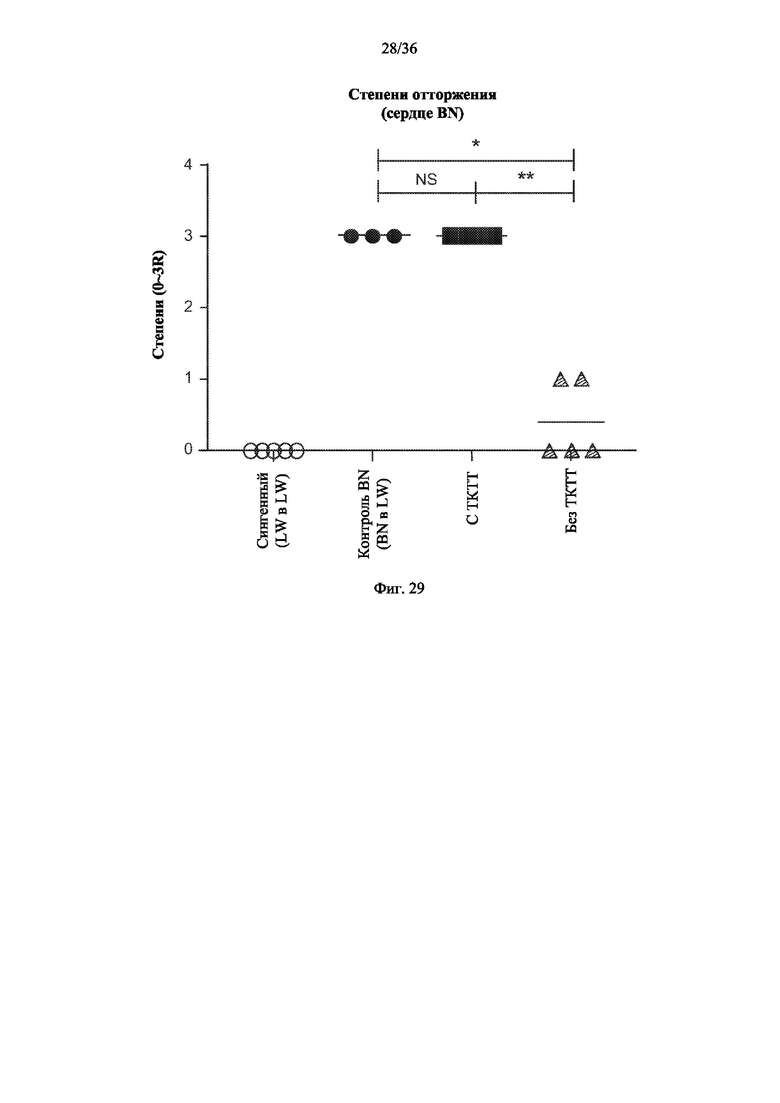

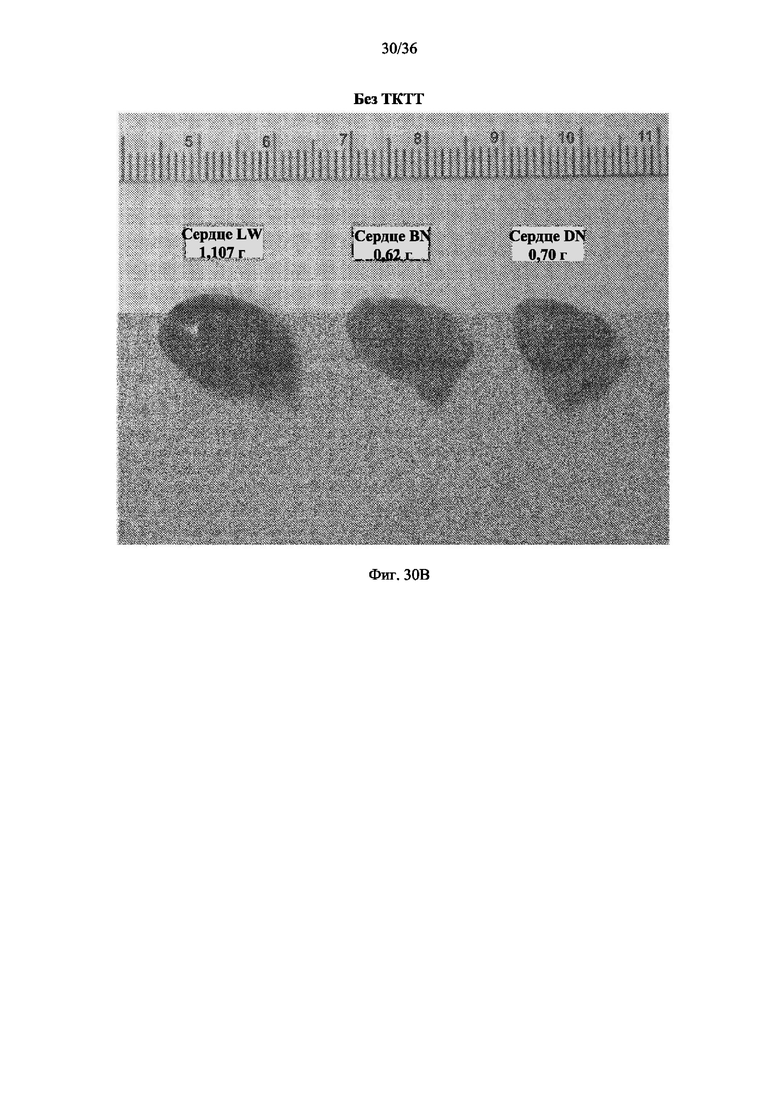
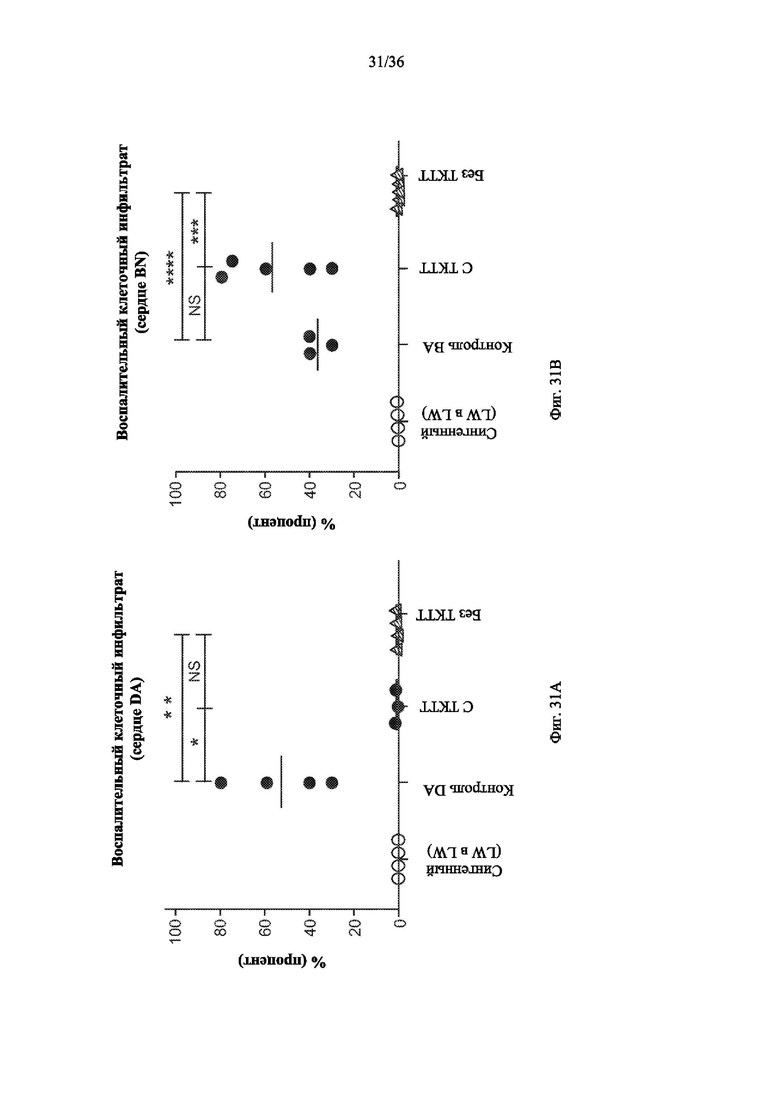
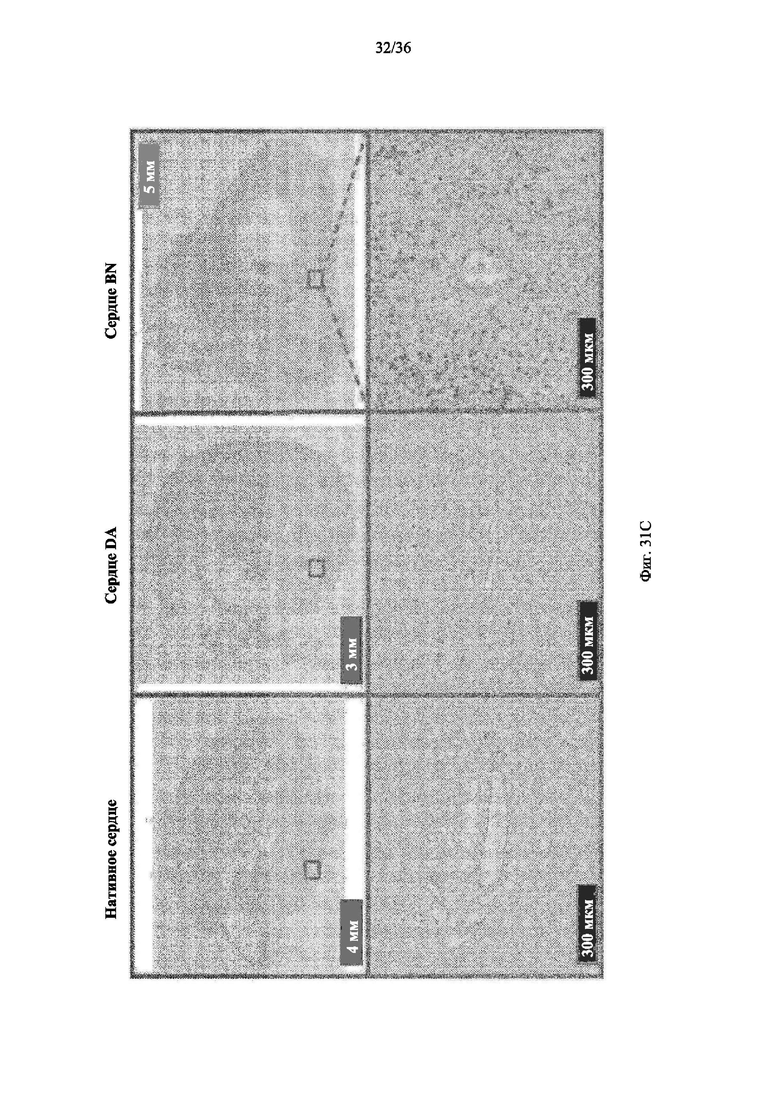

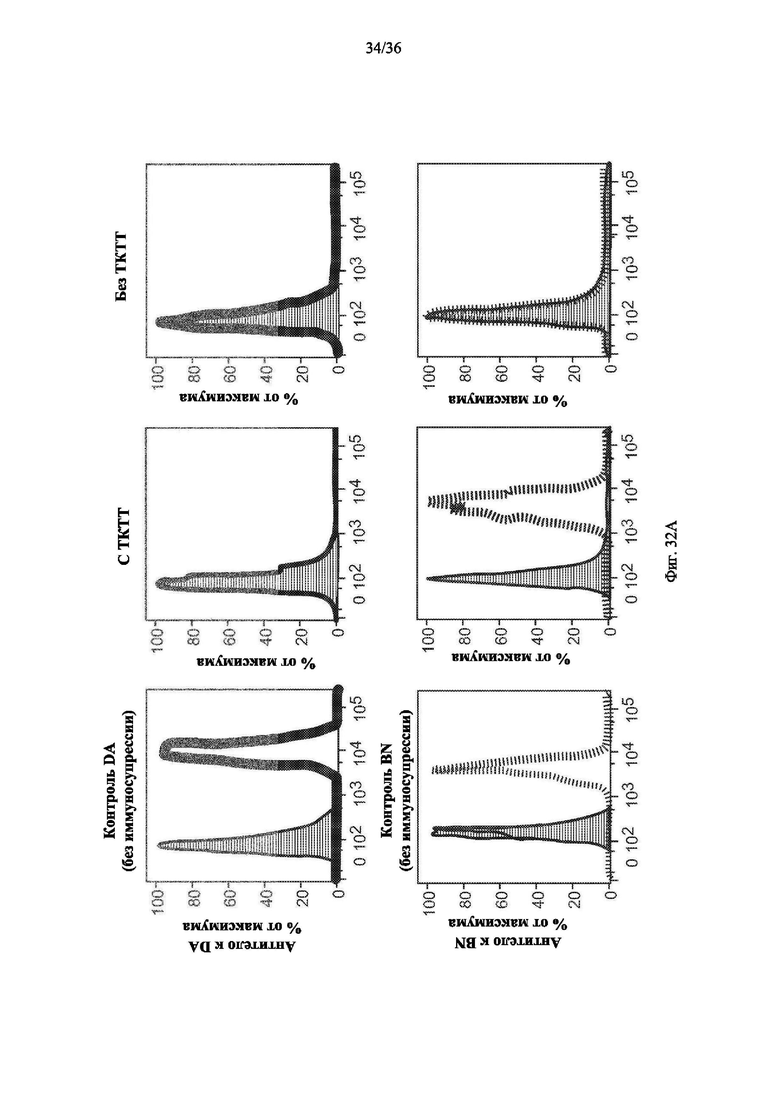
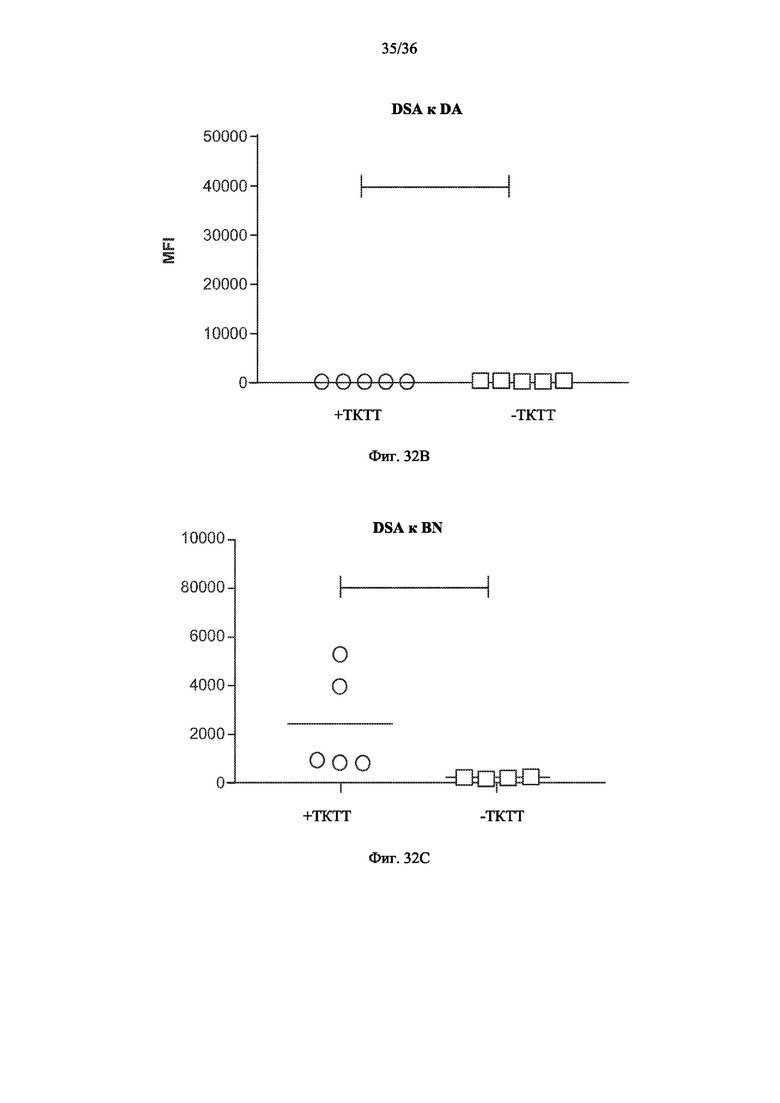

Группа изобретений относится к стимуляции донор-специфической толерантности к аллогенному трансплантату цельного органа, полученному от донора, у реципиента, нуждающегося в трансплантации цельного органа. Способ стимуляции донор-специфической толерантности к аллогенному трансплантату цельного органа, полученному от донора, у реципиента, нуждающегося в трансплантации цельного органа, где указанный цельный орган представляет собой сердце, почку, печень, легкое, поджелудочную железу, тонкую или толстую кишку или их комбинацию, где способ включает следующие стадии: (a) удаление тимуса у реципиента; (b) применение к указанному реципиенту схемы индукции иммуносупрессии, включающей один или более иммуносупрессивных препаратов, для истощения Т-клеток указанного реципиента и/или для подавления способности Т-клеток указанного реципиента отторгать трансплантированный цельный орган; (c) обеспечение как подходящего цельного органа человека, так и тимуса от донора; (d) трансплантацию цельного органа человека указанному реципиенту; (e) применение к указанному реципиенту схемы поддержания иммуносупрессии; (f) обеспечение продукта, полученного из аллогенной культивированной ткани постнатального тимуса, где указанный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, получен посредством: обеспечения подходящей ткани тимуса указанного донора цельного органа, полученного на стадии (c), обработки ткани тимуса указанного донора цельного органа асептическим образом с получением срезов ткани тимуса донора, подвергания указанных срезов ткани тимуса донора режиму кондиционирования на период до 21 дня посредством культивирования ткани тимуса донора в органной среде для тимуса с получением частично обедненных Т-клетками срезов ткани тимуса донора; где частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию на цитокератин (CK), наличие по меньшей мере одного тельца Гассаля и наличие интактных ядер эпителиальных клеток тимуса и других стромальных клеток в указанных частично обедненных Т-клетками срезах ткани тимуса донора; и (g) имплантацию продукта, полученного из аллогенной культивированной ткани постнатального тимуса, указанному реципиенту по истечении от 12 до 21 дня режима кондиционирования, при этом дозировка частично обедненных Т-клетками срезов ткани тимуса составляет 1000-20000 мм2 +/- 10% площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у указанного реципиента. Применение продукта, полученного из аллогенной культивированной ткани постнатального тимуса, для имплантации субъекту, подвергаемому трансплантации цельного органа для стимуляции донор-специфической толерантности, где указанный цельный орган представляет собой сердце, почку, печень, легкое, поджелудочную железу, тонкую или толстую кишку или их комбинацию и где указанный продукт получен путем: получения подходящей ткани тимуса от донора, где донорскую ткань тимуса подвергают режиму кондиционирования на период до 21 дня; причем режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов донорской ткани тимуса; где указанные частично обедненные Т-клетками срезы донорской ткани тимуса демонстрируют, между 5-м и 9-м днем режима кондиционирования, области, положительные по окрашиванию на CK, наличие по меньшей мере одного тельца Гассаля и наличие интактных ядер эпителиальных клеток тимуса и других стромальных клеток в указанных частично обедненных Т-клетками срезах ткани тимуса донора; и извлечение частично обедненных Т-клетками срезов донорской ткани тимуса в качестве продукта, полученного из аллогенной культивированной ткани постнатального тимуса. Вышеописанный способ и применение эффективно стимулируют донор-специфическую толерантность к аллогенному трансплантату цельного органа, полученному от донора, у реципиента, нуждающегося в трансплантации цельного органа, эффективно уменьшают отторжение трансплантата при трансплантации цельных органов, сохраняют жизнеспособность органов до и во время процедуры имплантации. 2 н. и 69 з.п. ф-лы, 33 ил., 9 табл., 5 пр.
1. Способ стимуляции донор-специфической толерантности к аллогенному трансплантату цельного органа, полученному от донора, у реципиента, нуждающегося в трансплантации цельного органа, где указанный цельный орган представляет собой сердце, почку, печень, легкое, поджелудочную железу, тонкую или толстую кишку или их комбинацию, где способ включает следующие стадии:
(a) удаление тимуса у реципиента;
(b) применение к указанному реципиенту схемы индукции иммуносупрессии, включающей один или более иммуносупрессивных препаратов, для истощения Т-клеток указанного реципиента и/или для подавления способности Т-клеток указанного реципиента отторгать трансплантированный цельный орган;
(c) обеспечение как подходящего цельного органа человека, так и тимуса от донора;
(d) трансплантацию цельного органа человека указанному реципиенту;
(e) применение к указанному реципиенту схемы поддержания иммуносупрессии;
(f) обеспечение продукта, полученного из аллогенной культивированной ткани постнатального тимуса, где указанный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, получен посредством: обеспечения подходящей ткани тимуса указанного донора цельного органа, полученного на стадии c), обработки ткани тимуса указанного донора цельного органа асептическим образом с получением срезов ткани тимуса донора, подвергания указанных срезов ткани тимуса донора режиму кондиционирования на период до 21 дня посредством культивирования ткани тимуса донора в органной среде для тимуса с получением частично обедненных Т-клетками срезов ткани тимуса донора; где частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию на цитокератин (CK), наличие по меньшей мере одного тельца Гассаля, и наличие интактных ядер эпителиальных клеток тимуса и других стромальных клеток в указанных частично обедненных Т-клетками срезах ткани тимуса донора; и
(g) имплантацию продукта, полученного из аллогенной культивированной ткани постнатального тимуса, указанному реципиенту по истечении от 12 до 21 дня режима кондиционирования, при этом дозировка частично обедненных Т-клетками срезов ткани тимуса составляет 1000-20000 мм2 +/- 10% площади поверхности ткани тимуса на площадь поверхности тела реципиента в м2, и дополнительно где имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз и толерантность у указанного реципиента.
2. Способ по п. 1, согласно которому удаление тимуса указанного реципиента осуществляют хирургическим путем.
3. Способ по п. 2, согласно которому удаление тимуса указанного реципиента осуществляют с помощью роботизированной хирургии.
4. Способ по п. 2, согласно которому удаление тимуса указанного реципиента осуществляют с помощью торакоскопической хирургии.
5. Способ по п. 1, дополнительно включающий стадию криоконсервации мононуклеарных клеток периферической крови от донора для использования в будущем в реакции смешанной культуры лимфоцитов для демонстрации клеточной толерантности.
6. Способ по п. 5, согласно которому реакцию смешанной культуры лимфоцитов для демонстрации клеточной толерантности проводят с использованием мононуклеарных клеток периферической крови от указанного реципиента и криоконсервированных мононуклеарных клеток периферической крови от донора после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса, в соответствии со стадией (g).
7. Способ по п. 6, согласно которому реакцию смешанной культуры лимфоцитов для демонстрации клеточной толерантности проводят с мононуклеарными клетками периферической крови от реципиента и криоконсервированными мононуклеарными клетками периферической крови от донора приблизительно через 6-12 месяцев после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
8. Способ по п. 7, согласно которому реакцию смешанной культуры лимфоцитов для демонстрации клеточной толерантности проводят с мононуклеарными клетками периферической крови от реципиента и криоконсервированными мононуклеарными клетками периферической крови от донора после того, как количество наивных Т-клеток достигает 10% от общего количества Т-клеток у реципиента.
9. Способ по п. 1, согласно которому имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, индуцирует тимопоэз у указанного субъекта в течение 12 месяцев после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
10. Способ по п. 1, где частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию на цитокератин 14 (CK 14).
11. Способ по п. 1, согласно которому гуморальную толерантность определяют по развитию гуморального иммунитета и отсутствию донор-специфических антител к главному комплексу гистосовместимости донора.
12. Способ по п. 1, согласно которому указанная схема индукции иммуносупрессии включает индукционный иммуносупрессивный препарат, выбранный из группы, состоящей из глюкокортикоида, кроличьего антитимоцитарного глобулина, лошадиного антитимоцитарного глобулина и алемтузумаба.
13. Способ по п. 1, согласно которому схема поддержания иммуносупрессии включает введение глюкокортикоида.
14. Способ по п. 13, согласно которому глюкокортикоид включает метилпреднизолона натрия сукцинат.
15. Способ по п. 14, согласно которому метилпреднизолона натрия сукцинат вводят внутривенно в дозе не более 4 мг/кг/сут после имплантации продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
16. Способ по п. 1, согласно которому схема поддержания иммуносупрессии включает введение глюкокортикоида с такролимусом или циклоспорином и дополнительное введение мофетила микофенолата, эквивалента мофетила микофенолата или азатроприна.
17. Способ по п. 1, согласно которому указанный цельный орган представляет собой часть целого органа.
18. Способ по п. 1, согласно которому указанный трансплантат цельного органа представляет собой трансплантат сердца.
19. Способ по п. 18, согласно которому трансплантат сердца представляет собой трансплантат сердца ребенка.
20. Способ по п. 18, согласно которому трансплантат сердца представляет собой трансплантат сердца взрослого.
21. Способ по п. 1, дополнительно включающий оценку реципиента на индекс панель-реактивных антител («PRA») HLA I класса или HLA II класса до трансплантации цельного органа.
22. Способ по п. 1, согласно которому у реципиентов с HLA-антителами проводят перекрестную пробу на совместимость с потенциальными донорами.
23. Способ по п. 22, согласно которому у реципиентов с HLA-антителами проводят виртуальную перекрестную пробу на совместимость с помощью UNET.
24. Способ по п. 21, согласно которому, если зарегистрирован индекс PRA > 20% в виртуальной перекрестной пробе на совместимость, способ дополнительно включает стадию проведения плазмафереза в операционной во время трансплантации цельного органа реципиенту.
25. Способ по п. 21, согласно которому, если зарегистрирован индекс PRA > 70% в виртуальной перекрестной пробе на совместимость, способ дополнительно включает стадию фактического проведения перекрестной пробы на совместимость потенциального донора и проведение плазмафереза в операционной во время трансплантации цельного органа реципиенту.
26. Способ по п. 1, согласно которому указанный цельный орган является несовпадающим по HLA.
27. Способ по п. 26, согласно которому несовпадение по HLA определяют путем типирования аллелей HLA HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DRB3, HLA-DRB4, HLA-DRB5, HLA-DQA1, HLA- DPB1, HLA-DPA1 у донора и реципиента.
28. Способ по п. 27, согласно которому по меньшей мере один из аллелей HLA HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1, HLA-DRB3, HLA-DRB4, HLA-DRB5, HLA-DQA1, HLA- DPB1, HLA-DPA1 отличается у донора и реципиента.
29. Способ по п. 1, согласно которому часть указанного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, хирургическим путем имплантируют в четырехглавую мышцу бедра реципиента.
30. Способ по п. 29, согласно которому оставшуюся часть указанного продукта, полученного из аллогенной культивированной ткани постнатального тимуса, подвергают криоконсервации в жидком азоте для будущей трансплантации реципиенту.
31. Способ по п. 1, согласно которому режим кондиционирования осуществляют в течение периода от приблизительно 12 дней до приблизительно 21 дня.
32. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 12 дней.
33. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 13 дней.
34. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 14 дней.
35. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 15 дней.
36. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 16 дней.
37. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 17 дней.
38. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 18 дней.
39. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 19 дней.
40. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 20 дней.
41. Способ по п. 31, согласно которому период кондиционирования составляет приблизительно 21 день.
42. Способ по п. 12, согласно которому схема индукции иммуносупрессии включает антитимоцитарный глобулин кроличьего происхождения.
43. Способ по п. 42, согласно которому антитимоцитарный глобулин кроличьего происхождения вводят внутривенно в дозе приблизительно 1,5 мг/кг/сут в течение приблизительно от 3 до 7 дней.
44. Способ по п. 43, согласно которому антитимоцитарный глобулин вводят ежедневно в течение 3-14 дней в дозе приблизительно 15 мг/кг/сут путем внутривенного введения.
45. Способ по п. 12, согласно которому схема индукции иммуносупрессии включает алемтузумаб.
46. Способ по п. 45, согласно которому алемтузумаб вводят в дозе приблизительно 0,25 мг/кг в течение 4 дней внутривенно реципиентам с массой тела менее 35 кг.
47. Способ по п. 45, согласно которому алемтузумаб вводят в дозе приблизительно от 3 до 20 мг в течение 4 дней внутривенно реципиентам с массой тела более 35 кг.
48. Способ по п. 1, согласно которому схема поддержания иммуносупрессии включает один или более иммуносупрессивных препаратов, выбранных из группы, состоящей из ингибитора кальциневрина и ингибитора инозинмонофосфат дегидрогеназы и азатиоприна.
49. Способ по п. 48, согласно которому иммуносупрессивный препарат представляет собой ингибитор кальциневрина.
50. Способ по п. 48, согласно которому иммуносупрессивный препарат представляет собой ингибитор инозинмонофосфат дегидрогеназы.
51. Способ по п. 50, согласно которому ингибитор инозинмонофосфат дегидрогеназы представляет собой мофетила микофенолат.
52. Способ по п. 51, согласно которому мофетила микофенолат вводят перорально или внутривенно.
53. Способ по п. 52, согласно которому мофетила микофенолат вводят в дозе от приблизительно 15 до приблизительно 25 мг/кг два-три раза в сутки.
54. Способ по п. 48, согласно которому ингибитор инозинмонофосфат дегидрогеназы представляет собой микофеноловую кислоту.
55. Способ по п. 54, согласно которому микофеноловую кислоту вводят в дозе от приблизительно 25 до приблизительно 50 мг/кг в 2 или 3 дозах в сутки.
56. Способ по п. 1, согласно которому схема поддержания иммуносупрессии дополнительно включает глюкокортикоид, выбранный из группы, состоящей из метилпреднизолона, преднизона и преднизолона.
57. Способ по п. 56, согласно которому глюкокортикоид вводят в постепенно снижающейся дозировке, и дозу поддерживают на уровне 4 мг/кг/сут или ниже.
58. Способ по п. 48, согласно которому ингибитор кальциневрина представляет собой такролимус.
59. Способ по п. 48, согласно которому ингибитор кальциневрина представляет собой циклоспорин А.
60. Способ по п. 1, согласно которому введение одного или более иммуносупрессивных препаратов схемы поддержания иммуносупрессии постепенно прекращают после того, как количество наивных Т-клеток достигает 10% от общего количества Т-клеток.
61. Способ по п. 1, согласно которому имплантированный продукт, полученный из аллогенной культивированной ткани постнатального тимуса, подвергают биопсии через 2-12 месяцев после имплантации для оценки признаков тимопоэза с помощью иммунохимии.
62. Способ по любому из пп. 1-61, причем частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию на цитокератин (CK), имеющие кружевовидный рисунок.
63. Способ по любому из пп. 10-61 или 62, причем частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию цитокератина 14 (CK 14), имеющие кружевовидный рисунок.
64. Способ по любому из пп. 1-61, 62 или 63, отличающийся тем, что указанный трансплантат цельного органа получен от умершего донора.
65. Способ по любому из пп. 1-17, 21-61, 62 или 63, отличающийся тем, что указанный трансплантат цельного органа получен от живого донора.
66. Применение продукта, полученного из аллогенной культивированной ткани постнатального тимуса, для имплантации субъекту, подвергаемому трансплантации цельного органа для стимуляции донор-специфической толерантности, где указанный цельный орган представляет собой сердце, почку, печень, легкое, поджелудочную железу, тонкую или толстую кишку или их комбинацию и где указанный продукт получен путем:
получения подходящей ткани тимуса от донора, где донорскую ткань тимуса подвергают режиму кондиционирования на период до 21 дня; причем режим кондиционирования для донорской ткани тимуса включает обработку донорской ткани тимуса асептическим образом в органной среде для тимуса с получением частично обедненных Т-клетками срезов донорской ткани тимуса; где указанные частично обедненные Т-клетками срезы донорской ткани тимуса демонстрируют, между 5-м и 9-м днем режима кондиционирования, области, положительные по окрашиванию на CK, наличие по меньшей мере одного тельца Гассаля, и наличие интактных ядер эпителиальных клеток тимуса и других стромальных клеток в указанных частично обедненных Т-клетками срезах ткани тимуса донора; и
извлечение частично обедненных Т-клетками срезов донорской ткани тимуса в качестве продукта, полученного из аллогенной культивированной ткани постнатального тимуса.
67. Применение по п. 66, причем частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию на цитокератин 14 (CK 14).
68. Применение по п. 66 или 67, отличающееся тем, что частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют между 5-м и 9-м днем режима кондиционирования области, положительные по окрашиванию на цитокератин (CK), имеющие кружевовидный рисунок.
69. Применение по п. 67 или 68, причем частично обедненные Т-клетками срезы ткани тимуса донора демонстрируют в период с 5 по 9 день режима кондиционирования области, положительные по окрашиванию на цитокератин 14 (CK 14), имеющие кружевовидный рисунок.
70. Применение по любому из пп. 66, 67, 68 или 69, отличающееся тем, что указанный трансплантат цельного органа получен от умершего донора.
71. Применение по любому из пп. 66, 67, 68 или 69, отличающееся тем, что указанный трансплантат цельного органа получен от живого донора.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| LI В | |||
| et al | |||
| Thymic microenvironment reconstitution after postnatal human thymus transplantation// Clinical Immunology, (2011), vol | |||
| Способ закалки пил | 1915 |
|
SU140A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Нагревательный прибор для центрального отопления | 1920 |
|
SU244A1 |
| MARKERT M.L | |||
| et al | |||
| Factors affecting success of thymus transplantation for complete DiGeorge anomaly, American Journal of | |||
Авторы
Даты
2024-12-04—Публикация
2019-02-22—Подача