Область техники, к которой относится изобретение
Настоящее изобретение касается фармацевтических композиций с выделенными и обработанными клетками цельной крови или мононуклеарными клетками периферической крови (PBMC), а также указанных фармацевтических композиций для применения при профилактике и/или лечении отторжения твердых органов или клеточных трансплантатов у людей-реципиентов при трансплантации.
Уровень техники
Вследствие различных заболеваний или несчастных случаев либо по многим другим причинам больные и раненые люди нуждаются в замене своих органов путем трансплантации органов. Согласно Глобальной обсерватории по донорству и трансплантации (http://www.transplant-observatory.org/), в 2016 году во всем мире было проведено 135860 пересадок органов. Однако количество пациентов, которые в этом нуждаются и в настоящее время находятся в списке ожидающих, гораздо больше. Помимо сравнительно небольшого числа доноров органов, донорские органы и реципиенты также должны быть совместимыми, чтобы уменьшить риск отторжения иммунной системой реципиента и тем самым повысить вероятность приживления и сроки функционирования пересаженных органов.
Иммунная система млекопитающих, в частности человека, должна различать и распознавать «свое» и «чужое», а также бороться со всевозможным «чужим» материалом, который может нанести вред организму. Наряду с распознаванием клеток или других частей типа нуклеиновых кислот, происходящих из чужеродных организмов, например, из бактерий или вирусов, иммунная система также распознает (и должна распознавать) клетки или другие части чужеродных организмов, принадлежащих к тому же биологическому виду. Этот аспект является одним из главных недостатков при медицинской трансплантации органов или клеток, так как обычно иммунная система реципиента распознает пересаженный орган или клетки как чужие и атакует и разрушает пересаженный орган или клетки. Этот естественный защитный механизм организма млекопитающих, в частности человека, является одной из основных причин неудачных трансплантаций или убывающей функциональности пересаженного органа со временем. Чтобы уменьшить риск для пациента, опосредованный способностью иммунной системы распознавать и атаковать трансплантаты, обычно подбирают донора и реципиента с близкими клеточными профилями, служащими отличительной чертой «своего» и «чужого». Такая совместимость донора и реципиента часто, но не обязательно, достигается у близких родственников.
Однако, поскольку указанные клеточные профили все-таки различаются даже у ближайших родственников, то их соответствия недостаточно, чтобы предотвратить иммунную реакцию против трансплантата. Поэтому необходимо, и это стандартный подход, еще больше подавить иммунную систему реципиента, чтобы сильно уменьшить риск иммунной реакции против трансплантата.
Обычно при этом иммунную систему широко и неспецифическим образом подавляют для того, чтобы трансплантат не подвергался атаке со стороны иммунной системы и смог прижиться и функционировать в течение длительного времени в организме реципиента, а также для того, чтобы избежать чрезмерных и опасных воспалительных реакций у пациента.
На современном уровне подобное лечение пациентов после трансплантации представляет собой одновременный прием целого ряда препаратов, которые неспецифическим образом ослабляют иммунную систему пациента. Например, текущая общепринятая терапия при пересадке почек - это множественная иммуносупрессия, включающая антительную индукционную терапию, применение ингибиторов кальцинейрина (например, циклоспорина A, Sandimmun®), ингибиторов пролиферации клеток (например, микофеноловой кислоты, производных MPA) и кортикостероидов (Ekberg H et al., NEJM 2007).
Таким образом, реципиенты трансплантатов обычно зависят от иммуносупрессии всю оставшуюся жизнь. Одним из главных недостатков такого лечения, как описано выше, является подавление всей иммунной системы как таковой. При этом действие иммунной системы реципиента подавляется и в отношении всех других чужеродных организмов, клеток или иных субстанций. Следовательно, реципиенты подвергаются высокому риску инфекционных заболеваний. Кроме того, побочные эффекты подавления иммунной системы, в частности, включают нарушение заживления ран, повышение риска раковых заболеваний и значительное повышение риска сердечно-сосудистых заболеваний (Morath C et al., JASN 2004, Opelz G et al., AJT 2013).
Более того, другой проблемой при иммуносупрессии у реципиентов при трансплантации является ее “ограниченная” эффективность: известно, что, несмотря на длительную интенсивную иммуносупрессию, более половины пациентов страдают хроническим отторжением и долгосрочной потерей трансплантата (Sellares J et al., AJT 2012).
На сегодняшний день реципиенты трансплантатов «привязаны» к иммуносупрессии на всю жизнь со всеми ее недостатками и с риском того, что все-таки может произойти хроническое отторжение.
Сущность изобретения
Основной задачей настоящего изобретения является обеспечение улучшенной профилактики и/или лечения отторжения органов или клеточных трансплантатов у реципиентов при трансплантации, с помощью которых преодолеваются или по меньшей мере уменьшаются недостатки существующих подходов к предотвращению отторжения.
Основная задача настоящего изобретения решается при помощи фармацевтических композиций, включающих или состоящих из:
a) выделенных клеток цельной крови и/или мононуклеарных клеток периферической крови (PBMC), обработанных терапевтически эффективным количеством активного вещества, и
b) необязательно, фармацевтически приемлемого носителя,
для применения при профилактике и/или лечении отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком, причем указанные клетки цельной крови или PBMC выделены или происходят из организма донора трансплантата,
при этом профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту фармацевтической композиции, причем количество фармацевтической композиции выбрано таким образом, чтобы ввести, по меньшей мере, 0,25×106 клеток, предпочтительно, по меньшей мере, 1,5×106 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, предпочтительно за одну процедуру введения,
причем активное вещество включает или представляет собой одно или несколько веществ, выбранных из группы, содержащей химиотерапевтические средства, ингибиторы протеасом, иммунодепрессанты и антипролиферативные вещества.
Разрабатываемая альтернатива неспецифической иммуносупрессии должна быть лечебной, а не симптоматической терапией. Задача состоит в том, чтобы повлиять на иммунную систему таким образом, чтобы она все еще могла служить защитой от бактерий, вирусов, раковых клеток и т.д., но в то же время можно было специально отключать нежелательные реакции со стороны иммунной системы, например, направленные против чужеродных донорских трансплантатов. При обработке клеток крови, скажем, моноцитов активными веществами, например, митомицином C (обработанные митомицином C мононуклеарные клетки периферической крови здесь обозначены как модифицированные иммунные клетки, сокращенно МИК), они превращаются не в стимулирующие, а, скорее, в супрессивные клетки, близкие супрессорным клеткам миелоидного происхождения (MDSC) раковых больных.
В заявке WO 2010/000730 раскрывается, что фармацевтическая композиция, содержащая выделенные клетки крови, обработанные терапевтически эффективным количеством химиотерапевтического средства, может применяться для обеспечения и достижения специализированной или целевой иммуносупрессии на фоне аутоиммунного заболевания. После вымывания активного вещества, если это происходит, МИК повторно вводятся в организм реципиента трансплантата. Таким образом, в заявке WO 2010/000730 подробно описывается конкретная терапия на модели рассеянного склероза у мышей (экспериментальная мышиная модель аутоиммунного энцефалита (EAE) с весьма специфическим режимом дозирования, применяемым на мышиной модели, в частности, на модели аутоиммунного EAE.
Стандартная процедура, которая использовалась ранее, заключается в применении иммунодепрессантов, вызывающих общее ослабление иммунной системы и связанные с этим побочные эффекты. В таком жестком лечении химическими иммунодепрессантами больше не будет необходимости благодаря настоящему изобретению, так как количество иммунодепрессантов можно снижать до минимума либо они вообще больше не потребуются пациентам, получающим фармацевтические композиции по изобретению.
Изобретение предполагает персонализированную, специфичную для пациента иммуносупрессию, которая направлена на причины отторжения и лишена побочных эффектов, тем самым значительно отличаясь от доступных в настоящее время методов лечения. Клеточная терапия может проводиться централизованно в стандартной форме по индивидуальным показаниям; а персонализация достигается за счет клеток донорской крови и нет необходимости в дорогостоящих приспособлениях. Разработанный способ легко вписывается в повседневную клиническую практику, так как в нем используются существующие структуры и больницам не нужно совершать дорогостоящие инвестиции в специальные лаборатории. Наконец, значительно снижаются затраты на лечение, так как больше не требуется или значительно сокращается пожизненный прием лекарств.
Лечение или предотвращение отторжения путем введения МИК обладает большей или по крайней мере эквивалентной эффективностью, в сравнении с золотым стандартом иммуносупрессии с помощью нескольких препаратов, при одновременном уменьшении побочных эффектов. Поэтому оно способно принести огромную пользу пациентам и имеет большие экономические перспективы.
Для обеспечения оптимизированной терапии исключительное значение имеет специальная схема лечения, в частности, особый режим дозирования. Иммунная система млекопитающих, в частности человека, строго регулируется, поэтому эффектом подавления иммунной системы будут обладать и низкие дозы вводимых обработанных клеток цельной крови или обработанных PBMC. Однако предполагается, что в этом случае потребуется больше времени для достижения и установления всеобъемлющего и длительного прицельного подавления иммунной системы. Таким образом, ожидается, что более высокие дозы обеспечат индивидуальную иммуносупрессию за более короткое время.
С другой стороны, повышение дозы также может достигнуть предела, так как при более высоких дозах возрастает риск, например, возникновения тромбоза или эмболии. Поскольку этих побочных эффектов обязательно следует избегать, то особое внимание необходимо уделять конкретному режиму дозирования. Однако следует отметить, что индивидуальное подавление иммунной системы обеспечивается при высоких дозах и поэтому при рассмотрении возможных вариантов лечения для людей-реципиентов трансплантатов этот фактор также следует учитывать.
Неожиданно оказалось, что при режиме дозирования обработанных клеток, как описано выше, составляющем, по меньшей мере, 0,25×106 клеток на кг массы тела реципиента, являющегося человеком, предпочтительно, по меньшей мере, 1,5×106 клеток на 1 кг массы тела, обнаруживаются стабильное функционирование трансплантата, выживаемость трансплантата и пациента и отсутствие отторжения или побочных эффектов, связанных с лечением (см. пример 1).
Термины “пациент”, “субъект”, “реципиент” или “реципиент трансплантата” в настоящем описании могут применяться взаимозаменяемо и означают пациента, нуждающегося в трансплантации органа или клеток, либо планирующего трансплантацию, а также пациента, которому уже сделана такая трансплантация, причем трансплантация могла произойти даже месяцы, годы или десятилетия назад.
Термин “донор” в настоящем описании предпочтительно означает лицо, сдающее клетки цельной крови. Это лицо, будь то живой донор или мертвый донор, может быть донором пересаженного органа. Однако в некоторых случаях пациент также может быть донором.
Термин “выделенные клетки цельной крови”, предпочтительно, относится к клеткам, полученным из образца крови или из клеток селезенки. Клетки крови можно получить путем взятия крови у донора, необязательно включая лейкаферез. Кроме того, клетки крови также можно выделить из клеток селезенки. Особенно предпочтительно, термин “выделенные клетки цельной крови” означает лейкоциты, которые получают методом лейкафереза, как описано выше, или же выделяют из клеток крови, полученных, как описано выше, методами, хорошо известными специалистам.
Термин “PBMC” или “мононуклеарные клетки периферической крови” обозначает отдельный тип клеток периферической крови с одним круглым ядром, например, лимфоциты, моноциты или дендритные клетки. PBMC можно выделить из цельной крови с помощью фиколла, гидрофильного полисахарида, который разделяет слои крови, причем моноциты и лимфоциты образуют лейкоцитарную пленку под слоем плазмы. Эта лейкоцитарная пленка содержит PBMC. Кроме того, PBMC можно выделить из цельной крови методом гипотонического лизиса, при котором будут предпочтительно лизироваться эритроциты. Данный метод обычно приводит к получению нейтрофилов и других полиморфноядерных (PMN) клеток. Кроме того, PBMC также можно получить из цельной крови методом лейкафереза. Такой метод обычно обеспечивает получение PBMC, PMN и небольших количеств эритроцитов и тромбоцитов.
Предпочтительно, PBMC содержат моноциты и лимфоциты или представляют собой указанные клетки.
Обычно, клетки цельной крови и/или PBMC получают из образца крови донора, при необходимости используя лейкаферез. В некоторых случаях фракцию, полученную в результате лейкафереза, можно обработать фиколлом.
Дополнительно или альтернативно, указанные клетки могут происходить из организма донора, например, их можно получить путем обеспечения прицельной дифференцировки стволовых клеток, взятых у донора. Обычно такие клетки происходят или их получают от одного донора. Однако также возможно использование двух или нескольких доноров. В этом случае термин “донор” может включать одного, двух, нескольких или всех доноров.
Как правило, предпочтительно, клетки получают в условиях надлежащей производственной практики (GMP).
Обычно количество клеток определяется путем ручного или автоматизированного подсчета клеток. Подсчет клеток, предпочтительно, проводится с помощью красителя для окрашивания живых/мертвых клеток с тем, чтобы можно было определить количество жизнеспособных клеток. Кроме того, проводится анализ состава клеток в препарате методом проточной цитометрии. Предпочтительно, фармацевтическая композиция содержит моноциты, лимфоциты и в меньшем количестве гранулоциты, тромбоциты и эритроциты.
Термин “клетки, обработанные…”, согласно настоящему изобретению, предпочтительно, означает обработку в соответствии со следующей процедурой. Клетки получают, как описано выше, и промывают. Затем к клеткам (106 клеток/мл) добавляют активное вещество до концентрации 10-100 мкг/мл на 30 мин. После этого клетки тщательно промывают для удаления активного вещества. Как правило, клетки вводятся пациенту, как описано здесь, через 4-48 часов после обработки, описанной выше.
Предпочтительно обработка клеток, описанная выше, проводится по следующей методике.
Сначала полученные клетки тщательно промывают буфером для промывания. Затем добавляют буфер к восстановленному активному веществу (веществам) в пропорции примерно 4:1. После этого смесь буфера и активного вещества добавляют к клеткам (106-109 клеток/мл) до концентрации 10-105 мкг/мл. После инкубации в течение 30 мин при 37°C клетки осторожно центрифугируют. После этого клетки тщательно промывают для удаления активного вещества. Для контроля качества конечный продукт тестируют на количество клеток, жизнеспособность и состав клеток методом проточной цитометрии, а также на стерильность методом прямого посева согласно Ph. Eur. 2.6.1, на отсутствие эндотоксинов с помощью теста с лизатом амебоцитов Limulus согласно Pharm Eur 2.6.14 и на вымывание активного вещества методом высокоэффективной жидкостной хроматографии. Кроме того, согласно соответствующим инструкциям, в образцах донорской крови определяют маркеры инфекционных заболеваний.
Термин “активное вещество” означает любое вещество или комбинацию веществ, которые представляют собой или, по крайней мере, включают одно или несколько веществ, выбранных из группы, содержащей химиотерапевтические средства, ингибиторы протеасом, иммунодепрессанты, антипролиферативные вещества и их комбинации. Таким образом, активное вещество может представлять собой одно, два, три, четыре, пять и более различных веществ.
Предпочтительно одно, два, три и более либо все активные вещества представляют собой химиотерапевтические средства, выбранные из группы, состоящей из алкилирующих агентов (таких, как бусульфан, карбоплатин, кармустин, хлорамбуцил, цисплатин, циклофосфамид, например, цитоксан, дакарбазин, ифосфамид, ломустин, мехоларетамин, мелфалан, прокарбазин, стрептозоцин и тиотепа), антинеопластических антибиотиков (таких, как блеомицин, дактиномицин, даунорубицин, доксорубицин типа митомицина C, митоксантрон, пентостатин и пликамицин), антиметаболитов [таких, как фтордезоксиуридин, кладрибин, цитарабин, флоксуридин, флударабин, фторурацил, например, 5-фторурацил (5FU), гемцитабин, гидроксимочевина, меркаптопурин, метотрексат и тиогуанин], ингибиторов кальцинейрина (таких, как циклоспорин, такролимус), метотрексата, азатиоприна, ингибиторов mTOR (таких, как эверолимус, сиролимус), блокаторов костимуляторов типа абатацепта, ингибиторов JAK типа руксолитиниба и производных из природных источников [таких, как микофенолят (мофетил), доцетаксель, этопозид, иринотекан, таксаны (например, паклитаксель), тенипозид, топотекан, винбластин, винкристин, винорелбин, стероиды (например, глюкокортикоиды типа преднизона) и тамоксифен].
Предпочтительно одно, два, три и более либо все активные вещества представляют собой ингибиторы протеасом, выбранные из группы, состоящей из бортезомиба (например, Velcade®), карфилзомиба (например, Kyprolis®) и иксазомиба (например, Ninlaro®).
Предпочтительно одно, два, три и более либо все активные вещества представляют собой иммуносупрессоры, выбранные из группы, содержащей микофеноловую кислоту, ингибиторы mTOR, азатиоприн, такролимус и циклоспорин.
Предпочтительно одно, два, три и более либо все активные вещества представляют собой антипролиферативные вещества, выбранные из группы, содержащей микофеноловую кислоту, азатиоприн, циклофосфамид и ингибиторы mTOR.
Особенно предпочтительно, активное вещество включает или представляет собой одно или несколько веществ, выбранных из группы, содержащей митомицин C, церамид C2, туникамицин, микофенолят-мофетил, метаболиты триптофана (типа кинуренина, например, траниласта) и их полусинтетические производные.
Особенно предпочтительно, активное вещество включает или представляет собой метаболиты триптофана (типа кинуренина, например, траниласта) и/или митомицин C.
В настоящем изобретении “терапевтически эффективное количество” означает количество указанного соединения, достаточное для лечения определенного заболевания при разумном соотношении польза/риск. В целом, термин “терапевтически эффективное количество” означает такое количество указанного соединения, которое является физиологически значимым и улучшает здоровье индивида. Вещество, т.е. указанное соединение, является физиологически значимым, если его присутствие приводит к изменению физиологии человека-реципиента. Например, при лечении патологического состояния введение указанного соединения, которое облегчает или останавливает дальнейшее развитие заболевания, будет считаться и физиологически значимым, и терапевтически эффективным.
Термины “лечить” или “лечение” отторжения органа или клеточного трансплантата в настоящем изобретении, предпочтительно, понимается как подавление отторжения с тем, чтобы пересаженный орган и/или клетки оставались функциональными.
Термины “предотвращение” или “профилактика” отторжения органа или клеточного трансплантата, предпочтительно, понимаются как ингибирование или по меньшей мере ослабление такого отторжения у субъекта, как раскрыто в настоящем описании, в течение определенного периода времени. Следует понимать, что такой период времени зависит от введенного количества композиции по изобретению, а также от индивидуальных свойств субъекта и различных факторов, таких, как тяжесть заболевания, возраст, вес тела, общее состояние здоровья, пол и диета пациента, время введения, способ введения, продолжительность лечения, а также препаратов, которые применяются в сочетании или одновременно с лечением. Такая профилактика требует подавления лишь сравнительно небольшого числа неактивных иммунных клеток. В исходном состоянии без стимулирования, по оценкам, только примерно один клон-предшественник на 100 000 T-клеток CD8+ проявляет специфичность к определенному антигену (Blattmann et al., 2002, J. Exp. Med., 195: 657-664).
При остром отторжении пересаженного органа происходит экспансия клонов иммунных клеток, распознающих донорскую ткань. А при вирусных инфекциях в течение 7-8 дней происходит резкое возрастание количества специфичных клонов T-клеток, вплоть до 50 000 раз, что составляет от 15 до 20 циклов пролиферации (Williams & Bevan, 2007, Ann. Rev. Immunol., 25:171-192). Таким образом, необходимо успешно подавить активность большого количества клеток. Более того, активные иммунные клетки находятся в другом физиологическом состоянии по сравнению с покоящимися иммунными клетками. Для того, чтобы инициировать пролиферацию и различные эффекторные функции, наивным T-клеткам CD4+ и CD8+ необходимо встретиться с антигенами в лимфоидных органах, презентированными антиген-презентирующими клетками (APC). Напротив, активированные и подвергнутые экспансии T-клетки устремляются в периферические ткани, чтобы обнаружить и впоследствии устранить источники антигенов. При этом чрезвычайно сложном процессе активированные клетки экспрессируют смесь различных сигнальных и эффекторных молекул типа цитокинов и хемокинов, проявляющих бесчисленные функции в отношении как иммунных, так и неиммунных клеток. Воздействие чужеродных антигенов обычно приводит к появлению так называемых долгоживущих клеток памяти, составляющих 5-10% от исходного количества активированных эффекторных клеток. Качество клеток памяти имеет значение для более быстрого и эффективного ответа на те же самые антигены при последующих контактах с ними (Harty & Badovinac, 2008, Nat. Rev. Immunol., 8:107-119; Williams & Bevan, 2007, Ann. Rev. Immunol., 25:171-192; Sprent & Surh, 2002, Ann. Rev. Immunol., 20: 551-579; Rogers et at., 2000, J. Immunol., 164:2338-2346). Поэтому эффективность фармацевтической композиции по настоящему изобретению при лечении отторжения пересаженных органов была неожиданной.
Однако следует иметь в виду, что такое лечение и/или профилактика могут быть эффективными не у всех субъектов, получающих композиции по настоящему изобретению. Тем не менее, требуется, чтобы у статистически значимой части субъектов в группе или популяции эффективно предотвращалось или по крайней мере проявлялось ослабление отторжения органа или клеточного трансплантата либо сопровождающих его симптомов. С этой точки зрения предполагается, что в такой группе или популяции субъектов в норме, то есть без профилактических мер, согласно настоящему изобретению, будет развиваться более сильное отторжение органа или клеточного трансплантата.
С другой стороны, частота такого отторжения в группе субъектов, получавших композицию по изобретению предложенным способом, будет значительно ниже, чем обычно регистрируемая частота в группе субъектов, не получавших композицию по изобретению или получавших ее, но не в соответствии со способом, согласно изобретению. Будет ли такая частота статистически значимой, могут без особого труда установить специалисты в данной области, используя различные хорошо известные инструменты статистической оценки, например, определение доверительных интервалов, определение значения p, t-критерий Стьюдента, критерий Манна-Уитни и т.п. Предпочтительно, доверительные интервалы составляют не менее 90%, не менее 95%, не менее 97%, не менее 98% или не менее 99%. Значения p предпочтительно составляют 0,1, 0,05, 0,01, 0,005 или 0,0001. Предпочтительно, лечение и/или профилактика будет эффективной для, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80% или, по меньшей мере, 90% субъектов в данной группе или популяции.
В качестве иммунодепрессантов очень полезны предварительно обработанные выделенные клетки цельной крови или PBMC по настоящему изобретению при определенной схеме дозирования, как изложено здесь, при введении для предотвращения иммунного отторжения пересаженных клеток, тканей или органов. Примеры пересаженных клеток, тканей и органов, страдающих от эффектов отторжения, включают сердце, почки, печень, костный мозг, кожу, роговицу, легкие, поджелудочную железу, конечности, мышцы, нервы, двенадцатиперстную кишку, тонкий и толстый кишечник, островковые клетки поджелудочной железы, аллогенные гемопоэтические стволовые клетки, T-клетки с химерными антигенными рецепторами, донорские лимфоциты при вливании, аллогенные гемопоэтические стволовые клетки либо их комбинации (например, части лица или матки), аллогенные T-клетки с химерными антигенными рецепторами и др.
Предпочтительно, настоящее изобретение охватывает лечение отторжения следующих органов, клеток и тканей: сердца, почек, печени, костного мозга, кожи, роговицы, легких, поджелудочной железы, конечностей, мышц, нервов, двенадцатиперстной кишки, тонкого и толстого кишечника, островковых клеток поджелудочной железы, аллогенных гемопоэтических стволовых клеток, T-клеток с химерными антигенными рецепторами, донорских лимфоцитов при вливании, аллогенных гемопоэтических стволовых клеток либо их комбинаций (например, частей лица или матки), аллогенных T-клеток с химерными антигенными рецепторами и др.
Предпочтительно, фармацевтические композиции по изобретению также могут применяться для лечения и/или профилактики болезни “трансплантат против хозяина”.
В настоящем изобретении термин “фармацевтически приемлемый носитель” означает нетоксичный, инертный твердый, полутвердый или жидкий наполнитель, разбавитель, инкапсулирующий материал или рецептурное вещество любого типа. Некоторые примеры таких материалов, которые могут служить фармацевтически приемлемыми носителями, включают сахара, такие, как лактоза, глюкоза и сахароза; крахмалы, такие, как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие, как натриевая карбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; наполнители типа масла какао и воска для свечей; масла, такие, как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли типа пропиленгликоля; сложные эфиры типа этилолеата и этиллаурата; агар; буферные вещества типа гидроксида магния и гидроксида алюминия; альгиновую кислоту; апирогенную воду; изотонический солевой раствор; раствор Рингера; этиловый спирт, фосфатные буферные растворы; нетоксичные совместимые смазывающие вещества типа лаурилсульфата натрия и стеарата магния; а также красители, высвобождающие вещества, покрывающие вещества, подсластители, ароматизаторы и отдушки. В композициях также могут присутствовать консерванты и антиоксиданты, на усмотрение производителя.
Композиции по настоящему изобретению можно вводить перорально, ректально, парентерально, интрацистернально, интравагинально, внутрибрюшинно, буккально или в виде перорального или назального спрея. Термин “парентерально” в настоящем изобретении означает такие способы введения, которые включают внутривенное, внутримышечное, внутрибрюшинное, внутригрудинное, подкожное и внутрисуставное введение, предпочтительно, в виде вливания. Предпочтительно введение осуществляется внутривенно, внутримышечно или подкожно, предпочтительно, путем инфузии.
Фармацевтические композиции по настоящему изобретению для парентерального введения, предпочтительно, представляют собой фармацевтически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии, а также стерильные порошки, которые подлежат восстановлению в стерильных растворах или дисперсиях для инъекций непосредственно перед применением. Примеры подходящих водных и неводных носителей, разбавителей, растворителей или доставляющих веществ включают воду, этанол, полиолы (такие, как глицерол, пропиленгликоль, полиэтиленгликоль и др.), карбоксиметилцеллюлозу и их подходящие смеси, растительные масла (типа оливкового масла) и сложные органические эфиры для инъекций типа этилолеата. Надлежащую текучесть можно поддерживать, например, при помощи покрывающих материалов типа лецитина, за счет обеспечения требуемого размера частиц в случае дисперсий и при использовании поверхностно-активных веществ.
Как описано выше, ожидается, что более высокие дозы вводимых клеток обеспечат индивидуальную иммуносупрессию за более короткое время. Так, предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту по меньшей мере, 5×106 клеток, по меньшей мере, 1×107 клеток, по меньшей мере, 5×107 клеток, по меньшей мере, 1×108 клеток или, по меньшей мере, 1,5×108 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента.
Однако, чтобы избежать или уменьшить риск, например, возникновения тромбоза или эмболии, как описано выше, предпочтительно, количество фармацевтической композиции выбирают таким образом, чтобы вводить максимум 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента.
Предпочтительно, введение фармацевтической композиции осуществляется за одну процедуру, однако также возможны две, три и более процедур.
Наряду с количеством клеток или в качестве альтернативы важны и временные точки для введения, позволяющие иммунной системе развить эффективное/достаточное персонализированное/прицельное подавление. Так, предпочтительно клетки вводятся реципиенту, по меньшей мере, за 1 день до трансплантации, предпочтительно, по меньшей мере, за 2 дня, за 3 дня, за 4 дня, за 5 дней, за 6 дней, за 7 дней, за 8 дней, за 9 дней, за 10 дней, за 14 дней, за 21 день или за 28 дней до трансплантации.
Специалистам должно быть известно то, что конкретная комбинация количества клеток и времени введения может зависеть от индивидуальных свойств субъекта и различных факторов, таких, как тяжесть заболевания, возраст, масса тела, общее состояние здоровья, пол и диета пациента, способ введения, продолжительность лечения, а также препаратов, применяемых в комбинации или одновременно с лечением, или же от природы органа, подлежащего трансплантации.
Известно, что клетки Breg CD19+CD24highCD38high играют важную роль в поддержании долгосрочной функции аллотрансплантатов и повышении толерантности к трансплантатам (Newell KA et al., J Clin Invest 2010; Silva HM et al., Mol Med 2012; Chesneau M et al., Am J Transplant 2014; Shabir S et al., Am J Transplant 2015; Tebbe B et al., PLoS One 2016; Svachova V et al., Transpl Int 2016). Tebbe et al. обнаружили, что у пациентов, получающих обычные дозы иммуносупрессора (CyA в качестве ингибитора кальцинейрина), временное количество B-лимфоцитов CD19+CD24highCD38high находится в пределах 0-5% в течение первого года после трансплантации (Tebbe et al., PLoS One 2016). У пациентов с количеством указанных клеток более 1% не наблюдалось эпизодов отторжения.
Неожиданно оказалось, что введение описанных в настоящей заявке специфических клеток по схеме дозирования, составляющей не менее 1×108 клеток, предпочтительно, по меньшей мере 1,5×108 клеток на 1 кг массы тела реципиента, по меньшей мере за 5 дней, предпочтительно по меньшей мере за 6 дней и особенно предпочтительно по меньшей мере за 7 дней до трансплантации приводит к резкому повышению количества клеток Breg CD19+ CD24highCD38high и тем самым делает лечение еще более эффективным. Эта корреляция на сегодняшний момент времени еще не была известна, не говоря уже о том, что корреляция вообще существует. Содержание Breg у прошедших трансплантацию контрольных субъектов, не подвергавшихся воздействию МИК, была сравнима с описанной Tebbe et al., тогда как у пациентов, которым были введены МИК, содержание Breg находилось даже в пределах 5-40% на 180-й день после трансплантации, что намного превышает значения у контрольных субъектов (медиана: 1%) и у этих же пациентов до трансплантации (см. пример 1 и фиг. 3 и 4).
Таким образом, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту по меньшей мере 1×108, предпочтительно, по меньшей мере 1,3×108 и, особенно предпочтительно, по меньшей мере 1,5×108 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 5 дней, предпочтительно, за 6 дней и, особенно предпочтительно, за 7 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от 1×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 5 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 6 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 7 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1,3×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 5 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1,3×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 6 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1,3×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 7 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1,5×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 5 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1,5×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 6 дней до трансплантации.
Особенно предпочтительно, профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту от по меньшей мере 1,5×108 до 1×1012 обработанных клеток цельной крови или обработанных PBMC на 1 кг массы тела реципиента, причем введение осуществляется по меньшей мере за 7 дней до трансплантации.
Кроме того, особенно предпочтительно, при этой специальной обработке активное вещество включает или представляет собой митомицин C.
Все, что было здесь сказано в отношении фармацевтических композиций для использования, также применимо и к фармацевтическим композициям независимо от их использования.
Соответственно, другой аспект настоящего изобретения предусматривает фармацевтическую композицию, включающую или состоящую из:
a) выделенных клеток цельной крови или мононуклеарных клеток периферической крови (PBMC), обработанных терапевтически эффективным количеством активного вещества, и
b) необязательно, фармацевтически приемлемого носителя,
причем композиция пригодна для профилактики или лечения отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком, а указанные клетки цельной крови или PBMC выделены или происходят из организма донора трансплантата,
при этом композиция характеризуется тем, что:
общее количество обработанных клеток цельной крови или обработанных PBMC в фармацевтической композиции составляет в пределах от 7,5×106 клеток до 1,8×1014 клеток, предпочтительно, от 3,0×107 до 9,0×1012 клеток и, особенно предпочтительно, от 6,0×107 клеток до 7,5×1011 клеток, и/или
концентрация обработанных клеток цельной крови или обработанных PBMC в фармацевтической композиции составляет в пределах от 102 клеток/мл до 1010 клеток/мл, предпочтительно, от 106 клеток/мл до 109 клеток/мл.
Следующий аспект настоящего изобретения предусматривает способ получения ex vivo фармацевтической композиции, согласно изобретению, включающий следующие стадии:
a) получение образца клеток крови от донора и, необязательно, выделение мононуклеарных клеток периферической крови (PBMC) из данного образца клеток крови,
b) обработку ex vivo клеток, полученных на стадии а), терапевтически эффективным количеством активного вещества,
c) необязательно, обеспечение фармацевтически приемлемого носителя и добавление его к обработанным клеткам, полученным на стадии b).
Сначала полученные клетки тщательно промывают буфером для промывания. Затем добавляют буфер к восстановленному активному веществу в пропорции примерно 4:1. После этого смесь буфера и активного вещества добавляют к клеткам (106-109 клеток/мл) до концентрации 10-105 мкг/мл. После инкубации в течение 30 мин при 37°C клетки осторожно центрифугируют. После этого клетки тщательно промывают для удаления активного вещества. Для контроля качества конечный продукт тестируют на количество клеток, жизнеспособность и состав клеток методом проточной цитометрии, а также на стерильность методом прямого посева согласно Ph. Eur. 2.6.1, на отсутствие эндотоксинов с помощью теста с лизатом амебоцитов Limulus согласно Pharm Eur 2.6.14 и на вымывание активного вещества методом высокоэффективной жидкостной хроматографии. Кроме того, согласно соответствующим инструкциям, в образцах донорской крови определяют маркеры инфекционных заболеваний.
Все, что было сказано здесь в отношении фармацевтической композиции для использования, в отношении фармацевтической композиции независимо от ее использования, а также в отношении ингредиентов таких композиций, также применимо и к фармацевтической композиции, полученной способом, раскрытым в настоящем описании.
Предпочтительно, в фармацевтической композиции, полученной способом, раскрытым в настоящем описании, общее количество обработанных клеток цельной крови или обработанных PBMC находится в пределах от 7,5×106 клеток до 1,8×1014 клеток, предпочтительно, от 3,0×107 до 9,0×1012 клеток и, особенно предпочтительно, от 6,0×107 до 7,5×1011 клеток и/или в пределах от 102 клеток/мл до 1010 клеток/мл, предпочтительно, от 106 клеток/мл до 109 клеток/мл.
Также предпочтительно, в фармацевтической композиции, полученной способом, раскрытым в настоящем описании, концентрация обработанных клеток цельной крови или обработанных PBMC находится в пределах от 102 клеток/мл до 1010 клеток/мл, предпочтительно от 106 клеток/мл до 109 клеток/мл.
Также предпочтительно, в фармацевтической композиции, полученной способом, раскрытым в настоящем описании, активное вещество включает или представляет собой одно или несколько веществ, выбранных из группы, содержащей химиотерапевтические средства, ингибиторы протеасом, иммунодепрессанты, антипролиферативные вещества и их комбинации, а предпочтительное активное вещество включает или представляет собой одно или несколько веществ, выбранных из группы, содержащей митомицин C, церамид C2, туникамицин, микофенолят-мофетил, метаболиты триптофана и их полусинтетические производные, и, особенно предпочтительно, активное вещество включает или представляет собой митомицин C.
Кроме того, в фармацевтической композиции, полученной способом, раскрытым в настоящем описании, предпочтительно, присутствует фармацевтически приемлемый носитель, который включает или представляет собой одно или нескольких веществ, выбранных из группы, состоящей из сахаров, таких, как лактоза, глюкоза и сахароза; крахмалов, таких, как кукурузный крахмал и картофельный крахмал; целлюлозы и ее производных, таких, как натриевая карбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; порошкообразного трагаканта; солода; желатина; талька; наполнителей типа масла какао и воска для свечей; масел, таких как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликолей типа пропиленгликоля; сложных эфиров типа этилолеата и этиллаурата; агара; буферных веществ типа гидроксида магния и гидроксида алюминия; альгиновой кислоты; апирогенной воды; изотонического солевого раствора; раствора Рингера; этилового спирта, фосфатных буферных растворов; нетоксичных совместимых смазывающих веществ типа лаурилсульфата натрия и стеарата магния; а также красителей, высвобождающих веществ, покрывающих веществ, подсластителей, ароматизаторов и отдушек, консервантов и антиоксидантов.
Краткое описание фигур
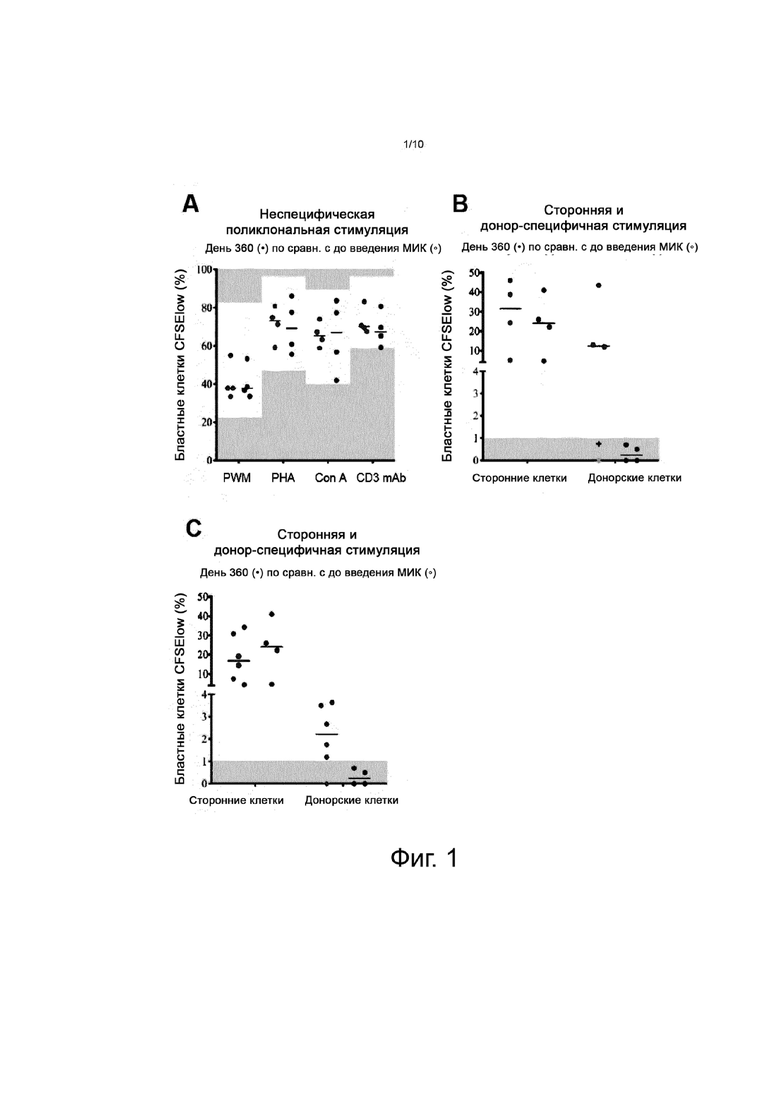
На фиг. 1 схематически представлено поддержание интактной общей иммунной системы, когда проводилась неспецифическая поликлональная стимуляция (фиг. 1A) либо сторонняя или донор-специфичная стимуляция (фиг. 1B и C). Состояние иммунной системы после сторонней и донор-специфичной стимуляции сравнивалась с состоянием у пациентов до лечения (фиг. 1B) или у контрольных субъектов без обработки (фиг. 1C).
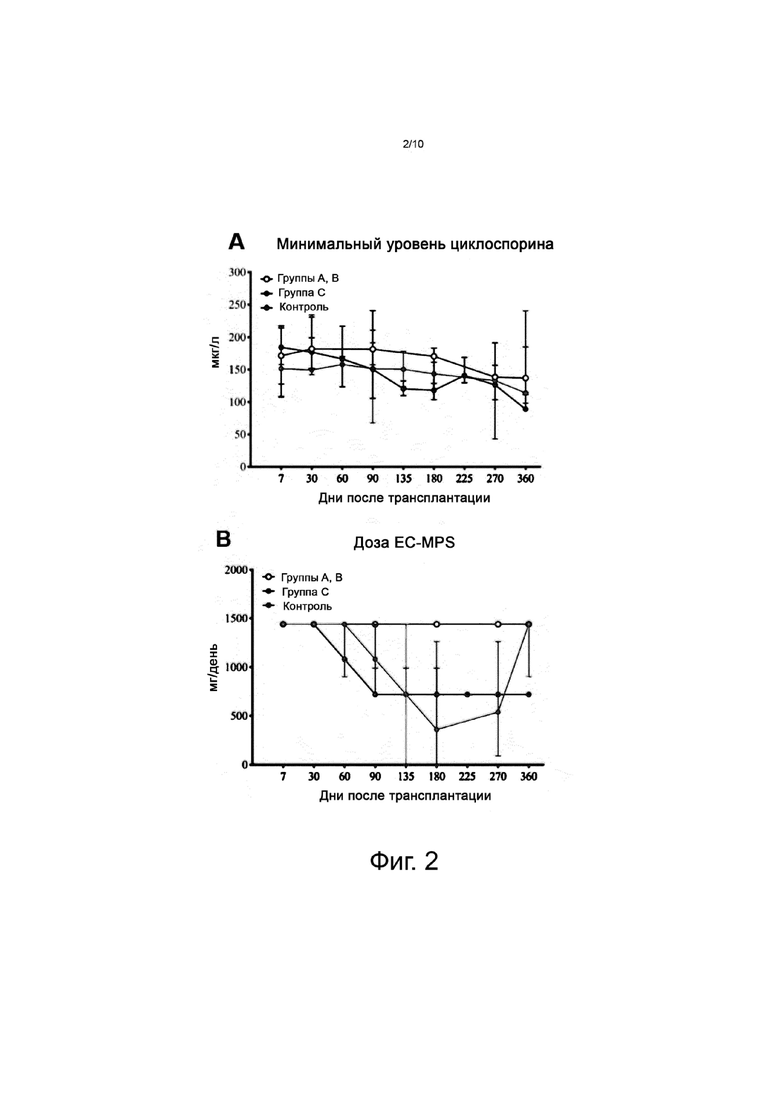
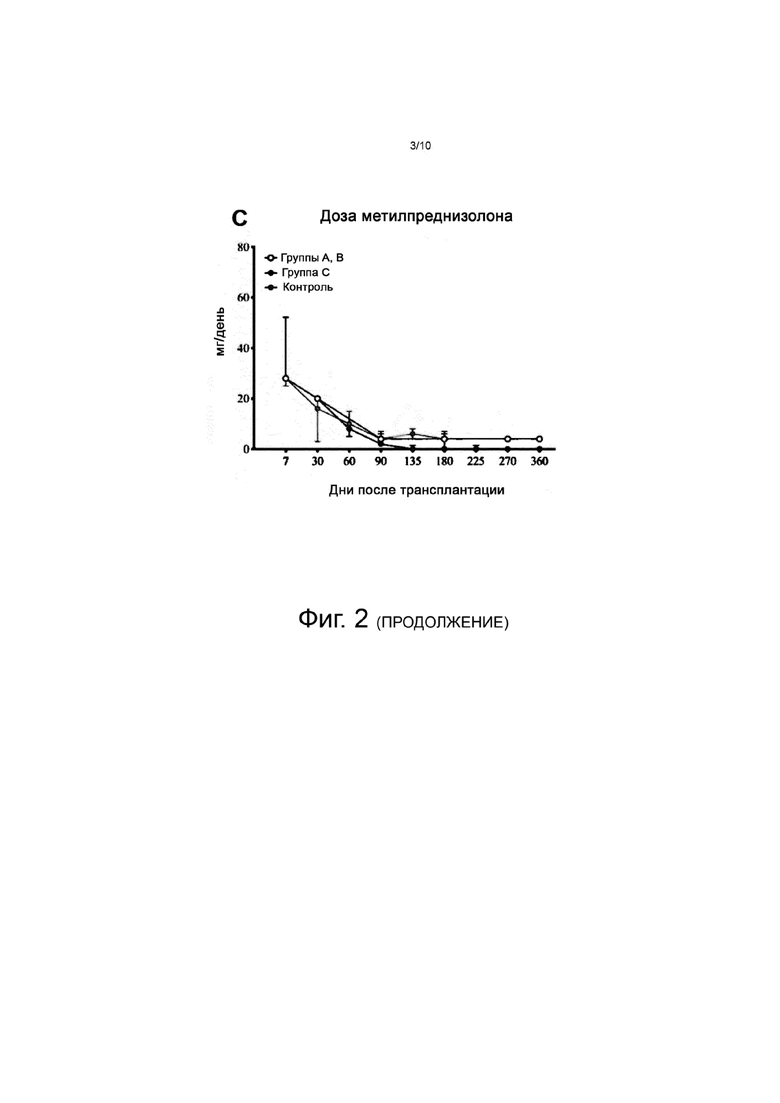
На фиг. 2 схематически представлена иммуносупрессия, т.е. минимальный уровень циклоспорина A (A), суточная доза микофенолята натрия с энтеросолюбильным покрытием (EC-MPS) (B) и суточная доза метилпреднизолона (C) у пациентов в группах A, B, C и в контроле.
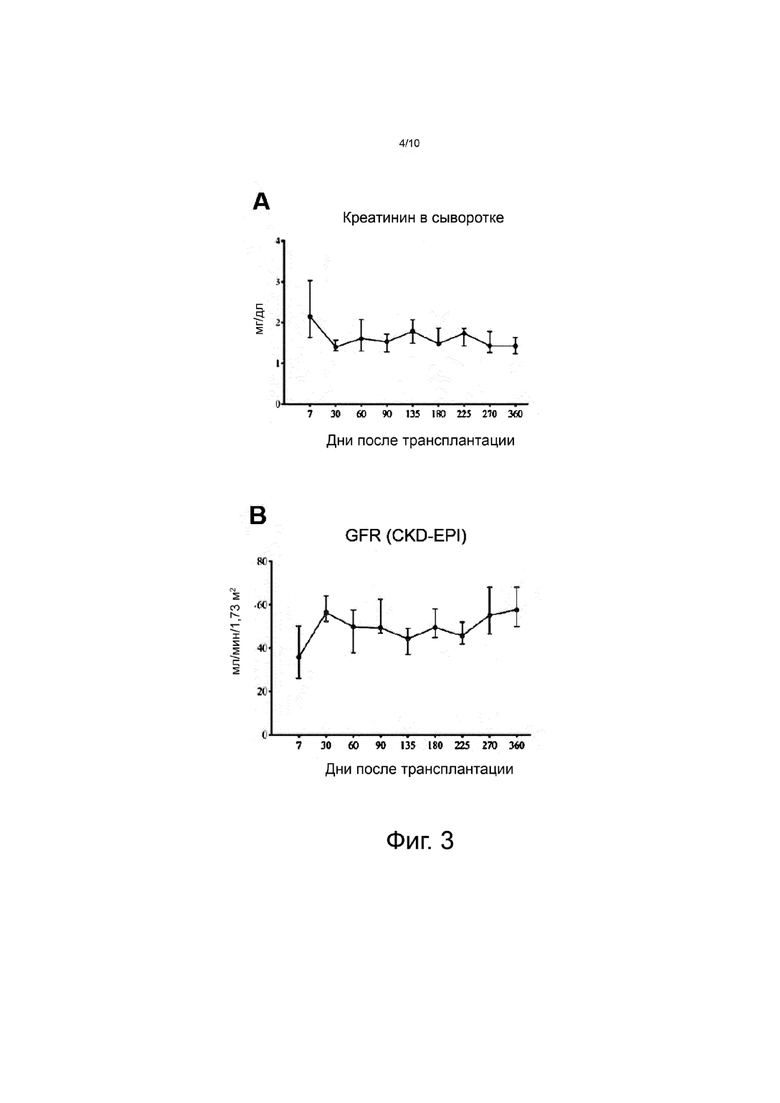
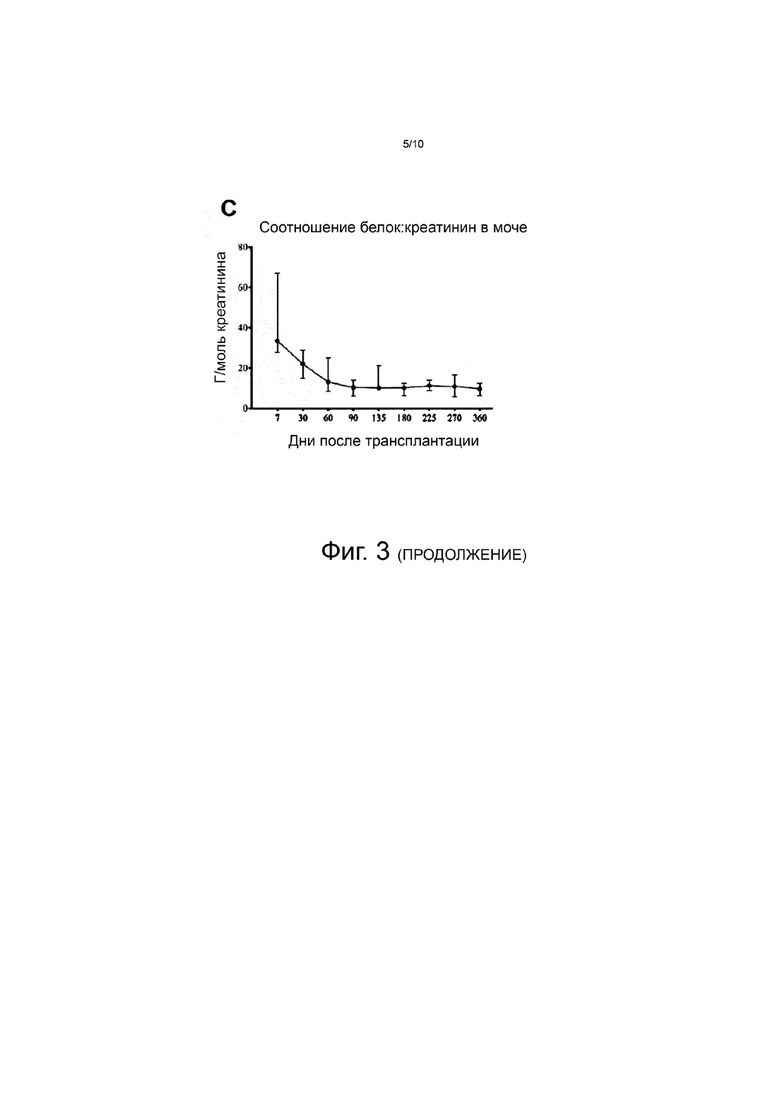
На фиг. 3 представлена достигнутая и поддерживаемая функция органа (почек) при анализе по уровню креатинина в сыворотке (фиг. 3A), по скорости клубочковой фильтрации (GFR, рассчитанной по формуле Совместного проекта по эпидемиологии хронических заболеваний почек (CKD-EPI) (фиг. 3B) или по соотношению белка к креатинину в моче (фиг. 3C).
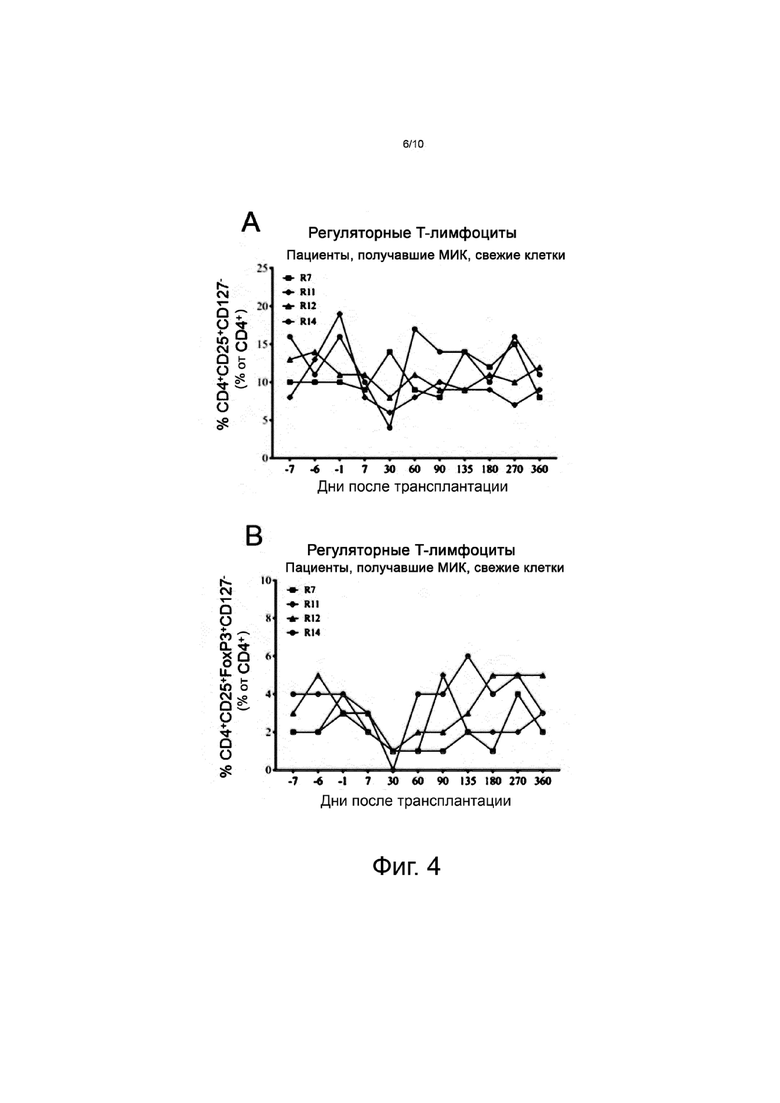
На фиг. 4 представлено содержание регуляторных T-лимфоцитов до и после лечения, при этом анализировали T-лимфоциты CD4+CD25+CD127− (фиг. 4A) или CD4+CD25+FoxP3+CD127− (фиг. 4B).
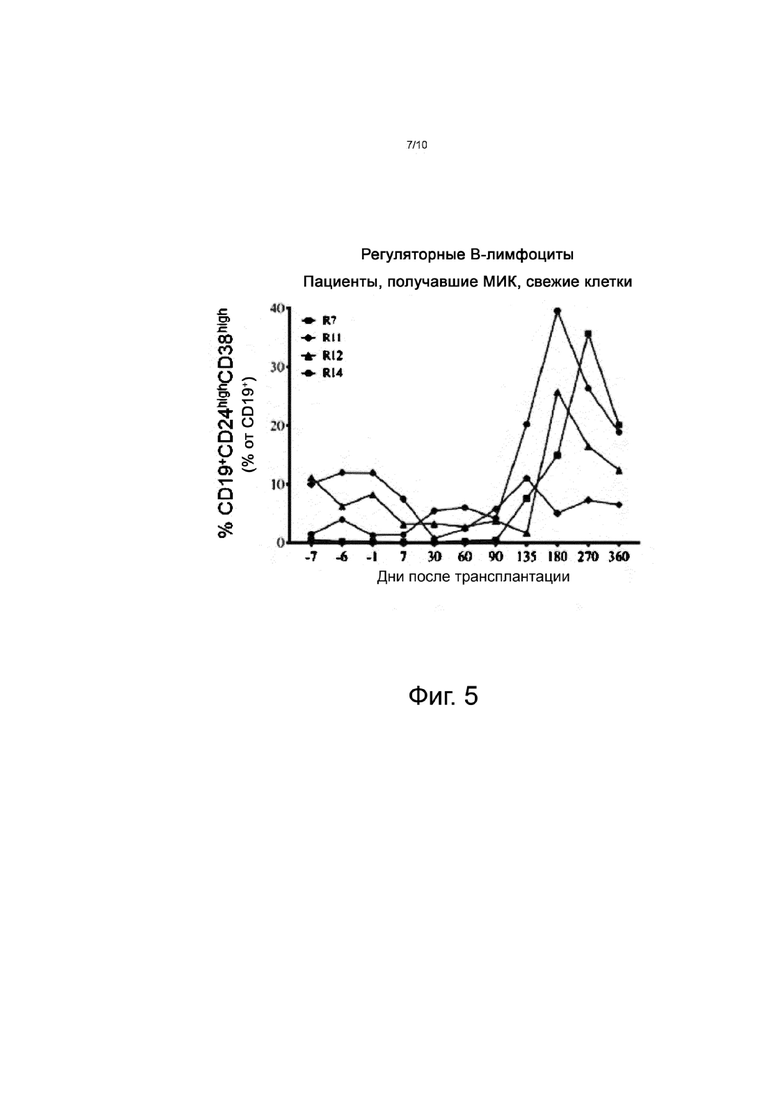
На фиг. 5 представлено содержание регуляторных B-лимфоцитов до и после лечения в опытной группе C, при этом анализировали регуляторные B-лимфоциты CD19+CD24highCD38high.
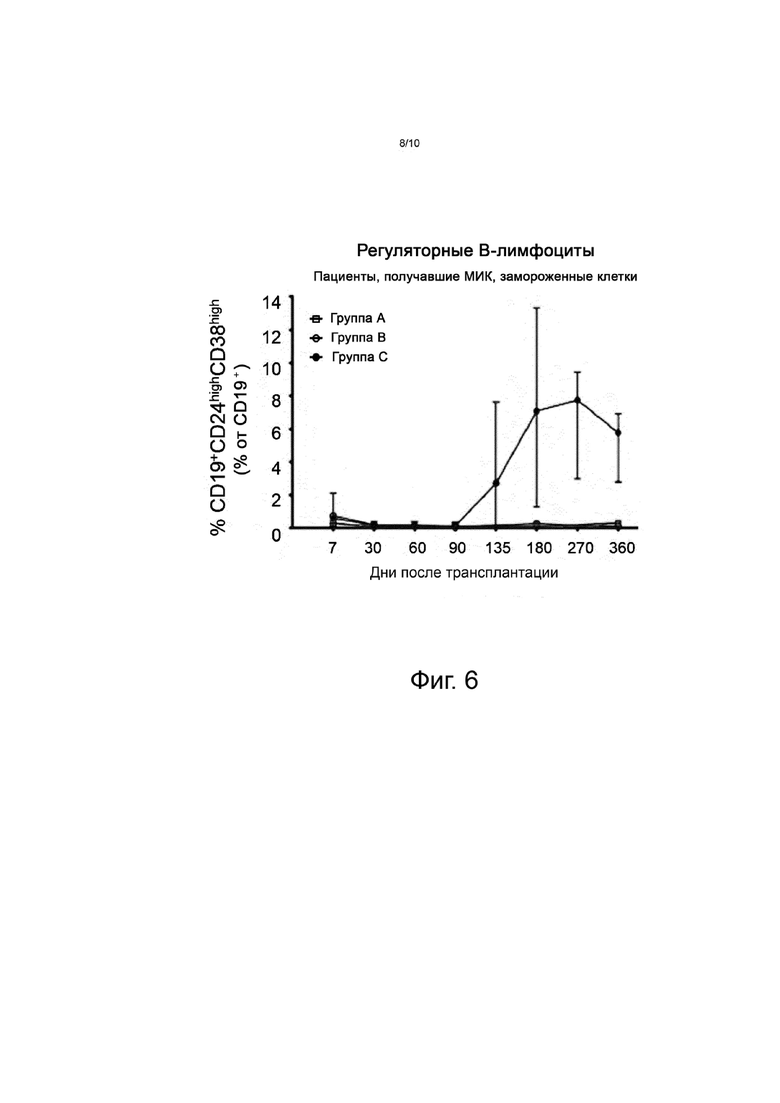
На фиг. 6 представлено содержание регуляторных B-лимфоцитов до и после лечения в опытных группах A, B и C, при этом анализировали регуляторные B-лимфоциты CD19+CD24highCD38high.
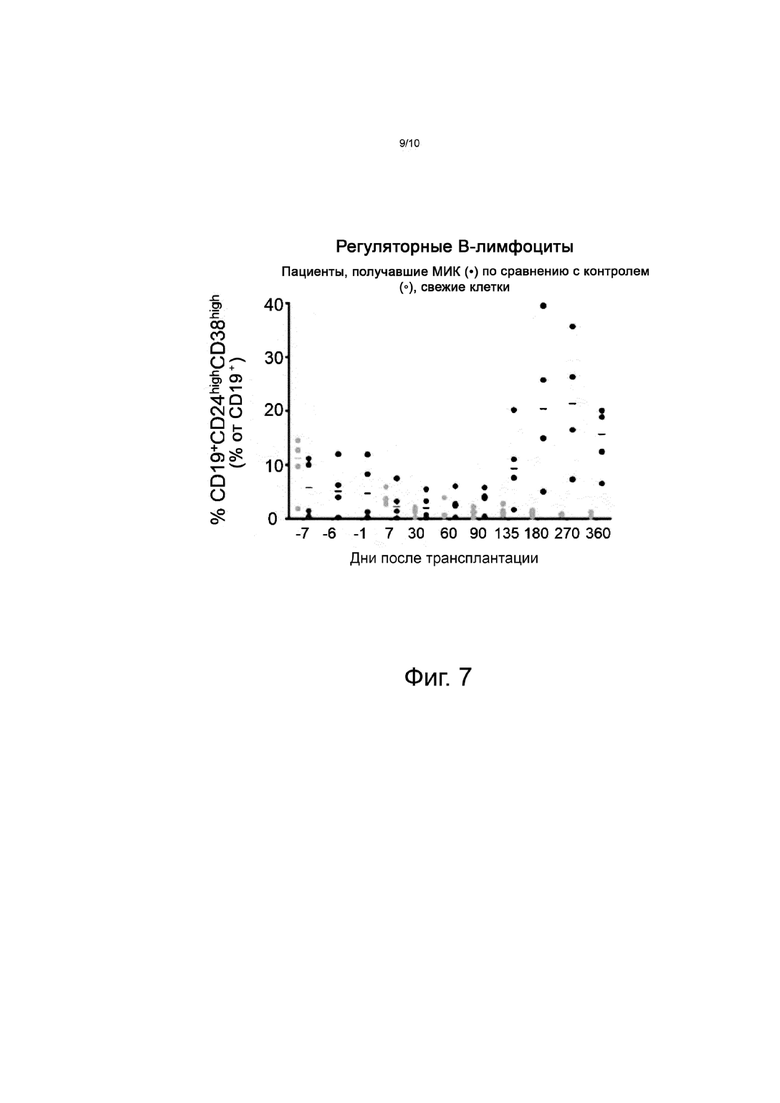
На фиг. 7 представлено содержание регуляторных B-лимфоцитов до и после лечения в сравнении с контролями без лечения, при этом анализировали B-лимфоциты CD19+CD24highCD38high.
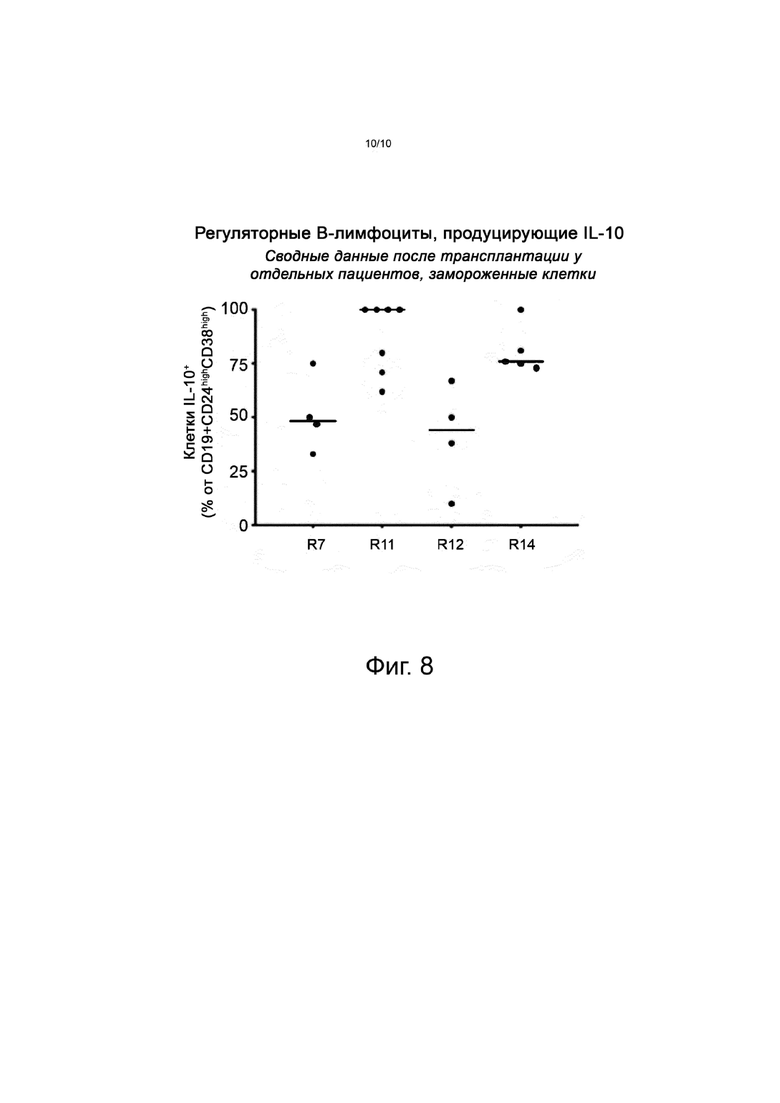
На фиг. 8 представлены уровни клеток IL-10+ среди регуляторных B-лимфоцитов CD19+CD24highCD38high у пациентов группы C.
Раскрытие сущности изобретения
В изобретении раскрывается способ лечения или предотвращения отторжения пересаженного органа или реакции “трансплантат против хозяина” у реципиента трансплантата, который является человеком, включающий следующие стадии:
a) получение образца клеток крови от донора, предпочтительно от донора трансплантата, и, необязательно, выделение мононуклеарных клеток периферической крови (PBMC) из данного образца клеток крови,
b) обработку данного образца клеток крови или полученных из него PBMC терапевтически эффективным количеством активного вещества и
c) введение обработанного образца клеток крови или полученных из него PBMC реципиенту трансплантата, тем самым обеспечивая предотвращение отторжения органа или клеточного трансплантата,
причем количество клеток во вводимом обработанном образце клеток крови или количество полученных из образца PBMC составляет по меньшей мере 0,25×106 клеток на кг массы тела, предпочтительно, по меньшей мере 1,5×106 клеток на кг массы тела реципиента.
Все признаки описанной здесь фармацевтической композиции и/или фармацевтической композиции для использования также применимы к раскрытому в настоящем описании способу, если это возможно.
Для данного способа предпочтительно вводимые реципиенту обработанные клетки крови или PBMCs включают или состоят из лимфоцитов, моноцитов и/или дендритных клеток.
Также предпочтительно, в данном способе химиотерапевтическое средство выбрано из группы, содержащей митомицин C, церамид C2, туникамицин, микофенолят-мофетил, метаболиты триптофана и их полусинтетические производных, а также ингибиторы протеасом.
Также в данном способе, предпочтительно, активное вещество включает или представляет собой метаболиты триптофана (типа кинуренина, например, траниласта) и/или митомицин C.
Предпочтительно, в данном способе количество клеток во вводимом обработанном образце клеток крови или полученных из него PBMC составляет по меньшей мере 5×106 клеток, по меньшей мере 1×107 клеток, по меньшей мере 5×107 клеток, по меньшей мере 1×108 клеток или по меньшей мере 1,5×108 клеток на 1 кг массы тела реципиента.
Также предпочтительно, в данном способе обработанный образец клеток крови или полученные из него PBMC вводятся реципиенту по меньшей мере за 1 день до трансплантации, по меньшей мере за 2 дня, за 3 дня, за 4 дня, за 5 дней, за 6 дней, за 7 дней, за 8 дней, за 9 дней, за 10 дней, за 14 дней, за 21 день или за 28 дней до трансплантации.
Специалистам должно быть известно то, что конкретная комбинация количества клеток и времени введения может зависеть от нескольких индивидуальных свойств пациента и различных факторов, таких, как тяжесть заболевания, возраст, масса тела, общее состояние здоровья, пол и диета пациента, способ введения, продолжительность лечения, а также препаратов, применяемых в комбинации или одновременно с лечением, или же от природы органа, подлежащего трансплантации.
Предпочтительно, в данном способе введение обработанного образца клеток крови или полученных из него PBMC осуществляется внутривенно, предпочтительно, путем инфузии.
Изобретение также предусматривает способ лечения или предотвращения отторжения пересаженного органа у реципиента трансплантата, который является человеком, включающий введение реципиенту композиции, содержащей:
a) выделенные клетки крови или мононуклеарные клетки периферической крови (PBMC), обработанные терапевтически эффективным количеством активного вещества, и
b) необязательно, фармацевтически приемлемый носитель,
причем количество обработанных клеток крови или PBMC в композиции выбрано таким образом, чтобы ввести по меньшей мере 0,25×106 клеток, предпочтительно, по меньшей мере 1,5×106 обработанных клеток крови или PBMC на 1 кг массы тела реципиента.
Предпочтительно, указанный способ также подходит для лечения или предотвращения реакции “трансплантат против хозяина”.
Все признаки описанной здесь фармацевтической композиции и/или фармацевтической композиции для использования также применимы к раскрытому в настоящем описании способу, если это возможно.
В данном способе предпочтительно вводимые реципиенту обработанные клетки крови или PBMC включают лимфоциты, моноциты и/или дендритные клетки.
Особенно предпочтительно, активное вещество включает или представляет собой одно или несколько веществ, выбранных из группы, содержащей митомицин C, церамид C2, туникамицин, микофенолят-мофетил, метаболиты триптофана (типа кинуренина, например, траниласта) и их полусинтетические производные.
Также в данном способе предпочтительное активное вещество включает или представляет собой метаболиты триптофана (типа кинуренина, например, траниласта) и/или митомицин C.
Предпочтительно, в данном способе количество клеток во вводимом обработанном образце клеток крови или полученных из указанного образца PBMC составляет по меньшей мере 5×106 клеток, по меньшей мере 1×107 клеток, по меньшей мере 5×107 клеток, по меньшей мере 1×108 клеток или по меньшей мере 1,5×108 клеток на 1 кг массы тела реципиента.
Также предпочтительно, в данном способе обработанный образец клеток крови или полученные из него PBMC вводятся реципиенту по меньшей мере за 1 день до трансплантации, по меньшей мере за 2 дня, за 3 дня, за 4 дня, за 5 дней, за 6 дней, за 7 дней, за 8 дней, за 9 дней, за 10 дней, за 14 дней, за 21 день или за 28 дней до трансплантации.
Специалистам должно быть известно то, что конкретная комбинация количества клеток и времени введения может зависеть от индивидуальных свойств пациента и различных факторов, таких, как тяжесть заболевания, возраст, масса тела, общее состояние здоровья, пол и диета пациента, способ введения, продолжительность лечения, а также препаратов, применяемых в комбинации или одновременно с лечением, или же от природы органа, подлежащего трансплантации.
Предпочтительно, в данном способе введение обработанного образца клеток крови или полученных из него PBMC осуществляется внутривенно, предпочтительно, путем инфузии.
Предпочтительные воплощения и другие аспекты настоящего изобретения вытекают из прилагаемой формулы изобретения и следующих ниже примеров, причем эти примеры не предназначены для ограничения изобретения.
Примеры
Пример 1. Исследование TOL-1
Проводили 30-дневное сплошное одноцентровое клиническое испытание I фазы для определения безопасности и применимости внутривенного введения МИК для персонализированной иммуносупрессии на живых реципиентах трансплантатов донорских почек (исследование TOL-1, Ethics номер: AFmo-549/2014, EudraCT номер: 2014-002086-30, идентификатор согласно ClinicalTrials.gov: NCT02560220) с последующей фазой наблюдения вплоть до 360-го дня после трансплантации (Ethics номера: 082/2005, 083/2005, S-395/2011). Исследование проводилось в соответствии с положениями Хельсинкской декларации и Рекомендаций по надлежащей клинической практике.
Первичным критерием оценки была безопасность и применимость внутривенного введения МИК по измерению частоты нежелательных явлений (НЯ) у пациентов с хронической болезнью почек 4 или 5 стадии (т.е. GFR <30 мл/мин), которым пересаживали почечный трансплантат от живого донора. НЯ регистрировали в соответствии с Общими критериями терминологии для нежелательных явлений (CTCAE), версия 4.03.
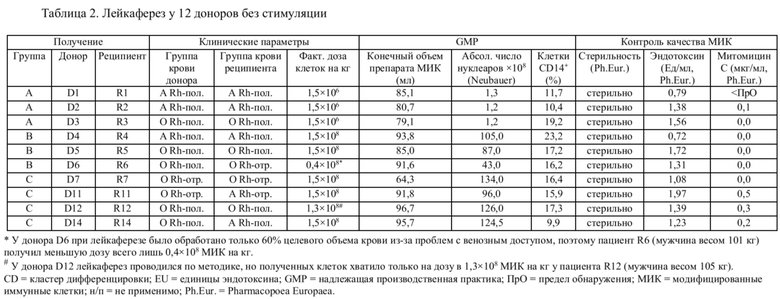
С августа 2015 г. по февраль 2017 г. проводился отбор 14 пар доноров и реципиентов для включения в исследование. В общей сложности 12 донорам проводили лейкаферез, а 10 пациентов прошли курс лечения препаратом МИК. Фаза наблюдения продлилась еще 330 дней до февраля 2018 г.
Перед пересадкой почек 10 пациентов (группы A, B, C) получали МИК от своих доноров. Пациенты получали либо 1,5×106 МИК на кг массы тела в день -2 (n = 3, группа A), либо 1,5×108 МИК на 1 кг массы тела в день -2 (n = 3, группа B) или в день -7 (n = 4, группа C) перед пересадкой живой донорской почки.
Исходные характеристики пациентов представлены в таблице 1.
CMV = цитомегаловирус; DSA = донор-специфичные антитела к HLA A, B, DR, DQ; DTT = дитиотреитол; EBV = вирус Эпштейна-Барр; ESRD = терминальная стадия почечной недостаточности; HLA = антигены лейкоцитов человека; PRA = комплект реакционно-способных антител.
Четыре пациента (R8, R9, R10, R13) проходили скрининг, но не получали клеточной терапии.
Все остальные пациенты (n = 10: R1, R2, R3, R4, R5, R6, R7, R11, R12, R14), а также соответствующие доноры проходили лечение согласно протоколу (как описано выше).
Лейкаферез у доноров без стимуляции проводили с помощью устройства для афереза Spectra Optia® (Terumo BCT, Eschborn, Германия). МИК получали в условиях надлежащей производственной практики (GMP). Препараты МИК вводили пациентам однократно в один день с лейкаферезом у доноров и получением препаратовю. Пациенты группы A получали дозу в 1,5×106 МИК на 1 кг массы тела за 2 дня до трансплантации. Пациенты группы B получали дозу в 1,5×108 МИК на 1 кг массы тела за 2 дня до трансплантации. Пациентам группы C вводили МИК в дозе 1,5×108 МИК на 1 кг массы тела еще за 7 дней до трансплантации. Пациентов разбивали на группы A (R1-R3), B (R4-R6) или C (R7, R11, R12, R14) и вводили МИК. Фактические вводимые дозы МИК приведены в таблице 2.
Препараты вводили пациентам поэтапно с увеличением дозы от группы A к группе B и с учетом возможных нежелательных реакций на конечный препарат МИК, таких как эмболия, воспаление, аллергия или нежелательные реакции на митомицин C или буфер. Поскольку слишком небольшое количество клеток МИК создает риск сенсибилизации реципиента (у реципиентов группы A обнаруживался только 1% клеток МИК от их числа у пациентов групп B и C), то МИК вводили по меньшей мере за 2 дня до трансплантации в фазе эскалации дозы. От группы B к группе C время введения было изменено со дня 2 на день 7 перед трансплантацией.
При посещении реципиента V3 в день 1 перед операцией по пересадке исключали сенсибилизацию реципиента препаратом МИК путем перекрестного сопоставления CDC и ELISA и скрининга антител к HLA по методу Luminex.
Посещения реципиентов после трансплантации приходились на день 7±1 (V4) и день 30±4 (V5, конец исследования). Фаза наблюдения продолжалась до 360-го дня после трансплантации почки с частыми амбулаторными посещениями в дни 60±14, 90±14, 135±1, 180±21, 225±28, 270±28, 360±35.
Иммуносупрессия заключалась во введении циклоспорина A (CyA), микофенолята натрия с энтеросолюбильным покрытием (EC-MPS) и метилпреднизолона (MPS) со дня операции. У пациентов группы C иммуносупрессивная терапия сводилась до низких доз CyA и низких доз EC-MPS без стероидов во время фазы наблюдения после 30-го дня, чтобы избежать инфекционных осложнений при комбинированной клеточной и иммуносупрессивной терапии. Пациенты групп A и B получали иммуносупрессивную терапию по стандартной схеме. Эти стандарты известны специалистам. Иммуносупрессивная терапия у пациентов контрольной группы подбиралась таким образом, чтобы обеспечить иммуносупрессию, сравнимую с той, которая достигалась у пациентов группы C. Детали иммуносупрессивной терапии у пациентов во время исследования TOL-1 и фазы наблюдения представлены на фиг. 2A-C.
Данные, собранные за первые 30 дней после трансплантации, показали, что инфузия МИК хорошо переносится. Всего у 10 прошедших лечение пациентов случилось 69 нежелательных явлений (НЯ), включая 3 тяжелых НЯ (ТНЯ). НЯ были маловероятно связаны (n = 1), либо не связаны (n = 68) с терапией МИК. За все время исследования не было выявлено ни положительных результатов перекрестной совместимости, ни донор-специфичных антител de novo, ни эпизодов отторжения при отличном функционировании пересаженных почек у всех пациентов (см. фиг. 3A-C и таблицу 2).
Пример 1.1. Отсутствие заметного донорского химеризма после введения МИК
Уже через сутки после введения МИК у всех 10 пациентов не отмечалось донорского химеризма. Отсутствие донорского химеризма подтверждалось в день 1 до и в дни 7 и 30 после трансплантации.
Пример 1.2. Отличные клинические результаты вплоть до одного года после трансплантации
Во время фазы наблюдения не обнаруживалось никаких донор-специфичных антител de novo или эпизодов отторжения и у всех пациентов отлично функционировали пересаженные почки (см. фиг. 3A-C и таблицу 3). На 360-й день после операции средний уровень креатинина в сыворотке составлял 1,4 мг/дл (1,1-2,1), средняя рСКФ - 58 мл/мин (37-75) и средний уровень белка в моче - 10 г/моль креатинина (3-19). Не отмечалось оппортунистических инфекций. У 4 из 10 пациентов случилось всего 10 эпизодов не-оппортунистических инфекций. Сюда вошли 3 эпизода инфекции мочевыводящих путей у пациента R7 c малым объемом мочевого пузыря и 2 эпизода инфекции мочевыводящих путей у пациента R12. Не отмечалось впервые возникшего диабета (NODAT), лейкопении, эпизодов диареи, посттрансплантационных лимфопролиферативных заболеваний (PTLD) или других злокачественных новообразований. Общий показатель интенсивности антигипертензивной терапии снижался на 360-й день после трансплантации по сравнению с показателем до операции, особенно у пациентов группы C, хотя сохранялось нормальное кровяное давление.
У всех пациентов отмечалось отличное функционирование пересаженных почек без протеинурии вплоть до 360-го дня после операции (см. фиг. 3C).
(0,5-1,5)
(0,17-2,5)
(-2,25-0)
- n (%)
Кроме того, биопсия по протоколу на 7-й день после трансплантации не выявила отторжения аллотрансплантатов. У пациентов R2 и R14 проводилась биопсия по показаниям из-за временного повышения креатинина в сыворотке, но не выявила отклонений. У обоих пациентов креатинин в сыворотке вернулся к исходному уровню без дополнительных процедур. У пациента R1 из группы A, получившего лишь 1% от количества клеток МИК, вводимого в группах B и C, обнаружились пограничные изменения при биопсии на 77-й день. У этого пациента биопсия проводилась после повышения креатинина в сыворотке на 0,2 мг/дл от исходного уровня. У пациента R11 была обнаружена инфекция мочевыводящих путей, вызванная E. coli, на 128-й день после операции, потребовавшая хинолонового антибиотика. Уровень креатинина в сыворотке возрос с 1,31 мг/дл до приема антибиотика до максимума в 1,81 мг/дл на 157-й день. Процедура биопсии выявила сильное интерстициальное воспаление (i3) с почти полным отсутствием тубулита (t1), что свидетельствует об аллергическом интерстициальном нефрите. После введения метилпреднизолона по 125 мг на протяжении 3 дней уровень креатинина в сыворотке вернулся к исходному уровню у обоих пациентов.
Таким образом, было установлено, что биопсия также подтверждает отсутствие отторжения аллотрансплантатов.
Пример 1.3. Реакции Т-лимфоцитов против донора у пациентов, получавших МИК
У пациентов из группы C сохранялась пролиферация лимфоцитов в ответ на неспецифические поликлональные стимуляторы на 360-й день после трансплантации по сравнению с таковой до введения МИК, что указывает на сохранение интактного общего иммунитета (см. фиг. 1A). Это подтверждалось при аллогенной стимуляции клетками от стороннего субъекта (см. фиг. 1B). Напротив, T-клеточный ответ против донора отсутствовал на 360-й день по сравнению с таковым до введения МИК (см. фиг. 1B). В то время как у пациентов, получавших МИК, были подавлены реакции Т-лимфоцитов, у 5 из 6 контрольных пациентов сохранялась реакционная способность по отношению к донору (см. фиг. 1C).
Пример 1.4. Антитела к HLA и титры антител против бактериальных и вирусных антигенов
В течение фазы наблюдения не обнаруживалось никаких донор-специфичных антител de novo. Этот результат поднял вопрос о том, происходит ли реакция B-клеток памяти на не связанные с донором антигены, индуцированная во время предыдущих иммунизаций. Титры антител против кори (в среднем 4400 мЕд/мл, 200-11000), эпидемического паротита (в среднем 400 мЕд/мл, 230-8000), краснухи (в среднем 41 Ед/мл, 9-160), ветряной оспы (в среднем 1350 мЕд/мл, 410-3500), дифтерии (в среднем 0,165 Ед/мл, 0,04-0,33) и столбняка (в среднем 1,45 Ед/мл, 0,5-2,1) были самыми низкими на 30-й день после пересадки почек, но в дальнейшем достигали уровней до трансплантации.
Пример 1.5. Уровни T-лимфоцитов, B-лимфоцитов и NK-клеток до трансплантации и через 1 год после трансплантации
Количество T-лимфоцитов CD4+ и CD8+, а также активированных T-лимфоцитов CD4+ и CD8+ оставалось стабильным до и после трансплантации. Уровни B-лимфоцитов CD19+ были самыми высокими на 30-й день после операции, в среднем 300 клеток/мкл (149-561), но возвращались к уровням до трансплантации на 180-й день со средним значением 35 клеток/мкл (25-247). Для NK-клеток CD16+CD56+ данные были обратными: количество этих клеток было на самом низком уровне на 30-й день после трансплантации, в среднем 60 клеток/мкл (33-73), но возрастало до среднего уровня, составляющего 104 клетки/мкл (93-154) на 180-й день.
Пример 1.6. Количество регуляторных T-лимфоцитов не изменяется, но сильно возрастает количество регуляторных B-лимфоцитов, начиная со 135-го дня после трансплантации
Количество регуляторных T-лимфоцитов (Treg) было низким на 30-й день после трансплантации (см. фиг. 4A-B) в период самой сильной иммуносупрессивной терапии. Затем среднее содержание T-лимфоцитов CD4+CD25+FoxP3+CD127− повышалось с 1% (0-1) до 3% (1-5) на 180-й день (см. фиг. 4B). Это значение было сравнимо с уровнем в 2,5% (2-4) до трансплантации и до лечения.
Интересно, что содержание незрелых B-лимфоцитов CD19+CD24highCD38high (регуляторных B-лимфоцитов, Breg) было низким до 90-го дня после трансплантации со средним значением 2,0% (0,1-5,5) на 30-й день (см. фиг. 4 и 5). После этого уровень Breg возрастал до среднего значения 20,4% (5,0-39,6) на 180-й день, намного превысив уровни до трансплантации, которые в среднем составляли всего 5,7% (0,4-11,2) до введения МИК. Только у пациента R11, нуждающегося в системной терапии метилпреднизолоном, за 1 месяц до этого, уровень Breg на 180-й день был ниже - 5,0%. У этого пациента уровень Breg снова возрастал, достигая 17,0% при последнем наблюдении на 670-й день. Не только относительное содержание, но и абсолютное количество Breg возрастало от среднего в 4,5 клеток/мкл (0,3-14,8) на 30-й день до 10 клеток/мкл (3,8-15,3) на 180-й день и 14,2 клеток/мкл (4,0-23,9) на 270-й день.
Содержание Breg у пациентов группы C в сравнении с содержанием Breg по 40 измерениям у 31 совместимого реципиента трансплантата почки без введения МИК представлено на фиг. 7. До введения МИК эти значения были сравнимы между пациентами группы C и контрольными пациентами со средним значением 5,7% против 11,2%, соответственно. Напротив, у получавших МИК пациентов содержание Breg резко возрастало после трансплантации и было в 19, 26 и 13 раз выше на 180-й, 270-й и 360-й день после трансплантации, соответственно, по сравнению с контролем.
Особый интерес представлял вопрос о том, возрастает ли уровень Breg также и у пациентов в группах A (получавших меньшую дозу клеток в день 2) и B (получавших полную дозу клеток в день 2). Для этого проводили анализ Breg в замороженных образцах. Как и ожидалось, у пациентов в группе C обнаруживались самые высокие уровни Breg, превышающие значения у пациентов в группах A и B в 68 и 20 раз, соответственно, на 180-й день после трансплантации (см. фиг. 6). Наиболее важно то, что в период после трансплантации большинство клеток Breg от пациентов группы C продуцировали иммуносупрессивный цитокин IL-10 (в среднем 44-100%) (см. фиг. 8).
Группа изобретений относится к применению фармацевтической композиции при профилактике и/или лечении отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком. Применение фармацевтической композиции, включающей или состоящей из: лейкоцитов и/или мононуклеарных клеток периферической крови (PBMC), обработанных терапевтически эффективным количеством активного вещества, при профилактике и/или лечении отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком, причем указанные лейкоциты или PBMC выделены или происходят от донора трансплантата, при этом профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту фармацевтической композиции, причем количество фармацевтической композиции выбрано таким образом, чтобы ввести от 1×108 до 1×1012 обработанных лейкоцитов или обработанных PBMC на 1 кг массы тела реципиента, причем клетки вводятся реципиенту за 5-28 дней до трансплантации, при этом активное вещество включает или представляет собой митомицин С. Применение фармацевтической композиции, включающей или состоящей из: лейкоцитов или мононуклеарных клеток периферической крови (PBMC), обработанных терапевтически эффективным количеством активного вещества, причем активное вещество представляет собой или включает митомицин С, при профилактике или лечении отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком, а указанные лейкоциты или PBMC выделены или происходят от донора трансплантата, при этом композиция характеризуется тем, что: общее количество обработанных лейкоцитов или обработанных PBMC в фармацевтической композиции составляет от 1×108 до 1×1012, причем клетки вводятся реципиенту за 5-28 дней до трансплантации. Вышеописанное применение у человека обеспечивает увеличение количества Breg CD19+CD24highCD38high, что повышает эффективность трансплантационной терапии, обеспечивает эффективную профилактику и/или лечение отторжения органа или клеточного трансплантата у человека. 2 н. и 7 з.п. ф-лы, 8 ил., 3 табл., 1 пр.
1. Применение фармацевтической композиции, включающей или состоящей из:
лейкоцитов и/или мононуклеарных клеток периферической крови (PBMC), обработанных терапевтически эффективным количеством активного вещества,
при профилактике и/или лечении отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком, причем указанные лейкоциты или PBMC выделены или происходят от донора трансплантата,
при этом профилактика и/или лечение отторжения органа или клеточного трансплантата включает введение реципиенту фармацевтической композиции, причем количество фармацевтической композиции выбрано таким образом, чтобы ввести от 1×108 до 1×1012 обработанных лейкоцитов или обработанных PBMC на 1 кг массы тела реципиента,
причем клетки вводятся реципиенту за 5-28 дней до трансплантации,
при этом активное вещество включает или представляет собой митомицин С.
2. Применение по п. 1, где композиция содержит фармацевтически приемлемый носитель.
3. Применение по любому из пп. 1 и 2, где клетки вводятся за одну процедуру введения.
4. Применение по любому из предыдущих пунктов, в котором PBMC включают моноциты и лимфоциты.
5. Применение по любому из пп. 2-4, в котором фармацевтически приемлемый носитель, если он содержится в композиции, включает или представляет собой одно или несколько веществ, выбранных из группы, состоящей из сахаров, таких как лактоза, глюкоза и сахароза; крахмалов, таких как кукурузный крахмал и картофельный крахмал; целлюлозы и ее производных, таких как натриевая карбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; порошкообразного трагаканта; солода; желатина; талька; наполнителей типа масла какао и воска для свечей; масел, таких как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликолей типа пропиленгликоля; сложных эфиров типа этилолеата и этиллаурата; агара; буферных веществ типа гидроксида магния и гидроксида алюминия; альгиновой кислоты; апирогенной воды; изотонического солевого раствора; раствора Рингера; этилового спирта, фосфатных буферных растворов; нетоксичных совместимых смазывающих веществ типа лаурилсульфата натрия и стеарата магния; а также красителей, высвобождающих веществ, покрывающих веществ, подсластителей, ароматизаторов и отдушек, консервантов и антиоксидантов.
6. Применение по любому из предыдущих пунктов, в котором введение осуществляют внутривенно, внутримышечно или подкожно, предпочтительно путем инфузии.
7. Применение фармацевтической композиции, включающей или состоящей из:
лейкоцитов или мононуклеарных клеток периферической крови (PBMC), обработанных терапевтически эффективным количеством активного вещества, причем активное вещество представляет собой или включает митомицин С,
при профилактике или лечении отторжения органа или клеточного трансплантата у реципиента трансплантата, который является человеком, а указанные лейкоциты или PBMC выделены или происходят от донора трансплантата,
при этом композиция характеризуется тем, что:
общее количество обработанных лейкоцитов или обработанных PBMC в фармацевтической композиции составляет от 1×108 до 1×1012,
причем клетки вводятся реципиенту за 5-28 дней до трансплантации.
8. Применение по п. 7, где композиция содержит фармацевтически приемлемый носитель.
9. Применение по любому из пп.1-8, где клетки вводятся реципиенту через 4-48 часов после их обработки активным веществом.
| KLEIST CHRISTIAN ET AL | |||
| "Generation of suppressive blood cells for control of allograft rejection.", CLINICAL SCIENCE (LONDON, ENGLAND: 1979) MAY 2015, (201505), vol | |||
| Сепаратор-центрофуга с периодическим выпуском продуктов | 1922 |
|
SU128A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| EHSER S ET AL | |||
| "Suppressive dendritic cells as | |||
Авторы
Даты
2023-11-01—Публикация
2019-05-17—Подача