[001] Данная заявка на изобретение направлена на медицинский сектор и включает долговременно рассасывающийся подкожный имплантат с длительным высвобождением фармакологически активного вещества, предварительно концентрированного в полимере, для лечения хронической надпочечниковой недостаточности или гипокортицизма.
Состояние техники (Предыстория изобретения)
[002] Хроническая надпочечниковая недостаточность, или гипокортицизм, является патологией и может быть разделена на два типа: первичный и вторичный. Хроническая первичная надпочечниковая недостаточность, также известная как болезнь Аддисона (ad), характеризуется нарушением зон, ответственных за выработку минералокортикоидов и глюкокортикоидов, что приводит к дефициту базового производства кортизола и повышенному уровню адренокортикотропного гормона (АКТГ). С другой стороны, хроническая вторичная недостаточность надпочечников характеризуется неспособностью гипофиза секретировать адренокортикотропный гормон (АКТГ), при этом заболевание характеризуется низкой продукцией АКТГ и кортизола без нарушения секреции минералокортикоидов. В обоих случаях наблюдается нарушение выработки андрогенов и предшественников андрогенов надпочечников, таких как DHEA.
[003] Правильная диагностика и лечение имеют решающее значение для обеспечения качества жизни пациентов с хронической недостаточностью надпочечников или гипокортицизмом.
[004] Пациенты, страдающие этим заболеванием, имеют пониженное качество жизни с точки зрения здоровья, повышенные сердечно-сосудистые факторы риска, риск остеопороза, повышенную смертность и часто медленно начинают получать лечение из-за наличия клинических признаков, очень похожих на симптомы других заболеваний. Серьезным осложнением, которое может возникнуть у пациентов, имеющих заболевание, и непроходящих лечение или недостаточно проходящих лечение, является аддисонический криз. Аддисонический криз вызывается стрессовыми событиями для пациента, такими как, например, инфекции, травмы, операции, обезвоживание. У нормальных пациентов после стрессового события система реагирует увеличением секреции кортизола. С другой стороны, у пациентов, страдающих этим заболеванием, наблюдается дефицит секреции кортизола, и этот дефицит секреции перед лицом стрессовых событий завершается кризом надпочечников. Надпочечниковый криз (Аддисонический), если его не лечить быстро, может привести пациента к смерти.
[005] Лечение первичной хронической надпочечниковой недостаточности осуществляется путем замены глюкокортикоидов и минералокортикоидов. При вторичной хронической надпочечниковой недостаточности лечение проводится путем замены только глюкокортикоидов. Наиболее часто используемыми глюкокортикоидами являются гидрокортизон и ацетат кортизона. Рекомендуемая дозировка для пациентов с хронической недостаточностью надпочечников составляет 20-30 мг перорального гидрокортизона (НС) в день, что эквивалентно 25-37,5 мг ацетата кортизона (СА), разделенного на две или три дозы, причем половина или две трети общей дозы вводится утром, сразу после пробуждения. Другой вариант глюкокортикоидов-преднизолон, который имеет длительный срок службы. Его дозировка составляет от 3 до 5 мг в день, только в одной дозе или делится на два раза. Минералокортикоид, используемый только для пациентов с болезнью Аддисона, представляет собой флудрокортизон, а дозировка составляет 0,05-0,2 мг в день, принимается один раз утром.
[006] Целью заменительной терапии гидрокортизоном у пациентов с хронической недостаточностью надпочечников является оптимизация качества жизни этих пациентов и минимизация побочных эффектов лечения. Это должно быть сделано из адекватности дозировок лекарств в зависимости от клинических симптомов пациента и путем попытки имитировать естественный цикл секреции кортизола, также известный как циркадный цикл. Циркадный цикл характеризуется повышенной секрецией кортизола в течение дня, главным образом под воздействием света, и снижением секреции кортизола ночью, чтобы позволить отдых.
[007] Среди доступных вариантов лекарств для лечения хронической надпочечниковой недостаточности есть несколько аспектов, которые следует учитывать. Чтобы ацетат кортизона стал биологически активным для использования в организме, он сначала должен метаболизироваться до кортизола (гидрокортизона) через фермент в печени. Способность данного фермента может ограничивать количество ацетата кортизона, превращенного в кортизол, поэтому рекомендуется использовать сам гидрокортизон, а не ацетат кортизона.
[008] С другой стороны, преднизолон имеет гораздо более длительный биологический период полураспада, чем гидрокортизон и ацетат кортизона, что может привести к гораздо большей активности этого глюкокортикоида ночью. Повышенная активность этого глюкокортикоида ночью неблагоприятна для лечения, так как концентрация этого препарата в организме должна быть максимально приближена к циркадному циклу.
[009] Гидрокортизон представляет собой наиболее широко используемый препарат и показан для лечения хронической надпочечниковой недостаточности. Однако, несмотря на то, что пероральное лечение гидрокортизоном восстанавливает уровень гормонов надпочечников, оно не восстанавливает нормальный биоритм кортизола в соответствии с циркадным циклом. Исследования показывают, что путем измерения уровня циркулирующего кортизола пероральное лечение гидрокортизоном генерирует в организме очень высокую дозу лекарства сразу после перорального приема и оставляет его недолеченным в течение нескольких часов после его введения.
[010] Кроме того, другие исследования указывают на то, что многие пациенты с первичной надпочечниковой недостаточностью, получающие традиционное заместительное лечение глюкокортикоидами и минералокортикоидами, все еще испытывают некоторые симптомы, такие как усталость, тошнота и головная боль. Это может быть связано с невозможностью имитировать естественный циркадный ритм кортизола, поскольку естественный пик начинается с начала быстрого движения глаз в ранние утренние часы, а пик гидрокортизона утром происходит через некоторое время после приема препарата внутрь. Эта временная надпочечниковая недостаточность первым делом с утра вызывает симптомы усталости, усталости, тошноты и головной боли, которые улучшаются через 30-60 минут после приема лекарства.
[011] Помимо перорального приема, существует еще одна форма введения гидрокортизона пациентам с хронической недостаточностью надпочечников через инсулиновую помпу, содержащую препарат. Было проведено исследование, сравнивающее лечение гидрокортизоном у пациентов, страдающих болезнью Аддисона, перорально и путем непрерывной подкожной инфузии препарата. Непрерывная подкожная инфузия проводилась с использованием инсулиновой помпы. В течение дня устройство высвобождало в организм различные дозировки раствора гидрокортизона, и пациентам приходилось менять раствор и инфузионный аппарат каждые три дня. Результаты исследования показали, что технология непрерывной подкожной инфузии препарата может восстановить циркадный ритм кортизола и нормализовать утренние уровни АКТГ у пациентов с болезнью Аддисона, результат, который не обнаруживается при пероральном лечении. Кроме того, пероральное лечение привело к существенному изменению структуры глюкокортикоидных метаболитов и метаболической активности ферментов, в то время как непрерывная подкожная инфузия восстановила метаболизм глюкокортикоидов, близкий к норме. Лечение непрерывной подкожной инфузией по-прежнему приводило к более физиологическому циркадному биоритму кортизола и вызывало изменения в метаболизме глюкокортикоидов, аналогичные метаболизму здорового человека.
[012] Традиционные пути введения, как пероральный, так и непрерывная подкожная инфузия, имеют несколько недостатков по сравнению с инновациями, предложенными в настоящем документе. Одним из недостатков является более низкая терапевтическая приверженность. По данным Всемирной организации здравоохранения, терапевтическая приверженность определяется взаимодействием между системой здравоохранения и персоналом, социально-экономическими факторами, факторами, связанными с пациентом, лечением и заболеванием. Соблюдение режима лечения является одним из основных факторов, связанных с успехом или неудачей лекарственного терапевтического подхода. Часто терапевтический результат не так положителен, как ожидалось, из-за поведения пациента, по разным причинам он не продолжает лечение, и при этом препарат не дает ожидаемого эффекта.
[013] Хронические заболевания, такие как первичная и вторичная хроническая недостаточность надпочечников, заставляют пациента принимать по крайней мере одно лекарство, часто более одного раза в день, на неопределенный срок, чтобы держать болезнь под контролем. Увеличение количества лекарств, принимаемых пациентом в день, снижает приверженность к лечению примерно на 20%, а лекарства, используемые в нескольких дозах, также снижают приверженность по сравнению с однократной дозой.
[014] Кроме того, примерно 50% пациентов с хроническими заболеваниями не принимают свои лекарства в соответствии с предписаниями. Постоянство приема лекарств среди этих пациентов очень низкое и резко снижается после первых шести месяцев терапии. Хронические заболевания длительны и могут значительно ухудшить качество жизни страдающих от них из-за возможности высокой физической, эмоциональной и/или экономической нагрузки. Лечение этих хронических состояний требует постоянного внимания и приверженности пациентов, а сочетание длительного лечения с отсутствием симптомов после приема лекарств снижает приверженность лечению традиционными лекарственными подходами.
[015] Пероральный путь наиболее подвержен сбоям, поскольку он всегда зависит от активного участия (или соответствия) пациента. Пациенты обычно правильно используют препарат только через 5 дней после консультации с врачом или при появлении острых симптомов. Однако, чтобы получить все преимущества лекарственной терапии, важно, чтобы пациент использовал рекомендуемые дозы в промежутках времени, указанных врачом. В то время как при подкожной инфузии также необходимо сотрудничество пациента для замены раствора препаратом, очистки устройства и введения новой иглы два-три раза в неделю. Кроме того, пациент несет ответственность за правильное хранение раствора лекарства, которое будет использоваться, что очень важно для успеха лечения. Эта зависимость от пациента значительно ухудшает терапевтическую приверженность и приводит к нарушению лечения.
[016] Наиболее эффективным способом повышения приверженности пациентов к лечению является упрощение дозировок лекарств. При многих хронических заболеваниях разработка препаратов с пролонгированным высвобождением позволила упростить дозировки.
[017] Другим недостатком перорального применения гидрокортизона является легкость неправильного использования назначенного лекарства, повышение риска недодозировки или сверхфизиологических доз, приводящих пациентов к возможному рецидиву симптомов, ухудшающих их общее состояние при лечении.
[018] Таким образом, можно найти третий вариант, известный как биорассасывающиеся гидрокортизоновые имплантаты или гранулы для лечения хронической недостаточности надпочечников. Такие имплантаты демонстрируют замедленное высвобождение лекарственного средства в течение длительного периода времени, чтобы лечить заболевание, делать лечение независимым от приема лекарств пациентом и пытаться воспроизвести циркадный цикл кортизола в организме, тем самым улучшая его клинические симптомы.
[019] Термины "имплантат" или "гранула" относятся к этой фармацевтической форме, уже закрепленной в официальных сборниках стандартов для лекарственных средств и фармацевтических веществ. Они характеризуются тем, что представляют собой твердые стерильные препараты подходящего размера и формы для парентеральной имплантации и высвобождения активного вещества(веществ) в течение длительного периода времени.
[020] Термины "длительное высвобождение", "медленное высвобождение" или "замедленное высвобождение" относятся к форме высвобождения лекарственного средства через имплантат, которая происходит непрерывно и постепенно в течение длительного периода времени и не приводит к немедленному и концентрированному высвобождению лекарственного средства в организме.
[021] Биоразлагаемые полимеры или биоразрушаемые полимеры относятся к полимерам, которые разлагаются in vivo и эрозия которых происходит с течением времени одновременно с высвобождением терапевтического агента и/или впоследствии. Биоразлагаемый полимер может представлять собой гомополимер, сополимер или полимер, сжимающий более двух полимерных звеньев. В некоторых случаях биоразлагаемый полимер может включать смешивание двух или более гомополимеров или сополимеров.
[022] Под биоразлагаемыми имплантатами или биоразрушаемыми имплантатами понимаются имплантаты, которые имеют некоторый механизм постепенного уменьшения их массы в течение длительного периода времени высвобождения. Силы, участвующие в данном уменьшении массы, могут представлять собой взаимодействие клеток или силы сдвига на поверхности имплантата. Кроме того, возможна эрозия, а также постепенное растворение ее компонентов. Термины также относятся к полной деградации и абсорбции организмом, которая происходит в том месте, где были применены имплантаты, исключая необходимость удаления имплантатов в конце лечения.
[023] Ссылаясь на патентные регистрации, касающиеся рассасывающихся имплантатов, в документе US 4957119 (Контрацептивный имплантат) упоминается имплантат из полимерного материала, который может высвобождать контрацептивное средство в течение относительно длительного времени при корректировке подкожным или местным путем. Имплантат включает материал ядра из сополимера этилена и винилацетата, который действует как матрица для контрацептивного вещества, мембраны из этилена и винилацетата, окружающей материал ядра, и контактного слоя на границе между материалом ядра и мембраной, который предотвращает разделение материала от ядра мембраны.
[024] Хотя в регистрации US 4957119 заявлен разлагаемый имплантат, используются разные активные вещества, его производство осуществляется посредством экструзии, а период высвобождения активного вещества очень длительный (не менее 1 года), что отличает настоящее изобретение от рассасывающегося подкожного имплантата.
[025] Второй регистрационный номер US9980850 (Биоразлагаемый контрацептивный имплантат и способы его применения) описывает биоразлагаемый контрацептивный имплантат и способы применения в форме биоразлагаемой гранулы с контролируемым высвобождением для подкожной имплантации. Биоразлагаемый осадок обеспечивает пролонгированное высвобождение контрацептивного средства в течение длительного периода времени. Продукты биоэрозии растворимы в воде, био-абсорбируются или делают и то, и другое, что исключает необходимость хирургического удаления имплантата.
[026] Так же, как и в первой упомянутой предыдущей регистрации, в данной регистрации US 9980850 также используются разные активные вещества, период высвобождения активного вещества очень длительный (от 6 месяцев до 4 лет), и предпочтительным способом изготовления гранул является процесс формования за счет горячего слияния.
[027] Принимая во внимание недостатки и ранее существовавшие проблемы в традиционных методах лечения хронической надпочечниковой недостаточности или гипокортицизма, настоящее изобретение направлено на лечение патологии, улучшение клинических симптомов пациентов и попытку воспроизвести циркадный ритм с помощью разлагаемого подкожного имплантата с пролонгированным высвобождением активного вещества, способного высвобождать препарат непосредственно в кровоток во избежание печеночного метаболизма. Другим преимуществом настоящего изобретения является улучшение приверженности пациентов к лечению, поскольку им не нужно помнить о периодическом применении лекарств. Кроме того, в конце лечения имплантатами нет необходимости их удалять, проводится только повторная установка новых для поддержания лечения.
Описание рисунков
[028] Для лучшего понимания настоящего изобретения прилагаются следующие чертежи:
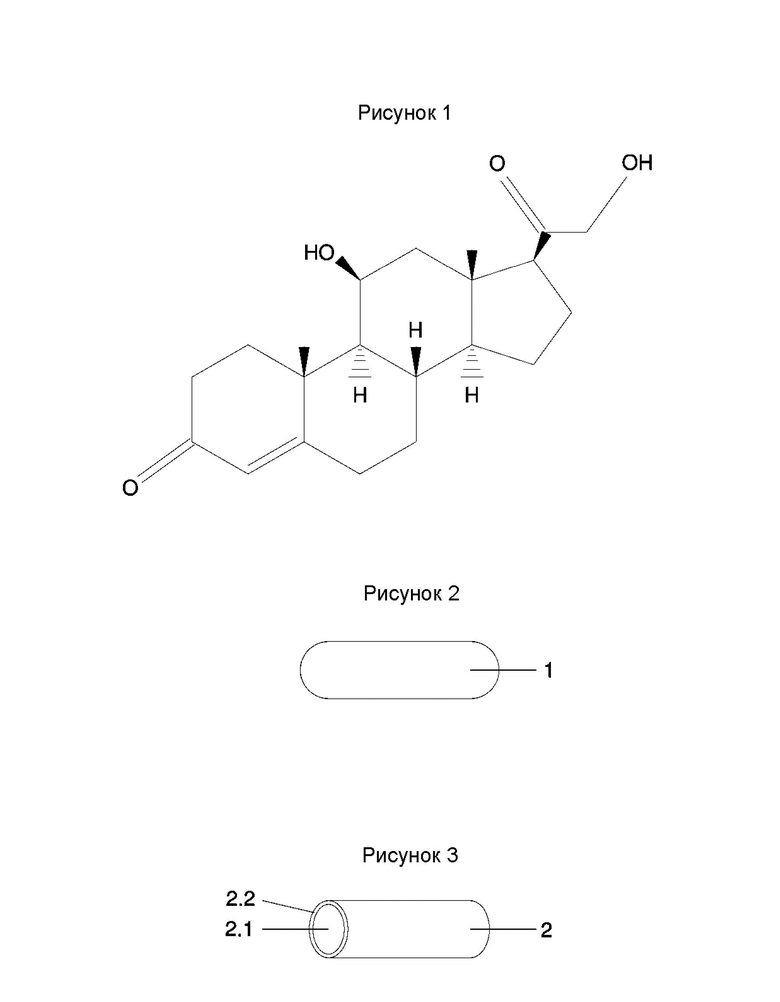
[029] Рисунок 1 - Представление химической структуры вещества гидрокортизона;
[030] Рисунок 2 - Размеры биорассасывающегося гидрокортизонового имплантата;
[031] Рисунок 3 - Размеры небиорассасывающегося гидрокортизонового имплантата;
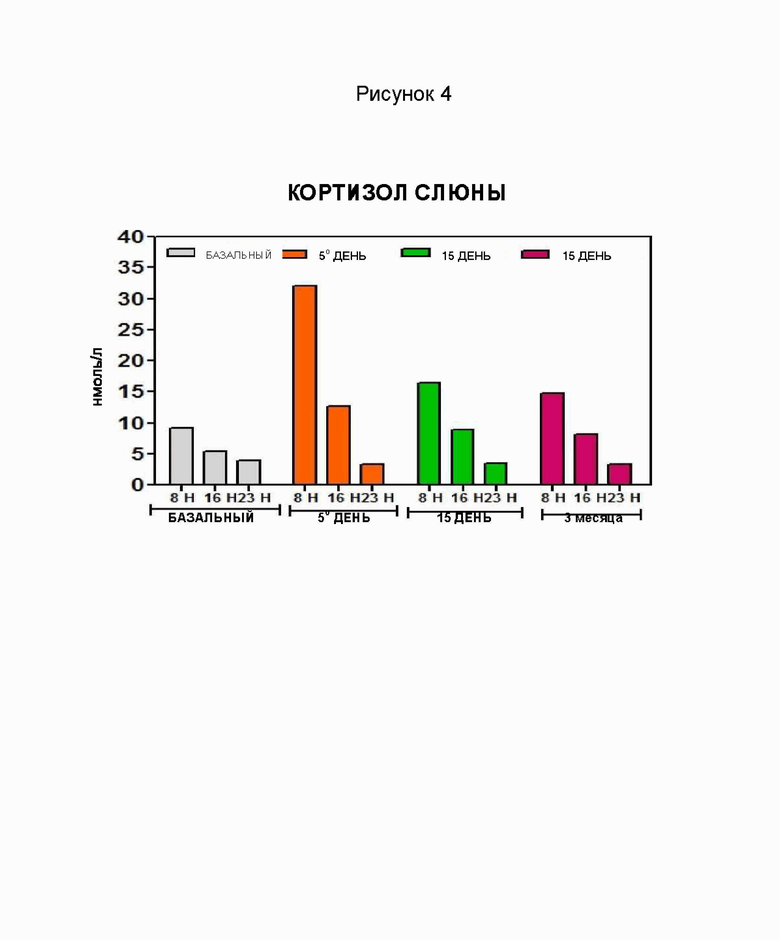
[032] Рисунок 4 - График содержания кортизола в слюне у пациентов, проходящих лечение гидрокортизоновыми имплантатами.
Подробное описание изобретения
[033] Настоящее изобретение представляет собой биоразлагаемый гидрокортизоновый имплантат в полимерной матрице. Имплантат вводится подкожно и имеет непрерывное высвобождение актива в течение длительного периода времени. Это высвобождение направлено на обеспечение эффективного, постоянного и длительного уровня препарата в сыворотке для лечения хронической недостаточности надпочечников.
[034] «Активное вещество», «активный» или «лекарственное средство» относится к гидрокортизоновому веществу, которое имеет химическую структуру, показанную на рисунке 1.
[035] Имплантат по настоящему изобретению может иметь в своем составе только гидрокортизон, но предпочтительно он образован частицами гидрокортизона, однородно распределенными в биоразлагаемой и биорассасывающейся полимерной матрице. Данная полимерная матрица может быть образована полимером или смесью полимеров. Количество гидрокортизона, присутствующего в имплантате, может варьироваться от 5 до 250 мг на имплантат, а его состав составляет от 1 до 20% биоразлагаемого полимера пропорционально его весу. Желательно иметь от 40 до 200 мг и от 2 до 10% биоразлагаемого полимера пропорционально весу.
[036] Используемый биоразлагаемый полимер может представлять собой: поли(D-молочную кислоту), поли(L-молочную кислоту), поли(рацемическую молочную кислоту), поли(гликолевую кислоту), поли(капролактон), метилцеллюлозу, этилцеллюлозу, гидроксипропилцеллюлозу (НРС) гидроксипропилметилцеллюлоза (НРМС), поливинилпирролидон (PVP), поливиниловый спирт) (PVA), поли(этиленоксид) (РЕО), полиэтиленгликоль, крахмал, натуральную и синтетическую камедь и воск.
[037] Имплантаты могут иметь любой размер, форму или структуру, что облегчает их изготовление и внутрикожное введение, однако для получения более постоянного и равномерного высвобождения активного вещества необходимо использовать геометрические формы, сохраняющие площадь поверхности во времени.
[038] Таким образом, имплантат, разработанный и продемонстрированный в настоящей заявке, имеет цилиндрическую форму, стержнеобразную форму, снабженную прямыми или закругленными концами, длиной от 2 до 25 мм и диаметром от 1 до 6 мм. Схематический рисунок примера размера имплантата (1) показан на рисунке 2.
[039] Изготовление гидрокортизонового имплантата может осуществляться путем добавления от 5 до 250 мг препарата в раствор выбранной биоразлагаемой полимерной матрицы в пропорции от 1 до 20% по отношению к массе гидрокортизона, с образованием однородной смеси. Если полимерный растворитель также не является растворителем гидрокортизона, он будет распространен в виде частиц или суспензии, и может быть использован миксер, чтобы сделать раствор однородным. Затем этот раствор сушат и затем формуют до формы имплантата (1) или другой желаемой формы.
[040] Другой возможный способ изготовления имплантата гидрокортизона - из смеси от 5 до 250 мг лекарственного средства и от 1 до 20% биоразлагаемой полимерной матрицы, выбранной по отношению к массе этого лекарственного средства, в его сухих, порошкообразных формах. Лекарственное средство и полимерная матрица добавляются в подходящую емкость и смесь приводится в однородное состояние.
[041] Смесь активных веществ для изготовления имплантата может быть сформирована под давлением или при нагревании, чтобы не снижать эффективность лекарственного средства и не разрушать полимерный материал. Вариантами техники формования имплантата могут быть: литье под давлением, горячее формование, прессование или экструзия.
[042] Для настоящего изобретения выбранным методом было прессование. В этом методе смешивание активов в порошкообразном виде добавляется в форму, и под смесью применяется механическая сила, вызывающая сжатие частиц и, следовательно, формование имплантата в соответствующем формате (1). После этого происходит наполнение и стерилизация имплантата гидрокортизоном. Его стерилизация может производиться теплом или гамма-лучами. Стерилизацию желательно проводить теплом, в печи при 90°С, в течение 1 часа.
[043] Имплантат может иметь полимерную мембрану с покрытием толщиной от 0,1 до 0,7 мм. Полимер, используемый для покрытия, должен быть биорассасывающимся и обеспечивать прохождение активного вещества. Покрытие имплантата предпочтительно делается путем погружения имплантата в полимерный раствор. Покрытие может покрывать всю поверхность имплантата, включая края, только его продольную поверхность с краями без покрытия или покрытие только по краям имплантата без покрытия его длины. Полимеры, которые могут быть использованы для покрытия: Поли(молочная кислота-гликолевая кислота) (PLGA) и сополимеры D, L-молочной кислоты.
[044] Еще одним вариантом имплантата для лечения хронической надпочечниковой недостаточности являются небиоразлагаемые имплантаты. Небиоразлагаемые или небиоразрушаемые имплантаты (2) (рисунок 3) имеют центральное ядро (2.1), образованное полимерной матрицей в процентном соотношении от 1 до 20% по отношению к массе препарата, в данном случае от 5 до 250 мг гидрокортизона, ядро которого окружено неразлагаемой полимерной мембраной (2.2), контролирующей скорость высвобождения лекарственного средства.
[045] Материалом изготовления полимерной мембраны, окружающей имплант, могут быть: силикон, уретан, акрилаты и их сополимеры, сополимеры поливинилиденфторида, полиэтиленвинилацетат-этиленвинил, диметилполисилоксан. Такая мембрана имеет толщину от 0,2 до 1 мм и отлита из собственного оборудования. После формования мембраны из полимерного материала происходит вставка активной смеси, образующей центральное ядро (2.1) имплантата (2). Полимеры, используемые в полимерной матрице смеси, используют те же соединения и процесс, что и биорассасывающийся имплантат.
[046] Высвобождение лекарственного средства в данной системе происходит посредством диффузии с относительно постоянной скоростью, и скорость высвобождения лекарственного средства можно изменять за счет толщины или материала этой мембраны. В этой системе необходимо удалить имплантат в конце лечения.
[047] Лечение хронической надпочечниковой недостаточности с использованием гидрокортизоновых имплантатов должно определяться в соответствии с тяжестью симптомов и клиническим состоянием пациента. Выработка кортизола у нормальных пациентов, не страдающих этим заболеванием, составляет примерно от 8,7 до 12,2 мг в день. Что касается имплантата, то он высвобождает от 0,6 до 1,2 мг гидрокортизона в день, в зависимости от количества присутствующего в нем препарата. Лечение имплантатами действует как параллельное производство гидрокортизона с замедленным высвобождением, поскольку у пациентов с хронической недостаточностью надпочечников выработка эндогенного кортизола ниже, чем у нормальных пациентов. На практике при использовании 3-5 имплантатов гидрокортизона с выделением от 1,8 до 6,0 мг гидрокортизона в день наблюдается значительное улучшение клинической картины и качества жизни пациента.
[048] Однако для того, чтобы определить индивидуальное лечение для каждого пациента, врачу необходимо оценить клиническое состояние этого пациента, использовать свои лабораторные тесты в качестве поддержки для принятия решения о дозировке и ежедневном высвобождении препарата гидрокортизона имплантатами, начните прием с частичных доз ниже максимально возможной выработки, чтобы контролировать ремиссию симптомов и развитие клинического состояния пациента. После этой первой оценки доза может быть скорректирована путем установки дополнительных имплантатов, в случае необходимости. Кроме того, в случае отторжения или каких-либо побочных реакций после установки имплантата его можно удалить в течение первых нескольких дней лечения.
[049] Использование предлагаемого здесь имплантата является безопасным и эффективным при лечении хронической недостаточности надпочечников или гипокортицизма, учитывая, что терапия не зависит от воли пациента или дисциплины в отношении действия лекарственного средства, что гарантирует поддержание дозировки и регулярность лечения. Следует отметить, что пациенты, страдающие хроническими патологиями, часто прекращают лечение, когда замечают изменение симптомов или когда они испытывают некоторый дискомфорт из-за побочных эффектов или реакций, становясь более восприимчивыми к ухудшению своей клинической картины. Таким образом, использование данных имплантатов в терапевтических целях предотвращает прекращение лечения и гарантирует надлежащее лечение, а также его эффективность.
[050] Кроме того, изобретение предлагает пациентам с хронической недостаточностью надпочечников терапию постоянными и стабильными дозами с непрерывным высвобождением активного начала. Постоянное поддержание дозы обеспечивает регуляцию, более похожую на циркадный ритм эндогенного кортизола, и не блокирует оставшуюся функциональную активность надпочечников, сохраняя при этом физиологическую выработку.
[051] Еще одним преимуществом данного изобретения является то, что высвобождение лекарственного средства через имплантаты происходит непосредственно в кровоток, что делает его действие намного более эффективным и предотвращает печеночный метаболизм лекарственного средства.
[052] Другое преимущество изобретения заключается в виде и способе подачи имплантата, биоразлагаемом и разлагаемым, не требующем его удаления после периода лечения, поскольку он не оставляет следов в тканях.
[053] Было проведено исследование для оценки эффективности использования гидрокортизоновых имплантатов, описанных здесь, для лечения хронической недостаточности надпочечников. Было отобрано пять пациентов, пораженных этим заболеванием. Среди основных симптомов, о которых сообщали пациенты, были: чрезмерная усталость, низкая энергия, увеличение веса, задержка воды, умственная усталость, бессонница, тяга к сладкому, снижение иммунитета, повышенная болевая чувствительность, тревога, депрессия и трудности в преодолении стрессовых ситуаций. [054] Образцы слюны этих пациентов собирали для определения базального уровня кортизола (ТО) утром и снижения уровня кортизола в течение 24 часов. Уровни кортизола, обнаруженные у нормальных людей, у которых нет патологии, составляют от 13,1 до 23,5 нмоль/л утром, от 3,0 до 8,0 нмоль/л днем и от 1,0 до 2,9 нмоль/л вечером.
[055] Результаты, полученные по базальному кортизолу слюны (Т0) у этих пациентов, составили 8,86±0,89 нмоль/л утром, 5,42±0,44 нмоль/л днем и 3,5±0,57 ночью. Данные результаты свидетельствуют о значительном снижении уровня кортизола, секретируемого надпочечниками в течение дня, и последующем нарушении ответной реакции гипоталамо-гипофизарно-надпочечниковой оси, характерной для этой патологии.
[056] Для оценки ответа на лечение имплантатами использовали три имплантата гидрокортизона по 100 мг каждый, которые вводили в жировой слой на спине пациентов.
[057] После установки имплантатов новые сборы слюны проводили утром, днем и вечером: через 24 часа после имплантации (Т1), через пять дней после имплантации (Т5), через семнадцать дней после имплантации (Т17) и через девяносто дней после имплантации (Т90) для определения уровня кортизола.
[058] При анализе данных, полученных от кортизола слюны пациентов, можно наблюдать, что все они показали значительное повышение уровня кортизола в момент времени Т1, достигнув максимального пика высвобождения во время Т5 и поддержание уровня кортизола в пределах ожидаемых ориентировочных значений после времени Т17. Через 90 дней (Т90) уровни поддерживались в пределах физиологической нормы. Такое поведение показано на графике на рисунке 4.
[059] Из этого исследования можно сделать вывод, что разработанный имплантат соответствует целям лечения хронической надпочечниковой недостаточности, поскольку непрерывное высвобождение препарата поддерживалось в течение предложенного минимального периода 90 дней, происходило восстановление нормального физиологических уровней кортизола в течение 24 часов, у пациентов наблюдалось восстановление циркадного ритма и большая ремиссия ранее отмеченных неблагоприятных симптомов заболевания.
Группа изобретений относится к долгосрочному разлагаемому подкожному имплантату с пролонгированным высвобождением предварительно концентрированного фармацевтически активного вещества в полимере для лечения хронической надпочечниковой недостаточности или гипокортизолизма, который характеризуется тем, что биоразлагаемый гидрокортизоновый имплантат остается в полимерной матрице при том, что в составе биоразлагаемого имплантата от 5 до 250 мг гидрокортизона, однородно распределенного в указанной биорассасывающейся полимерной матрице, причем состав полимерной матрицы составляет от 1 до 20% биоразлагаемого полимера по отношению к массе гидрокортизона, и также относится к долгосрочному разлагаемому подкожному имплантату с пролонгированным высвобождением предварительно концентрированного фармацевтически активного вещества в полимере для лечения хронической надпочечниковой недостаточности или гипокортизолизма, который характеризуется тем, что имплантат представлен в небиоразлагаемой или небиоразрушаемой форме (2), имеющей центральное ядро (2.1), образованное полимерной матрицей в процентном соотношении от 1 до 20% по отношению к массе лекарственного средства, в данном случае от 5 до 250 мг гидрокортизона, ядро окружено неразлагаемой полимерной мембраной (2.2). Группа изобретений обеспечивает снижение воспаления и боли, а также восстановление циркадного цикла пациента с целью восстановления физиологии жизни-бодрствования днем и сна ночью. 2 н. и 6 з.п. ф-лы, 4 ил.
1. Долгосрочный разлагаемый подкожный имплантат с пролонгированным высвобождением предварительно концентрированного фармацевтически активного вещества в полимере для лечения хронической надпочечниковой недостаточности или гипокортизолизма, который характеризуется тем, что биоразлагаемый гидрокортизоновый имплантат остается в полимерной матрице при том, что в составе биоразлагаемого имплантата от 5 до 250 мг гидрокортизона, однородно распределенного в указанной биорассасывающейся полимерной матрице, причем состав полимерной матрицы составляет от 1 до 20% биоразлагаемого полимера по отношению к массе гидрокортизона.
2. Имплантат согласно п.1, в котором биоразлагаемый полимер представляет собой поли(d-молочную кислоту), поли(l-молочную кислоту), поли(рацемическую молочную кислоту), поли(гликолевую кислоту), поли(капролактон), метилцеллюлозу, этилцеллюлозу, гидроксипропилцеллюлозу (ГПЦ), гидроксипропилметилцеллюлозу (ГПМЦ), поливинилпирролидон (ПВП), поли(виниловый спирт) (ПВС), поли(этиленоксид) (ПЭО), полиэтиленгликоль, крахмал, натуральную камедь, синтетическую камедь и воск.
3. Имплантат согласно пп.1 и 2, который характеризуется геометрической формой имплантата (1), представляющей собой цилиндрическую форму, стержнеобразную форму, снабженную прямыми или закругленными концами, длиной от 2 до 25 мм и диаметром от 1 до 6 мм.
4. Имплантат согласно пп.1-3, который характеризуется тем, что гидрокортизоновый имплантат изготавливают путем добавления от 5 до 250 мг препарата в выбранный раствор биорассасывающейся полимерной матрицы в пропорции от 1 до 20% по отношению к массе препарата до образования однородной смеси, с высушиванием раствора и последующим формованием до формы имплантата (1).
5. Имплантат согласно пп.1-3, который характеризуется тем, что гидрокортизоновый имплантат изготавливают путем получения смеси от 5 до 250 мг препарата и биорассасывающейся полимерной матрицы в пропорции от 1 до 20% по отношению к массе препарата в сухой порошкообразной форме, с добавлением лекарственного средства и полимерной матрицы в емкость до приведения в однородное состояние смеси с последующим помещением смеси в форму для формования путем сжатия под действием механической силы, вызывающей сжатие частиц и последующее формование имплантата в соответствующем формате (1), наконец, происходит заполнение и стерилизация гидрокортизонового имплантата нагреванием в печи при 90°C в течение 1 часа.
6. Имплантат согласно пп.1-4, который характеризуется тем, что биоразлагаемый имплантат имеет полимерную мембрану с биорассасывающимся покрытием толщиной от 0,1 до 0,7 мм для прохождения активного вещества на всей поверхности имплантата, включая края, только на продольной поверхности с краями без покрытия или покрытие только по краям имплантата без покрытия его длины, причем указанное покрытие образовано поли(молочной кислотой-со-гликолевой кислотой) (ПЛГК) и сополимерами d,l-молочной кислоты.
7. Долгосрочный разлагаемый подкожный имплантат с пролонгированным высвобождением предварительно концентрированного фармацевтически активного вещества в полимере для лечения хронической надпочечниковой недостаточности или гипокортизолизма, который характеризуется тем, что имплантат представлен в небиоразлагаемой или небиоразрушаемой форме (2), имеющей центральное ядро (2.1), образованное полимерной матрицей в процентном соотношении от 1 до 20% по отношению к массе лекарственного средства, в данном случае от 5 до 250 мг гидрокортизона, ядро окружено неразлагаемой полимерной мембраной (2.2).
8. Имплантат в соответствии с п.7, который характеризуется тем, что материалом для изготовления полимерной мембраны, окружающей небиоразлагаемый имплантат, являются силикон, уретан, акрилаты и их сополимеры, поливинилиденфторидные сополимеры, полиэтилен винил ацетат-этиленвинил и диметилполисилоксан, обладающие вышеупомянутой мембраной толщиной от 0,2 до 1 мм, и после его формования происходит введение гидрокортизона, образующего центральное ядро (2.1) имплантата (2).
| BR 102016018206 A2, 06.03.2018 | |||
| WO 2007089544 A2, 09.08.2007 | |||
| WO 2009035562 A2, 19.03.2009. |
Авторы
Даты
2024-12-09—Публикация
2020-08-31—Подача