Изобретение относится к химии и технологии получения борорганических соединений, в частности С-арилзамещенных 1,2-дикарба-клозо-додекаборанов (12) (opтo-карборанов), в том числе содержащих заместители при атомах бора, представленных формулой
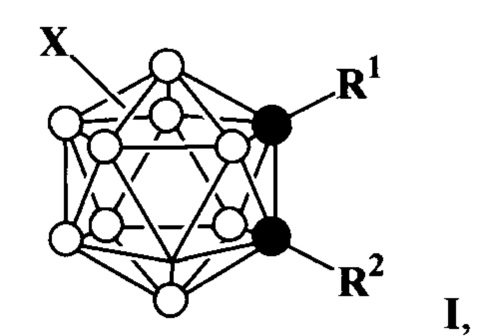
где в качестве арильного заместителя могут выступать как моноядерные (фенил), так и аннелированные полиядерные (нафтил, антраценил, пиренил) ароматические группы, а заместители при атомах бора могут представлять собой атомы галогенов (фтор, хлор, бром, иод), или арильную группу, находящиеся в разных положениях бороуглеродного каркаса.
Такие арилзамещенные opтo-карбораны являются перспективными для создания на их основе устройств молекулярной электроники [Li, X., Yan, Н., Zhao, Q. Chem. Eur. J., 2016, v. 22, №6, p.1888; Ochi, J., Tanaka, K., Chujo, Y. Angew. Chem. Int. Ed., 2020, v. 132, №25, p.9925] и медицинских препаратов [Scholz, M., Hey-Hawkins, E. Chem. Rev., 2011, v. 111, №11, p.7035; Stockmann, P., Gozzi, M., Kuhnert, R., Sarosi, M.B., Hey-Hawkins, E. Chem. Soc. Rev., 2019, v. 48, №13, p.3497].
Известные традиционные способы получения С-арилзамещенных орто-карборанов основаны на взаимодействии соответствующих арилацетиленов с декабораном(14) в присутствии мягких оснований Льюиса, таких, как диметилсульфид, ацетонитрил, и N,N-диметиланилин [Heying, T.L., Ager, J.W., Clark, S.L., Mangold, D.J., Goldstein, H.L., Hillman, M., Polak, R.J., Szymanski, J.W. Inorg. Chem., 1963, v. 2, №6, p.1089; Ohta, K., Goto, A.T., Endo, Y. Inorg. Chem., 2005, v. 44, №23, p.8569; Marsh, A.V., Dyson, M., Cheetham, N.J., Bidwell, M., Little, M., White, A.J.P., Warriner, C.N., Swain, A.C., McCulloch, I., Stavrinou, P.N., Meskers, S.C.J.; Heeney, M. Adv. Electron. Mater., 2020, v. 6, №8, 2000312; Kim, S., Lee, J.H., So, H., Kim, M., Mun, M.S., Hwang, H., Park, M.H., Lee, K.M. Inorg. Chem. Front., 2020, v. 7, №16, p.2949]. Однако при использовании этого подхода целевые продукты образуются с низкими выходами (особенно в случае аннелированных полиядерных арилов), кроме того, такой подход не может быть использован для синтеза С-арилпроизводных орто-карборанов, содержащих заместители при атомах бора.
Известен способ получения С-арилзамещенных карборанов, в котором используют реакции их С-медных производных с арилиодидами (Coult, R., Fox, М.А., Gill, W.R., Herbertson, P.L., MacBride, J.A.H., Wade, K. J. Organomet. Chem., 1993, v.462, №1-2, p.19. Ohta, K., Goto, A.T., Endo, Y. Inorg. Chem., 2005, v.44, №23, p.8569. Naito, H., Nishino, K., Morisaki, Y, Tanaka, K., Chujo, Y. Angew. Chem. Int. Ed., 2017, v.56, №1, p.254.). Этот способ можно использовать для получения С-арилпроизводных орто-карборанов, содержащих заместители при атомах бора, но целевые продукты образуются с невысокими выходами.
Еще один способ получения С-арил производных opтo-карборанов основан на взаимодействии С-литиевых производных карборанов с соответствующими арилиодидами и арилбромидами в присутствии Pd-катализатора (Lu, J.-Y, Wan, Н., Zhang, J., Wang, Z., Li, Y, Du, Y, Li, C, Liu, Z.-T., Liu, Z.-W, Lu, J. Chem. Eur. J., 2016, v.22, №49, p.17542.). Этот способ может быть использован для получения С-арилзамещенных орто-карборанов, содержащих заместители при атомах бора, однако выход целевых продуктов при использовании арилбромидов существенно ниже, чем при использовании арилиодидов. Кроме того, использование палладиевого катализатора и дорогих фосфиновых лигандов увеличивает стоимость целевых продуктов.
Наиболее близким и принятым в качестве прототипа является недавно опубликованный способ синтеза С-арилзамещенных opтo-карборанов, основанный на реакциях кросс-сочетания карборанильных реактивов Гриньяра с арилиодидами в присутствии каталитических количеств хлорида никеля NiCb (Tang, С, Xie, Z. Angew. Chem. Int. Ed., 2015, v.54, №26, p.7662. Wu, X., Guo, J., Cao, Y, Zhao, J., Jia, W, Chen, Y, Jia, D. Chem. Sci., 2018, v.9, №23, p.5270. Wu, X., Guo, J., Zhao, J., Che, Y, Jia, D., Chen, Y. Dyes and Pigments, 2018, v. 154, p.44). Этот способ также может быть использован для получения С-арилпроизводных opmo-карборана, содержащих дополнительные заместители при атомах бора, однако, несмотря на длительное время реакции, в ряде случаев он приводит только к незначительным выходам целевых продуктов.
Задача данного изобретения заключается в создании простого, эффективного и технологичного способа получения С-арилзамещенных opmo-карборанов формулы I, в том числе содержащих заместители при атомах бора, где в качестве арильного заместителя могут выступать моно- и полиядерные ароматические группы, а заместители при атомах бора могут представлять собой атомы галогенов (фтор, хлор, бром, иод), или арильные группы, находящиеся в разных положениях бороуглеродного каркаса.
Поставленная задача решена заявляемым способом получения С-арилзамещенных opтo-карборанов формулы (I)
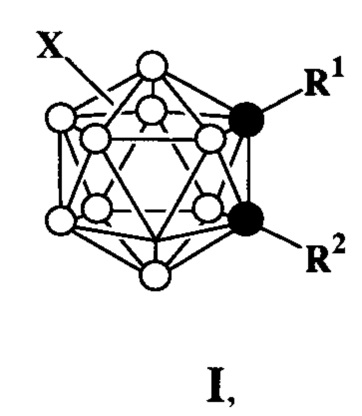
где R1=Н, Ar при R2=Ar; R2=Н, Ar при R1=Ar;
Ar = фенил, 1'-нафтил, 2'-антраценил, 1'-пиренил;
X = Н, F, Cl, Br, I, фенил.
Способ включает обработку незамещенного или B-замещенного opтo-карборана избытком бутилмагнийбромида в тетрагидрофуране в атмосфере аргона, взаимодействие полученного реактива Гриньяра с арилбромидом в том же растворителе при 120-150°С в присутствии 0,1-0,35 эквивалента безводного хлорида никеля по отношению к эквиваленту орто-карборана в тетрагидрофуране при микроволновом облучении в замкнутом объеме в течение 1-2 ч, при этом мольное соотношение незамещенного или B-замещенного орто-карборана и арилбромида составляет 1:1,5-2,0 для получения моноарилзамещенных орто-карборанов и 1:3,0 для получения диарилзамещенных opтo-карборанов; последующее охлаждение реакционной смеси, выделение целевого продукта известными приемами и его очистку колоночной хроматографией на силикагеле, где в качестве элюента используют хлористый метилен и петролейный эфир с объемным соотношением 1:1-4 или этилацетат и петролейный эфир с объемным соотношением 1:9.
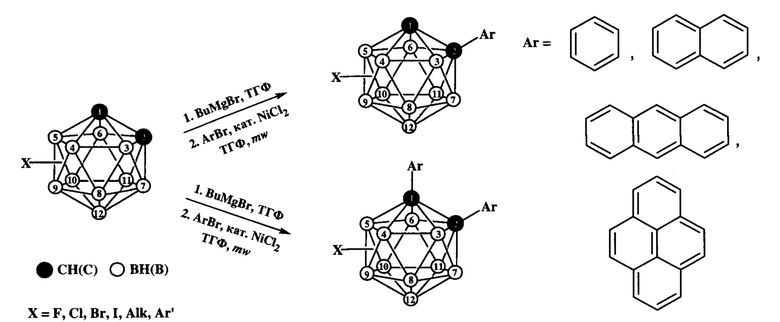
Достигнутый технический результат состоит в создании универсального и технологичного способа синтеза С-арилзамещенных opтo-карборанов, позволяющего получать как моно-, так и диарилпроизводные, в том числе B-замещенные, использовать более доступные и дешевые арилбромиды, вместо арилиодидов, уменьшить продолжительность процесса, увеличить его производительность и снизить энергозатраты.
Кроме того, не требуется заменять использующийся при получении реактивов Гриньяра растворитель на другой, это упрощает общую технологию процесса.
Более того, в ряде случаев заявляемый способ позволяет получать с хорошим и высоким выходом целевые С-арилзамещенные opтo-карбораны формулы I, которые образуются лишь в следовых количествах при использовании других способов или вообще не были известны ранее.
Получение С-арилзамещенных opтo-карборанов и их B-замещенных производных проводят с использованием системы микроволнового синтеза «NOVA 2S». В сухой реакционный сосуд для работы под давлением (30 мл) в атмосфере аргона помещают 1 эквивалент opтo-карборана или его B-замещенного производного и 15-20 мл сухого тетрагидрофурана. Полученный раствор охлаждают до 0°С, по каплям добавляют 4 эквивалента свежеприготовленного бутилмагнийбромида BuMgBr и перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 1,5-3,0 эквивалента арилбромида и 0,10 - 0,35 эквивалента хлорида никеля NiCl2, реакционный сосуд закрывают и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1-2 часов при 120-150°С. После этого реакционный сосуд охлаждают до 60°С и открывают. Реакционную смесь упаривают на роторном испарителе под вакуумом. К остатку добавляют 10% водный раствор соляной кислоты (10 мл), полученную смесь помещают на 5 минут в ультразвуковую баню, а затем фильтруют на стеклянном фильтре Шотта. Осадок на фильтре растворяют в ацетоне (60 мл) и полученный раствор упаривают в вакууме досуха. Сухой остаток подвергают очистке колоночной хроматографией на силикагеле.
Ниже приведены примеры осуществления предлагаемого способа. Пример 1. Получение 1-фенил-орто-карборана.
В сухой реакционный сосуд для работы под давлением (30 мл) в атмосфере аргона помещают 144,0 мг (1,00 ммоль) орто-карборана и 18 мл сухого тетрагидрофурана. Полученный раствор охлаждают до 0°С, по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr и перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 210 мкл (2,00 ммоль) бромбензола и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2, реакционный сосуд закрывают и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. После этого реакционный сосуд охлаждают до 60°С и открывают. Реакционную смесь упаривают на роторном испарителе под вакуумом. К остатку добавляют 10% водный раствор соляной кислоты (10 мл), полученную смесь помещают на 5 минут в ультразвуковую баню, а затем фильтруют на стеклянном фильтре Шотта. Осадок на фильтре растворяют в ацетоне (60 мл) и полученный раствор упаривают в вакууме досуха. Сухой остаток подвергают очистке колоночной хроматографией на силикагеле (элюент - этилацетат и петролейный эфир 1:9). Выход целевого продукта 91%. Спектральные данные целевого продукта идентичны описанным в литературе (Tang, С, Xie, Z. Angew. Chem. Int. Ed., 2015, v.54, №26, p.7662.).
Пример 2. Получение 1-(1'-нафтил)-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 144,0 мг (1,00 ммоль) орто-карборана и 17 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 210 мкл (1,50 ммоль) 1-бромнафталина и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - этилацетат и петролейный эфир 1:9). Выход целевого продукта 50%. Спектральные данные целевого продукта идентичны описанным в литературе (Tang, С, Xie, Z. Angew. Chem. Int. Ed., 2015, v.54, №26, p.7662.)
Пример 3. Получение 1,2-бис(1'-нафтил)-орто-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 144,0 мг (1,00 ммоль) opтo-карборана и 17 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 420 мкл (3,00 ммоль) 1-бромнафталина и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - этилацетат и петролейный эфир 1:9). Выход целевого продукта 45%. Спектральные данные целевого продукта идентичны описанным в литературе (Tang, С, Xie, Z. Angew. Chem. Int. Ed., 2015, v.54, №26, p.7662.)
Пример 4. Получение 1-(2'-антраценил)-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 144,0 мг (1,00 ммоль) opтo-карборана и 18 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 385,7 мг (1,50 ммоль) 2-бромантрацена и 13,0 мг (0,01 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - этилацетат и петролейный эфир 1:9). Выход целевого продукта 60%. Спектральные данные целевого продукта идентичны описанным в литературе (Wu, X., Guo, J., Jia, W, Zhao, J., Jia, D.; Shan, H. Dyes and Pigments, 2019, v.162, p.855.)
Пример 5. Получение 1,2-бис(2'-антраценил)-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 144,0 мг (1,00 ммоль) opтo-карборана и 19 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 771,5 мг (3,00 ммоль) 2-бромантрацена и 13,0 мг (0,01 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - этилацетат и петролейный эфир 1:9). Выход целевого продукта 37%. Спектральные данные целевого продукта идентичны описанным в литературе (Wu, X., Guo, J., Jia, W., Zhao, J., Jia, D.; Shan, H. Dyes and Pigments, 2019, v.162, p.855.)
Пример 6. Получение 1-(1'-пиренил)-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 144,0 мг (1,00 ммоль) opтo-карборана и 18 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 562,3 мг (2,00 ммоль) 1-бромпирена и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - этилацетат и петролейный эфир 1:9). Выход целевого продукта 88%. Спектральные данные целевого продукта идентичны описанным в литературе (Wu, X., Guo, J., Zhao, J., Che, Y.; Jia, D.; Chen, Y. Dyes and Pigments, 2018, v.154, p.44.)
Пример 7. Получение 1-(2'-антраценил)-3-фенил-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 220,0 мг (1,00 ммоль) 3-фенил-орто-карборана и 19 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 514,3 мг (2,00 ммоль) 2-бромантрацена и 13,0 мг (0,01 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:4). Выход целевого продукта 72%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,28 (с, 2Н), 7,95 (м, 2Н), 7,85 (с, 1Н), 7,76 (д, 1Н), 7,48 (м, 2Н), 7,37-7,35 (м, 2Н), 7,18 (д, 1Н), 7,11-7,05 (м, 3Н), 4,48 (с, 1Н, СНкарб), 1,71-3,77 (м, 9Н, ВН). Спектр ЯМР 11В (CDCl3, δ, м.д.): -2,1 (с, 1В), -3,7 (д, 2В), -7,9 (д, 1В), -9,7 (д, 1В), -10,7 (д, 2В), -11,6 (д, 2В), -14,4 (д, 1В).
Пример 8. Получение 1-(2'-антраценил)-3-фтор-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 162,0 мг (1,00 ммоль) 3-фтор-opтo-карборана и 18 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 385,7 мг (1,50 ммоль) 2-бромантрацена и 13,0 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:2). Выход целевого продукта 53%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,46 (с, 1Н), 8,43 (с, 1Н), 8,12 (с, 1Н), 8,03-8,01 (м, 3Н), 7,54-7,51 (м, 2Н), 7,46 (д, 1Н), 4,27 (с, 1H, СНкарб), 1,21-3,73 (м, 9Н, ВН). Спектр ЯМР 11B (CDC13, 5, м.д.): 0,4 (с, 1В), -6,1 (д, 2В), -12,1 (м, 4В), -13,9 (д, 1В), -16,6 (д, 1В), -17,7 (д, 1В). Спектр ЯМР 19F (CDCl3, δ, м.д.): -195,5.
Пример 9. Получение 1.2-бис(2'-антраценил)-3-фтор-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 162,0 мг (1,00 ммоль) 3-фтор-opтo-карборана и 18 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 771,4 мг (3,00 ммоль) 2-бромантрацена и 13,0 мг (0,01 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:2). Выход целевого продукта 41%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,28 (с, 2Н), 8,26 (с, 2Н), 8,20 (с, 2Н), 7,90-7,86 (м, 4Н), 7,72 (д, 2Н), 7,52 (д, 2Н), 7,43-7,41 (м, 4Н), 1,78-3,54 (м, 9Н, ВН). Спектр ЯМР 11В (CDC13, 6, м.д.): 1,5 (с, 1В), -5,6 (д, 2В), -10,9 (д, 2В), -12,3 (м, 4 В), -17,5 (д, 1В). Спектр ЯМР 19F (CDC13, 5, м.д.): -184,4.
Пример 10. Получение 1-(2'-антраценил)-3-иод-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 270,0 мг (1,00 ммоль) 3-иод-opтo-карборана и 17 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 514,3 мг (2,00 ммоль) 2-бромантрацена и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:4). Выход целевого продукта 66%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,48 (с, 1Н), 8,44 (с, 1H), 8,04-8,01 (м, 4Н), 7,54-7,52 (м, 2Н), 7,32 (д, 1Н), 4,39 (с, 1H, СНкарб), 1,69-3,86 (м, 9Н, ВН). Спектр ЯМР 11В (CDC13, 5, м.д.): -2,2 (д, 1В), -3,1 (д, 1В), -6,7 (д, 1В), -9,7 (м, 5 В), -12,9 (д, 1В),-23,3 (с, 1В).
Пример 11. Получение 1-(2'-антраценил)-9,12-дихлор-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 213,1 мг (1,00 ммоль) 9,12-дихлор-орто-карборана и 18 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 514,3 мг (2,00 ммоль) 2-бромантрацена и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:4). Выход целевого продукта 82%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,44 (с, 1H), 8,43 (с, 1H), 8,18 (с, 1H), 8.04-7.99 (м, 3Н), 7.55-7.53 (м, 2Н), 7,46 (д, 1H), 4,02 (с, 1Н, СНкарб), 1,79-3,83 (м, 8Н, ВН). Спектр ЯМР 11B (CDCl3, δ, м.д.): 7,3 (с, 1В), 6,2 (с, 1В), -7,9 (д, 2В), -12,1 (д, 2В),-14,4 (м, 4 В).
Пример 12. Получение 1-(2'-антраценил)-9,12-дибром-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 302,0 мг (1,00 ммоль) 9,12-дихлор-opтo-карборана и 19 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 385,7 мг (1,50 ммоль) 2-бромантрацена и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:1). Выход целевого продукта 68%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,45 (с, 1Н), 8,43 (с, 1H), 8.17 (с, 1Н), 8.04-7.99 (м, 3Н), 7,55-7,53 (м, 2Н), 7,45 (д, 1H), 4,21 (с, 1Н, СНкарб), 1,84-3,88 (м, 8Н, ВН). Спектр ЯМР 11В (CDCl3, δ, м.д.): 0,7 (с, 1В), -0,3 (с, 1В), -7,0 (д, 2В), -11,3 (м, 2В),-13,4(м, 4 В).
Пример 13. Получение 1,2-бис(2'-антраценил)-9,12-дибром-opтo-карборана.
Синтез проводят аналогично примеру 1.
В реакционный сосуд в атмосфере аргона помещают 302,0 мг (1,00 ммоль) 9,12-дихлор-орто-карборана и 19 мл тетрагидрофурана. Полученный раствор охлаждают до 0°С и по каплям добавляют 645,3 мг (4,00 ммоль) свежеприготовленного бутилмагнийбромида BuMgBr, реакционную смесь перемешивают в течение 12 часов. После этого к реакционной смеси добавляют 771,5 мг (3,00 ммоль) 2-бромантрацена и 45,4 мг (0,35 ммоль) хлорида никеля NiCl2 и подвергают микроволновому облучению в системе микроволнового синтеза при перемешивании в течение 1 часа при 150°С. Полученный продукт подвергают очистке колоночной хроматографией на силикагеле (элюент - хлористый метилен и петролейный эфир 1:1). Выход целевого продукта 42%.
Спектральные данные: Спектр ЯМР 1Н (CDCl3, δ, м.д.): 8,29 (с, 2Н), 8,19 (с, 2Н), 8.18 (с, 2Н), 7,91-7,85 (м, 4Н), 7,72 (д, 2Н), 7,45-7,42 (м, 6Н, CHAr), 1,14-4,21 (м, 8Н, ВН). Спектр ЯМР 11B (CDCl3, δ, м.д.): 1,16 (с, 2В), -8,52 (м, 6В), -12,39 (м, 2В).
| название | год | авторы | номер документа |
|---|---|---|---|
| КАРБОРАНОВЫЕ ПРОИЗВОДНЫЕ 4,4-ДИФТОР-4-БОРА-3а,4а-ДИАЗА-s-ИНДАЦЕНА, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2022 |
|
RU2789401C1 |
| КАРБОРАНИЛЬНЫЕ ПРОИЗВОДНЫЕ ФТОРИРОВАННЫХ ПОРФИРИНОВ И ИХ МЕТАЛЛОКОМПЛЕКСЫ, ПРОЯВЛЯЮЩИЕ СВОЙСТВА ФОТОСЕНСИБИЛИЗАТОРА, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2402554C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,7,8,9-ТЕТРААЛКИЛ-4-МЕТИЛ-4-АЗА-10-МАГНЕЗАТРИЦИКЛО[5.2.1.0]ДЕЦ-8-ЕН-3,5-ДИОНОВ | 2006 |
|
RU2313529C1 |
| 3,5-ДИАРИЛИЗОКСАЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2021 |
|
RU2801861C2 |
| ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ EGFR | 2021 |
|
RU2815022C1 |
| АНАЛОГИ ВИТАМИНА D, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМОПЗИЦИЯ | 1997 |
|
RU2183622C2 |
| СПОСОБ ПОЛУЧЕНИЯ С, С'-КАРБОРАНДИКАРБОНОВЫХ КИСЛОТ | 2014 |
|
RU2559625C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4-(3,5-ДИФЕНИЛФУРАН-2-ИЛ)БУТАН-2-ОНА | 2016 |
|
RU2634000C1 |
| СРЕДСТВО ПЕПТИДНОЙ ПРИРОДЫ, ВКЛЮЧАЮЩЕЕ ПСМА-СВЯЗЫВАЮЩИЙ ЛИГАНД НА ОСНОВЕ ПРОИЗВОДНОГО МОЧЕВИНЫ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ КОНЪЮГАТА С ЛЕКАРСТВЕННЫМ И ДИАГНОСТИЧЕСКИМ АГЕНТОМ | 2018 |
|
RU2697519C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,8,9,10-ТЕТРААЛКИЛ-11-МАГНЕЗАТРИЦИКЛО[6.2.1.0]УНДЕЦ-9-ЕН-3,6-ДИОНОВ | 2006 |
|
RU2313528C1 |
Изобретение относится к области химии и технологии борорганических соединении, конкретно к методу синтеза С-арилзамещенных 1,2-дикарба-клозо-додекаборанов(12) (opтo-карборанов) и их B-замещенных производных. Способ получения C-арилзамещенных орто-карборанов формулы (I)
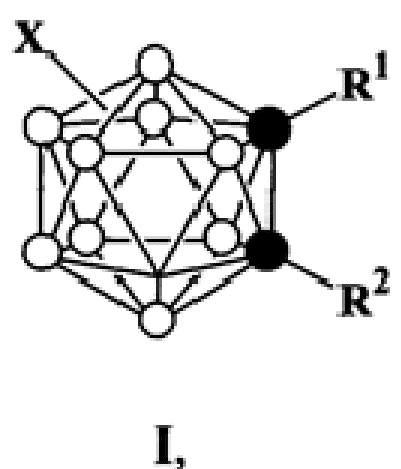
где R1 = Н, Ar при R2 = Ar; R2 = Н, Ar при R1 = Ar; Ar = фенил, 1'-нафтил, 2'-антраценил, 1'-пиренил; X = Н, F, Cl, Br, I, фенил, включает обработку незамещенного или B-замещенного орто-карборана избытком бутилмагнийбромида в тетрагидрофуране в атмосфере аргона, взаимодействие полученного реактива Гриньяра с арилбромидом в том же растворителе при 120-150°С в присутствии 0,1-0,35 эквивалента безводного хлорида никеля по отношению к эквиваленту орто-карборана в тетрагидрофуране при микроволновом облучении в замкнутом объеме в течение 1-2 ч. Мольное соотношение незамещенного или B-замещенного орто-карборана и арилбромида составляет 1:1,5-2,0 для получения моноарилзамещенных орто-карборанов и 1:3,0 для получения диарилзамещенных орто-карборанов. После охлаждения реакционной смеси выделяют целевой продукт и очищают его колоночной хроматографией. Технический результат – обеспечение простым и эффективным способом получения желаемого продукта. 2 з.п. ф-лы, 13 пр.
1. Способ получения C-арилзамещенных орто-карборанов формулы (I)
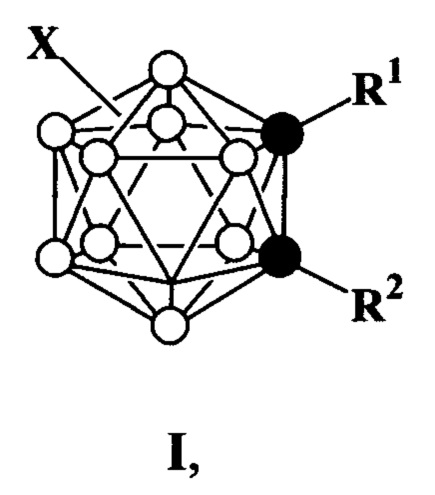
где R1 = Н, Ar при R2 = Ar; R2 = Н, Ar при R1 = Ar;
Ar = фенил, 1'-нафтил, 2'-антраценил, 1'-пиренил;
X = Н, F, Cl, Br, I, фенил,
включающий обработку незамещенного или B-замещенного орто-карборана избытком бутилмагнийбромида в тетрагидрофуране в атмосфере аргона, взаимодействие полученного реактива Гриньяра с арилбромидом в том же растворителе при 120-150°С в присутствии 0,1-0,35 эквивалента безводного хлорида никеля по отношению к эквиваленту орто-карборана в тетрагидрофуране при микроволновом облучении в замкнутом объеме в течение 1-2 ч, при этом мольное соотношение незамещенного или B-замещенного орто-карборана и арилбромида составляет 1:1,5-2,0 для получения моноарилзамещенных орто-карборанов и 1:3,0 для получения диарилзамещенных орто-карборанов; последующее охлаждение реакционной смеси, выделение целевого продукта известными приемами и его очистку колоночной хроматографией.
2. Способ по п. 1, в котором колоночную хроматографию проводят на силикагеле, а в качестве элюента используют хлористый метилен и петролейный эфир с объемным соотношением 1:1-4.
3. Способ по п. 1, в котором колоночную хроматографию проводят на силикагеле, а в качестве элюента используют этилацетат и петролейный эфир с объемным соотношением 1:9.
| Wu X | |||
| et al | |||
| Mechanically Triggered Reversible Stepwise Tricolor Switching and Thermochromism of Anthracene-o-carborane Dyad | |||
| Chem | |||
| Sci., v | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Телефонная трансляция с катодными лампами | 1921 |
|
SU5270A1 |
| Tang С | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Chem | |||
| Int | |||
| Ed., v | |||
Авторы
Даты
2024-12-09—Публикация
2023-12-28—Подача