Изобретение относится к медицине, а именно к онкологии и лучевой терапии.
Согласно действующим гайдлайнам, стандартом лечения высокозлокачественных глиом (ВЗГ) головного мозга является послеоперационный курс химиолучевой терапии в дозе 60 Гр на фоне приема Темозоломида как составляющая комплексного лечения первичных ВЗГ. Однако, медиана локального контроля у данной когорты составляет порядка 7 месяцев. Рецидивы локализуются до 90-95% случаев в полях предшествующего облучения, что ограничивает повторное использование стандартных методик лучевой терапии у таких больных ввиду высоких рисков неврологической токсичности, связанных с ростом кумулятивной дозы.
Возможности повторного облучения значительно расширись после знакового исследования, ознаменовавшегося введением в клиническую практику Бевацизумаба (Friedman HS, Prados MD, Wen PY, et al. Bevacizumab alone and in combination with irinotecan in recurrent glioblastoma. J Clin Oncol. 2009;27(28):4733-4740. doi:10.1200/JCO.2008.19.8721).
Применение Бевацизумаба сочетании с лучевой терапией в сравнении только с его системным введением в отдельных исследованиях, включенных в крупный мета-анализ, коррелировало с увеличением медианы безрецидивной выживаемости вплоть до 12 месяцев и снижением развития токсичности со стороны центральной нервной системы до 9% у пациентов с ВЗГ (Marwah R, Xing D, Squire T, Soon YY, Gan HK, Ng SP. Reirradiation versus systemic therapy versus combination therapy for recurrent high-grade glioma: a systematic review and meta-analysis of survival and toxicity. J Neurooncol. 2023;164(3):505-524. doi:10.1007/s11060-023-04441-0). В случае конкурентного режима введения Бевацизумаба ключевую роль, по-видимому, играли как его цитотоксические свойства, так и противовоспалительное, и радимодифицирующее влияния.
Известны способы применения стереотаксической лучевой терапии на основе фотонного излучения с введением Бевацизумаба в дозе 10 мг/кг в 1-й день лечения (Zhang JF, Okai B, Iovoli A, et al. Bevacizumab and gamma knife radiosurgery for first-recurrence glioblastoma. J Neurooncol. 2024;166(1):89-98. doi:10.1007/s11060-023-04524-y; Park KJ, Kano H, Iyer A, Liu X, Niranjan A, Flickinger JC, Lieberman FS, Lunsford LD, Kondziolka D. Salvage gamma knife stereotactic radiosurgery followed by bevacizumab for recurrent glioblastoma multiforme: a case-control study. J Neurooncol. 2012 Apr;107(2):323-33. doi: 10.1007/s11060-011-0744-9). Подходы позволяют увеличить медиану безрецидивной выживаемости до 7,7 месяцев, снизить риски радиационной токсичности до 10%.
Основными недостатками таких способов является реализация преимущественно профилактического в отношении рисков радиационного некроза эффекта Бевацизумаба, так как его синергетические с облучением свойства не успевают реализоваться за время курса стереотаксической лучевой терапии, а также невозможность его применения к рецидивам большого объема.
Наиболее близкими являются два следующих способа.
Первый способ гипофракционированной модулированной по интенсивности фотонной лучевой терапии заключается в подведении 35 Гр в 10 ежедневных фракциях на фоне Бевацизумаба в дозе 10 мг/кг в 1-й и 15-й дни лучевого лечения (Tsien CI, Pugh SL, Dicker AP, et al. NRG Oncology/RTOG1205: A Randomized Phase II Trial of Concurrent Bevacizumab and Reirradiation Versus Bevacizumab Alone as Treatment for Recurrent Glioblastoma. J Clin Oncol. 2023;41(6):1285-1295. doi:10.1200/JCO.22.00164).
Во втором случае применялась импульсная фотонная лучевая терапия с пониженной мощностью дозы в режиме стандартного фракционирования (10 импульсных доз по 0,2 Гр каждые 3 минуты, до 2 Гр) до 52 Гр за 26 фракций с внутривенным введением Бевацизумаба в дозе 10 мг/кг (Bovi JA, Prah MA, Retzlaff AA, et al. Pulsed Reduced Dose Rate Radiotherapy in Conjunction With Bevacizumab or Bevacizumab Alone in Recurrent High-grade Glioma: Survival Outcomes. Int J Radiat Oncol Biol Phys. 2020;108(4):979-986. doi:10.1016/j.ijrobp.2020.06.020). Методики позволяют увеличить медиану безрецидивной выживаемости до 7,1 и 12 месяцев соответственно для первого и второго способов с уровнем токсичности в работе Christina I Tsien и соавт. до 5%.
Недостатком данных способов является невозможность их безопасной реализации без снижения покрытия дозой целевых объемов облучения при локализации рецидивов вблизи критических структур, а также более широкое перекрытие предыдущего поля облучения, что приводит к росту кумулятивной дозы.
Целью настоящего изобретения является повышение эффективности терапии пациентов с рецидивами высокозлокачественных глиом (рВЗГ) головного мозга.
Задачей изобретения является обеспечение высоким покрытием радикальной дозой целевых объемов облучения, минимизация пересечения с предыдущими полями облучения, снижение рисков острой и поздней радиационной токсичности, а также некоторое увеличение показателей выживаемости.
Технический результат достигается тем, что так же, как и в известном способе (прототипе), проводят фотонную лучевую терапию на фоне Бевацизумаба.
Особенностью данного способа является то, что на этапе оконтуривания определяют первичный объем рецидива или его хирургического ложа с/без остаточной ткани (GTVr) по данным серий магнитно-резонансной томографии T1 и T2/FLAIR, определяют клинический объем мишени CTVr путем отступа 15 мм от GTVr с исключением из объема естественных барьеров при их интактности, формируют планируемый объем мишени PTVr путем отступа от CTVr на 3 мм, при завершении дозиметрического планирования проводят курс протонной терапии активным сканирующим пучком протонов в физической разовой очаговой дозе (РОД) 1,81 Гр до физической суммарной очаговой дозы (СОД) в 50,68 Гр, что с учетом относительной биологической эффективности протонного излучения 1,1 эквивалентно РОД 2,0 ГрЭ и СОД 56 ГрЭ, за 28 фракций на область рВЗГ головного мозга на фоне внутривенного введения Бевацизумаба в дозе 5-10 мг/кг каждые 2 недели на 1-й, 15-й и 30 дни курса протонной терапии соответственно. При необходимости дополнительно используют данные позитронно-эмиссионной компьютерной томографии с аминокислотными трейсерами (BTVr), а CTVr получают путем отступа 15 мм от GTVr + BTVr».
Способ поясняется подробным описанием, клиническими примерами и иллюстрациями, на которых изображено:
Фиг. 1 - Схема протокола лечения рВЗГ: Бевацизумаб вводился в дозе 5-10 мг/кг каждые 2 недели (на 1-й, 15-й и 30-й дни курса протонной терапии соответственно).
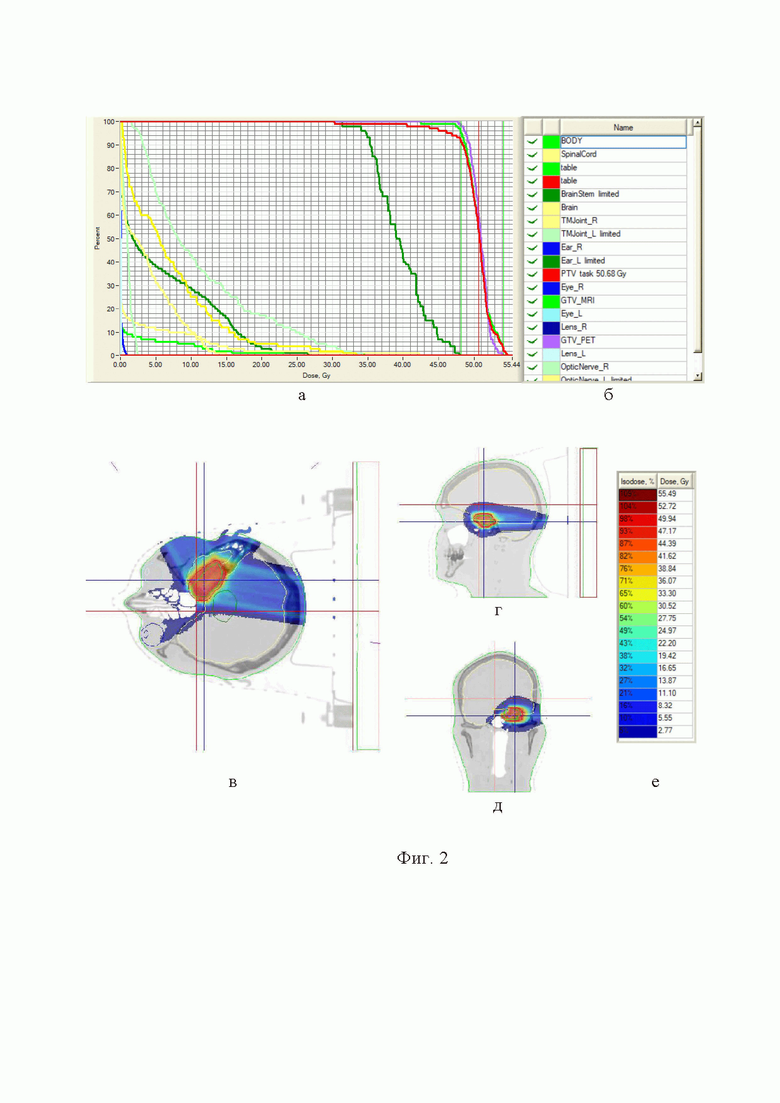
Фиг. 2 - гистограмма пациентки И.: а) доза-объем; б) с перечнем критических структур; в) распределение облучения по направлениям в аксиальной, г) сагиттальной и д) фронтальной проекциях; е) с градиентом доз (дозы представлены в физических эквивалентах).
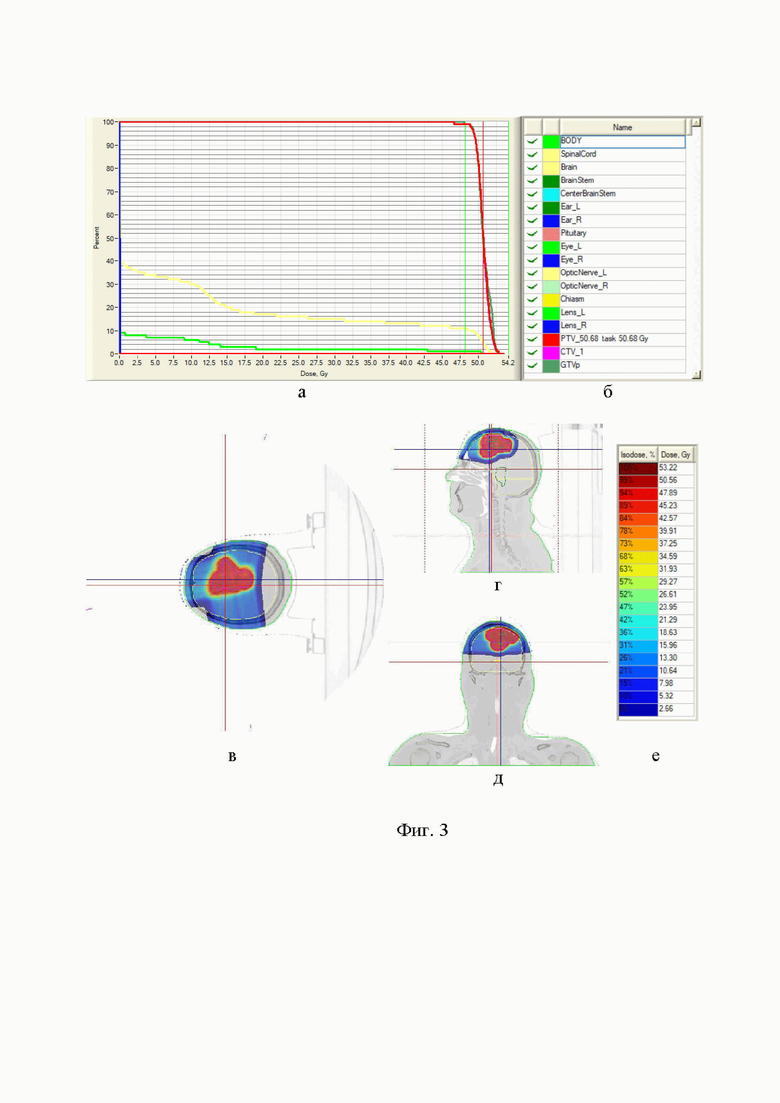
Фиг. 3 - гистограмма пациента Г.: а) доза-объем; б) с перечнем критических структур; в) распределение облучения по направлениям в аксиальной, г) сагиттальной и д) фронтальной проекциях; е) с градиентом доз (дозы представлены в физических эквивалентах).
Способ осуществляют следующим образом.
У пациентов с рВЗГ головного мозга на этапе оконтуривания первичный объем рецидива или его хирургического ложа с/без остаточной ткани (GTVr) определяют по данным серий магнитно-резонансной томографии (МРТ) T1 и T2/FLAIR. В дополнение к МРТ могут использовать данные позитронно-эмиссионной компьютерной томографии с аминокислотными трейсерами (BTVr). Клинический объем мишени (CTVr) формируют путем добавления отступов от GTVr + BTVr до 15 мм с исключением из объема естественных барьеров в случае их интактности. Планируемый объем мишени (PTVr) формируют путем отступа от CTVr на 3 мм. При завершении дозиметрического планирования проводят курс протонной терапии активным сканирующим пучком протонов в физической разовой очаговой дозе (РОД) 1,81 Гр до физической суммарной очаговой дозы (СОД) в 50,68 Гр, что эквивалентно РОД 2,0 ГрЕ и СОД 56 ГрЕ (относительная биологическая эффективность протонного излучения 1,1) за 28 фракции на область рВЗГ головного мозга на фоне внутривенного введения Бевацизумаба в дозе 5-10 мг/кг каждые 2 недели на 1-й, 15-й и 30 дни курса протонной терапии соответственно, согласно схеме на Фиг.1.
Предложенным способом проведена химиолучевая терапия у 19 пациентов с рецидивами морфологически подтвержденных ВЗГ (10 глиобластом Grade 4, 5 астроцитом и 2 олигодендроглиомы Grade 3, 1 глиосаркома Grade 4). У всех пациентов в предлагаемом режиме отмечалась хорошая переносимость курса лечения, проведенного в полном объеме. В отдельных случаях отмечалось увеличение периода безрецидивной выживаемости вплоть до 20 месяцев на момент последнего наблюдения. Не было зарегистрировано явлений неврологической и гематологической токсичности, ассоциированной с проводимым лечением, ≥3 степени тяжести.
Осуществление способа показано на конкретных клинических примерах.
Пример 1.
Пациентка И., 1972 г.р. Диагноз: Глиобластома левой височной доли. Комбинированное лечение в 2021 г. 12 курсов МХТ по схеме: Темозоломид. Рецидив в 2022 году.
Проведен повторный курс дистанционной лучевой терапии активным сканирующим пучком протонов на область рецидива опухоли, определяемой по данным серий МРТ Т1, Т2/FLAIR и ПЭТ/КТ с 18F-фторэтилтирозином. Отступ на CTVr не проводился ввиду выполнения визуализирующих исследований <2 недель до планирования лечения. Отступ на PTVr составил 3 мм. Облучение проводилось до СОД 56,0 ГрЕ за 28 фракций по 2,0 ГрЕ. Бевацизумаб вводился в конкурентном режиме в дозе 5,0 мг/кг на 1-й, 15-й и 30-й дни курса протонной терапии. Объем PTVr составил 15,1 см3.
Как видно из Фиг. 2 (а, б, в, г, д, е), несмотря на значительную близость полей облучения к стволу мозга и зрительному тракту, нагрузки на данные критические структуры были соблюдены при сохранении покрытия PTV на уровне 93%.
После завершения курса продолжена монохимиотерапия Бевацизумабом. На момент последнего наблюдения через 12,5 месяцев с момента окончания курса протонной терапии проведено 15 курсов (30 введений) Бевацизумаба. Отмечена стабилизация процесса, лучевых осложнений за время наблюдения не выявлено.
Пример 2.
Пациент Г., 1971 г.р. Диагноз: Олигодендроглиома левой лобной доли Grade 3, комбинированное лечение в 2020 году. 6 курсов химиотерапии Темозоломидом. Рецидив в 2021 году.
Проведен повторный курс дистанционной лучевой терапии активным сканирующим пучком протонов на область рецидива опухоли, определяемой по данным серий МРТ Т1 и Т2/FLAIR с отступами на CTVr и PTVr +15 и +3 мм соответственно в РОД 2,0 ГрЕ до СОД 56,0 ГрЕ за 28 фракций на фоне введения Бевацизумаба 10 мг/кг каждые 2 недели на 1-й, 15-й и 30 дни курса протонной терапии. Объем PTVr составил 133 см3.
На иллюстрациях (Фиг. 3 а, б, в, г, д, е) наглядно демонстрируется оптимальное соотношение нагрузок на критические структуры и покрытия rPTV.
После окончания курса продолжена монохимиотерапия Бевацизумабом. При контрольном обследовании через 20 месяцев – стабилизация процесса, признаков лучевых осложнений не наблюдалось.
При использовании способа не требовалось проведения дополнительных исследований в рамках предлучевой подготовки, доказана хорошая переносимость лечения без возникновения острых и поздних лучевых осложнений. Наблюдалось высокое качество жизни пациентов после проведения лечения.
Предложенный способ обеспечивает увеличение эффективности лечения рВЗГ головного мозга у взрослых путем сочетания физических и радиобиологических свойств протонного излучения с радиомодифицирующими и цитотоксическими эффектами Бевацизумаба за счет высокого покрытия радикальной дозой целевых объемов облучения при минимальном пересечении с предыдущими полями облучения, приводя к снижению радиационной токсичности и некоторому улучшению показателей выживаемости.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования эффективности комбинированной адаптивной стереотаксической лучевой терапии с бевацизумабом у мужчин со злокачественными глиомами головного мозга | 2023 |
|
RU2801419C1 |
| Способ стажированной лучевой терапии в лечении метастатических опухолей головного мозга при раке молочной железы | 2023 |
|
RU2827299C1 |
| Способ лучевой терапии больных с диссеминированной меланомой кожи и слизистых с множественным метастатическим поражением головного мозга | 2024 |
|
RU2836084C2 |
| Способ адъювантной адаптивной стереотаксической лучевой терапии в лечении первичных злокачественных глиальных опухолей головного мозга | 2021 |
|
RU2759405C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С РЕЦИДИВАМИ РАКА ГРУДНОГО ОТДЕЛА ПИЩЕВОДА В ПИЩЕВОДНО-ЖЕЛУДОЧНОМ АНАСТОМОЗЕ | 2019 |
|
RU2728192C1 |
| СПОСОБ ПАЛЛИАТИВНОЙ ЛУЧЕВОЙ ТЕРАПИИ ПРОЛАКТИНОМЫ ГИПОФИЗА У КРЫС | 2024 |
|
RU2828981C2 |
| СПОСОБ ЛЕЧЕНИЯ АРТЕРИОВЕНОЗНЫХ МАЛЬФОРМАЦИЙ ГОЛОВНОГО МОЗГА | 2013 |
|
RU2534233C1 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО РАКА ЖЕЛУДКА | 2020 |
|
RU2725079C2 |
| СПОСОБ НЕОАДЪЮВАНТНОГО ТЕРМОХИМИОЛУЧЕВОГО ЛЕЧЕНИЯ РАКА ПРЯМОЙ КИШКИ | 2018 |
|
RU2704205C2 |
| СПОСОБ ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО ПЛОСКОКЛЕТОЧНОГО РАКА АНАЛЬНОГО КАНАЛА | 2023 |
|
RU2809447C2 |

Изобретение относится к медицине, а именно к онкологии и лучевой терапии, и может быть использовано при комплексном лечении рецидива высокозлокачественных глиом (рВЗГ) головного мозга у взрослых. На этапе оконтуривания определяют первичный объем рецидива или его хирургического ложа с/без остаточной ткани (GTVr) по данным серий магнитно-резонансной томографии T1 и T2/FLAIR. Определяют клинический объем мишени CTVr путем отступа 15 мм от GTVr с исключением из объема естественных барьеров при их интактности. Формируют планируемый объем мишени PTVr путем отступа от CTVr на 3 мм. При завершении дозиметрического планирования проводят курс протонной терапии активным сканирующим пучком протонов в физической разовой очаговой дозе (РОД) 1,81 Гр до физической суммарной очаговой дозы (СОД) 50,68 Гр, что с учетом относительной биологической эффективности протонного излучения 1,1 эквивалентно РОД 2,0 ГрЭ и СОД 56 ГрЭ, за 28 фракций на область рВЗГ головного мозга на фоне внутривенного введения Бевацизумаба в дозе 5-10 мг/кг каждые 2 недели на 1-й, 15-й и 30-й дни курса протонной терапии соответственно. Способ обеспечивает увеличение эффективности лечения рВЗГ головного мозга у взрослых путем сочетания физических и радиобиологических свойств протонного излучения с радиомодифицирующими и цитотоксическими эффектами Бевацизумаба за счет высокого покрытия радикальной дозой целевых объемов облучения при минимальном пересечении с предыдущими полями облучения, приводя к снижению радиационной токсичности и улучшению показателей общей и безрецидивной выживаемости. 1 з.п. ф-лы, 3 ил., 2 пр.
1. Способ лечения рецидивов высокозлокачественных глиом (рВЗГ) головного мозга, включающий проведение химиолучевой терапии на фоне Бевацизумаба, отличающийся тем, что на этапе оконтуривания определяют первичный объем рецидива или его хирургического ложа с/без остаточной ткани (GTVr) по данным серий магнитно-резонансной томографии T1 и T2/FLAIR, определяют клинический объем мишени CTVr путем отступа 15 мм от GTVr с исключением из объема естественных барьеров при их интактности, формируют планируемый объем мишени PTVr путем отступа от CTVr на 3 мм, при завершении дозиметрического планирования проводят курс протонной терапии активным сканирующим пучком протонов в физической разовой очаговой дозе (РОД) 1,81 Гр до физической суммарной очаговой дозы (СОД) 50,68 Гр, что с учетом относительной биологической эффективности протонного излучения 1,1 эквивалентно РОД 2,0 ГрЭ и СОД 56 ГрЭ, за 28 фракций на область рВЗГ головного мозга на фоне внутривенного введения Бевацизумаба в дозе 5-10 мг/кг каждые 2 недели на 1-й, 15-й и 30-й дни курса протонной терапии соответственно.
2. Способ по п.1, отличающийся тем, что при необходимости дополнительно используют данные позитронно-эмиссионной компьютерной томографии с аминокислотными трейсерами (BTVr), а CTVr получают путем отступа 15 мм от GTVr + BTVr.
| CASTELLANO A | |||
| et al | |||
| Advanced imaging techniques for radiotherapy planning of gliomas | |||
| Cancers, 2021, 13 (5), 1063 | |||
| Способ комбинированного лечения больных с метастатическим поражением головного мозга немелкоклеточным раком легкого | 2021 |
|
RU2778607C1 |
| СПОСОБ ЛЕЧЕНИЯ РЕЦИДИВА ЗЛОКАЧЕСТВЕННЫХ ГЛИОМ ГОЛОВНОГО МОЗГА | 2018 |
|
RU2684019C1 |
| US 10857237 B2, 08.12.2020 | |||
| US 20230023987 A1, 26.01.2023 | |||
| US 20230010671 A1, 12.01.2023 | |||
| КИРЕЕВА Т.А | |||
| и др | |||
| Протонная терапия в лечении диффузной астроцитомы ствола головного | |||
Авторы
Даты
2025-02-14—Публикация
2024-06-06—Подача