Область техники, к которой относится изобретение
Изобретение относится к композициям и способам лечения бактериальных вагинальных инфекций.
Предшествующая область техники
Бактериальный вагиноз (БВ) – одно из наиболее частых вагинальных заболеваний у женщин репродуктивного возраста. БВ характеризуется изменением вагинальной флоры, при котором нормальная популяция вагинальных лактобактерий сокращается и замещается чрезмерно размножающимися факультативными и анаэробными бактериями, такими как Gardnerella vaginalis, Atopobium, Prevotella, Bacteriodes, Peptostreptococcus и Mobiluncus..
БВ связан с увеличением объема выделений, имеющих неприятный рыбный запах, из влагалища. Значение рН влагалища повышается от нормального диапазона (pH 3-4) до значений примерно выше pH 4.5. Наличие запаха и повышенное значение рН вызваны высокой концентрацией во влагалище аминов, прежде всего, триэтиламина. Эти амины улетают при повышении рН, например при добавлении KОН или при взаимодействии со спермой.
Как правило, клинический диагноз БВ ставится при наличии трех или более из следующих четырех клинических критериев (известных как критерии Амзеля): (1) патологические выделения; (2) значение рН, большее или равное примерно 4,5; (3) «рыбный» запах аминов при добавлении 10% KОН к выделениям; (4) наличие ключевых эпителиальных клеток (где границы клеток затемнены бактериями) в количестве, превышающем или равном примерно 20% вагинальных эпителиальных клеток при микроскопическом исследовании мазка влагалищного отделяемого.
Как правило, БВ лечат антибактериальными препаратами, обладающими активностью в отношении анаэробных микроорганизмов, например метронидазолом или клиндамицином. Чаще всего используют метронидазол, который выпускают в виде пероральных таблеток, а также вагинальных кремов и гелей. Часто предпочитают вагинальные лекарственные дозированные формы, поскольку они ограничивают системное воздействие препарата, обеспечивая при этом высокую локальную концентрацию антибактериального препарата. Например, стандартные пероральные дозы метронидазола, применяемые для лечения БВ, составляют 500 мг два раза в сутки в течение семи дней, тогда как вагинальный гель с концентрацией метронидазола 0,75%, как правило, применяют при дозировке 5 г геля, содержащего 37,5 мг метронидазола, один раз в сутки в течение пяти дней. После введения разовой дозы 0,75% геля метронидазола, содержащего 37,5 мг метронидазола, фармакокинетический профиль демонстрирует гораздо более низкое содержание препарата в крови (Cмакс 237 нг/мл и AUC 4,977 нг.ч/мл), по сравнению с содержанием после приема стандартной пероральной таблетки 500 мг (Cмакс 12,785 нг/мл и AUC 133,395 нг.ч/мл).
Вульвовагинальный кандидоз (ВВК), известный также как кандидозный вагинит, представляет собой другую распространенную вагинальную инфекцию, характеризующуюся чрезмерным ростом дрожжей. Первичные симптомы ВВК включают в себя зуд, жжение и раздражение влагалища и/или вульвы. Сопутствующие признаки включают эритему, отек и экскориацию. В большинстве случаев возбудителем является Candida albicans. Микроорганизмы Candida можно выращивать в питательной среде или увидеть при исследовании мазка влагалищного отделяемого.
Как правило, ВВК лечат азольными противогрибковыми препаратами, проявляющими активность в отношении микроорганизмов вида Candida. Дозированные формы включают в себя пероральные препараты на основе триазола, такие как флуконазол, и азолсодержащие вагинальные кремы или суппозитории, такие как миконазол, клотримазол и терконазол.
В некоторых случаях пациентки одновременно страдают БВ и вульвовагинальным кандидозом (ВВК). По данным микробиологических исследований до 15% женщин, перенесших вагинальную инфекцию, одновременно инфицированы микроорганизмами БВ наряду с дрожжевыми грибками, такими как Candida. В таких случаях для успешного лечения необходимо применение более чем одного препарата – антибактериального для лечения БВ и противогрибкового для лечения ВВК. Часто такое лечение включает в себя пероральную дозированную форму, например пероральный метронидазол и вагинальную дозированную форму, например крем на основе миконазола.
В случае антибактериальных и противогрибковых препаратов, используемых для лечения вагинальных инфекций, большое значение имеют степень и продолжительность высвобождения лекарственного средства. В частности, при рассмотрении препаратов, которые легко всасываются через слизистую оболочку влагалища, таких как метронидазол, фармакокинетический профиль в некоторой степени отражает степень и продолжительность высвобождения препарата из лекарственной формы.
Например, два имеющихся в продаже вагинальных геля на водной основе, применяемых для лечения БВ, имеют близкие фармакокинетические профили, даже несмотря на то, что они содержат разное количество лекарственного средства в одной дозе. Вагинальный гель на основе 1,3% метронидазола с содержанием 65 мг метронидазола на дозу обеспечивает концентрацию в крови (Cмакс 239 нг/мл и AUC 5434 нг*ч/мл), которая почти идентична таковой для геля на основе 0,75% метронидазола с содержанием 37,5 мг метронидазола на дозу (Cмакс 237 нг/мл и AUC 4,977 нг*ч/мл).
В настоящем изобретении предоставлен уникальный гелевый препарат на основе метронидазола и терконазола для лечения БВ и ВВК. Неожиданно оказалось, что препарат на основе комбинации противогрибкового средства терконазола и антибактериального средства метронидазола проявляет повышенную антибактериальную биодоступность по сравнению с препаратом на основе только одного антибактериального средства. Кроме того, было показано, что подобная повышенная биодоступность предпочтительна для лечения БВ у женщин, страдающих как БВ, так и ВВК, по сравнению с действием только антибактериального препарата.
Краткое описание изобретения
Терапевтическая композиция, такая как вагинальный гель, для лечения бактериального вагиноза (БВ) и обеспечивающая повышенную биодоступность метронидазола, содержит, помимо метронидазола, терконазол, физиологически доступный загуститель и буферную систему, при помощи которой буферное значение рН композиции составляет примерно от 3,75 примерно до 4,25. Соответствующее молярное соотношение метронидазола и терконазола предпочтительно находится в диапазоне примерно от 3 примерно до 4, более предпочтительно, примерно 3,5.
Краткое описание чертежей
На чертежах:
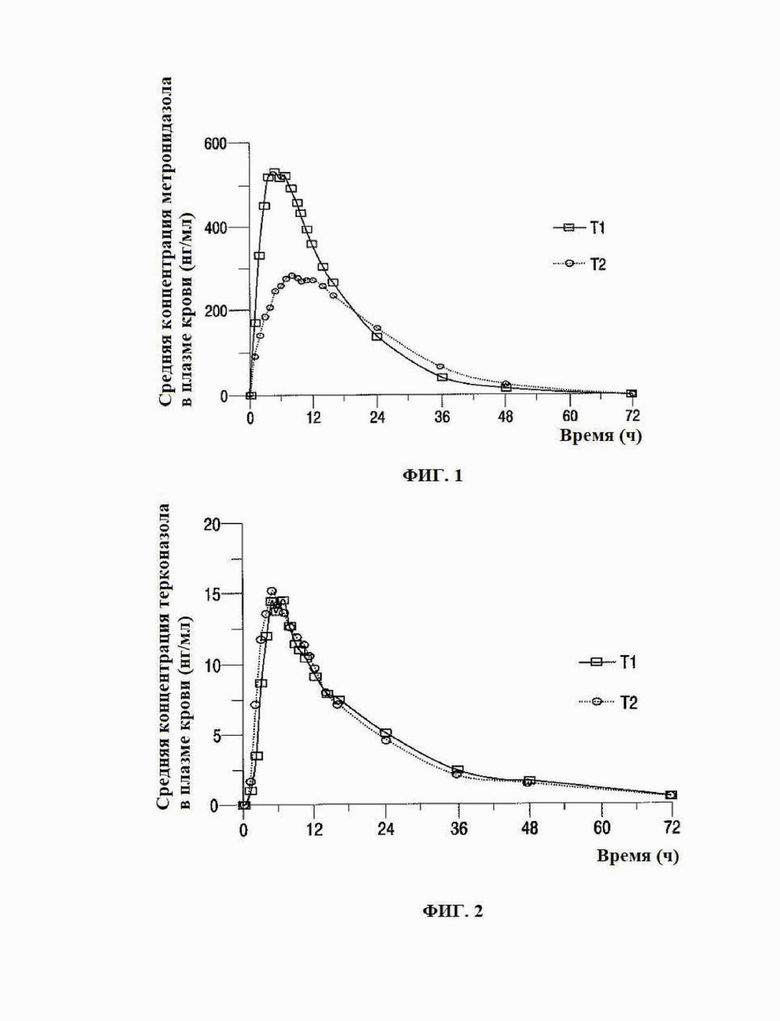
фиг. 1 представляет собой график биодоступности метронидазола самого по себе и в комбинации с терконазолом в гелеобразном носителе, а
фиг. 2 представляет собой график биодоступности терконазола самого по себе и в комбинации с метронидазолом в том же гелеобразном носителе.
Описание предпочтительных вариантов осуществления
Определения
Термин «буферная система» или «буфер», используемый в описании и прилагаемой формуле изобретения, относится к растворяющему агенту или агентам, которые при растворении в воде стабилизируют полученный раствор от значительного изменения рН при добавлении кислот или оснований. Предпочтительной буферной системой для целей настоящего изобретения является система лимонная кислота – цитрат натрия.
Термины «разовая доза» или «разовая лекарственная форма», используемые в описании и прилагаемой формуле изобретения, относятся к физически дискретным единицам настоящей композиции, пригодным для введения людям женского пола. Каждая единица содержит заранее определенное количество метронидазола и терконазола, рассчитанное для получения желаемого терапевтического эффекта. Разовая лекарственная форма, которую следует вводить какому-либо конкретному пациенту, определяется и зависит от (1) конкретного терапевтического эффекта, который должен быть достигнут (2) и скорости высвобождения действующих веществ из конкретной используемой композиции.
Термин «влагалище», используемый в описании и прилагаемой формуле изобретения, включает область влагалища в целом, включая вульву и шейку матки.
Количество вводимой интравагинально терапевтической композиции для лечения бактериального вагиноза (БВ) может изменяться в широком диапазоне в зависимости от возраста и физического состояния пациентки, степени поражения, частоты введения и тому подобных факторов.
Активные ингредиенты в настоящих терапевтических композициях представляют собой метронидазол (1-(2-гидроксиэтил)-2-метил-5-нитроимидазол; M=171,156 г/моль) и терконазол цис-1-[п-[[2-(2,4-дихлорфенил)-2-(1H-1,2,4-триазол-1-илметил)-1,3-диоксолан-4-ил]метокси]фенил]-4-изопропилпиперазин; M=532,462 г/моль). Термины «метронидазол» и «терконазол», используемые в описании и прилагаемой формуле изобретения, также включают в себя аналоги и производные данных соединений, проявляющие терапевтическую активность при описанном здесь применении.
Метронидазол и терконазол являются коммерчески доступными соединениями.
Подходящие физиологически приемлемые загустители представляют собой производные целлюлозы, такие как гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза натрия, а также полимеры полиакриловой кислоты, сшитые с полимерами полиакриловой кислоты и коммерчески доступные от Lubrizol Corporation, Кливленд, Огайо, под обозначениями CARBOPOL 934, CARBOPOL 940, CARBOPOL 950 и т.д.
Настоящие композиции могут также содержать необязательные консерванты, хелатирующие вещества, сорастворитель, стабилизаторы вязкости и т.д.
Подходящие консерванты представляют собой низшие алкиловые эфиры парагидроксибензойной кислоты, например, метилпарабен, пропипарабен и т.д., бензоат натрия, этилендиаминтетрауксусную кислоту (EDTA) и т.д.
Подходящими сорастворителями являются двухатомные и полиатомные спирты, такие как пропиленгликоль, глицерин, сорбит, 1,2,6-гексантриол и т.д.
Подходящим стабилизатором вязкости является метионин и т.д. В гелеобразных композициях согласно изобретению метронидазол и терконазол присутствуют в соответствующем молярном соотношении, составляющем примерно от 3 примерно до 4, предпочтительно примерно 3,5.
Концентрация метронидазола в композициях составляет по меньшей мере примерно 0,5 массового процента из расчета на массу композиции, предпочтительно в диапазоне примерно от 0,75 массового процента примерно до 1 массового процента, а более предпочтительно составляет примерно 0,9 массового процента.
Концентрация терконазола в композициях составляет по меньшей мере примерно 0,4 массового процента из расчета на массу композиции, предпочтительно в диапазоне примерно от 0,6 массового процента примерно до 1,2 массового процента, а более предпочтительно составляет примерно 0,8 массового процента.
Количество метронидазола в разовой дозе обычно составляет по меньшей мере примерно 20 мг и не превышает примерно 100 мг. Предпочтительная разовая доза метронидазола в гелевом носителе находится в диапазоне примерно от 20 примерно до 60 мг, наиболее предпочтительно примерно 45 мг.
Количество терконазола в разовой дозе обычно составляет по меньшей мере примерно 16 мг и не превышает примерно 80 мг. Предпочтительная разовая доза терконазола в гелевом носителе находится в диапазоне примерно от 16 примерно до 50 мг, наиболее предпочтительно примерно 40 мг.
Экспериментальные композиции, состав которых приведен ниже в таблице 1, получали для определения биодоступности метронидазола и терконазола в виде однокомпонентных гелей, в также комбинированного геля. Данные экспериментальные гели также использовали для лечения женщин со смешанным (сочетанным) БВ и ВВК. Приведенные процентные доли в таблице 1 представляют собой массовые процентные доли.
Таблица 1. Экспериментальные композиции
Перекрестное исследование биодоступности после однократного введения препарата проводили на здоровых добровольцах женского пола с использованием препаратов, представленных в приведенной выше таблице 1. Пять грамм каждого препарата помещали в вагинальный аппликатор и вводили каждому пациенту. Каждый аппликатор соответствовал 45 мг метронидазола, или 40 мг терконазола, или 45 мг метронидазола и 40 мг терконазола. Исследование проводили на двадцати четырех (24) пациентках, из которых двадцать одна (21) завершила исследование. Пациентки находились в медицинском учреждении по меньшей мере за 12 часов до введения лекарственного препарата и до 24 часов после этого. После этого пациентки являлись в исследовательский центр через 36, 48 и 72 часа. Пациенток лечили каждым из этих гелей в соответствии со схемой рандомизации.
Образцы плазмы крови получали от пациенток за 90 минут до введения дозы (0 ч) и после введения дозы с часовыми интервалами, начиная с одного часа после введения дозы в течение первых двенадцати часов и затем через 14 ч, 16 ч, 24 ч, 36 ч, 48 ч и 72 ч в каждом периоде исследования.
Проводили три отдельных периода исследования. Между периодами исследования сохранялся семидневный период вымывания, за исключением трех случаев между периодом исследования II и периодом исследования III из-за наступления менструации. В этих трех случаях период вымывания составлял 14 дней.
На фиг. 1 представлен линейный график зависимости наблюдаемой средней концентрации метронидазола в плазме в зависимости от времени для геля метронидазол + терконазол (T1) и геля на основе одного метронидазола (T2). Отчетливо видна повышенная биодоступность метронидазола в присутствии терконазола.
Фиг. 2 представляет собой линейный график зависимости наблюдаемой средней концентрации терконазола в плазме от времени для геля метронидазол + терконазол (T1) и геля, содержащего только терконазол (T3), и показывает, что биодоступность терконазола не повышается в присутствии метронидазола.
В приведенных ниже таблицах 2 и 3 представлены наблюдаемые фармакокинетические параметры.
Таблица 2. Биодоступность метронидазола
Из приведенных выше данных видно, что максимальная концентрация в плазме (Cмакс), а также площадь под кривой (AUC) для метронидазола значительно выше для геля метронидазол + терконазол (p<0,001 для всех параметров). Биодоступность метронидазола значительно возрастала при совместном применении с терконазолом.
Таблица 3. Биодоступность терконазола
Из результатов, представленных в таблице 3, видно, что присутствие метронидазола не оказывало существенного влияния на биодоступность терконазола.
Кроме того, композиции настоящего изобретения более эффективны, чем метронидазол в отдельности, для лечения инфекций бактериального вагиноза (БВ) у женщин со смешанным (сочетанным) БВ и ВВК.
Те же три экспериментальных препарата тестировали на женщинах, которые соответствовали всем клиническим и лабораторным критериям, необходимым для постановки диагноза как БВ, так и ВВК. Женщинам вводили пятиграммовый аппликатор, заполненный гелем, перед сном в течение 3 дней подряд. Через 7-14 дней проводили оценку на предмет их клинического излечения как от БВ, так и от ВВК.
Излечение от БВ определяли как исчезновение аномальных выделений, отрицательный тест на запах аминов при действии KOH и отрицательный результат на наличие 20% или более ключевых клеток при исследовании мазка отделяемого из влагалища. Ожидалось, что в случае женщин, страдающих и БВ, и ВВК, комбинация метронидазол+ терконазол излечивает от БВ в значительно большей степени, чем один терконазол, и обеспечит такие же показатели эффективности излечения от БВ, как один метронидазол. Однако показатели излечения от БВ для этих женщин оказались неожиданно более высокими по сравнению с пациентками, применявшими гель на основе одного метронидазола, как видно из приведенной ниже таблицы 4.
Таблица 4. Показатели эффективности излечения от БВ
(T3)
Излечение от ВВК определяли как исчезновение всех симптомов и признаков, связанных с ВВК. Ожидалось, что в случае женщин, страдающих как БВ, так и ВВК, комбинация метронидазол + терконазол излечивает от ВВК значительно эффективнее, чем один только метронидазол, и обеспечит такие же показатели эффективности излечения ВВК, как и терконазол в отдельности для ВВК. Эти ожидания оправдались, как видно из приведенной ниже таблицы 5:
Таблица 5. Показатели эффективности излечения от ВВК
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВАГИНИТА И СПОСОБ ЕГО ЛЕЧЕНИЯ | 1991 |
|
RU2032402C1 |
| СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ БАКТЕРИАЛЬНОГО ВАГИНОЗА | 2004 |
|
RU2261715C1 |
| СПОСОБ ЛЕЧЕНИЯ БАКТЕРИАЛЬНОГО ВАГИНОЗА | 2009 |
|
RU2393870C1 |
| СПОСОБ МЕСТНОГО ЛЕЧЕНИЯ БАКТЕРИАЛЬНОГО ВАГИНОЗА | 2003 |
|
RU2236851C1 |
| ПРИМЕНЕНИЕ ОЛИГОМЕРОВ МОЛОЧНОЙ КИСЛОТЫ В ЛЕЧЕНИИ ГИНЕКОЛОГИЧЕСКИХ РАССТРОЙСТВ | 2008 |
|
RU2459620C2 |
| Способ лечения рецидивирующего бактериального вагиноза у женщин, инфицированных вирусом простого герпеса | 2021 |
|
RU2770293C1 |
| ПОЛИМЕР ДЛЯ ДОСТАВКИ ЛЕКАРСТВ С ГИДРОХЛОРИДНОЙ СОЛЬЮ КЛИНДАМИЦИНА | 2007 |
|
RU2444364C2 |
| ПРИМЕНЕНИЕ ТОТАРОЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТОТАРОЛ | 2018 |
|
RU2812223C2 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ УРОГЕНИТАЛЬНЫХ ИНФЕКЦИЙ | 1996 |
|
RU2073520C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПОДХОДЯЩАЯ ДЛЯ ВНУТРИВЛАГАЛИЩНОЙ ДОСТАВКИ | 2021 |
|
RU2828262C1 |
Композиция, имеющая гелеобразную консистенцию, содержит метронидазол, терконазол, физиологически приемлемый загуститель и воду. Композиция применима для лечения бактериального вагиноза, а также вульвовагинального кандидоза. 4 н.п. ф-лы, 5 табл., 2 ил.
1. Композиция для лечения бактериального вагиноза (БВ), имеющая гелеобразную консистенцию и содержащая метронидазол, терконазол, физиологически приемлемый загуститель и воду, в которой метронидазол присутствует в диапазоне концентрации от 0,75 мас.% до 1 мас.% в расчете на массу композиции, терконазол присутствует в диапазоне концентрации от 0,6 мас.% до 1,2 мас.% в расчете на массу композиции, метронидазол присутствует совместно с буферной системой, которая обеспечивает буферное значение рН композиции в диапазоне от 3,75 до 4,25, в которой метронидазол и терконазол присутствуют в мольном соотношении 3,5:1 соответственно, в которой физиологически приемлемый загуститель является гидроксипропилметилцеллюлозой, а буферная система включает лимонную кислоту и цитрат натрия.
2. Композиция для лечения бактериального вагиноза (БВ), имеющая гелеобразную консистенцию и содержащая метронидазол, терконазол, физиологически приемлемый загуститель и воду, в которой метронидазол присутствует совместно с буферной системой, которая обеспечивает буферное значение рН композиции в диапазоне от 3,75 до 4,25, в которой концентрация метронидазола составляет 0,9 мас.%, концентрация терконазола составляет 0,8 мас.%, физиологически приемлемый загуститель представляет собой гидроксипропилметилцеллюлозу, а буферная система включает лимонную кислоту и цитрат натрия.
3. Способ лечения бактериального вагиноза у пациента, являющегося человеком, включающий в себя введение композиции по п. 1 во влагалище пациента, нуждающегося в подобном лечении.
4. Способ лечения бактериального вагиноза у пациента, являющегося человеком, включающий в себя введение композиции по п. 2 во влагалище пациента, нуждающегося в подобном лечении.
| WO 9955333 A1, 04.11.1999 | |||
| US 2006093675 A1, 04.05.2006 | |||
| WO 2005087270 A1, 22.09.2005 | |||
| US 2003180366 A1, 25.09.2003 | |||
| US 2008063668 A1, 2008.03.13 | |||
| US 8258164 B2, 04.09.2012 | |||
| US 2015265609 A1, 24.09.2015 | |||
| US 5840744 A, 1998.11.24 | |||
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВАГИНИТА И СПОСОБ ЕГО ЛЕЧЕНИЯ | 1991 |
|
RU2032402C1 |
Авторы
Даты
2025-02-19—Публикация
2021-04-22—Подача