Область техники, к которой относится изобретение
Изобретение относится к области абдоминальной хирургии и может быть использовано для хирургического лечения заболевания рецидивных форм гастроэзофагеальной рефлюксной болезни (ГЭРБ) и грыж пищеводного отверстия диафрагмы (ГПОД) у больных, которым ранее было выполнено антирефлюксное оперативное лечение.
Уровень техники
Согласно Монреальскому соглашению от 2006 г., гастроэзофагеальная рефлюксная болезнь описывается как состояние, при котором заброс содержимого из желудка в пищевод вызывает клинические симптомы и/или осложнения, приводящие к снижению качества жизни пациентов [Vakil N, van Zanten SV, Kahrilas P, Dent J, Jones R; Global Consensus Group. The Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus. Am J Gastroenterol. 2006 Aug;101(8):1900-20; quiz 1943. https://doi.org/10.1111/j.1572-0241.2006.00630.x]. Распространенность заболевания охватывает значительную часть населения развитых стран, в том числе Российской Федерации. Диспепсические симптомы проявляются у 18-46 % пациентов, обращающихся за помощью к врачам амбулаторного звена или врачам-хирургам, и выражаются в виде мучительной изжоги, отрыжки и др. [Hunt R, Armstrong D, Katelaris P, Afihene M, Bane A, Bhatia S, Chen MH, Choi MG, Melo AC, Fock KM, Ford A, Hongo M, Khan A, Lazebnik L, Lindberg G, Lizarzabal M, Myint T, Moraes-Filho JP, Salis G, Lin JT, Vaidya R, Abdo A, LeMair A; Review Team:. World Gastroenterology Organisation Global Guidelines: GERD Global Perspective on Gastroesophageal Reflux Disease. J Clin Gastroenterol. 2017 Jul;51(6):467-478. https:// doi.org/10.1097/MCG.0000000000000854]. К этиологическим факторам, обусловливающим развитие патологического рефлюкса, можно отнести нарушение функционирования нижнего пищеводного сфинктера (например, вследствие врожденной слабости нижнего пищеводного сфинктера, системных заболеваний соединительной ткани и др.), однако наиболее частой причиной развития стойких симптомов ГЭРБ является изменение нормальной анатомии зоны пищеводно-желудочного перехода в виде наличия грыжи пищеводного отверстия диафрагмы (ГПОД) [Schlottmann F, Andolfi C, Herbella FA, Rebecchi F, Allaix ME, Patti MG. GERD: Presence and Size of Hiatal Hernia Influence Clinical Presentation, Esophageal Function, Reflux Profile, and Degree of Mucosal Injury. Am Surg. 2018 Jun 1;84(6):978-982]. Корреляция между ГЭРБ и наличием ГПОД достоверно подтверждена во многих исследованиях, при этом наличие грыжи наблюдается у 83 % пациентов с ГЭРБ, тогда как распространенность ГЭРБ при наличии ГПОД достигает 68 % [Antoniou SA, Koch OO, Antoniou GA, Asche KU, Kaindlstorfer A, Granderath FA, Pointner R. Similar symptom patterns in gastroesophageal reflux patients with and without hiatal hernia. Dis Esophagus. 2013 Jul;26(5):538-43. https://doi.Org/10.1111/j.1442-2050.2012.01368.x; Ouyang W, Dass C, Zhao H, Kim C, Criner G COPDGene Investigators. Multiplanar MDCT measurement of esophageal hiatus surface area: association with hiatal hernia and GERD. Surg Endosc. 2016 Jun;30(6):2465- 72. https://doi.org/10.1007/s00464-015-4499-9].
Следует отметить, что наличие ГПОД у пациентов с патологическим рефлюксом является неоспоримым показанием к хирургическому лечению, поскольку основным фактором развития рефлюкса в этом случае является дефект анатомических структур пищеводно-желудочного перехода, который не подлежит коррекции посредством консервативной терапии. При этом лапароскопическая фундопликация остается «золотым стандартом» в современной малоинвазивной антирефлюксной хирургии, обеспечивая эффективность и безопасность методики в 95 % случаев [Balci D, Turkcapar AG. Assessment of quality of life after laparoscopic Nissen fundoplication in patients with gastroesophageal reflux disease. World J Surg. 2007 Jan;31(1):116-21. https://doi.org/10.1007/ s00268-005-0658-9]. Однако, несмотря на высокую эффективность и безопасность оперативного вмешательства, в ряде случаев наблюдается развитие рецидивов заболевания.
В большинстве случаев симптомы рецидива ГПОД, как и первичной грыжи, не поддаются консервативной терапии, вызывая необходимость проведения ревизионного вмешательства в объеме восстановления первичной анатомии зоны кардиоэзофагеального перехода и формирования новой фундопликационной манжеты. Следует отметить, что оперативное вмешательство, направленное на формирование физиологичной и адекватно функционирующей фундопликационной манжеты, имеет ряд технических особенностей, соблюдение которых представляется необходимым для достижения успешного результата в случаях работы как с первичными, так и рецидивными ГПОД.
Из уровня техники известны различные способы лечения как первичных, так и рецидивных грыж пищеводного отверстия диафрагмы.
В частности, известен способ пластики грыж пищеводного отверстия диафрагмы (Патент РФ №2438601), в соответствии с которым рассекают желудочно-диафрагмальную связку слева и справа и часть желудочно-селезеночной связки. Выделяют ножки диафрагмы и сшивают их позади пищевода узловыми швами. Укрывают дефект и линию шва протезом. Укрывают протез желудочно-диафрагмальной и желудочно-селезеночной связкой с последующей их фиксацией к протезу узловыми швами. Выполняют фундопликацию с фиксацией созданной манжеты к диафрагме узловыми швами на толстом желудочном зонде.
Однако установка протеза может привести к развитию осложнений в отдалённом послеоперационном периоде, таких как эрозия и перфорации стенки пищевода. Кроме того, данный способ характерен для лечения первичных грыж пищеводного отверстия диафрагмы и не подходит для лечения рецидивных грыж пищеводного отверстия диафрагмы.
Известен способ оперативного лечения грыжи пищеводного отверстия диафрагмы (патент РФ №2661017), согласно которому мобилизуют малый сальник, входят в сальную сумку, визуализируют правую ножку диафрагмы. Осуществляют мобилизацию пищевода путем выделения среднего пучка правой ножки диафрагмы и выделения пищевода из заднего средостения и формирование симметричной фундопликационной манжеты. Выделение среднего пучка правой ножки диафрагмы производят при пересечении желудочно-диафрагментальной связки, а формирование манжеты производят сшиванием передней и задней стенок желудка медиальнее малой кривизны проксимального отдела на уровне ножек диафрагмы и одновременно той же лигатурой сшивают правую и левую ножки пищеводного отверстия диафрагмы.
Однако фиксация манжетки к ножкам пищеводного отверстия диафрагмы несёт высокий риск развития выраженного болевого синдрома при приёме пищи, в связи с сокращением ножек пищеводного отверстия диафрагмы и подвижностью стенок желудка (грубая фиксация стенки желудка).
Известен способ хирургического лечения рецидива грыжи пищеводного отверстия диафрагмы, заключающийся в выполнении гастрошунтирования по Ру (Roux-en-Y). Суть метода заключается в формировании малого желудочка (gastro-pouch), с формированием гастро-энтеро анастомоза и межкишечного анастомоза (Landreneau J. P. et al. Minimally invasive Roux-en-Y reconstruction as a salvage operation after failed nissen fundoplication //Surgical Endoscopy. - 2020. - Т. 34. - С. 2211-2218. https://doi.org/10.1007/s00464-019- 07010-7).
К недостаткам данного способа следует отнести высокий риск послеоперационных осложнений: развитие несостоятельности анастомозов, развитие острой печёночной недостаточности; сохранение у пациента гастроэзофагеального рефлюкса; развитие синдрома мальабсорбции и прочих специфичных осложнений.
Известен также способ фундопликации Галлямова Э.А. и соавт. (Патент РФ №2291672), в соответствии с которым мобилизуют малый сальник, входят в сальниковую сумку, визуализируют правую ножку диафрагмы, мобилизацию пищевода начинают с выделения среднего пучка правой ножки диафрагмы, сохраняют желудочнодиафрагмальную связку в качестве ориентира, разделяющего желудок на переднюю и заднюю стенки, выделяют пищевод из заднего средостения, восстанавливая его абдоминальную позицию, двигаясь сзади пищевода вдоль медиального пучка правой ножки диафрагмы, завершают мобилизацию пищевода и мышечной петли вокруг него, подходя к задней стенке дна желудка со стороны малой кривизны, под пищеводом, после чего проводят заднюю стенку желудка позади пищевода и формируют фундопликационную манжету путем фиксации передней и задней стенок дна желудка к стенке пищевода на протяжении.
Однако данный способ также характерен для первичных грыж пищеводного отверстия диафрагмы и не подходит для лечения различных форм рецидивных грыж пищеводного отверстия диафрагмы. Кроме того, известное решение характеризуется недостаточно сформированным антирефлюксным механизмом.
Наиболее близким к заявленному способу является способ рефундопликации (Гололобов Г.Ю, Ерин С.А., и соавт. Лапароскопическая коррекция рецидива гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы после дважды провальной фундопликации. Клинический случай. Хирургическая практика. 2023;8(4):6—20. doi.org/10.38181/2223- 2427-2023-4-1), в соответствии с которым после осуществления лапароскопического доступа и ревизии органов брюшной полости производят мобилизацию абдоминального отдела пищевода, освобождение правой и левой ножки пищеводного отверстия диафрагмы по контуру пищеводного отверстия диафрагмы, выполняют демонтаж ранее наложенной манжетки, удаление инородных тел, атравматичное выделение блуждающих нервов, осуществляют доступ к задней стенке дна желудка, выполняют заднюю крурорафию с помощью нерассасывающегося синтетического шовного материала, фиксацию пищевода к ножкам пищеводного отверстия диафрагмы, формируют фундопликационную манжету по типу «short floppy» Nissen длиной 20 мм с её фиксацией к передней и задней стенкам пищевода.
Однако данный способ применим только при достаточной мобилизации задней стенки дна желудка. Согласно способу, фиксацию манжетки к стенкам пищевода производят после формирования самой манжетки, а не непосредственно при её формировании, что может привести к развороту фундопликационной манжеты и её соскальзыванию. Отсутствие передней крурорафии может привести к миграции фундопликационной манжеты в заднее средостенье. Кроме того, при описании способа не указана локализация стенок желудка при формировании фундопликационной манжетки.
Технической проблемой, на решение которой направлено изобретение, является разработка малоинвазивного, прецизионного и наиболее эффективного способа хирургического лечения всех форм рецидива грыж пищеводного отверстия диафрагмы, который позволит улучшить непосредственные и отдаленные результаты лечения (в том числе снизить до минимума количество интраоперационных, ранних и поздних послеоперационных осложнений), снизить количество рецидивов заболевания и улучшить качество жизни пациентов после хирургического лечения.
Раскрытие изобретения
Техническим результатом, на достижение которого направлено заявленное изобретение, является уменьшение рисков развития интраоперационных и послеоперационных осложнений, а также рисков развития повторного рецидива заболевания за счет формирования адекватного антирефлюксного механизма.
Способ обеспечивает выполнение технологически правильного антирефлюксного вмешательства.
Технический результат достигается за счет реализации способа лапароскопической рефундопликации, включающего установку назогастрального зонда, выполнение декомпрессии желудка, установку троакаров, наложение карбоксиперитонеума, введение печёночного ретрактора с тракцией левой доли печени кверху, выполнение адгезиолизиса в области кардиоэзофагельного перехода, вскрытие малого сальника выше печёночной ветви блуждающего нерва с последующей мобилизацией правой и левой ножек пищеводного отверстия диафрагмы, мобилизацию ранее установленной фундопликационной манжеты и абдоминального отдела пищевода с низведением их в брюшную полость, демонтаж ранее установленной фундопликационной манжеты с восстановлением первичной анатомии зоны пищеводно-желудочного перехода, атравматичное выделение правого и левого блуждающих нервов, выполнение доступа к задней стенке дна желудка в бессосудистой зоне позади пищеводного отверстия диафрагмы с пересечением коротких желудочных артерий, выполнение задней и передней крурорафии по диаметру пищевода, фиксацию пищевода к правой и левой ножкам пищеводного отверстия диафрагмы узловыми швами синтетическим не рассасывающимся шовным материалом, формирование новой фундопликационной манжеты, установку дренажа, контроль гемостаза, десуфляцию, удаление троакаров, при этом перед формированием фундопликационной манжеты оценивают степень мобилизации задней стенки дна желудка, и при её достаточной мобилизации заднюю стенку дна желудка проводят под пищеводом в сторону малой кривизны, переднюю стенку дна желудка проводят над пищеводом в сторону малой кривизны, и обе стенки фиксируют к правой стенке пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся шовным материалом, захватывая в один шов последовательно переднюю стенку дна желудка, правую стенку пищевода на уровне кардиоэзофагеального перехода и заднюю стенку дна желудка, с формированием симметричной фундопликационной манжеты не ротирующей и не сдавливающей пищевод; при недостаточной мобилизации задней стенки дна желудка выполняют проведение передней стенки дна желудка в сторону малой кривизны и её фиксацию к передней стенке пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся шовным материалом, затем выполняют проведение задней стенки дна желудка под пищеводом в сторону малой кривизны и ее фиксацию к задней стенке пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся шовным материалом.
В случае миграции ранее установленной фундопликационной манжеты в средостенье осуществляют мобилизацию фундопликационной манжеты по направлению пищевода в брюшную полость, с последующей мобилизацией абдоминального отдела пищевода.
После этапа выделения правого и левого блуждающих нервов при наличии инородных тел в зоне пищевода и/или манжеты производят их удаление.
После этапа мобилизации абдоминального отдела пищевода при наличии параэзофагеальной грыжи производят мобилизацию содержимого и удаление грыжевого мешка.
Таким образом, предлагаемый способ позволяет сформировать адекватный антирефлюксный механизм даже при наличии рубцового процесса после ранее выполненной фундопликации в зависимости от доступного объёма мобилизации задней стенки дна желудка, без использования инородного материала, что снижает риски послеоперационных осложнений. Восстановление нормальной анатомии позволяет выявить вид рецидива и технические ошибки предшествующей операции, устранить технические ошибки, удалить инородный материал и грыжевой мешок при их наличии, а также сформировать технически верную манжету правильными стенками желудка, не суживающую, не ротирующую пищевод и не деформирующую желудок. Выполнение задней и передней крурорафии по диаметру пищевода позволяет избежать компрессии пищевода, а также миграцию манжеты в средостенье. Фиксация пищевода к ножкам пищевого отверстия диафрагмы узловыми швами также предотвращает миграцию абдоминального отдела пищевода в сторону заднего средостенья. Фиксация манжеты к правой стенке пищевода при её формировании так, чтобы задняя стенка дна желудка, правая стенка пищевода и передняя стенка дна желудка оказались в одном шве, позволяют сформировать симметричную манжету, которая не ротирует, не сдавливает и не деформирует пищевод. Данная манжета является максимально физиологичной, позволяет полностью купировать симптомы ГЭРБ. Использование предлагаемого способа предотвращает развитие гастроэзофагеального рефлюкса.
Краткое описание чертежей
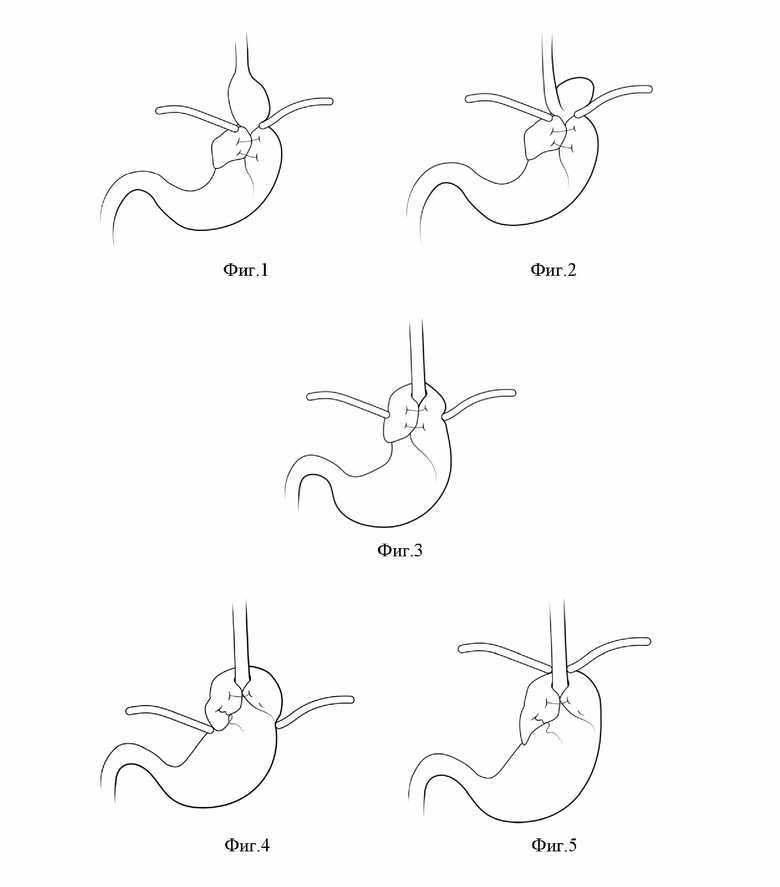
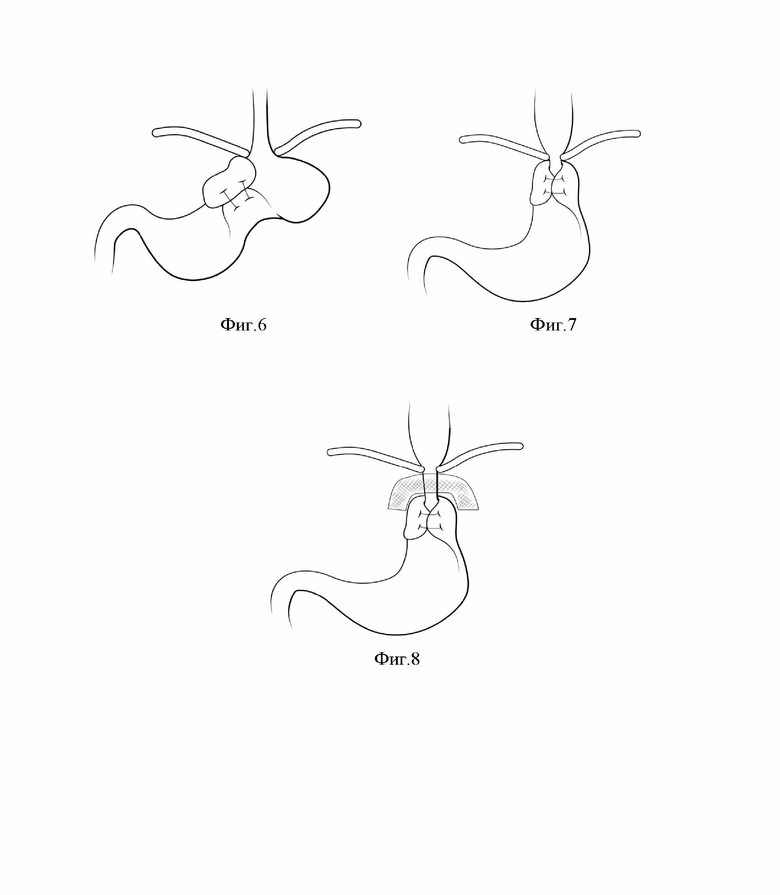
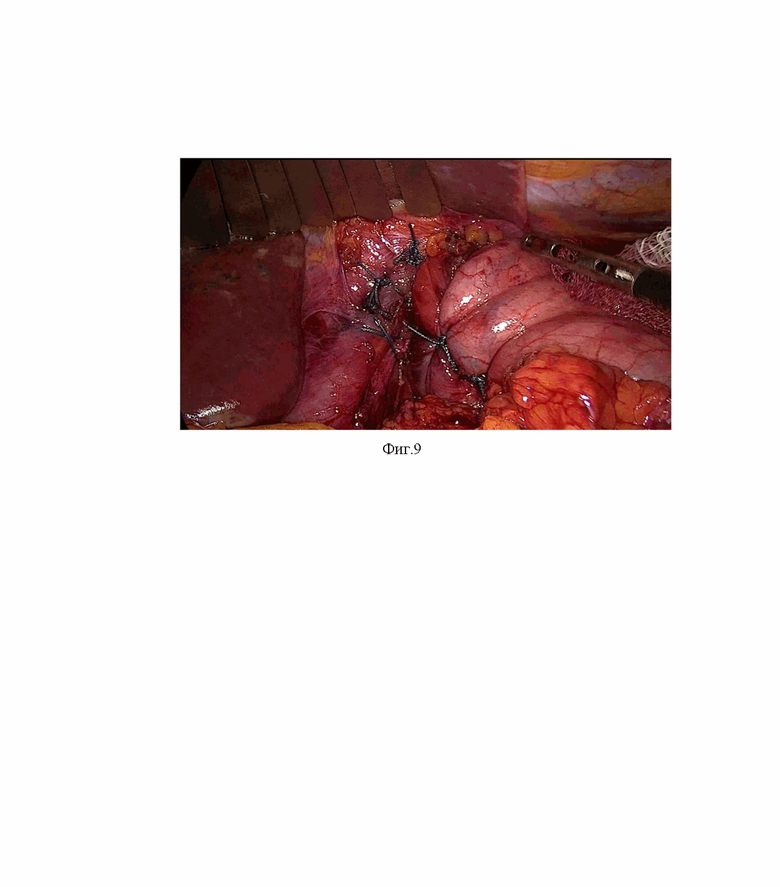
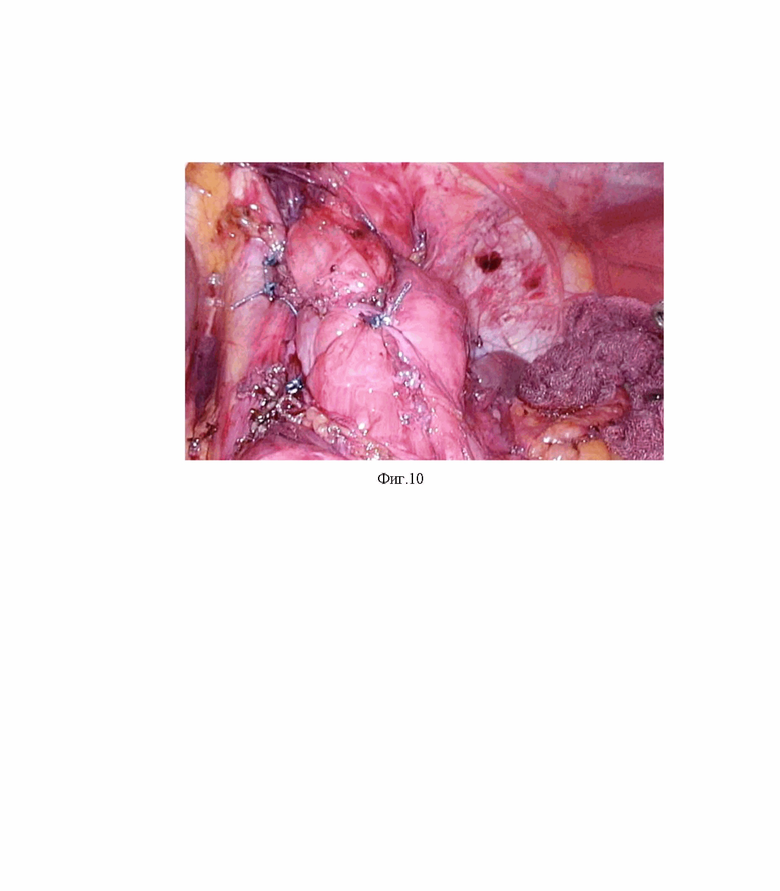
Изобретение поясняется иллюстрациями, где на Фиг. 1-8 представлены иллюстрации видов рецидива ГЭРБ и ГПОД; на Фиг. 9 представлено фото сформированной фундопликационной манжеты при достаточной мобилизации задней стенки дна желудка; на Фиг.10 - сформированная фундопликационная манжета при недостаточной мобилизации задней стенки дна желудка.
Осуществление изобретения
Существует несколько вариантов рецидива ГПОД, которые возникают либо вследствие прогрессирования заболевания, либо, чаще всего, в случае технических ошибок первичного оперативного вмешательства, которые неизбежно приведут к рецидиву ГПОД и ГЭРБ. В зависимости от причины или комплекса причин рецидивов, могут выполняться те или иные этапы оперативного вмешательства.
Можно выделить следующие виды рецидивов (известные классификации [Suppiah A.,2017; Horgan S., 1999; Hinder R.A., 1997], дополненные классификацией авторов):
1. Феномен телескопа (slipped Nissen) (Фиг.1);
2. Параэзофагеальная грыжа, чаще задний / латеральный дефект с вовлечением дна с гастроэзофагеальным переходом и ротацией манжетки (Фиг.2);
3. Миграция неизменённой манжеты в средостение (Фиг.3);
4. Несостоятельность манжеты (с/без миграции гастроэзофагеального перехода)
(Фиг.4, 5);
5. Рецидив ГЭРБ без анатомических изменений (недостаточно сформированный антирефлюксный механизм);
6. «Gas-bloat» синдром;
7. Провальнальная фундопликация:
a) Пищевое отверстие диафрагмы в неизменённом виде, т.е. не тронутое
хирургом (фиброзное или напряжённое);
b) Технически некорректно сформированная манжета (использование стенки тела желудка) (Фиг.6);
c) Гиперфункция манжетки (tight Nissen) (Фиг.7);
d) Сдавление пищевода сетчатым имплантом (crural stenosis) (Фиг.8);
e) Миграция манжеты вследствие отсутствия крурорафии;
f) Феномен телескопа вследствие отсутствия фиксации манжеты к пищеводу;
g) Травматизация n. Vagus;
h) Отсутствие мобилизации абдоминальной части пищевода;
i) Сохранение грыжевого мешка;
j) Использование рассасывающей нити на этапах формировании манжеты.
У пациентов может быть выявлен как изолированный вид, так и сочетание нескольких вышеописанных видов рецидива.
Предлагаемый способ применим при лечении всех форм рецидива ГЭРБ и ГПОД в представленной классификации, и может быть реализован следующим образом.
Перед операцией пациенту производят установку назогастрального зонда для декомпрессии желудка, выполняют общую анестезию.
Затем в асептических условиях через верхний параумбиликальный разрез-прокол до 12 мм производят вход в брюшную полость троакаром №1 (диаметр 10 мм), накладывают карбоксиперитонеум до 12 мм. рт. ст. с введением лапароскопической видеокамеры. Производят обзорную лапароскопию органов брюшной полости (печени, тонкой и толстой кишки, селезёнки, органов малого таза). Под визуальным контролем в брюшную полость вводят дополнительные троакары (№2 диаметром 10 мм в эпигастрий, №3 диаметром 5 мм в правое подреберье, №4 диаметром 13 мм в левое подреберье и №5 диаметром 5 мм параректально слева в мезогастральной области при необходимости. Пациенту придают положение Фаулера с расположением оптики по типу «взгляд сверху». Через троакар №2 вводят эдектрохирургический инструмент (как правило ультразвуковой коагулятор). Далее через троакары №2 и № 3 вводят мягкие кишечные зажимы. Через троакар №5 ассистент вводит печеночный ретрактор (лепестковый или типа «Golf Finger») для отведения вверх левой доли печени. На этом этапе проводится оценка состояния желудка, области пищеводного отверстия диафрагмы, наличие и степень спаечного процесса в зоне хирургического интереса. Благодаря использованию ультразвуковой энергии можно выполнять точечную диссекцию тканей без риска повреждения близлежащий структур, находящихся в спаечном процессе.
Одним из ключевых шагов при повторных антирефлюксных операциях является этап восстановления «нормальной» анатомии. Выполняют адгезиолизис в области кардиоэзофагеального перехода, вскрытие малого сальника, выход на основание ножек пищеводного отверстия диафрагмы с последующей мобилизацией каждой ножки. На данном этапе можно увидеть наличие или отсутствие ранее выполненной задней крурорафии, при её наличии производят снятие крурорафических швов. Следующим этапом выполняют частичную мобилизацию доступной части нижней порции заднего средостения, мобилизацию пищевода как латерально, так и медиально, пересечение мембранны лаймера-бертелли. При наличии дополнительно ветви от левой желудочной артерии к левой доле печени, которая сопровождает печеночную ветвь блуждающего нерва, диссекцию выполняют с сохранением артерии. Следующим этапом, при наличии миграции «старой» манжеты в средостенье, выполняют абдоминизацию манжетки с последующей абдоминизацией абдоминального отдела пищевода. На данном этапе оценивают состояние манжетки при её наличии, характер анатомического рецидива, а также оценивают наличие или отсутствие ранее выполненной абдоминизации пищевода. На этом этапе также выполняют ликвидацию параэзофагеальной грыжи и/или старого грыжевого мешка, который ранее не удалён при прошлой операции, при их наличии. Следующим этапом производят разбор старой фундопликационной манжеты с дальнейшей мобилизацией задней стенки дна желудка. На данном этапе оценивают, из каких стенок сформирована фундопликационная манжетка (стенки дна желудка или иные стенки желудка). Часто выраженный спаечный процесс не позволяет безопасно мобилизовать полностью заднюю стенку, при данной ситуации выполняют частичную мобилизацию задней стенки дна желудка. Далее производят атравматичное выделения правого и левого n. Vagus. На данном этапе оценивают состояние блуждающего нерва (пересечённый или целый). Затем производят удаление инородного материала (полипропиленовая сетка, лента из ксеноперекарда, LINX и т.д.) при его наличии.
После восстановления первичной анатомии выполняют заднюю и переднюю крурорафию Z-образными и узловыми швами по диаметру пищевода синтетическим не рассасывающимся полифиламентным шовным материалом, без ущемления. В случае сохранения остаточной полости больших размеров в средостении, в последнюю устанавливают силиконовый дренаж, который далее подключают к режиму активной аспирации. Затем производят тракцию пищевода вниз, выполняют фиксацию одним узловым швом правой и левой стенки пищевода к правой и левой ножке пищеводного отверстия диафрагмы, соответственно, синтетическим не рассасывающимся полифиламентным шовным материалом.
Окончательным этапом операции является этап формирования фундопликационной манжеты, которая не ротирует, не деформирует и не сдавливает пищевод. При этом предварительно оценивают степень мобилизации задней стенки дна желудка: при достаточной мобилизации проведение задней стенки дна желудка в сторону малой кривизны возможно без натяжения, ротации и деформации пищевода и желудка, при недостаточной мобилизации - данное проведение невозможно выполнить без натяжения, ротации и деформации пищевода и желудка. В случае достаточной мобилизации заднюю стенку дна желудка проводят под пищеводом в сторону малой кривизны, переднюю стенку дна желудка проводят над пищеводом в сторону малой кривизны, затем с помощью атравматичного не рассасывающегося полифиламентного шовного материала производят фиксацию обеих стенок к правой стенке пищевода по меньшей мере двумя узловыми швами, при этом при формировании каждого узлового шва осуществляют вкол-выкол в переднюю стенку дна желудка, затем следующий вкол-выкол в правую стенку пищевода на уровне кардиоэзофагеального перехода с последующим вколом-выколом на задней стенке дна желудка и затягивание узла. Таким образом формируют симметричную, не ротирующую и не сдавливающую пищевод манжету (длиной, преимущественно, около 20 мм).
При недостаточной мобилизации задней стенки дна желудка ввиду выраженного спаечного процесса в области дна, выполняют проведение передней стенки дна желудка в сторону малой кривизны и её фиксацию к передней стенке пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся полифиламентным шовным материалом, затем выполняют проведение задней стенки дна желудка под пищеводом в сторону малой кривизны и ее фиксацию к задней части пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся полифиламентным шовным материалом.
На заключительном этапе операции при необходимости устанавливают дренаж (5 мм) в левое поддиафрагмальное пространство через доступ в левом подреберье. Проводят контроль гемостаза, десуфляцию и затем удаляют троакары.
В соответствии с заявляемым способом было проведено 50 операций, в процессе которых отсутствовали осложнения. 40 пациентам не потребовалась терапия по поводу ГЭРБ в отдалённом послеоперационном периоде, 10 пациентов отмечали улучшение качества жизни, несмотря на приём терапии по поводу ГЭРБ.
Примеры реализации изобретения
Пример 1. Пациент K., 46 лет. Предъявлял жалобы на изжогу после приёма пищи, вздутие живота, боль в эпигастральной области после приёма пищи, рвоту съеденной пищей. Поступил в клинику с диагнозом рецидивная ГПОД. Диагноз был подтверждён с помощью рентгеноскопии и эзофагогастроскопии. Известно, что в 2017 году пациенту выполнена лапароскопическая фундопликация по Ниссену с пластикой полипропиленовой сеткой.
Пациент был обследован и подготовлен к операции. Перед операцией установлен назогастральный зонд, выполнена декомпрессия желудка. Выполнена операция - лапароскопическая рефундопликация. При этом после установки 5 лапароскопических портов и наложения карбоксиперитонеума до 12 мм рт. ст. был выполнен обзор органов брюшной полости. Далее через эпигастральный троакар установлен печёночный ретрактор, произведена тракция левой доли печени кверху. С использованием ультразвукового диссектора выполнен адгезиолизис в области кардиоэзофагельного перехода. При ревизии зоны операционного интереса в условиях выраженного рубцово-спаечного процесса в тканях было определено наличие элементов фундопликационной манжеты и металлических скоб с сетчатым имплантом. После выделения ножек пищеводного отверстия диафрагмы было установлено расширение отверстия до 2-х диаметров пищевода, также была отмечена миграция ранее установленного сетчатого протеза в заднее средостение. В ходе работы в зоне кардиоэзофагеального перехода интраоперационная картина свидетельствовала об отсутствии ранее выполненной крурорафии, также выявлен параэзофагеальный дефект с наличием грыжевого мешка без наличия параэзофагеальной грыжи, что явилось признаком сохраненного в ходе предшествующих вмешательств грыжевого мешка. По мере выполнения мобилизации абдоминального отдела пищевода было выявлено отсутствие рубцово-спаечного процесса, на основании чего можно было судить об отсутствии ранее выполненной адекватной мобилизации пищевода. После освобождения правой и левой ножек по контуру пищеводного отверстия диафрагмы был выполнен демонтаж фундопликационной манжеты с удалением полипропиленовой сетки, фиксирующих скоб и клипс. На данном этапе оперативного вмешательства было установлено, что манжета была сформирована из прекардиальной части желудка (передней и задней стенки тела желудка). После восстановления первичной анатомии зоны пищеводно-желудочного перехода было произведено выделение нижнего сегмента пищевода, низведение его в брюшную полость и атравматичное выделение левого и правого блуждающих нервов. Таким образом у пациента выявлен рецидив по типу провальной фундопликации (по представленной классификации). Далее в бессосудистой зоне позади пищеводного отверстия диафрагмы осуществлен доступ к задней стенке дна желудка с пересечением коротких желудочных артерий. Ввиду наличия большого дефекта в области заднего средостения было выполнено дренирование полости, после чего была произведена задняя крурорафия одним Z-образным швом и одним узловым швом, а также передняя крурорафия одним узловым швом с помощью нерассасывающегося синтетического полифиламентного шовного материала (Ethibond 2,0) таким образом, что пищеводное отверстие диафрагмы соответствовало калибру пищевода. Дополнительно произведена фиксация пищевода к правой и левой ножкам ПОД узловыми швами. Затем была сформирована фундопликационная манжета посредством проводения задней стенки дна желудка под пищеводом в сторону малой кривизны, передней стенки дна желудка – над пищеводом в сторону малой кривизны, и фиксации обеих стенок одним швом к правой стенке пищевода, выполняя два узловых шва синтетическим полифиламентными не рассасывающимся шовным материалом, сохраняя принцип симметричной не ротирующей и не сдавливающей пищевод манжеты. На заключительном этапе операции устанавливали дренаж (5 мм) в левое поддиафрагмальное пространство через доступ в левом подреберье. Производили контроль гемостаза, десуфляцию и затем удаление троакаров. Послеоперационный период протекал без осложнений, проводилась комплексная послеоперационная медикаментозная терапия, контроль анализов и активизация пациента. Через 1 день после операции выполнена рентгеноскопия с водорастворимым контрастным веществом - затёков нет, контраст свободно проходим в желудок. После рентгеноскопии произвели удаление назогастрального зонда, пациент начал самостоятельное питание. В удовлетворительном состоянии на 5-е сутки пациент был выписан на амбулаторное лечение. Проведенное через 3 месяца контрольное рентгеноскопическое исследование показало отсутствие задержки контрастного вещества в пищеводе. Данных по поводу дисфагии и изжоги - нет.
Пример 2. Пациентка Ш., 74 года. Жалобы на невозможность к отрыжке и рвоте, вздутие после приёма жидкой пищи, боли при приёме твёрдой пищи. По данным рентгеноскопии пищевода и желудка - состояние после фундопликации, данных за рецидив ГПОД нет, диагностирован gas bloat синдром. Известно, что в 2021 году пациенту выполнена лапаротомия, фундопликация по Ниссену. Пациент был обследован и подготовлен к операции. Выполнена операция - лапароскопическая рефундопликация. При этом после установки 5 лапароскопических портов и наложения карбоксиперитонеума до 12 мм рт. ст. был выполнен обзор органов брюшной полости. Далее через эпигастральный троакар установлен печёночный ретрактор, произведена тракция левой доли печени кверху. Устанавлен назогастральный зонд, выполнена декомпрессия желудка. С использованием ультразвукового диссектора выполнен адгезиолизис в области кардиоэзофагельного перехода. После вскрытия малого сальника произведена мобилизация основания ножек пищеводного отверстия диафрагмы, при мобилизации отмечено расширение отверстия до 2-х диаметров пищевода. В ходе работы в зоне кардиоэзофагеального перехода интраоперационная картина свидетельствовала об отсутствии ранее выполненной крурорафии. По мере выполнения абдоминизации пищевода было выявлено отсутствие рубцово-спаечного процесса, на основании чего можно было судить об отсутствии ранее выполненной адекватной мобилизации пищевода. После освобождения правой и левой ножек по контуру пищеводного отверстия диафрагмы был выполнен демонтаж фундопликационной манжеты. После восстановления первичной анатомии зоны пищеводно-желудочного перехода было произведено выделение нижнего сегмента пищевода, низведение его в брюшную полость и атравматичное выделение левого и правого блуждающих нервов. Таким образом у пациента выявлен рецидив по типу провальной фундопликации (по представленной классификации). Далее в бессосудистой зоне позади пищеводного отверстия диафрагмы осуществлен доступ к задней стенке дна желудка с пересечением коротких желудочных артерий. Выполнена задняя крурорафия 2- мя Z-образными швами и передняя крурорафия одним узловым швом по диаметру пищевода. Дополнительно произведена фиксация пищевода к правой и левой ножкам ПОД узловыми швами. С учетом выраженного спаечного процесса в области дна желудка (ранее выполненной манжеты), затрудняющего мобилизацию задней стенки дна желудка, была выполнена парциальная рефундопликация, при которой переднюю стенку дна желудка проводили в сторону малой кривизны и фиксировали к передней стенке пищевода двумя узловыми швами синтетическим не рассасывающимся шовным материалом, затем выполнили проведение задней стенки дна желудка под пищеводом в сторону малой кривизны и ее фиксацию к задней части пищевода двумя узловыми швами синтетическим не рассасывающимся шовным материалом. На заключительном этапе операции устанавливали дренаж (5 мм) в левое поддиафрагмальное пространство через доступ в левом подреберье. Производили контроль гемостаза, десуфляцию и затем удаление троакаров. Послеоперационный период протекал без осложнений, проводилась комплексная послеоперационная медикаментозная терапия, контроль анализов и активизация пациента. Через 1 день после операции выполнена рентгеноскопия с водорастворимым контрастным веществом - затёков нет, контраст свободно проходим в желудок. После рентгеноскопии произвели удаление назогастрального зонда, пациент начал самостоятельное питание. В удовлетворительном состоянии на 6-е сутки пациент был выписан на амбулаторное лечение. Проведенное через 3 месяца контрольное рентгеноскопическое исследование показало отсутствие задержки контрастного вещества в пищеводе. Данных по поводу дисфагии и изжоги - нет.
Таким образом, предлагаемый способ позволяет осуществлять безопасное лечение пациентов с рецидивом грыжи пищеводного отверстия диафрагмы с минимальными рисками интраоперационных осложнений в виде перфораций стенки пищевода и желудка, повреждение блуждающих нервов, и, как следствие, предотвращает возможные послеоперационные осложнения и снижает риски развития повторного рецидива заболевания.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АХАЛАЗИИ КАРДИИ С ПРИМЕНЕНИЕМ ГИДРОПРЕПАРОВКИ ТКАНЕЙ ПИЩЕВОДА ПОД ЭНДОСКОПИЧЕСКИМ КОНТРОЛЕМ | 2022 |
|
RU2794632C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АХАЛАЗИИ КАРДИАЛЬНОГО ОТДЕЛА ПИЩЕВОДА | 2021 |
|
RU2757527C1 |
| Способ фиксации дна желудка при выполнении робот-ассистированной лапароскопической фундопликации | 2023 |
|
RU2813330C1 |
| УСТРОЙСТВО ДЛЯ ЛАПАРОСКОПИЧЕСКОЙ ГИДРОПРЕПАРОВКИ ПОДСЛИЗИСТОГО СЛОЯ ПИЩЕВОДА | 2023 |
|
RU2812571C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГРЫЖ ПИЩЕВОДНОГО ОТВЕРСТИЯ ДИАФРАГМЫ | 2015 |
|
RU2611912C1 |
| Способ хирургического лечения ожирения в сочетании с грыжей пищеводного отверстия диафрагмы и гастроэзофагеальной рефлюксной болезнью | 2022 |
|
RU2794406C1 |
| Способ пластики грыжи пищеводного отверстия диафрагмы при хирургическом лечении морбидного ожирения | 2024 |
|
RU2840047C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГРЫЖИ ПИЩЕВОДНОГО ОТВЕРСТИЯ ДИАФРАГМЫ И ГАСТРОЭЗОФАГЕАЛЬНОЙ РЕФЛЮКСНОЙ БОЛЕЗНИ | 2016 |
|
RU2638282C1 |
| Способ антимиграционной фундопликационной манжетки при грыжах пищеводного отверстия диафрагмы | 2022 |
|
RU2800103C1 |
| СПОСОБ ПЛАСТИКИ ПИЩЕВОДНОГО ОТВЕРСТИЯ ДИАФРАГМЫ | 2013 |
|
RU2525732C1 |
Изобретение относится к медицине, а именно к абдоминальной хирургии, и может быть использовано при хирургическом лечении рецидива гастроэзофагеальной рефлюксной болезни грыжи пищеводного отверстия диафрагмы. Осуществляют демонтаж ранее установленной фундопликационной манжеты с восстановлением первичной анатомии зоны пищеводно-желудочного перехода, выполняют заднюю и переднюю крурорафию по диаметру пищевода, фиксацию пищевода к правой и левой ножкам пищеводного отверстия диафрагмы и формирование новой фундопликационной манжеты. При этом перед формированием фундопликационной манжеты оценивают степень мобилизации задней стенки дна желудка, и при ее достаточной мобилизации заднюю стенку дна желудка проводят под пищеводом в сторону малой кривизны, переднюю стенку дна желудка проводят над пищеводом в сторону малой кривизны, и обе стенки фиксируют к правой стенке пищевода по меньшей мере двумя узловыми швами, захватывая в один шов последовательно переднюю стенку дна желудка, правую стенку пищевода на уровне кардиоэзофагеального перехода и заднюю стенку дна желудка, с формированием симметричной фундопликационной манжеты. При недостаточной мобилизации задней стенки дна желудка выполняют проведение передней стенки дна желудка в сторону малой кривизны и ее фиксацию к передней стенке пищевода по меньшей мере двумя узловыми швами, затем выполняют проведение задней стенки дна желудка под пищеводом в сторону малой кривизны и ее фиксацию к задней стенке пищевода по меньшей мере двумя узловыми швами. Изобретение обеспечивает уменьшение рисков развития интраоперационных и послеоперационных осложнений, а также рисков развития повторного рецидива заболевания за счет формирования адекватного антирефлюксного механизма. 3 з.п. ф-лы, 10 ил., 2 пр.
1. Способ лапароскопической рефундопликации при рецидивах гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы, включающий установку назогастрального зонда, выполнение декомпрессии желудка, установку троакаров, наложение карбоксиперитонеума, введение печеночного ретрактора с тракцией левой доли печени кверху, выполнение адгезиолизиса в области кардиоэзофагельного перехода, вскрытие малого сальника выше печеночной ветви блуждающего нерва с последующей мобилизацией правой и левой ножек пищеводного отверстия диафрагмы, мобилизацию ранее установленной фундопликационной манжеты и абдоминального отдела пищевода с низведением их в брюшную полость, демонтаж ранее установленной фундопликационной манжеты с восстановлением первичной анатомии зоны пищеводно-желудочного перехода, атравматичное выделение правого и левого блуждающих нервов, выполнение доступа к задней стенке дна желудка в бессосудистой зоне позади пищеводного отверстия диафрагмы с пересечением коротких желудочных артерий, выполнение задней и передней крурорафии по диаметру пищевода, фиксацию пищевода к правой и левой ножкам пищеводного отверстия диафрагмы узловыми швами синтетическим не рассасывающимся шовным материалом, формирование фундопликационной манжеты, установку дренажа, контроль гемостаза, десуфляцию, удаление троакаров, при этом перед формированием фундопликационной манжеты оценивают степень мобилизации задней стенки дна желудка, и при ее достаточной мобилизации заднюю стенку дна желудка проводят под пищеводом в сторону малой кривизны, переднюю стенку дна желудка проводят над пищеводом в сторону малой кривизны, и обе стенки фиксируют к правой стенке пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся шовным материалом, захватывая в один шов последовательно переднюю стенку дна желудка, правую стенку пищевода на уровне кардиоэзофагеального перехода и заднюю стенку дна желудка, с формированием симметричной фундопликационной манжеты; при недостаточной мобилизации задней стенки дна желудка выполняют проведение передней стенки дна желудка в сторону малой кривизны и ее фиксацию к передней стенке пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся шовным материалом, затем выполняют проведение задней стенки дна желудка под пищеводом в сторону малой кривизны и ее фиксацию к задней части пищевода по меньшей мере двумя узловыми швами синтетическим не рассасывающимся шовным материалом.
2. Способ по п.1, отличающийся тем, что в случае миграции ранее установленной фундопликационной манжеты в средостенье осуществляют мобилизацию фундопликационной манжеты по направлению пищевода в брюшную полость, с последующей мобилизацией абдоминального отдела пищевода.
3. Способ по п.1, отличающийся тем, что после этапа выделения правого и левого блуждающих нервов при наличии инородных тел в зоне пищевода и/или манжеты производят их удаление.
4. Способ по п.1, отличающийся тем, что после этапа мобилизации абдоминального отдела пищевода при наличии параэзофагеальной грыжи производят мобилизацию содержимого и удаление грыжевого мешка.
| ГОЛОЛОБОВ Г.Ю | |||
| и др | |||
| Лапароскопическая коррекция рецидива гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы после дважды провальной фундопликации | |||
| Клинический случай | |||
| Хирургическая практика | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АХАЛАЗИИ КАРДИАЛЬНОГО ОТДЕЛА ПИЩЕВОДА | 2021 |
|
RU2757527C1 |
| СПОСОБ ФУНДОПЛИКАЦИИ | 2008 |
|
RU2371108C1 |
| СЕМЕНЯКИН И.В | |||
| и др | |||
| Сравнительный анализ | |||
Авторы
Даты
2025-02-25—Публикация
2024-05-28—Подача