Изобретение относится к области медицины, в частности к офтальмоонкологии, и может быть использовано в органосохранном лечении увеальной меланомы на основе применения транссклеральной фотодинамической терапии.
Известен способ фотодинамической терапии меланомы хориоидеи [1]. В рамках данного способа внутривенно вводят ФС хлоринового ряда в дозе 0,8-1 мг/кг веса. При этом 70% дозы вводят капельно в течение 10 минут. Через 1,5 часа оставшиеся 30% дозы вводят болюсно. По окончании введения ФС облучают новообразование лазером транспупиллярно с длиной волны, соответствующей максимуму поглощения ФС светового излучения с перекрытием соседних полей. При этом облучают периферию опухоли с захватом здоровых тканей не менее 1 мм от офтальмоскопически видимой границы опухоли. Причем плотность энергии на одно поле 25-40 Дж/см2. Затем облучают всю поверхность опухоли концентрично от периферии к центру с плотностью энергии 110-120 Дж/см2 на одно поле. Через 2 недели повторяют внутривенное введение ФС и транспупиллярное лазерное облучение поверхности опухоли. Проводят от 2 до 4 сеансов внутривенного введения ФС и лазерного облучения поверхности опухоли до достижения полной ее резорбции.
К недостаткам данного способа можно отнести то, что разрушающее воздействие оказывается только на вершину опухоли. Поскольку рост опухоли и развитие ее сосудистой сети начинается с ее основания (от склеры), транспупиллярного воздействия зачастую недостаточно, чтобы разрушить весь опухолевый субстрат. Кроме того, облучение опухоли от периферии к центру может снизить эффективность фотодинамической терапии за счет перекрытия поступления кислорода к центру опухоли. Еще одним негативным фактором является проведение облучения через 1,5 часа после введения фотосенсибилизатора, что приводит к излишнему облучению здоровых тканей, так как фотосенсибилизатор выводится полностью из здоровых тканей через 3 часа после его введения. Также к недостаткам данной методики можно отнести повторное лазерное облучение через 2 недели, что сопряжено с повышенной лазерной нагрузкой на окружающие ткани, усилением экссудативной реакции и рисками послеоперационных осложнений (катаракта, отслойка сетчатки и др.).
Также известен способ органосохраняющего лечения внутриглазных опухолей [2], в ходе которого предварительно осуществляют транспупиллярную фотодинамическую терапию, а затем через 3-20 суток проводят транссклеральную фотодинамическую терапию.
К недостаткам данного способа можно отнести необходимость двухэтапного подхода с широким временным интервалом, выбор которого осуществляется эмпирически, необходимость повторного введения фотосенсибилизатора, отсутствие данных о расчёте дозы препарата, а также отсутствие индивидуального подбора параметров лазерного излучения в зависимости от характеристик опухоли и использование зонда-световода единого диаметра. Также к недостаткам можно отнести высокие риски распространения опухолевых клеток в системный кровоток, а именно угрозу гематогенного метастазирования при проведении эндорезекции опухоли (в случае наличия остаточных активных опухолевых клеток). Также известен способ органосохраняющего лечения меланомы хориоидеи на основе применения гибридной фотодинамической терапии [3], в ходе которого осуществляют транспупиллярную и транссклеральную фотодинамическую терапию одновременно. При этом используют фотосенсибилизатор «Фотолон» в расчете 0,8 мг/кг веса.
Наиболее близким к заявляемому изобретению является способ лечения внутриглазных опухолей [4], в ходе которого внутривенно вводят фотосенсибилизатор фотосенс из расчета 0,1-1,0 мг/кг веса больного. Через 48-72 часа с момента введения фотосенса проводят фотодинамическую терапию лазерным излучением на длине волны 675 нм, при этом облучение подводят транссклерально после определения места проекции основания опухоли на склеру трансиллюминационным путем. Облучают экспозиционной дозой 80-800 мВт/см2 с помощью цилиндрического световода, располагая его на таком расстоянии от склеры, чтобы диаметр пучка лазерного излучения перекрывал на 1-2 мм диаметр основания опухоли в месте проекции ее на склере. Данное изобретение выбрано в качестве прототипа заявляемого способа.
К недостаткам двух вышеприведенных способов можно отнести отсутствие возможности выбора индивидуальных параметров лазерного излучения в зависимости от метрических характеристик опухоли. Это в разных случаях может приводить как к недостаточному лазерному воздействию, так и к излишнему облучению. Первое может привести к неполному охвату всего основания опухоли и соответственно к неполному регрессу или последующему рецидиву увеальной меланомы.
При этом не только параметры лазерного-излучения, но и особенности конструкции инструментов, применяемых для доставки лазерного излучения, а также варианты их применения (транссклеральный) играют важную роль в достижении планируемого хирургического эффекта. В вышеприведенных способах отсутствует возможность персонифицированного подбора транссклеральных зондов-наконечников различных диаметров в зависимости от метрических характеристик опухоли. Это может привести к излишнему повреждению здоровых тканей и возникновению послеоперационных осложнений.
На сегодняшний день известны различные зонды-наконечники, используемые в фотодинамической терапии, как цилиндрической [5, 6, 7], так и конусообразной формы [8, 9]. Также известны транссклеральные зонды-наконечники [10, 11, 12], но не известен набор транссклеральных зондов-наконечников, позволяющий осуществлять эффективный и персонифицированный подход в лечении увеальных меланом. В связи с этим заявляемый набор не имеет аналогов и прототипа. Несовершенная конструкция зонда для транссклеральных воздействий может вести к неправильной ориентации излучающего элемента и к гипо- или гиперкоагуляционному эффекту. При этом для разных клинических ситуаций могут подходить разные по характеристикам зонды и, соответственно, разные параметры облучения. Исходя из этих предпосылок, было разработано заявляемое изобретение.
Технической проблемой является необходимость разработки эффективного и персонифицированного подхода в органосохранном лечении пациентов с увеальной меланомой на основе применения транссклеральной фотодинамической терапии.
Технический результат состоит в повышении эффективности и избирательности органосохранного лечения пациентов с увеальной меланомой с помощью транссклеральной фотодинамической терапии и в снижении рисков послеоперационных осложнений.
Технический результат достигается тем, что в способе лечения увеальной меланомы на основе применения транссклеральной фотодинамической терапии, в ходе которого пациенту внутривенно капельно вводят фотосенсибилизатор хлоринового ряда, после чего в условиях кратковременного общего наркоза осуществляют лазерное облучение опухоли длиной волны 662 нм транссклерально с помощью лазерной установки, согласно изобретению определяют локализацию опухоли, диаметр основания, а перед облучением на лазерный световод устанавливают инновационный транссклеральный зонд-наконечник, причем
при локализации опухоли в преэкваториальных отделах и диаметре основания от 10,1 до 15,0 мм используют транссклеральный зонд-наконечник, диаметр которого находится в диапазоне 12,5-17,5 мм, а облучение проводят с мощностью лазера от 0,9 Вт до 1,6 Вт, со временем экспозиции от 10 до 15 мин;
при локализации опухоли в преэкваториальных отделах и диаметре основания опухоли от 7,1 до 10,0 мм используют транссклеральный зонд-наконечник, диаметр которого находится в диапазоне 9,0-12,4 мм, а облучение проводят с мощностью лазера от 0,51 Вт до 0,9 Вт, со временем экспозиции от 10 до 15 мин;
при локализации опухоли в преэкваториальных отделах и диаметре основания опухоли от 5,1 до 7,0 мм используют транссклеральный зонд-наконечник, диаметр которого находится в диапазоне 6,5-8,9 мм, а облучение проводят с мощностью лазера от 0,26 Вт до 0,4 Вт, со временем экспозиции от 10 до 15 мин;
при локализации опухоли в преэкваториальных отделах и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого находится в диапазоне 4,0-6,4 мм, а облучение проводят с мощностью лазера от 0,16 Вт до 0,25 Вт, со временем экспозиции от 10 до 15 мин;
при локализации опухоли в пределах экватора глазного яблока и при диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого находится в диапазоне 2,5-3,9 мм, а облучение проводят с мощностью лазера от 0,04 Вт до 0,1 Вт, со временем экспозиции от 10 до 15 мин;
при постэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого находится в диапазоне 1,5-2,4 мм, а облучение проводят с мощностью лазера от 0,02 Вт до 0,04 Вт, со временем экспозиции от 10 до 15 мин;
Технический результат достигается тем, что набор транссклеральных зондов-наконечников включает шесть зондов, характеризующихся тем, что сторона, предназначенная для сопряжения с глазом пациента, выполнена круглой формы, причем с этой стороны
у первого зонда-наконечника диаметр находится в диапазоне 12,5-17,5 мм;
у второго зонда-наконечника диаметр находится в диапазоне 9,0-12,4 мм;
у третьего зонда-наконечника диаметр находится в диапазоне 6,5-8,9 мм;
у четвертого зонда-наконечника диаметр находится в диапазоне 4,0-6,4 мм;
у пятого зонда-наконечника диаметр находится в диапазоне 2,5-3,9 мм;
у шестого зонда-наконечника диаметр находится в диапазоне 1,5-2,4 мм.
Благодаря инновационным зондам-наконечникам и их персонифицированному подбору удается повысить эффективность лечения и сократить время проведения операции, что сокращает как нахождение пациента в наркозе, так и минимизирует излишнюю травматизацию склеры. Такая технология исключает необходимость постоянного перемещения зонда-наконечника по склере.
Таким образом, заявляемое изобретение является новым, эффективным, относительно простым в исполнении, малоинвазивным, хорошо прогнозируемым и достаточно щадящим способом лечения увеальной меланомы. Возможность его применения во многом связана с использованием лазеров соответствующего диапазона, инструментария, а также оптимально подобранными параметрами облучения.
В рамках заявляемого способа используют набор инновационных транссклеральных зондов-наконечников с диаметрами 12,5-17,5, 9,0-12,4, 6,5-8,9, 4,0-6,4, 2,5-3,9, 1,5-2,4 мм. Согласно исследованию, проведенному авторами изобретения, именно такие параметры зондов-наконечников обеспечивают повышение эффективности и избирательности лечения увеальных меланом с помощью транссклеральной фотодинамической терапии и снижение рисков послеоперационных осложнений. Однако в наиболее предпочтительном варианте реализации используют транссклеральные зонды-наконечники 15±0,2, 10±0,2, 7±0,2, 5±0,2, 3±0,2 и 2±0,2 мм и используют уточненные параметры облучения, а именно:
при преэкваториальной локализации опухоли и диаметре основания от 10,1 до 15,0 мм используют транссклеральный зонд-наконечник с диаметром 15±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 1,5 Вт и временем экспозиции 10 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 7,1 до 10,0 мм используют транссклеральный зонд-наконечник с диаметром 10±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,66 Вт и временем экспозиции 10 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 5,1 до 7,0 мм используют транссклеральный зонд-наконечник с диаметром 7±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,33 Вт и временем экспозиции 10 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник с диаметром 5±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,16 Вт и временем экспозиции 15 мин;
при локализации опухоли в пределах экватора глазного яблока и при диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник с диаметром 3±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,06 Вт и временем экспозиции 10 мин;
при постэкваториальной локализации опухоли и диаметре основания опухоли от 3,0до 5,0 мм используют транссклеральный зонд-наконечник с диаметром 2±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,03 Вт и временем экспозиции 10 мин.
В предпочтительном варианте реализации изобретения внутренняя поверхность инновационных зондов-наконечников выполнена ступенчатой. Это позволяет повысить коэффициент отражения лазерного излучения и снижает потери мощности лазерного излучения до минимума, что обеспечивает достаточное лазерное воздействие и положительно влияет на эффективность лечения в целом.
Также в предпочтительном варианте реализации изобретения каждый зонд-наконечник оснащен элементом, позволяющим его идентифицировать при подключении к лазеру. В наиболее предпочтительном варианте реализации изобретения в качестве элемента, позволяющего идентифицировать зонд-наконечник при подключении к лазеру, использована радиочастотная метка.
Также в одном из предпочтительных вариантов реализации изобретения каждый зонд-наконечник оснащен стеклом, установленным внутри корпуса со стороны, предназначенной для сопряжения с глазом пациента. Использование такого зонда-наконечника позволяет фокусировать лазерное излучение, что снижает пороговую энергию, необходимую для коагуляции ткани и ведет к меньшему повреждению склеры.
Заявляемое изобретение поясняется чертежами.
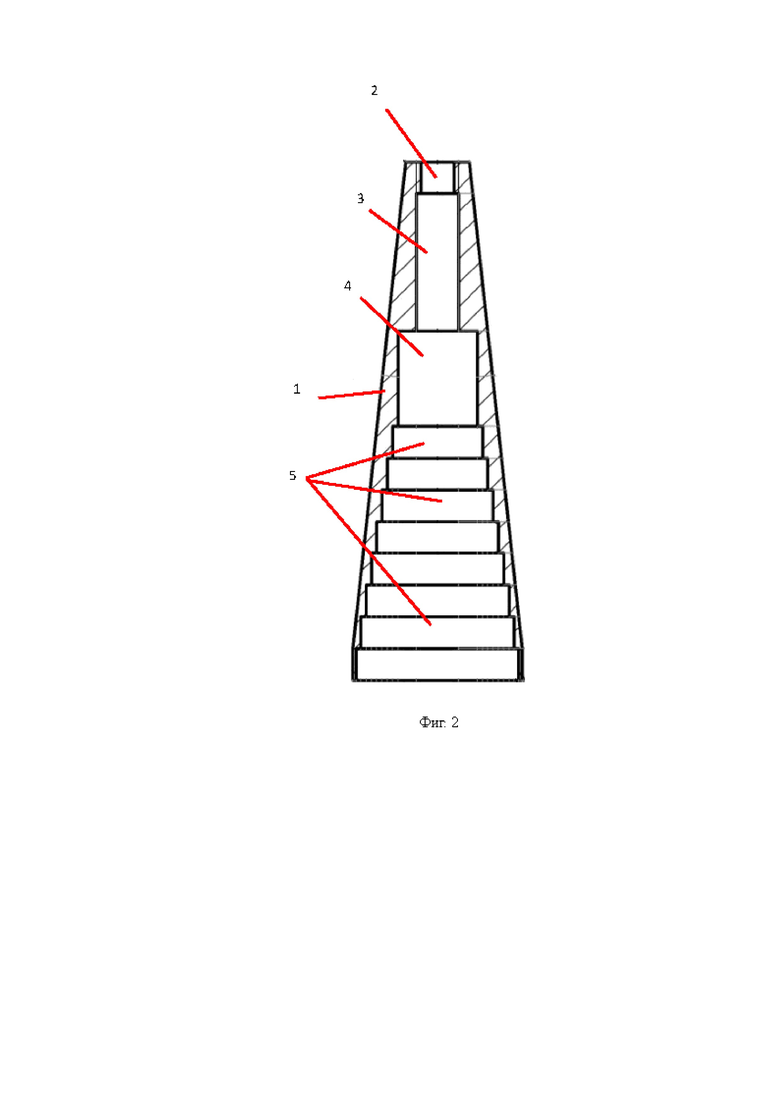
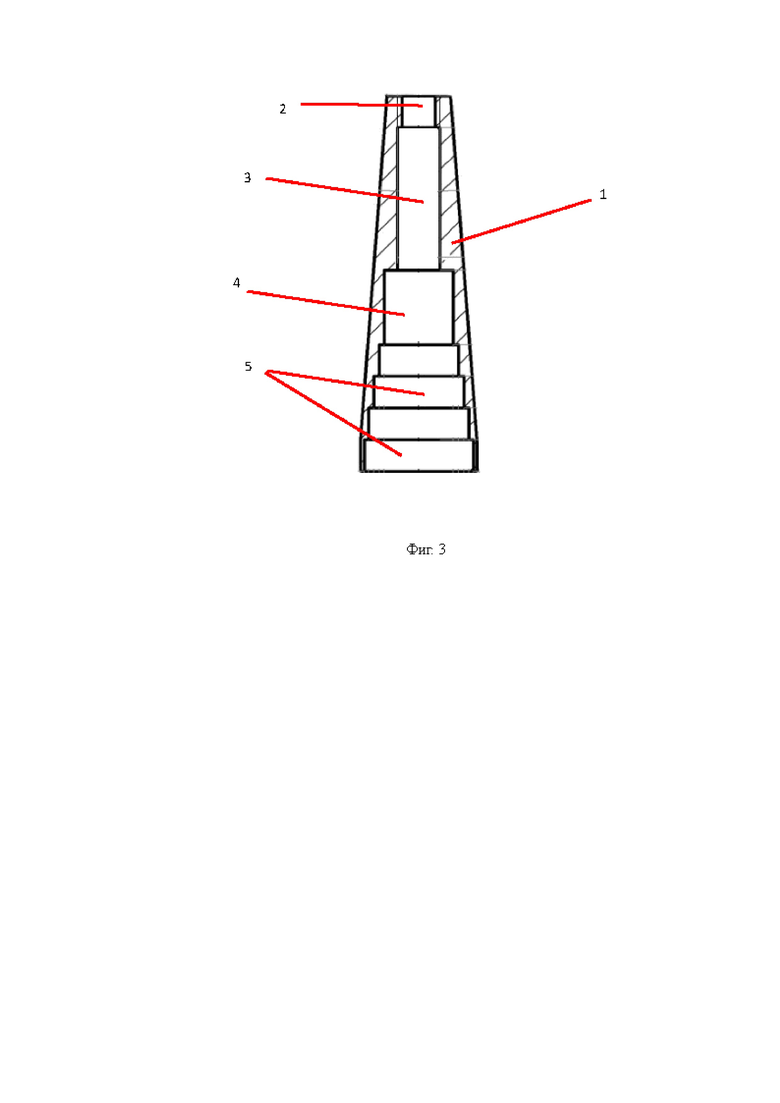
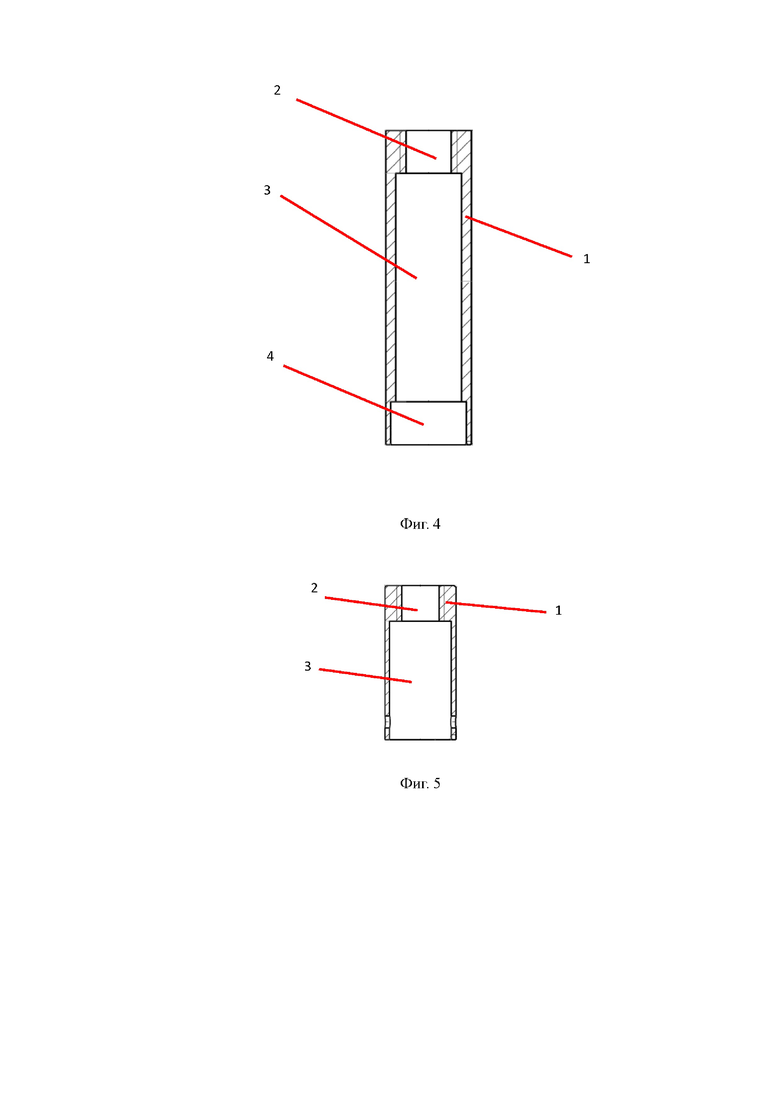
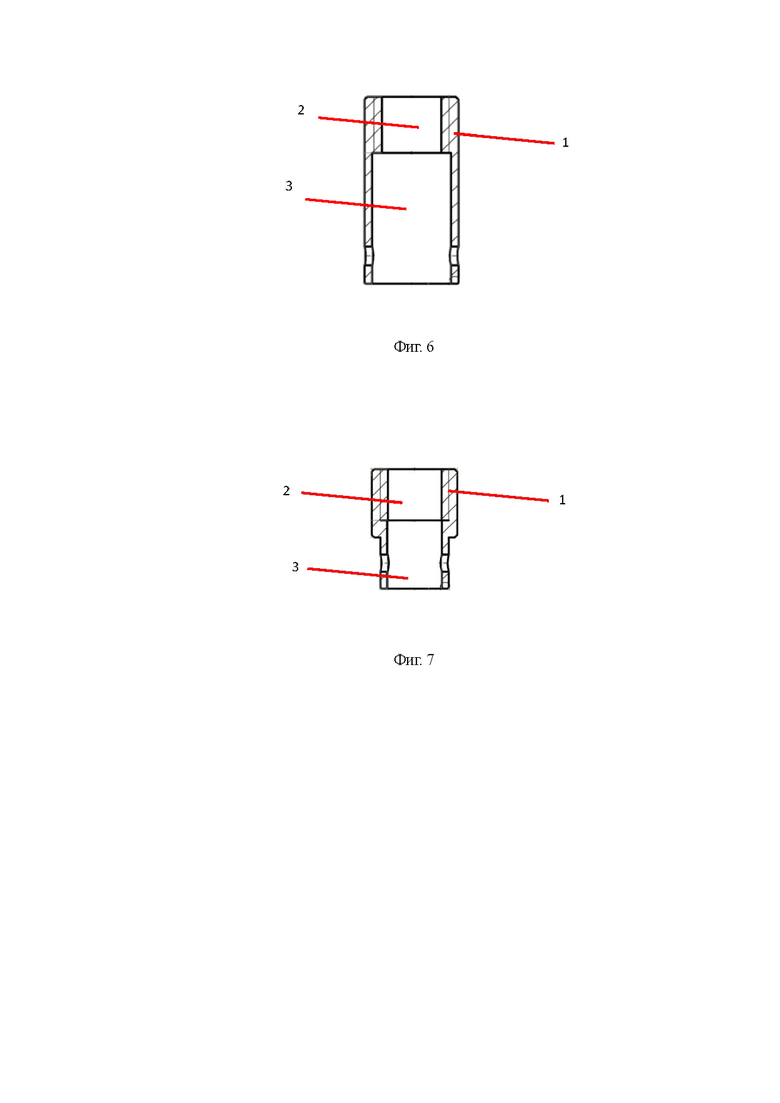
Фотография набора трансклеральных зондов-наконечников приведена на фиг. 1. Первый (наиболее крупный) транссклеральный зонд-наконечник (12,5-17,5 мм) в продольном разрезе представлен на фиг. 2. Второй транссклеральный зонд-наконечник (9,0-12,4 мм) в продольном разрезе представлен на фиг. 3. Третий транссклеральный зонд-наконечник (6,5-8,9 мм) в продольном разрезе представлен на фиг. 4. Четвертый транссклеральный зонд-наконечник (4,0-6,4 мм) в продольном разрезе представлен на фиг. 5. Пятый транссклеральный зонд-наконечник (2,5-3,9 мм) в продольном разрезе представлен на фиг. 6. Шестой транссклеральный зонд-наконечник (1,5-2,4 мм) в продольном разрезе представлен на фиг. 7.
Первый зонд-наконечник (12,5-17,5 мм) включает корпус 1, выполненный в форме полого усеченного конуса. Большее основание конуса предназначено для сопряжения с глазом пациента, а меньшее – с лазером. Внутренняя поверхность корпуса 1 выполнена ступенчатой. Причем при рассмотрении в продольном сечении ширина ступеней 2, 3, 4 и 5 увеличивается от меньшего основания усеченного конуса к большему, а высота первой ступени 2 меньше высоты второй и третьей ступеней 3, 4. При этом высота второй ступени 3 больше высоты третьей ступени 4, а высота остальных ступеней 5 одинаковая и равна высоте первой ступени 2. Предпочтительно такой зонд-наконечник содержит восемь ступеней, обозначенных позицией 5. Большее основание, предназначенное для сопряжения с глазом пациента, выполнено диаметром 12,5-17,5 мм. В предпочтительном варианте реализации диаметр составляет 15±0,2 мм. Общая длина первого зонда-наконечника предпочтительно составляет 50±8 мм.
Второй зонд-наконечник (9,0-12,4 мм) конструктивно выполнен похожим на первый, за исключением меньших длины и диаметра большего основания, предназначенного для сопряжения с глазом, составляет 9,0-12,4 мм. В предпочтительном варианте реализации диаметр составляет 10±0,2 мм. Общая длина второго зонда-наконечника предпочтительно составляет 35±5 мм.
Третий зонд-наконечник (6,5-8,9 мм) включает корпус 1, выполненный в форме полого цилиндра. Одно основание со стороны, предназначенной для сопряжения с лазером, выполнено с меньшим внутренним диаметром по сравнению с основанием со стороны, предназначенной для сопряжения с глазом пациента. Внутренняя поверхность выполнена ступенчатой. При рассмотрении в продольном разрезе ширина ступеней 2, 3 и 4 увеличивается от основания со стороны, предназначенной для сопряжения с лазером, к основанию со стороны, предназначенной для сопряжения с глазом пациента. Высота первой и третей ступеней 2, 4 совпадают, а высота второй ступени 3 превышает высоты первой и третьей ступеней 2, 4. Диаметр основания со стороны, предназначенной для сопряжения с глазом пациента, составляет 6,5-8,9 мм. В предпочтительном варианте реализации диаметр составляет 7±0,2 мм. Общая длина третьего зонда-наконечника предпочтительно составляет 22±4 мм.
Четвертый зонд-наконечник (4,0-6,4 мм) конструктивно соответствует третьему, за исключением меньших длины, внешнего диаметра с обеих сторон и внутреннего диаметра основания со стороны, предназначенной для сопряжения с глазом пациента. Также в конструкции четвертого зонда-наконечника отсутствует третья ступень. Зонд содержит только цилиндрический корпус 1, а также первую и вторую ступени 2, 3. Диаметр основания со стороны, предназначенной для сопряжения с глазом пациента, составляет 4,0-6,4 мм. В предпочтительном варианте реализации диаметр составляет 5±0,2 мм. Общая длина четвертого зонда-наконечника предпочтительно составляет 13±3 мм.
Пятый зонд-наконечник конструктивно соответствует четвертому, за исключением меньших длины, внешнего диаметра с обеих сторон и внутреннего диаметра основания со стороны, предназначенной для сопряжения с глазом пациента. Также по сравнению с четвертым зондом-наконечником в пятом вторая ступень 3 выполнена с меньшей длиной. Таким образом, пятый зонд-наконечник включает цилиндрический корпус 1, первую и вторую ступени 2, 3. Диаметр основания со стороны, предназначенной для сопряжения с глазом пациента, составляет 2,5-3,9 мм. В предпочтительном варианте реализации диаметр составляет 3±0,2 мм. Общая длина пятого зонда-наконечника предпочтительно составляет 10±2,5 мм.
Шестой зонд-наконечник выполнен в виде двух соединенных между собой цилиндров разного внешнего диаметра, представляющих собой корпус 1. Причем внешний диаметр корпуса 1 со стороны, предназначенной для сопряжения с лазером, превышает внешний диаметр корпуса 1 со стороны, предназначенной для сопряжения с глазом пациента. Внутренний диаметр с обеих сторон одинаковым, при этом зонд-наконечник содержит две ступени, первую ступень 1, соответствующую аналогичной ступени пятого зонда-наконечника, и вторую ступень 6. Вторая ступень содержит выступ, расположенный радиально. Выступ обеспечивает сохранение ступенчатой структуры шестого зонда-наконечника при выполнении его ступеней одинаковой ширины при рассмотрении в продольном разрезе. При этом высота второй ступени 6 превышает высоту первой ступени 2. Диаметр основания со стороны, предназначенной для сопряжения с глазом пациента, составляет 1,5-2,4 мм. В предпочтительном варианте реализации диаметр составляет 2±0,2 мм. Общая длина шестого зонда-наконечника предпочтительно составляет 7±2 мм.
В предпочтительном варианте реализации изобретения каждый зонд-наконечник оснащен элементом, позволяющим его идентифицировать при подключении к лазеру. В наиболее предпочтительном варианте реализации изобретения в качестве элемента, позволяющего идентифицировать зонд-наконечник при подключении к лазеру, использована радиочастотная метка. Эти элементы не показаны на чертежах. Также в одном из предпочтительных вариантов реализации изобретения каждый зонд-наконечник оснащен стеклом, установленным внутри корпуса со стороны, предназначенной для сопряжения с глазом пациента.
При выборе конкретного транссклерального зонда-наконечника ориентируются на его диаметр, под которым понимают внешний диаметр у основания конуса или цилиндра со стороны, предназначенной для сопряжения с глазом пациента.
Специалисту ясно, что приведенные параметры относятся к вариантам реализации и не ограничивают возможные иные варианты в рамках формулы заявляемого изобретения. Кроме того, заявляемый способ наиболее эффективен для опухолей с элевацией до 6,5 мм (включительно). При элевации опухоли более 6,5 мм наиболее эффективным является гибридная фотодинамическая терапия, подразумевающая использование заявляемого способа с транспупиллярной фотодинамической терапией (например, по аналогии с патентом RU 2785609) [3].
Заявляемый способ осуществляют следующим образом.
До начала операции пациенту проводят ультразвуковое исследование глаза с целью определения локализации и размеров (элевации и диаметра основания) опухоли.
Пациенту внутривенно капельно за 3 часа до операции вводят фотосенсибилизатор на основе хлорина е6, типа «Фоторан» или «Фотолон» в расчете 0,8-1,2 мг/кг веса. До начала лечения при помощи дозиметра проводят измерение лазерного излучения, которое должно соответствовать установленным параметрам на экране лазерного аппарата. Пациенту выполняют наркоз общий интубационный, затем осуществляют конъюктивальный доступ и устанавливают держалки на глазодвигательные мышцы в проекции опухоли. Далее выполняют интраоперационную диафаноскопию для маркировки границ опухоли, после чего осуществляют индивидуальный подбор инновационного зонда-наконечника (12,5-17,5, 9,0-12,4, 6,5-8,9, 4,0-6,4, 2,5-3,9, 1,5-2,4 мм) в зависимости от локализации и диаметра основания опухоли.
При преэкваториальной локализации опухоли и диаметре основания от 10,1 до 15,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 12,5-17,5 мм, а облучение проводят с мощностью лазера 0,9-1,6 Вт и временем экспозиции 10-15 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 7,1 до 10,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 9,0-12,4 мм, а облучение проводят с мощностью лазера 0,51-0,9 Вт и временем экспозиции 10-15 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 5,1 до 7,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 6,5-8,9, а облучение проводят с мощностью лазера 0,26-0,4 Вт и временем экспозиции 10-15 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 4,0-6,4, а облучение проводят с мощностью лазера 0,1-0,25 Вт и временем экспозиции 10-15 мин;
при локализации опухоли в пределах экватора глазного яблока и при диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 2,5-3,9, а облучение проводят с мощностью лазера 0,04-0,1 Вт и временем экспозиции 10-15 мин;
при постэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 1,5-2,4, а облучение проводят с мощностью лазера 0,02-0,04 Вт и временем экспозиции 10-15 мин.
Выбранный зонд-наконечник удерживают за корпус 1 и соединяют с лазером с одной стороны, а противоположную сторону прикладывают к глазу пациента в соответствии с локализацией опухоли, после чего осуществляется лазерное излучение. Ступени 2, 3, 4, 5, 6 (при их наличии) обеспечивают отражение излучения и снижение потерь мощности.
Опухоль облучают последовательно, концентрично по направлению от центра к периферии новообразования, с перекрытием соседних полей на 10-15% площади и с захватом здоровых тканей не менее 1,5 мм. По окончании операции накладывают рассасывающийся шов на конъюнктиву (викрил 8:0).
Заявляемое изобретение поясняется примерами.
Пример 1. Клинический случай.
Пациент А, мужчина, в возрасте 45 л., поступил с диагнозом меланома цилиарного тела T3aN0M0 IIВ стадия правого глаза. Локализация преэкваториальная в нижних отделах, при проведении комплексного ультразвукового исследования: элевация опухоли – 6,5 мм, диаметр основания - 13,1 мм, в режиме ЦДК - гиперваскулярная. Учитывая клинико-инструментальные данные, было принято решение провести лечение с использованием заявляемого способа.
Пациенту вводили фотосенсибилизатор «Фоторан» в расчете 0,8 мг/кг веса за 3 часа до операции. Наркоз общий интубационный. Далее осуществили конъюнктивальный доступ и установили держалки на глазодвигательные мышцы в проекции опухоли. Для маркировки границ опухоли была выполнена интраоперационная диафаноскопия. При проведении операции использовали зонд-наконечник, диаметр основания которого со стороны, предназначенной для сопряжения с глазом пациента, составлял 15 мм. Опухоль облучали с захватом здоровых тканей (не менее 1 мм от каждой границы), одной экспозицией (зонд 15 мм) в течение 10 минут. При этом параметры лазерного излучения были автоматизированы для используемого зонда и составляли: мощность – 1,5 Вт, плотность мощности с учетом потерь в склере составила 0,4 Вт/см2; плотность энергии за время экспозиции 10 мин составила 240 Дж/см2. По окончании операции наложили рассасывающийся шов на конъюнктиву (викрил 8:0).
В результате был достигнут регресс опухоли 87%.
Пример 2. Клинический случай.
Пациент Б, мужчина, в возрасте 67 л., поступил с диагнозом меланома цилиохориоидальной зоны T2aN0M0 IIA cтадия правого глаза. Локализация преэкваториальная в наружных отделах глазного яблока, при проведении комплексного ультразвукового исследования: элевация опухоли – 6,1 мм, диаметр основания опухоли 8,9 мм, в режиме ЦДК - гиперваскулярная. Учитывая клинико-инструментальные данные, было принято решение провести лечение с использованием заявляемого способа.
Пациенту вводили фотосенсибилизатор «Фоторан» в расчете 1,2 мг/кг веса за 3 часа до операции. Пациенту выполнили наркоз общий интубационный. Далее провели конъюктивальный доступ и установили держалки на глазодвигательные мышцы. Затем осуществили транспупиллярную диафаноскопию для маркировки границ опухоли. При проведении операции использовали зонд-наконечник, диаметр основания которого со стороны, предназначенной для сопряжения с глазом пациента, составлял 10 мм. Выбранный зонд удерживали за корпус и соединили с лазером с соответствующей стороны. Опухоль облучали с захватом здоровых тканей не менее 1,5 мм от определяемой границы, одной экспозицией (зонд 10 мм) в течение 10 минут. Причем облучение проводили с мощностью лазера 0,66 Вт, плотность мощности с учетом потерь в склере составила 0,4 Вт/см2; плотностью энергии за время экспозиции 10 мин составила 240 Дж/см2. По окончании операции наложили рассасывающийся шов на конъюнктиву (викрил 8:0).
В результате был достигнут регресс опухоли 86%.
Пример 3. Клинический случай.
Пациентка В, женщина, в возрасте 52 г., поступила с диагнозом меланома цилиохориоидальной зоны T1aN0M0 I стадия левого глаза. Локализация преэкваториальная, элевация опухоли 4,2 мм, диаметр основания опухоли 5,3 мм. В режиме ЦДК – гиперваскулярная. Учитывая клинико-инструментальные данные, было принято решение провести лечение с использованием заявляемого способа.
Пациенту вводили фотосенсибилизатор «Фотолон» в расчете 1 мг/кг веса за 3 часа до операции. Пациенту выполнили наркоз общий интубационный. Далее провели конъюктивальный доступ и установили держалки на глазодвигательные мышцы. Затем осуществили транспупиллярную диафаноскопию для маркировки границ опухоли. При проведении операции использовали зонд-наконечник, диаметр основания которого со стороны, предназначенной для сопряжения с глазом пациента, составлял 7 мм. Выбранный зонд удерживали за корпус и соединили с лазером с соответствующей стороны. Опухоль облучали с захватом здоровых тканей не менее 1,5 мм от определяемой границы, одной экспозицией (зонд 7 мм) в течение 12 минут. Причем облучение проводили с мощностью лазера 0,33 Вт, плотность мощности с учетом потерь в склере составила 0,4 Вт/см2; плотность энергии за время экспозиции 12 мин составила 310 Дж/см2. По окончании операции наложили рассасывающийся шов на конъюнктиву (викрил 8:0).
В результате был достигнут регресс опухоли 93%.
Пример 4. Клинический случай.
Пациентка Г, женщина, в возрасте 49 л., поступила с диагнозом меланома цилиарного тела T1aN0M0 I стадия левого глаза. Локализация преэкваториальная, элевация опухоли – 3,9 мм, диаметр основания опухоли 4,6 мм. В режиме ЦДК – гиперваскулярная. Учитывая клинико-инструментальные данные, было принято решение провести лечение с использованием заявляемого способа.
Пациенту вводили фотосенсибилизатор «Фотолон» в расчете 0,9 мг/кг веса за 3 часа до операции. Пациенту выполнили наркоз общий интубационный. Далее провели конъюктивальный доступ и установили держалки на глазодвигательные мышцы. Затем осуществили транспупиллярную диафаноскопию для маркировки границ опухоли. При проведении операции использовали зонд-наконечник, диаметр основания которого со стороны, предназначенной для сопряжения с глазом пациента, составлял 5 мм. Выбранный зонд удерживали за корпус и соединили с лазером с соответствующей стороны. Опухоль облучали с захватом здоровых тканей не менее 1,5 мм от определяемой границы опухоли. Диапазон диаметра пятна лазерного излучения составлял 5 мм. Опухоль облучали последовательно, концентрично по направлению от центра к периферии новообразования, с перекрытием соседних полей на 10-15% площади и с захватом здоровых тканей. Причем облучение проводили с мощностью лазера 0,16 Вт, плотность мощности с учетом потерь в склере составила порядка 0,4 Вт/см2; плотность энергии за время экспозиции 15 мин составила 360 Дж/см2. По окончании операции наложили рассасывающийся шов на конъюнктиву (викрил 8:0).
В результате был достигнут регресс опухоли 89%.
Пример 5. Клинический случай.
Пациентка В, женщина, в возрасте 42 г., поступила с диагнозом Меланома хориоидеи T2aN0M0 IIA стадия правого глаза. Локализация в пределах экватора глаза, элевация опухоли – 6,2 мм, диаметр основания опухоли 4,1 мм. В режиме ЦДК гиперваскулярная. Учитывая клинико-инструментальные данные, было принято решение провести лечение с использованием заявляемого способа.
Пациенту вводили фотосенсибилизатор «Фотолон» в расчете 0,8 мг/кг веса за 3 часа до операции. Пациенту выполнили наркоз общий интубационный. Далее провели конъюктивальный доступ и установили держалки на глазодвигательные мышцы. Затем осуществили транспупиллярную диафаноскопию для маркировки границ опухоли. При проведении операции использовали зонд-наконечник, диаметр основания которого со стороны, предназначенной для сопряжения с глазом пациента, составлял 3 мм. Выбранный зонд удерживали за корпус и соединили с лазером с соответствующей стороны. Опухоль облучали с захватом здоровых тканей не менее 1,5 мм от определяемой границы опухоли. Опухоль облучали последовательно, концентрично по направлению от центра к периферии новообразования, с перекрытием соседних полей на 10-15% площади и с захватом здоровых тканей. Причем облучение проводили с мощностью лазера 0,06 Вт, плотность мощности с учетом потерь в склере составила 0,43 Вт/см2; плотностью энергии 260 Дж/см2, со временем экспозиции 10 мин. По окончании операции наложили рассасывающийся шов на конъюнктиву (викрил 8:0).
В результате был достигнут регресс опухоли 94%.
Пример 6. Клинический случай.
Пациентка В, женщина, в возрасте 60 л., поступила с диагнозом меланома хориоидеи T1aN0M0 I стадия левого глаза. Локализация постэкваториальная, элевация опухоли – 2,2 мм, диаметр основания опухоли 3,2 мм. В режиме ЦДК – гиперваскулярная. Учитывая клинико-инструментальные данные, было принято решение провести лечение с использованием заявляемого способа.
Пациенту вводили фотосенсибилизатор «Фотолон» в расчете 1 мг/кг веса за 3 часа до операции. Пациенту выполнили наркоз общий интубационный. Далее провели конъюнктивальный доступ и установили держалки на глазодвигательные мышцы. Затем осуществили транспупиллярную диафаноскопию для маркировки границ опухоли. При проведении операции использовали зонд-наконечник, диаметр основания которого со стороны, предназначенной для сопряжения с глазом пациента, составлял 2 мм. Выбранный зонд удерживали за корпус и соединили с лазером с соответствующей стороны. Опухоль облучали с захватом здоровых тканей не менее 1,5 мм от определяемой границы опухоли. Опухоль облучали последовательно, концентрично по направлению от центра к периферии новообразования, с перекрытием соседних полей на 10-15% площади и с захватом здоровых тканей. Причем облучение проводили с мощностью лазера 0,03 Вт, плотность мощности с учетом потерь в склере составила 0,45 Вт/см2; плотностью энергии 270 Дж/см2, со временем экспозиции 10 мин. По окончании операции наложили рассасывающийся шов на конъюнктиву (викрил 8:0).
В результате был достигнут регресс опухоли 90%.
Список литературы
1. Способ фотодинамической терапии меланомы хориоидеи: патент RU 2318511, Российская Федерация, заявка RU 2006134584, заявл. 02.10.2006, опубл. 10.03.2008.
2. Способ органосохраняющего лечения внутриглазных опухолей: патент RU 2452444, Российская Федерация, заявка RU 2010141381, заявл. 11.10.2010, опубл. 10.06.2012.
3. Способ органосохраняющего лечения меланомы хориоидеи на основе применения гибридной фотодинамической терапии: патент RU 2785609, Российская Федерация, RU 2021119430, заявл. 02.07.2021, опубл. 09.12.2022.
4. Способ лечения внутриглазных опухолей: патент RU 2290905, Российская Федерация, заявка RU 2005121930, заявл. 12.07.2005, опубл. 10.01.2007.
5. Устройство клеточного эксперимента для исследований фотодинамической терапии: заявка CN 103789207, Китайская Народная Республика, заявка CN 201410055651, заявл. 19.02.2014, опубл. 14.05.2014.
6. Система фотодинамической терапии заболеваний слизистой оболочки полости рта: заявка CN 116920282A, Китайская Народная Республика, заявл. 06.07.2023, опубл. 24.10.2023.
7. Аппарат и способ переключаемой фотодинамической терапии: заявка US 2004267335, Соединенные Штаты Америки, заявл. 23.04.2004, опубл. 30.12.2004.
8. Аппарат фотодинамической обработки для локализованного нацеливания при лечении рака и способ борьбы с ним: патент KR 102447033, Республика Корея, заявка KR 20200076410, заявл.·23.06.2020, опубл. 26.09.2022.
9. Устройство фотодинамической терапии локального нацеливания для лечения рака и способ борьбы с ним: заявка CN 114173893A, Китайская Народная Республика, заявка CN 202080003911, заявл. 30.06.2020, опубл. 11.03.2022.
10. Системы усиления оптической передачи через биологические ткани: заявка US 2017065345, Соединенные Штаты Америки, заявл. 18.11.2016, опубл. 09.03.2017.
11. Лазерный аппарат и способ передачи лазерного излучения: международная заявка WO 9515508A1, заявл. 30.11.1994, опубл. 08.06.1995.
12. Транссклеральный оптический зонд: патент RU 16248, Российская Федерация, заявка RU 2000116730, заявл. 26.06.2000, опубл. 20.12.2000.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ КОНТАКТНОГО ТРАНССКЛЕРАЛЬНОГО ОБЛУЧЕНИЯ ГЛАЗА И СПОСОБ ЕГО ПРИМЕНЕНИЯ ПРИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ | 2008 |
|
RU2358698C1 |
| Способ транссклеральной лазерной термотерапии внутриглазных опухолей | 2021 |
|
RU2761292C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ | 2004 |
|
RU2271790C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2290905C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ЛИЗИСА И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ МЕЛАНОМЫ ХОРИОИДЕИ | 2011 |
|
RU2463027C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2294780C1 |
| Способ органосохраняющего лечения меланомы хориоидеи на основе применения гибридной фотодинамической терапии | 2021 |
|
RU2785609C1 |
| СПОСОБ ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2010 |
|
RU2452444C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ДЕСТРУКЦИИ И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ МЕЛАНОМЫ ХОРИОИДЕИ | 2007 |
|
RU2336059C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2295944C1 |

Группа изобретений относится к медицине, а именно к офтальмологии. Лечение увеальной меланомы осуществляют посредством транссклеральной фотодинамической терапии, в ходе которого пациенту внутривенно капельно за 3 часа до операции вводят фотосенсибилизатор хлоринового ряда, после чего в условиях кратковременного общего наркоза осуществляют лазерное транссклеральное облучение опухоли с помощью лазерной установки с длиной волны 662 нм. При этом перед проводимым лечением, согласно полученным клинико-инструментальным данным по локализации и диаметру основания опухоли, на лазерный световод устанавливают транссклеральный зонд-наконечник соответствующего диаметра, причем при преэкваториальной локализации опухоли и диаметре основания используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в соответствующем диапазоне, а облучение проводят с соответствующей мощностью лазера и соответствующим временем экспозиции. В частном случае при преэкваториальной локализации опухоли и соответствующем диаметре основания используют транссклеральный зонд-наконечник с соответствующим диаметром со стороны, предназначенной для сопряжения с глазом, а облучение проводят с соответствующей мощностью лазера и соответствующим временем экспозиции. В частном случае в качестве фотосенсибилизатора используют «Фоторан» или «Фотолон». При этом лечение увеальной меланомы осуществляют посредством набора транссклеральных зондов-наконечников, который включает шесть зондов, в котором сторона, предназначенная для сопряжения с глазом пациента, выполнена круглой формы, причем с этой стороны у зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в соответствующем диапазоне. В частном случае внутренняя поверхность зондов-наконечников выполнена ступенчатой, а каждый зонд-наконечник оснащен элементом, позволяющим его идентифицировать при подключении к лазеру. В качестве элемента, позволяющего идентифицировать зонд-наконечник при подключении к лазеру, использована радиочастотная метка. В частном случае каждый зонд-наконечник со стороны, предназначенной для сопряжения с глазом пациента, оснащен стеклом. Группа изобретений позволяет эффективно и избирательно органосохранно проводить лечение пациентов с увеальной меланомой с помощью транссклеральной фотодинамической терапии и снизить риск послеоперационных осложнений. 2 н. и 8 з.п. ф-лы, 7 ил., 6 пр.
1. Способ лечения увеальной меланомы на основе применения транссклеральной фотодинамической терапии, в ходе которого пациенту внутривенно капельно за 3 часа до операции вводят фотосенсибилизатор хлоринового ряда, после чего в условиях кратковременного общего наркоза осуществляют лазерное транссклеральное облучение опухоли с помощью лазерной установки с длиной волны 662 нм, отличающийся тем, что перед проводимым лечением согласно полученным клинико-инструментальным данным по локализации и диаметру основания опухоли на лазерный световод устанавливают транссклеральный зонд-наконечник соответствующего диаметра, причем
при преэкваториальной локализации опухоли и диаметре основания от 10,1 до 15,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 12,5-17,5 мм, а облучение проводят с мощностью лазера 0,9-1,6 Вт и временем экспозиции 10-15 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 7,1 до 10,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 9,0-12,4 мм, а облучение проводят с мощностью лазера 0,51-0,9 Вт и временем экспозиции 10-15 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 5,1 до 7,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 6,5-8,9, а облучение проводят с мощностью лазера 0,26-0,4 Вт и временем экспозиции 10-15 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 4,0-6,4, а облучение проводят с мощностью лазера 0,1-0,25 Вт и временем экспозиции 10-15 мин;
при локализации опухоли в пределах экватора глазного яблока и при диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 2,5-3,9, а облучение проводят с мощностью лазера 0,04-0,1 Вт и временем экспозиции 10-15 мин;
при постэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник, диаметр которого со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 1,5-2,4, а облучение проводят с мощностью лазера 0,02-0,04 Вт и временем экспозиции 10-15 мин.
2. Способ по п.1, отличающийся тем, что
при преэкваториальной локализации опухоли и диаметре основания от 10,1 до 15,0 мм используют транссклеральный зонд-наконечник с диаметром 15±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 1,5 Вт и временем экспозиции 10 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 7,1 до 10,0 мм используют транссклеральный зонд-наконечник с диаметром 10±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,66 Вт и временем экспозиции 10 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 5,1 до 7,0 мм используют транссклеральный зонд-наконечник с диаметром 7±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,33 Вт и временем экспозиции 10 мин;
при преэкваториальной локализации опухоли и диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник с диаметром 5±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,16 Вт и временем экспозиции 15 мин;
при локализации опухоли в пределах экватора глазного яблока и при диаметре основания опухоли от 3,0 до 5,0 мм используют транссклеральный зонд-наконечник с диаметром 3±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,06 Вт и временем экспозиции 10 мин;
при постэкваториальной локализации опухоли и диаметре основания опухоли от 3,0до 5,0 мм используют транссклеральный зонд-наконечник с диаметром 2±0,2 мм со стороны, предназначенной для сопряжения с глазом, а облучение проводят с мощностью лазера 0,03 Вт и временем экспозиции 10 мин.
3. Способ по п.1, отличающийся тем, что в качестве фотосенсибилизатора используют «Фоторан».
4. Способ по п.1, отличающийся тем, что в качестве фотосенсибилизатора используют «Фотолон».
5. Набор транссклеральных зондов-наконечников, включающий шесть зондов, характеризующихся тем, что сторона, предназначенная для сопряжения с глазом пациента, выполнена круглой формы, причем с этой стороны
у первого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 12,5-17,5 мм;
у второго зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 9,0-12,4 мм;
у третьего зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 6,5-8,9 мм;
у четвертого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 4,0-6,4 мм;
у пятого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 2,5-3,9 мм;
у шестого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, находится в диапазоне 1,5-2,4 мм.
6. Набор по п.5, отличающийся тем, что со стороны, предназначенной для сопряжения с глазом пациента,
у первого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, составляет 15±0,2 мм;
у второго зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, составляет 10±0,2 мм;
у третьего зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, составляет 7±0,2 мм;
у четвертого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, составляет 5±0,2 мм;
у пятого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, составляет 3±0,2 мм;
у шестого зонда-наконечника диаметр со стороны, предназначенной для сопряжения с глазом, составляет 2±0,2 мм.
7. Набор по п.5, отличающийся тем, что внутренняя поверхность зондов-наконечников выполнена ступенчатой.
8. Набор по п.5, отличающийся тем, что каждый зонд-наконечник оснащен элементом, позволяющим его идентифицировать при подключении к лазеру.
9. Набор по п.8, отличающийся тем, что в качестве элемента, позволяющего идентифицировать зонд-наконечник при подключении к лазеру, использована радиочастотная метка.
10. Набор по п.5, отличающийся тем, что каждый зонд-наконечник со стороны, предназначенной для сопряжения с глазом пациента, оснащен стеклом.
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2290905C1 |
| Способ органосохраняющего лечения меланомы хориоидеи на основе применения гибридной фотодинамической терапии | 2021 |
|
RU2785609C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ЛИЗИСА И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ МЕЛАНОМЫ ХОРИОИДЕИ | 2011 |
|
RU2463026C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ | 2004 |
|
RU2271790C1 |
| Самкович Е.В | |||
| и др | |||
| Фотодинамическая терапия в комбинированном лечении меланомы хориоидеи | |||
| Вопросы онкологии | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| Способ приготовления пищевого продукта сливкообразной консистенции | 1917 |
|
SU69A1 |
| Способ получения целлюлозы из стеблей хлопчатника | 1912 |
|
SU505A1 |
| Yordi S | |||
| et al | |||
| Photodynamic therapy for choroidal melanoma: What is the response rate? Surv | |||
Авторы
Даты
2025-03-05—Публикация
2024-06-12—Подача