Область техники
[0001]
Настоящее изобретение относится к соединениям, применимым для лечения и/или профилактики инфекции, вызванной респираторно-синцитиальным вирусом (далее именуемым «RSV»), и связанных с ней заболеваний, вызванных инфекцией, а также к содержащим их фармацевтическим композициям. В частности, настоящее изобретение относится к производным амида, обладающим ингибирующей активностью в отношении RSV.
Уровень техники
[0002]
Респираторно-синцитиальный вирус (RSV) человека представляет собой отрицательно-полярный одноцепочечный РНК вирус, который принадлежит к роду Pneumovirus семейства Paramyxoviridae и является наиболее частой причиной бронхиолита и пневмонии у детей в возрасте до 1 года. Большинство детей заражаются RSV до двухлетнего возраста, и примерно 1-3% инфицированных нуждаются в госпитализации. Пожилые люди и взрослые с заболеваниями сердца, легких или иммунной системы особенно восприимчивы и подвержены высокому риску тяжелых заболеваний и осложнений (не-патентный документ 1).
[0003]
Существует два антигенных подтипа RSV: А и В. Эти два типа циркулируют одновременно во время вспышек RSV. Однако соотношение этих типов различается географически и сезонно, и это рассматривается как одна из причин разного клинического воздействия в каждой вспышке. Следовательно, с точки зрения лечения RSV, желательны агенты, эффективные против обоих подтипов А и В (не-патентный документ 1).
[0004]
На сегодняшний день не существует вакцины, которая могла бы предотвратить заражение RSV. Паливизумаб представляет собой моноклональное антитело, используемое в профилактических целях для предотвращения инфекции RSV у детей из группы высокого риска, например, у недоношенных детей и детей с заболеваниями сердца или легких. Высокая стоимость лечения паливизумабом ограничивает применение этого препарата. Аналог нуклеиновой кислоты, рибавирин, был одобрен в Соединенных Штатах в качестве единственного противовирусного средства для лечения RSV инфекции, но его эффективность ограничена и есть опасения по поводу профиля побочных эффектов. Следовательно, существует потребность в безопасном и эффективном лечении RSV, которое можно было бы широко использовать для всех типов RSV и возрастных групп от младенцев до пожилых людей (не-патентный документ 1).
[0005]
Ингибиторы, таргетирующие белок F, участвующий в слиянии мембран RSV, такие как Зиресовир, JNJ-53718678 и RV-521, ингибиторы, таргетирующие белок N, участвующий в стабилизации генома, такие как EDP-938, и ингибиторы, таргетирующие полимеразу белка L, такие как PC786, находятся в стадии клинической разработки для терапии RSV (не-патентный документ 2).
На сегодняшний день неизвестно ни одно производное амида, обладающее ингибирующей активностью в отношении RSV, такое как описано в настоящей заявке.
Документ известного уровня техники
Не-патентный документ
[0006]
Не-патентный документ 1: Cellular and Molecular Life Sciences, 2020, Jun 16, 1-14
Не-патентный документ 2: Expert Opinion on Investigational Drugs, 2020, Mar 29, 3, 285-294
Сущность изобретения
Проблема, решаемая изобретением
[0007]
Целью настоящего изобретения является предложение новых соединений, обладающих ингибирующей активностью в отношении RSV. Более предпочтительно, настоящее изобретение предлагает соединения, полезные для лечения и/или профилактики инфекции RSV и родственных заболеваний, вызванных инфекцией, и содержащие их лекарственные средства.
Средства для решения проблемы
[0008]
Настоящее изобретение относится к следующим пунктам (1) - (17).
(1) Соединение формулы (I):
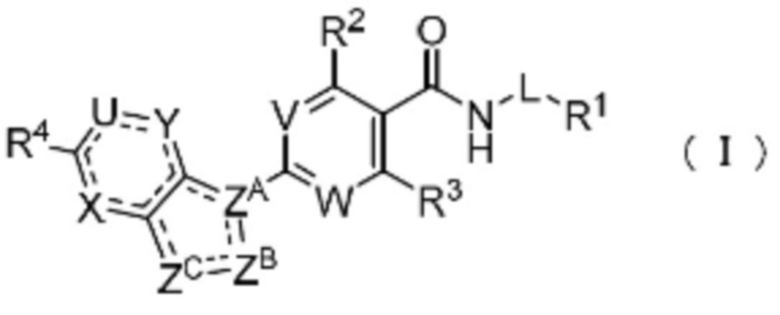
где:
пунктирная линия показывает присутствие или отсутствие связи;
R1 представляет собой карбокси, циано, замещенный или незамещенный ароматический гетероциклил, -C(=O)-NR1BR1C или -CH=CHC(=O)-OH;
R1B и R1C каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный аминосульфонил или замещенный или незамещенный не ароматический гетероциклилсульфонил;
L представляет собой замещенный или незамещенный не ароматический карбоциклилдиил, замещенный или незамещенный не ароматический гетероциклилдиил или замещенный или незамещенный алкилен;
R2 представляет собой замещенный или незамещенный алкил;
R3 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкилокси, замещенный или незамещенный амино или замещенный или незамещенный карбамоил;
X представляет собой =CRX- или =N-;
Y представляет собой =CRY- или =N-;
U представляет собой -CRU= или -N=;
V представляет собой -CRV= или -N=;
W представляет собой =CRW- или =N-;
ZA представляет собой -C= или -N-;
ZB представляет собой -CR5R6-, -CR5=, -NR5- или -N=;
ZC представляет собой -CR7R8-, -CR7=, -NR7- или =N-;
RX, RY, RV и RW каждый независимо представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил;
RU представляет собой атом водорода, замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил или замещенный или незамещенный не ароматический карбоциклил;
R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил, или R5 и R6 взяты вместе с образованием оксо;
R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, замещенный или незамещенный алкилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца; или
R5 и R7 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного ароматического углеродного кольца; или
R4 представляет собой атом водорода, замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный ароматический карбоциклилокси, замещенный или незамещенный ароматический гетероциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, замещенный или незамещенный карбамоил, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклил или замещенный или незамещенный не ароматический гетероциклилкарбонил, или R4 и RU взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического гетероциклического кольца,
или его фармацевтически приемлемая соль.
(2) Соединение по пункту (1), где R1 представляет собой карбокси,
или его фармацевтически приемлемая соль.
(3) Соединение по пункту (1) или (2), где L представляет собой замещенный или незамещенный не ароматический карбоциклилдиил,
или его фармацевтически приемлемая соль.
(4) Соединение по любому из пунктов (1) - (3), где R3 представляет собой атом водорода,
или его фармацевтически приемлемая соль.
(5) Соединение по любому из пунктов (1) - (4), где V представляет собой -N= и W представляет собой =N-,
или его фармацевтически приемлемая соль.
(6) Соединение по любому из пунктов (1) - (5), где группа формулы:
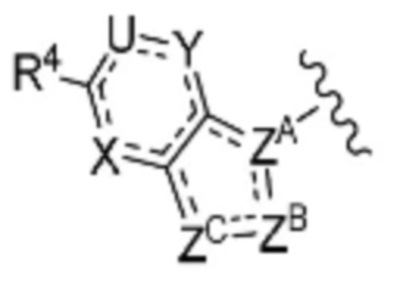
представляет собой
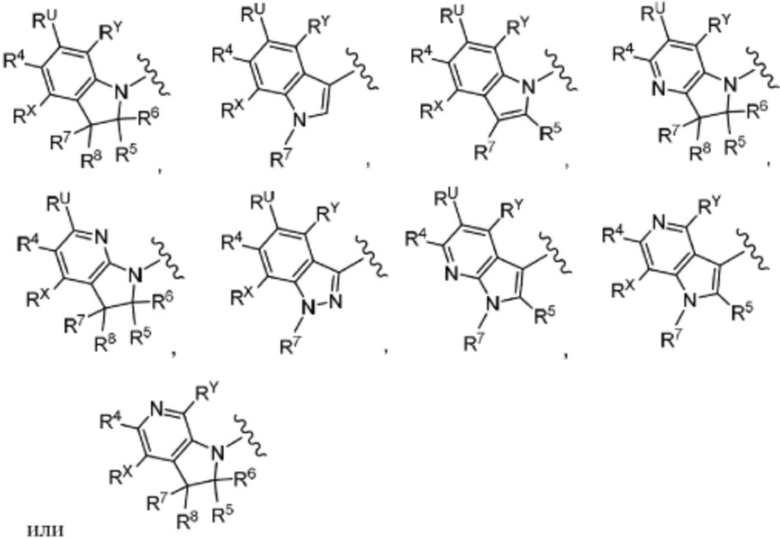
где каждый символ такой, как определен в пункте (1),
или его фармацевтически приемлемая соль.
(7) Соединение по любому из пунктов (1) - (6), где группа формулы:

представляет собой
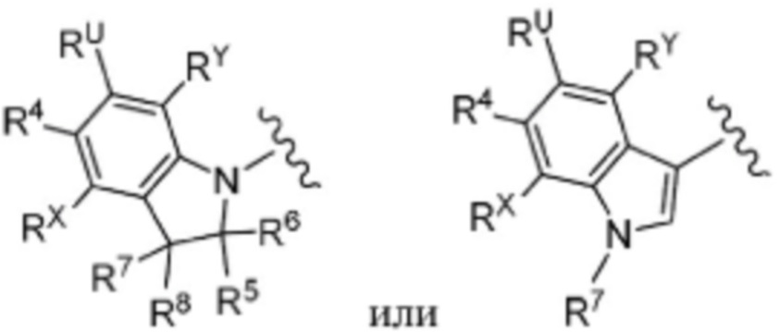
где каждый символ такой, как определен в пункте (1),
или его фармацевтически приемлемая соль.
(8) Соединение по любому из пунктов (1) - (7), где группа формулы:

представляет собой
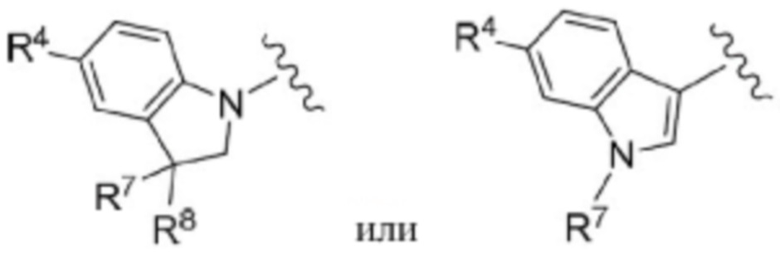
где каждый символ такой, как определен в пункте (1),
или его фармацевтически приемлемая соль.
(9) Соединение по любому из пунктов (1) - (8), где группа формулы:

представляет собой
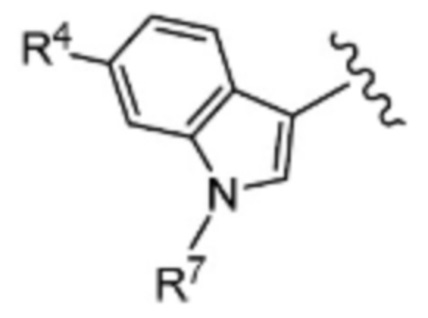
где
R4 такой, как определен в пункте (1); и
R7 представляет собой замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил или замещенный или незамещенный не ароматический карбоциклилсульфонил,
или его фармацевтически приемлемая соль.
(10) Соединение по любому из пунктов (1) - (8), где группа формулы:

представляет собой
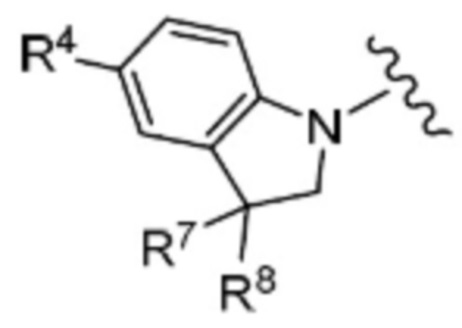
где
R4 такой, как определен в пункте (1); и
R7 и R8 каждый независимо представляет собой атом водорода или замещенный или незамещенный алкил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца,
или его фармацевтически приемлемая соль.
(11) Соединение по любому из пунктов (1) - (10), где R4 представляет собой замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный ароматический карбоциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил или замещенный или незамещенный не ароматический карбоциклил,
или его фармацевтически приемлемая соль.
(12) Соединение по любому из пунктов (1) - (11), где R4 представляет собой замещенный или незамещенный не ароматический гетероциклилокси или замещенный или незамещенный не ароматический карбоциклилокси,
или его фармацевтически приемлемая соль.
(13) Соединение по пункту (1), выбранное из группы, состоящей из соединений I-082, I-162, I-481, I-496, I-503, I-506, I-549, I-552, I-568, I-569, I-570, I-571, I-591, I-613, I-617 и I-618,
или его фармацевтически приемлемая соль.
(14) Фармацевтическая композиция, содержащая соединение по любому из пунктов (1) - (13) или его фармацевтически приемлемая соль.
(15) Фармацевтическая композиция по пункту (14), обладающая активностью против вируса RS.
(16) Способ лечения и/или профилактики инфекции RSV, отличающийся тем, что вводят соединение по любому из пунктов (1) - (13) или его фармацевтически приемлемую соль.
(17) Соединение по любому из пунктов (1) - (13) или его фармацевтически приемлемая соль для лечения и/или профилактики инфекции RSV.
(18) Применение соединения по любому из пунктов (1) - (13), или его фармацевтически приемлемая соль для производства лекарственного средства для лечения и/или профилактики инфекции RSV.
Эффект изобретения
[0009]
Соединения по настоящему изобретению обладают ингибирующей активностью в отношении RSV и могут быть использованы в качестве терапевтических и/или профилактических агентов против инфекции RSV и родственных заболеваний, вызванных инфекцией.
Способ осуществления изобретения
[0010]
Далее будет описано значение каждого термина, используемого в настоящей спецификации. Если специально не указано иное, каждый термин используется в одном и том же смысле, либо отдельно, либо в комбинации с другими терминами.
Термин «состоит из» означает наличие только составляющих элементов.
Термин «содержать» означает, что элементы не ограничиваются составляющими элементами, и элементы, которые не описаны, не исключаются.
Далее настоящее изобретение будет описано с указанием типовых вариантов осуществления. По всему настоящему описанию, следует понимать, что, если специально не указано иное, выражение в единственном числе также включает в себя понятие его множественного числа. Следовательно, следует понимать, что, если специально не указано иное, артикль для формы единственного числа (например, в случае английского языка «a», «an», «the» и т.п.) также включает в себя понятие его формы множественного числа.
Кроме того, следует понимать, что, если специально не указано иное, термины, используемые в настоящем описании, используются в значениях, обычно используемых в вышеописанном уровне техники. Соответственно, если не указано иное, все термины и научные и технические термины, используемые в настоящем описании, имеют те же значения, которые обычно понимаются специалистами в области техники, к которой относится настоящее изобретение. В случае противоречия, приоритет отдается настоящей спецификации (включая определения).
[0011]
«Галоген» включает атом фтора, атом хлора, атом брома и атом йода. В частности, предпочтительными являются атом фтора и атом хлора.
[0012]
«Алкил» включает линейные или разветвленные углеводородные группы, каждая из которых содержит от 1 до 15 атомов углерода, предпочтительно, от 1 до 10 атомов углерода, более предпочтительно, от 1 до 6 атомов углерода, и еще более предпочтительно, от 1 до 4 атомов углерода. Примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, изогексил, н-гептил, изогептил, н-октил, изооктил, н-нонил и н-децил.
Предпочтительные варианты «алкила» включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил и н-пентил. Более предпочтительные варианты включают метил, этил, н-пропил, изопропил и трет-бутил.
[0013]
«Алкенил» включает линейные или разветвленные углеводородные группы, каждая из которых имеет одну или несколько двойных связей в любом положении и имеет от 2 до 15 атомов углерода, предпочтительно, от 2 до 10 атомов углерода, более предпочтительно, от 2 до 6 атомов углерода, и еще более предпочтительно, 2 до 4 атомов углерода. Примеры включают винил, аллил, пропенил, изопропенил, бутенил, изобутенил, пренил, бутадиенил, пентенил, изопентенил, пентадиенил, гексенил, изогексенил, гексадиенил, гептенил, октенил, ноненил, деценил, ундеценил, додеценил, тридеценил, тетрадеценил и пентадеценил.
Предпочтительные варианты «алкенила» включают винил, аллил, пропенил, изопропенил и бутенил. Более предпочтительные варианты включают этенил и н-пропенил.
[0014]
«Алкинил» включает линейные или разветвленные углеводородные группы, каждая из которых имеет одну или несколько тройных связей в любом положении и имеет от 2 до 10 атомов углерода, предпочтительно, от 2 до 8 атомов углерода, более предпочтительно, от 2 до 6 атомов углерода, и еще более предпочтительно, 2 до 4 атомов углерода. Алкинил может дополнительно иметь двойную связь в любом положении. Примеры включают этинил, пропинил, бутинил, пентинил, гексинил, гептинил, октинил, нонинил и децинил.
Предпочтительные варианты «алкинила» включают этинил, пропинил, бутинил и пентинил. Более предпочтительные варианты включают этинил и пропинил.
[0015]
«Алкилен» включает линейные или разветвленные двухвалентные углеводородные группы, каждая из которых содержит от 1 до 15 атомов углерода, предпочтительно, от 1 до 10 атомов углерода, более предпочтительно, от 1 до 6 атомов углерода, и еще более предпочтительно, от 1 до 4 атомов углерода. Примеры включают метилен, этилен, триметилен, пропилен, тетраметилен, пентаметилен и гексаметилен.
[0016]
«Ароматический карбоциклил» означает циклическую ароматическую углеводородную группу, имеющую одно кольцо или два или несколько колец. Примеры включают фенил, нафтил, антрил и фенантрил.
Предпочтительные варианты осуществления «ароматического карбоциклила» включают фенил.
[0017]
«Ароматическое углеродное кольцо» означает кольцо, полученное из вышеуказанного «ароматического карбоциклила».
[0018]
«R5 и R7 вместе с атомами углерода, к которым они присоединены, образуют замещенное или незамещенное ароматическое углеродное кольцо» включает, например, следующие кольца.
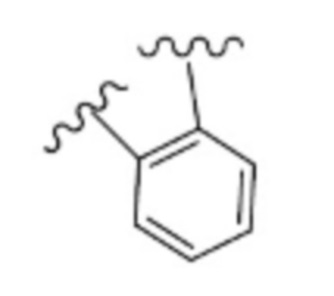
[0019]
«Не ароматический карбоциклил» означает циклическую насыщенную углеводородную группу или циклическую не ароматическую ненасыщенную углеводородную группу, обе из которых имеют одно кольцо или два или несколько колец. «Не ароматический карбоциклил», имеющий два или несколько колец, также включает не ароматический карбоциклил, имеющий одно кольцо или два или несколько колец, с которыми слито кольцо в указанном выше «ароматическом карбоциклиле».
Кроме того, «не ароматический карбоциклил» также включает группу с мостиковой связью или группу, образующую спирокольцо, как указано ниже.
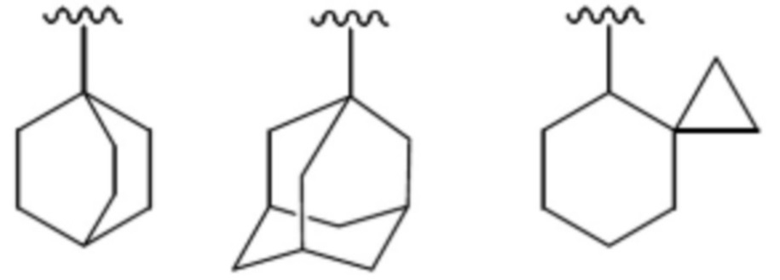
Не ароматический карбоциклил, имеющий одно кольцо, предпочтительно, имеет от 3 до 16 атомов углерода, более предпочтительно, от 3 до 12 атомов углерода, и еще более предпочтительно, от 4 до 8 атомов углерода. Примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклодецил, циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил и циклогексадиенил.
Не ароматический карбоциклил, имеющий два или несколько колец, предпочтительно имеет от 8 до 20 атомов углерода, и более предпочтительно, от 8 до 16 атомов углерода. Примеры включают инданил, инденил, аценафтил, тетрагидронафтил и флуоренил.
[0020]
«Не ароматическое углеродное кольцо» означает кольцо, полученное из вышеуказанного «не ароматического карбоциклила».
[0021]
Примеры «R5 и R7 вместе с атомами углерода, к которым они присоединены, образуют замещенное или незамещенное не ароматическое углеродное кольцо» включают следующие кольца.
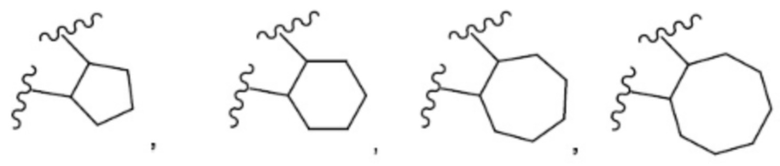 .
.
[0022]
Примеры «R7 и R8 вместе с атомом углерода, к которому они присоединены, образуют замещенное или незамещенное не ароматическое углеродное кольцо» включают следующие кольца.
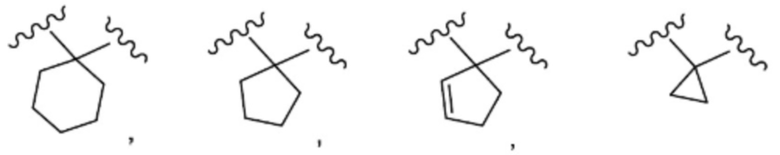 .
.
[0023]
«Не ароматический карбоциклилдиил» означает двухвалентную группу, полученную из вышеуказанного «не ароматического углеродного кольца». Примеры включают циклопропандиил, циклобутандиил, циклопентандиил, циклогександиил, циклогептандиил, циклооктандиил, бицикло[2,2,2]октандиил, бицикло[2,2,1]гептандиил, адамантандиил. Один атом углерода может иметь две связывающие руки. Примеры включают циклогексан-1,1-диил и адамантан-2,2-диил.
[0024]
«Ароматический гетероциклил» означает ароматическую циклическую группу, имеющую одно кольцо или два или несколько колец, которая имеет один или несколько одинаковых или разных гетероатомов, необязательно выбранных из O, S и N в кольце(ах).
Ароматический гетероциклил, имеющий два или несколько колец, также включает ароматический гетероциклил, имеющий одно кольцо или два или несколько колец, с которым конденсировано кольцо в указанном выше «ароматическом карбоциклиле», и связывающая сторона может переноситься любым из колец.
Ароматический гетероциклил, имеющий одно кольцо, предпочтительно, представляет собой 5-8-членное кольцо, и более предпочтительно, 5- или 6-членное кольцо. Примеры 5-членного ароматического гетероциклила включают пирролил, имидазолил, пиразолил, триазолил, тетразолил, фурил, тиенил, изоксазолил, оксазолил, оксадиазолил, изотиазолил, тиазолил и тиадиазолил. Примеры 6-членного ароматического гетероциклила включают пиридилпиридазинил, пиримидинил, пиразинил и триазинил.
Ароматический гетероциклил, имеющий два кольца, предпочтительно представляет собой 8-10-членное кольцо, и более предпочтительно, 9- или 10-членное кольцо. Примеры включают индолил, изоиндолил, индазолил, индолизинил, хинолинил, изохинолинил, цинолинил, фталазинил, хиназолинил, нафтиридинил, хиноксалинил, пуринил, птеридинил, бензимидазолил, бензизоксазолил, бензоксазолил, бензоксадиазолил, бензизотиазолил, бензотиазолил, бензотиадиазолил, бензофурил, изобензофурил, бензотиенил, бензотриазолил, имидазопиридил, триазолопиридил, имидазотиазолил, пиразинопиридазинил, оксазолопиридил и тиазолопиридил.
Ароматический гетероциклил, имеющий три или несколько колец, предпочтительно представляет собой 13-15-членное кольцо. Примеры включают карбазолил, акридинил, ксантенил, фенотиазинил, феноксатиинил, феноксазинил и дибензофурил.
[0025]
«Ароматическое гетероциклическое кольцо» означает кольцо, полученное из вышеуказанного «ароматического гетероциклила».
[0026]
«Не ароматический гетероциклил» означает не ароматическую циклическую группу, имеющую одно кольцо или два или несколько колец, которая имеет один или несколько одинаковых или разных гетероатомов, необязательно выбранных из О, S и N в кольце(ах). Не ароматический гетероциклил, имеющий два или несколько колец, также включает не ароматический гетероциклил, имеющий одно кольцо или два или несколько колец, к которому относится кольцо в каждом из вышеуказанных «ароматического карбоциклила», «не ароматического карбоциклила» и/или «ароматического гетероциклила» конденсируется, а также не ароматический карбоциклил, имеющий одно кольцо или два или несколько колец, с которым конденсировано кольцо в указанном выше «ароматическом гетероциклиле», и связывающую руку может нести любое из колец.
Кроме того, «не ароматический гетероциклил» также включает мостиковую группу или группу, образующую спирокольцо, как указано ниже.
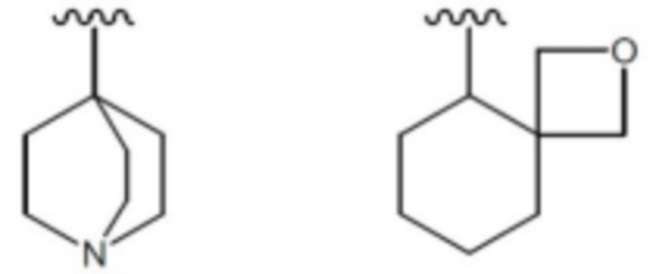 .
.
Не ароматический гетероциклил, имеющий одно кольцо, предпочтительно представляет собой 3-8-членное кольцо, и более предпочтительно, 5- или 6-членное кольцо.
Примеры 3-членного не ароматического гетероциклила включают тииранил, оксиранил и азиридинил. Примеры 4-членного не ароматического гетероциклила включают оксетанил и азетидинил. Примеры 5-членного не ароматического гетероциклила включают оксатиоланил, тиазолидинил, пирролидинил, пирролинил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, тетрагидрофурил, дигидротиазолил, тетрагидроизотиазолил, диоксоланил, диоксолил и тиоланил. Примеры 6-членного не ароматического гетероциклила включают диоксанил, тианил, пиперидил, пиперазинил, морфолинил, морфолино, тиоморфолинил, тиоморфолино, дигидропиридил, тетрагидропиридил, тетрагидропиранил, дигидроксазинил, тетрагидропиридазинил, гексагидропиримидинил, диоксазинил, тиинил и тиазинил. Примеры 7-членного не ароматического гетероциклила включают гексагидроазепинил, тетрагидродиазепинил и оксепанил.
Не ароматический гетероциклил, имеющий два или несколько колец, предпочтительно представляет собой 8-20-членное кольцо, и более предпочтительно, 8-10-членное кольцо. Примеры включают индолинил, изоиндолинил, хроманил и изохроманил.
[0027]
«Не ароматическое гетероциклическое кольцо» означает кольцо, полученное из вышеуказанного «не ароматического гетероциклила».
[0028]
Примеры «R7 и R8 вместе с атомом углерода, к которому они присоединены, образуют замещенное или незамещенное не ароматическое гетероциклическое кольцо» включают следующие кольца.
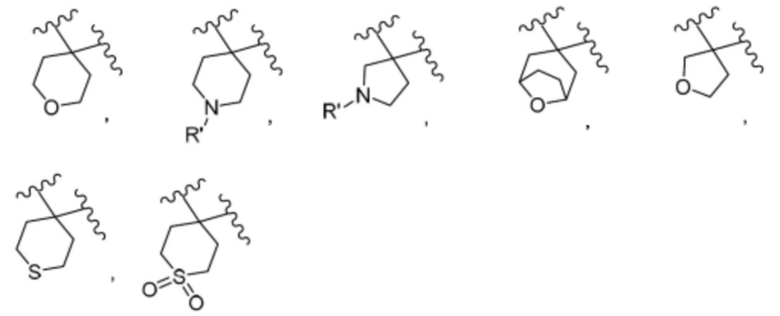
где
R' представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкилоксикарбонил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный неароматический карбоциклил, замещенный или незамещенный карбамоил, замещенный или незамещенный неароматический гетероциклил или замещенный или незамещенный алкилкарбонил.
[0029]
Примеры «R4 и RU вместе с атомом углерода, к которому они присоединены, образуют замещенное не ароматическое гетероциклическое кольцо» включают следующие кольца.
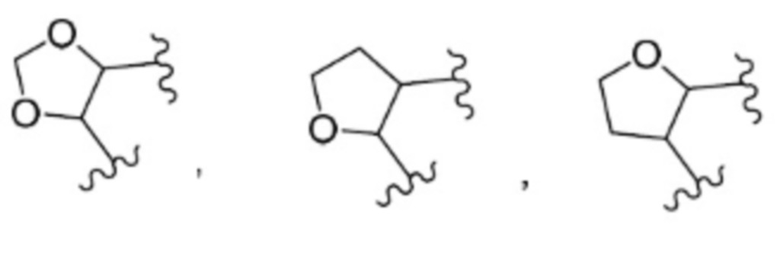
[0030]
«Не ароматический гетероциклилдиил» означает двухвалентную группу, полученную из вышеуказанного «не ароматического гетероциклического кольца». «Не ароматический гетероциклилдиил» включает не ароматический кольцевой диил, содержащий от 1 до 9 атомов углерода, содержащий от 1 до 4 атомов азота, кислорода и/или серы. Примеры включают пирролиндиил, пирролидиндиил, имидазолиндиил, имидазолидиндиил, пиразолиндиил, пиразолидиндиил, пиперидиндиил, пиперазиндиил, морфолиндиил, тетрагидропирандиил. Один атом углерода может иметь две связывающие руки. Примеры включают тетрагидропиран-4,4-диил и пиперидин-4,4-диил.
[0031]
«Триалкилсилил» означает группу, имеющую три из указанных выше «алкилов», связанных с атомом кремния. Три алкильные группы могут быть одинаковыми или разными. Примеры включают триметилсилил, триэтилсилил и трет-бутилдиметилсилил.
[0032]
В настоящей спецификации, фраза «может быть замещен группой заместителей α» означает, что «может быть замещен одной или несколькими группами, выбранными из группы заместителей α». То же самое применяется для групп заместителей β, γ и γ'.
[0033]
Примеры заместителей для «замещенного алкила», «замещенного алкенила», «замещенного алкинила», «замещенного алкилокси», «замещенного алкенилокси», «замещенного алкинилокси», «замещенного алкилкарбонилокси», «замещенного алкенилкарбонилокси», «замещенного алкинилкарбонилокси», «замещенного алкилкарбонила», «замещенного алкенилкарбонила», «замещенного алкинилкарбонила», «замещенного алкилоксикарбонила», «замещенного алкенилоксикарбонила», «замещенного алкинилоксикарбонила», «замещенного алкилсульфанила», «замещенного алкенилсульфанила», «замещенного алкинилсульфанила», «замещенного алкилсульфинила», «замещенного алкенилсульфинила», «замещенного алкинилсульфинила», «замещенного алкилсульфонила», «замещенного алкенилсульфонила» и «замещенного алкинилсульфонила» включают следующую группу заместителей A. Одна или несколько групп, выбранных из следующей группы заместителей A, могут быть присоединены к атому углерода в любом положении.
Группа заместителей A: галоген, гидрокси, карбокси, формил, формилокси, сульфанил, сульфино, сульфо, тиоформил, тиокарбокси, дитиокарбокси, тиокарбамоил, циано, нитро, нитрозо, азидо, гидразино, уреидо, амидино, гуанидино, пентафтортио, триалкилсилил, алкилокси, который может быть замещен группой заместителей α, алкенилокси, который может быть замещен группой заместителей α, алкинилокси, который может быть замещен группой заместителей α, алкилкарбонилокси, который может быть замещен группой заместителей α, алкенилкарбонилокси, который может быть замещен группой заместителей α, алкинилкарбонилокси, который может быть замещен группой заместителей α, алкилкарбонил, который может быть замещен группой заместителей α, алкенилкарбонил, который может быть замещен группой заместителей α, алкинилкарбонил, который может быть замещен группой заместителей α, алкилоксикарбонил, который может быть замещен группой заместителей α, алкенилоксикарбонил, который может быть замещен группой заместителей α, алкинилоксикарбонил, который может быть замещен группой заместителей α, алкилсульфанил, который может быть замещен группой заместителей α, алкенилсульфанил, который может быть замещен группой заместителей α, алкинилсульфанил, который может быть замещен группой заместителей α, алкилсульфинил, который может быть замещен группой заместителей α, алкенилсульфинил, который может быть замещен группой заместителей α, алкинилсульфинил, который может быть замещен группой заместителей α, алкилсульфонил, который может быть замещен группой заместителей α, алкенилсульфонил, который может быть замещен группой заместителей α, алкинилсульфонил, который может быть замещен группой заместителей α,
амино, который может быть замещен группой заместителей β, имино, который может быть замещен группой заместителей β, карбамоил, который может быть замещен группой заместителей β, сульфамоил, который может быть замещен группой заместителей β,
ароматический карбоциклил, который может быть замещен группой заместителей γ, не ароматический карбоциклил, который может быть замещен группой заместителей γ', ароматический гетероциклил, который может быть замещен группой заместителей γ, не ароматический гетероциклил, который может быть замещен группой заместителей γ', ароматический карбоциклилокси, который может быть замещен группой заместителей γ, не ароматический карбоциклилокси, который может быть замещен группой заместителей γ', ароматический гетероциклилокси, который может быть замещен группой заместителей γ, не ароматический гетероциклилокси, который может быть замещен группой заместителей γ', ароматический карбоциклилкарбонилокси, который может быть замещен группой заместителей γ, не ароматический карбоциклилкарбонилокси, который может быть замещен группой заместителей γ', ароматический гетероциклилкарбонилокси, который может быть замещен группой заместителей γ, не ароматический гетероциклилкарбонилокси, который может быть замещен группой заместителей γ', ароматический карбоциклилкарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилкарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилкарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилкарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилоксикарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилоксикарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилалкилокси, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкилокси, который может быть замещен группой заместителей γ', ароматический гетероциклилалкилокси, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкилокси, который может быть замещен группой заместителей γ', ароматический карбоциклилалкилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкилоксикарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилалкилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкилоксикарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфанил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфанил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфинил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфонил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ, и не ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ'.
[0034]
Группа заместителей α: галоген, гидрокси, карбокси, алкилокси, галогеналкилокси, алкенилокси, алкинилокси, сульфанил и циано.
[0035]
Группа заместителей β: галоген, гидрокси, карбокси, циано, алкил, который может быть замещен группой заместителей α, алкенил, который может быть замещен группой заместителей α, алкинил, который может быть замещен группой заместителей α, алкилкарбонил, который может быть замещен группой заместителей α, и алкенилкарбонил, который может быть замещен группой α, алкинилкарбонил, который может быть замещен группой α, алкилсульфанил, который может быть замещен группой α, алкенилсульфанил, который может быть замещен группой α, алкинилсульфанил, который может быть замещен группой α алкилсульфинил, который может быть замещен группой заместителей α, алкенилсульфинил, который может быть замещен группой заместителей α, алкинилсульфинил, который может быть замещен группой заместителей α, алкилсульфонил, который может быть замещен группой заместителей α алкенилсульфонил, который может быть замещен группой заместителей α, алкинилсульфонил, который может быть замещен группой заместителей α,
ароматический карбоциклил, который может быть замещен группой заместителей γ, не ароматический карбоциклил, который может быть замещен группой заместителей γ', ароматический гетероциклил, который может быть замещен группой заместителей γ, не ароматический гетероциклил, который может быть замещен группой заместителей γ', ароматический карбоциклилалкил, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкил, который может быть замещен группой заместителей γ', ароматический гетероциклилалкил, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкил, который может быть замещен группой заместителей γ', ароматический карбоциклилкарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилкарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилкарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилкарбонил, который может быть замещен группой γ', ароматический карбоциклилоксикарбонил, который может быть замещен группой γ, не ароматический карбоциклилоксикарбонил, который может быть замещен группой γ', ароматический гетероциклилоксикарбонил, который может быть замещен группой γ, не ароматический гетероциклилоксикарбонил, который может быть замещен группой γ', ароматический карбоциклилсульфанил, который может быть замещен группой γ, не ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфанил, который может быть замещен группой γ, не ароматический гетероциклилсульфанил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфинил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфинил, который может быть замещен группой γ', ароматический карбоциклилсульфонил, который может быть замещен группой γ, не ароматический карбоциклилсульфонил, который может быть замещен группой γ', ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ, и не ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ'.
[0036]
Группа заместителей γ: группа заместителей α, алкил, галогеналкил, гидроксиалкил, алкенил, алкинил, алкилкарбонил, галогеналкилкарбонил, алкенилкарбонил и алкинилкарбонил.
[0037]
Группа заместителей γ': группа заместителей γ и оксо.
[0038]
Примеры заместителей на кольце «замещенного ароматического углеродного кольца» и «ароматического гетероциклического кольца» для «замещенного ароматического карбоциклила», «замещенного ароматического гетероциклила», «замещенного ароматического карбоциклилокси», «замещенного ароматического гетероциклилокси», «замещенного ароматического карбоциклилкарбонилокси», «замещенного ароматического гетероциклилкарбонилокси», «замещенного ароматического карбоциклилкарбонила», «замещенного ароматического гетероциклилкарбонила», «замещенного ароматического карбоциклилоксикарбонила», «замещенного ароматического гетероциклилоксикарбонила», «замещенного ароматического карбоциклилсульфанила», «замещенного ароматического гетероциклилсульфанила», «замещенного ароматического карбоциклилсульфинила», «замещенного ароматического гетероциклилсульфинила», «замещенного ароматического карбоциклилсульфонила», «замещенного ароматического гетероциклилсульфонила», «замещенного ароматического углеродного кольца, образованного R5 и R7 вместе с атомом углерода, к которому они присоединены» включают следующую группу заместителей B. Одна или несколько групп, выбранных из следующей группы заместителей B, могут быть присоединены к атому в лбом положении кольца.
Группа заместителей B: галоген, гидрокси, карбокси, формил, формилокси, сульфанил, сульфино, сульфо, тиоформил, тиокарбокси, дитиокарбокси, тиокарбамоил, циано, нитро, нитрозо, азидо, гидразино, уреидо, амидино гуанидино, пентафтортио, триалкилсилил,
алкил, замещенный группой заместителей α, алкенил, замещенный группой заместителей α, алкинил, замещенный группой заместителей α, алкилокси, замещенный группой заместителей α, алкенилокси, замещенный группой заместителей α, алкинилокси, замещенный группой заместителей α, алкилкарбонилокси, который может быть замещен группой заместителей α, алкенилкарбонилокси, который может быть замещен группой заместителей α, алкинилкарбонилокси, который может быть замещен группой заместителей α, алкилкарбонил, который может быть замещен группой α, алкенилкарбонил, который может быть замещен группой α, алкинилкарбонил, который может быть замещен группой α, алкилоксикарбонил, который может быть замещен группой α, алкенилоксикарбонил, который может быть замещен группой α, алкинилоксикарбонил, который может быть замещен группой α, алкилсульфанил, который может быть замещен группой заместителей α, алкенилсульфанил, который может быть замещен группой заместителей α, алкинилсульфанил, который может быть замещен группой заместителей α, алкилсульфинил, который может быть замещен группой заместителей α, алкенилсульфинил, который может быть замещен группой α, алкинилсульфинил, который может быть замещен группой α, алкилсульфонил, который может быть замещен группой α, алкенилсульфонил, который может быть замещен группой α, алкинилсульфонил, который может быть замещен группой α,
амино, который может быть замещен группой заместителей β, имино, который может быть замещен группой заместителей β, карбамоил, который может быть замещен группой заместителей β, сульфамоил, который может быть замещен группой заместителей β,
ароматический карбоциклил, который может быть замещен группой заместителей γ, не ароматический карбоциклил, который может быть замещен группой заместителей γ', ароматический гетероциклил, который может быть замещен группой заместителей γ, не ароматический гетероциклил, который может быть замещен группой заместителей γ', ароматический карбоциклилокси, который может быть замещен группой заместителей γ, не ароматический карбоциклилокси, который может быть замещен группой заместителей γ', ароматический гетероциклилокси, который может быть замещен группой заместителей γ, не ароматический гетероциклилокси, который может быть замещен группой заместителей γ', ароматический карбоциклилкарбонилокси, который может быть замещен группой заместителей γ, не ароматический карбоциклилкарбонилокси, который может быть замещен группой заместителей γ', ароматический гетероциклилкарбонилокси, который может быть замещен группой заместителей γ, не ароматический гетероциклилкарбонилокси, который может быть замещен группой заместителей γ', ароматический карбоциклилкарбонил, который может быть замещен группой γ, не ароматический карбоциклилкарбонил, который может быть замещен группой γ', ароматический гетероциклилкарбонил, который может быть замещен группой γ, не ароматический гетероциклилкарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилоксикарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилоксикарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилалкил, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкил, который может быть замещен группой заместителей γ', ароматический гетероциклилалкил, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкил, который может быть замещен группой заместителей γ', ароматический карбоциклилалкилокси, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкилокси, который может быть замещен группой заместителей γ', ароматический гетероциклилалкилокси, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкилокси, который может быть замещен группой заместителей γ', ароматический карбоциклилалкилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкилоксикарбонил, который может быть замещен группой γ', ароматический гетероциклилалкилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкилоксикарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилалкилоксиалкил,, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкилоксиалкил, который может быть замещен группой заместителей γ', ароматический гетероциклилалкилоксиалкил, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкилоксиалкил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфанил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфанил, который может быть замещен группой γ', ароматический карбоциклилсульфинил, который может быть замещен группой γ, не ароматический карбоциклилсульфинил, который может быть замещен группой γ', ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфонил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ, и не ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ'.
[0039]
Примеры заместителей на кольце «не ароматического углеродного кольца» или «не ароматического гетероциклического кольца» для «замещенного не ароматического карбоциклила», «замещенного не ароматического гетероциклила», «замещенного не ароматического карбоциклилокси», «замещенного не ароматического гетероциклилокси», «замещенного не ароматического карбоциклилкарбонилокси», «замещенного не ароматического гетероциклилкарбонилокси», «замещенного не ароматического карбоциклилкарбонила», «замещенного не ароматического гетероциклилкарбонила», «замещенного не ароматического карбоциклилоксикарбонила», «замещенного не ароматического гетероциклилоксикарбонила», «замещенного не ароматического карбоциклилсульфанила», «замещенного не ароматического гетероциклилсульфанила», «замещенного не ароматического карбоциклилсульфинила», «замещенного не ароматического гетероциклилсульфинила», «замещенного не ароматического карбоциклилсульфонила», «замещенного не ароматического гетероциклилсульфонила», «замещенного не ароматического карбоциклилдиила», «замещенного не ароматического гетероциклилдиила», «замещенного не ароматического карбоциклилоксиимино», «замещенного не ароматического карбоциклилиминоокси», «замещенного не ароматического углеродного кольца, образованного R5 и R7 вместе с атомом углерода, к которому они присоединены», «замещенного не ароматического углеродного кольца, образованного R7 и R8 вместе с атомом углерода, к которому они присоединены», «замещенного не ароматического гетероциклического кольца, образованного R7 и R8 вместе с атомом углерода, к которому они присоединены» и «замещенного не ароматического гетероциклического кольца, образованного R4 и RU вместе с атомом углерода, к которому они присоединены» включают следующую группу заместителей C. Одна или несколько групп, выбранных из следующей группы заместителей C, могут быть присоединены к атому в любому положении кольца.
Группа заместителей C: группа заместителей B и оксо.
[0040]
Когда «не ароматическое углеродное кольцо» или «не ароматическое гетероциклическое кольцо» замещено «оксо», оно означает кольцо, в котором два атома водорода на атоме углерода замещены следующим образом.
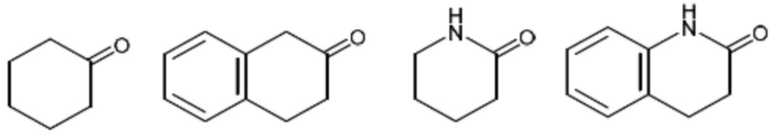
[0041]
Примеры группы заместителей для «замещенного амино», «замещенного имино», «замещенного карбамоила» и «замещенного сульфамоила» перечислены в группе заместителей D, следующим образом, и могут представлять собой одну или две группы, выбранные из группы заместителей D.
Группа заместителей D: галоген, гидрокси, карбокси, циано, алкил, который может быть замещен группой заместителей α, алкенил, который может быть замещен группой заместителей α, алкинил, который может быть замещен группой заместителей α, алкилкарбонил, который может быть замещен группой заместителей α, и алкенилкарбонил, который может быть замещен группой заместителей α, алкинилкарбонил, который может быть замещен группой заместителей α, алкилсульфанил, который может быть замещен группой заместителей α, алкенилсульфанил, который может быть замещен группой заместителей α алкинилсульфанил, алкилсульфинил, который может быть замещен группой заместителей α, алкенилсульфинил, который может быть замещен группой заместителей α, алкинилсульфинил, который может быть замещен группой заместителей α, алкилсульфонил, который может быть замещен группой заместителей α, алкенилсульфонил, который может быть замещен группой заместителей α, алкинилсульфонил, который может быть замещен группой заместителей α,
амино, который может быть замещен группой заместителей β, имино, который может быть замещен группой заместителей β, карбамоил, который может быть замещен группой заместителей β, сульфамоил, который может быть замещен группой заместителей β, сульфамоил, который может быть замещен группой заместителей,
ароматический карбоциклил, который может быть замещен группой заместителей γ, не ароматический карбоциклил, который может быть замещен группой заместителей γ', ароматический гетероциклил, который может быть замещен группой заместителей γ, не ароматический гетероциклил, который может быть замещен группой заместителей γ', ароматический карбоциклилалкил, который может быть замещен группой заместителей γ, не ароматический карбоциклилалкил, который может быть замещен группой заместителей γ', ароматический гетероциклилалкил, который может быть замещен группой заместителей γ, не ароматический гетероциклилалкил, который может быть замещен группой заместителей γ', ароматический карбоциклилкарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилкарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилкарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилкарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилоксикарбонил, который может быть замещен группой заместителей γ', ароматический гетероциклилоксикарбонил, который может быть замещен группой заместителей γ, не ароматический гетероциклилоксикарбонил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфанил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфанил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфанил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфинил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ, не ароматический гетероциклилсульфинил, который может быть замещен группой заместителей γ', ароматический карбоциклилсульфонил, который может быть замещен группой заместителей γ, не ароматический карбоциклилсульфонил, который может быть замещен группой заместителей γ', ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ, и не ароматический гетероциклилсульфонил, который может быть замещен группой заместителей γ'.
[0042]
В соединении формулы (I), предпочтительные варианты осуществления R1, R1B, R1C, L, R2, R3, X, Y, U, V, W, ZA, ZB, ZC, R5, R6, R7, R8, RX, RY, RV, RW, RU и R4 показаны ниже. Варианты осуществления соединения формулы (I) включают любую комбинацию следующих конкретных примеров.
[0043]
R1 представляет собой карбокси, циано, замещенный или незамещенный ароматический гетероциклил, -C(=O)-NR1BR1C или -CH=CHC(=O)-OH; где R1B и R1C каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный аминосульфонил или замещенный или незамещенный не ароматический гетероциклилсульфонил (далее обозначенный как a-1).
R1 представляет собой карбокси или -C(=O)-NR1BR1C; где R1B и R1C каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный аминосульфонил или замещенный или незамещенный не ароматический гетероциклилсульфонил (далее обозначен как a-2).
R1 представляет собой карбокси (далее обозначен как a-3).
[0044]
L представляет собой замещенный или незамещенный не ароматический карбоциклилдиил, замещенный или незамещенный не ароматический гетероциклилдиил или замещенный или незамещенный алкилен (далее обозначен как b-1).
L представляет собой замещенный или незамещенный не ароматический карбоциклилдиил или замещенный или незамещенный не ароматический гетероциклилдиил (далее обозначен как b-2).
L представляет собой замещенный или незамещенный не ароматический карбоциклилдиил (далее обозначен как b-3).
L представляет собой замещенный или незамещенный адамантандиил или замещенный или незамещенный циклогександиил (далее обозначен как b-4).
L представляет собой замещенный или незамещенный адамантан-2,2-диил или замещенный или незамещенный циклогексан-1,1-диил (далее обозначен как b-5).
L представляет собой не ароматический карбоциклилдиил, замещенный одним или несколькими заместителями, выбранными из группы заместителей a (группа заместителей a: циано, алкилокси, гидрокси и галоген) или незамещенный не ароматический карбоциклилдиил (далее обозначен как b-6).
L представляет собой адамантандиил, замещенный одним или несколькими заместителями, выбранными из группы заместителей a, или незамещенный адамантандиил (далее обозначен как b-7).
L представляет собой адамантан-2,2-диил, замещенный одним или несколькими заместителями, выбранными из группы заместителей a, или незамещенный адамантан-2,2-диил (далее обозначен как b-8).
L представляет собой циклогександиил, замещенный галогеном или незамещенный циклогександиил (далее обозначен как b-9).
L представляет собой циклогексан-1,1-диил, замещенный галогеном или незамещенный циклогексан-1,1-диил (далее обозначен как b-10).
L представляет собой адамантандиил, замещенный одним или несколькими заместителями, выбранными из группы заместителей a, незамещенный адамантандиил, циклогександиил, замещенный галогеном или незамещенный циклогександиил (далее обозначен как b-11).
L представляет собой адамантан-2,2-диил, замещенный одним или несколькими заместителями, выбранными из группы заместителей a, незамещенный адамантан-2,2-диил, циклогексан-1,1-диил, замещенный галогеном или незамещенный циклогексан-1,1-диил (далее обозначен как b-12).
L представляет собой адамантан-2,2-диил, замещенный одним или несколькими заместителями, выбранными из группы заместителей a (далее обозначен как b-13).
L представляет собой не замещенный адамантан-2,2-диил (далее обозначен как b-14).
L представляет собой циклогексан-1,1-диил, замещенный галогеном (далее обозначен как b-15).
L представляет собой незамещенный циклогексан-1,1-диил (далее обозначен как b-16).
[0045]
R2 представляет собой замещенный или незамещенный алкил (далее обозначен как c-1).
R2 представляет собой алкил, замещенный галогеном или не замещенный алкил (далее обозначен как c-2).
R2 представляет собой алкил, замещенный галогеном (далее обозначен как c-3).
[0046]
R3 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкилокси, замещенный или незамещенный амино или замещенный или незамещенный карбамоил (далее обозначен как d-1).
R3 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкилокси или замещенный или незамещенный амино (далее обозначен как d-2).
R3 представляет собой атом водорода или замещенный или незамещенный алкил (далее обозначен как d-3).
R3 представляет собой атом водорода или алкил замещенный одним или несколькими заместителями, выбранными из группы заместителей b (группа заместителей b: диалкиламино, амино и гидрокси) или не замещенный алкил (далее обозначен как d-4).
R3 представляет собой атом водорода (далее обозначен как d-5).
[0047]
X представляет собой =CRX- или =N-, где RX представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил (далее обозначен как e-1).
X представляет собой =CRX- или =N-, где RX представляет собой атом водорода, галоген или замещенный или незамещенный алкил (далее обозначен как e-2).
X представляет собой =CRX- или =N-, где RX представляет собой атом водорода, галоген или незамещенный алкил (далее обозначен как e-3).
X представляет собой =CH- или =N- (далее обозначен как e-4).
X представляет собой =CH- (далее обозначен как e-5).
X представляет собой =N- (далее обозначен как e-6).
[0048]
Y представляет собой =CRY- или =N-, где RY представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил (далее обозначен как f-1).
Y представляет собой =CRY- или =N-, где RY представляет собой атом водорода или галоген (далее обозначен как f-2).
Y представляет собой =CH- или =N- (далее обозначен как f-3).
Y представляет собой =CH- (далее обозначен как f-4).
Y представляет собой =N- (далее обозначен как f-5).
[0049]
U представляет собой -CRU= или -N=, где RU представляет собой атом водорода, замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил или замещенный или незамещенный не ароматический карбоциклил (далее обозначен как g-1).
U представляет собой -CRU= или -N=, где RU представляет собой атом водорода, галоген, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный не ароматический гетероциклилокси или замещенный или незамещенный алкилокси (далее обозначен как g-2).
U представляет собой -CRU= или -N=, где RU представляет собой атом водорода, галоген, не ароматический карбоциклилокси, замещенный пиразолилом, или незамещенный не ароматический карбоциклилокси, не ароматический гетероциклилокси, замещенного оксетанилом, или незамещенный не ароматический гетероциклилокси, или незамещенный алкилокси (далее обозначен как g-3).
U представляет собой -CH= или -N= (далее обозначен как g-4).
U представляет собой -CH= (далее обозначен как g-5).
U представляет собой -N= (далее обозначен как g-6).
[0050]
V представляет собой -CRV= или -N=, где RV представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил (далее обозначен как h-1).
V представляет собой -CRV= или -N=, где RV представляет собой атом водорода, циано или замещенный или незамещенный карбамоил (далее обозначен как h-2).
V представляет собой -CRV= или -N=, где RV представляет собой атом водорода, циано или незамещенный карбамоил (далее обозначен как h-3).
V представляет собой -CH= или -N= (далее обозначен как h-4).
V представляет собой -CH= (далее обозначен как h-5).
V представляет собой -N= (далее обозначен как h-6).
[0051]
W представляет собой =CRW- или =N-, где RW представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил (далее обозначен как i-1).
W представляет собой =CH- или =N- (далее обозначен как i-2).
W представляет собой =CH- (далее обозначен как i-3).
W представляет собой =N- (далее обозначен как i-4).
[0052]
ZA представляет собой -C= или -N- (далее обозначен как j-1).
ZA представляет собой -C= (далее обозначен как j-2).
ZA представляет собой -N- (далее обозначен как j-3).
[0053]
ZB представляет собой -CR5R6-, -CR5=, -NR5- или -N=, где R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-1).
ZB представляет собой -CR5R6-, -CR5= или -NR5-, где R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-2).
ZB представляет собой -CR5R6- или -CR5=, где R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-3).
ZB представляет собой -CR5R6-, где R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-4).
ZB представляет собой -CR5=, где R5 представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил (далее обозначен как k-5).
ZB представляет собой -CR5R6- или -CR5=, где R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-6).
ZB представляет собой -CR5R6-, где R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-7).
ZB представляет собой -CR5=, где R5 представляет собой атом водорода или замещенный или незамещенный не ароматический гетероциклил (далее обозначен как k-8).
ZB представляет собой -CR5R6- или -CR5=, где R5 и R6 каждый независимо представляет собой атом водорода (далее обозначен как k-9).
ZB представляет собой -CR5R6-, где R5 и R6 каждый независимо представляет собой атом водорода (далее обозначен как k-10).
ZB представляет собой -CR5=, где R5 представляет собой атом водорода (далее обозначен как k-11).
ZB представляет собой -CR5R6- или -CR5=, где R5 и R6 каждый независимо представляет собой атом водорода или незамещенный не ароматический гетероциклил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-12).
ZB представляет собой -CR5R6-, где R5 и R6 каждый независимо представляет собой атом водорода или незамещенный не ароматический гетероциклил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как k-13).
ZB представляет собой -CR5=, где R5 представляет собой атом водорода или незамещенный не ароматический гетероцикл (далее обозначен как k-14).
ZB представляет собой -CH2- (далее обозначен как k-15).
ZB представляет собой -CH= (далее обозначен как k-16).
[0054]
ZC представляет собой -CR7R8-, -CR7=, -NR7- или =N-, где R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, замещенный или незамещенный алкилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-1).
ZC представляет собой -CR7R8-, -CR7= или -NR7-, где R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, замещенный или незамещенный алкилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-2).
ZC представляет собой -CR7R8- или -NR7-, где R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, замещенный или незамещенный алкилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-3).
ZC представляет собой -CR7R8-, где R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, замещенный или незамещенный алкилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-4).
ZC представляет собой -NR7-, где R7 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил или замещенный или незамещенный алкилсульфонил (далее обозначен как l-5).
ZC представляет собой -CR7R8- или -NR7-, где R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-6).
ZC представляет собой -CR7R8-, где R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-7).
ZC представляет собой -NR7-, где R7 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, или замещенный или незамещенный не ароматический карбоциклилсульфонил (далее обозначен как l-8).
ZC представляет собой -CR7R8- или -NR7-, где R7 и R8 каждый независимо представляет собой атом водорода, алкил замещенный одним или несколькими заместителями, выбранными из группы заместителей c (группа заместителей c: галоген, гидрокси, алкилокси, не ароматический карбоциклил, не ароматический карбоциклил, замещенный галогеном, не ароматический гетероциклил, не ароматический гетероциклилкарбонил и ароматический карбоциклил) или незамещенный алкил, не ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей d (группа заместителей d: галоген, алкилокси, циано, гидрокси, галогеналкил и алкилокси, замещенного фенилом) или незамещенный не ароматический карбоциклил, не ароматический гетероциклил, замещенный галогеналкилом или незамещенный не ароматический гетероциклил, ароматический карбоциклил замещенный одним или несколькими заместителями, выбранными из группы заместителей e (группа заместителей e: галоген, алкил, галогеналкил, алкилокси и циано) или незамещенный ароматический карбоциклил, ароматический гетероциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей f (группа заместителей f: алкил, галоген, галогеналкил, алкилокси, гидрокси и циано) или незамещенный ароматический гетероциклил, незамещенный не ароматический карбоциклилоксикарбонил, незамещенный не ароматический гетероциклилоксикарбонил, незамещенный не ароматический карбоциклилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием не ароматического углеродного кольца, замещенного галогеном или незамещенного не ароматического углеродного кольца, или с образованием не ароматического гетероциклического кольца, замещенного одним или несколькими заместителями, выбранными из группы заместителей g (группа заместителей g: алкил, галогеналкил, алкилкарбонил, алкилоксикарбонил, замещенный фенилом, алкилоксикарбонил, не ароматический гетероциклил, алкилкарбамоил, не ароматический карбоциклил, ароматический гетероциклил и ароматический гетероциклил, замещенный галогеном) или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-9).
ZC представляет собой -CR7R8-, где R7 и R8 каждый независимо представляет собой атом водорода, незамещенный алкил, незамещенный не ароматический карбоциклил, незамещенный не ароматический гетероциклил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием не ароматического углеродного кольца, замещенного галогеном, или незамещенного не ароматического углеродного кольца, или с образованием не ароматического гетероциклического кольца, замещенного одним или несколькими заместителями, выбранными из группы заместителей g или незамещенного не ароматического гетероциклического кольца (далее обозначен как l-10).
ZC представляет собой -NR7-, где R7 представляет собой атом водорода, алкил замещенный одним или несколькими заместителями, выбранными из группы заместителей c, или незамещенный алкил, не ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей d, или незамещенный не ароматический карбоциклил, не ароматический гетероциклил, замещенный галогеналкилом или незамещенный не ароматический гетероциклил, ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей e, или незамещенный ароматический карбоциклил, ароматический гетероциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей f, или незамещенный ароматический гетероциклил, незамещенный не ароматический карбоциклилоксикарбонил, незамещенный не ароматический гетероциклилоксикарбонил, или незамещенный не ароматический карбоциклилсульфонил (далее обозначен как l-11).
ZC представляет собой -CR7R8-, где R7 и R8 каждый независимо представляет собой незамещенный алкил (далее обозначен как l-12).
ZC представляет собой -NR7-, где R7 представляет собой незамещенный алкил (далее обозначен как l-13).
[0055]
R4 представляет собой атом водорода, замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный ароматический карбоциклилокси, замещенный или незамещенный ароматический гетероциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, замещенный или незамещенный карбамоил, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклил или замещенный или незамещенный не ароматический гетероциклилкарбонил, или R4 и RU взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как m-1).
R4 представляет собой замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный ароматический карбоциклилокси, замещенный или незамещенный ароматический гетероциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, замещенный или незамещенный карбамоил, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклилкарбонил, или R4 и RU взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как m-2).
R4 представляет собой замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный ароматический карбоциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, замещенный или незамещенный карбамоил, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклилкарбонил, или R4 и RU взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как m-3).
R4 представляет собой алкилокси замещенный одним или несколькими заместителями, выбранными из группы заместителей h (группа заместителей h: галоген, гидрокси, алкилокси, циано, алкилкарбонилокси, замещенный ароматический гетероциклил (заместители: алкил или алкилокси), не ароматический гетероциклил, замещенный не ароматический гетероциклил (заместители: ароматический гетероциклил, алкил или галоген), ароматический гетероциклиламино, ароматический карбоциклил, и ароматический карбоциклил, замещенный алкилокси) или незамещенный алкилокси;
не ароматический гетероциклилокси замещенный одним или несколькими заместителями, выбранными из группы заместителей j (группа заместителей j: алкил, галоген, галогеналкил, цианоалкил, алкилкарбонил, алкилкарбамоил, алкилоксикарбонил, алкилоксиалкил, алкилсульфонилалкил, не ароматический гетероциклил, замещенный ароматический гетероциклил (заместители: алкил, алкилокси, галоген, галогеналкил или циано), ароматический гетероциклил, не ароматический карбоциклил, не ароматический карбоциклил, замещенный галогеном, замещенный не ароматический гетероциклил (заместители: галоген или алкилкарбонил), не ароматический гетероциклилалкил, не ароматический карбоциклилалкил, не ароматический карбоциклилалкил, замещенный галогеном, ароматический гетероциклилалкил, замещенный алкилом, не ароматический гетероциклилкарбонил, не ароматический карбоциклилкарбонил, ароматический гетероциклилкарбонил, ароматический карбоциклилалкилоксикарбонил, и не ароматический карбоциклилсульфонил) или незамещенный не ароматический гетероциклилокси;
не ароматический карбоциклилокси замещенный одним или несколькими заместителями, выбранными из группы заместителей k (группа заместителей k: алкил, галоген, галогеналкил, алкилокси, алкилсульфонил, галогеналкиламино, алкиламино, ароматический гетероциклил, не ароматический гетероциклил, замещенный галогеном, не ароматический гетероциклил, ароматический гетероциклил, замещенный галогеном, ароматический гетероциклиламино, замещенный галогеном, не ароматический гетероциклилалкил, замещенный галогеном, не ароматический карбоциклилокси, и не ароматический карбоциклилиминоокси, замещенный галогеном) или незамещенный не ароматический карбоциклилокси;
ароматический карбоциклилокси;
алкил или замещенный одним или несколькими заместителями, выбранными из группы заместителей l (группа заместителей l: галоген, ароматический карбоциклил, ароматический карбоциклил, замещенный алкилокси, не ароматический гетероциклил, и замещенный не ароматический гетероциклил (заместители: ароматический гетероциклил, не ароматический гетероциклил, замещенный алкилом или галогеном), и не ароматический карбоциклилоксиимино, замещенный галогеном) или незамещенный алкил;
алкенил, замещенный одним или несколькими заместителями, выбранными из группы заместителей m (группа заместителей m: ароматический карбоциклил, замещенный алкилокси, не ароматический гетероциклил, и не ароматический гетероциклил, замещенный ароматическим карбоциклилалкилоксикарбонилом) или незамещенный алкенил;
амино, замещенный одним или несколькими заместителями, выбранными из группы заместителей n (группа заместителей n: ароматический карбоциклилалкил, замещенный алкилокси, ароматический карбоциклилкарбонил, замещенный алкилокси, не ароматический гетероциклил, замещенный ароматическим гетероциклилом, ароматический гетероциклил, ароматический карбоциклилсульфонил, ароматический карбоциклилкарбонил, алкил, и ароматический гетероциклил, замещенный галогеналкилом) или незамещенный амино;
карбамоил, замещенный галогеналкилом, или незамещенный карбамоил;
гидрокси;
галоген;
ароматический карбоциклил, замещенный алкилоксиалкилом, или незамещенный ароматический карбоциклил;
незамещенный ароматический гетероциклил;
не ароматический гетероциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей o (группа заместителей o: ароматический гетероциклил, ароматический карбоциклилалкил, ароматический гетероциклилалкил и галогеналкил) или незамещенный не ароматический гетероциклил;
не ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей p (группа заместителей p: карбамоил и диалкилкарбамоил) или незамещенный не ароматический карбоциклил;
не ароматический гетероциклилкарбонил, замещенный одним или несколькими заместителями, выбранными из группы заместителей q (группа заместителей q: ароматический гетероциклил, галогеналкил, не ароматический гетероциклил, замещенный галогеном, ароматический гетероциклил, замещенный галогеном, галоген, и алкилокси) или незамещенный не ароматический гетероциклилкарбонил;
не ароматический карбоциклилоксиимино, замещенный галогеном; или
R4 и RU взяты вместе с атомом углерода, к которому они присоединены, с образованием не ароматического гетероциклического кольца, замещенного галогеном, или незамещенного не ароматического гетероциклического кольца (далее обозначен как m-4).
R4 представляет собой замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный карбамоил, или замещенный или незамещенный не ароматический гетероциклилкарбонил (далее обозначен как m-5).
R4 представляет собой алкилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей h, или незамещенный алкилокси, не ароматический гетероциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей j, или незамещенный не ароматический гетероциклилокси, не ароматический карбоциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей k, или незамещенный не ароматический карбоциклилокси, карбамоил, замещенный галогеналкилом, или незамещенный карбамоил, или не ароматический гетероциклилкарбонил, замещенный одним или несколькими заместителями, выбранными из группы заместителей q, или незамещенный не ароматический гетероциклилкарбонил (далее обозначен как m-6).
R4 представляет собой замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, или замещенный или незамещенный не ароматический карбоциклилокси (далее обозначен как m-7).
R4 представляет собой алкилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей h, или незамещенный алкилокси, не ароматический гетероциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей j, или незамещенный не ароматический гетероциклилокси, или не ароматический карбоциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей k, или незамещенный не ароматический карбоциклилокси (далее обозначен как m-8).
R4 представляет собой замещенный или незамещенный алкилокси (далее обозначен как m-9).
R4 представляет собой алкилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей h, или незамещенный алкилокси (далее обозначен как m-10).
R4 представляет собой замещенный или незамещенный не ароматический гетероциклилокси (далее обозначен как m-11).
R4 представляет собой не ароматический гетероциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей j, или незамещенный не ароматический гетероциклилокси (далее обозначен как m-12).
R4 представляет собой замещенный или незамещенный не ароматический карбоциклилокси (далее обозначен как m-13).
R4 представляет собой не ароматический карбоциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей k, или незамещенный не ароматический карбоциклилокси (далее обозначен как m-14).
R4 представляет собой не ароматический карбоциклилокси, замещенный одним или несколькими заместителями, выбранными из группы заместителей k (далее обозначен как m-15).
R4 представляет собой замещенный не ароматический карбоциклилокси (заместитель: не ароматический гетероциклил, замещенный галогеном) (далее обозначен как m-16).
R4 представляет собой замещенный не ароматический гетероциклилокси (заместители: ароматический гетероциклил) (далее обозначен как m-17).
R4 представляет собой замещенный не ароматический гетероциклилокси (заместители: ароматический гетероциклил замещенный галогеном) (далее обозначен как m-18).
R4 представляет собой замещенный не ароматический гетероциклилокси (заместители: галогеналкил) (далее обозначен как m-19).
R4 представляет собой замещенный не ароматический карбоциклилокси (заместитель: галогеналкиламино) (далее обозначен как m-20).
[0056]
Кроме того, примеры соединения формулы (I) охватывают все комбинации конкретных примеров, как показано выше.
Предпочтительные варианты осуществления группы формулы:
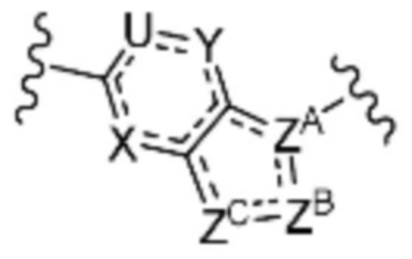
и R1, R1B, R1C, L, R2, R3, V, W, R5, R6, R7, R8, RX, RY, RV, RW, RU и R4 показаны ниже.
[0057]
Группа формулы:

представляет собой одну из представленных формулой (I-a), (I-b), (I-c), (I-d), (I-e), (I-f), (I-g), (I-h) или (I-i) следующим образом.
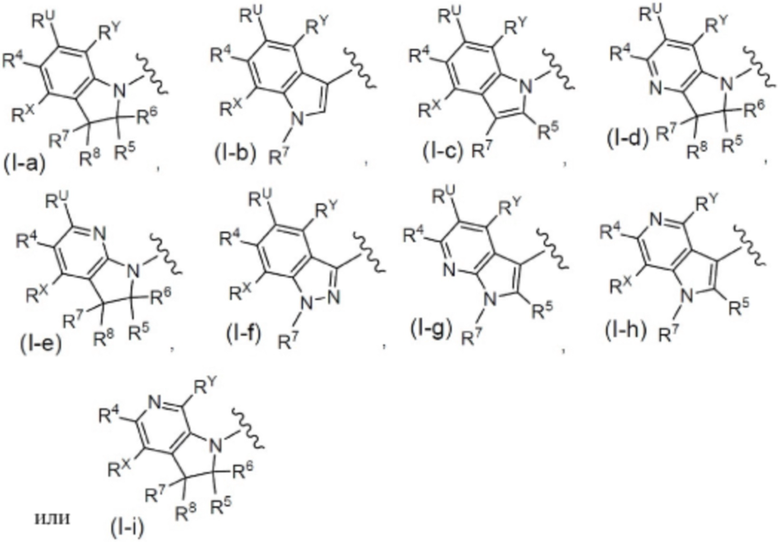
[0058]
Группа формулы:

представляет собой одну из представленных формулой (I-a), (I-b), (I-h) или (I-i).
[0059]
Группа формулы:

представляет собой одну из представленных формулой (I-a), (I-b) или (I-i).
[0060]
Группа формулы:

представляет собой одну из представленных формулой (I-a) или (I-b).
[0061]
Группа формулы:

представляет собой одну из представленных формулой (I-a).
[0062]
Группа формулы:

представляет собой одну из представленных формулой (I-b).
[0063]
RX представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил (далее обозначен как ee-1).
RX представляет собой атом водорода, галоген или замещенный или незамещенный алкил (далее обозначен как ee-2).
RX представляет собой атом водорода, галоген или незамещенный алкил (далее обозначен как ee-3)
RX представляет собой атом водорода (далее обозначен как ee-4).
[0064]
RY представляет собой атом водорода, циано, галоген, замещенный или незамещенный алкил или замещенный или незамещенный карбамоил (далее обозначен как ff-1).
RY представляет собой атом водорода или галоген (далее обозначен как ff-2).
RY представляет собой атом водорода (далее обозначен как ff-3).
[0065]
RU представляет собой атом водорода, замещенный или незамещенный алкилокси, замещенный или незамещенный не ароматический гетероциклилокси, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный амино, гидрокси, галоген, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический гетероциклил или замещенный или незамещенный не ароматический карбоциклил (далее обозначен как gg-1).
RU представляет собой атом водорода, галоген, замещенный или незамещенный не ароматический карбоциклилокси, замещенный или незамещенный не ароматический гетероциклилокси или замещенный или незамещенный алкилокси (далее обозначен как gg-2).
RU представляет собой атом водорода, галоген, не ароматический карбоциклилокси, замещенный пиразолилом, или незамещенный не ароматический карбоциклилокси, не ароматический гетероциклилокси, замещенный оксетанилом, или незамещенный не ароматический гетероциклилокси, или незамещенный алкилокси (далее обозначен как gg-3).
RU представляет собой атом водорода (далее обозначен как gg-4).
[0066]
R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как kk-1).
R5 представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, гидрокси или замещенный или незамещенный алкил (далее обозначен как kk-5).
R5 и R6 каждый независимо представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как kk-6).
R5 представляет собой атом водорода, замещенный или незамещенный не ароматический гетероциклил (далее обозначен как kk-8).
R5 и R6 каждый независимо представляет собой атом водорода (далее обозначен как kk-9).
R5 представляет собой атом водорода (далее обозначен как kk-10).
R5 и R6 каждый независимо представляет собой атом водорода, незамещенный не ароматический гетероциклил, или R5 и R6 взяты вместе с образованием оксо (далее обозначен как kk-12).
R5 представляет собой атом водорода или незамещенный не ароматический гетероциклил (далее обозначен как kk-14).
[0067]
R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, замещенный или незамещенный алкилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как ll-1).
R7 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил или замещенный или незамещенный алкилсульфонил (далее обозначен как ll-5).
R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, замещенный или незамещенный не ароматический карбоциклилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как ll-6).
R7 и R8 каждый независимо представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного не ароматического углеродного кольца или замещенного или незамещенного не ароматического гетероциклического кольца (далее обозначен как ll-7).
R7 представляет собой атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный не ароматический карбоциклил, замещенный или незамещенный не ароматический гетероциклил, замещенный или незамещенный ароматический карбоциклил, замещенный или незамещенный ароматический гетероциклил, замещенный или незамещенный не ароматический карбоциклилоксикарбонил, замещенный или незамещенный не ароматический гетероциклилоксикарбонил, или замещенный или незамещенный не ароматический карбоциклилсульфонил (далее обозначен как ll-8).
R7 и R8 каждый независимо представляет собой атом водорода, алкил замещенный одним или несколькими заместителями, выбранными из группы заместителей c или незамещенного алкил, не ароматический карбоциклил замещенный одним или несколькими заместителями, выбранными из группы заместителей d, или незамещенный не ароматический карбоциклил, не ароматический гетероциклил, замещенный галогеналкилом, или незамещенный не ароматический гетероциклил, ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей e, или незамещенный ароматический карбоциклил, ароматический гетероциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей f, или незамещенный ароматический гетероциклил, незамещенный не ароматический карбоциклилоксикарбонил, незамещенный не ароматический гетероциклилоксикарбонил, незамещенный не ароматический карбоциклилсульфонил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены с образованием не ароматического углеродного кольца, замещенного галогеном, или незамещенного не ароматического углеродного кольца или не ароматического гетероциклического кольца, замещенного одним или несколькими заместителями, выбранными из группы заместителей g, или незамещенного не ароматического гетероциклического кольца (далее обозначен как ll-9).
R7 и R8 каждый независимо представляет собой атом водорода, незамещенный алкил, незамещенный не ароматический карбоциклил, незамещенный не ароматический гетероциклил, или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием не ароматического углеродного кольца, замещенного галогеном, или незамещенного не ароматического углеродного кольца или не ароматического гетероциклического кольца, замещенного одним или несколькими заместителями, выбранными из группы заместителей g, или незамещенного не ароматического гетероциклического кольца (далее обозначен как ll-10).
R7 и R8 каждый независимо представляет собой незамещенный алкил (далее обозначен как ll-11).
R7 представляет собой атом водорода, алкил, замещенный одним или несколькими заместителями, выбранными из группы заместителей c, или незамещенный алкил, не ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей d, или незамещенный не ароматический карбоциклил, не ароматический гетероциклил, замещенный галогеналкилом, или незамещенный не ароматический гетероциклил, ароматический карбоциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей e, или незамещенный ароматический карбоциклил, ароматический гетероциклил, замещенный одним или несколькими заместителями, выбранными из группы заместителей f, или незамещенный ароматический гетероциклил, незамещенный не ароматический карбоциклилоксикарбонил, незамещенный не ароматический гетероциклилоксикарбонил или незамещенный не ароматический карбоциклилсульфонил (далее обозначен как ll-12).
R7 представляет собой незамещенный алкил (далее обозначен как ll-13).
R7 и R8 взяты вместе с атомом углерода, к которому они присоединены с образованием незамещенного не ароматического гетероциклического кольца (далее обозначен как ll-14).
R7 и R8 взяты вместе с атомом углерода, к которому они присоединены с образованием не ароматического углеродного кольца, замещенного галогеном (далее обозначен как ll-15).
R7 представляет собой замещенное не ароматическое углеродное кольцо (заместитель: галоген) (далее обозначен как ll-16).
R7 представляет собой замещенный алкил (заместитель: алкилокси) (далее обозначен как ll-17).
[0068]
R1 такой, как определен в вышеуказанных (a-1), (a-2) или (a-3).
[0069]
L такой, как определен в вышеуказанных (b-1), (b-2), (b-3), (b-4), (b-5), (b-6), (b-7), (b-8), (b-9), (b-10), (b-11), (b-12), (b-13), (b-14), (b-15) или (b-16).
[0070]
R2 такой, как определен в вышеуказанных (c-1), (c-2) или (c-3).
[0071]
R3 такой, как определен в вышеуказанных (d-1), (d-2), (d-3), (d-4) или (d-5).
[0072]
V такой, как определен в вышеуказанных (h-1), (h-2), (h-3), (h-4), (h-5) или (h-6).
[0073]
W такой, как определен в вышеуказанных (i-1), (i-2), (i-3) или (i-4).
[0074]
R4 такой, как определен в вышеуказанных (m-1), (m-2), (m-3), (m-4), (m-5), (m-6), (m-7), (m-8), (m-9), (m-10), (m-11), (m-12), (m-13), (m-14), (m-15), (m-16), (m-17), (m-18), (m-19) или (m-20).
[0075]
(1-A)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-a),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R5 и R6 такие, как определены в (kk-9),
R7 и R8 такие, как определены в (ll-14),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-17).
[0076]
(1-B)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-b),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R7 такой, как определен в (ll-15),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-3), и
R4 такой, как определен в (m-17).
[0077]
(1-C)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-b),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R7 такой, как определен в (ll-15),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-16).
[0078]
(1-D)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-b),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R7 такой, как определен в (ll-13),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-16).
[0079]
(1-E)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-i),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
R5 и R6 такие, как определены в (kk-9),
R7 и R8 такие, как определены в (ll-14),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-18).
[0080]
(1-F)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-a),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R5 и R6 такие, как определены в (kk-9),
R7 и R8 такие, как определены в (ll-14),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-16).
[0081]
(1-G)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-a),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R5 и R6 такие, как определены в (kk-9),
R7 и R8 такие, как определены в (ll-14),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-19).
(1-H)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-a),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R5 и R6 такие, как определены в (kk-9),
R7 и R8 такие, как определены в (ll-14),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-20).
(1-I)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-b),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R7 такой, как определен в (ll-17),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-16).
[0082]
(1-J)
В одном варианте осуществления, соединение формулы (I) представляет собой соединение,
где
группа формулы:

такая, как определена в (I-a),
RX такой, как определен в (ee-4),
RY такой, как определен в (ff-3),
RU такой, как определен в (gg-4),
R5 и R6 такие, как определены в (kk-9),
R7 и R8 такие, как определены в (ll-11),
R1 такой, как определен в (a-3),
L такой, как определен в (b-14),
R2 такой, как определен в (c-3),
R3 такой, как определен в (d-5),
V такой, как определен в (h-6),
W такой, как определен в (i-4), и
R4 такой, как определен в (m-16).
[0083]
Соединения формулы (I) не ограничены конкретными изомерами, но включают все возможные изомеры (например, кето-енольные изомеры, имин-енаминовые изомеры, диастереоизомеры, оптические изомеры, вращательные изомеры и т.д.), рацематы или их смеси.
[0084]
Один или несколько атомов водорода, углерода и/или другого(их) атома(ов) соединения формулы (I) могут быть замещены изотопом(ами) водорода, углерода и/или другого(их) атома(ов), соответственно. Примеры таких изотопов включают водород, углерод, азот, кислород, фосфор, серу, фтор, йод и хлор, как в случае 2H, 3H, 11C, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F, 123I и 36Cl, соответственно. Соединения формулы (I) также включают соединения, замещенные такими изотопами. Соединения, замещенные изотопами, также применимы в качестве фармацевтических продуктов и включают все меченые радиоактивным изотопом формы соединений формулы (I). Кроме того, в настоящее изобретение также включен «способ введения радиоактивной метки» для получения «форм с радиоактивной меткой», и «формы с радиоактивной меткой» можно использовать в качестве инструментов для исследований метаболической фармакокинетики, исследований по анализу связывания и/или диагностики.
[0085]
Радиоактивно меченые соединения формулы (I) могут быть получены способами, хорошо известными в данной области техники. Например, меченые тритием соединения формулы (I) могут быть получены введением трития в некоторые соединения формулы (I) посредством реакции каталитического дегалогенирования с использованием трития. Этот способ включает взаимодействие соединения, обозначенного формулой (I), с соответствующим галоген-замещенным предшественником и газообразным тритием в присутствии или в отсутствие основания в присутствии подходящего катализатора, т.е. Pd/C. Этот способ включает другие подходящие способы получения меченых тритием соединений, описанные в "Isotopes in the Physical and Biomedical Sciences, Vol. 1, Labeled Compounds (Part A), Chapter 6 (1987). 14С-меченые соединения могут быть получены с применением исходных материалов, содержащих 14С углерод.
[0086]
Примеры фармацевтически приемлемых солей соединений формулы (I) включают соли соединений формулы (I) со щелочными металлами (например, литием, натрием и калием), щелочноземельными металлами (например, кальцием и барием), магнием, переходными металлами (например, цинк и железо), аммиаком, органическими основаниями (например, триметиламином, триэтиламином, дициклогексиламином, этаноламином, диэтаноламином, триэтаноламином, меглумином, этилендиамином, пиридином, пиколином и хинолином) и аминокислотами, или соли с неорганическими кислотами (например, хлористоводородной кислотой, серной кислотой, азотной кислотой, угольной кислотой, бромистоводородной кислотой, фосфорной кислотой и йодистоводородной кислотой) и органическими кислотами (например, муравьиной кислотой, уксусной кислотой, пропионовой кислотой, трифторуксусной кислотой, лимонной кислотой, молочной кислотой, винной кислотой, щавелевой кислотой, малеиновой кислотой, фумаровой кислотой, янтарной кислотой, миндальной кислотой, глутаровой кислотой, яблочной кислотой, бензойной кислотой, фталевой кислотой, аскорбиновой кислотой, бензолсульфоновой кислотой, п-толуолсульфоновой кислотой, метансульфоновой кислотой, этансульфоновой кислотой и трифторуксусной кислотой). Эти соли могут быть получены в соответствии с обычно проводимыми способами.
[0087]
Соединения формулы (I) или их фармацевтически приемлемые соли могут образовывать сольваты (например, гидраты и подобные), сокристаллы и/или кристаллические полиморфы. Настоящее изобретение охватывает эти различные сокристаллы сольватов и кристаллические полиморфы. «Сольваты» могут представлять собой сольваты, в которых любое количество молекул растворителя (например, молекул воды и подобных) координировано с соединениями формулы (I). Когда соединения формулы (I) или их фармацевтически приемлемые соли оставляют выстаиваться в атмосфере, соединения могут поглощать воду, что приводит к присоединению адсорбированной воды или образованию гидратов. Перекристаллизация соединений формулы (I) или их фармацевтически приемлемых солей может давать кристаллические полиморфы. «Сокристалл» означает, что соединение формулы (I) или его соль и противомолекула существуют в одной и той же кристаллической решетке, которая может содержать любое количество противомолекул.
[0088]
Соединения формулы (I) по настоящему изобретению или их фармацевтически приемлемые соли могут образовывать пролекарства, и настоящее изобретение также включает такие различные пролекарства. Пролекарство представляет собой производное соединения по настоящему изобретению, имеющее группу, которая может разлагаться химически или метаболически, и представляет собой соединение, которое становится фармацевтически активным соединением по настоящему изобретению in vivo в результате сольволиза или в физиологических условиях. Пролекарства включают соединения, которые подвергаются ферментативному окислению, восстановлению, гидролизу и подобным в физиологических условиях в живом организме и превращаются в соединения формулы (I); соединения, которые гидролизуются кислотой желудочного сока или подобными и превращаются в соединения формулы (I); и подобные. Способы выбора и получения подходящего производного пролекарства описаны, например, в “Design of Prodrugs, Elsevier, Amsterdam, 1985”. Пролекарство может иметь активность per se.
[0089]
Когда соединение формулы (I) или его фармацевтически приемлемая соль имеет гидроксильную(ые) группу(ы), пролекарства могут представлять собой производные ацилокси и производные сульфонилокси, которые получают, например, взаимодействием соединения, имеющего гидроксильную(ые) группу(ы), с подходящим ацилгалогенидом, подходящим ангидридом кислоты, подходящим сульфонилхлоридом, подходящим сульфонилангидридом или смешанным ангидридом, или путем взаимодействия с конденсирующим агентом. Примеры включают CH3COO-, C2H5COO-, трет-BuCOO-, C15H31COO-, PhCOO-, (м-NaOOCPh)COO-, NaOOCCH2CH2COO-, CH3CH(NH2)COO-, CH2N(CH3)2COO-, CH3SO3-, CH3CH2SO3-, CF3SO3-, CH2FSO3-, CF3CH2SO3-, p-CH3-O-PhSO3-, PhSO3- и p-CH3PhSO3-.
[0090]
Следующие примеры составов приведены только в качестве примеров и не предназначены для ограничения объема изобретения.
Соединение по настоящему изобретению можно вводить в виде фармацевтической композиции любым обычным путем, в частности, энтерально, например, перорально, например, в форме таблетки или капсулы; парентерально, например, в виде препарата или суспензии для инъекции; и местно, например, в форме лосьона, геля, мази или крема, или в виде фармацевтической композиции в трансназальной форме или в форме суппозитория. Фармацевтическая композиция, содержащая соединение по настоящему изобретению в свободной форме или в форме фармацевтически приемлемой соли вместе с по меньшей мере одним фармацевтически приемлемым носителем или разбавителем, может быть получена путем смешивания, гранулирования или нанесения покрытия обычным способом. Например, пероральная композиция может представлять собой таблетку, гранулированный препарат или капсулу, каждая из которых содержит эксципиент, разрыхлитель, связующий агент, смазывающий агент и подобные, а также активный ингредиент и подобные. Кроме того, композиция для инъекции может быть приготовлена в виде раствора или суспензии, может быть стерилизована, и может содержать консервант, стабилизатор, буферный агент и подобный.
[0091]
Соединения по изобретению полезны при следующих симптомах, вызванных RSV, и такие симптомы, вызванные RSV, варьируются от легких симптомов, подобных обычной простуде, до тяжелых заболеваний нижних дыхательных путей, таких как бронхиолит и пневмония. Другими словами, он полезен при таких симптомах простуды, как кашель, насморк и лихорадка, а также при таких симптомах, как свистящее дыхание и затрудненное дыхание, возникающих в более тяжелых случаях, а также при таких заболеваниях, как бронхит и пневмония, которые возникают как в результате ухудшения этих симптомов.
[0092]
(Способ получения соединений по изобретению)
Соединения формулы (I) по настоящему изобретению могут быть получены, например, с помощью общего способа синтеза, описанного ниже. Что касается экстракции, очистки и подобных, то можно проводить обработку, проводимую в обычных экспериментах по органической химии.
Соединения по настоящему изобретению могут быть получены с использованием способов, известных в данной области техники.
[0093]
(Способ A)
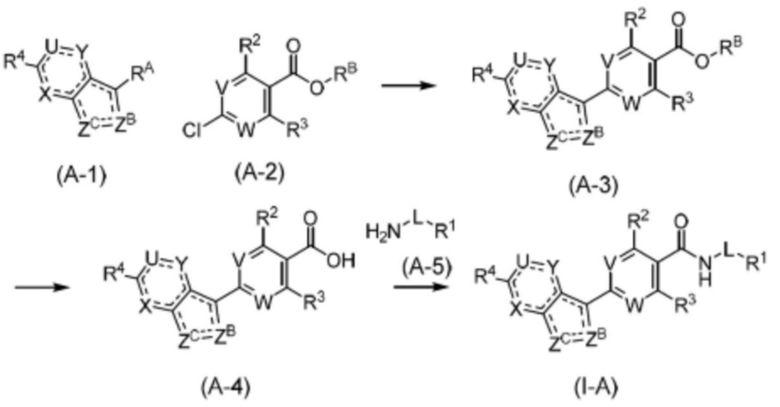
где каждый символ такой, как определен выше, и RA представляет собой -B(OH)2, -Sn(C1-C6 алкил)3, и т.д., и RB представляет собой C1-C6 алкил, и т.д.
Стадия 1
Соединение (А-3) может быть получено реакцией Соединения (А-1) с Соединением (А-2) в растворителе (например, тетрагидрофуране, толуоле, диметилформамиде, 1,4-диоксане, этаноле, воде и т.д.) или их смешанном растворителе, в присутствии металлического катализатора (например, тетракис(трифенилфосфин)палладия, дихлорида бис(трифенилфосфин)палладия(II), бис(три-трет-бутилфосфин)палладия и т.д.) и основания (например, карбоната калия, гидрокарбоната натрия, фосфата натрия, гидрофосфата натрия, фосфата калия, гидрофосфата калия, гидроксида лития, гидроксида натрия, гидроксида калия, трет-бутоксида калия и т.д.) при температуре от 20°С до температуры кипения с обратным холодильником растворителя в течение от 0,1 до 48 часов, предпочтительно, от 0,5 до 12 часов.
[0094]
Стадия 2
Реакцию снятия защиты с карбоксильной защитной группы Соединения (А-3) можно проводить обычным способом, например, как описано в Protective Groups in Organic Synthesis, Theodora W Green (John Wiley & Sons).
[0095]
Стадия 3
Соединение (I-A) может быть получено реакцией Соединения (A-4) с Соединением (A-5) в растворителе (например, диметилформамиде, тетрагидрофуране, дихлорметане, ацетонитриле, воде и т.д.) или их смешанном растворителе, в присутствии или отсутствие основания (например, триэтиламина, пиридина, диизопропиламина, 1-метилимидазола и т.д.) с использованием агента дегидратации-конденсации (например, дициклогексилкарбодиимида, карбонилдиимидазола, EDC⋅HCl, ГАТУ и т.д.).
Альтернативно, ацилирующий реагент (например, тионилхлорид, оксалилхлорид и т.д.) добавляют к Соединению (А-4) в растворителе (например, тетрагидрофуране, 1,4-диоксане, дихлорметане, диметилформамиде и т.д.) в присутствии или в отсутствие основания (например, пиридина, триэтиламина, диизопропиламина, 1-метилимидазола и т.д.) с образованием хлорангидрида, который затем добавляют к Соединению (А-5), и реакцию проводят при температуре от -20°С до 60°С, предпочтительно, от -10°С до 30°С, в течение от 0,1 до 24 часов, предпочтительно, от 0,5 до 12 часов, с получением соединения (I-A).
[0096]
(Способ B)
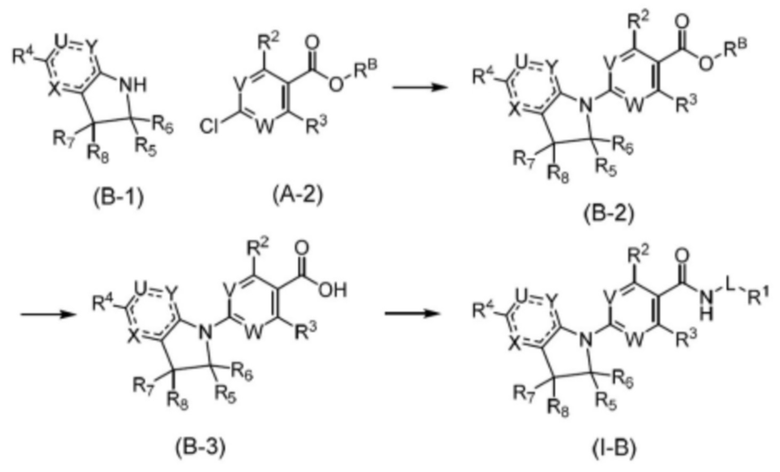
где каждый символ такой, как определен выше.
Стадия 1
Соединение (B-2) может быть получено реакцией Соединения (B-1) с Соединением (A-2) в растворителе (например, 1,4-диоксане, толуоле, тетрагидрофуране, диметилформамиде, N-метилпирролидоне и т.д.) в присутствии или в отсутствие основания (например, триэтиламина, диизопропиламина, карбоната цезия, карбоната калия, гидрида натрия и т.д.) или кислоты (например, толуолсульфоновой кислоты, уксусной кислоты, хлороводорода, серной кислоты, и т.д.) при температуре от 20°С до температуры кипения с обратным холодильником растворителя, предпочтительно, от 40°С до 120°С, в течение от 0,1 часа до 48 часов, предпочтительно, от 0,5 часа до 12 часов.
Альтернативно, Соединение (В-2) может быть получено реакцией Соединения (В-1) с Соединением (А-2) в растворителе (например, 1,4-диоксане, толуоле, тетрагидрофуране, диметилформамид, е N-метилпирролидоне, бутаноле, воде и т.д.) или их смешанном растворителе, в присутствии или в отсутствие лиганда (например, Xantphos, дифенилфосфиноферроцена, X-phos и т.д.) и в присутствии металлического катализатора (например, ацетата палладия, бис(дибензилиденацетон)палладия, тетракис(трифенилфосфин)палладия, дихлорида бис(трифенилфосфин)палладия(II), бис(три-трет-бутилфосфина, и т.д.), и основания (например, трет-бутоксида калия, трет-бутоксида натрия, карбоната натрия, карбоната калия, карбоната цезия, фосфата натрия, гидрофосфата натрия, гидроксида лития, гидроксида натрия и т.д.) в течение от 0,1 до 48 часов, предпочтительно, от 0,5 до 12 часов, при температуре от 20°С до температуры кипения с обратным холодильником растворителя или, в некоторых случаях, до температуры микроволнового излучения.
[0097]
Стадия 2 и Стадия 3
Соединение (I-B) может быть получено проведением Стадии 2 и Стадии 3 из Способа A, с использованием Соединения (B-2).
[0098]
(Способ C)
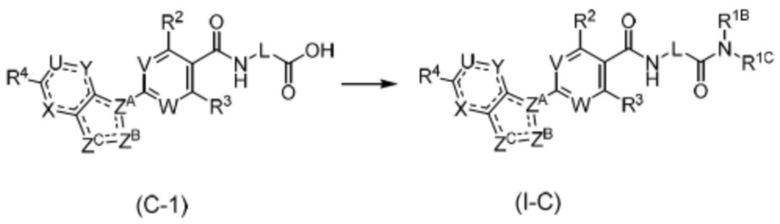
где каждый символ такой, как определен выше
Стадия 1
Соединение (I-C) может быть получено реакцией Соединения (C-1) с NHR1BR1C в растворителе (например, диметилформамиде, тетрагидрофуране, дихлорметане, ацетонитриле, воде и т.д.) или их смешанном растворителе, в присутствии агента дегидратации-конденсации (например, дициклогексилкарбодиимида, карбонилдиимидазола, EDC⋅HCl, ГАТУ и т.д.) и основания (например, триэтиламина, пиридина, диизопропиламина, 1-метилмимдазола, гидрида натрия и т.д.).
[0099]
(Способ D)
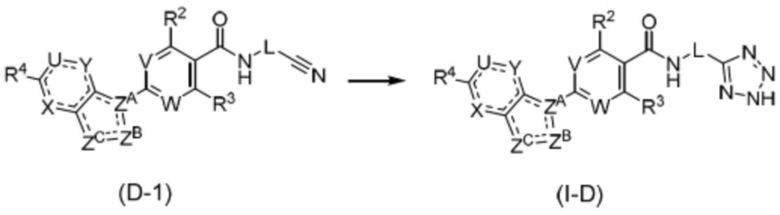
где каждый символ такой, как определен выше.
Стадия 1
Соединение (I-D) может быть получено реакцией Соединения (D-1) с соединением азида (например, азидотриметилсилана, азида натрия, азида трибутилолова и т.д.) в растворителе (например, 1,4-диоксане, диметилформамиде, воде и т.д.) или их смешанном растворителе, в присутствии добавки (например, дибутилстаннана, хлорида цинка, хлорида аммония и т.д.) при температуре от 60°C до температуры кипения с обратным холодильником растворителя, или в некоторых случаях, при температуре при микроволновом облучении, в течение от 0,5 до 48 часов, предпочтительно, от 1 до 4 часов.
[0100]
(Способ E)
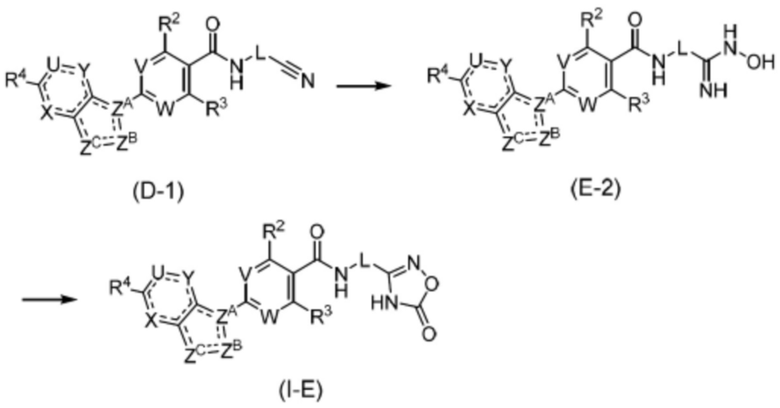
где каждый символ такой, как определен выше.
Стадия 1
Соединение (E-2) может быть получено реакцией Соединения (D-1) с гидроксиамином, и т.д., в растворителе (например, метаноле, этаноле, тетрагидрофуране, воде и т.д.) или их смешанном растворителе, в присутствии или в отсутствие основания (например, карбоната калия, триэтиламина и т.д.) при температуре от комнатной до температуры кипения с обратным холодильником растворителя, или в некоторых случаях, при температуре при микроволновом облучении.
[0101]
Стадия 2
Соединение (I-E) может быть получено реакцией Соединения (E-2) с 1,1'-карбонилдиимидазолом или этилхлорформиатом в растворителе (например, диметилформамиде, хлороформе, дихлорметане, тетрагидрофуране, толуоле и т.д.) или их смешанном растворителе, в присутствии основания (например, триэтиламина, ДБУ, карбоната калия, и т.д.) при температуре от комнатной до температуры кипения с обратным холодильником растворителя.
[0102]
(Способ F)
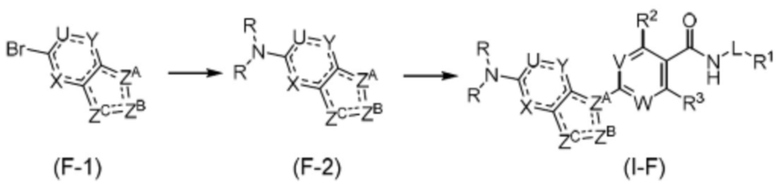
где R представляет собой группу, независимо выбранную из группы заместителей n, и другие символы такие, как определены выше.
Стадия 1
Соединение (F-2) может быть получено реакцией Соединения (F-1) с амином в растворителе (например, 1,4-диоксане, толуоле, тетрагидрофуране, диметилформамиде, N-метилпирролидоне, бутаноле, воде и т.д.) или их смешанном растворителе, в присутствии или в отсутствие лиганда (например, Xantphos, дифенилфосфиноферроцена, X-Phos, BINAP и т.д.) и в присутствии металлического катализатора (например, ацетата палладия, бис(дибензилиденацетон)палладия, тетракис(трифенилфосфин)палладия, дихлорида бис(трифенилфосфин)палладия(II), бис(три-трет-бутилфосфина), и т.д.) и основания (например, трет-бутоксида калия, трет-бутоксида натрия, карбоната натрия, карбоната калия, карбоната цезия, фосфата натрия, гидрофосфата натрия, гидроксида лития, гидроксида натрия, и т.д.) при температуре от 20°C до температуры кипения с обратным холодильником растворителя или, в некоторых случаях, при температуре при микроволновом облучении в течение 0,1 до 48 часов, предпочтительно, в течение от 0,5 до 12 часов.
[0103]
Стадия 2
Соединение (I-F) может быть получено проведением Стадии 1 из Способа A или Стадии 1 из Способа B, с использованием Соединения (F-2).
[0104]
(Способ G)
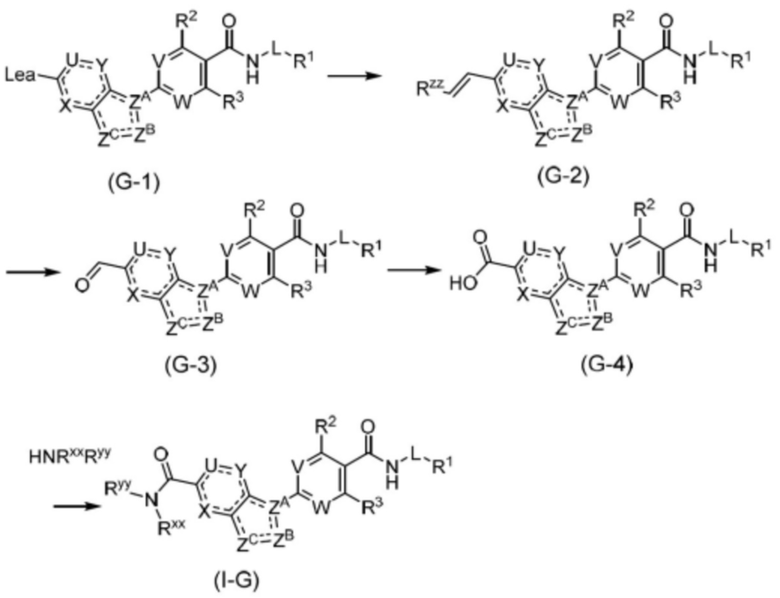
где каждый символ такой, как определен выше, Lea представляет собой уходящую группу, Rzz представляет собой атом водорода, C1-C6 алкил, и т.д., Rxx и Ryy каждый независимо представляет собой атом водорода, C1-C6 алкил, и т.д., или Rxx и Ryy взяты вместе с соседним атомом азота с образованием кольца.
Стадия 1
Соединение (G-2) может быть получено проведением Стадии 1 из Способа A, с использованием Соединения (G-1).
[0105]
Стадия 2
Соединение (G-3) может быть получено реакцией Соединения (G-2) в растворителе (например, 1,4-диоксане, тетрагидрофуране или воде, и т.д.) или их смешанном растворителе, с добавлением периодата натрия или оксона и хлорида рутения или осмита калия. Альтернативно, озонид получают окислением озона с последующей обработкой восстанавливающим агентом (например, цинком, диметилсульфидом, трифенилфосфином и т.д.) с получением Соединения (G-3).
[0106]
Стадия 3
Соединение (G-4) может быть получено реакцией Соединения (G-3) в растворителе (например, тетрагидрофуране, трет-бутаноле, воде, и т.д.) или их смешанном растворителе, с добавлением дигидрофосфата натрия и хлорита натрия в присутствии 2-метил-2-бутена, сульфаминовой кислоты и т.д.
[0107]
Стадия 4
Соединение (I-G) может быть получено проведением Стадии 1 из Способа C, с использованием Соединения (G-4).
[0108]
(Способ H)
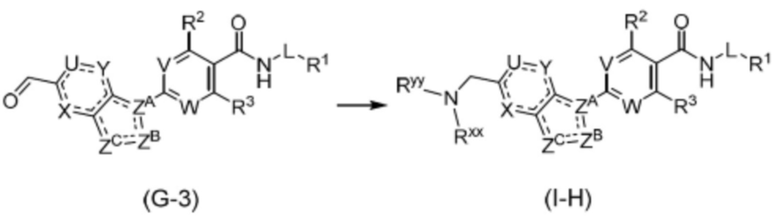
где каждый символ такой, как определен выше, и Rxx и Ryy представляют собой атомы водорода, C1-C6 алкил, или Rxx и Ryy взяты вместе с соседним атомом азота с образованием кольца.
Стадия 1
Соединение (I-H) может быть получено реакцией Соединения (G-3) с NHRyyRxx в растворителе (например, хлороформе, тетрагидрофуране, ацетонитриле, уксусной кислоте и т.д.) или их смешанном растворителе, в присутствии восстанавливающего агента (например, триацетоксиборгидрида натрия, 2-пиколинбора и т.д.) при температуре от комнатной до температуры кипения с обратным холодильником растворителя в течение от 0,1 до 48 часов, предпочтительно, в течение от 0,5 до 8 часов.
[0109]
(Способ J)
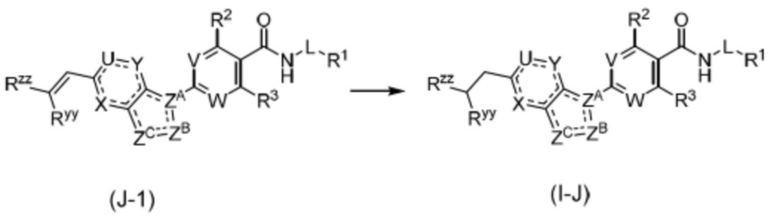
где каждый символ такой, как определен выше, и Rzz и Ryy представляют собой атомы водорода, C1-C6 алкил, ароматический карбоциклил, ароматический гетероциклил, и т.д.
Стадия 1
Соединение (I-J) может быть получено каталитическим гидрированием Соединения (J-1) в растворителе (например, тетрагидрофуране, метаноле, толуоле, хлороформе и т.д.) или их смешанном растворителе, в присутствии гетерогенного катализатора (например, палладия на угле, гидроксида палладия, никеля Ренея, оксида платины и т.д.).
[0110]
Поскольку соединение по настоящему изобретению обладает действием против RSV, т.е. действием, ингибирующим CPE (цитопатический эффект), это соединение полезно в качестве терапевтического и/или профилактического агента для лечения таких заболеваний, как бронхиолит и пневмония.
Кроме того, соединение по настоящему изобретению применимо в качестве лекарственного средства, и предпочтительно, соединение по настоящему изобретению обладает одним или несколькими из следующих превосходных свойств.
а) Ингибирующая активность в отношении ферментов CYP (например, CYP1A2, CYP2C9, CYP2C19, CYP2D6 и CYP3A4) слабая.
b) Демонстрируется удовлетворительная фармакокинетика, такая как высокая биодоступность и достаточный клиренс.
с) Метаболическая стабильность высокая.
d) Необратимая ингибирующая активность не демонстрируется в отношении ферментов CYP (например, CYP3A4) в диапазоне концентраций условий измерения, описанных в настоящей спецификации.
е) Мутагенность не демонстрируется.
f) Сердечно-сосудистый риск низкий.
g) Проявляется высокая растворимость.
h) Проявляется высокое ингибирующее действие СРЕ RSV типа A и высокое ингибирующее действие RSV типа B.
i) Количество вируса в легких уменьшается.
[0111]
Фармацевтические композиции по настоящему изобретению можно вводить перорально или парентерально. Примеры парентерального введения включают чрескожное, подкожное, внутривенное, внутриартериальное, внутримышечное, внутрибрюшинное, трансмукозальное, ингаляционное, трансназальное, закапывание в глаз, закапывание в ухо и интравагинальное введение.
[0112]
Для перорального введения, фармацевтическую композицию готовят в любой обычно используемой дозированной форме, такой как твердый препарат для внутреннего применения (например, таблетка, порошок, гранула, капсула, пилюля или пленка) или жидкий препарат для внутреннего применения (например, суспензия, эмульсия, эликсир, сироп, лимонад, спиртовой препарат, ароматический водный препарат, экстракт, отвар, настойка и т.д.) и вводят. Таблетка может представлять собой драже, таблетку с пленочным покрытием, таблетку с энтеросолюбильным покрытием, таблетку с замедленным высвобождением, пастилку, подъязычную таблетку, буккальную таблетку, жевательную таблетку или таблетку, распадающуюся во рту; порошковый препарат и гранулированный препарат могут представлять собой сухие сиропы; и капсула может быть мягкой капсулой, микрокапсулой или капсулой с замедленным высвобождением.
[0113]
Для парентерального введения, фармацевтическую композицию соответствующим образом вводят в любой дозированной форме, которая обычно используется, такой как препарат для инъекций, инфузия или препарат для наружного применения (например, глазные капли, назальные капли, ушные капли, аэрозоль, ингалятор, лосьон, пропитывающее средство, мазь, средство для полоскания горла, клизма, мазь, пластырь, желе, крем, пластырь, припарка, порошкообразный препарат для наружного применения или суппозиторий). Препарат для инъекций может представлять собой эмульсию типа М/В, В/М, М/В/М или В/М/В, или подобные.
[0114]
Фармацевтическую композицию можно получить путем смешивания эффективного количества соединения по настоящему изобретению с различными фармацевтическими добавками, подходящими для дозированной формы, такими как эксципиент, связующий агент, разрыхлитель и смазывающий агент, если это необходимо. Кроме того, фармацевтическую композицию можно превратить в фармацевтическую композицию для применения у ребенка, пожилого человека, пациента с серьезным заболеванием или хирургической операцией путем соответствующего изменения эффективного количества соединения по настоящему изобретению, дозированной формы и/или различных фармацевтических добавок. Например, фармацевтическая композиция для применения у ребенка может быть введена новорожденному (менее 4 недель после рождения), младенцу (от 4 недель после рождения до 1 года), ребенку дошкольного возраста (от 1 года до 7 лет), ребенку (от 7 лет до менее 15 лет) или пациенту в возрасте от 15 до 18 лет. Например, фармацевтическая композиция для пожилых людей может быть введена пациенту в возрасте 65 лет или старше.
[0115]
Желательно устанавливать вводимое количество фармацевтической композиции по настоящему изобретению с учетом возраста и массы тела пациента, типа и степени заболевания, пути введения и подобных; однако в случае перорального введения, доза обычно составляет от 0,05 до 100 мг/кг/день и предпочтительно находится в диапазоне от 0,1 до 10 мг/кг/день. В случае парентерального введения, вводимое количество может сильно варьироваться в зависимости от пути введения; однако вводимое количество обычно составляет от 0,005 до 10 мг/кг/день и предпочтительно, находится в диапазоне от 0,01 до 1 мг/кг/день. Его можно вводить один раз в день или несколько раз в день.
[0116]
Соединение по настоящему изобретению можно использовать в комбинации с ингибиторами L-белка, ингибиторами F-белка, ингибиторами фермента N-белка и т.д. (далее именуемыми как сопутствующее лекарственное средство) с целью усиления действия соединения, уменьшения вводимого количества соединения или подобного. При этом время введения соединения по настоящему изобретению и сопутствующего лекарственного средства не ограничено, и их можно вводить одновременно в мишень введения, или можно вводить с разницей во времени. Кроме того, соединение по настоящему изобретению и сопутствующее лекарственное средство можно вводить в виде двух или нескольких видов препаратов, каждый из которых включает активные ингредиенты, или можно вводить в виде одного препарата, включающего эти активные ингредиенты.
[0117]
Количество вводимого сопутствующего лекарственного средства может быть соответствующим образом выбрано на основе клинически используемой дозы. Кроме того, соотношение смеси соединения по настоящему изобретению и сопутствующего лекарственного средства может быть надлежащим образом выбрано в соответствии с целью введения, путем введения, заболеванием-мишенью, симптомами, комбинацией и подобными. Например, когда мишенью введения является человек, можно использовать от 0,01 до 100 массовых частей сопутствующего лекарственного средства на 1 массовую часть соединения по настоящему изобретению.
ПРИМЕРЫ
[0118]
Далее настоящее изобретение будет описано более подробно ч помощью Примеров, Эталонных примеров и Экспериментальных примеров; однако, настоящее изобретение не предназначено для ограничения ими.
[0119]
Используемые в настоящем документе сокращения имеют следующие значения.
Boc2O: ди-трет-бутилдикарбонат
ДИАД: диизопропилазодикарбоксилат
DMEAD: бис(2-метоксиэтил)азодикарбоксилат
ДМАП: 4-диметиламинопиридин
ГАТУ: гексафторфосфат O-(7азабензотриазол-1-ил)-1,1,3,3-тетраметилурония
Me4tBuXphos: 2-ди-трет-бутилфосфино-3,4,5,6-тетраметил-2',4',6'-триизопропил-1,1'-бифенил
TolBINAP: 2,2'-бис(ди-п-толилфосфино)-1,1'-бинафтил
Ts: тозил
Pd2(dba)3: трис(дибензилиденацетон)биспалладий
PdCl2(dppf): аддукт дихлорида 1,1'-бис(дифенилфосфино)ферроцен]палладия(II) и дихлорметана
Pd(PPh3)4: тетракис(трифенилфосфин)палладий
Xantphos Pd G3: метансульфонат [(4,5-бис(дифенилфосфино)-9,9-диметилксантен)-2-(2'-амино-1,1'-бифенил)]палладия(II)
Xantphos Pd G2: хлор[(4,5-бис(дифенилосфино)-9,9-диметилксантен)-2-(2'-амино-1,1'-бифенил)]палладий(II)
X-Phos: 2,4,6-триизопропил-2'-(дициклогексилфосфино)бифенил
[0120]
(Способ идентификации соединения)
ЯМР анализ, полученный в каждом Примере, проводят при 400 MГц, и измерение проводят с применением ДМСО-d6 и CDCl3. Кроме того, когда данные ЯМР показаны, существуют случаи, при которых все измеренные пики не описаны.
Термин ВУ в спецификации означает время удержания при ЖХ/МС: анализе жидкостной хроматографии/массы, и время удержания измеряют в следующих условиях.
(Способ 1)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты.
Градиент: Линейный градиент 5% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 2)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-400 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты.
Градиент: Линейный градиент 5% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 3)
Колонка: Shim-pack XR-ODS (2,2 мкм, в.д. 50×3,0 мм) (Shimadzu)
Скорость потока: 1,6 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-800 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты
Градиент: Линейный градиент 10% - 100% растворитель [B] проводят в течение 3 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 4)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 210-500 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты
Градиент: Линейный градиент 5% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 5)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] 10 мМ водный раствор, содержащий карбонат аммония, и [B] ацетонитрил
Градиент: Линейный градиент 5% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 6)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-400 нм)
Подвижная фаза: [A] 10 мМ водный раствор, содержащий карбонат аммония, и [B] ацетонитрил
Градиент: Линейный градиент 5% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 7)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты
Градиент: Линейный градиент 70% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 8)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,8 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] 10 мМ водный раствор, содержащий карбонат аммония, и [B] ацетонитрил
Градиент: Линейный градиент 50% - 100% растворитель [B] проводят в течение 3,5 минут, и затем 100% растворитель [B] сохраняют в течение 0,5 минут.
(Способ 9)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,6 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты
Градиент: Линейный градиент 25% - 95% растворитель [B] проводят в течение 1,5 минут, и затем 95% растворитель [B] сохраняют в течение 1,5 минут.
(Способ 10)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) BEH C18 (1,7 мкм) в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,6 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты
Градиент: Линейный градиент 25% - 95% растворитель [B] проводят в течение 1,5 минут, и затем 95% растворитель [B] сохраняют в течение 1,5 минут.
(Способ 11)
Колонка: ACQUITY UPLC (зарегистрированная торговая марка) CSH C18 (1,7 мкм в.д. 2,1×50 мм) (Waters)
Скорость потока: 0,6 мл/мин
Длина волны определения УФ: 254 нм (интервал определения 190-500 нм)
Подвижная фаза: [A] водный раствор, содержащий 0,1% муравьиной кислоты, и [B] ацетонитрильный раствор, содержащий 0,1% муравьиной кислоты
Градиент: Линейный градиент 25% - 95% растворитель [B] проводят в течение 1,5 минут, и затем 95% растворитель [B] сохраняют в течение 1,5 минут.
В описании, указание МС (m/z) означает значение, наблюдаемое при масс-спектрометрии.
[0121]
Пример 1
Синтез Соединения (I-023)
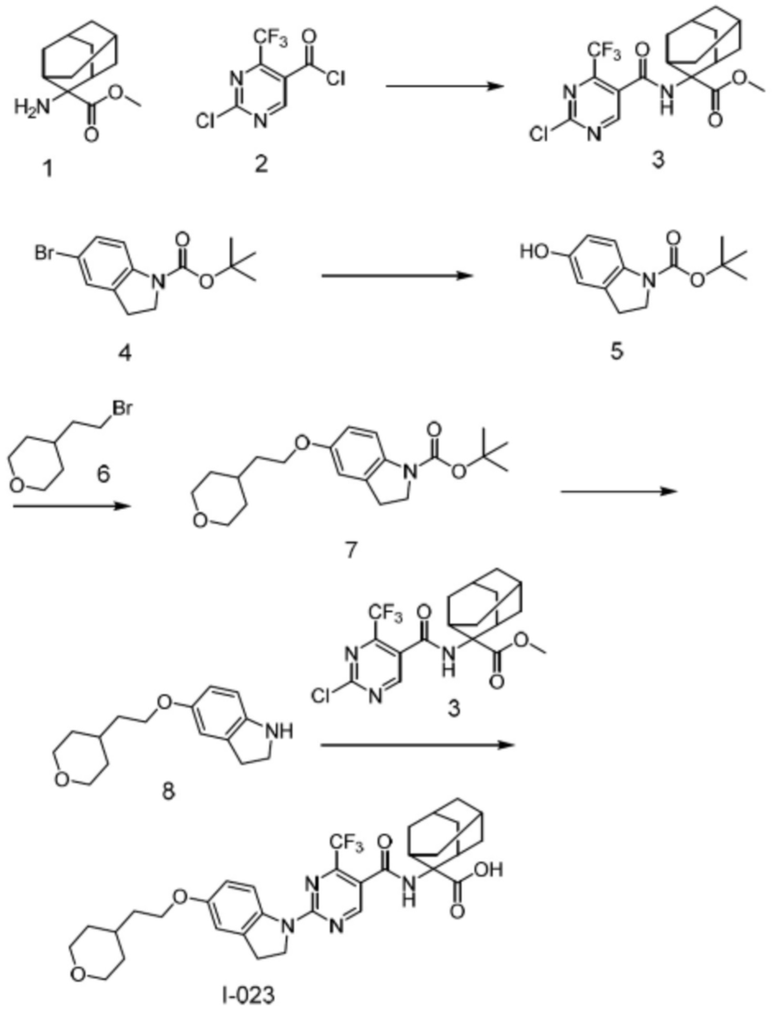
Стадия 1: Синтез Соединения 3
К Соединению 1 (910 мг, 3,62 ммоль) добавляют хлороформ (20 мл) и диизопропилэтиламин (0,76 мл, 4,34 ммоль), и затем Соединение 2 (887 мг, 3,62 ммоль) при охлаждении льдом. Смесь нагревают до комнатной температуры и перемешивают в течение 2 часов, и затем добавляют воду. Смесь экстрагируют хлороформом, и два слоя разделяют. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток добавляют с этилацетатом-гексаном. Твердое вещество фильтруют с получением Соединения 3 (1,34 г, выход 81%).
1H-ЯМР (CDCl3) δ: 1,75-1,82 (м, 6H), 1,87-1,97 (м, 4H), 2,15 (м, 2H), 2,60 (с, 2H), 3,78 (с, 3H), 6,00 (с, 1H), 8,98 (с, 1H).
[0122]
Стадия 2: Синтез Соединения 5
К Соединению 4 (22,6 г, 76 ммоль) добавляют 1,4-диоксан (158 мл), бис(пинаколато)дибор (25 г, 98 ммоль), PdCl2(dppf) (6,2 г, 7,6 ммоль) и ацетат калия (11,1 г, 1 14 ммоль), и смесь перемешивают при 100°C. Через 3 часов, смесь охлаждают до комнатной температуры и фильтруют через Целит (зарегистрированная торговая марка). Фильтрат концентрируют при пониженном давлении, и в остаток добавляют диизопропиловый эфир для осаждения твердого вещества. Выпавшее в осадок твердое вещество удаляют фильтрацией, и фильтрат концентрируют при пониженном давлении.
Концентрированный остаток растворяют в тетрагидрофуране (226 мл) и смешивают с 1 моль/л водного раствора гидроксида натрия (114 мл, 114 ммоль), и добавляют 30% водного раствора перекиси водорода (11,6 мл, 114 ммоль). После перемешивания при комнатной температуре в течение 1 часа, реакцию гасят добавлением водного тиосульфата натрия. Два слоя разделяют экстракцией с этилацетатом, и органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 5 (7,7 г, выход 43%).
1H-ЯМР (CDCl3) δ: 1,57 (с, 9H), 3,04 (т, J=8,8Гц, 2H), 3,96 (м, 2H), 4,58 (с, 1H), 6,61 (д, J=8,8Гц, 1H), 6,64 (с, 1H), 7,34 (шс, 0,4H), 7,73 (шс, 0,6H).
[0123]
Стадия 3: Синтез Соединения 7
К Соединению 5 (2,5 г, 10,6 ммоль) добавляют диметилформамид (25 мл), Соединение 6 (3,08 г, 15,9 ммоль) и карбонат калия (2,94 г, 21,3 ммоль), и смесь перемешивают при 60°C в течение 5 часов. Реакционный раствор добавляют с водой и экстрагируют этилацетатом. Два слоя разделяют, и органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 7 (2,55 г, выход 69%).
1H-ЯМР (CDCl3) δ: 1,35 (м, 2H), 1,57 (с, 9H), 1,60-1,82 (м, 5H), 3,05 (т, J=8,8Гц, 2H), 3,40 (тд, J=12,0, 1,6Гц, 2H), 3,90-4,00 (м, 6H), 6,68 (д, J=8,8Гц, 1H), 6,72 (с, 1H), 7,34 (шс, 0,4H), 7,73 (шс, 0,6H).
[0124]
Стадия 4: Синтез Соединения 8
К Соединению 7 (2,55 г, 7,34 ммоль) добавляют дихлорметан (20 мл) и трифторуксусную кислоту (10 мл, 130ммоль). После перемешивания при комнатной температуре в течение 1 часа, водный раствор бикарбоната натрия добавляют для нейтрализации смеси. Два слоя разделяют экстракцией с хлороформом, и органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении с получением Соединения 8 (1,95 г) в виде неочищенного продукта.
1H-ЯМР (CDCl3) δ: 1,35 (м, 2H), 1,61-1,84 (м, 5H), 2,78 (шс, 1H), 3,01 (т, J=8,4Гц, 2H), 3,40 (тд, J=12,0, 1,6Гц, 2H), 3,54 (т, J=8,4Гц, 2H), 3,91-4,00 (м, 4H), 6,57-6,61 (м, 2H), 6,76 (с, 1H).
[0125]
Стадия 5: Синтез Соединения (I-023)
К Соединению 8 (107 мг, 0,43 ммоль) добавляют 1,4-диоксан (3 мл), триэтиламин (0,149 мл, 1,08 ммоль) и Соединение 3 (150 мг, 0,36 ммоль), и смесь перемешивают при 50°C в течение 2 часов. Смесь добавляют с водой и экстрагируют хлороформом. Органический слой промывают водой, сушат над безводным сульфатом магния, и растворитель удаляют при пониженном давлении.
К остатку добавляют тетрагидрофуран (2 мл), этанол (2 мл) и 4 моль/л водный раствор гидроксида лития (0,90 мл, 3,6 ммоль). Смесь перемешивают при 90°C в течение 8 часов и добавляют 10% водный раствор лимонной кислоты. Смесь экстрагируют хлороформ, и два слоя разделяют. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения (I-023) (90 мг, выход 41%).
1H-ЯМР (ДМСО-d6) δ: 1,22 (м, 2H), 1,53-1,72 (м, 11H), 1,80 (шс, 2H), 2,03-2,16 (м, 4H), 2,54 (с, 2H), 3,19 (т, J=8,4Гц, 2H), 3,28 (м, 2H), 3,83 (дд, J=11,2, 0,8Гц, 2H), 4,00 (т, J=6,4Гц, 2H), 4,21 (т, J=8,4Гц, 2H), 6,82 (дд, J=8,8, 1,2Гц, 1H), 6,94 (д, J=1,2Гц, 1H), 8,16 (д, J=8,8Гц, 1H), 8,46 (с, 1H), 8,67 (с, 1H), 12,3 (с, 1H).
[0126]
Пример 2
Синтез Соединения (I-033)
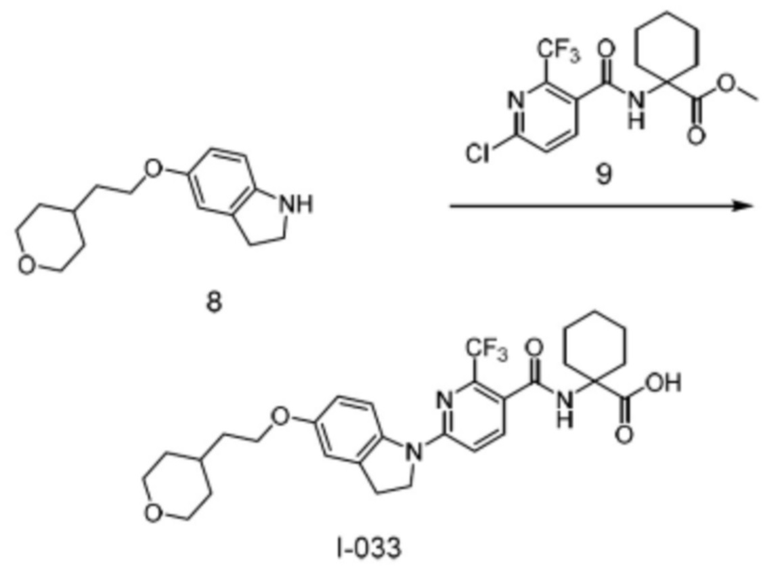
Стадия 1: Синтез Соединения (I-033)
Соединение 8 (41 мг, 0,16 ммоль) и Соединение 9 (40 мг, 0,11 ммоль), которое синтезируют по той же методике, что и Соединение 3, растворяют в 1,4-диоксане (0,5 мл), и добавляют Xantphos Pd G3 (10 мг, 0,01 ммоль) и карбонат калия (38 мг, 0,27 ммоль). После перемешивания при 100°C в течение 3 часов, добавляют воду. Смесь экстрагируют хлороформом, и органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении.
К остатку добавляют этанол (0,5 мл) и тетрагидрофуран (0,5 мл) для растворения, и добавляют 4 моль/л водный раствор гидроксида лития (0,27 мл). Смесь перемешивают при 50°C в течение 4 часов. Добавляют водный раствор лимонной кислоты, и смесь экстрагируют хлороформом. Органический слой промывают водой, сушат над безводным сульфатом магния, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения (I-033) (20 мг, выход 33%).
1H-ЯМР (ДМСО-d6) δ: 1,15-1,30 (м, 3H), 1,50-1,78 (м, 12H), 2,03-2,10 (м, 2H), 3,22 (м, 2H), 3,29 (м, 2H), 3,83 (дд, J= 10,8, 3,2Гц, 2H), 3,98 (т, J=6,4Гц, 2H), 4,06 (т, J=8,0Гц, 2H), 6,77 (дд, J=8,8, 3,5Гц, 1H), 6,89 (с, 1H), 7,06 (д, J=8,8Гц, 1H), 7,72 (д, J=8,8Гц, 1H), 8,24 (д, J=8,8Гц, 1H), 8,44 (с, 1H), 12,2 (с, 1H).
[0127]
Пример 3
Синтез Соединения (I-082)
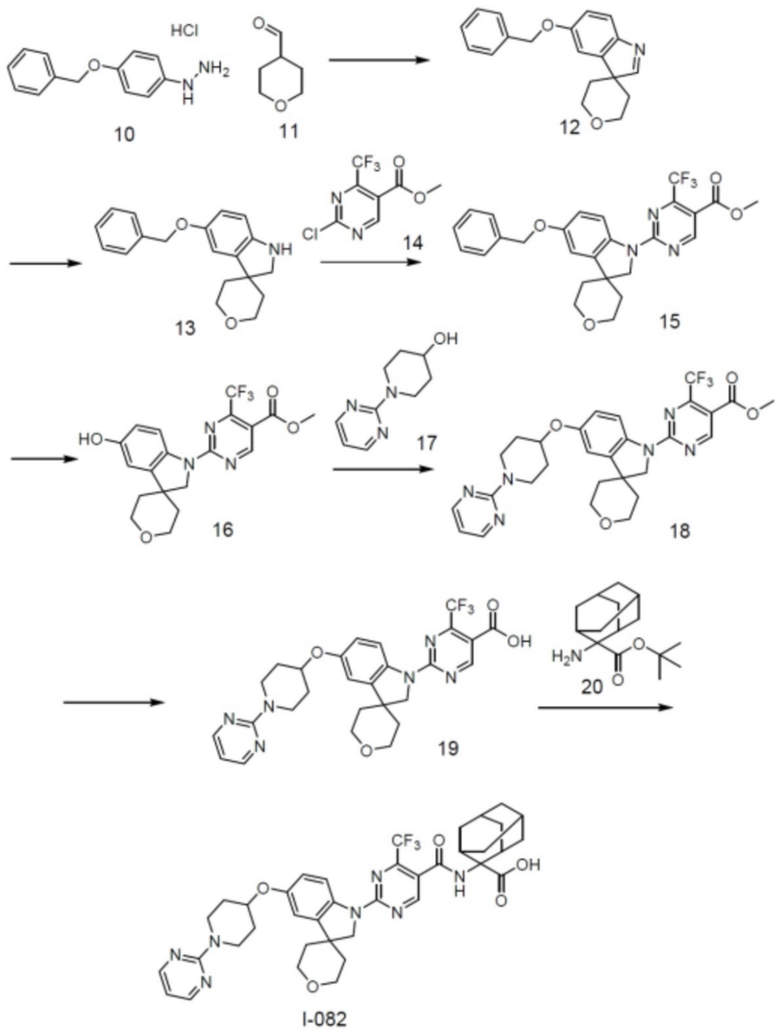
Стадия 1: Синтез Соединения 12
Соединение 10 (31 г, 124 ммоль) и Соединение 11 (16,9 г, 148 ммоль) суспендируют в дихлорметане (600 мл) и охлаждают на ледяной бане. Добавляют трифторуксусную кислоту (19 мл, 247 ммоль). Через 30 минут, смесь нагревают до 45°C, и перемешивают в течение 3 часов. В смесь добавляют водный раствор карбоната натрия для нейтрализации при охлаждении на льду и фильтруют через Целит (зарегистрированная торговая марка). Два слоя фильтрата разделяют, и органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и диэтиловый эфир добавляют к остатку. Твердое вещество фильтруют с получением Соединения 12 (9,04 г, выход 25%).
1H-ЯМР (CDCl3) δ: 1,63 (м, 2H), 1,93 (ддд, J=13,6, 10,0, 4,0Гц, 2H), 3,90 (м, 2H), 4,10 (м, 2H), 5,10 (с, 2H), 6,97 (дд, J=8,4, 2,4Гц, 1H), 7,06 (д, J=2,4Гц, 1H), 7,34 (м, 1H), 7,40 (м, 2H), 7,45 (м, 2H), 7,56 (д, J=8,4Гц, 1H), 8,32 (с, 1H).
ЖХ/МС(ИЭР):m/z= 294 [M+H]+, ВУ=1,96 мин, ЖХ/МС Способ 1
[0128]
Стадия 2: Синтез Соединения 13
Соединение 12 (18 г, 61,4 ммоль) суспендируют в метаноле (180 мл), и боргидрид натрия (2,55 г, 67,5 ммоль) добавляют при охлаждении на льду. Через 10 минут, смесь нагревают до комнатной температуры, и перемешивают в течение 2 часов. водный хлорид аммония добавляют при охлаждении льдом, и смесь экстрагируют хлороформом. Органический слой промывают водой и сушат над безводным сульфатом магния. В остаток добавляют диизопропиловый эфир и растворитель удаляют при пониженном давлении. Твердое вещество фильтруют с получением Соединения 13 (16,1 г, выход 89%).
1H-ЯМР (CDCl3) δ: 1,65 (д, J=13,6Гц, 2H), 1,94 (м, 2H), 3,52 (м, 2H), 3,55 (м, 2H), 3,96 (м, 2H), 4,99 (с, 2H), 6,59 (д, J=8,4Гц, 1H), 6,70 (д, J=8,4, 2,4Гц, 1H), 6,79 (д, J=2,4Гц, 1H), 7,26 (с, 1H), 7,31 (м, 1H), 7,38 (м, 2H), 7,43 (м, 2H).
ЖХ/МС(ИЭР):m/z= 296 [M+H]+, ВУ=1,67 мин, ЖХ/МС Способ 1
[0129]
Стадия 3: Синтез Соединения 15
Соединение 13 (16,1 г, 54,5 ммоль) растворяют в 1,4-диоксане (242 мл) и добавляют триэтиламин (17,4 мл, 125 ммоль) и Соединение 14 (14,4 г, 60 ммоль), и смесь перемешивают при 50°C в течение 3 часов. После охлаждения, добавляют воду и смесь экстрагируют хлороформ. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и этилацетат-гексан добавляют к остатку. Твердое вещество фильтруют с получением Соединения 15 (25,3 г, выход 93%).
1H-ЯМР (ДМСО-d6) δ: 1,58 (м, 2H), 1,98 (м, 2H), 3,52 (м, 2H), 3,86 (с, 3H), 3,90 (м, 2H), 4,27 (м, 2H), 5,12 (с, 2H), 6,98 (м, 1H), 7,13 (д, J=2,4Гц, 1H), 7,34 (м, 1H), 7,40 (м, 2H), 7,47 (м, 2H), 8,21 (м, 1H), 9,11 (с, 1H).
ЖХ/МС(ИЭР):m/z= 500 [M+H]+, ВУ=3,10 мин, ЖХ/МС Способ 1
[0130]
Стадия 4: Синтез Соединения 16
К Соединению 15 (25,3 г, 50,7 ммоль) добавляют хлороформ (253 мл) и тетрагидрофуран (127 мл) для растворения, и добавляют 5% масс. гидроксид палладия (5 г, 1,78 ммоль). Смесь перемешивают в течение 2 часов при комнатной температуре в атмосфере водорода. Смесь фильтруют через Целит (зарегистрированная торговая марка), и фильтрат концентрируют при пониженном давлении. Этилацетат-гексан добавляют к остатку, и твердое вещество фильтруют с получением Соединения 16 (19,6 г, выход 95%).
1H-ЯМР (ДМСО-d6) δ: 1,58 (м, 2H), 1,88 (м, 2H), 3,52 (м, 2H), 3,86 (с, 3H), 3,89 (м, 2H), 4,24 (м, 2H), 6,71 (дд, J=8,8, 2,4Гц, 1H), 6,76 (д, J=2,4Гц, 1H), 8,13 (м, 1H), 9,09 (с, 1H), 9,42 (с, 1H).
ЖХ/МС(ИЭР):m/z= 410 [M+H]+, ВУ=2,20 мин, ЖХ/МС Способ 1
[0131]
Стадия 5: Синтез Соединения 18
Соединение 16 (16,1 г, 39,3 ммоль), Соединение 17 (10,6 г, 59,0 ммоль), трифенилфосфин (16,5 г, 62,9 ммоль) растворяют в тетрагидрофуране (217 мл) и охлаждают на ледяной бане, и ДИАД (11,47 мл, 59,0 ммоль) добавляют по каплям. После добавления, смесь нагревают до 40°C, и перемешивают в течение 2 часов. Реакционную смесь оставляют охлаждаться до комнатной температуры и концентрируют при пониженном давлении. Добавляют этилацетат-диизопропиловый эфир, и твердое вещество фильтруют с получением Соединения 18 (20,3 г, выход 91%).
1H-ЯМР (ДМСО-d6) δ: 1,52-1,63 (м, 4H), 1,97-2,05 (м, 4H), 3,46-3,58 (м, 4H), 3,87 (с, 3H), 3,90 (м, 2H), 4,20-4,28 (м, 4H), 4,69 (м, 1H), 6,61 (т, J=4,8Гц, 1H), 6,96 (м, 1H), 7,11 (д, J=2,0Гц, 1H), 8,22 (м, 1H), 8,36 (д, J=4,8Гц, 2H), 9,12 (с, 1H).
ЖХ/МС(ИЭР):m/z= 571 [M+H]+, ВУ=2,95 мин, ЖХ/МС Способ 1
[0132]
Стадия 6: Синтез Соединения 19
К Соединению 18 (20,3 г, 35,6 ммоль) добавляют тетрагидрофуран (203 мл), этанол (203 мл) и 4 моль/л водный раствор гидроксида лития (44,5 мл, 178 ммоль). После перемешивания при 50°C в течение 4 часов, смесь оставляют охлаждаться до комнатной температуры, и добавляют 10% водный раствор лимонной кислоты. Добавляют воду, и выпавшее в осадок твердое вещество фильтруют с получением Соединения 19 (19 г, выход 96%).
1H-ЯМР (ДМСО-d6) δ: 1,52-1,61 (м, 4H), 1,97-2,05 (м, 4H), 3,46-3,57 (м, 4H), 3,90 (м, 2H), 4,24 (м, 2H), 4,26 (с, 2H), 4,69 (м, 1H), 6,61 (т, J=4,4Гц, 1H), 6,96 (дд, J=8,8, 2,8Гц, 1H), 7,10 (д, J=2,8Гц, 1H), 8,22 (д, J=8,8Гц, 1H), 8,36 (д, J=4,4Гц, 2H), 9,11 (с, 1H), 13,54 (с, 1H).
ЖХ/МС(ИЭР):m/z= 557 [M+H]+, ВУ=2,44 мин, ЖХ/МС Способ 1
[0133]
Стадия 7: Синтез Соединения (I-082)
К Соединению 19 (795 мг, 1,43 ммоль) добавляют диметилформамид (8 мл), Соединение 20 (431 мг, 1,71 ммоль), ГАТУ (706 мг, 1,86 ммоль) и триэтиламин (0,495 мл, 3,57 ммоль) при комнатной температуре. Смесь перемешивают в течение 2 часов. Добавляют воду к реакционному раствору, и выпавшее в осадок твердое вещество фильтруют. К твердому веществу добавляют дихлорметан (5 мл) и трифторуксусную кислоту (5 мл, 65 ммоль), и смесь перемешивают при комнатной температуре в течение 2 часов. Водный бикарбонат натрия добавляют для нейтрализации смеси, и затем 10% водный раствор лимонной кислоты добавляют для обратного подкисления, и смесь экстрагируют хлороформом. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения (I-082) (820 мг, выход 78%).
1H-ЯМР (ДМСО-d6) δ: 1,52-1,60 (м, 6H), 1,65-1,69 (м, 4H), 1,80 (м, 2H), 1,94-2,17 (м, 8H), 2,54 (шс, 2H), 3,46-3,58 (м, 4H), 3,90 (м, 2H), 4,22 (с, 2H), 4,26 (м, 2H), 4,67 (м, 1H), 6,61 (т, J=4,4Гц, 1H), 6,93 (дд, J=8,8, 2,0Гц, 1H), 7,08 (д, J=2,0Гц, 1H), 8,17 (д, J=8,8Гц, 1H), 8,36 (д, J=4,4Гц, 2H), 8,46 (s 1H), 8,68 (с, 1H), 12,34 (с, 1H).
[0134]
Пример 4
Синтез Соединения (I-148)
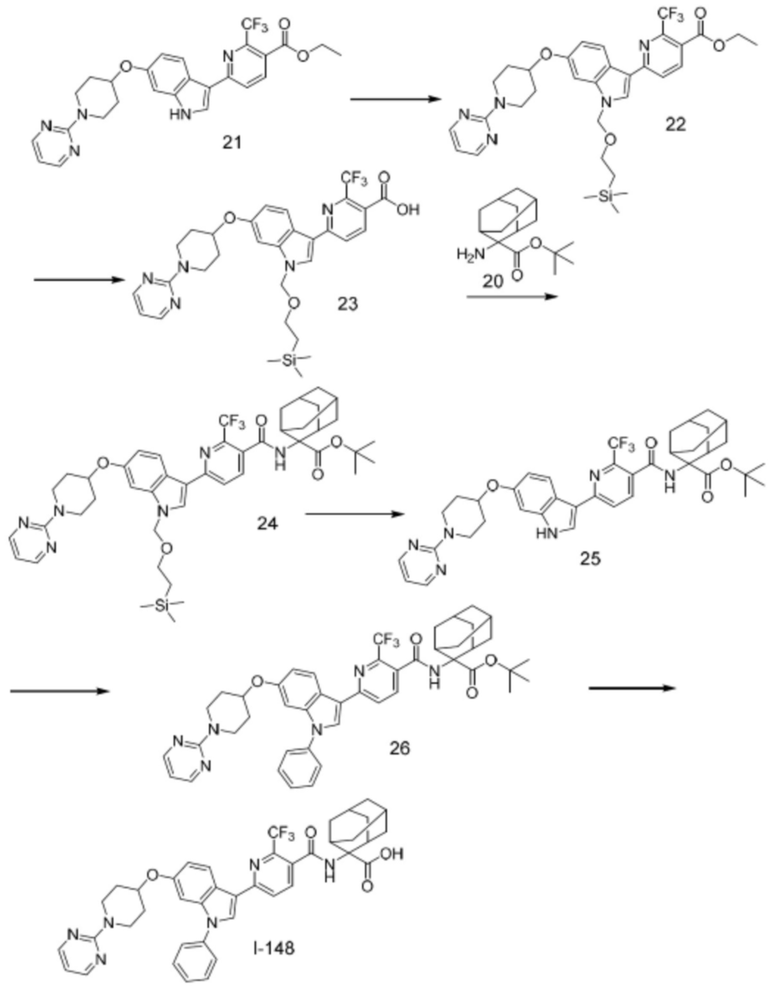
Стадия 1: Синтез Соединения 22
К раствору Соединения 21 (100 мг, 0,20 ммоль) (см. Пример 6 для способа синтеза) в диметилформамиде (1 мл) добавляют 60% масс. гидрид натрия (11 мг, 0,29 ммоль) и хлорид 2-(триметилсилил)этоксиметила (49 мг, 0,29 ммоль) при охлаждении на льду, и смесь перемешивают при комнатной температуре в течение 1,5 часов. Добавляют насыщенный водный раствор хлорида аммония, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 22 (74 мг, выход 59%).
ЖХ/МС(ИЭР):m/z= 642 [M+H]+, ВУ=1,182 мин, ЖХ/МС Способ 7
[0135]
Стадия 2: Синтез Соединения 23
К раствору Соединения 22 (74 мг, 0,12 ммоль) в этаноле (0,7 мл) добавляют 4 моль/л раствор гидроксида лития (0,28 мл, 1,16 ммоль), и смесь перемешивают при 50°C в течение 1 ч 40 мин. Добавляют 10% водный раствор лимонной кислоты, и смесь экстрагируют хлороформом. После сушки органического слоя с безводным сульфатом натрия, растворитель удаляют при пониженном давлении с получением Соединения 23 (73 мг) в виде неочищенного продукта.
ЖХ/МС(ИЭР):m/z= 614[M+H]+, ВУ= 3,04 мин, ЖХ/МС Способ 1
[0136]
Стадия 3: Синтез Соединения 24
Соединение 23 (71 мг, 0,12 ммоль) растворяют в диметилформамиде (1,0 мл), и добавляют Соединение 20 (30 мг, 0,12 ммоль), ГАТУ (52 мг, 0,14 ммоль) и триэтиламин (17 мг, 0,17 ммоль). После перемешивания при комнатной температуре в течение 17 часов, добавляют воду, и выпавшее в осадок твердое вещество фильтруют с получением Соединения 24 (93 мг, выход 96%).
ЖХ/МС(ИЭР):m/z= 847[M+H]+, ВУ=2,80 мин, ЖХ/МС Способ 7
[0137]
Стадия 4: Синтез Соединения 25
К раствору Соединения 24 (84 мг, 0,10 ммоль) в тетрагидрофуране (0,3 мл) добавляют 1 моль/л раствора фторида тетрабутиламмония-тетрагидрофурана (0,50 мл, 0,50 ммоль) и этилендиамина (89 мг, 1,50 ммоль), и смесь перемешивают при нагревании при кипении с обратным холодильником в течение 8 часов. Добавляют 10% водный раствор хлорида аммония, и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 25 (70 мг, выход 99%).
ЖХ/МС(ИЭР):m/z= 717[M+H]+, ВУ=1,42 мин, ЖХ/МС Способ 1
[0138]
Стадия 5: Синтез Соединения 26
К Соединению 25 (460 мг, 0,64 ммоль) добавляют 1,4-диоксан (6,9 мл), (1R,2R)-циклогексан-1,2-диамин (22 мг, 0,19 ммоль), трикалийфосфат (272 мг, 1,28 ммоль), йодбензол (236 мг, 1,16 ммоль) и йодид меди(I) (12 мг, 0,06 ммоль), и смесь перемешивают при нагревании при кипении с обратным холодильником в течение 8 часов. Добавляют воду, и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 26 (500 мг, выход 98%).
ЖХ/МС(ИЭР):m/z= 793[M+H]+, ВУ=3,71 мин, ЖХ/МС Способ 1
[0139]
Стадия 6: Синтез Соединения (I-148)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
1H-ЯМР (ДМСО-d6) δ: 1,66-1,71 (м, 10H), 2,00-2,13 (м, 6H), 2,59 (с, 2H), 3,53-3,57 (м, 2H), 4,16 (дд, J=13,0, 6,4, 3,9 Гц, 2H), 4,66-4,72 (м, 1H), 6,60 (т, J=4,8 Гц, 1H), 7,07-7,10 (м, 2H), 7,49 (т, J=7,3 Гц, 1H), 7,64-7,66 (м, 2H), 7,70-7,72 (м, 2H), 7,80 (д, J=8,3 Гц, 1H), 8,25 (д, J=8,3 Гц, 1H), 8,35 (д, J=4,8 Гц, 2H), 8,53-8,54 (м, 3H), 12,32 (с, 1H).
[0140]
Пример 5
Синтез Соединения (I-159) и Соединения (I-182)
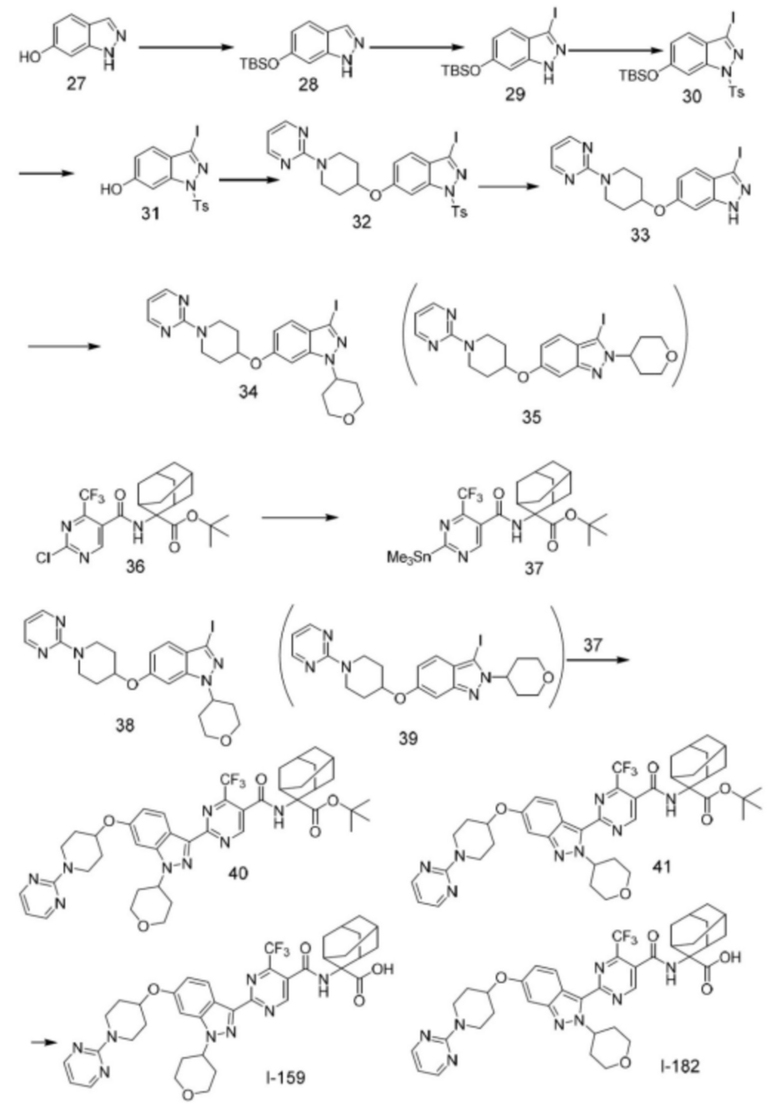
Стадия 1: Синтез Соединения 28
К раствору Соединения 27 (2,01 г, 15,00 ммоль) в диметилформамиде (20,1 мл) добавляют имидазол (1,53 г, 22,50 ммоль) и трет-бутилдиметилсилилхлорид (2,71 г, 18,00 ммоль), и смесь перемешивают при комнатной температуре в течение 40 минут. Добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 28 (3,79 г, выход 100%).
ЖХ/МС(ИЭР):m/z= 249 [M+H]+, ВУ=2,66 мин, ЖХ/МС Способ 1
[0141]
Стадия 2: Синтез Соединения 29
К раствору Соединения 28 (3,73 г, 15,00 ммоль) в тетрагидрофуране (74,5 мл) добавляют трет-бутоксид калия (3,87 г, 34,50 ммоль) и йод (8,76 г, 34,50 ммоль) при охлаждении льдом, и смесь перемешивают в течение 1 часа при охлаждении льдом. Добавляют 20% водный раствор тиосульфата натрия, смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении с получением Соединения 29 (5,42 г) в виде неочищенного продукта.
ЖХ/МС(ИЭР):m/z= 375 [M+H]+, ВУ= 3,09 мин, ЖХ/МС Способ 1
[0142]
Стадия 3: Синтез Соединения 30
К раствору Соединения 29 (5,42 г, 14,48 ммоль) в дихлорметане (54,2 мл) добавляют триэтиламин (2,49 г, 24,61 ммоль) и п-толуолсульфонилхлорид (2,49 г, 17,37 ммоль) при охлаждении льдом. Смесь перемешивают при комнатной температуре в течение 18 часов и отфильтровывают нерастворимый продукт. Фильтрат концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 30 (6,48 г, выход 82%).
ЖХ/МС(ИЭР):m/z= 529 [M+H]+, ВУ= 3,67 мин, ЖХ/МС Способ 1
[0143]
Стадия 4: Синтез Соединения 31
К раствору Соединения 30 (6,39 г, 12,09 ммоль) в тетрагидрофуране (31,9 мл) добавляют 1 моль/л раствора фторида тетрабутиламмония-тетрагидрофурана (13,3 мл, 13,3 ммоль) при охлаждении на льду, и смесь перемешивают при комнатной температуре в течение 30 минут. Добавляют 0,4 моль/л хлористоводородной кислоты, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат), и отверждают гексаном-этилацетатом с получением Соединения 31 (2,87 г, выход 57%).
ЖХ/МС(ИЭР):m/z= 415 [M+H]+, ВУ=2,30 мин, ЖХ/МС Способ 1
[0144]
Стадия 5: Синтез Соединения 32
Соединение синтезируют по методике, описанной на Стадии 3 Примера 6.
ЖХ/МС(ИЭР):m/z= 576 [M+H]+, ВУ=3,03 мин, ЖХ/МС Способ 1
[0145]
Стадия 6: Синтез Соединения 33
К Соединению 32 (6,09 г, 10,58 ммоль) добавляют этанол (122 мл), воду (146 мл) и 8 моль/л водного раствора гидроксида натрия (6,61 мл, 52,90 мл), и смесь перемешивают при 80°C в течение 80 минут. Органический растворитель удаляют при пониженном давлении, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток суспендируют в хлороформе, и твердое вещество отфильтровывают с получением Соединения 33 (2,93 г, выход 66%).
ЖХ/МС(ИЭР):m/z= 422 [M+H]+, ВУ=2,21 мин, ЖХ/МС Способ 1
[0146]
Стадия 7: Синтез Соединения 34 и Соединения 35
Соединение 33 (3,45 г, 8,19 ммоль) растворяют в диметилформамиде (34,5 мл), и добавляют карбонат цезия (5,33 г, 16,36 ммоль) и метансульфонат тетрагидро-2H-пиран-4-ила (681 мг, 16,36 ммоль), и смесь перемешивают при 80°C в течение 6 часов. Добавляют воду, и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 34 и Соединения 35 в виде примерно 4:1 смеси (4,20 г, выход 100%).
Соединение 34
ЖХ/МС(ИЭР):m/z= 506[M+H]+, ВУ=2,65 мин, ЖХ/МС Способ 1
Соединение 35
ЖХ/МС(ИЭР):m/z= 506[M+H]+, ВУ=2,39 мин, ЖХ/МС Способ 1
[0147]
Стадия 8: Синтез Соединения 37
Соединение 36 (2,00 г, 4,35 ммоль), которое синтезируют по той же методике, что и Соединение 3, суспендируют в толуоле (40 мл) и 1,1,1,2,2,2-гексаметилдистаннане (2,00 г, 4,35 ммоль) и Pd(PPh3)4 (0,75 г, 0,65 ммоль), и смесь перемешивают при нагревании при кипении с обратным холодильником в течение 1 часа. Добавляют воду, и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 37 (1,74 г, выход 68%).
ЖХ/МС(ИЭР):m/z= 590 [M+H]+, ВУ=3,34 мин, ЖХ/МС Способ 1
[0148]
Стадия 9: Синтез Соединения 40 и Соединения 41
4:1 смесь Соединения 38 и Соединения 39 (1,01 г, 2,00 ммоль) растворяют в диметилформамиде (20 мл), и добавляют Соединение 37 (1,74 г, 2,96 ммоль) и Pd(PPh3)4 (0,35 г, 0,30 ммоль), хлорид лития (0,17 г, 4,00 ммоль) и йодид меди(I) (38 мг, 0,20 ммоль), и смесь перемешивают при 95°C в течение 8,5 часов. Добавляют воду, и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 40 (505 мг, выход 31%) и Соединения 41 (120 мг, выход 8%).
Соединение 40.
ЖХ/МС(ИЭР):m/z= 803[M+H]+, ВУ=3,43 мин, ЖХ/МС Способ 1
Соединение 41
ЖХ/МС(ИЭР):m/z= 803[M+H]+, ВУ=3,50 мин, ЖХ/МС Способ 1
[0149]
Стадия 10: Синтез Соединения (I-159) и соединение (I-182)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
Соединение (I-159)
1H-ЯМР (CDCl3) δ: 1,78-1,83 (м, 6H), 1,92-1,95 (м, 4H), 2,03-2,12 (м, 6H), 2,23 (д, J=12,4 Гц, 2H), 2,56 (ддд, J=24,8, 12,4, 4,3 Гц, 2H), 2,67 (с, 2H), 3,64 (т, J=12,4 Гц, 2H), 3,79-3,85 (м, 2H), 4,14-4,21 (м, 4H), 4,70-4,76 (м, 2H), 6,38 (с, 1H), 6,51 (т, J=4,8 Гц, 1H), 6,97 (д, J=1,8 Гц, 1H), 7,06 (дд, J=9,0, 1,8 Гц, 1H), 8,34 (д, J=4,8 Гц, 2H), 8,49 (д, J=9,0 Гц, 1H), 9,16 (с, 1H), 12,12 (с, 1H).
Соединение (I-182)
1H-ЯМР (CDCl3) δ: 1,79-2,26 (м, 18H), 2,50 (ддд, J=24,2, 11,5, 4,2 Гц, 2H), 2,68 (с, 2H), 3,60 (т, J=11,5 Гц, 2H), 3,68-3,74 (м, 2H), 4,15-4,26 (м, 4H), 4,64-4,69 (м, 1H), 5,95 (тт, J=11,5, 4,0 Гц, 1H), 6,30 (с, 1H), 6,49 (т, J=4,8 Гц, 1H), 7,01 (дд, J=9,2, 1,9 Гц, 1H), 7,17 (д, J=1,9 Гц, 1H), 8,32-8,33 (м, 3H) 9,15 (с, 1H), 12,12 (с, 1H).
[0150]
Пример 6
Синтез Соединения (I-162)
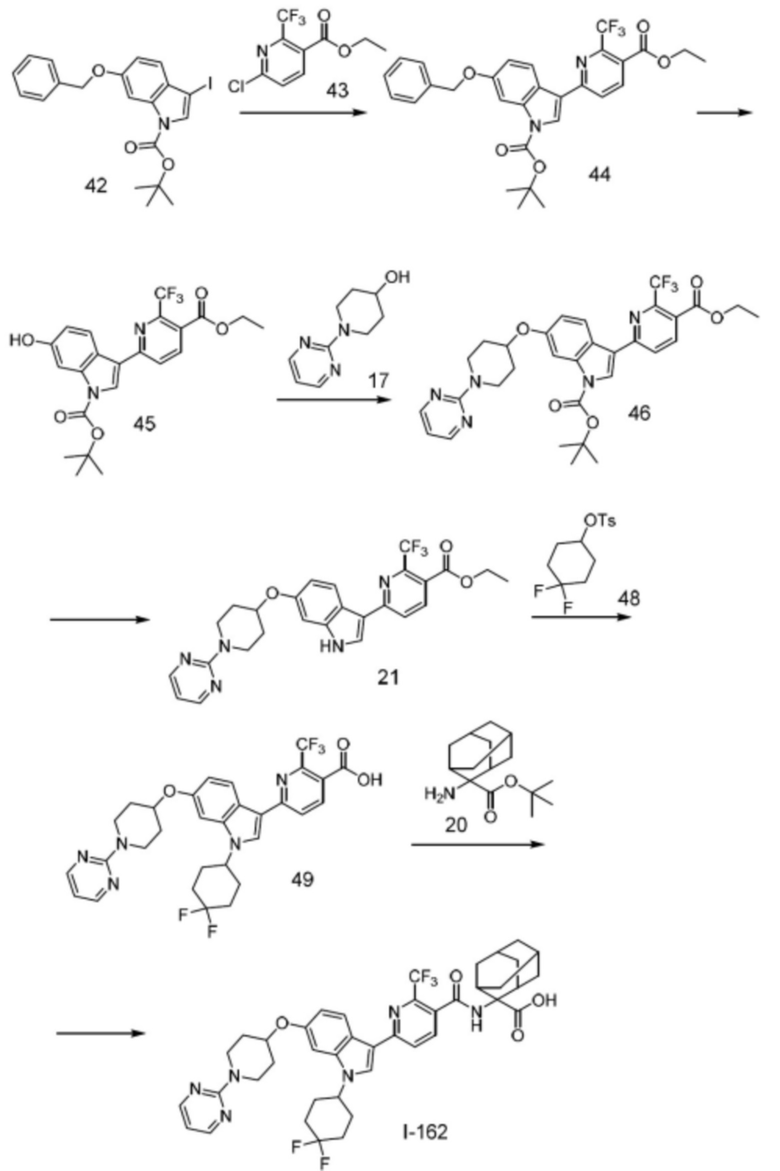
Стадия 1: Синтез Соединения 44
К Соединению 42 (10 г, 22,3 ммоль) добавляют тетрагидрофуран (100 мл) и триизопропилборат (4,19 г, 22,3 ммоль), и смесь охлаждают до -78°C сухим льдом-ацетоном. К раствору добавляют по каплям 1,59 моль/л раствор н-бутиллития-гексана (19,6 мл, 31,2 ммоль). Раствор перемешивают при -78°C в течение 20 минут. Реакцию гасят добавлением насыщенного водного раствора хлорида аммония, нагревают до комнатной температуры, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. К полученному остатку добавляют 1,4-диоксан (102 мл), Соединение 43 (6,2 г, 24,5 ммоль), PdCl2(dppf) (1,82 г, 2,23 ммоль) и 2,2 моль/л водный раствор карбоната калия (20,4 мл, 44,5 ммоль), и смесь перемешивают при 100°C в течение 2 часов. После охлаждения, добавляют воду, затем экстрагируют этилацетатом. Слои разделяют, и органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 44 (7,1 г, выход 59%).
1H-ЯМР (CDCl3) δ: 1,42 (т, J=7,2Гц, 3H), 1,70 (с, 9H), 4,44 (кв, J=7,2Гц, 2H), 5,17 (с, 2H), 7,10 (дд, J=8,8, 2,8Гц, 1H), 7,34 (м, 1H), 7,40 (м, 2H), 7,48 (м, 2H), 7,77-7,90 (м, 2H), 8,11-8,16 (м, 2H), 8,47 (д, J=8,8Гц, 1H).
ЖХ/МС(ИЭР):m/z= 541[M+H]+, ВУ=3,21 мин, ЖХ/МС Способ 1
[0151]
Стадия 2: Синтез Соединения 45
К Соединению 44 (30,7 г, 56,8 ммоль) добавляют тетрагидрофуран (307 мл) и 20% масс. палладий на активированном угле (6,34 г, 11,7 ммоль). Смесь перемешивают при комнатной температуре в атмосфере водорода в течение 2 часов. Смесь фильтруют с Целитом (зарегистрированная торговая марка), и фильтрат концентрируют при пониженном давлении. Этилацетат-гексан добавляют к остатку, и твердое вещество фильтруют с получением Соединения 45 (22,0 г, выход 86%).
1H-ЯМР (CDCl3) δ: 1,42 (т, J=7,2Гц, 3H), 1,71 (с, 9H), 4,44 (кв, J=7,2Гц, 2H), 4,94 (с, 1H), 6,93 (дд, J=8,8, 2,4Гц, 1H), 7,71 (шс, 1H), 7,88 (д, J=8,4Гц, 1H), 8,11 (с, 1H), 8,14 (д, J=8,4Гц, 1H), 8,46 (д, J=8,8Гц, 1H).
ЖХ/МС(ИЭР):m/z= 451 [M+H]+, ВУ=2,84 мин, ЖХ/МС Способ 1
[0152]
Стадия 3: Синтез Соединения 46
К Соединению 45 (3,27 г, 7,26 ммоль) добавляют тетрагидрофуран (39,2 мл), Соединение 17 (1,69 г, 9,44 ммоль), трифенилфосфин (2,48 г, 9,44 ммоль) и DMEAD (2,21 г, 9,44 ммоль). Смесь перемешивают при 50°C в течение 1 часа, реакцию гасят водой. Органический слой экстрагируют этилацетат, промывают водой, и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 46 (4,07 г, выход 92%).
1H-ЯМР (CDCl3) δ: 1,42 (т, J=7,2Гц, 3H), 1,72 (с, 9H), 1,90 (м, 2H), 2,06 (м, 2H), 3,76 (м, 2H), 4,19 (м, 2H), 4,44 (кв, J=7,2Гц, 2H), 4,67 (м, 1H), 6,48 (т, J=4,4Гц, 1H), 7,06 (дд, J=8,8, 2,0Гц, 1H), 7,83 (шс, 1H), 7,89 (д, J=8,0Гц, 1H), 8,13-8,16 (м, 2H), 8,32 (д, J=4,8Гц, 2H), 8,49 (д, J=8,8Гц, 1H).
ЖХ/МС(ИЭР):m/z= 612 [M+H]+, ВУ=3,59 мин, ЖХ/МС Способ 1
[0153]
Стадия 4: Синтез Соединения 21
К Соединению 46 (4,17 г, 6,82 ммоль) добавляют дихлорметан (41,7 мл) и трифторуксусную кислоту (41,7 мл, 541 ммоль), и смесь перемешивают при комнатной температуре в течение 1 часа 30 минут. Реакционный раствор концентрируют при пониженном давлении и нейтрализуют насыщенным водным раствором бикарбоната натрия. Смесь экстрагируют хлороформом и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и хлороформ добавляют к остатку. Твердое вещество фильтруют с получением Соединения 21 (800 мг, выход 22%). Фильтрат снова концентрируют при пониженном давлении. Добавляют толуол для отверждения остатка, и твердое вещество фильтруют с получением Соединения 21 (1,73 г, выход 48%). Фильтрат далее концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 21 (520 мг, выход 15%).
1H-ЯМР (CDCl3) δ: 1,42 (т, J=7,2Гц, 3H), 1,88 (м, 2H), 2,06 (м, 2H), 3,71 (м, 2H), 4,21 (м, 2H), 4,43 (кв, J=7,2Гц, 2H), 4,61 (м, 1H), 6,48 (т, J=4,8Гц, 1H), 6,98 (д, J=2,0Гц, 1H), 7,02 (дд, J=8,8, 2,0Гц, 1H), 7,78-7,84 (м, 2H), 8,11 (д, J=8,4Гц, 1H), 8,32 (д, J=4,8Гц, 2H), 8,42-8,48 (м, 2H).
ЖХ/МС(ИЭР):m/z= 512 [M+H]+, ВУ=2,80 мин, ЖХ/МС Способ 1
[0154]
Стадия 5: Синтез Соединения 49
Соединение 21 (800 мг, 1,56 ммоль) растворяют в диметилформамиде (12 мл), и добавляют 60% масс. гидрид натрия (94 мг, 2,35 ммоль) и Соединение 48 (681 мг, 2,35 ммоль) при охлаждении на льду. После перемешивания при 90°C в течение 30 минут, смесь снова охлаждают на ледяной бане и добавляют 60% масс. гидрид натрия (94 мг, 2,35 ммоль) и Соединение 48 (681 мг, 2,35 ммоль). После перемешивания при 90°C в течение 30 минут, смесь снова охлаждают на ледяной бане и добавляют 60% масс. гидрид натрия (94 мг, 2,35 ммоль) и Соединение 48 (681 мг, 2,35 ммоль). После перемешивания при 90°C в течение 30 минут, смесь снова охлаждают на ледяной бане и добавляют 60% масс. гидрид натрия (94 мг, 2,35 ммоль) и Соединение 48 (681 мг, 2,35 ммоль). После перемешивания при 90°C в течение 30 минут, смесь снова охлаждают на ледяной бане и добавляют 60% масс. гидрид натрия (94 мг, 2,35 ммоль) и Соединение 48 (681 мг, 2,35 ммоль), и смесь перемешивают при 90°C в течение 30 минут. Реакционный раствор выливают в 10% водный раствор лимонной кислоты для гашения реакции, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения 49 (900 мг, выход 96%).
1H-ЯМР (CDCl3) δ: 1,71-2,24 (м, 10H), 2,35 (м, 2H), 3,77 (м, 2H), 4,20 (м, 2H), 4,32 (м, 1H), 4,67 (м, 1H), 6,54 (т, J=4,8Гц, 1H), 6,96 (д, J=2,0Гц, 1H), 7,05 (дд, J=8,8, 2,0Гц, 1H), 7,80 (д, J=8,4Гц, 1H), 7,82 (с, 1H), 8,23 (д, J=8,0Гц, 1H), 8,39 (т, J=4,8Гц, 2H), 8,50 (д, J=8,8Гц, 1H).
ЖХ/МС(ИЭР):m/z= 602 [M+H]+, ВУ=2,71 мин, ЖХ/МС Способ 1
[0155]
Стадия 6: Синтез Соединения (I-162)
Соединение синтезируют по методике, описанной на Стадии 7 Примера 3.
1H-ЯМР (ДМСО-d6) δ: 1,55-1,71 (м, 8H), 1,81 (шс, 2H), 1,98-2,25 (м, 14H), 2,58 (с, 2H), 3,62 (м, 2H), 4,19 (м, 2H), 4,68-4,78 (м, 2H), 6,62 (т, J=4,8Гц, 1H), 6,98 (дд, J=8,8, 2,0Гц, 1H), 7,31 (д, J=2,0Гц, 1H), 7,73 (д, J=8,4Гц, 1H), 8,17 (д, J=8,4Гц, 1H), 8,37 (д, J=4,4Гц, 2H), 8,41-8,44 (м, 2H), 8,49 (s 1H), 12,32 (с, 1H).
ЖХ/МС(ИЭР):m/z= 779 [M+H]+, ВУ=3,06 мин, ЖХ/МС Способ 1
[0156]
Пример 7
Синтез Соединения (I-165)
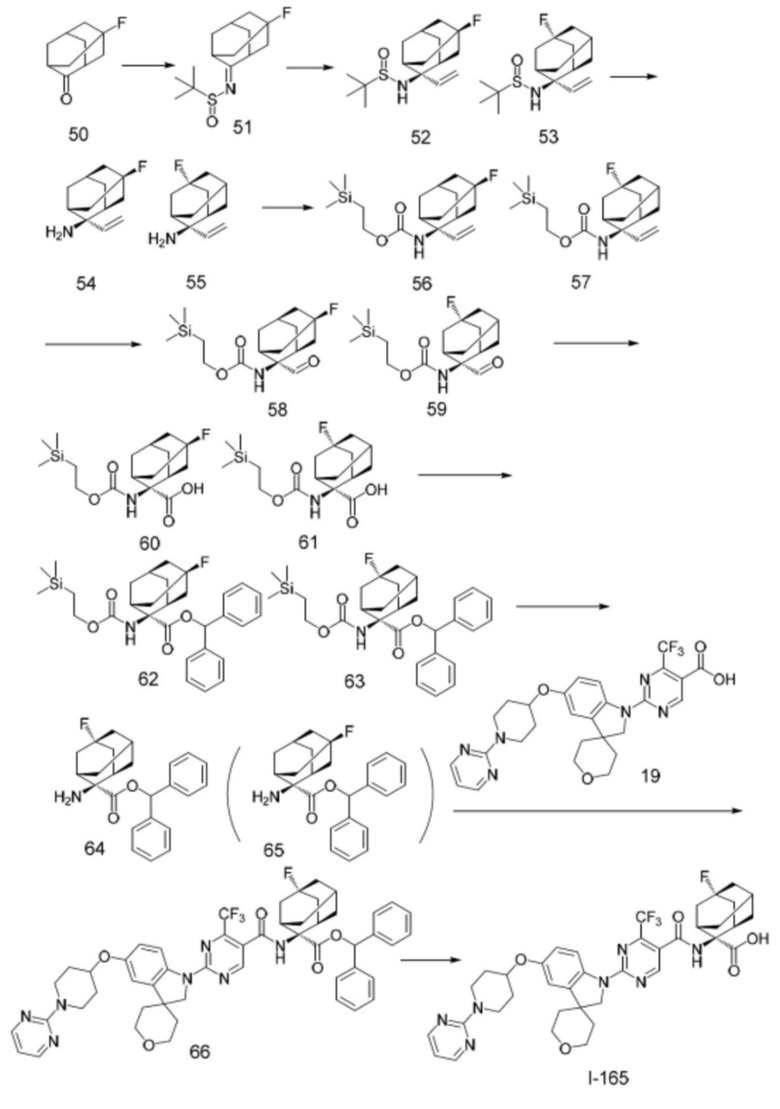
Стадия 1: Синтез Соединения 51
Соединение 50 (49,9 г, 297 ммоль) и 2-метил-2-пропансульфинамид (53,9 г, 445 ммоль) добавляют в тетрагидрофуран (250 мл), и тетраэтилортотитанат (137 мл, 653 ммоль) добавляют при комнатной температуре. Смесь перемешивают при 80°C в течение 1 часа и затем выливают в ацетонитрил (1 л). Добавляют воду (53,5 г) для гашения реакции. После перемешивания в течение 10 минут, добавляют безводный сульфат магния, и твердое вещество отфильтровывают. Фильтрат концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 51 (58,9 г, выход 70%). ЖХ/МС(ИЭР):m/z= 272 [M+H]+, ВУ=1,81 мин, ЖХ/МС Способ 2
[0157]
Стадия 2: Синтез смеси Соединения 52 и Соединения 53
Соединение 51 (70,3 г, 241 ммоль) растворяют в тетрагидрофуране (211 мл), и 1 моль/л бромида винилмагния (361 мл, 361 ммоль) добавляют по каплям при охлаждении на льду. Реакцию гасят водным раствором хлорида аммония, затем экстрагируют этилацетатом и промывают водой, и органический слой концентрируют при пониженном давлении. Полученное твердое вещество суспендируют с гексаном, и твердое вещество фильтруют с получением смеси Соединения 52 и Соединения 53 (46,1 г, выход 64%).
ЖХ/МС(ИЭР):m/z= 300 [M+H]+, ВУ=2,01 мин, ЖХ/МС Способ 2
[0158]
Стадия 3: Синтез смеси Соединения 54 и Соединения 55
К смеси Соединения 52 и Соединения 53 (70,7 г, 236 ммоль) добавляют 2 моль/л раствор хлороводорода в метаноле (354 мл, 708 ммоль) и перемешивают при комнатной температуре в течение 1 часа. Воду и этилацетат добавляют для экстракции. Водный слой нейтрализуют добавлением водного раствора бикарбоната натрия, затем экстрагируют хлороформом. Слой хлороформа сушат над безводным сульфатом магния, и растворитель удаляют при пониженном давлении с получением смеси Соединения 54 и Соединения 55 в виде неочищенного продукта (55,2 г).
ЖХ/МС(ИЭР):m/z= 196 [M+H]+, ВУ=1,01 мин, ЖХ/МС Способ 2
[0159]
Стадия 4: Синтез смеси Соединения 56 и Соединения 57
Смесь Соединения 54 и Соединения 55 (55,2 г, 223 ммоль) растворяют в тетрагидрофуране (497 мл), и добавляют 1-[2-(триметилсилил)этоксикарбонил]пирролидин-2,5-дион (100 г, 387 ммоль). После перемешивания при комнатной температуре в течение 1 часа, добавляют дополнительный 1-[2-(триметилсилил)этоксикарбонил]пирролидин-2,5-дион (12,5 г, 48,2 ммоль). После перемешивания в течение 1 часа 40 минут, добавляют водный раствор лимонной кислоты. Смесь экстрагируют этилацетатом. Органический слой промывают водой и концентрируют при пониженном давлении. Гексан добавляют к полученному твердому веществу, и нерастворимый продукт отфильтровывают. Фильтрат концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением смеси Соединения 56 и Соединения 57 (65,0 г, выход 86%).
1H-ЯМР (CDCl3) δ: 0,03 (с, 9H), 0,92-0,98 (м, 2H), 1,49-1,56 (м, 2H), 1,73-1,80 (м, 2H), 1,87-2,01 (м, 4H), 2,13-2,28 (м, 3H), 2,56 (шс, 2H), 4,09 (м, 2H), 4,62 (с, 1H), 5,20-5,31 (м, 2H), 6,10 (дд, J=17,6, 2,8Гц, 1H).
[0160]
Стадия 5: Синтез смеси Соединения 58 и Соединения 59
Смесь Соединения 56 и Соединения 57 (67,0 г, 197 ммоль) растворяют в ацетонитриле (1179 мл), и добавляют воду (395 мл), периодат натрия (127 г, 592 ммоль), 2,6-лутидин (63,4 г, 592 ммоль), дигидрат осмата калия (7,27 г, 19,7 ммоль). Смесь перемешивают при 60°C в течение 1 часа, затем добавляют периодат натрия (42,2 г, 197 ммоль). Через 2 часа, реакцию охлаждают на ледяной бане и гасят водным тиосульфатом натрия. Смесь экстрагируют этилацетатом, и органический слой промывают 10% водным раствором лимонной кислоты, и промывают 3% водным раствором бикарбоната натрия. Органический слой сушат над безводным сульфатом магния, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением смеси Соединения 58 и Соединения 59 (32,5 г, выход 48%).
1H-ЯМР (CDCl3) δ: 0,03 (с, 9H), 0,92-1,00 (м, 2H), 1,56-1,98 (м, 8H), 2,09-2,28 (м, 3H), 2,63-2,69 (м, 2H), 4,12 (м, 2H), 4,81-4,89 (м, 1H), 9,60-9,74 (м, 2H).
[0161]
Стадия 6: Синтез смеси Соединения 60 и Соединения 61
Смесь Соединения 58 и Соединения 59 (36,1 г, 106 ммоль) растворяют в трет-бутиловом спирте (361 мл) и воде (65 мл), и добавляют 2-метил-2-бутен (63,8 мл, 603 ммоль). Дигидрофосфат калия (57,5 г, 423 ммоль) и хлорит натрия (76 г, 846 ммоль) растворяют в воде (300 мл) и добавляют по каплям при охлаждении льдом. После перемешивания при охлаждении на льду в течение 1 часа, реакцию гасят водным тиосульфатом натрия. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом магния, и растворитель удаляют при пониженном давлении с получением смеси Соединения 60 и Соединения 61 в виде неочищенного продукта (45 г).
ЖХ/МС(ИЭР):m/z= 356 [M-H]-, ВУ=2,32 мин и 2,41 мин, ЖХ/МС Способ 2
[0162]
Стадия 7: Синтез смеси Соединения 62 и Соединения 63
Неочищенный продукт смеси Соединения 60 и Соединения 61 (45 г) растворяют в тетрагидрофуране (227 мл) и метаноле (227 мл), и добавляют дифенилдиазометан (61,8 г, 318 ммоль). После перемешивания при комнатной температуре в течение 2 часов, добавляют уксусную кислоту (18,2 мл). После перемешивания при комнатной температуре в течение 1 часа, добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водным раствором карбоната натрия и сушат над сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат). Фракцию концентрируют, и остаток отверждают добавлением гексана, и твердое вещество фильтруют с получением смеси Соединения 62 и Соединения 63 (21,5 г, выход 39%).
1H-ЯМР (CDCl3) δ: 0,03 (с, 9H), 0,73-0,94 (м, 2H), 1,50-1,56 (м, 2H), 1,75-1,96 (м, 6H), 2,10-2,20 (м, 3H), 2,84 (шс, 2H), 3,95 (м, 2H), 4,83 (шс, 1H), 6,90-6,93 (м, 1H), 7,25-7,31 (м, 10H).
[0163]
Стадия 8: Синтез Соединения 64
К смеси Соединения 62 и Соединения 63 (43,2 г, 82 ммоль) добавляют 1 моль/л раствора фторида тетрабутиламмония-тетрагидрофурана (866 мл) и уксусную кислоту (42,4 мл), и смесь перемешивают при нагревании при кипении с обратным холодильником в течение 15 часов. Водный раствор бикарбоната натрия добавляют для нейтрализации, затем экстрагируют этилацетатом. Органический слой промывают три раза водным раствором хлорида аммония, затем раствором бикарбоната натрия и насыщенным раствором соли. Органические слои сушат над безводным сульфатом магния, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) для отделения менее полярного Соединения 65 от высокополярного Соединения 64 с получением Соединения 64 (19,5 г, выход 56%).
1H-ЯМР (ДМСО-d6) δ: 1,30-1,35 (м, 2H), 1,65-1,77 (м, 6H), 1,99-2,11 (м, 3H), 2,19-2,27 (м, 2H), 2,35 (шс, 2H), 6,82 (с, 1H), 7,27 (м, 2H), 7,35 (м, 4H), 7,45 (м, 4H).
[0164]
Стадия 9: Синтез Соединения 66
Соединение 66 синтезируют по методике, описанной на Стадии 3 Примера 4.
ЖХ/МС(ИЭР):m/z= 918 [M+H]+, ВУ=3,06 мин, ЖХМС способ 1
[0165]
Стадия 10: Синтез Соединения (I-165)
Соединение 66 (66 мг, 0,072 ммоль) растворяют в дихлорметане (4 мл), и добавляют анизол (40 мг, 0,37 ммоль) и трифторуксусную кислоту (2 мл) при охлаждении льдом. После перемешивания в течение 30 минут при охлаждении льдом, реакционную смесь концентрируют при пониженном давлении. Остаток растворяют в дихлорметане и нейтрализуют водным карбонатом натрия. Раствор лимонной кислоты добавляют к водному слою, затем экстрагируют дихлорметаном. Объединенные органические слои сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения (I-165) (33 мг, выход 61%).
1H-ЯМР (ДМСО-d6) δ: 1,45-1,48 (м, 2H), 1,53-1,60 (м, 4H), 1,78-1,84 (м, 4H), 1,97-2,05 (м, 6H), 2,16-2,24 (м, 3H), 2,82 (с, 2H), 3,48-3,56 (м, 4H), 3,88-3,92 (м, 2H), 4,22-4,26 (м, 4H), 4,64-4,70 (м, 1H). 6,61 (т, J=4,8Гц, 1H), 6,94 (д, J=8,0Гц, 1H), 7,09 (д, J=2,4Гц, 1H), 8,17 (д, J=4,4Гц, 1H), 8,36 (д, J=4,8Гц, 2H), 8,63 (шс, 1H), 8,71 (с, 1H), 12,67 (шс, 1H).
[0166]
Пример 8
Синтез Соединения (I-228)
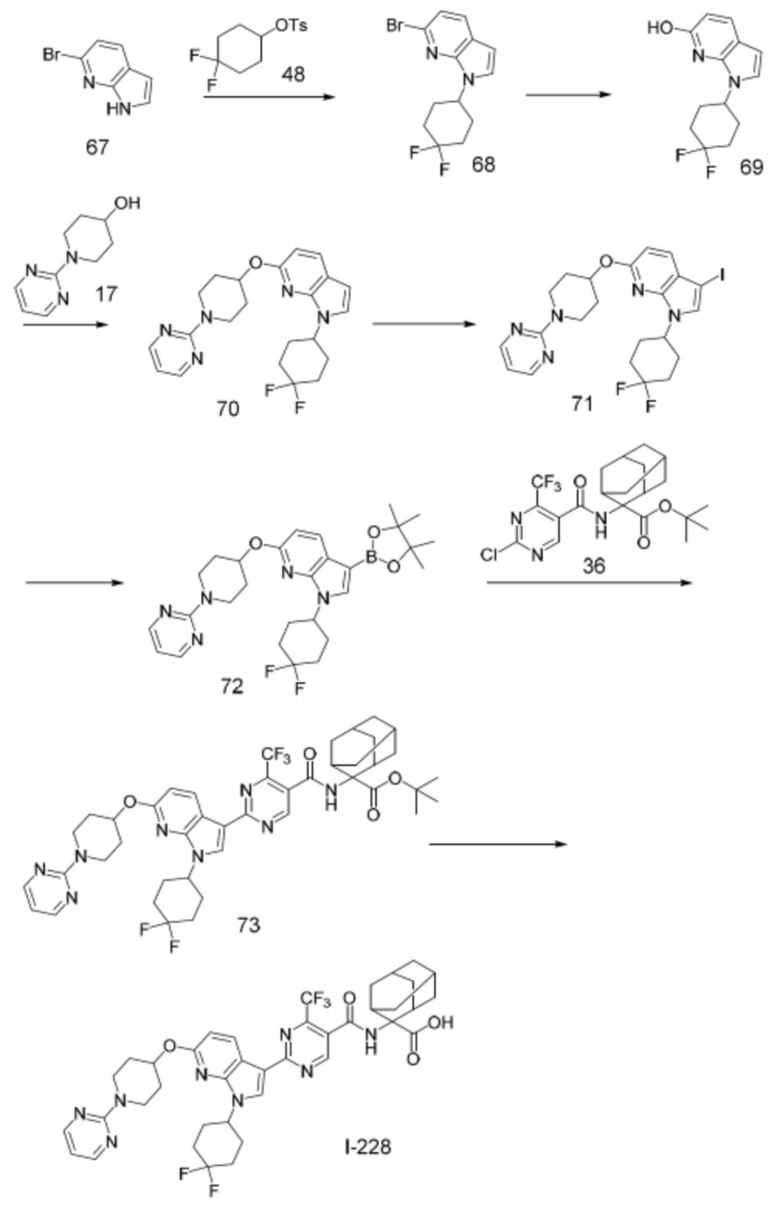
Стадия 1: Синтез Соединения 68
К раствору Соединения 67 (300 мг, 1,52 ммоль) в N-метилпирролидоне (4,42 мл) добавляют 60% масс. гидрид натрия (61 мг, 1,53 ммоль) при перемешивании под потоком аргона при комнатной температуре, и смесь перемешивают в течение 10 мин при комнатной температуре. Соединение 48 (442 мг, 1,52 ммоль) затем добавляют при комнатной температуре. После перемешивания при 100°C в течение 3 часов, добавляют Соединение 48 (442 мг, 1,52 ммоль) и 60% масс. гидрид натрия (61 мг, 1,53 ммоль), и смесь перемешивают при 80°C в течение 5 часов. После завершения реакции, насыщенный водный раствор хлорида аммония добавляют к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом натрия. Растворитель концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 68 (252 мг, выход 53%).
ЖХ/МС(DUIS):m/z= 315 [M+H]+, ВУ=1,59 мин, ЖХ/МС Способ 9
[0167]
Стадия 2: Синтез Соединения 69
Соединение 68 (50 мг, 0,16 ммоль) растворяют в 1,4-диоксане (0,5 мл) и воде (0,5 мл), и 8 моль/л раствора гидроксида калия (0,06 мл, 0,48 ммоль), Pd2(dba)3 (15 мг, 0,02 ммоль), 5-(ди-т-бутилфосфино)-1',3',5'-трифенил-1,4'-би-1H-пиразол (16 мг, 0,03 ммоль) добавляют при перемешивании под потоком аргона при комнатной температуре, и смесь перемешивают при 75°C. Через 2 часа добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 69 в виде неочищенного продукта (51 мг).
ЖХ/МС(DUIS):m/z= 253 [M+H]+, ВУ=1,04 мин, ЖХ/МС Способ 9
[0168]
Стадия 3: Синтез Соединения 70
К неочищенному продукту Соединения 69 (49 мг, 0,19 ммоль) в тетрагидрофуране (0,98 мл) добавляют Соединение 17 (70 мг, 0,39 ммоль), 1,9 моль/л раствор ДИАД-толуола (145 мкл, 0,28 ммоль), трифенилфосфин (74 мг, 0,28 ммоль) под потоком аргона при комнатной температуре, и смесь перемешивают в течение 2 часов при комнатной температуре. После завершения реакции, водный раствор бикарбоната натрия добавляют к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 70 (47 мг, 58%).
ЖХ/МС(DUIS):m/z= 414 [M+H]+, ВУ= 1,77 мин, ЖХ/МС Способ 9
[0169]
Стадия 4: Синтез Соединения 71
Соединение синтезируют по методике, описанной на Стадии 5 Примера 9.
ЖХ/МС(DUIS):m/z= 540 [M+H]+, ВУ=1,98 мин, ЖХ/МС Способ 9
[0170]
Стадия 5: Синтез Соединения 72
Соединение синтезируют по методике, описанной на Стадии 6 Примера 9.
ЖХ/МС(DUIS):m/z= 540 [M+H]+, ВУ=2,00 мин, ЖХ/МС Способ 9
[0171]
Стадия 6: Синтез Соединения 73
Соединение синтезируют по методике, описанной на Стадии 1 Примера 6.
ЖХ/МС(DUIS):m/z= 837 [M+H]+, ВУ=2,29 мин, ЖХ/МС Способ 9
[0172]
Стадия 7: Синтез Соединения (I-228)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
1H-ЯМР (ДМСО-d6) δ: 1,55-1,84 (м, 10H), 2,02-2,28 (м, 14H), 2,55-2,58 (м, 2H), 3,45-3,55 (м, 2H), 4,30-4,42 (м, 2H), 4,70-4,83 (м, 1H), 5,23-5,33 (м, 1H), 6,63 (т, J=4,8Гц, 1H), 6,79 (д, J=8,5Гц, 1H), 8,31 (с, 1H), 8,37 (д, J=4,6Гц, 2H), 8,61 (д, J=8,5Гц, 1H), 8,65 (шс, 1H), 8,87 (с, 1H), 12,51 (шс, 1H).
ЖХ/МС(ИЭР):m/z= 781 [M+H]+, ВУ=1,86 мин, ЖХ/МС Способ 10
[0173]
Пример 9
Синтез Соединения (I-268)
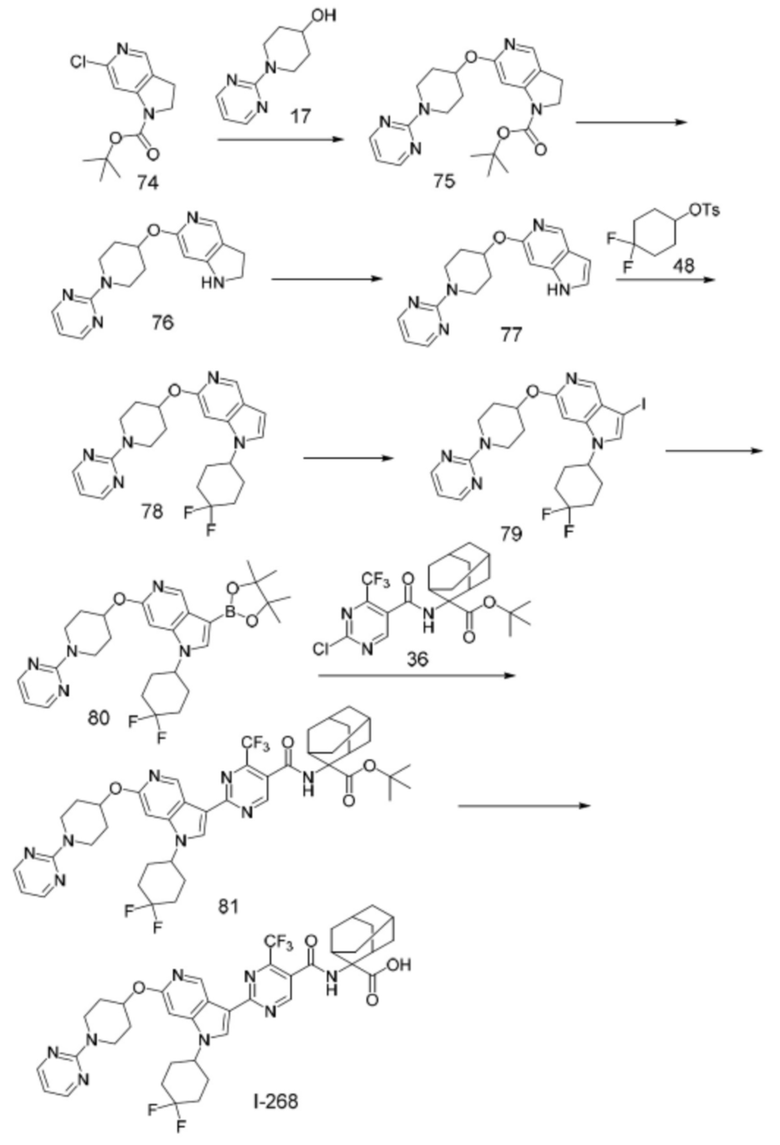
Стадия 1: Синтез Соединения 75
К раствору Соединения 17 (760 мг, 4,24 ммоль) в толуоле (10 мл) добавляют 60% масс. гидрид натрия (283 мг, 7,08 ммоль) при перемешивании под потоком аргона при комнатной температуре, и смесь перемешивают при 70°C в течение 15 мин. Соединение 74 (910 мг, 3,57 ммоль), Pd2(dba)3 (324 мг, 0,354 ммоль), (R)-(+)-TolBINAP (240 мг, 0,354 ммоль) добавляют при комнатной температуре, и смесь перемешивают при 100°C. Через 30 мин добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 75 (899 мг, выход 63%).
ЖХ/МС(DUIS):m/z= 398 [M+H]+, ВУ= 1,17 мин, ЖХ/МС Способ 9
[0174]
Стадия 2: Синтез Соединения 76
К раствору Соединения 75 (899 мг, 2,26 ммоль) в дихлорметане (2 мл) добавляют трифторуксусную кислоту (2 мл, 26,1 ммоль) при перемешивании под потоком аргона при комнатной температуре, и смесь перемешивают в течение 6 часов. После завершения реакции, водный раствор бикарбоната натрия добавляют к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении с получением Соединения 76 (695 мг, выход 100%).
ЖХ/МС(DUIS):m/z= 298 [M+H]+, ВУ=0,35 мин, ЖХ/МС Способ 9
[0175]
Стадия 3: Синтез Соединения 77
К раствору Соединения 76 (530 мг, 1,78 ммоль) в толуоле (15,9 мл) добавляют диоксид марганца (775 мг, 8,91 ммоль) при комнатной температуре при перемешивании под потоком аргона, и смесь перемешивают при 120°C в течение 6 часов. Затем, после перемешивания при комнатной температуре в течение 18 часов, диоксид марганца (775 мг, 8,91 ммоль) добавляют при комнатной температуре при перемешивании под потоком аргона, затем перемешивают при 120°C в течение 2 часов. После завершения реакции, раствор фильтруют через Целит (зарегистрированная торговая марка), промывают этилацетатом, и фильтрат концентрируют при пониженном давлении с получением Соединения 77 (342 мг, выход 65%).
ЖХ/МС(DUIS):m/z= 296 [M+H]+, ВУ=0,36 мин, ЖХ/МС Способ 9
[0176]
Стадия 4: Синтез Соединения 78
К раствору Соединения 77 (370 мг, 1,25 ммоль) в N-метилпирролидоне (7,4 мл) добавляют карбонат цезия (1,22 г, 3,74 ммоль) и Соединение 48(1,09 г, 3,75 ммоль) при комнатной температуре при перемешивании под потоком аргона, и смесь перемешивают при 120°C в течение 3 часов. Затем, карбонат цезия (1,22 г, 3,74 ммоль) и Соединение 48 (1,09 г, 3,75 ммоль) добавляют при комнатной температуре, и смесь перемешивают при 120°C в течение 2 часов. Дополнительно, карбонат цезия (1,22 г, 3,74 ммоль) и Соединение 48 (1,09 г, 3,75 ммоль) добавляют при комнатной температуре, и смесь перемешивают при 120°C в течение 2 часов. После завершения реакции, добавляют воду к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 78 (520 мг, выход 100%).
ЖХ/МС(DUIS):m/z= 414 [M+H]+, ВУ=0,91 мин, ЖХ/МС Способ 9
[0177]
Стадия 5: Синтез Соединения 79
К раствору Соединения 78 (470 мг, 1,14 ммоль) в диметилформамиде (4,7 мл) добавляют N-йодсукцинимид (280 мг, 1,25 ммоль) при комнатной температуре при перемешивании под потоком аргона, и смесь перемешивают при комнатной температуре в течение 30 минут. После завершения реакции, водный раствор бикарбоната натрия добавляют к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 79 (180 мг, выход 29%).
ЖХ/МС(ИЭР):m/z= 540 [M+H]+, ВУ=1,43 мин, ЖХ/МС Способ 10
[0178]
Стадия 6: Синтез Соединения 80
К раствору Соединения 79 (180 мг, 0,33 ммоль) в 1,4-диоксане (3,6 мл) добавляют триэтиламин (185 мкл, 1,33 ммоль), 4,4,5,5-тетраметил-1,3,2-диоксаборолан (195 мкл, 1,34 ммоль), X-Phos (32 мг, 0,07 ммоль), Pd2(dba)3 (31 мг, 0,03 ммоль) при комнатной температуре при перемешивании под потоком аргона, и смесь перемешивают при 95°C в течение 1 часа. После завершения реакции, добавляют воду к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 80 (111 мг, выход 62%).
ЖХ/МС(ИЭР):m/z= 540 [M+H]+, ВУ=1,29 мин, ЖХ/МС Способ 10
[0179]
Стадия 7: Синтез Соединения 81
Соединение синтезируют по методике, описанной на Стадии 1 Примера 6.
ЖХ/МС(ИЭР):m/z= 837 [M+H]+, ВУ=1,99 мин, ЖХ/МС Способ 10
[0180]
Стадия 8: Синтез Соединения (I-268)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
1H-ЯМР (ДМСО-d6) δ: 1,49-1,84 (м, 10H), 2,01-2,22 (м, 14H), 2,56-2,60 (м, 2H), 3,54-3,63 (м, 2H), 4,21-4,31 (м, 2H), 4,60-4,73 (м, 1H), 5,33-5,43 (м, 1H), 6,62 (т, J=4,8 Гц, 1H), 7,15 (с, 1H), 8,37 (д, J=4,8 Гц, 2H), 8,41 (шс, 1H), 8,51 (шс, 1H), 8,89 (с, 1H), 9,23 (с, 1H), 12,51 (шс, 1H).
ЖХ/МС(DUIS):m/z= 781 [M+H]+, ВУ=1,56 мин, ЖХ/МС Способ 9
[0181]
Пример 10
Синтез Соединения (I-269)
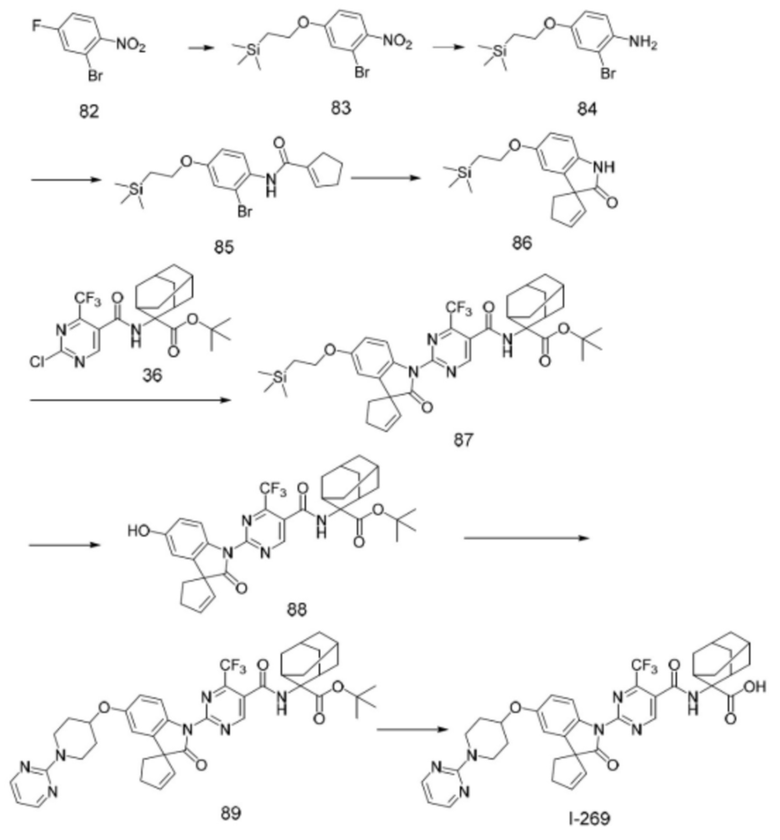
Стадия 1: Синтез Соединения 83
2-(Триметилсилил)этан-1-ол (1,08 г, 9,10 ммоль) растворяют в тетрагидрофуране (10 мл), и добавляют 60% масс. гидрид натрия (218 мг, 5,46 ммоль) при охлаждении на льду. Через 5 минут, добавляют Соединение 82 (1,00 г, 4,55 ммоль), и смесь перемешивают при комнатной температуре в течение 3 часов. Реакцию гасят водой, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 83 (1,45 г, выход 100%).
1H-ЯМР (CDCl3) δ: 1,10 (с, 9H), 1,16 (т, J=8,0Гц, 2H), 4,14 (т, J=8,0Гц, 2H), 6,88 (дд, J=9,2, 2,8Гц, 1H), 7,18 (д, J=2,8Гц, 1H), 7,98 (д, J=9,2Гц, 1H).
[0182]
Стадия 2: Синтез Соединения 84
Соединение 83 (500 мг, 1,57 ммоль) растворяют в этаноле (5 мл) и воде (1 мл), добавляют хлорид аммония (336 мг, 6,28 ммоль) и железо (438 ммоль, 7,85 ммоль), и смесь перемешивают при 90°C в течение 3 часов. Реакционный раствор охлаждают и затем разбавляют этилацетатом (30 мл), и нерастворимый продукт отфильтровывают с применением Целита (зарегистрированная торговая марка). К фильтрату добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 84 (303 мг, выход 67%).
ЖХ/МС(ИЭР):m/z= 288 [M+H]+, ВУ=2,83 мин, ЖХ/МС Способ 1
[0183]
Стадия 3: Синтез Соединения 85
Соединение 84 (1,93 г, 6,70 ммоль) растворяют в диметилформамиде (10 мл), и добавляют циклопент-1-ен-1-карбоновую кислоту (1,08 г, 1,44 ммоль), триэтиламин (3,39 г, 33,5 ммоль) и ГАТУ (3,80 г, 10,1 ммоль), и смесь перемешивают при комнатной температуре в течение 6 часов. К реакционному раствору добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают насыщенным водным раствором бикарбоната натрия и промывают водой. Органический слой сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 85 (816 мг, выход 32%).
ЖХ/МС(ИЭР):m/z= 382 [M+H]+, ВУ= 3,08 мин, ЖХ/МС Способ 1
[0184]
Стадия 4: Синтез Соединения 86
Соединение 85 (816 мг, 2,13 ммоль) растворяют в диметилформамиде (6 мл), и добавляют триэтиламин (1,08 г, 10,6 ммоль) и PdCl2(dppf) (156 мг, 0,213 ммоль), и смесь перемешивают при 80°C в течение 2 часов. Затем реакционный раствор оставляют охлаждаться, добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 86 (467 мг, выход 73%).
ЖХ/МС(ИЭР):m/z= 302 [M+H]+, ВУ=2,50 мин, ЖХ/МС Способ 1
[0185]
Стадия 5: Синтез Соединения 87
Соединение 86 (218 мг, 0,723 ммоль) растворяют в 1,4-диоксане (2 мл), и добавляют Соединение 36 (399 мг, 0,868 ммоль), карбонат цезия (707 мг, 2,17 ммоль) и Xantphos Pd G2 (129 мг, 0,145 ммоль), и смесь перемешивают при 100°C в течение 1 часа в атмосфере азота. После охлаждения, смесь разбавляют этилацетатом (10 мл), и нерастворимый продукт отфильтровывают. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 87 (404 мг, выход 77%).
ЖХ/МС(ИЭР):m/z= 725 [M+H]+, ВУ= 3,54 мин, ЖХ/МС Способ 1
[0186]
Стадия 6: Синтез Соединения 88
К Соединению 87 (404 мг, 0,557 ммоль) добавляют 1 моль/л раствора фторида тетрабутиламмония-тетрагидрофурана (10 мл, 10 ммоль), и смесь перемешивают при 80°C в течение 1 часа. После охлаждения, добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток растворяют в диметилформамиде (8 мл) и триэтиламине (169 мг, 1,67 ммоль) и добавляют ГАТУ (318 мг, 0,835 ммоль), и смесь перемешивают при комнатной температуре в течение 30 минут. Добавляют метанол (20 мл) и карбонат калия (231 мг, 1,67 ммоль), и смесь перемешивают при комнатной температуре в течение 30 минут, добавляют воду к реакционному раствору, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 88 (203 мг, выход 58%).
ЖХ/МС(ИЭР):m/z= 625 [M+H]+, ВУ=2,77 мин, ЖХ/МС Способ 1
[0187]
Стадия 7: Синтез Соединения 89
Соединение синтезируют по методике, описанной на Стадии 5 Примера 3.
ЖХ/МС(ИЭР):m/z= 786 [M+H]+, ВУ=3,11 мин, ЖХ/МС Способ 1
[0188]
Стадия 8: Синтез Соединения (I-269)
Соединение 89 (50 мг, 0,064 ммоль) растворяют в трифторуксусной кислоте (4 мл), и смесь перемешивают при комнатной температуре в течение 1 часа. Реакционный раствор концентрируют, растворяют в дихлорметане и нейтрализуют насыщенным водным раствором бикарбоната натрия. Водный раствор лимонной кислоты добавляют к реакционному раствору снова для подкисления, затем экстрагируют дихлорметаном. Органический слой сушат над безводным сульфатом натрия, и растворитель удаляют в вакууме. Остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения (I-269) (30 мг, выход 65%).
1H-ЯМР (CDCl3) δ: 1,77-2,05 (м, 15H), 2,19-2,27 (м, 3H), 2,61-2,67 (м, 3H), 2,70-2,76 (м, 1H), 2,78-2,87 (м, 1H), 3,69-3,75 (м, 2H), 4,11-4,19 (м, 2H), 4,51-4,57 (м, 1H), 5,53-5,56 (м, 1H), 6,24-6,27 (м, 1H), 6,49 (т, J=5,2Гц, 1H), 6,55 (шс, 1H), 6,81 (д, J=2,8Гц, 1H), 6,90 (дд, J=8,8, 2,4Гц, 1H), 7,88 (д, J=9,2Гц, 1H), 8,32 (д, J=4,8Гц, 2H), 9,12 (с, 1H).
[0189]
Пример 11
Синтез Соединения (I-270)
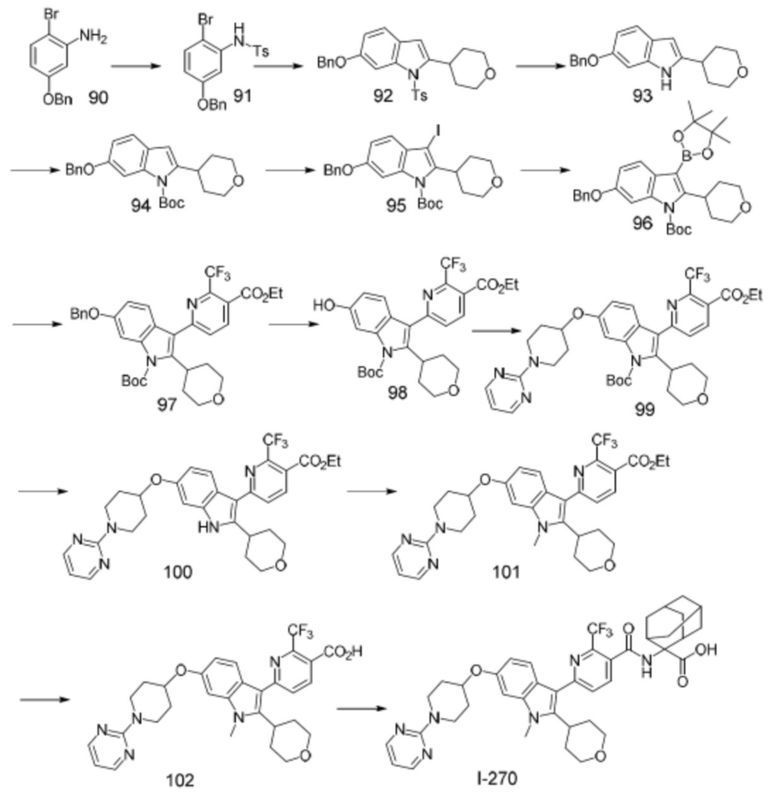
Стадия 1: Синтез Соединения 91
Соединение 90 (1,64 г, 5,60 ммоль) растворяют в дихлорметане (16,4 мл), и добавляют пиридин (1,33 г, 16,80 ммоль) и паратолуолсульфонилхлорид (2,14 г, 11,20 ммоль) при охлаждении льдом. После перемешивания при комнатной температуре в течение 1,5 часов, добавляют триэтиламин (1,70 г, 16,80 ммоль) и 1-метилпиперазин (1,12 г, 11,20 ммоль), и смесь перемешивают в течение 30 минут. Добавляют концентрированную хлористоводородную кислоту при охлаждении льдом, и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 91 (2,08 г, выход 86%).
ЖХ/МС(ИЭР):m/z= 432 [M+H]+, ВУ=2,76 мин, ЖХ/МС Способ 1
[0190]
Стадия 2: Синтез Соединения 92
Соединение 91 (0,45 г, 1,04 ммоль) растворяют в диметилформамиде (2,89 мл), и добавляют 4-этинилтетрагидро-2H-пиран (0,17 г, 1,56 ммоль), йодид меди(I) (39 мг, 0,21 ммоль), триэтиламин (2,11 г, 20,82 ммоль) и PdCl2(dppf) (76 мг, 0,10 ммоль), и смесь перемешивают при 100°C в течение 8 часов. После добавления воды, смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 92 (0,35 г, выход 73%).
ЖХ/МС(ИЭР):m/z= 462 [M+H]+, ВУ=2,99 мин, ЖХ/МС Способ 1
[0191]
Стадия 3: Синтез Соединения 93
К раствору Соединения 92 (200 мг, 0,43 ммоль) в тетрагидрофуране (0,4 мл) добавляют 1 моль/л раствора фторида тетрабутиламмония-тетрагидрофурана (8,67 мл, 8,67 ммоль), и смесь перемешивают при нагревании при кипении с обратным холодильником в течение 17 часов. После добавления 1 моль/л хлористоводородной кислоты, смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения 93 (130 мг, выход 98%).
ЖХ/МС(ИЭР):m/z= 308 [M+H]+, ВУ=2,35 мин, ЖХ/МС Способ 1
[0192]
Стадия 4: Синтез Соединения 94
К раствору Соединения 93 (130 мг, 0,42 ммоль) в тетрагидрофуране (1,3 мл) добавляют Boc2O (220 мг, 1,01 ммоль) и ДМАП (5,2 мг, 0,04 ммоль), и смесь перемешивают при комнатной температуре в течение 21 часа. Реакционный раствор концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 94 (160 мг, выход 93%).
ЖХ/МС(ИЭР):m/z= 408[M+H]+, ВУ=3,18 мин, ЖХ/МС Способ 1
[0193]
Стадия 5: Синтез Соединения 95
Йод (62 мг, 0,25 ммоль) растворяют в дихлорметане (0,5 мл), и добавляют пиридин (39 мг, 0,49 ммоль) и йодбензол бис(трифторацетат) (106 мг, 0,25 ммоль), и смесь перемешивают при комнатной температуре в течение 15 мин. К этому раствору добавляют раствор Соединения 94 (100 мг, 0,25 ммоль) в дихлорметане (2 мл) при охлаждении льдом, и смесь перемешивают при комнатной температуре в течение 30 минут. После добавления 10% водного раствора тиосульфата натрия, смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 95 (115 мг, выход 88%).
1H-ЯМР (CDCl3) δ: 1,63-1,65 (м, 2H), 1,67 (с, 9H), 2,70 (ддд, J=25,3, 11,8, 4,1 Гц, 2H), 3,53 (тд, J=11,8, 1,7 Гц, 2H), 3,76-3,82 (м, 1H), 4,11 (дд, J=11,8, 4,1 Гц, 2H), 5,13 (с, 2H), 6,99 (дд, J=8,6, 2,2 Гц, 1H), 7,29-7,33 (м, 2H), 7,38 (т, J=7,3 Гц, 2H), 7,45 (д, J=7,3 Гц, 2H), 7,60 (д, J=2,2 Гц, 1H).
[0194]
Стадия 6: Синтез Соединения 96
Соединение 95 (113 мг, 0,21 ммоль) растворяют в 1,4-диоксане (2,3 мл), и добавляют 2-изопропокси-4,4,5,5-тетраметил-1,3,2-диоксаборолан (163 мг, 1,27 ммоль), X-Phos (30 мг, 0,06 ммоль), Pd2(dba)3 (39 мг, 0,04 ммоль) и триэтиламин (129 мг, 1,27 ммоль), и смесь перемешивают при 95°C в течение 2,5 часов. Добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 96 (110 мг, выход 97%).
1H-ЯМР (CDCl3) δ: 1,40 (с, 12H), 1,67 (с, 9H), 1,73 (д, J=12,0 Гц, 2H), 2,42 (ддд, J=24,8, 12,0, 4,1 Гц, 2H), 3,50 (т, J=10,9 Гц, 2H), 3,72-3,77 (м, 1H), 4,07 (дд, J=10,9, 4,1 Гц, 2H), 5,11 (с, 2H), 6,92 (дд, J=8,5, 2,3 Гц, 1H), 7,29-7,39 (м, 3H), 7,45 (д, J=7,2 Гц, 2H), 7,59 (д, J=2,3 Гц, 1H), 7,77 (д, J=8,5 Гц, 1H).
[0195]
Стадия 7: Синтез Соединения 97
Соединение 96 (108 мг, 0,20 ммоль) растворяют в 1,4-диоксане (1,4 мл), и добавляют Соединение 43 (57 мг, 0,22 ммоль), PdCl2(dppf) (17 мг, 0,02 ммоль), воду (0,3 мл) и карбонат цезия (132 мг, 0,41 ммоль), и смесь перемешивают при нагревании при кипении с обратным холодильником в течение 1 часа. После охлаждения, добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 97 (92 мг, выход 73%).
ЖХ/МС(ИЭР):m/z= 625[M+H]+, ВУ= 3,45 мин, ЖХ/МС Способ 1
[0196]
Стадия 8: Синтез Соединения 98
К Соединению 97 (90 мг, 0,14 ммоль) добавляют тетрагидрофуран (0,63 мл), этанол (0,63 мл) и 20% масс. палладий на угле (18 мг, 0,17 ммоль). Смесь перемешивают в течение 2,5 часов при комнатной температуре в атмосфере водорода. Реакционную смесь фильтруют через Целит (зарегистрированная торговая марка), фильтрат концентрируют при пониженном давлении с получением Соединения 98 (100 мг) в виде неочищенного продукта.
ЖХ/МС(ИЭР):m/z= 535[M+H]+, ВУ=2,72 мин, ЖХ/МС Способ 1
[0197]
Стадия 9: Синтез Соединения 99
Соединение синтезируют по методике, описанной на Стадии 3 Примера 6.
ЖХ/МС(ИЭР):m/z= 696[M+H]+, ВУ=3,08 мин, ЖХ/МС Способ 1
[0198]
Стадия 10: Синтез Соединения 100
Соединение синтезируют по методике, описанной на Стадии 4 Примера 6.
ЖХ/МС(ИЭР):m/z= 596[M+H]+, ВУ=2,61 мин, ЖХ/МС Способ 1
[0199]
Стадия 11: Синтез Соединения 101
К раствору Соединения 100 (34 мг, 0,06 ммоль) в диметилформамиде (0,5 мл) добавляют 60% масс. гидрид натрия (3,4 мг, 0,09 ммоль) и метилйодид (16 мг, 0,11 ммоль) при охлаждении льдом, и смесь перемешивают при комнатной температуре в течение 1 часа. После добавления ледяной воды, смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 101 (26 мг, выход 75%).
ЖХ/МС(ИЭР):m/z= 610[M+H]+, ВУ=3,04 мин, ЖХ/МС Способ 1
[0200]
Стадия 12: Синтез Соединения 102
Соединение синтезируют по методике, описанной на Стадии 2 Примера 4.
ЖХ/МС(ИЭР):m/z= 582[M+H]+, ВУ=2,25 мин, ЖХ/МС Способ 1
[0201]
Стадия 13: Синтез Соединения (I-270)
Соединение синтезируют по методике, описанной на Стадии 6 Примера 6.
1H-ЯМР (CDCl3) δ: 1,78-2,32 (м, 20H), 2,70 (с, 2H), 3,48 (т, J=11,0 Гц, 2H), 3,73 (ддд, J=13,2, 8,3, 4,1 Гц, 2H), 3,91-3,94 (м, 4H), 4,08-4,15 (м, 2H), 4,19 (дкв, J=13,2, 4,1 Гц, 2H), 4,59-4,65 (м, 1H), 6,14 (с, 1H), 6,49 (т, J=4,7 Гц, 1H), 6,90-6,91 (м, 2H), 7,60 (д, J=8,2 Гц, 1H), 7,81 (д, J=8,2 Гц, 1H), 7,98 (д, J=8,2 Гц, 1H), 8,33 (д, J=4,7 Гц, 2H), 12,12 (с, 1H).
[0202]
Пример 12
Синтез Соединения (I-486)
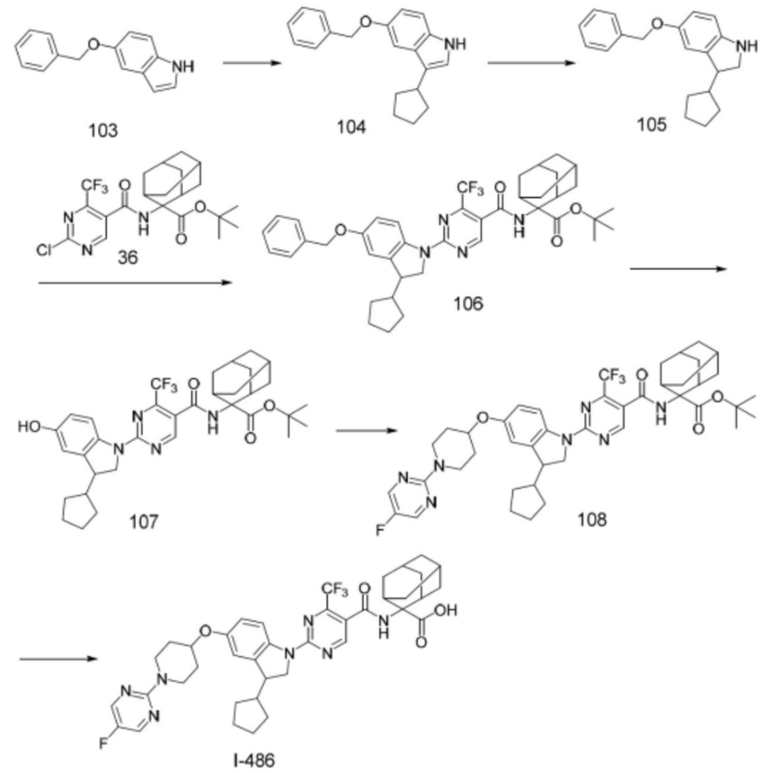
Стадия 1: Синтез Соединения 104
Раствор триэтилсилана (1,7 мл, 10,75 ммоль) и трихлоруксусной кислоты (1,1 г, 6,72 ммоль) в толуоле (5 мл) перемешивают при 70°C, и раствор Соединения 103 (1 г, 4,48 ммоль) и циклопентанона (414 мг, 4,93 ммоль) в толуоле (10 мл) добавляют по каплям. Смесь перемешивают при 70°C в течение 40 мин. Смесь охлаждают до комнатной температуры, и добавляют 10% водный раствор карбоната натрия. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 104 (600 мг, выход 46%).
ЖХ/МС(ИЭР):m/z= 292 [M+H]+, ВУ=2,98 мин, ЖХ/МС Способ 1
[0203]
Стадия 2: Синтез Соединения 105
Соединение 104 (570 мг, 1,96 ммоль) растворяют в уксусной кислоте (2 мл), и цианоборгидрид натрия (246 мг, 3,91 ммоль) добавляют при охлаждении льдом. После перемешивания при комнатной температуре в течение 50 минут, водный раствор карбоната калия добавляют для нейтрализации смеси. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 105 (340 мг, выход 59%).
ЖХ/МС(ИЭР):m/z= 294 [M+H]+, ВУ=1,74 мин, ЖХ/МС Способ 1
[0204]
Стадия 3: Синтез Соединения 106
Соединение 36 (266 мг, 0,58 ммоль), диизопропиламин (0,2 мл, 1,16 ммоль) и Соединение 105 (170 мг, 0,58 ммоль) растворяют в 1,4-диоксане (2,55 мл) и перемешивают при 90°C в течение 1 часа. Добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией на амино (гексан-этилацетат) с получением Соединения 106 (330 мг, выход 80%).
ЖХ/МС(ИЭР):m/z= 717 [M+H]+, ВУ=2,96 мин, ЖХ/МС Способ 7
[0205]
Стадия 4: Синтез Соединения 107
Соединение синтезируют по методике, описанной на Стадии 4 Примера 3.
ЖХ/МС(ИЭР):m/z= 627 [M+H]+, ВУ=3,42 мин, ЖХ/МС Способ 1
[0206]
Стадия 5: Синтез Соединения 108
Соединение синтезируют по методике, описанной на Стадии 5 Примера 3.
ЖХ/МС(ИЭР):m/z= 806 [M+H]+, ВУ=3,12 мин, ЖХ/МС Способ 7
[0207]
Стадия 6: Синтез Соединения (I-486)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
1H-ЯМР (CDCl3) δ: 1,23-1,72 (м, 5H), 1,81 (дд, J=14,9, 7,5 Гц, 9H), 1,95-1,99 (м, 8H), 2,15-2,21 (м, 3H), 2,68 (с, 2H), 3,38-3,41 (м, 1H), 3,66-3,68 (m 2H), 4,09-4,14 (м, 3H), 4,28 (т, J=10,5 Гц, 1H), 4,50-4,53 (м, 1H), 6,02 (с, 1H), 6,86-6,92 (м, 2H), 8,20 (с, 2H), 8,28 (д, J=8,3 Гц, 1H), 8,78 (с, 1H), 12,34 (с, 1H).
ЖХ/МС(ИЭР):m/z= 750 [M+H]+, ВУ=3,56 мин, ЖХ/МС Способ 1
[0208]
Пример 13
Синтез Соединения (I-591)
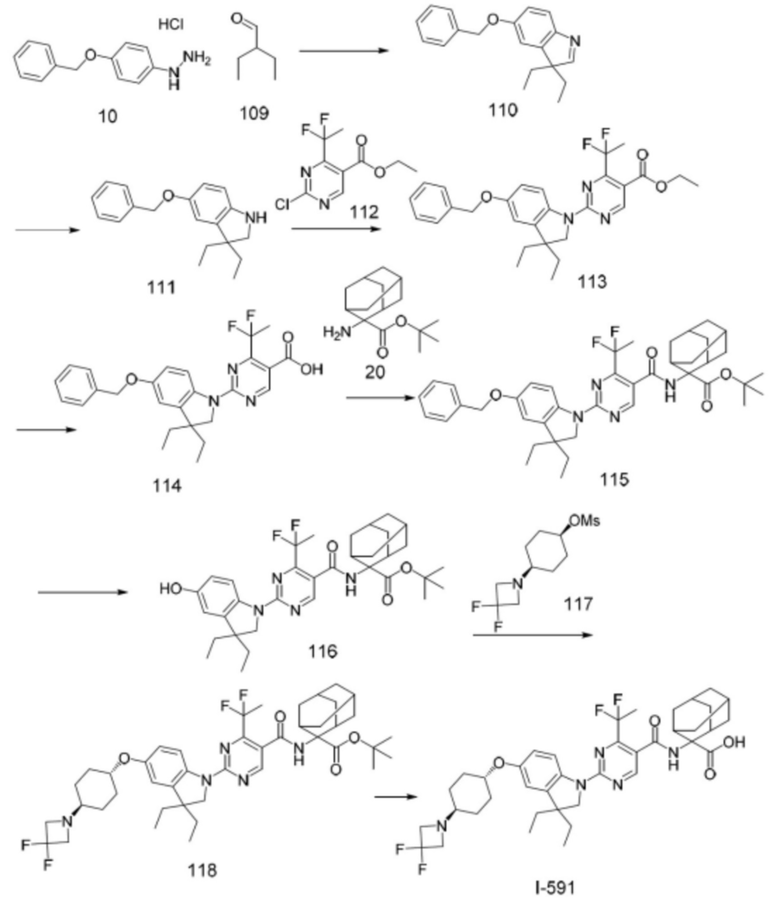
Стадия 1: Синтез Соединения 110
Соединение 10 (42 г, 166 ммоль) и Соединение 109 (16,6 г, 166 ммоль) суспендируют в дихлорметане (250 мл) и охлаждают на ледяной бане. Добавляют трифторуксусную кислоту (25,6 мл, 332 ммоль), и смесь нагревают до 45°C и перемешивают в течение 5 часов. Смесь охлаждают на ледяной бане, и нейтрализуют добавлением водного раствора карбоната натрия, затем экстрагируют хлороформом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 110 (8,9 г, выход 19%).
ЖХ/МС(ИЭР):m/z= 280 [M+H]+, ВУ=2,59 мин, ЖХ/МС Способ 1
[0209]
Стадия 2: Синтез Соединения 111
Соединение синтезируют по методике, описанной на Стадии 2 Примера 3.
ЖХ/МС(ИЭР):m/z= 282 [M+H]+, ВУ=1,57 мин, ЖХ/МС Способ 1
[0210]
Стадия 3: Синтез Соединения 113
Соединение синтезируют по методике, описанной на Стадии 3 Примера 3.
ЖХ/МС(ИЭР):m/z= 496 [M+H]+, ВУ=3,60 мин, ЖХ/МС Способ 1
[0211]
Стадия 4: Синтез Соединения 114
Соединение синтезируют по методике, описанной на Стадии 6 Примера 3.
ЖХ/МС(ИЭР):m/z= 468 [M+H]+, ВУ=3,14 мин, ЖХ/МС Способ 1
[0212]
Стадия 5: Синтез Соединения 115
Соединение 114 (570 мг, 1,22 ммоль) и Соединение 20 (429 мг, 1,71 ммоль) растворяют в диметилформамиде (8,6 мл), и ГАТУ (788 мг, 2,07 ммоль) и добавляют триэтиламин (0,39 мл, 2,8 ммоль). После перемешивания при комнатной температуре в течение 15 часов, добавляют воду. Выпавшее в осадок твердое вещество фильтруют и очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 115 (740 мг, выход 87%).
ЖХ/МС(ИЭР):m/z= 701 [M+H]+, ВУ= 3,88 мин, ЖХ/МС Способ 1
[0213]
Стадия 6: Синтез Соединения 116
Соединение синтезируют по методике, описанной на Стадии 4 Примера 3.
ЖХ/МС(ИЭР):m/z= 611 [M+H]+, ВУ=1,42 мин, ЖХ/МС Способ 7
[0214]
Стадия 7: Синтез Соединения 118
Соединение 116 (70 мг, 0,115 ммоль) растворяют в диметилформамиде (1,05 мл). Добавляют карбонат цезия (45 мг, 0,14 ммоль) и Соединение 117 (31 мг, 0,11 ммоль), и смесь перемешивают при 90°C в течение 1 часа. То же количество карбоната цезия и Соединения 117 добавляют четыре раза каждые 30 минут. После подтверждения потребления исходного материала, добавляют воду для гашения реакции. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией на амино (гексан-этилацетат) с получением Соединения 118 (63 мг, выход 70%).
ЖХ/МС(ИЭР):m/z= 784 [M+H]+, ВУ= 3,17 мин, ЖХ/МС Способ 1
[0215]
Стадия 8: Синтез Соединения (I-591)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
1H-ЯМР (ДМСО-d6) δ: 0,70 (т, J=7,3 Гц, 6H), 1,12-1,24 (м, 2H), 1,29-1,39 (м, 2H), 1,53-1,78 (м, 14H), 1,98-2,24 (м, 10H), 2,50-2,55 (м, 2H), 3,54 (т, J=12,4 Гц, 4H), 3,95 (с, 2H), 4,26-4,29 (м, 1H), 6,81-6,83 (м, 2H), 8,16 (д, J=8,8 Гц, 1H), 8,29 (с, 1H), 8,47 (с, 1H), 12,27 (шс, 1H).
[0216]
Пример 14
Синтез Соединения (I-594)
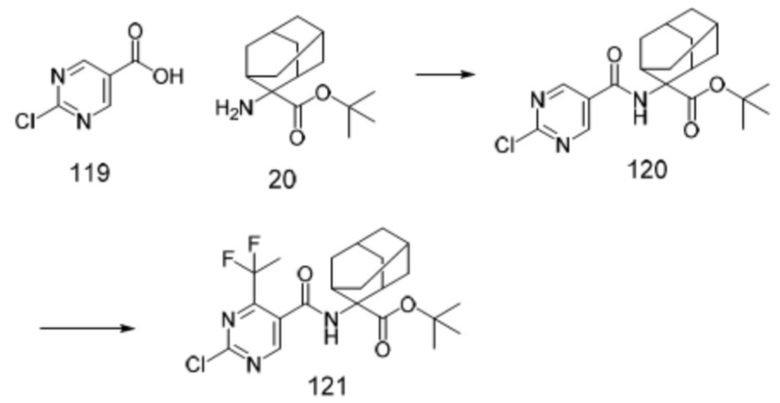
Стадия 1: Синтез Соединения 120
Соединение 119 (3 г, 18,9 ммоль) растворяют в дихлорметане (30 мл), и добавляют оксалилхлорид (1,8 мл, 20,8 ммоль) и диметилформамид (0,15 мл, 1,9 ммоль) при охлаждении на льду. После перемешивания при комнатной температуре в течение 1 часа, реакционный раствор концентрируют при пониженном давлении.
Остаток растворяют в дихлорметане (5 мл), и добавляют по каплям к раствору Соединения 20 (4,76 г, 18,9 ммоль) и триэтиламина (5,3 мл, 37,8 ммоль) в дихлорметане (30 мл) при охлаждении льдом. Через 1 час, реакцию гасят добавлением воды, затем экстрагируют хлороформом. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток суспендируют в этилацетате и диизопропиловом эфире. Твердое вещество фильтруют с получением Соединения 120 (7,0 г, выход 94%).
1H-ЯМР (CDCl3) δ: 1,46 (с, 9H), 1,73-1,82 (м, 6H), 1,86-1,99 (м, 4H), 2,17 (м, 2H), 2,59 (с, 2H), 6,14 (с, 1H), 8,95 (с, 2H).
[0217]
Стадия 2: Синтез Соединения 121
Соединение 120 (3,8 г, 9,7 ммоль) суспендируют в ацетонитриле (30 мл) и воде (15 мл), и добавляют 2,2-дифторпропионовую кислоту (2,1 г, 19,4 ммоль), нитрат серебра (4,9 г, 29,1 ммоль) и персульфата аммония (8,8 г, 38,8 ммоль). Смесь нагревают до 80°C и перемешивают в течение 1 часа. Реакцию охлаждают на ледяной бане, гасят водным раствором тиосульфата натрия, затем фильтруют через Целит (зарегистрированная торговая марка). Фильтрат экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 121 (670 мг, выход 15%).
1H-ЯМР (ДМСО-d6) δ: 1,42 (с, 9H), 1,56 (м, 2H), 1,65-1,79 (м, 4H), 1,99 (т, J=19,2Гц, 3H), 2,05 (м, 4H), 2,53 (с, 2H), 8,54 (с, 1H), 8,74 (с, 1H).
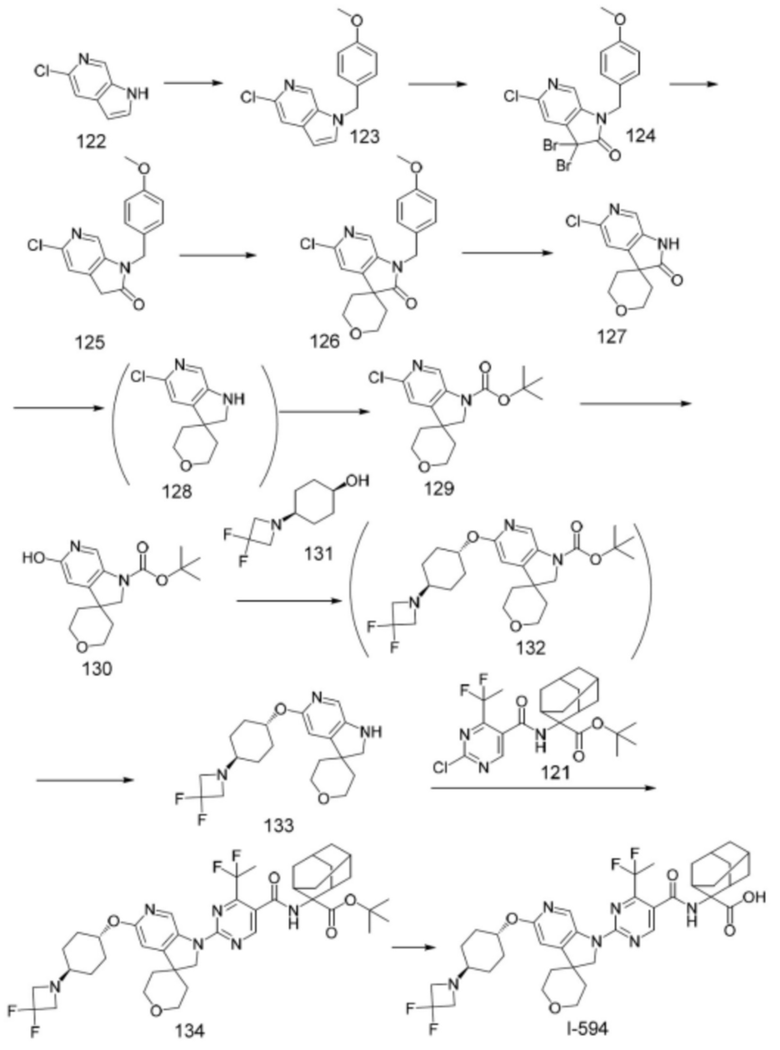
Стадия 1: Синтез Соединения 123
Соединение 122 (51,5 г, 337 ммоль) растворяют в диметилформамиде (386 мл), и добавляют карбонат цезия (165 г, 506 ммоль), 4-метоксибензилхлорид (53,4 г, 341 ммоль). После перемешивания при комнатной температуре в течение 45 минут добавляют воду. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток отверждают добавлением гексана и этилацетата, и фильтруют с получением Соединения 123 (90,9 г, выход 99%).
ЖХ/МС(ИЭР):m/z= 273 [M+H]+, ВУ=2,21 мин, ЖХ/МС Способ 1
[0218]
Стадия 2: Синтез Соединения 124
Соединение 123 (81,2 г, 298 ммоль) растворяют в 1,4-диоксане (812 мл), и добавляют трибромид пиридиния (349 г, 1,09 моль). После перемешивания при комнатной температуре в течение 45 минут добавляют воду. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении с получением Соединения 124 (154,6 г) в виде неочищенного продукта.
ЖХ/МС(ИЭР):m/z= 445 [M+H]+, ВУ=2,58 мин, ЖХ/МС Способ 1
[0219]
Стадия 3: Синтез Соединения 125
Неочищенный продукт Соединения 124 (154,6 г) растворяют в тетрагидрофуране (1065 мл) и метаноле (266 мл), и уксусную кислоту (42,6 мл) и цинк (97 г, 1490 ммоль) добавляют при охлаждении на льду. После перемешивания в течение 1 часа, реакционный раствор фильтруют через Целит (зарегистрированная торговая марка) для удаления нерастворимого продукта. Фильтрат концентрируют при пониженном давлении, и к полученному твердому веществу добавляют воду. Суспензию перемешивают при комнатной температуре, и твердое вещество фильтруют с получением Соединения 125 (87 г, выход 100%).
ЖХ/МС(ИЭР):m/z= 289 [M+H]+, ВУ=2,58 мин, ЖХ/МС Способ 1
[0220]
Стадия 4: Синтез Соединения 126
Соединение 125 (220 мг, 0,76 ммоль) растворяют в диметилформамиде (3,3 мл), и добавляют карбонат цезия (745 мг, 2,29 ммоль) и 2-йодэтиловый эфир (497 мг, 1,52 ммоль). После перемешивания при комнатной температуре в течение 3 часов добавляют воду. Смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 126 (245 мг, выход 90%).
ЖХ/МС(ИЭР):m/z= 359 [M+H]+, ВУ=2,05 мин, ЖХ/МС Способ 1
[0221]
Стадия 5: Синтез Соединения 127
К Соединению 126 (130 мг, 0,36 ммоль) добавляют трифторуксусную кислоту (0,52 мл) и трифторметансульфоновую кислоту (0,33 мл), и смесь перемешивают при 50°C в течение 1 часа. Реакционный раствор выливают в водный раствор карбоната натрия и нейтрализуют, затем экстрагируют этилацетатом. Органический слой промывают водой, сушат над безводным сульфатом натрия, и растворитель удаляют при пониженном давлении. Остаток отверждают добавлением этилацетата и диизопропилового эфира, и твердое вещество фильтруют с получением Соединения 127 (56 мг, выход 65%).
ЖХ/МС(ИЭР):m/z= 239 [M+H]+, ВУ=1,22 мин, ЖХ/МС Способ 1
[0222]
Стадия 6: Синтез Соединения 129
К Соединению 127 (640 мг, 2,68 ммоль) добавляют 0,91 моль/л раствора комплекса бора-тетрагидрофурана - тетрагидрофурана (20 мл, 18,2 ммоль), и смесь перемешивают при 70°C в течение 30 минут. После охлаждения на льду, добавляют метанол (10 мл), и смесь перемешивают при 80°C в течение 30 минут. После охлаждения, реакционный раствор концентрируют при пониженном давлении, и остаток растворяют в дихлорметане (10 мл). Добавляют триэтиламин (1,36 г, 13,4 ммоль), Boc2O (2,92 г, 13,4 ммоль), дметиламинопиридин (327 мг, 2,68 ммоль), и смесь перемешивают при комнатной температуре в течение 16 часов. Реакционный раствор концентрируют, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 129 (550 мг, выход 63%).
ЖХ/МС(ИЭР):m/z= 325 [M+H]+, ВУ=2,27 мин, ЖХ/МС Способ 1
[0223]
Стадия 8: Синтез Соединения 130
Соединение 129 (200 мг, 0,616 ммоль) растворяют в 1,4-диоксане (3 мл), и добавляют Me4tBuXphos (30 мг, 0,062 ммоль), Pd2(dba)3 (28 мг, 0,031 ммоль), 6 моль/л водный раствор гидроксида калия (0,36 мл, 2,16 ммоль), и смесь перемешивают при 100°C в течение 1 часа. После охлаждения, смесь нейтрализуют 2 моль/л раствором хлористоводородной кислоты и экстрагируют дихлорметаном. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении. Этилацетат-диизопропиловый эфир добавляют к полученному остатку, и выпавшее в осадок твердое вещество фильтруют с получением Соединения 130 (171 мг, выход 91%).
ЖХ/МС(ИЭР):m/z= 307 [M+H]+, ВУ=1,42 мин, ЖХ/МС Способ 1
[0224]
Стадия 9: Синтез Соединения 133
Соединение 130 (171 мг, 0,558 ммоль) растворяют в тетрагидрофуране (2 мл), и добавляют трифенилфосфин (293 мг, 1,12 ммоль), Соединение 131 (213 мг, 1,12 ммоль) и ДИАД (226 мг, 1,12 ммоль), и смесь перемешивают при комнатной температуре. Через 30 минут, добавляют трифенилфосфин (293 мг, 1,12 ммоль), Соединение 131 (213 мг, 1,12 ммоль) и ДИАД (226 мг, 1,12 ммоль). После перемешивания при комнатной температуре в течение 1 часа, растворитель удаляют при пониженном давлении.
Трифторуксусную кислоту (4 мл) добавляют к остатку и перемешивают при комнатной температуре в течение 1 часа. Реакционный раствор концентрируют. Дихлорметан добавляют к остатку для растворения. Водный раствор бикарбоната натрия добавляют для нейтрализации, и слои разделяют. Водный слой экстрагируют дихлорметан, и органические слои объединяют и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 133 (212 мг, выход 100%).
ЖХ/МС(ИЭР):m/z= 380 [M+H]+, ВУ=0,80 мин, ЖХ/МС Способ 1
[0225]
Стадия 10: Синтез Соединения 134
Соединение 133 (70 мг, 0,184 ммоль) растворяют в 1,4-диоксане (2 мл), и добавляют Соединение 121 (101 мг, 0,221 ммоль), карбонат калия (76 мг, 0,552 ммоль), Xanthos Pd G3 (26 мг, 0,028 ммоль). Смесь перемешивают при 80°C в течение 90 минут в атмосфере азота. Добавляют воду и экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют при пониженном давлении, и остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 134 (66 мг, выход 45%).
ЖХ/МС(ИЭР):m/z= 799 [M+H]+, ВУ=2,49 мин, ЖХ/МС Способ 8
[0226]
Стадия 11: Синтез Соединения (I-594)
Соединение 134 (66 мг, 0,083 ммоль) растворяют в трифторуксусной кислоте (4 мл) и перемешивают при комнатной температуре в течение 1 часа. Реакционный раствор концентрируют, растворяют в дихлорметане и нейтрализуют водным раствором бикарбоната натрия. Реакционный раствор снова подкисляют добавлением водного раствора лимонной кислоты, и экстрагируют дихлорметаном. Органический слой сушат над безводным сульфатом натрия. Растворитель удаляют, и остаток очищают колоночной хроматографией с силикагелем (хлороформ-метанол) с получением Соединения (I-594) (37 мг, выход 60%).
1H-ЯМР (ДМСО-d6) δ: 1,12-1,24 (м, 2H), 1,35-1,43 (м, 2H), 1,53-1,79 (м, 12H), 1,90-2,14 (м, 11H), 2,20-2,26 (м, 1H), 2,56 (с, 2H), 3,50-3,58 (м, 6H), 3,87-3,90 (м, 2H), 4,21 (с, 2H), 4,88-4,95 (м, 1H), 6,85 (с, 1H), 8,37 (шс, 1H), 8,54 (с, 1H), 8,91 (с, 1H), 12,33 (шс, 1H).
[0227]
(Эталонный пример)
Синтез Соединения 117 и Соединение 131
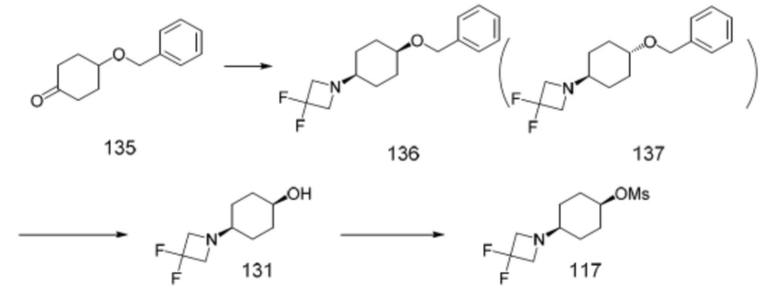
Стадия 1: Синтез Соединения 136 и Соединение 137
Соединение 135 (1,0 г, 4,90 ммоль) растворяют в дихлорметане (10 мл), и добавляют гидрохлорид 3,3-дифторазетидина (1,27 г, 9,79 ммоль), триэтиламин (1,26 мл, 9,79 ммоль), уксусную кислоту (0,28 мл, 4,90 ммоль) и триацетоксиборгидрид натрия (2,08 г, 9,79 ммоль) и перемешивают в течение 3 часов. Добавляют воду, затем экстрагируют хлороформом. Органический слой промывают водой и сушат над безводным сульфатом натрия. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат) с получением Соединения 136 (846 мг, 61% выход) и Соединения 137 (454 мг, выход 33%).
Соединение 136
1H-ЯМР (CDCl3) δ: 1,44-1,60 (м, 6H), 1,90-1,96 (м, 2H), 2,14-2,19 (м, 1H), 3,53 (т, J=12,4Гц, 4H), 3,55 (м, 1H), 4,50 (с, 2H), 7,23-7,28 (м, 1H), 7,30-7,36 (м, 4H).
ЖХ/МС(ИЭР):m/z= 282 [M+H]+, ВУ=1,24 мин, ЖХ/МС Способ 1
Соединение 137
1H-ЯМР (CDCl3) δ: 1,08-1,18 (м, 2H), 1,26-1,39 (м, 2H), 1,77-1,81 (м, 2H), 2,05-2,15 (м, 3H), 3,33-3,40 (м, 1H), 3,54 (т, J=11,6Гц, 4H), 4,54 (с, 2H), 7,25-7,30 (м, 1H), 7,31-7,34 (м, 4H).
ЖХ/МС(ИЭР):m/z= 282 [M+H]+, ВУ=1,20 мин, ЖХ/МС Способ 1
[0228]
Стадия 2: Синтез Соединения 131
Соединение 136 (0,72 г, 2,55 ммоль) растворяют в этаноле (10,7 мл), и добавляют 10% масс. палладий на угле (1,09 г, 0,51 ммоль). Смесь перемешивают при 50°C в течение 3 часов в атмосфере водорода. Реакционный раствор фильтруют через Целит (зарегистрированная торговая марка), и фильтрат концентрируют при пониженном давлении с получением Соединения 131 (0,42 г, выход 86%).
Соединение 131
1H-ЯМР (CDCl3) δ: 1,30 (шс, 1H), 1,44-1,61 (м, 6H), 1,69-1,79 (м, 2H), 2,20 (м, 1H), 3,53 (т, J=12,0Гц, 4H), 3,81 (м, 1H).
[0229]
Стадия 3: Синтез Соединения 117
Соединение 131 (300 мг, 1,57 ммоль) растворяют в дихлорметане (3 мл), и добавляют триэтиламин (0,44 мл, 3,14 ммоль) и метансульфонилхлорид (0,18 мл, 2,35 ммоль) при охлаждении на льду. Через 1 час 30 минут, добавляют водный раствор хлорида аммония, затем экстрагируют этилацетатом. Органический слой промывают водой и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении с получением Соединения 117 (419 мг, выход 99%).
1H-ЯМР (CDCl3) δ: 1,53-1,59 (м, 4H), 1,62-1,72 (м, 2H), 2,03-2,13 (м, 2H), 2,23 (м, 1H), 3,00 (с, 3H), 3,54 (т, J=12,0Гц, 4H), 4,86 (м, 1H).
[0230]
Пример 15
Синтез Соединения (I-570)
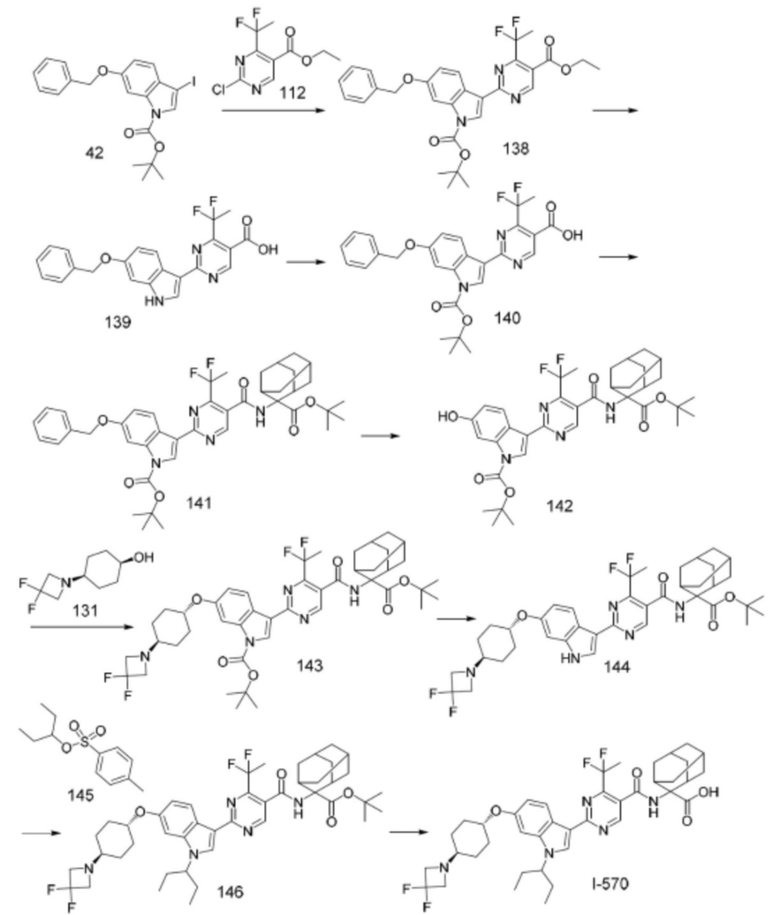
Стадия 1: Синтез Соединения 138
Соединение синтезируют по методике, описанной на Стадии 1 Примера 6.
1H-ЯМР (ДМСО-d6) δ: ч/млн 1,33 (т, J=7,15 Гц, 3 H), 1,67 (с, 9 H), 2,17 (т, J=19,32 Гц, 3 H), 4,38 (кв, J=7,15 Гц, 2 H), 5,21 (с, 2 H), 7,16 (дд, J=8,9, 2,3 Гц, 1 H), 7,32-7,38 (м, 1 H), 7,39-7,44 (м, 2 H), 7,48-7,52 (м, 2 H), 7,82 (д, J=2,1 Гц, 1 H), 8,43 (с, 1 H), 8,45 (д, J=8,9 Гц, 1 H), 9,19 (с, 1 H).
ЖХ/МС(DUIS):m/z= 538 [M+H]+, ВУ=2,08 мин, ЖХ/МС Способ 9
[0231]
Стадия 2: Синтез Соединения 139
К раствору Соединения 138 (7,48 г, 13,9 ммоль) в тетрагидрофуране (59,8 моль), метаноле (29,9 мл) и воде (15,0 мл) добавляют моногидрат гидроксида лития (2,92 г, 69,6 ммоль) при комнатной температуре, и смесь перемешивают в течение 5 часов при комнатной температуре. После завершения реакции, смесь концентрируют при пониженном давлении, и остаток разбавляют водой и нейтрализуют 2 моль/л хлористоводородной кислоты (35 мл, 70,0 ммоль), и раствор экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли, сушат над безводным сульфатом натрия, и концентрируют при пониженном давлении с получением Соединения 139 (4,81 г, выход 84%).
1H-ЯМР (ДМСО-d6) δ: ч/млн 2,14 (т, J=19,1 Гц, 3 H), 5,16 (с, 2 H), 6,96 (дд, J=8,8, 2,3 Гц, 1 H), 7,07 (д, J=2,3 Гц, 1 H), 7,29-7,37 (м, 1 H), 7,38-7,45 (м, 2 H), 7,47-7,52 (м, 2 H), 8,23 (д, J=2,9 Гц, 1 H), 8,34 (д, J=8,7 Гц, 1 H), 9,00 (с, 1 H), 11,76 (д, J=2,4 Гц, 1 H), 13,45 (шс, 1 H).
ЖХ/МС(DUIS):m/z= 410 [M+H]+, ВУ=1,32 мин, ЖХ/МС Способ 9
[0232]
Стадия 3: Синтез Соединения 140
К раствору Соединения 139 (4,8 г, 11,72 ммоль) в дихлорметане (48,0 мл) и диметилформамиде (2,0 мл) добавляют триэтиламин (2,45 мл, 17,58 ммоль), Boc2O (3,23 мл, 14,06 ммоль) и ДМАП (72 мг, 0,59 ммоль) при комнатной температуре при перемешивании под потоком аргона, и смесь перемешивают при комнатной температуре в течение 4 часов. После завершения реакции, добавляют воду, и смесь экстрагируют этилацетатом. Органический слой промывают 0,5 моль/л хлористоводородной кислоты и насыщенным раствором соли, сушат над безводным сульфатом магния, и концентрируют при пониженном давлении. Затем добавляют смесь гексана-этилацетата, и смесь обрабатывают ультразвуком и фильтруют. Промывают дополнительной смесью гексана-этилацетата и сушат с получением Соединения 140 (2,46 г, выход 41%).
1H-ЯМР (ДМСО-d6) δ: ч/млн 1,67 (с, 9 H), 2,16 (т, J=19,3 Гц, 3 H), 5,21 (с, 2 H), 7,16 (дд, J=8,8, 2,4 Гц, 1 H), 7,32-7,37 (м, 1 H), 7,39-7,44 (м, 2 H), 7,48-7,52 (м, 2 H), 7,83 (д, J=2,3 Гц, 1 H), 8,42 (с, 1 H), 8,46 (д, J=8,8 Гц, 1 H), 9,17 (с, 1 H), 13,81 (шс, 1 H).
ЖХ/МС(DUIS):m/z= 510 [M+H]+, ВУ=1,79 мин, ЖХ/МС Способ 9
[0233]
Стадия 4: Синтез Соединения 141
Соединение синтезируют по методике, описанной на Стадии 3 Примера 4.
1H-ЯМР (ДМСО-d6) δ: ч/млн 1,45 (с, 9 H), 1,54-1,60 (м, 2 H), 1,67 (с, 9 H), 1,68-1,73 (м, 4 H), 1,77-1,86 (м, 2 H), 2,10 (т, J=19,2 Гц, 3 H), 2,00-2,18 (м, 4 H), 2,52-2,57 (м, 2 H), 5,21 (с, 2 H), 7,16 (дд, J=8,9, 2,3 Гц, 1 H), 7,32-7,37 (м, 1 H), 7,39-7,44 (м, 2 H), 7,48-7,52 (м, 2 H), 7,82 (д, J=2,4 Гц, 1 H) 8,40 (с, 1 H), 8,48 (д, J=8,8 Гц, 1 H), 8,56 (шс, 1 H), 8,79 (с, 1 H).
ЖХ/МС(DUIS):m/z= 743 [M+H]+, ВУ=2,37 мин, ЖХ/МС Способ 9
[0234]
Стадия 5: Синтез Соединения 142
Соединение синтезируют по методике, описанной на Стадии 2 Примера 6.
1H-ЯМР (ДМСО-d6) δ: ч/млн 1,45 (с, 9 H), 1,57 (м, 2 H), 1,62-1,73 (м, 4 H), 1,67 (с, 9 H), 1,78-1,84 (м, 2 H), 2,10 (т, J=19,1 Гц, 3 H), 2,00-2,18 (м, 4 H), 2,51-2,55 (м, 2 H), 6,89 (дд, J=8,7, 2,3 Гц, 1 H), 7,63 (д, J=2,1 Гц, 1 H), 8,32 (с, 1 H), 8,36 (д, J=8,7 Гц, 1 H), 8,55 (шс, 1 H), 8,77 (с, 1 H), 9,68 (с, 1 H).
ЖХ/МС(DUIS):m/z= 653 [M+H]+, ВУ=1,92 мин, ЖХ/МС Способ 9
[0235]
Стадия 6: Синтез Соединения 143
Соединение синтезируют по методике, описанной на Стадии 5 Примера 3.
1H-ЯМР (ДМСО-d6) δ: ч/млн 1,12-1,25 (м, 2 H), 1,39-1,51 (м, 2 H), 1,45 (с, 9 H), 1,54-1,62 (м, 2 H), 1,68 (с, 9 H), 1,69-1,73 (м, 4 H), 1,75-1,85 (м, 4 H), 2,10 (t J=19,1 Гц, 3 H), 2,01 -2,18 (м, 6 H), 2,21-2,30 (м, 1 H), 2,52-2,55 (м, 2 H), 3,55 (т, J=12,3 Гц, 4 H), 4,32-4,42 (м, 1 H), 7,06 (дд, J=8,8, 2,3 Гц, 1 H), 7,69 (d J=2,1 Гц, 1 H), 8,40 (с, 1 H), 8,45 (д, J=8,8 Гц, 1 H), 8,55 (шс, 1 H), 8,78 (с, 1 H).
ЖХ/МС(DUIS):m/z= 826 [M+H]+, ВУ=1,88 мин, ЖХ/МС Способ 9
[0236]
Стадия 7: Синтез Соединения 144
Соединение синтезируют по методике, описанной на Стадии 2.
1H-ЯМР (ДМСО-d6) δ ч/млн 1,12-1,24 (м, 2 H), 1,37-1,42 (м, 2 H), 1,45 (с, 9 H), 1,53-1,61 (м, 2 H), 1,65-1,74 (м, 4 H), 1,75-1,85 (м, 4 H), 2,08 (т, J=19,0 Гц, 3 H), 2,00-2,19 (м, 6 H), 2,20-2,28 (м, 1 H), 2,52-2,55 (м, 2 H), 3,55 (т, J=12,4 Гц, 4 H), 4,25-4,37 (м, 1 H), 6,86 (дд, J=8,8, 2,3 Гц, 1 H), 7,00 (д, J=2,3Гц, 1 H) 8,19 (д, J=2,8 Гц, 1 H), 8,32 (д, J=8,8 Гц, 1 H), 8,46 (с, 1 H), 8,64 (с, 1 H), 11,62 (д, J=2,6 Гц, 1 H).
ЖХ/МС(DUIS):m/z= 726 [M+H]+, ВУ=1,47 мин, ЖХ/МС Способ 9
[0237]
Стадия 8: Синтез Соединения 146
К раствору Соединения 144 (50 мг, 0,07 ммоль) в N-метилпирролидоне (1,0 мл) добавляют карбонат цезия (67 мг, 0,21 ммоль) и Соединение 145 (50 мг, 0,21 ммоль) при комнатной температуре при перемешивании под потоком аргона, и смесь перемешивают при 100°C в течение 2 часов. Затем добавляют карбонат цезия (67 мг, 0,21 ммоль) и Соединение 145 (50 мг, 0,21 ммоль), и смесь перемешивают при 100°C в течение 3 часов. Затем добавляют карбонат цезия (67 мг, 0,21 ммоль) и Соединение 145 (50 мг, 0,21 ммоль), и смесь перемешивают при 100°C в течение 4 часов. После завершения реакции, добавляют воду к реакционному раствору, и смесь экстрагируют этилацетатом. Органический слой промывают насыщенным раствором соли, сушат над безводным сульфатом магния, и концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией с силикагелем (гексан-этилацетат). Дальнейшая очистка колоночной хроматографией на амино (гексан-этилацетат) дает Соединение 146 (42 мг, 77%).
1H-ЯМР (ДМСО-d6) δ: ч/млн 0,72 (т, J=7,3 Гц, 6 H), 1,19-1,28 (м, 2 H), 1,35-1,43 (м, 2 H), 1,45 (с, 9 H), 1,53-1,62 (м, 2 H), 1,65-1,72 (м, 4H), 1,74-1,83 (м, 4 H), 1,91 (квд, J=7,2 Гц, 4 H), 2,09 (т, J=19,0 Гц, 3 H), 2,01-2,18 (м, 6 H), 2,20-2,30 (м, 1 H), 2,52-2,56 (м, 2 H), 3,55 (т, J=12,4 Гц, 4 H), 4,32-4,47 (м, 2H), 6,89 (дд, J=8,9, 2,1 Гц, 1 H), 7,21 (д, J=1,9 Гц, 1 H), 8,24 (с, 1 H), 8,35 (д, J=8,8 Гц, 1 H), 8,45 (шс, 1 H), 8,63 (с, 1 H).
ЖХ/МС(ИЭР):m/z= 796 [M+H]+, ВУ=1,82 мин, ЖХ/МС Способ 10
[0238]
Стадия 9: Синтез Соединения (I-570)
Соединение синтезируют по методике, описанной на Стадии 8 Примера 10.
1H-ЯМР (ДМСО-d6) δ: ч/млн 0,71 (т, J=7,3 Гц, 6 H), 1,18-1,29 (м, 2 H), 1,34-1,47 (м, 2 H), 1,48-1,59 (м, 2 H), 1,59-1,73 (м, 4 H), 1,75-1,83 (м, 4 H), 1,86-1,94 (м, 4 H), 2,08 (т, J=19,0 Гц, 3H), 2,00-2,18 (м, 6 H), 2,19-2,28 (м, 1 H), 2,55-2,61 (м, 2 H), 3,55 (т, J=12,4 Гц, 4 H), 4,34-4,47 (м, 2 H), 6,88 (дд, J=8,9, 2,1 Гц, 1 H), 7,20 (д, J=1,9 Гц, 1 H), 8,21 (с, 1 H), 8,35 (д, J=8,8 Гц, 1 H), 8,46 (шс, 1 H), 8,64 (с, 1 H), 12,45 (шс, 1 H).
ЖХ/МС(DUIS):m/z= 740 [M+H]+, ВУ=1,36 мин, ЖХ/МС Способ 9
[0239]
Следующие соединения синтезируют согласно вышеуказанным общим способам синтеза и Примерам, как описано выше.
В структурной формуле, «клиновидный» и «пунктирная линия» означают стерео конфигурацию. В частности, для соединений, где указана стерео конфигурация, колонка «стереохимия» определена следующим образом.
пустая: как указано
a: рацемат
b: отдельный изомер, но его стереохимия неизвестна
c: диастереомерная смесь, при условии, что I-273, I-371, I-376, I-403, I-414, I 451, I-11, I-12 и I-13 включают их рацематы.
d: конфигурация группы-заместителя Zc(R7) такая, как показано, и конфигурация группы-заместителя R4 неизвестна
e: конфигурация группы-заместителя Zc(R7) неизвестна, и конфигурация группы-заместителя R4 такая, как показано
f: рацемат, и относительная конфигурация цис/транс является единственной, но неизвестной.
[0240]
[Таблица 1]
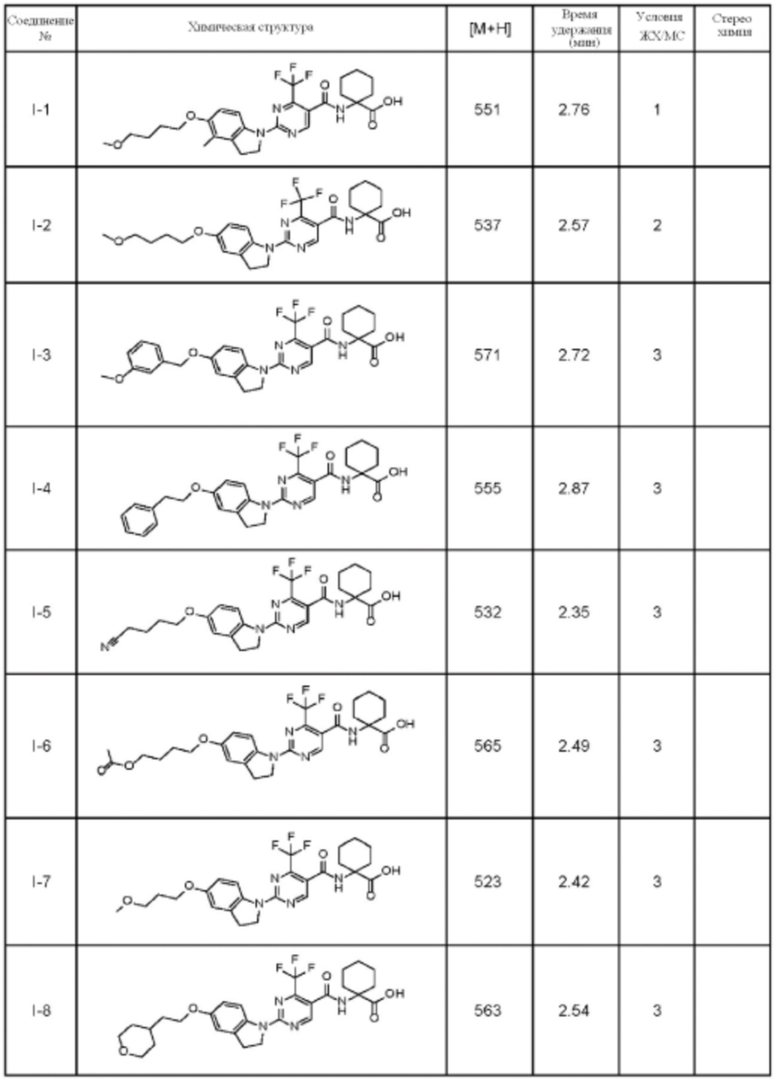
[0241]
[Таблица 2]
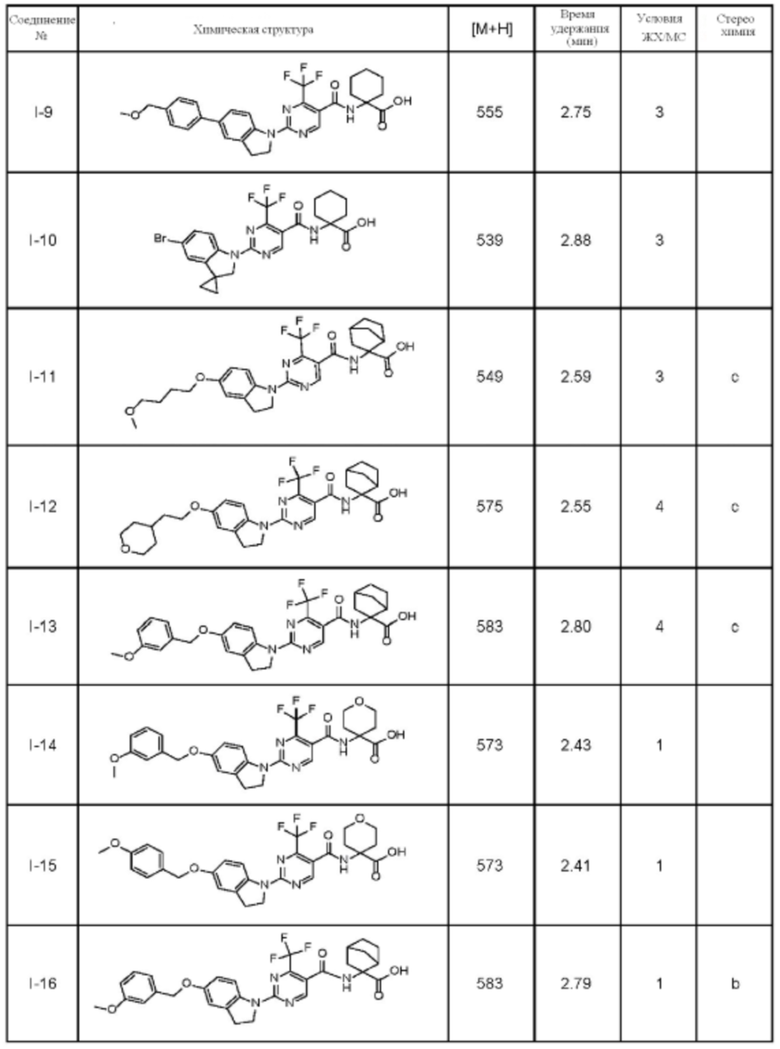
[0242]
[Таблица 3]
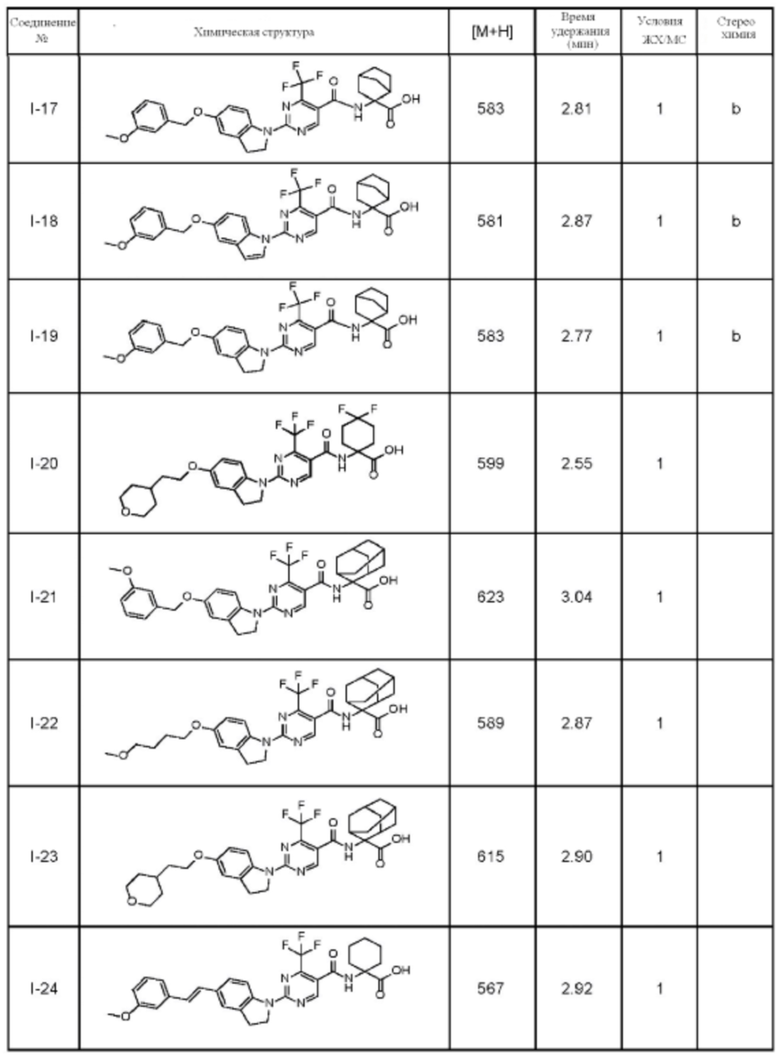
[0243]
[Таблица 4]
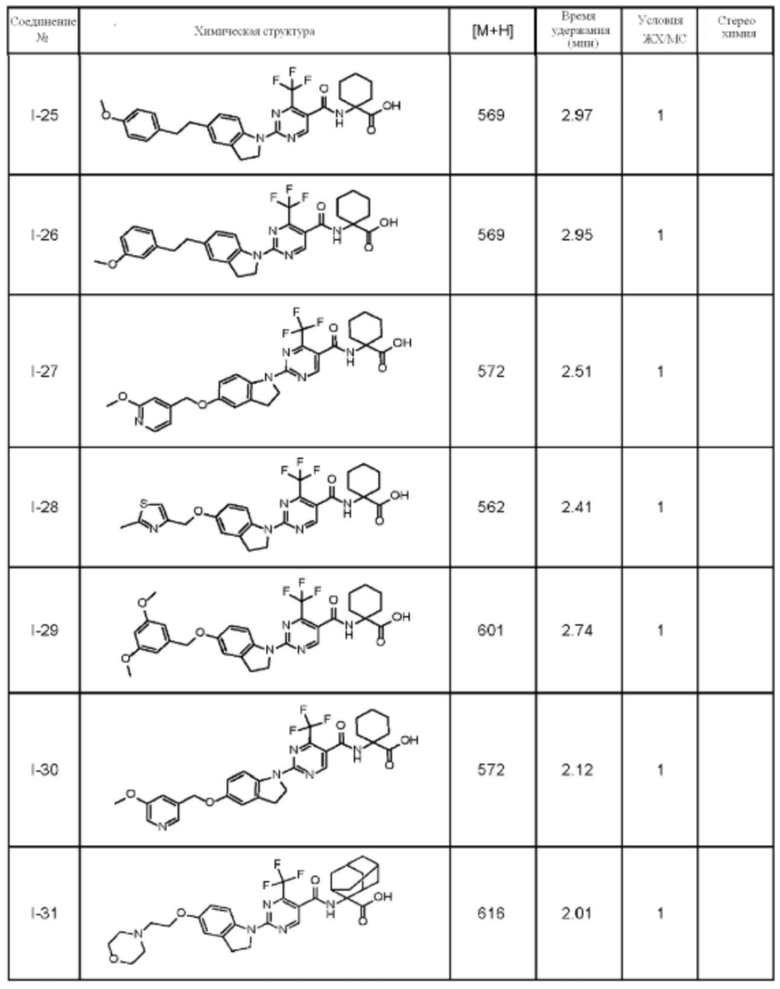
[0244]
[Таблица 5]
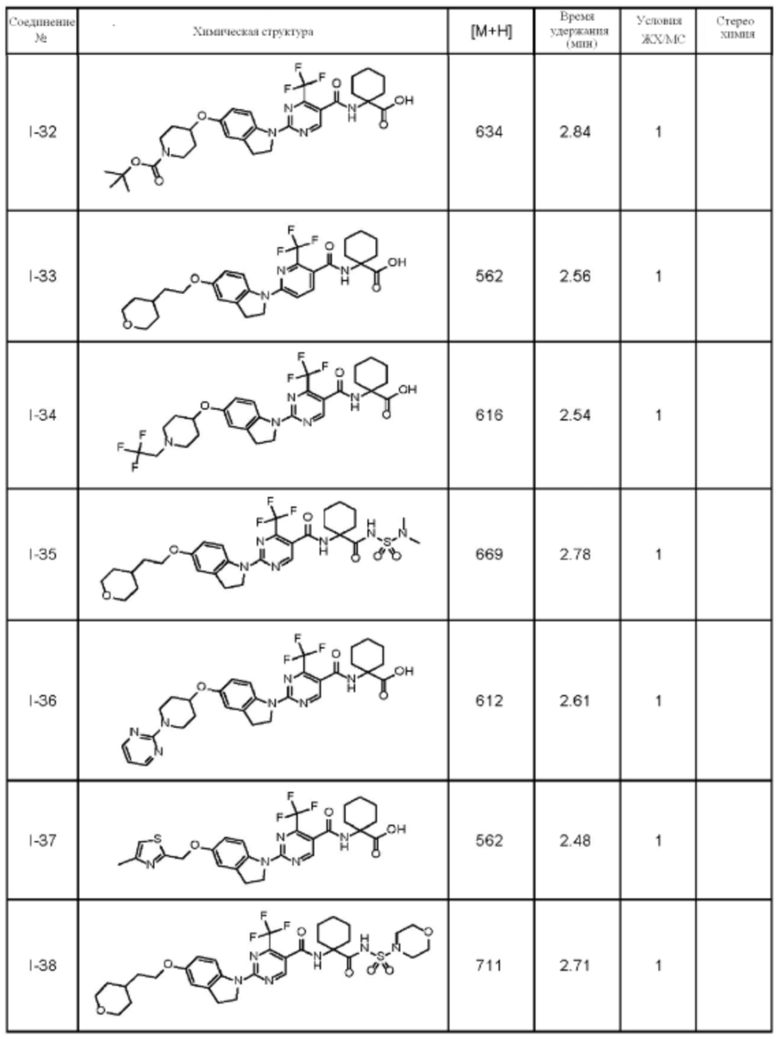
[0245]
[Таблица 6]
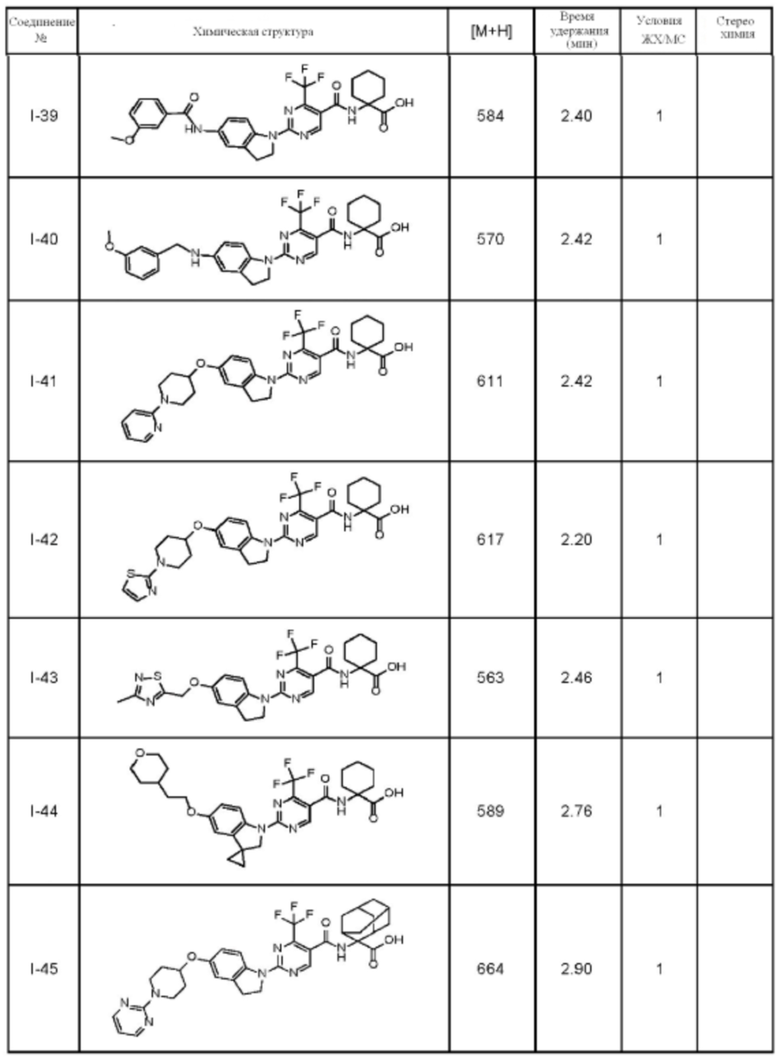
[0246]
[Таблица 7]
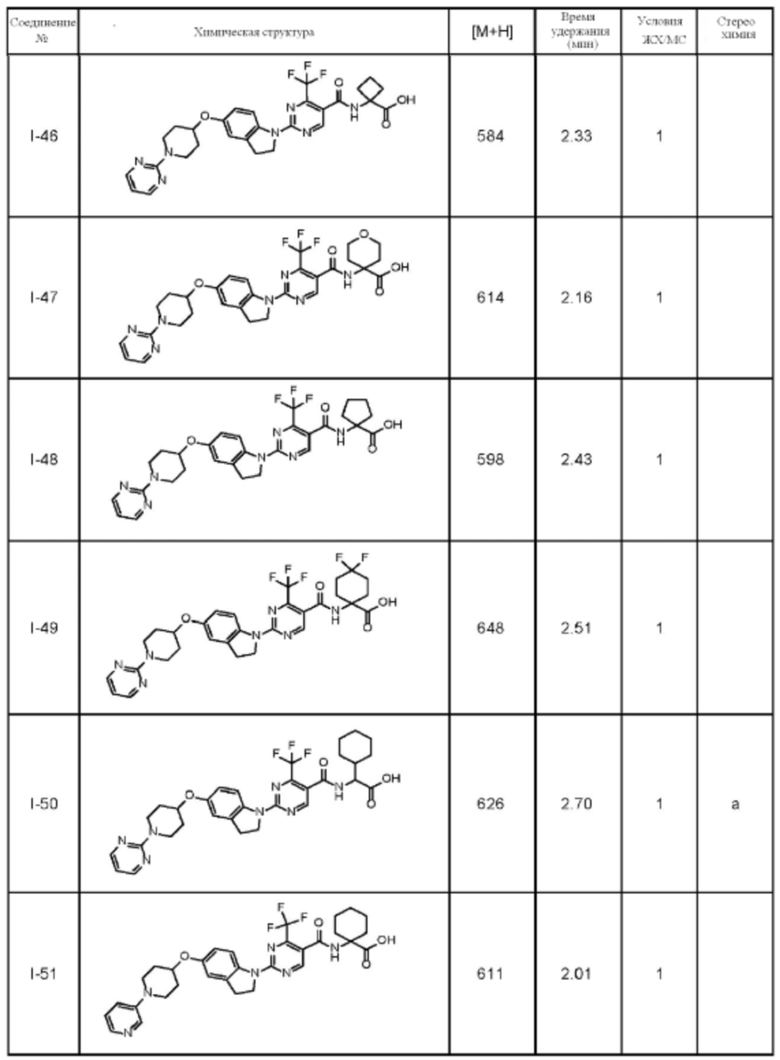
[0247]
[Таблица 8]
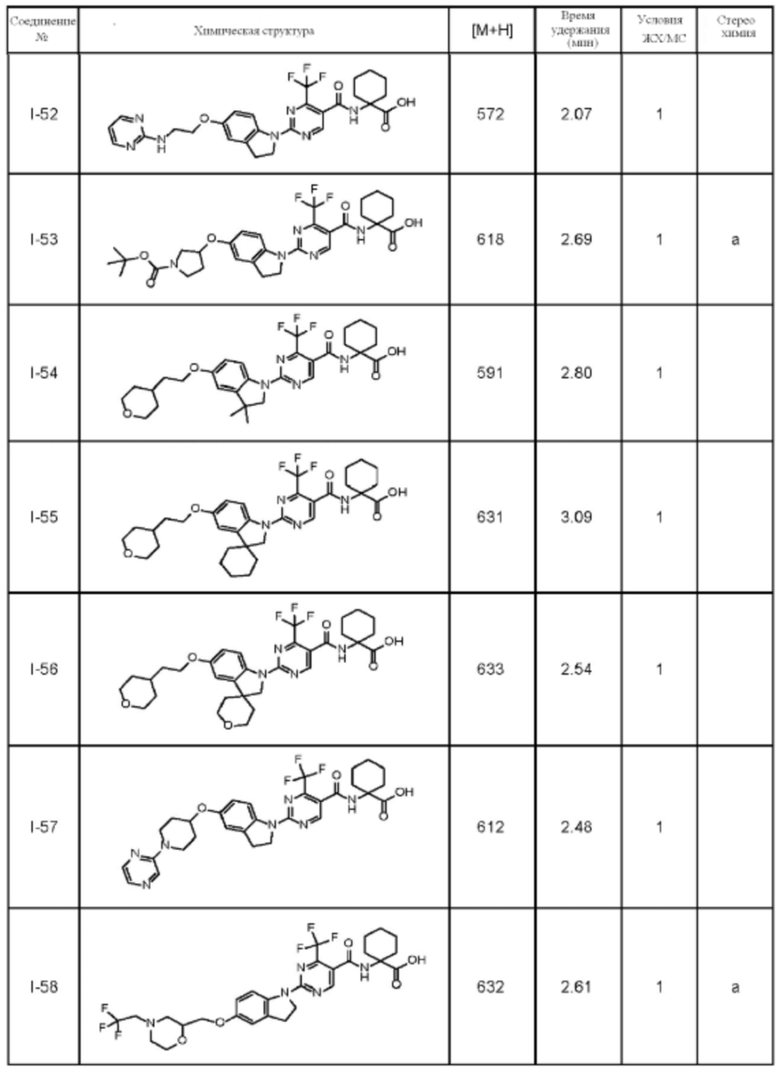
[0248]
[Таблица 9]
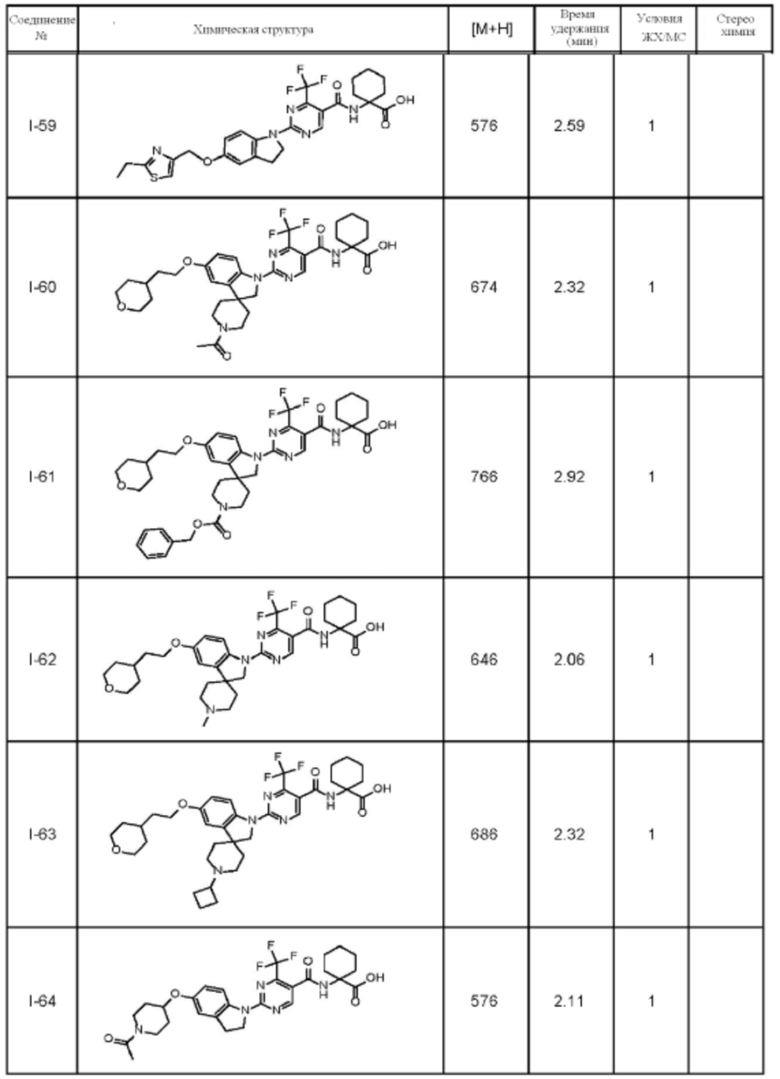
[0249]
[Таблица 10]
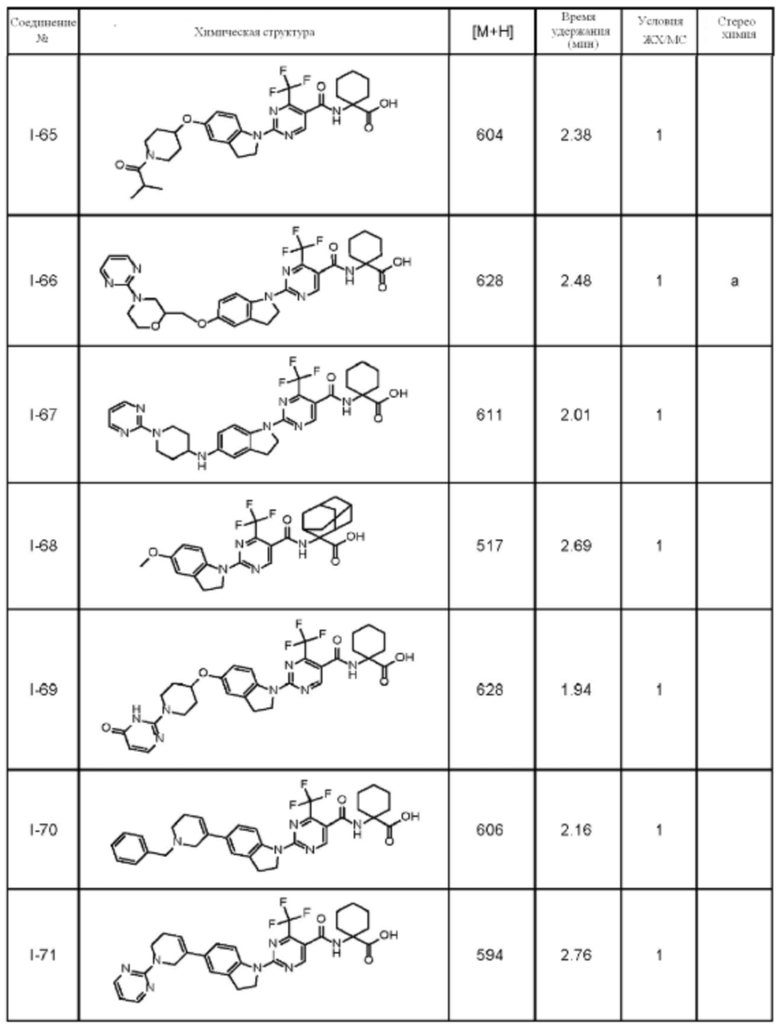
[0250]
[Таблица 11]
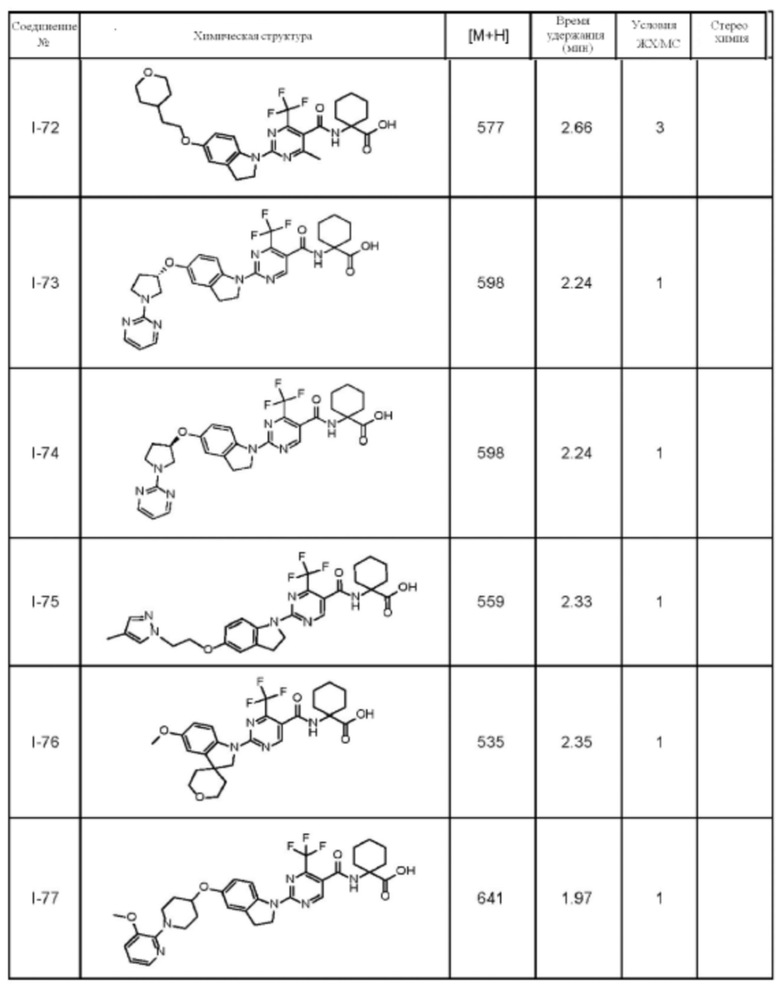
[0251]
[Таблица 12]
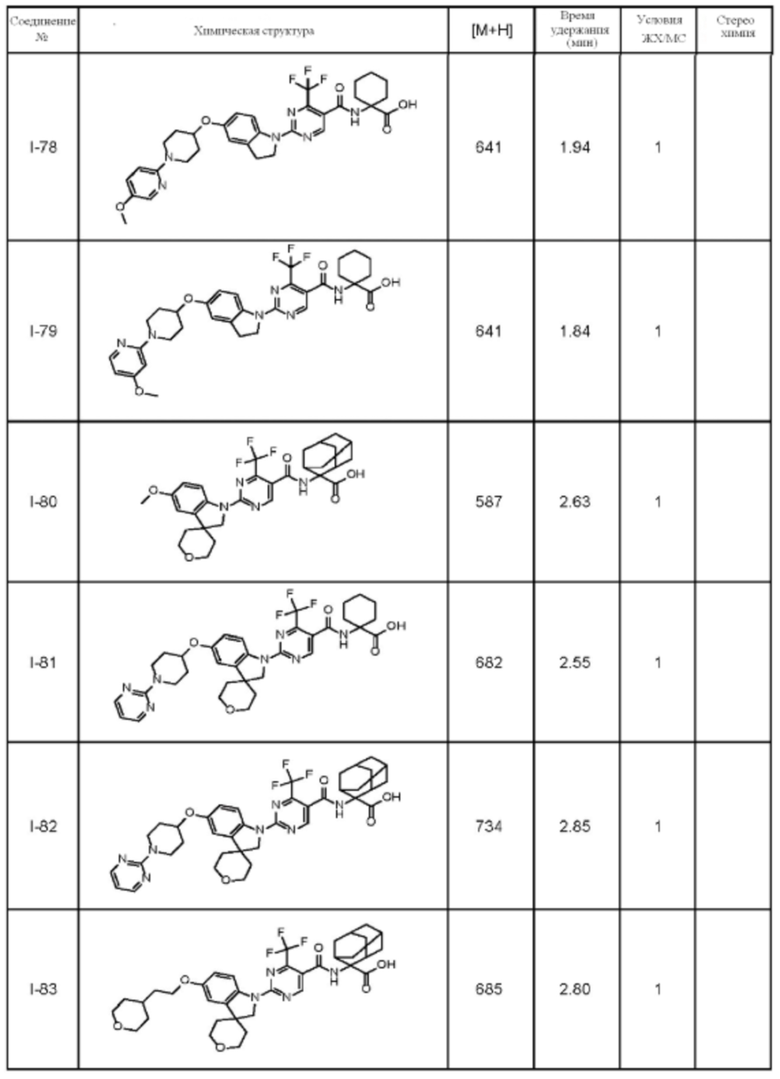
[0252]
[Таблица 13]
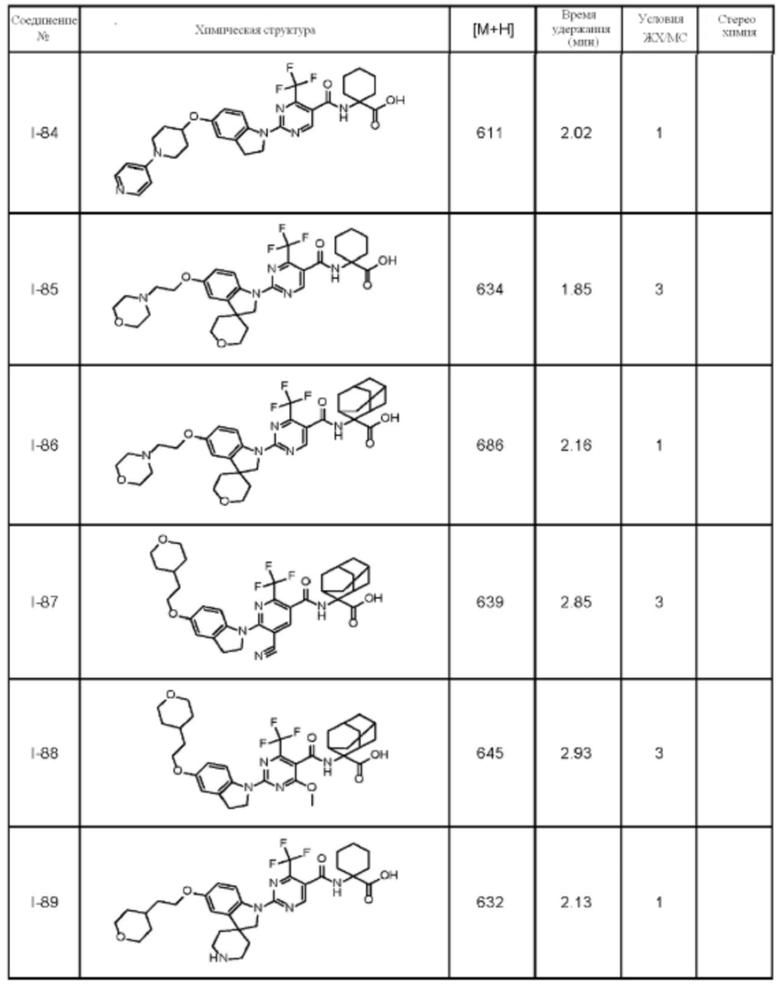
[0253]
[Таблица 14]
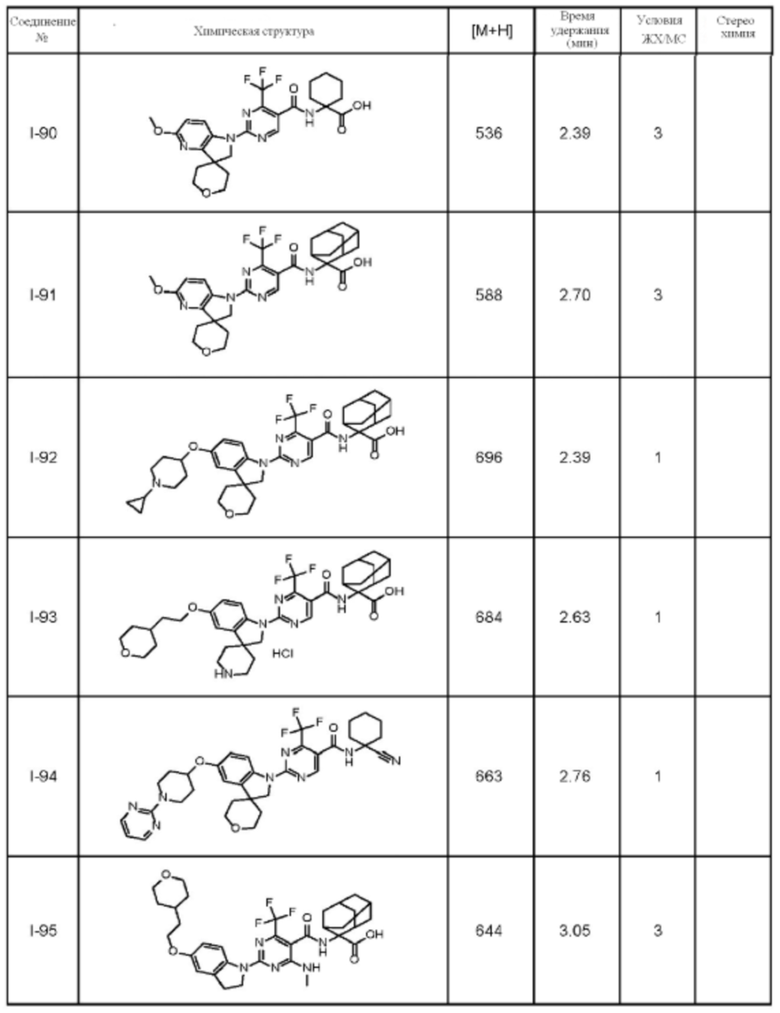
[0254]
[Таблица 15]
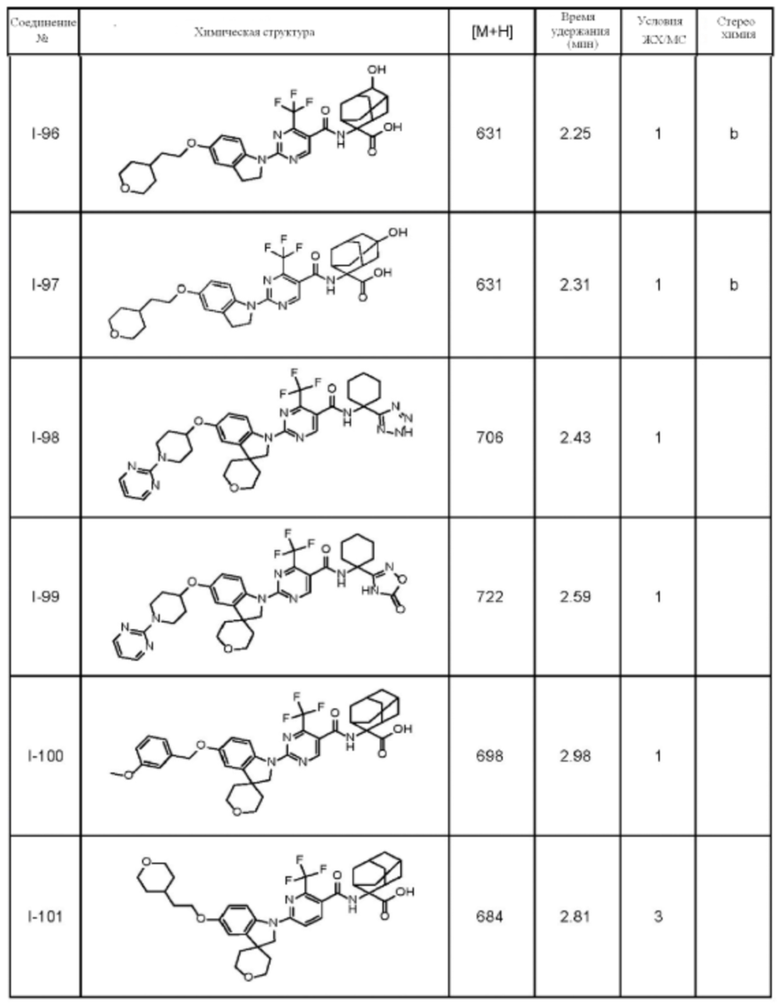
[0255]
[Таблица 16]
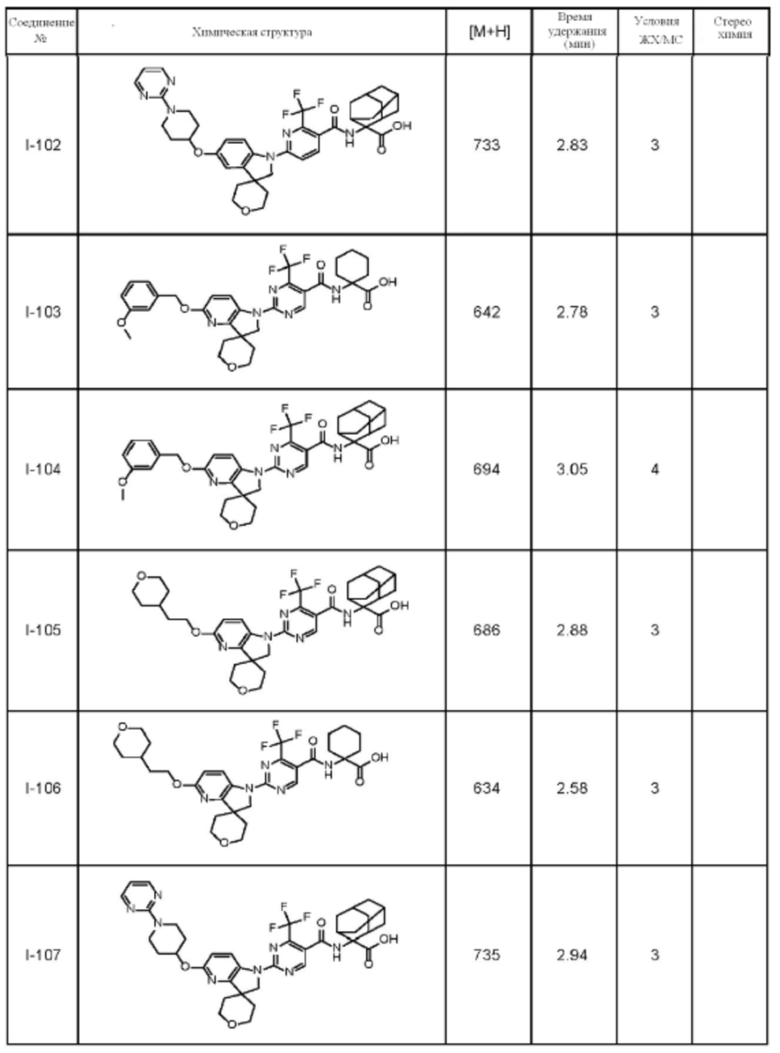
[0256]
[Таблица 17]
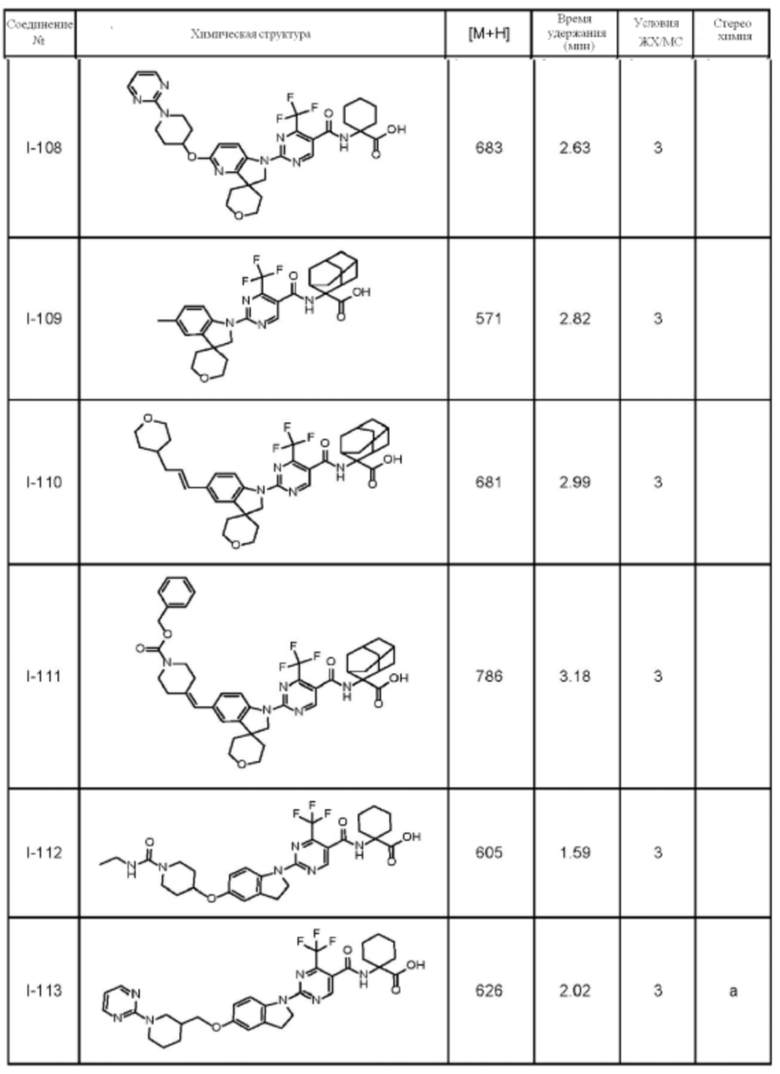
[0257]
[Таблица 18]
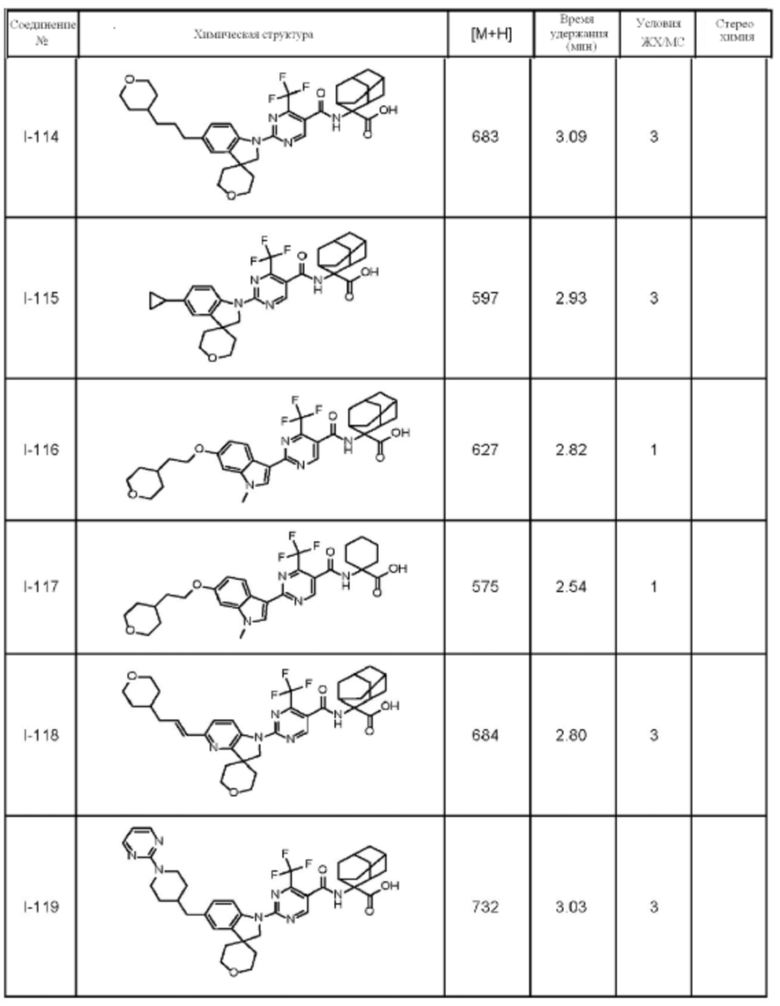
[0258]
[Таблица 19]
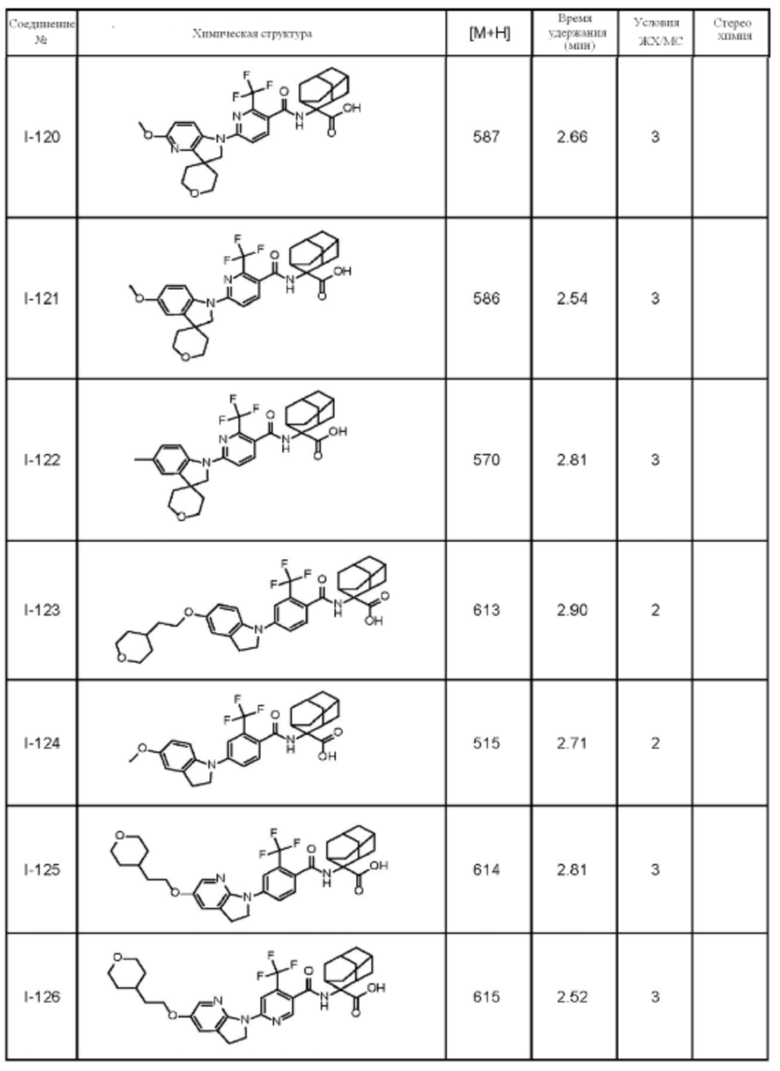
[0259]
[Таблица 20]
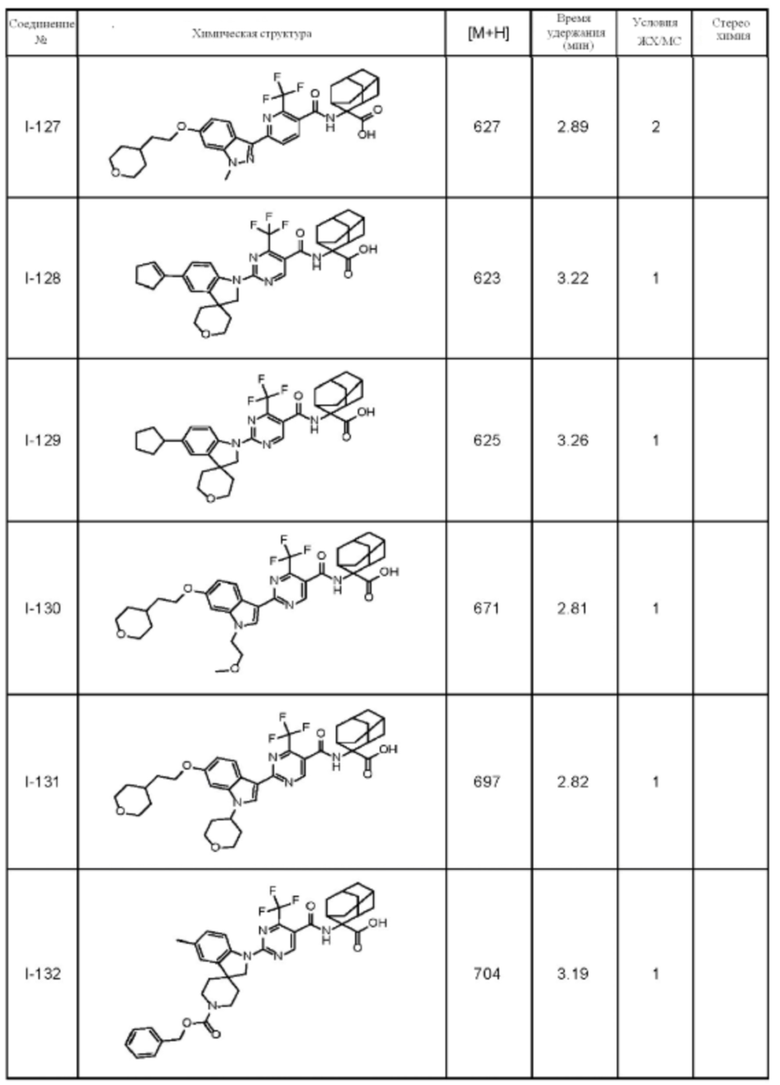
[0260]
[Таблица 21]
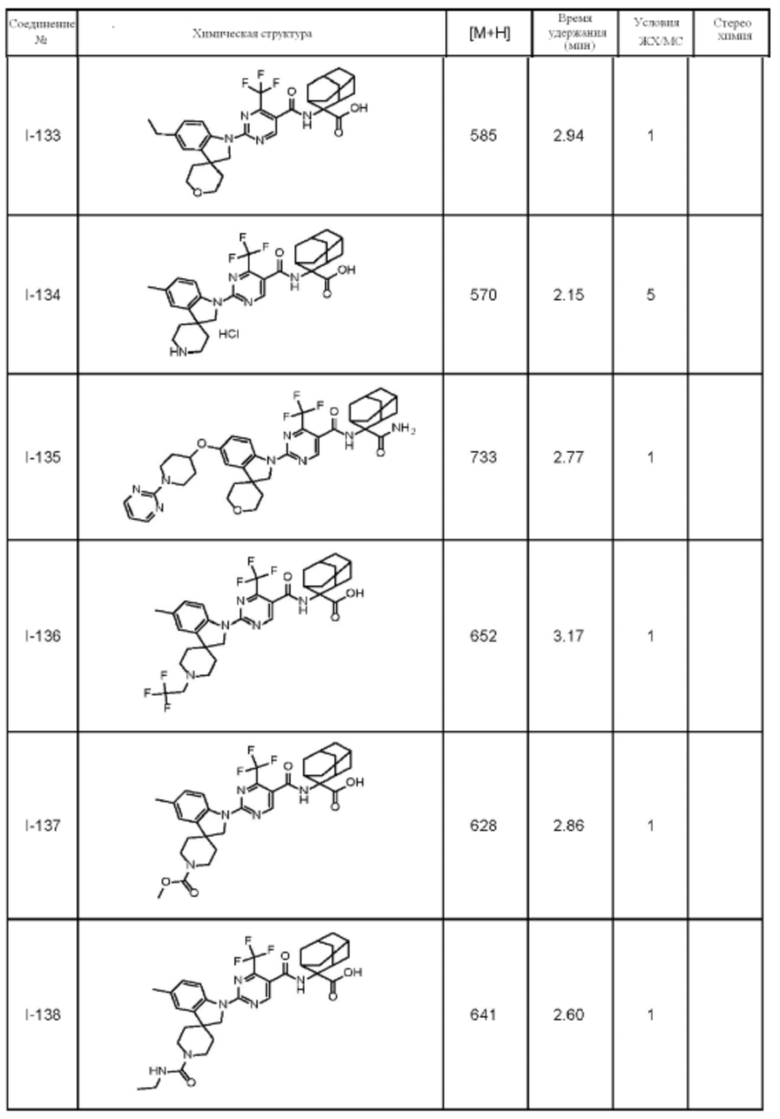
[0261]
[Таблица 22]
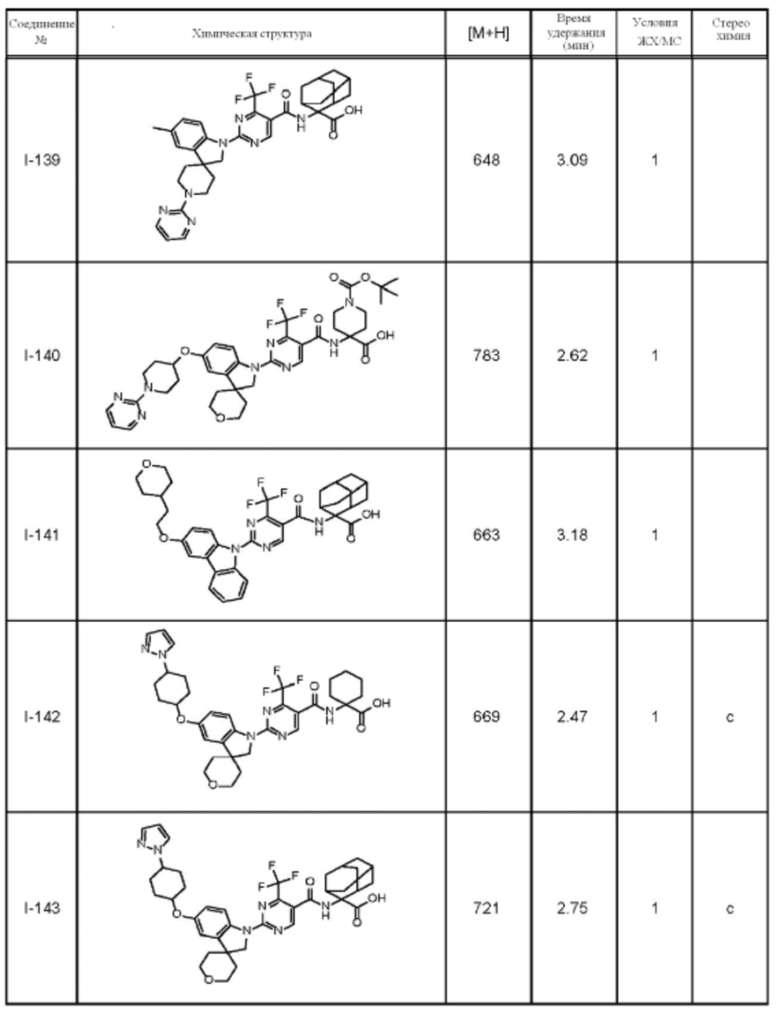
[0262]
[Таблица 23]
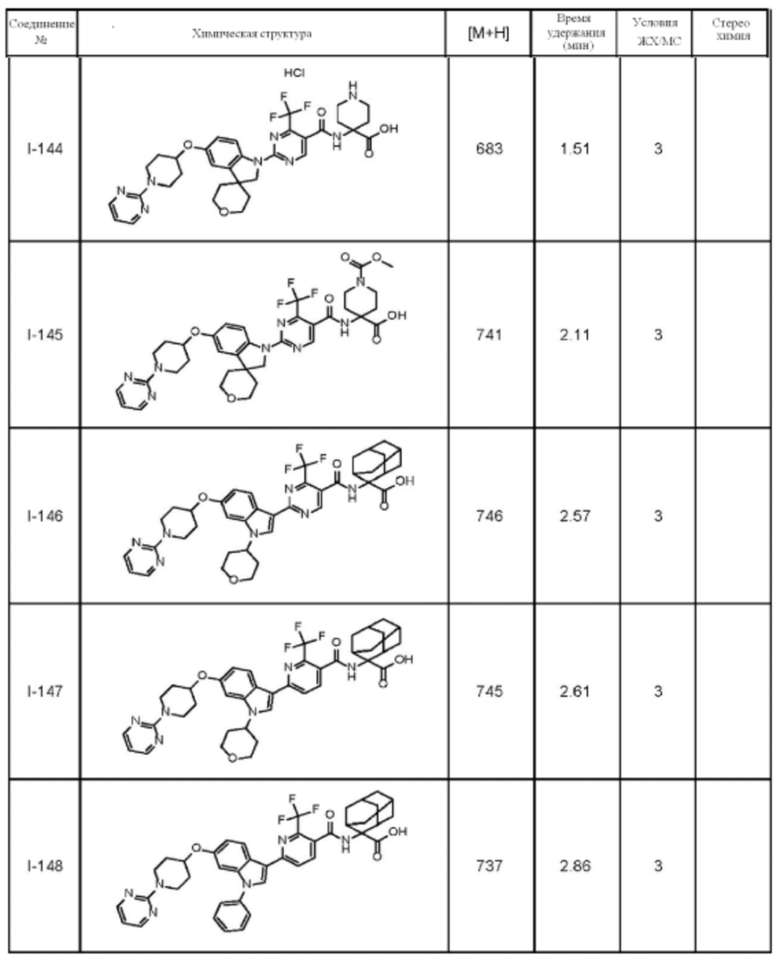
[0263]
[Таблица 24]
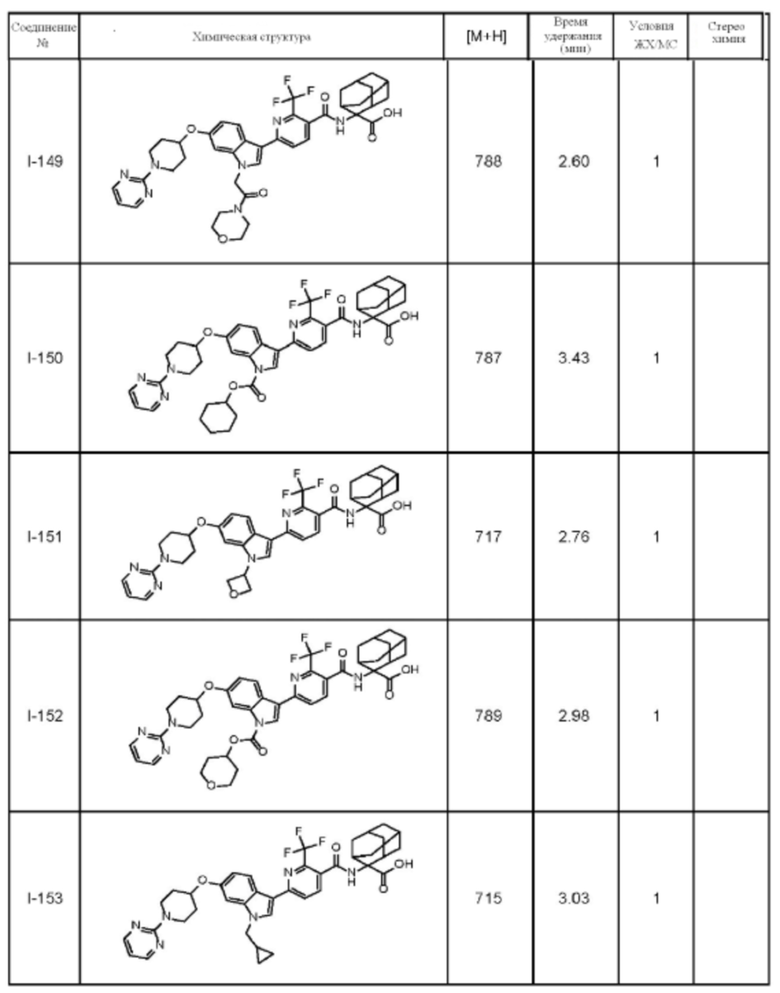
[0264]
[Таблица 25]
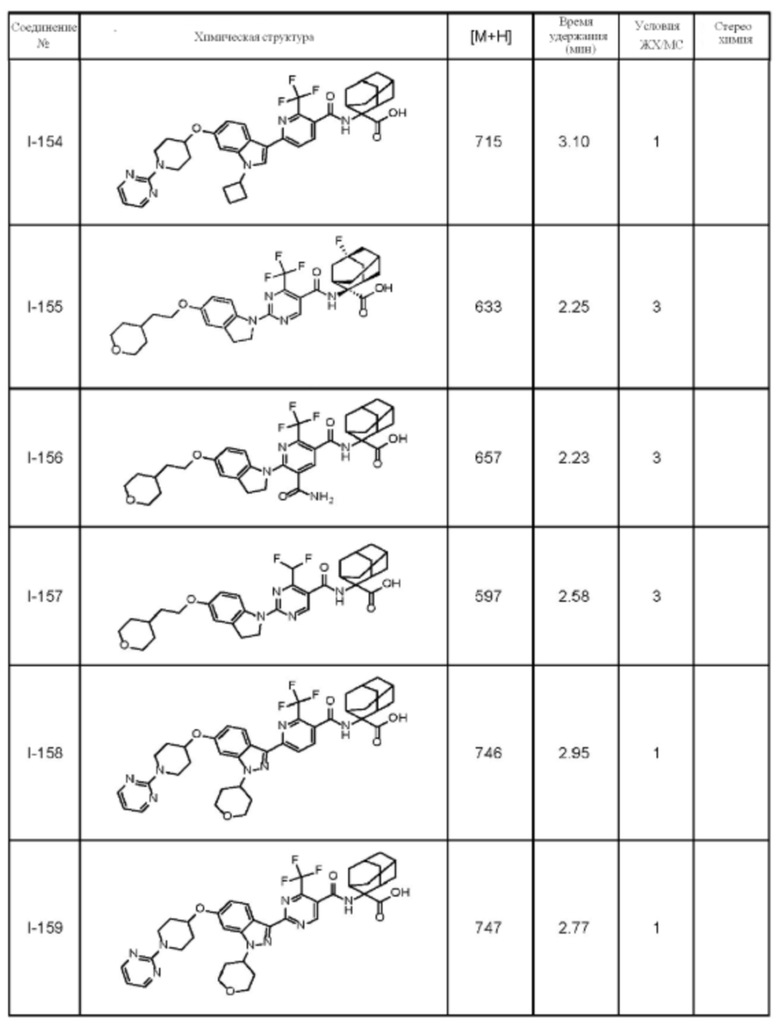
[0265]
[Таблица 26]
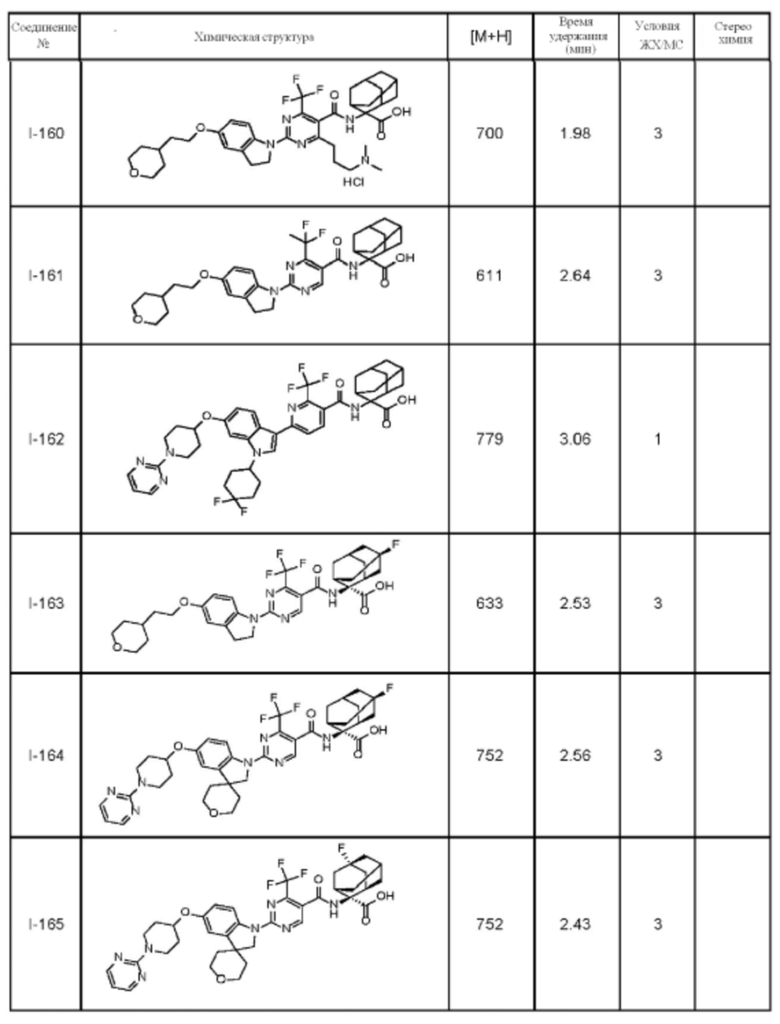
[0266]
[Таблица 27]
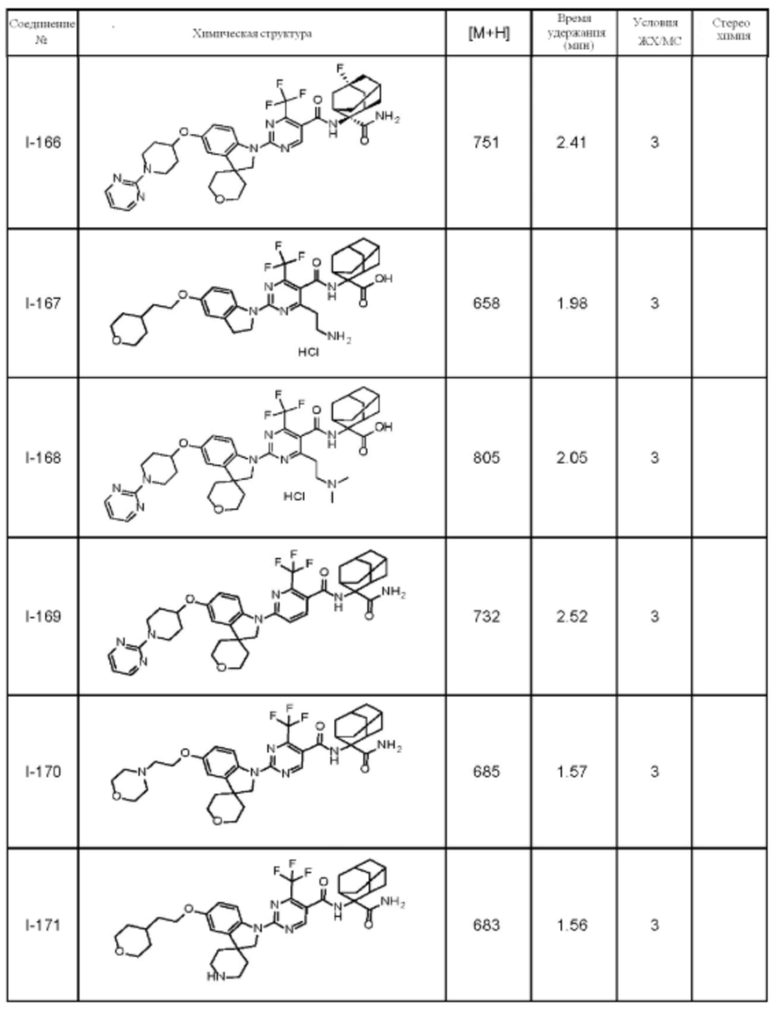
[0267]
[Таблица 28]
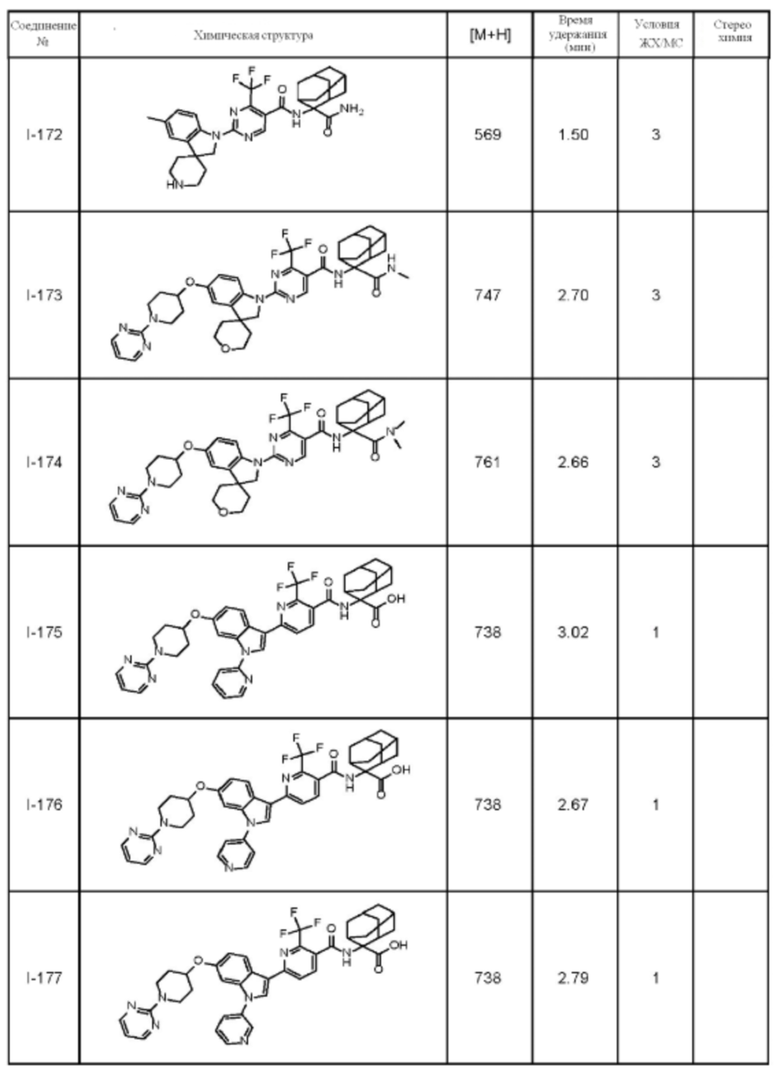
[0268]
[Таблица 29]
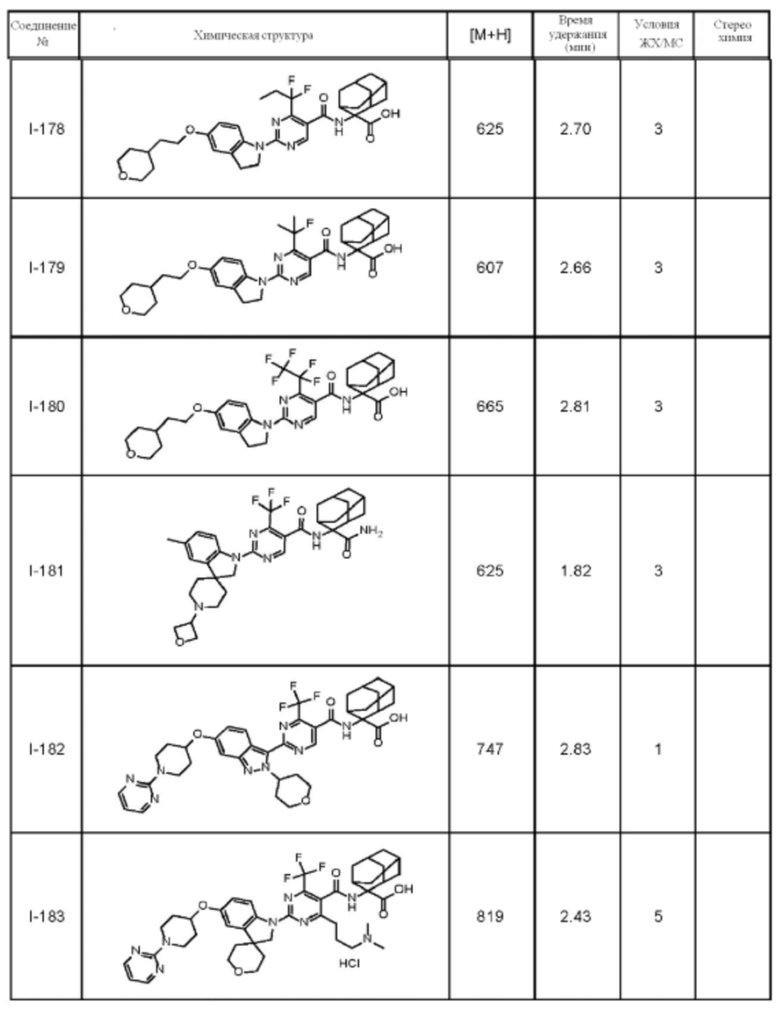
[0269]
[Таблица 30]
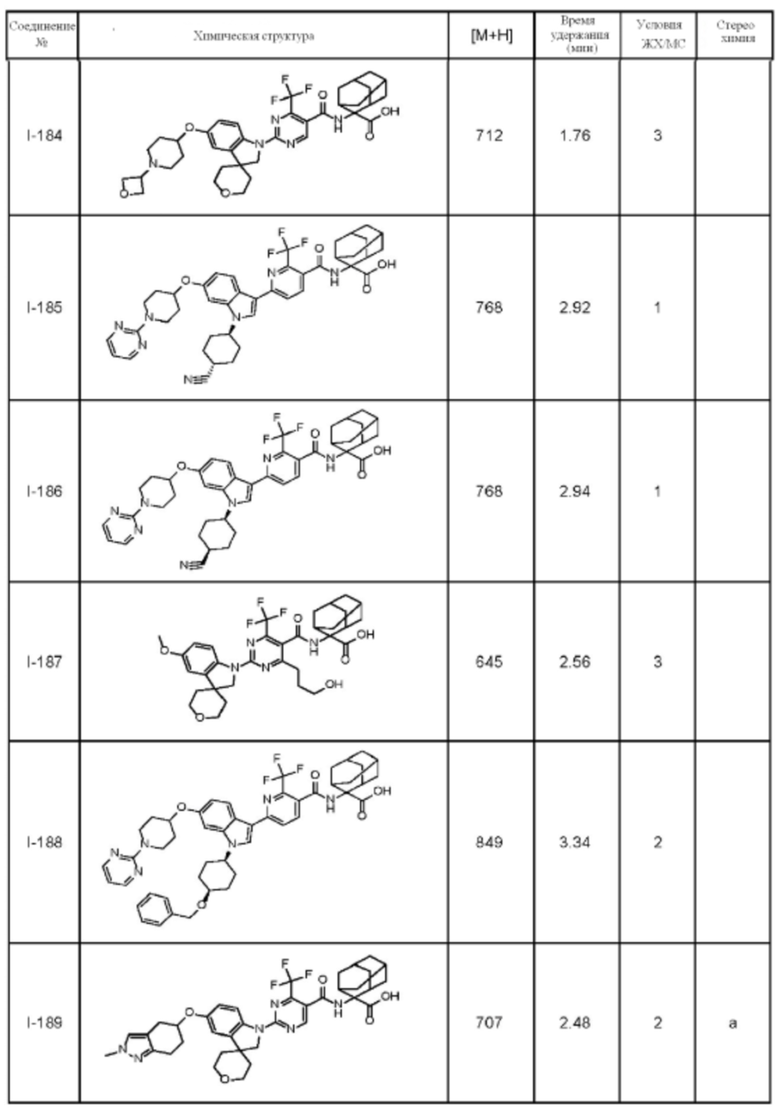
[0270]
[Таблица 31]
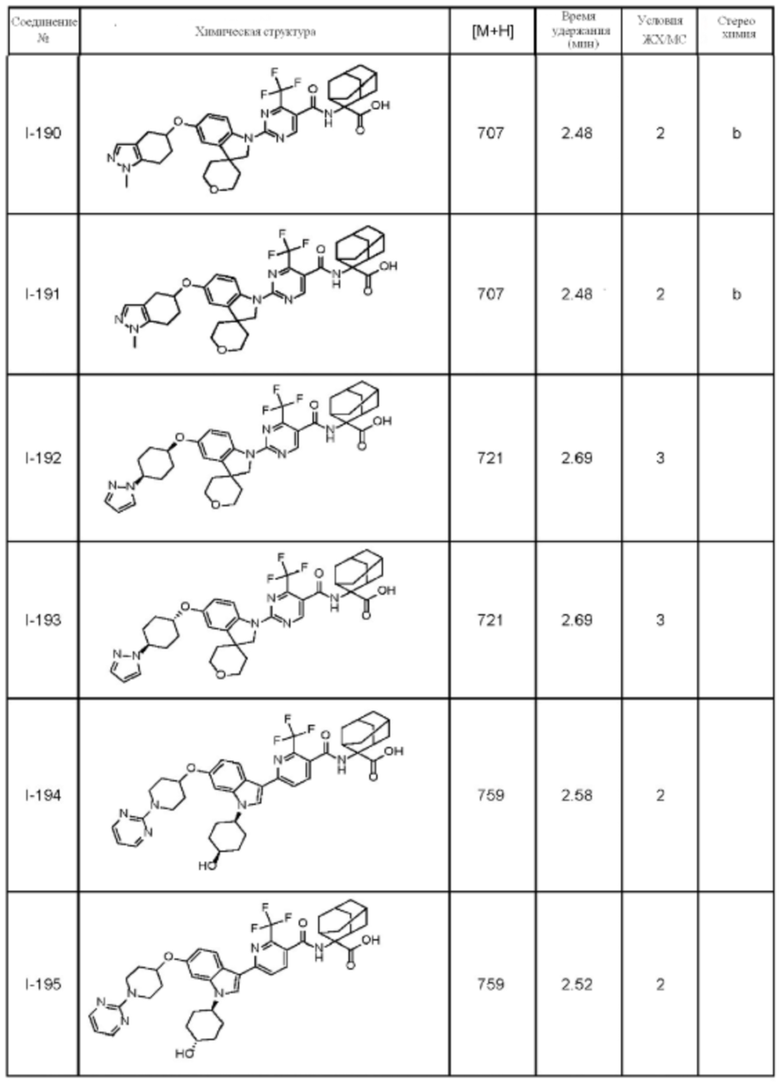
[0271]
[Таблица 32]
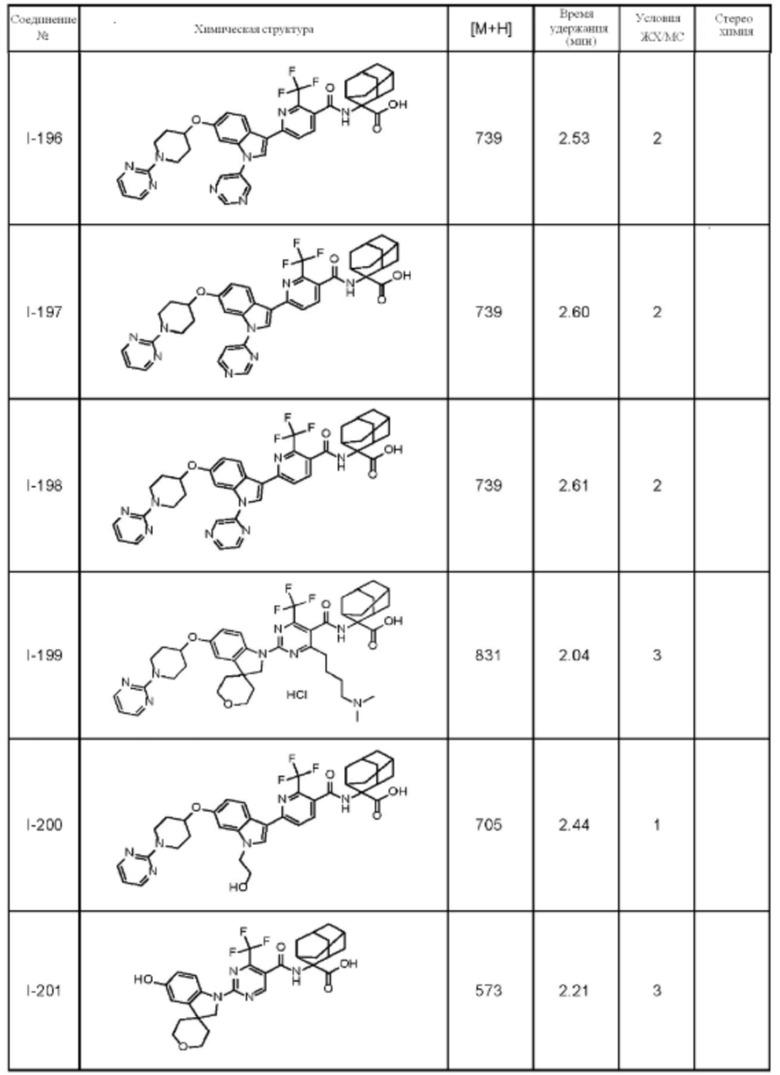
[0272]
[Таблица 33]
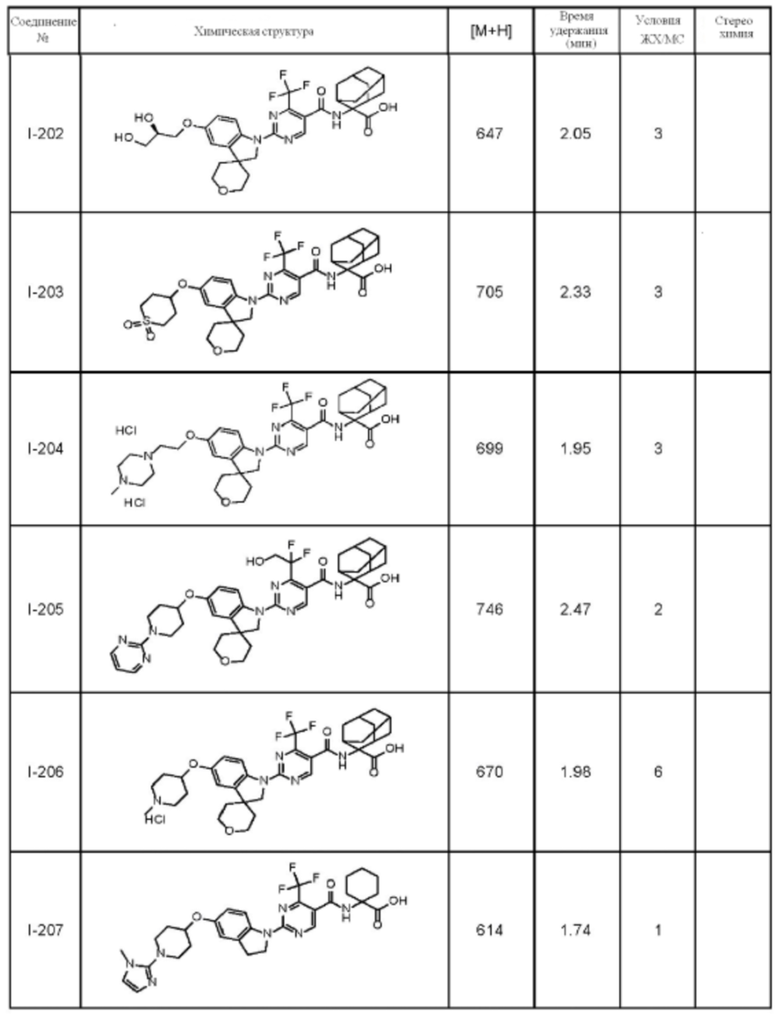
[0273]
[Таблица 34]
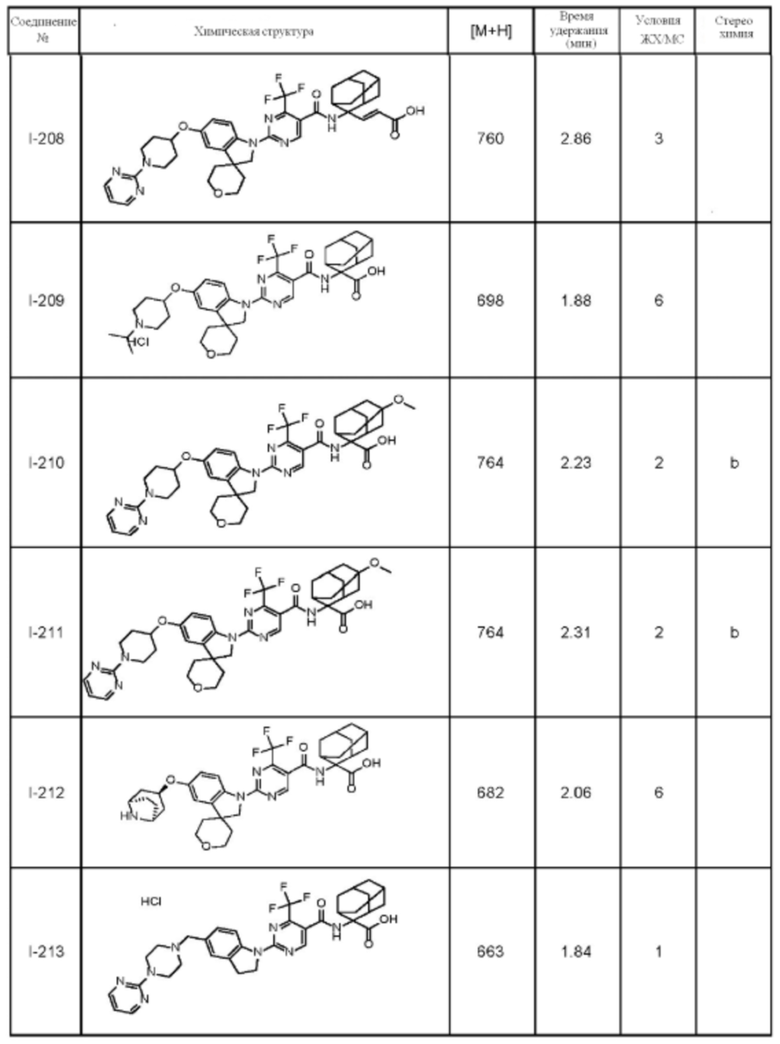
[0274]
[Таблица 35]
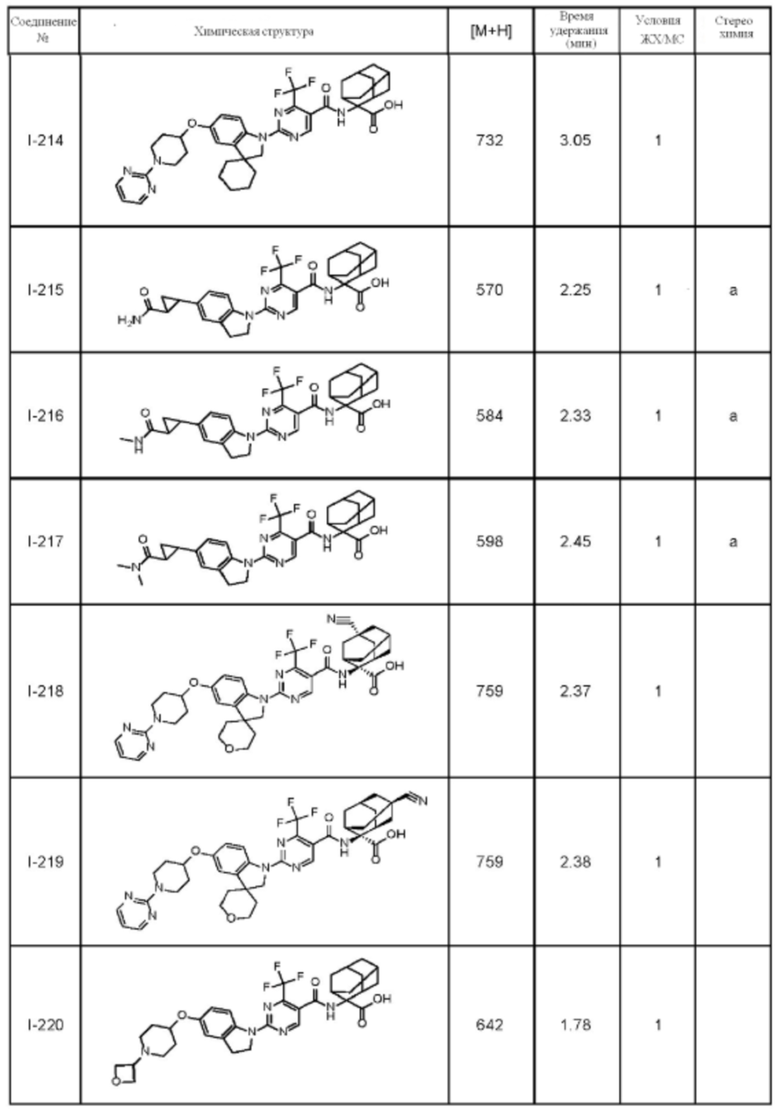
[0275]
[Таблица 36]
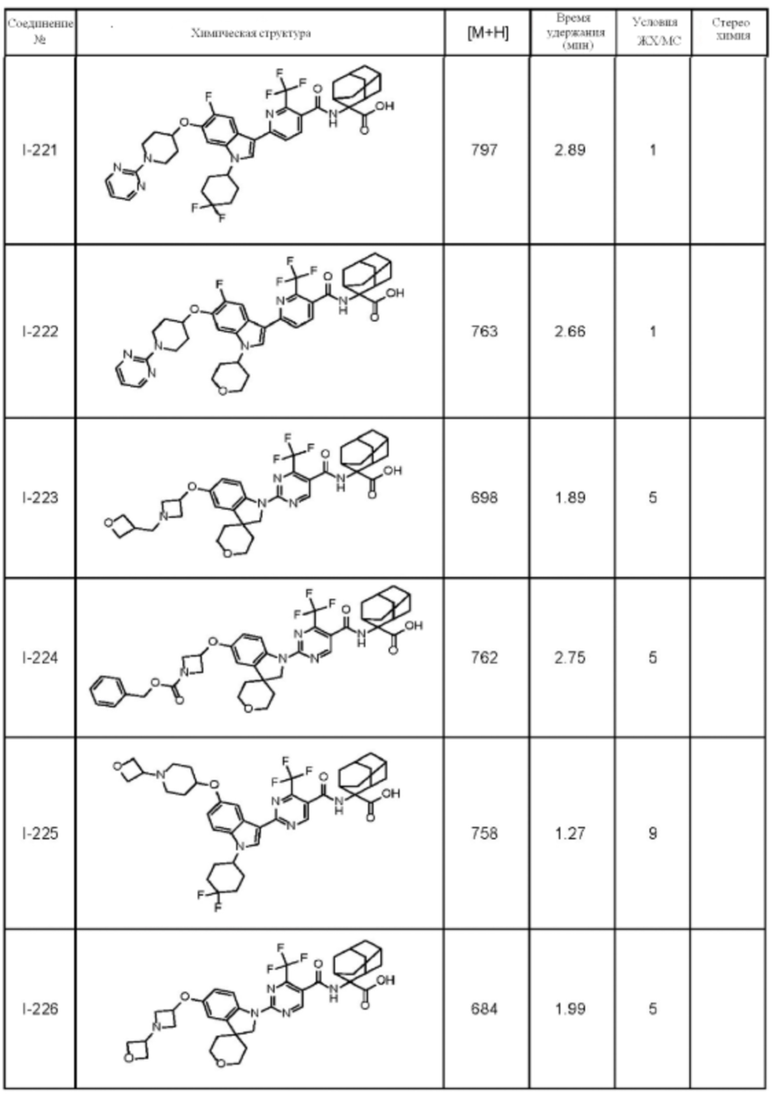
[0276]
[Таблица 37]
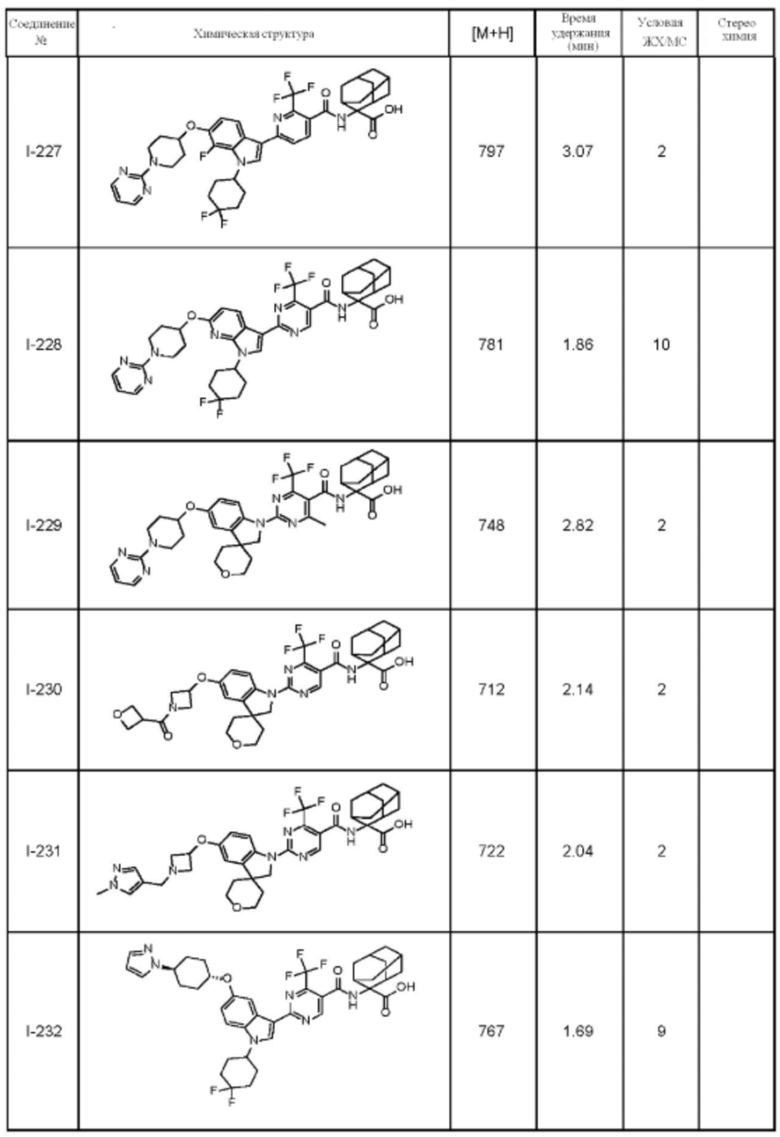
[0277]
[Таблица 38]
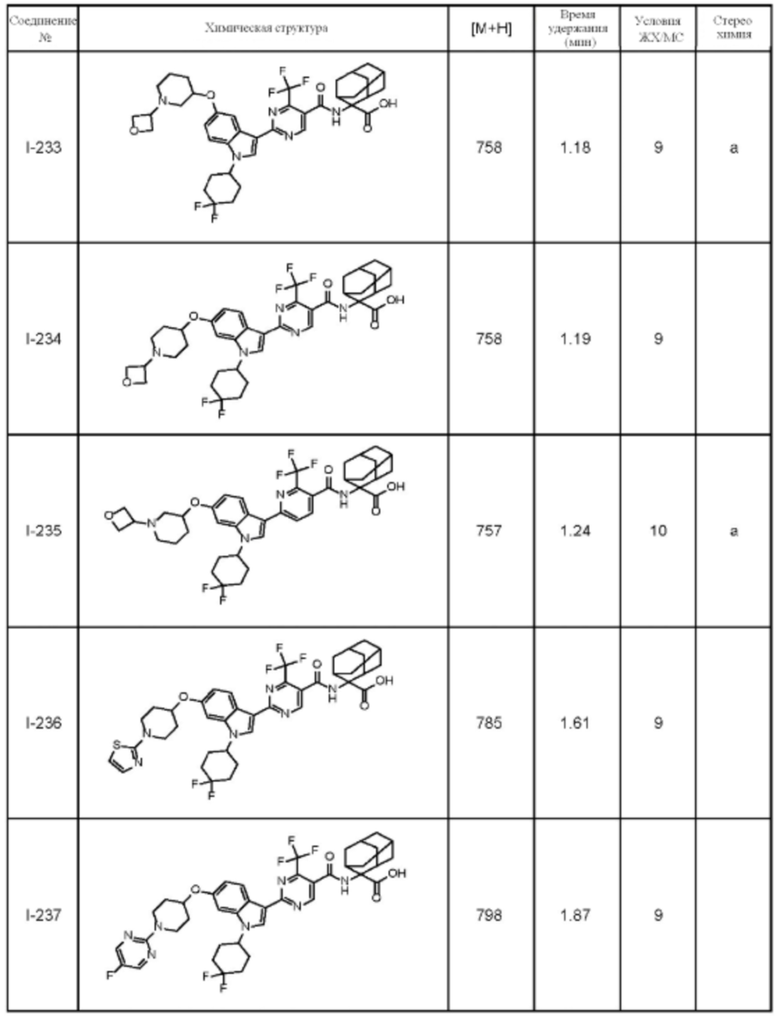
[0278]
[Таблица 39]
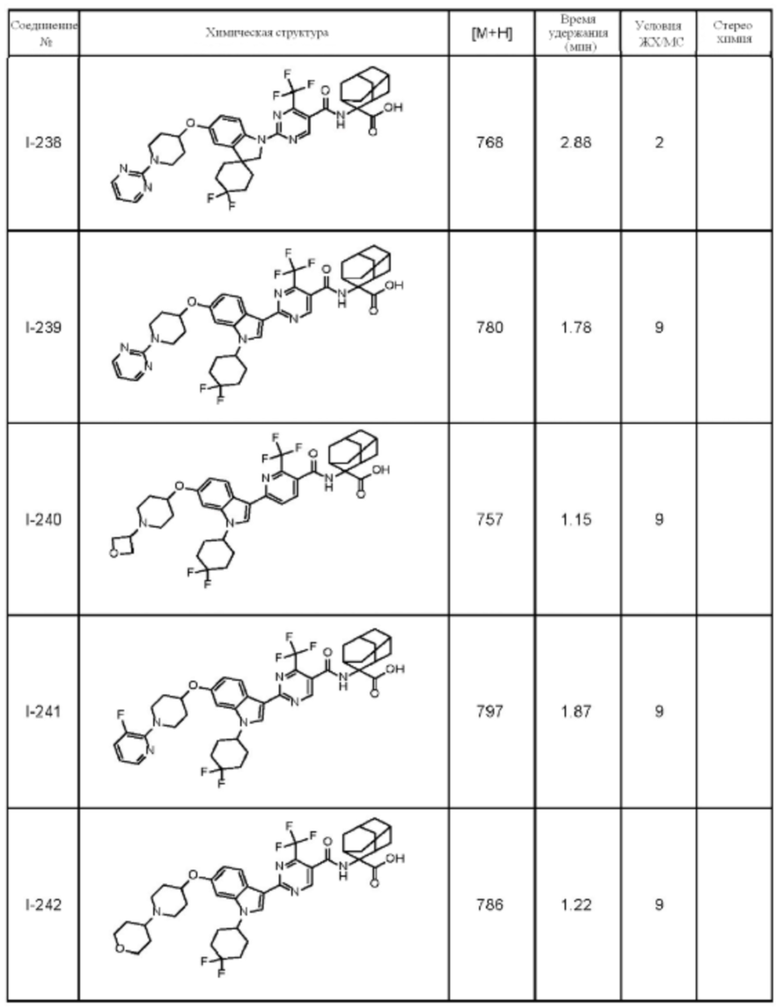
[0279]
[Таблица 40]
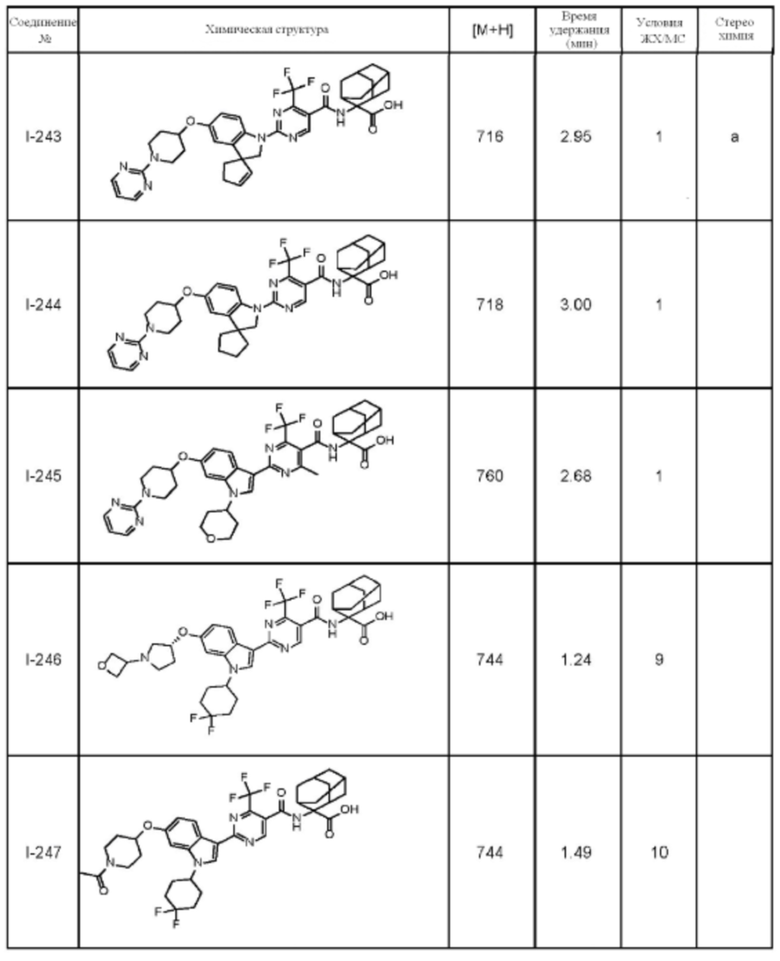
[0280]
[Таблица 41]
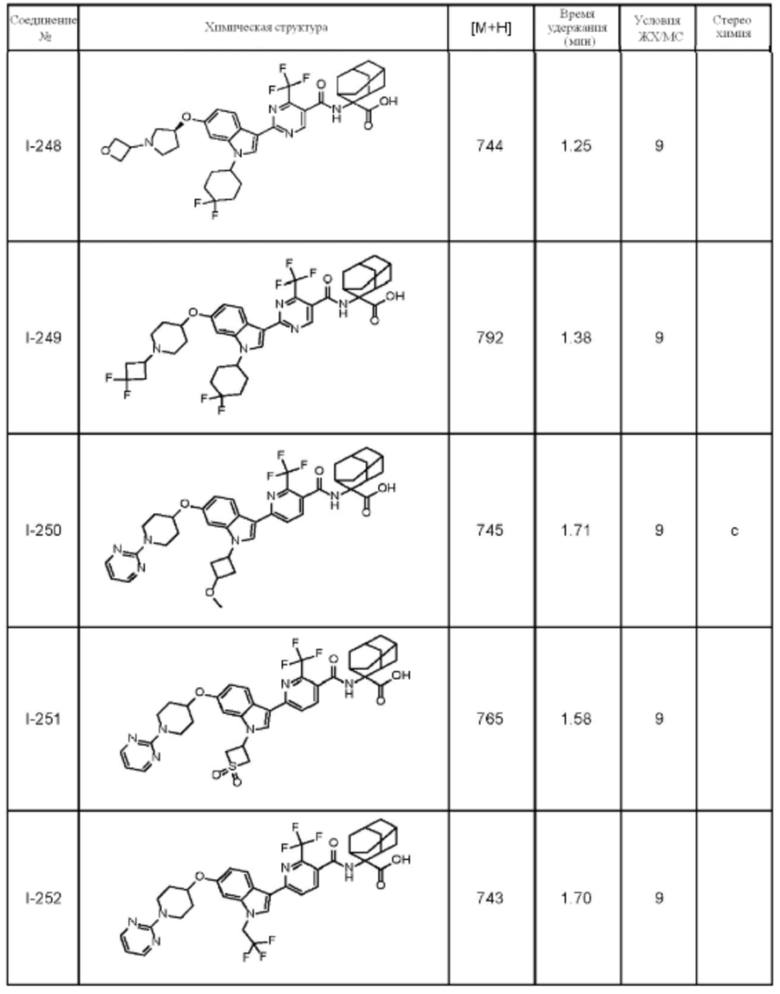
[0281]
[Таблица 42]
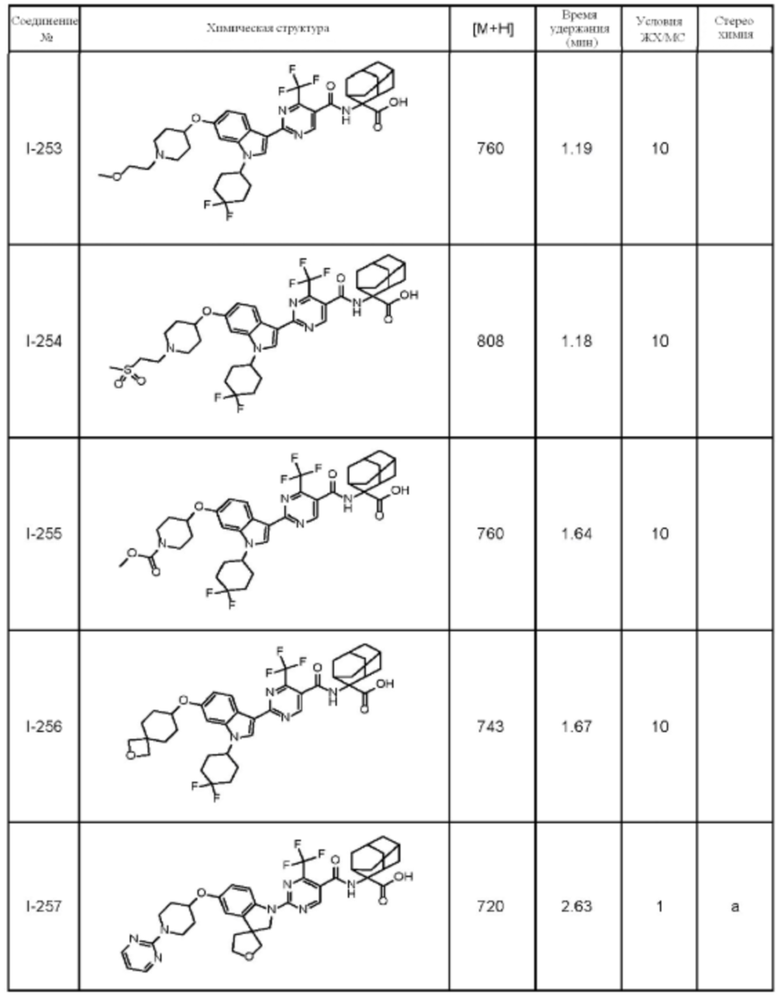
[0282]
[Таблица 43]
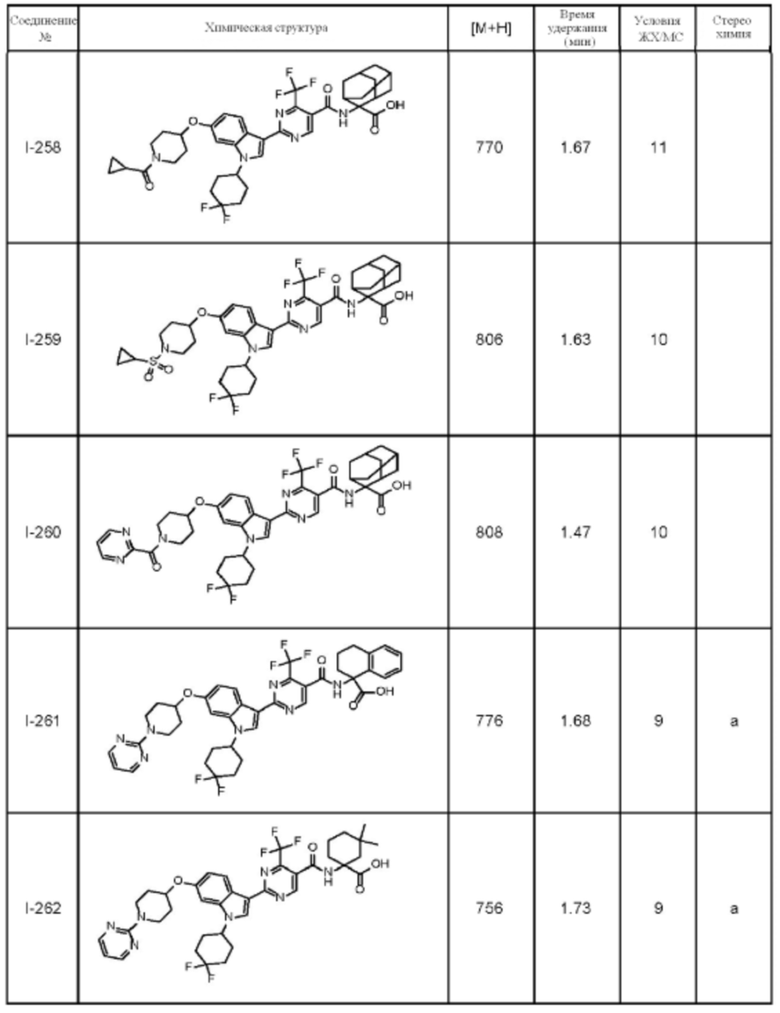
[0283]
[Таблица 44]
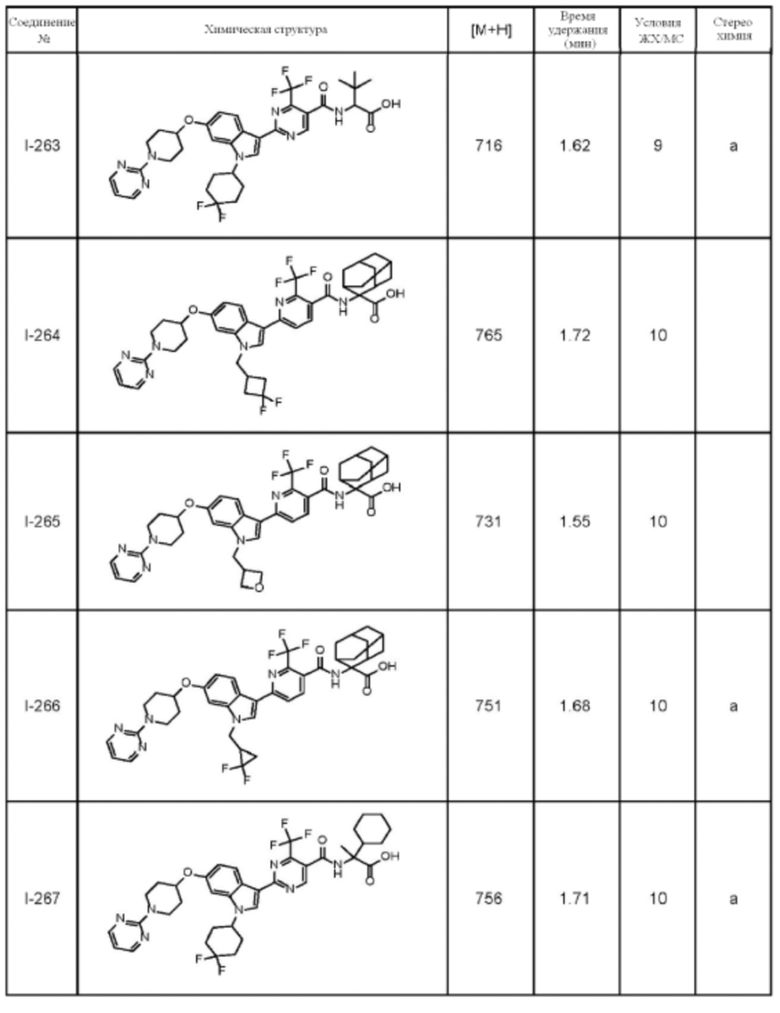
[0284]
[Таблица 45]
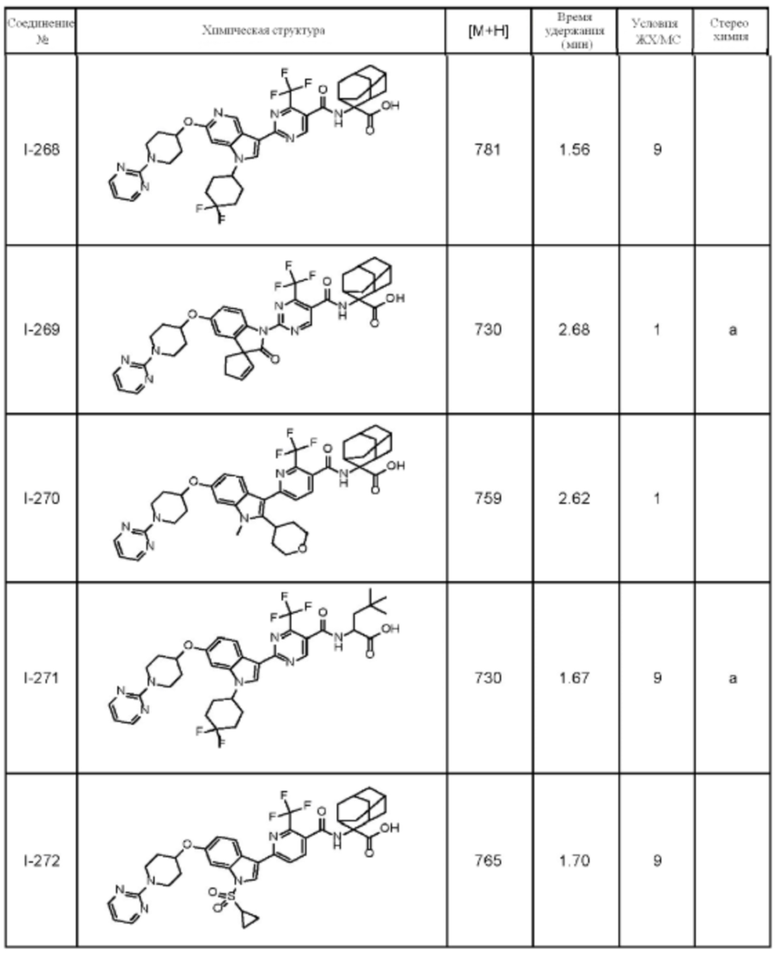
[0285]
[Таблица 46]
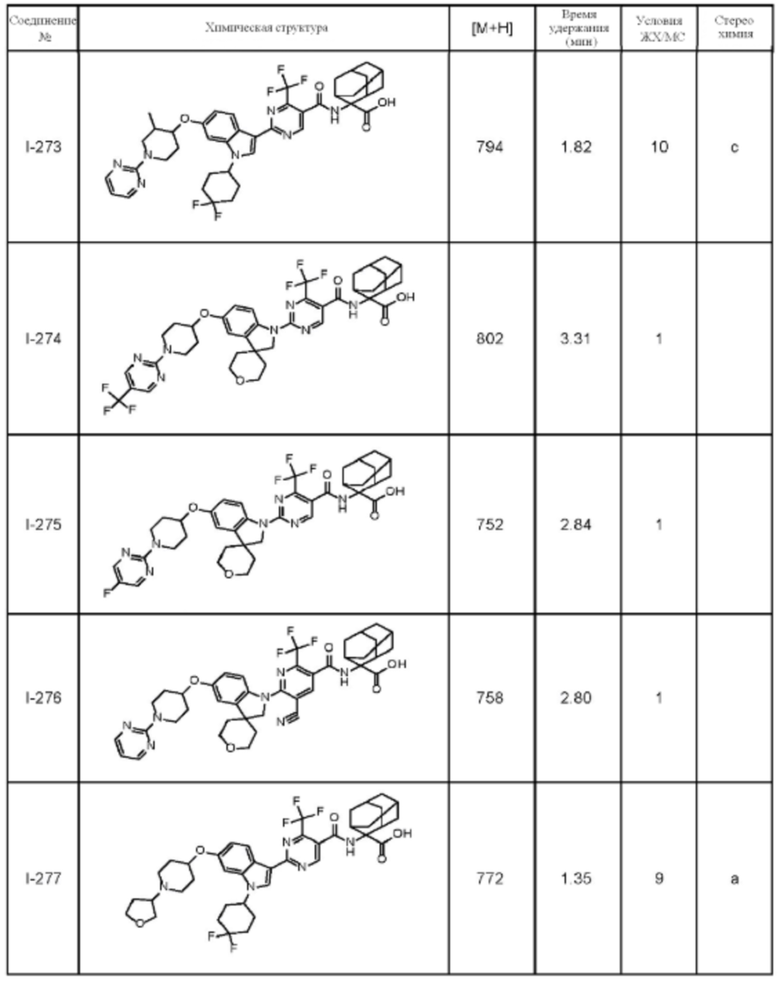
[0286]
[Таблица 47]
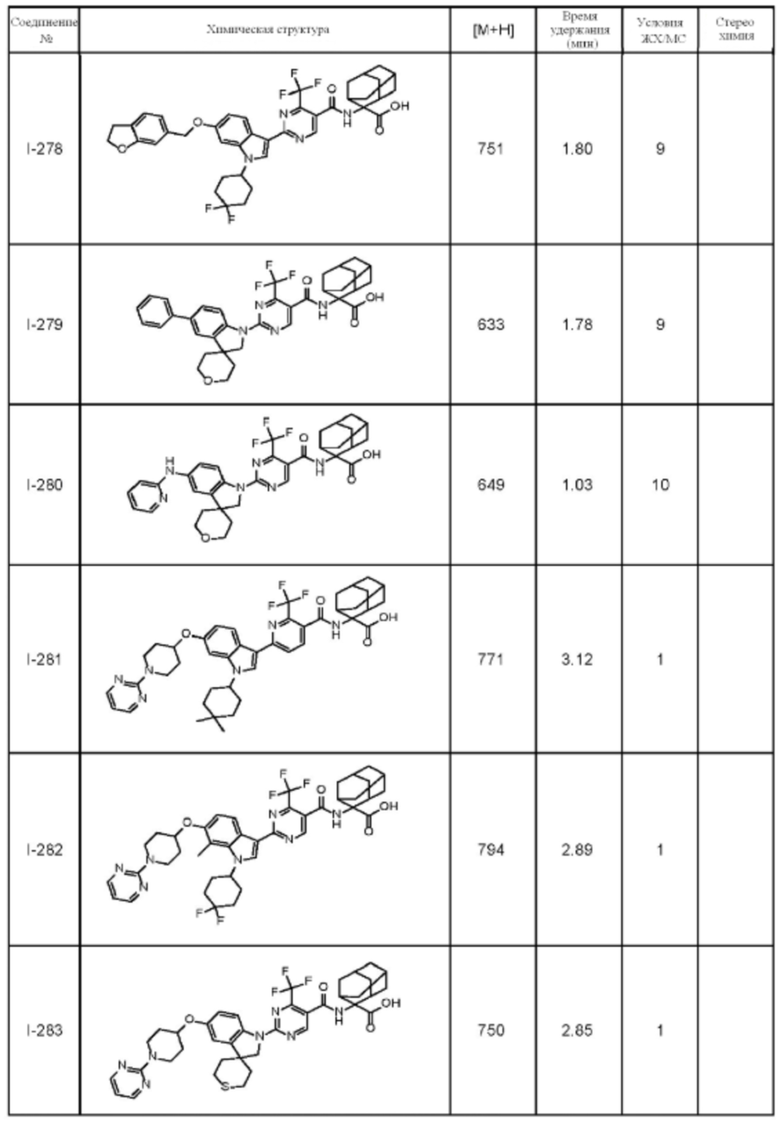
[0287]
[Таблица 48]
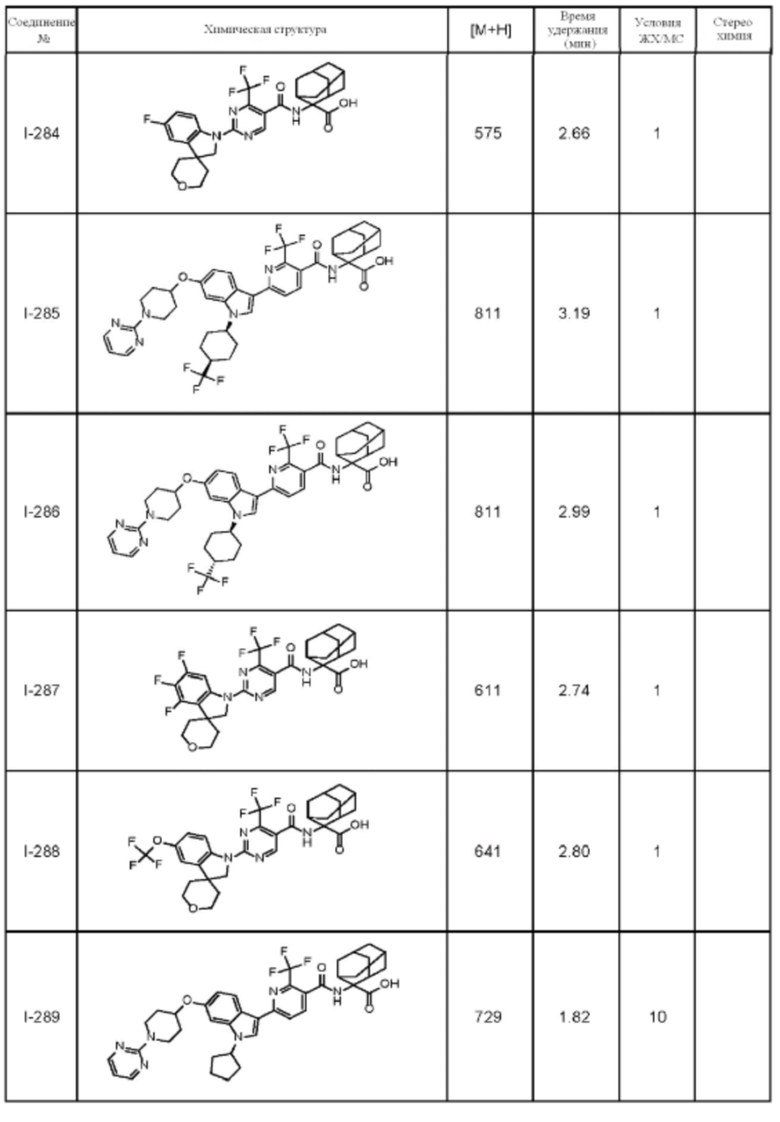
[0288]
[Таблица 49]
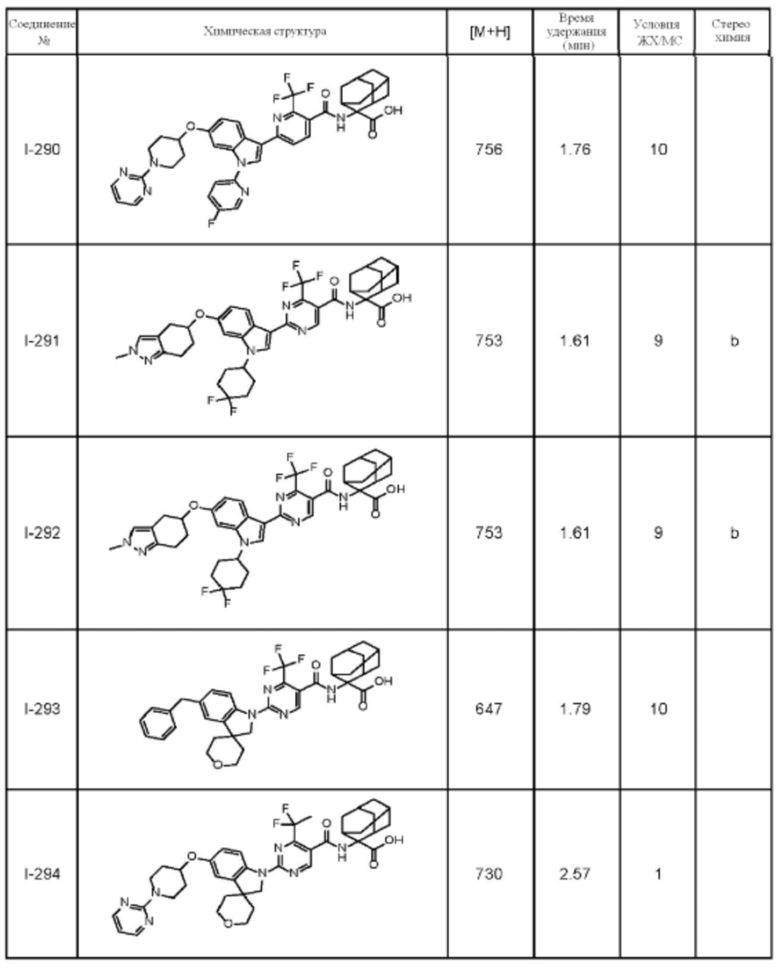
[0289]
[Таблица 50]
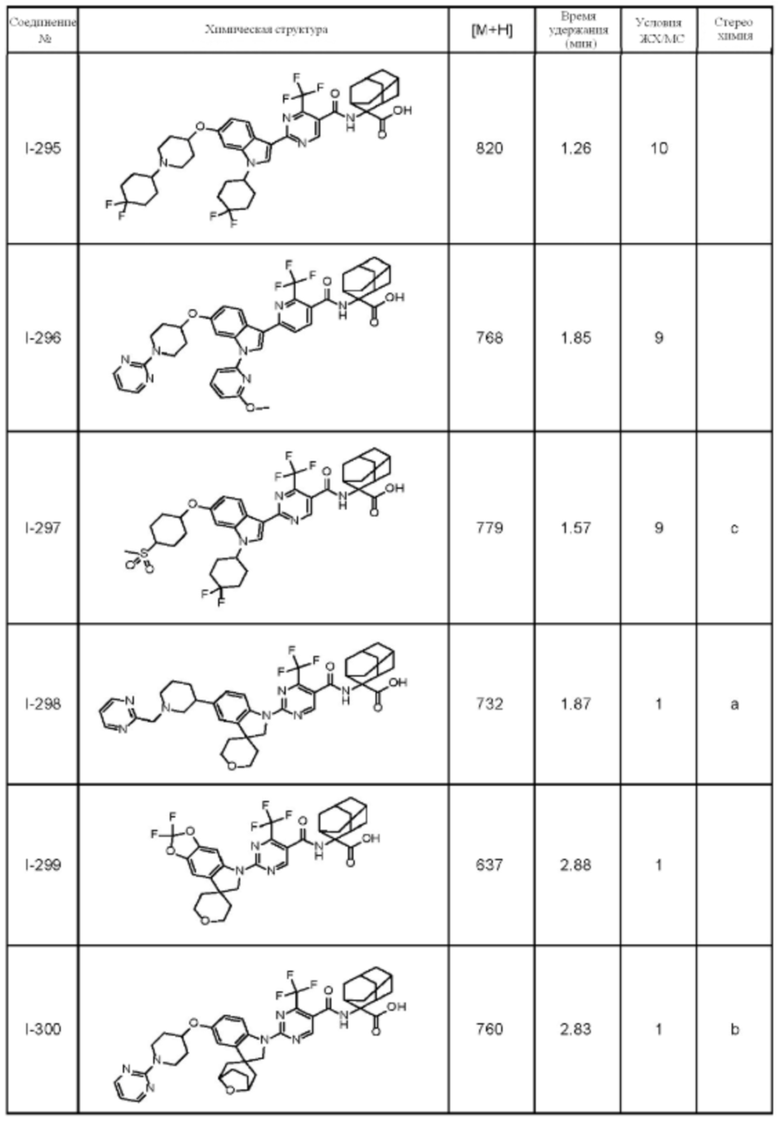
[0290]
[Таблица 51]
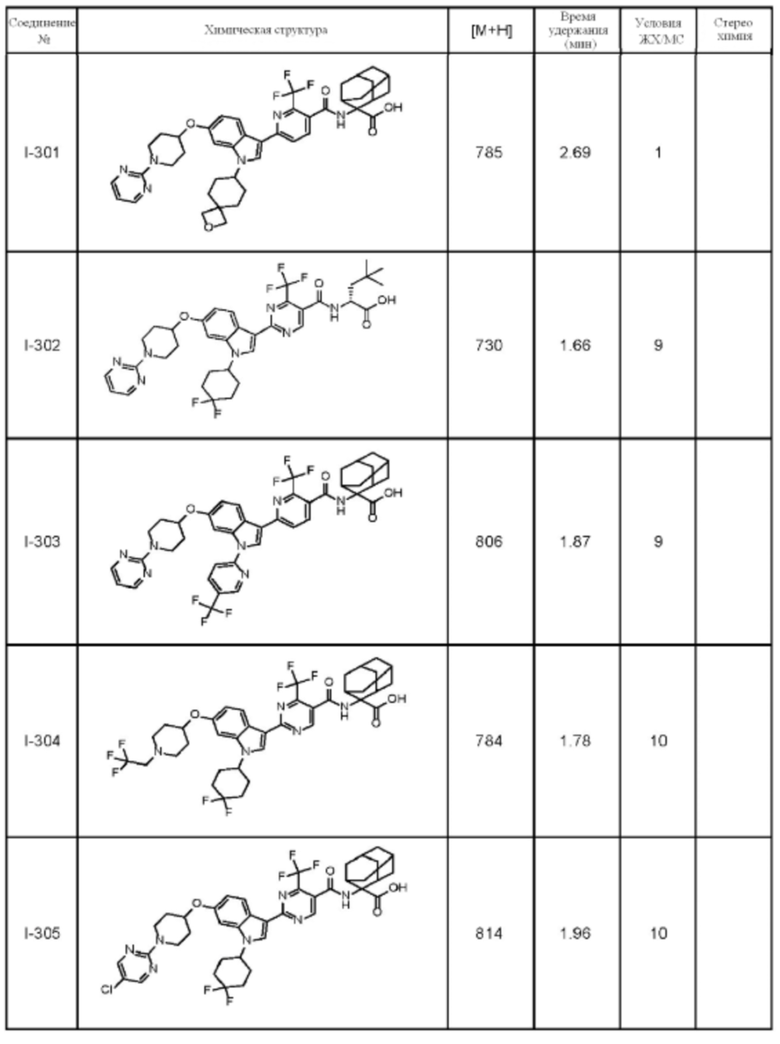
[0291]
[Таблица 52]
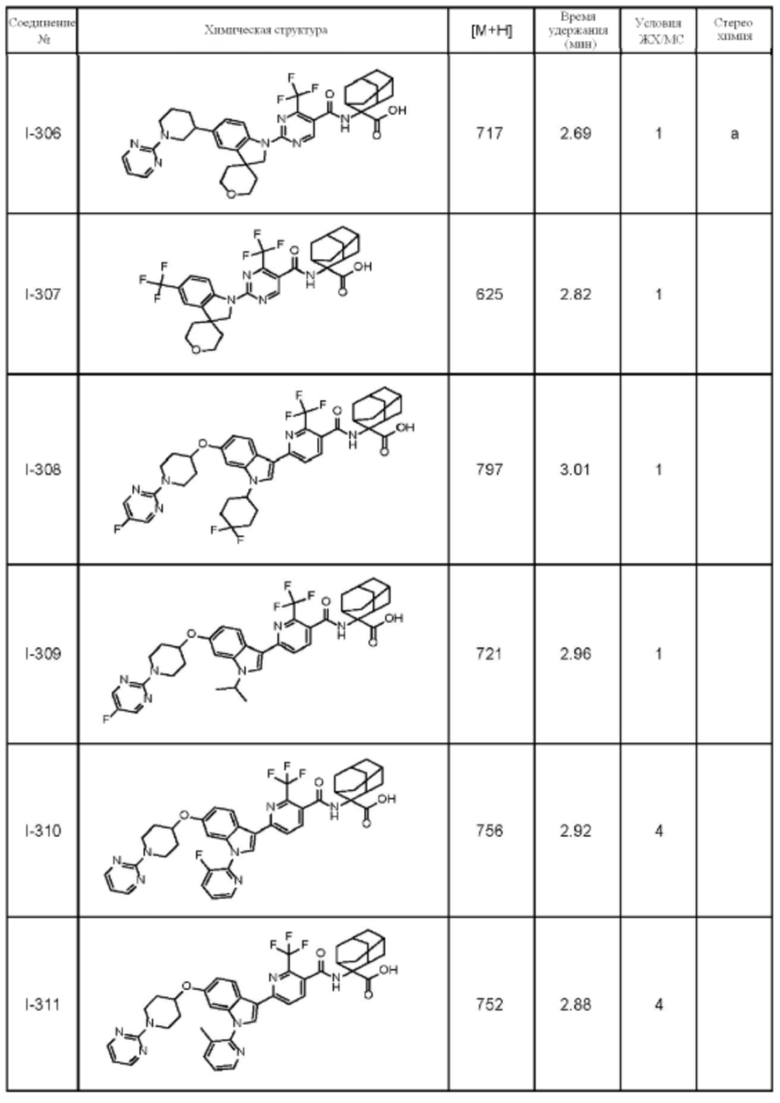
[0292]
[Таблица 53]
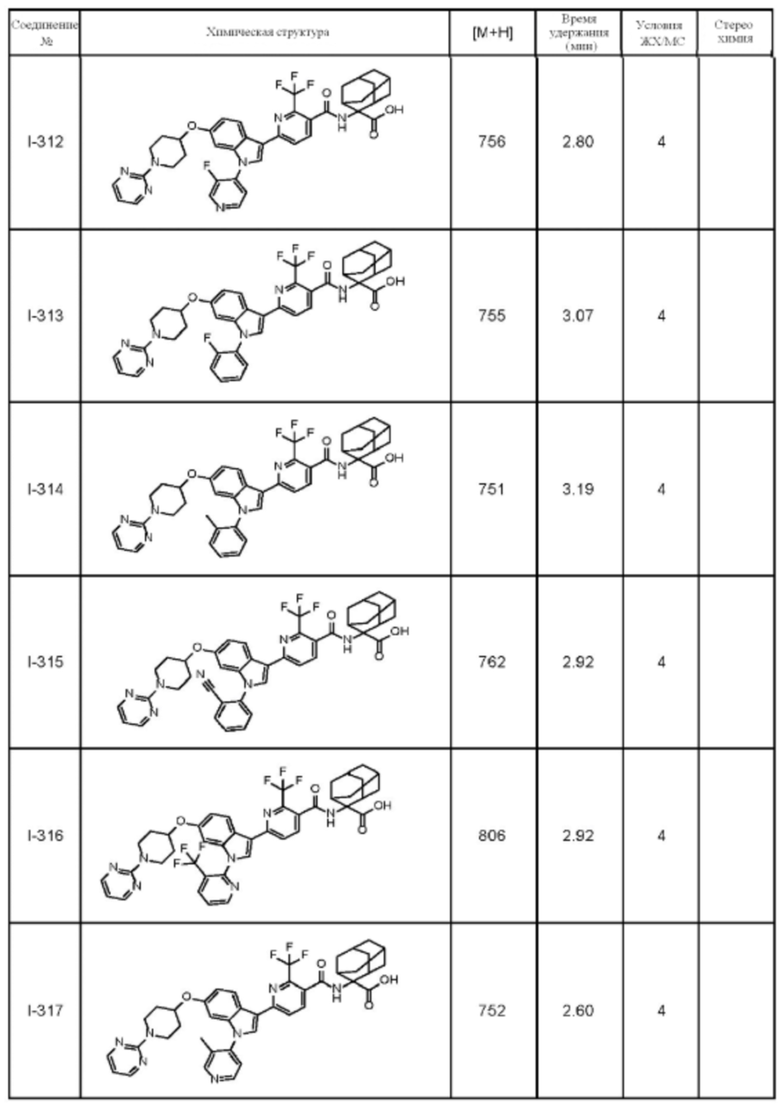
[0293]
[Таблица 54]
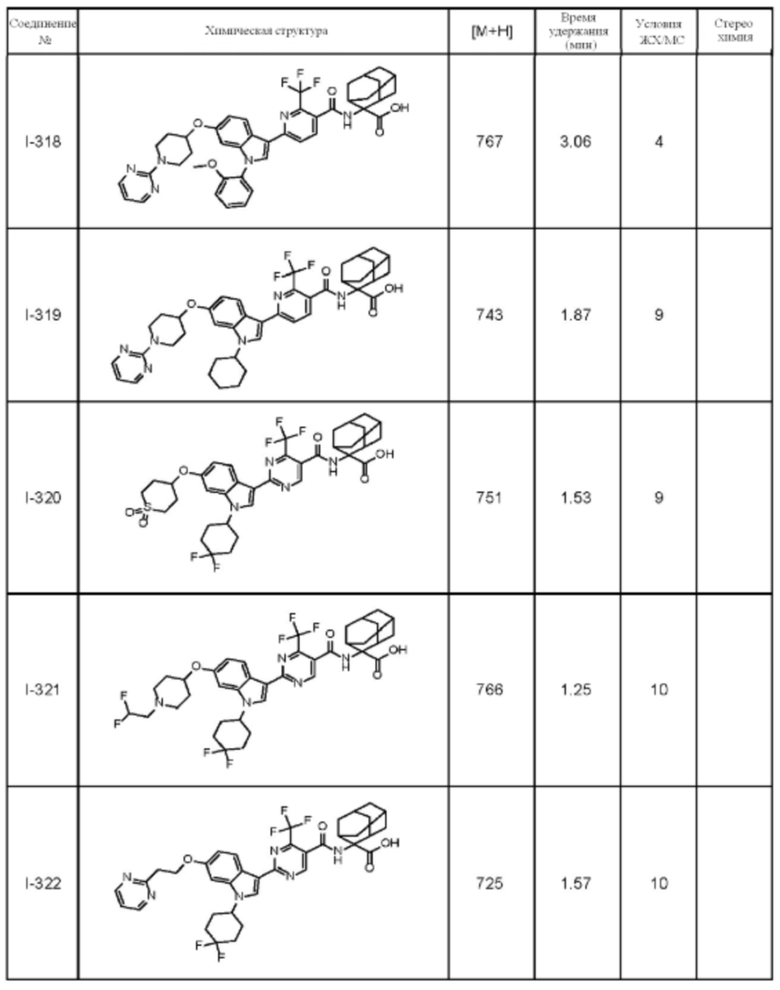
[0294]
[Таблица 55]
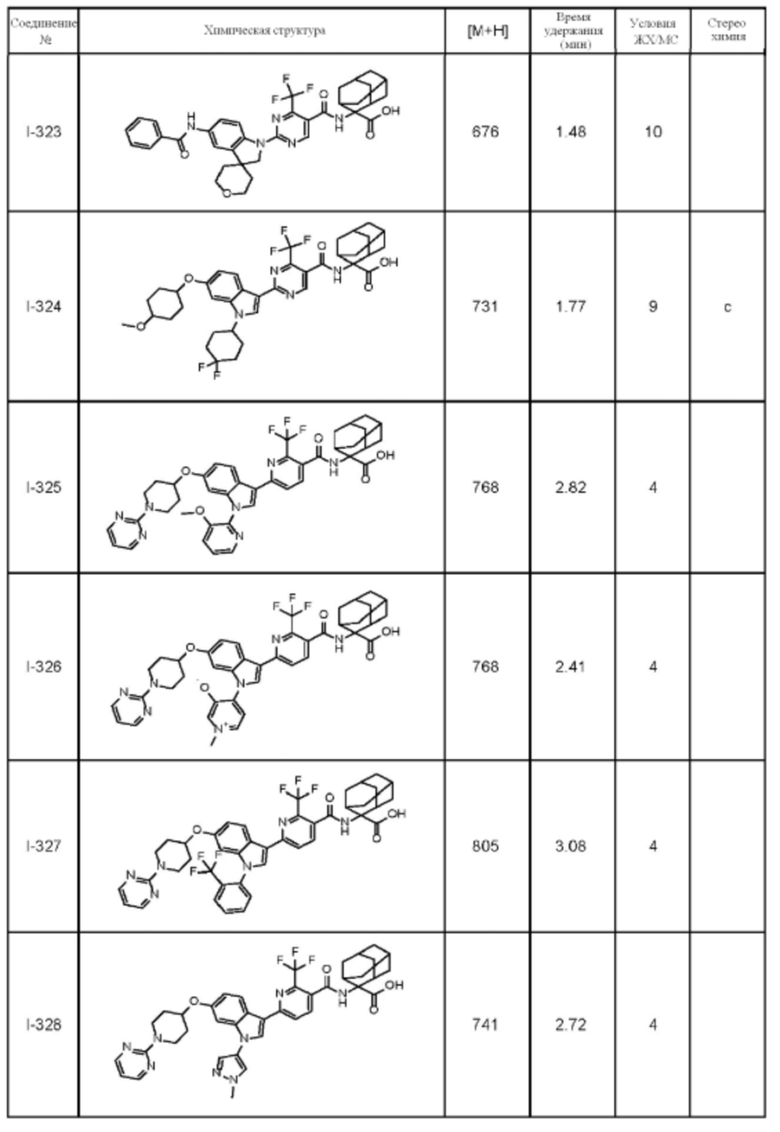
[0295]
[Таблица 56]
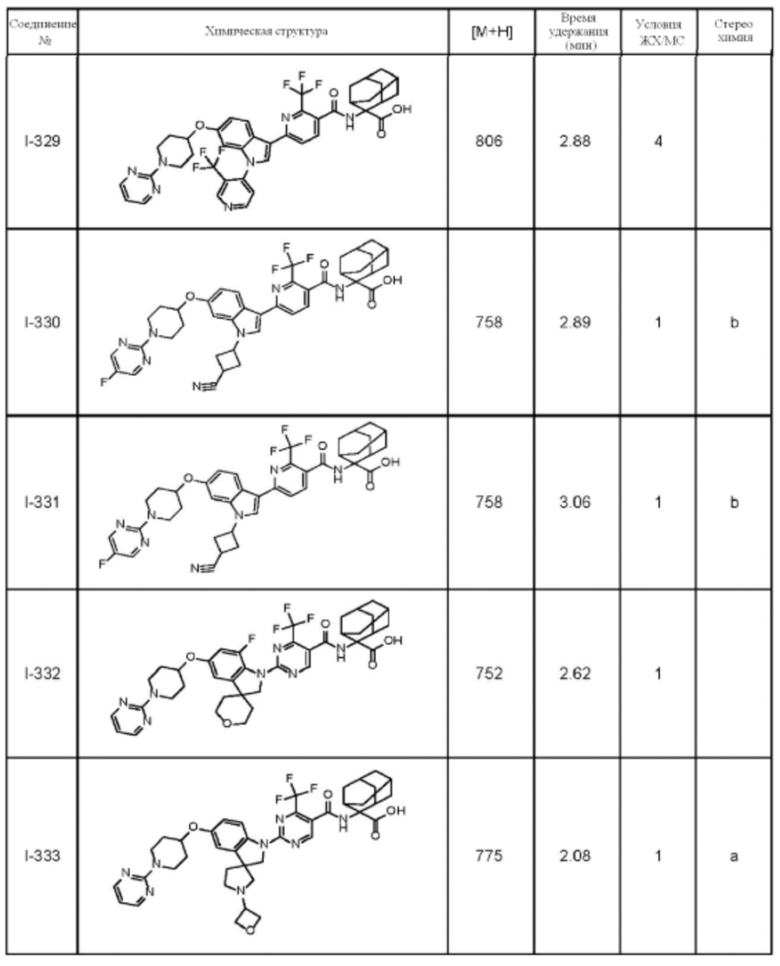
[0296]
[Таблица 57]
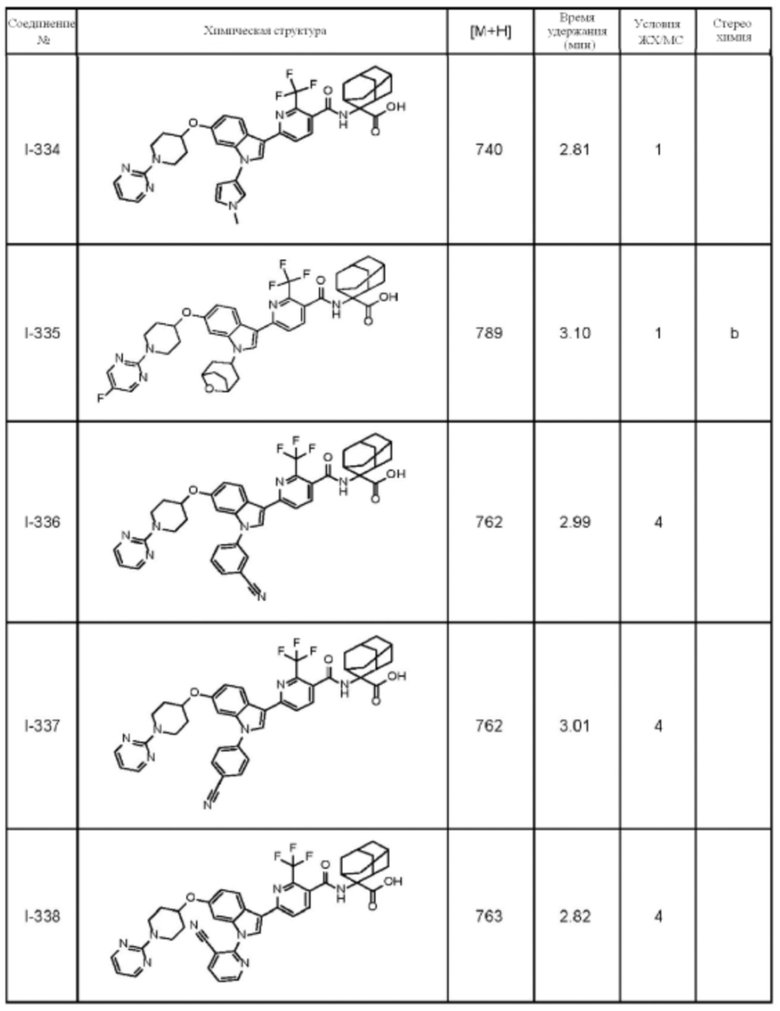
[0297]
[Таблица 58]
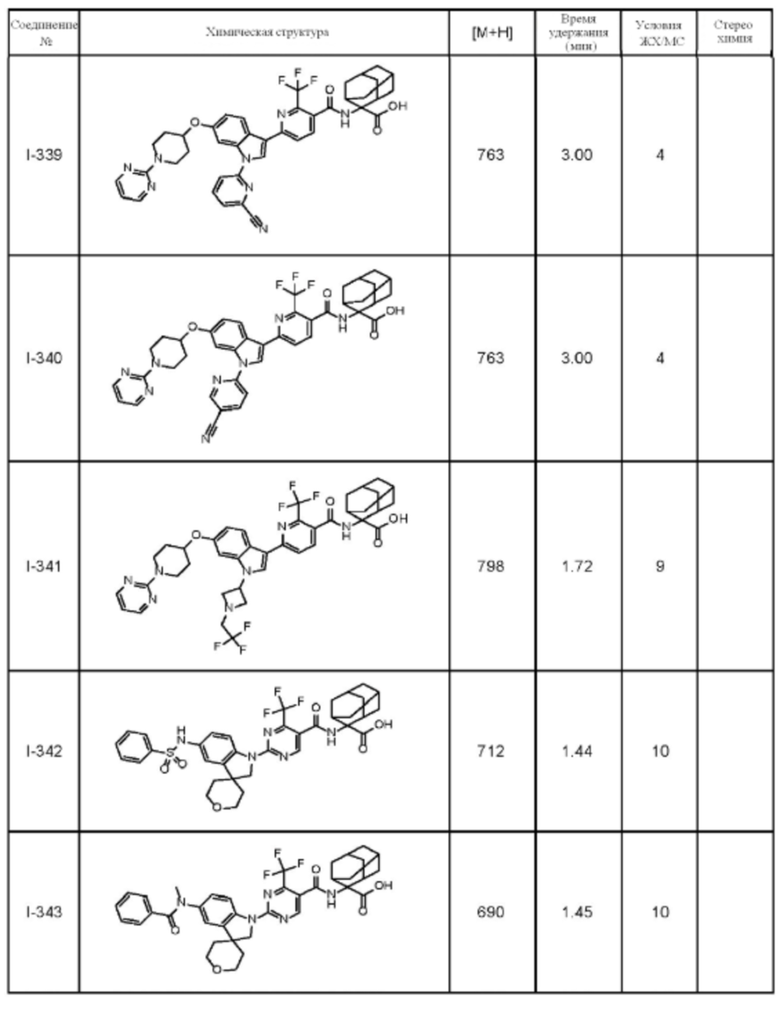
[0298]
[Таблица 59]
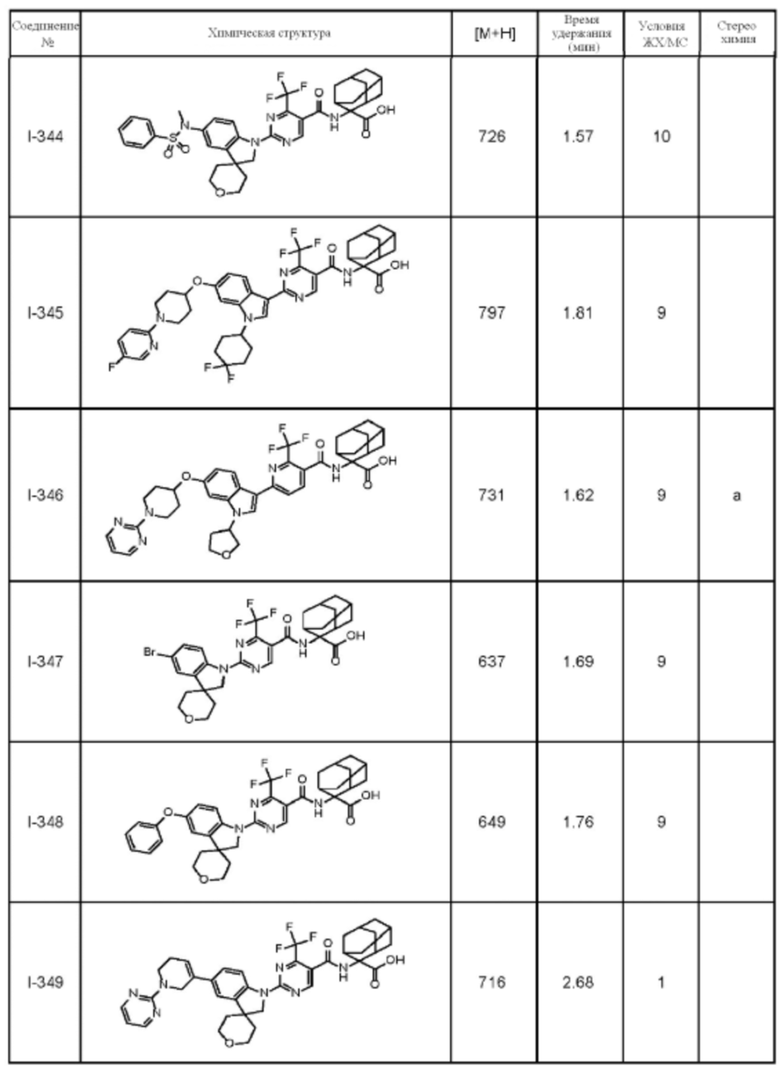
[0299]
[Таблица 60]
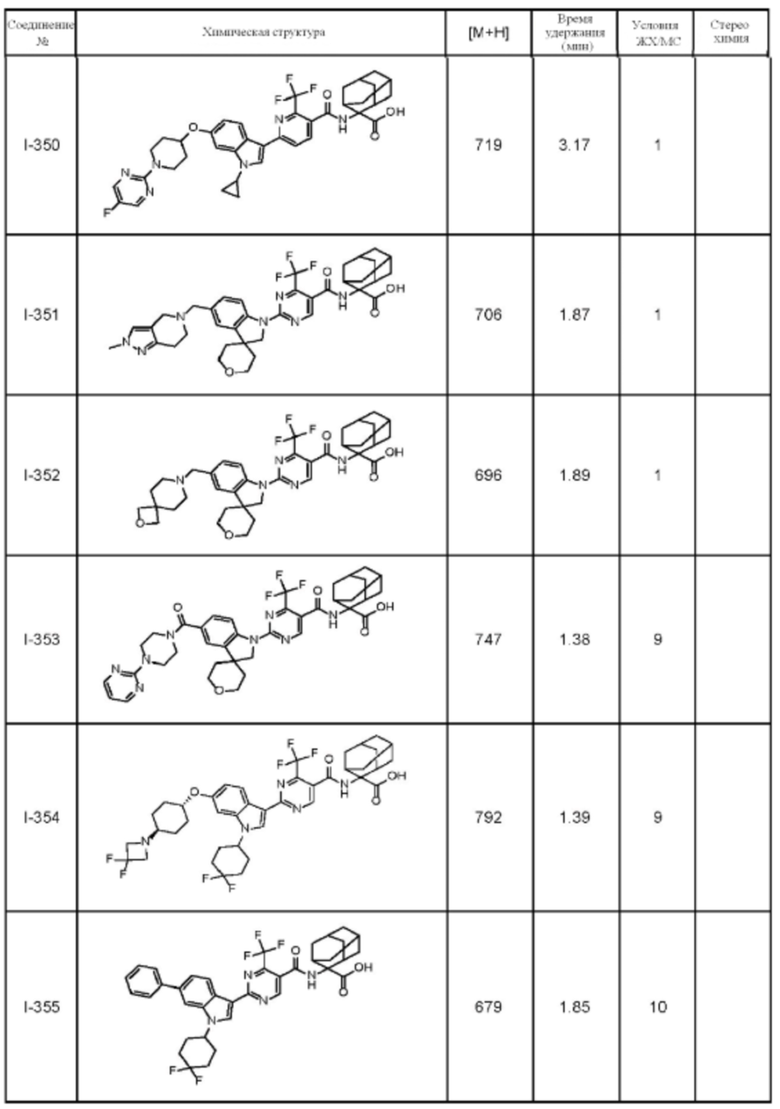
[0300]
[Таблица 61]
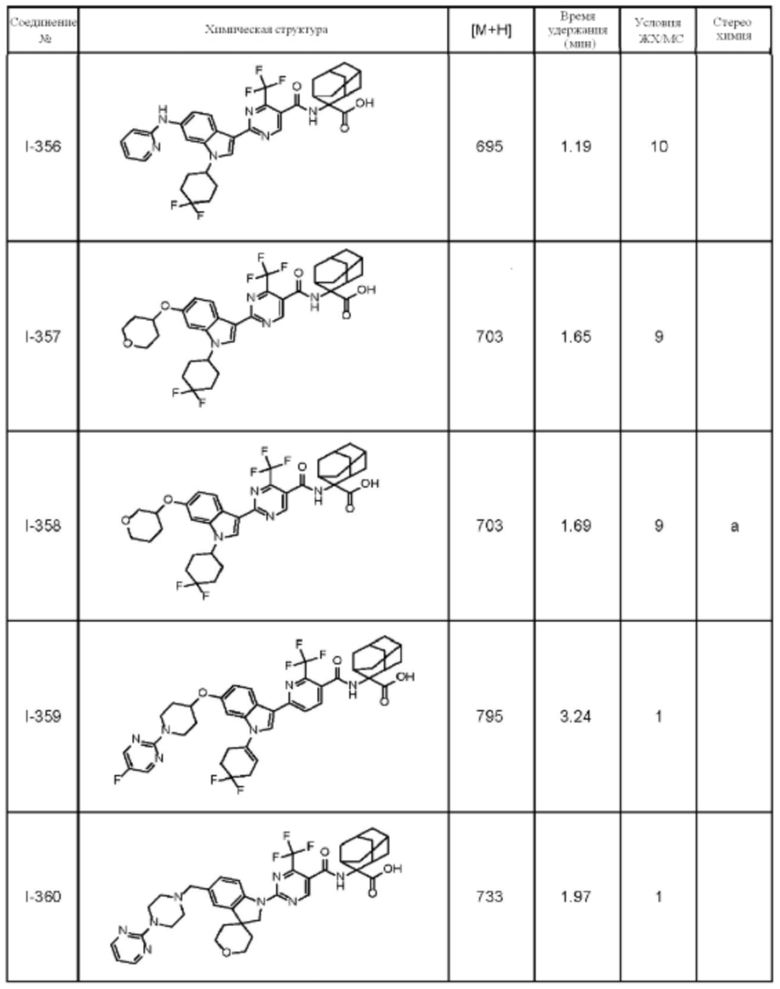
[0301]
[Таблица 62]
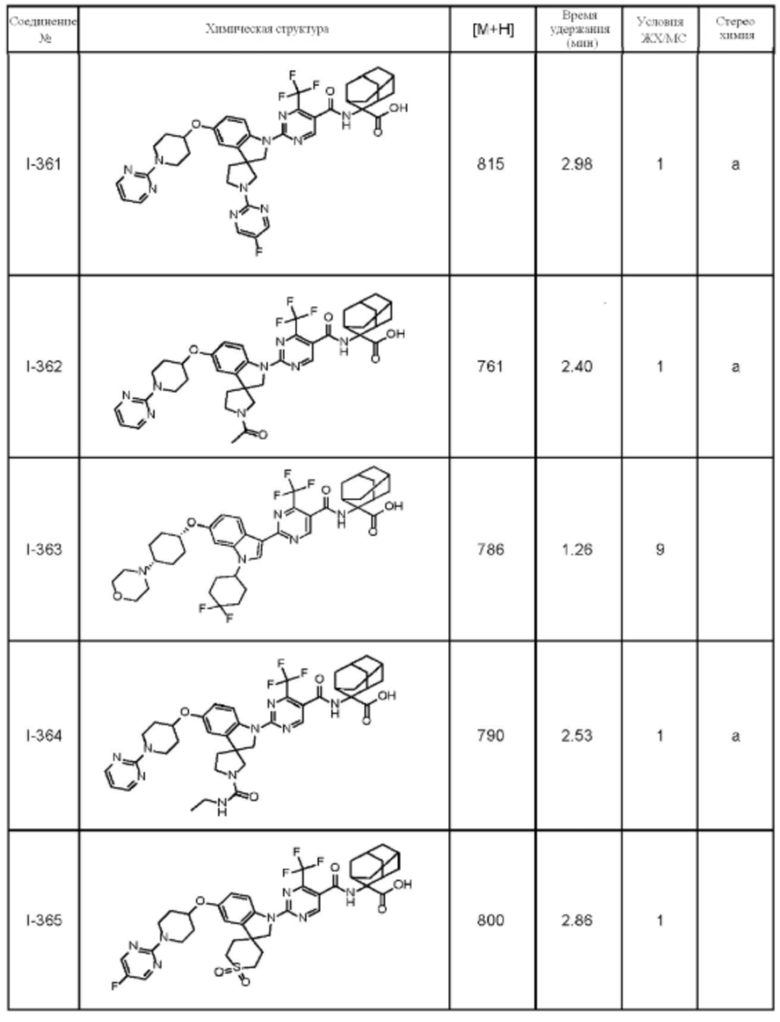
[0302]
[Таблица 63]
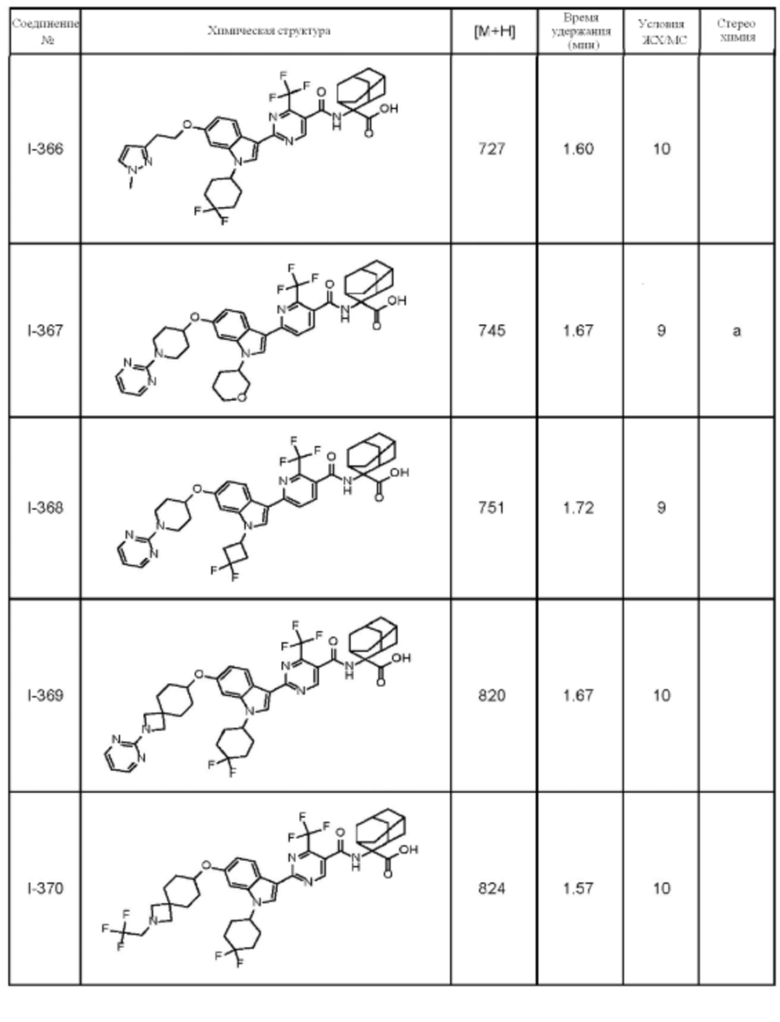
[0303]
[Таблица 64]
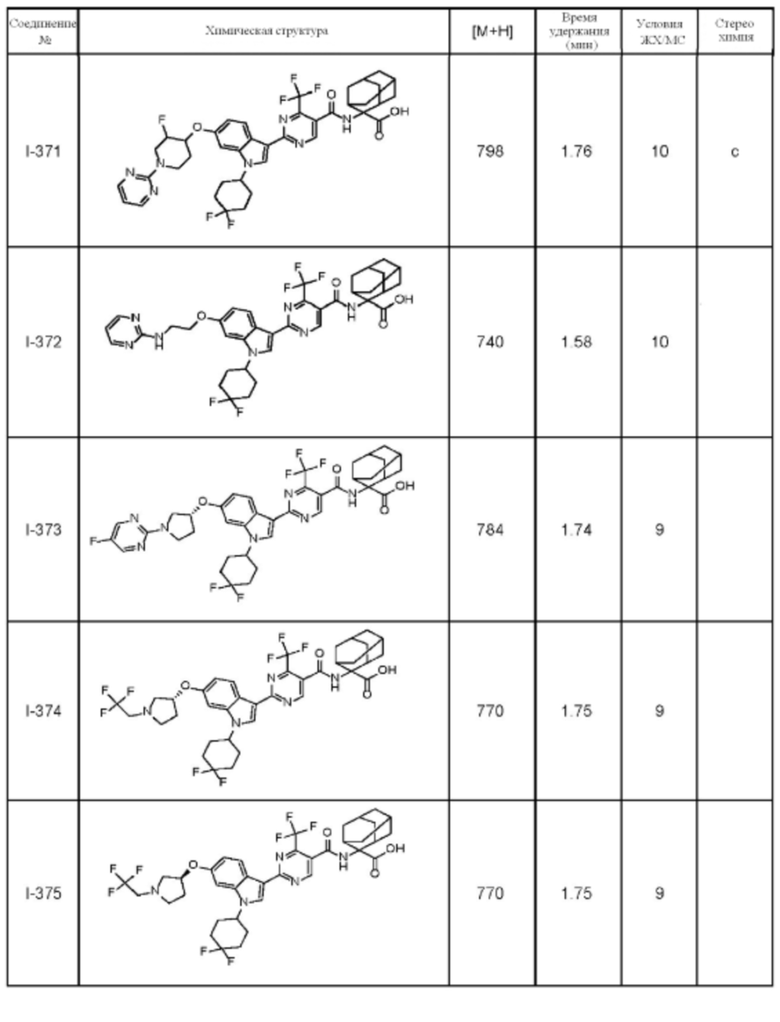
[0304]
[Таблица 65]
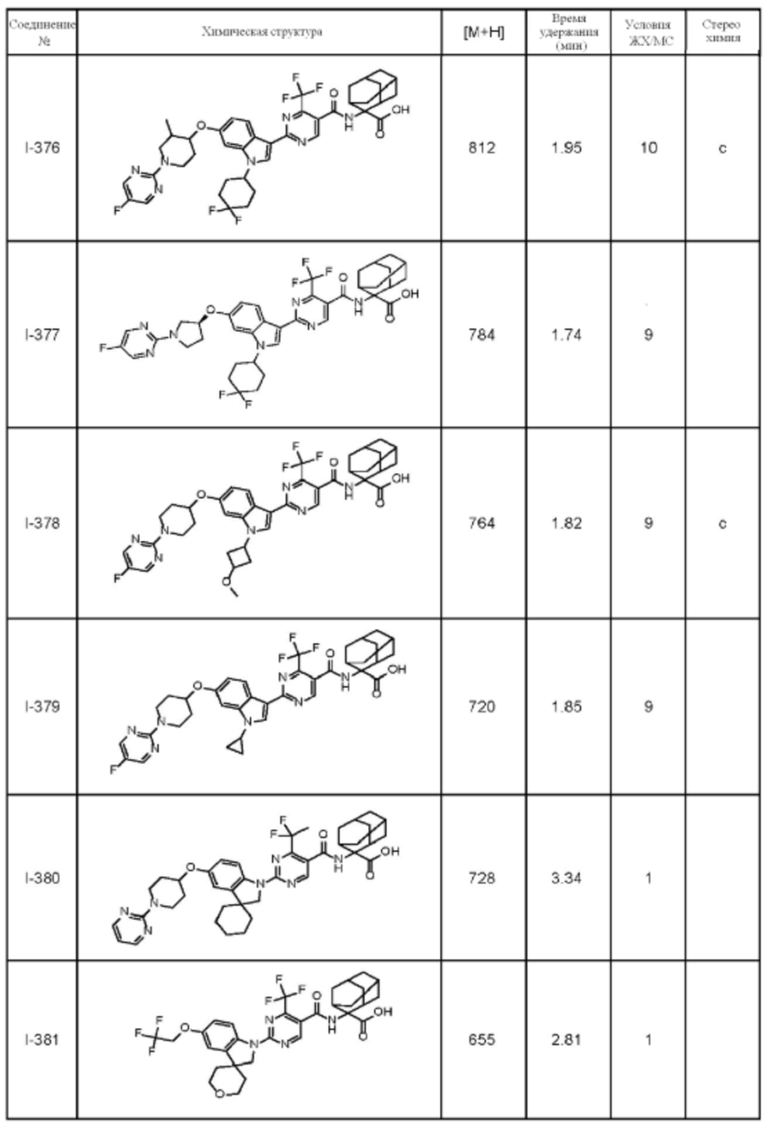
[0305]
[Таблица 66]
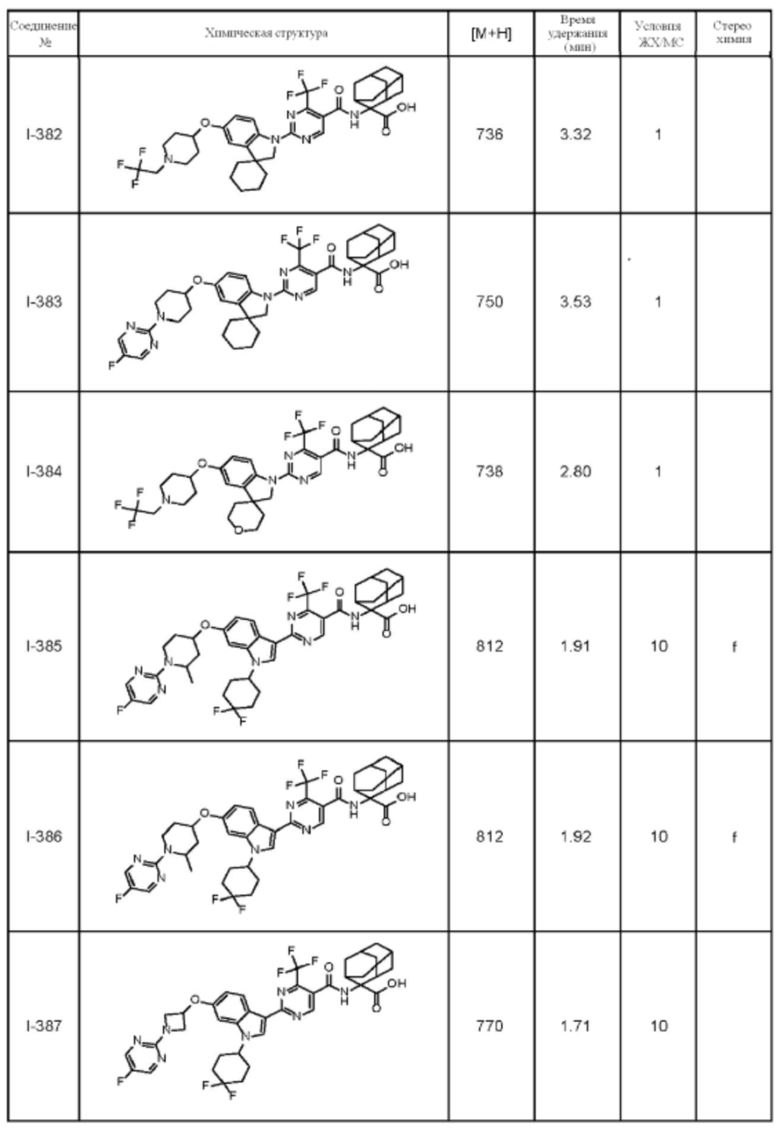
[0306]
[Таблица 67]
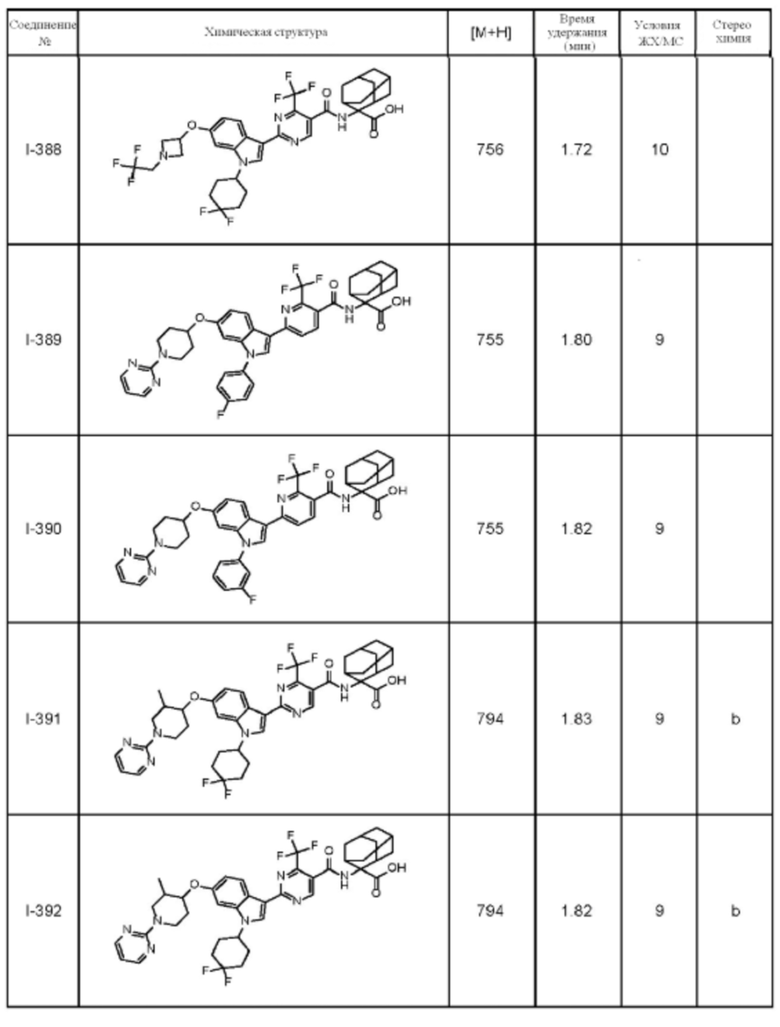
[0307]
[Таблица 68]
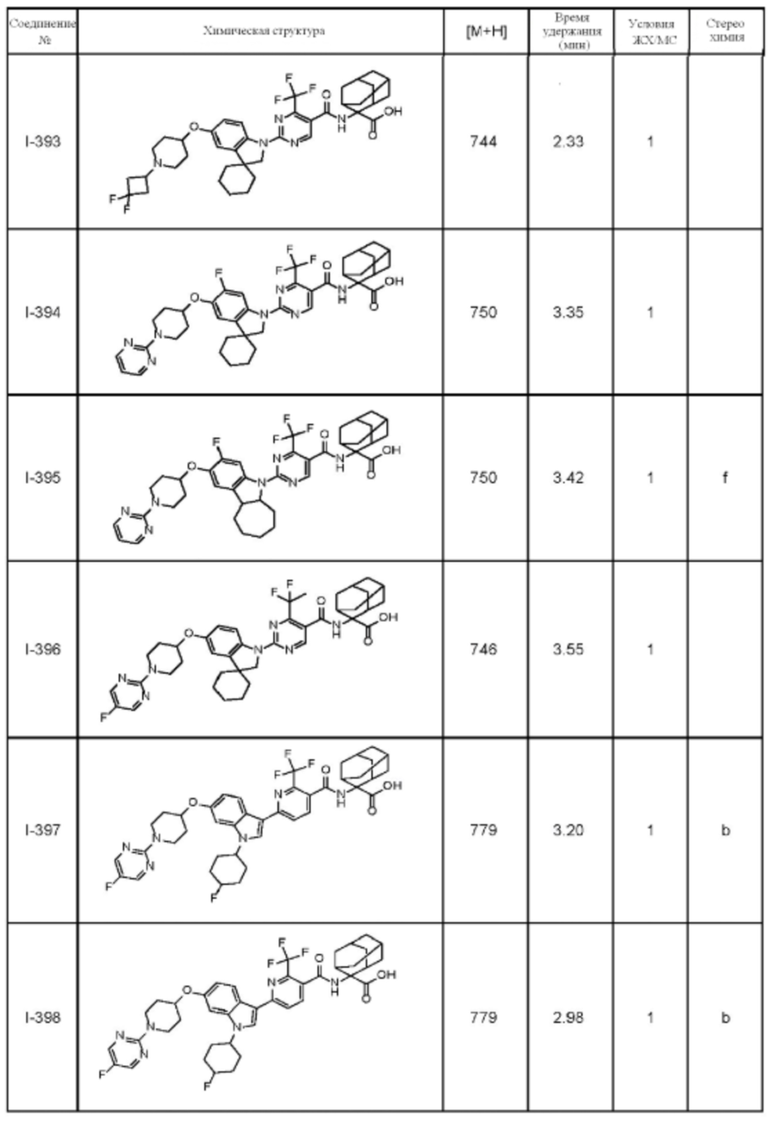
[0308]
[Таблица 69]
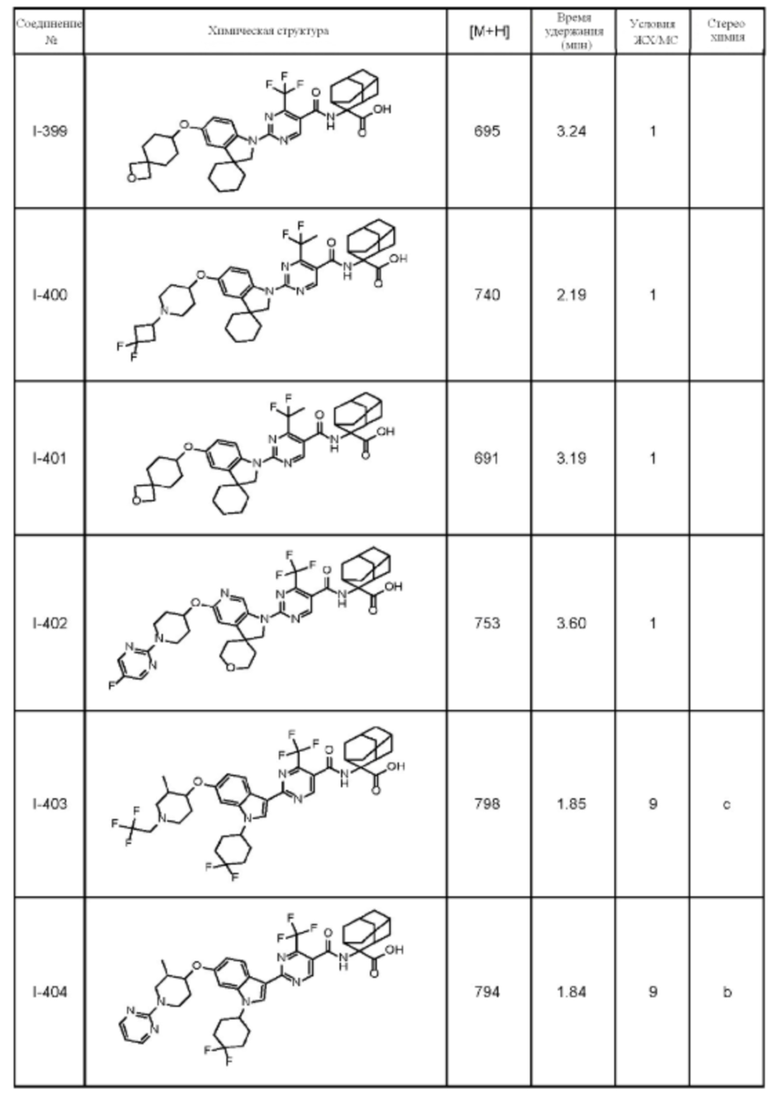
[0309]
[Таблица 70]
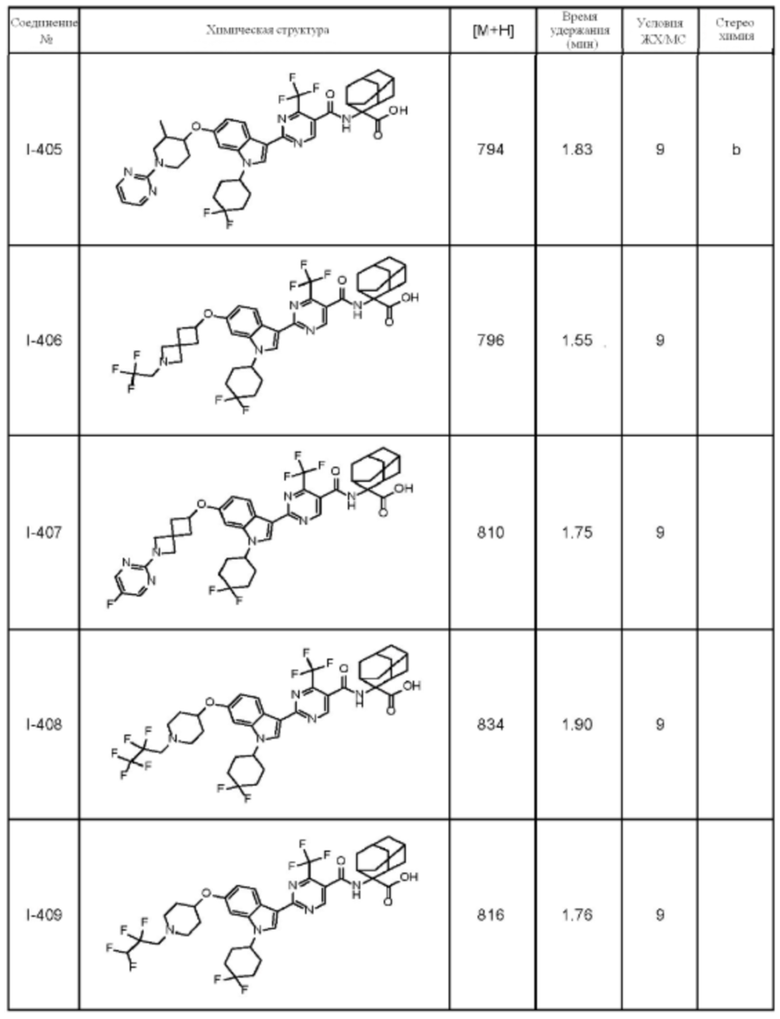
[0310]
[Таблица 71]
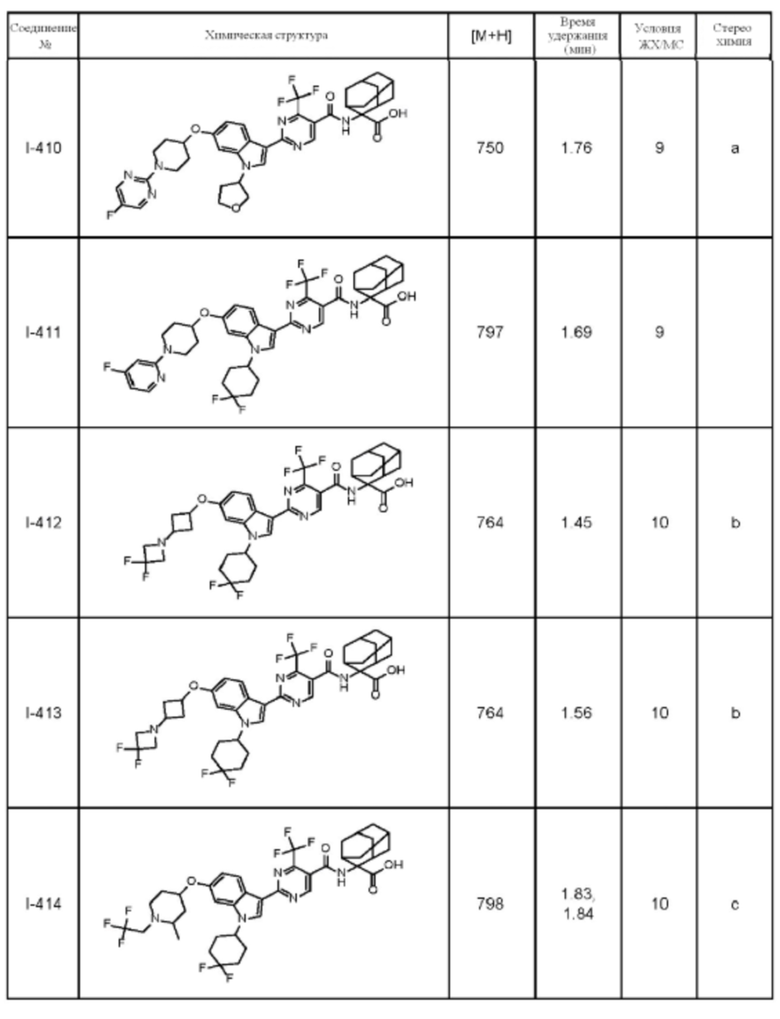
[0311]
[Таблица 72]
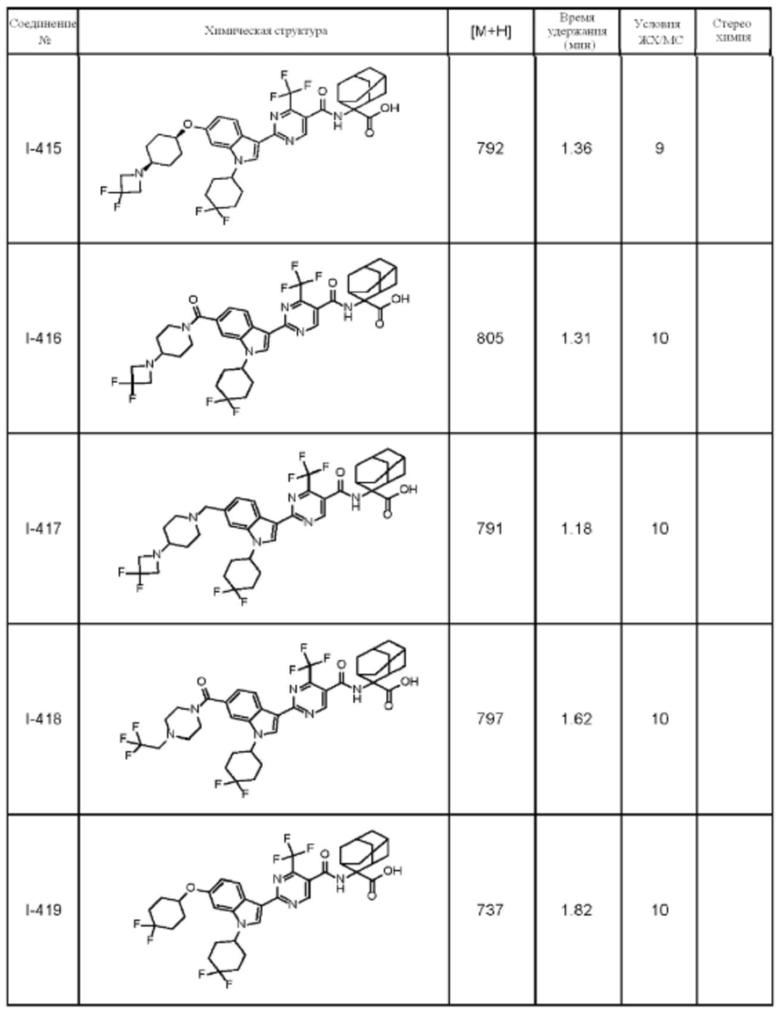
[0312]
[Таблица 73]
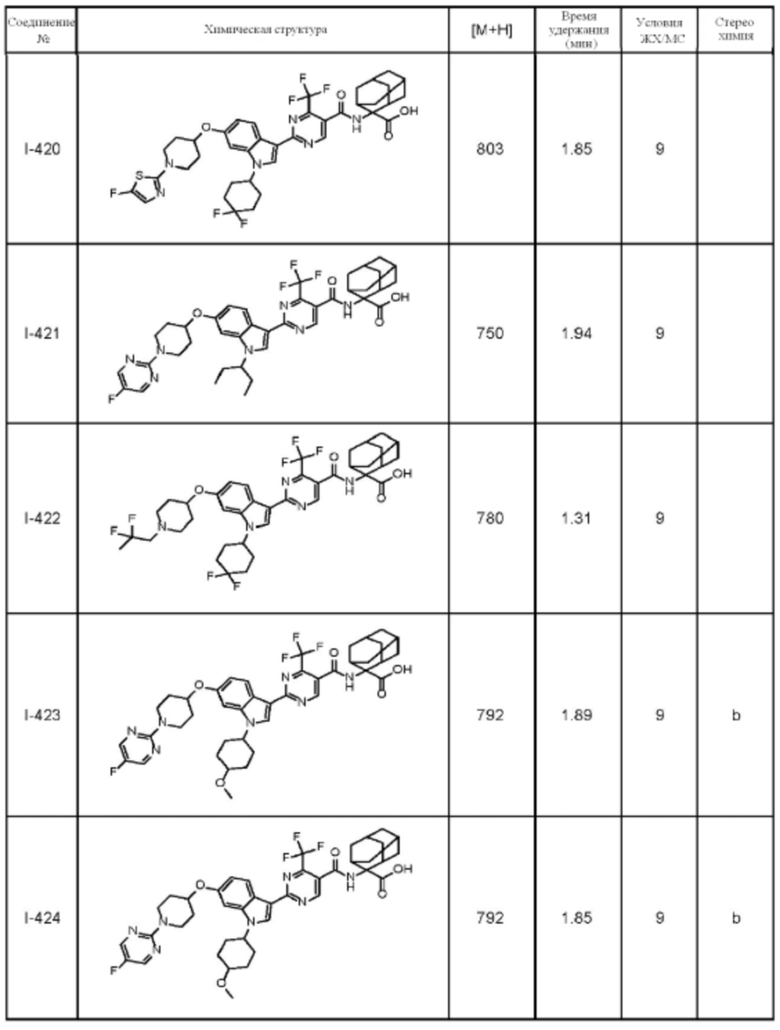
[0313]
[Таблица 74]
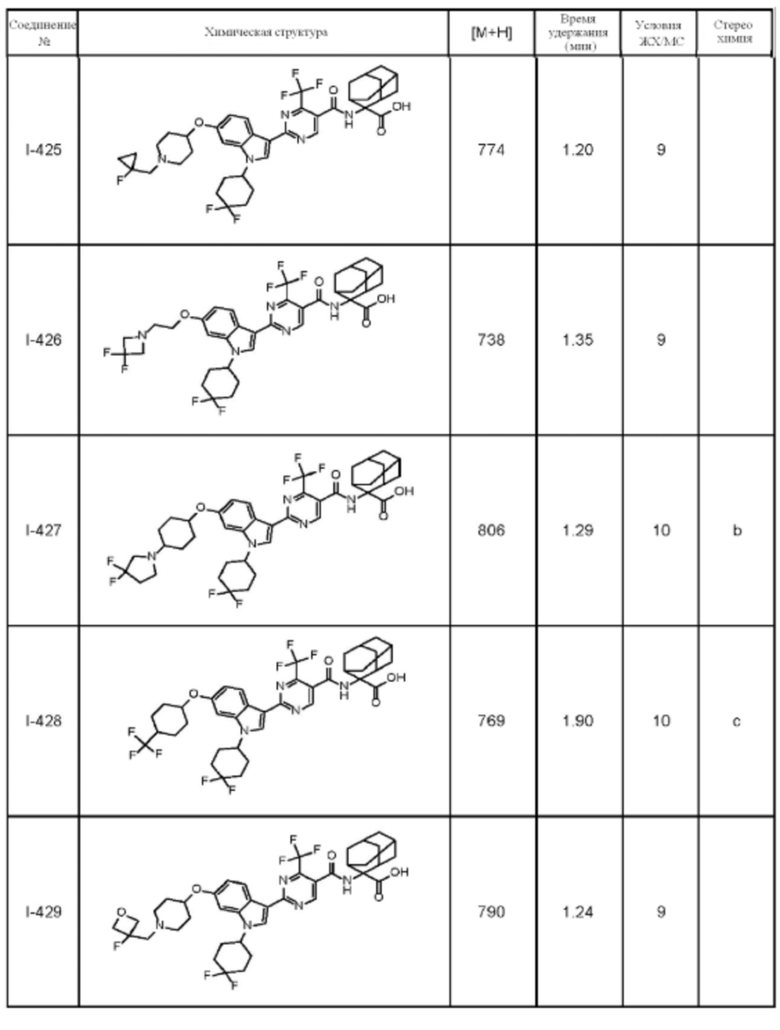
[0314]
[Таблица 75]
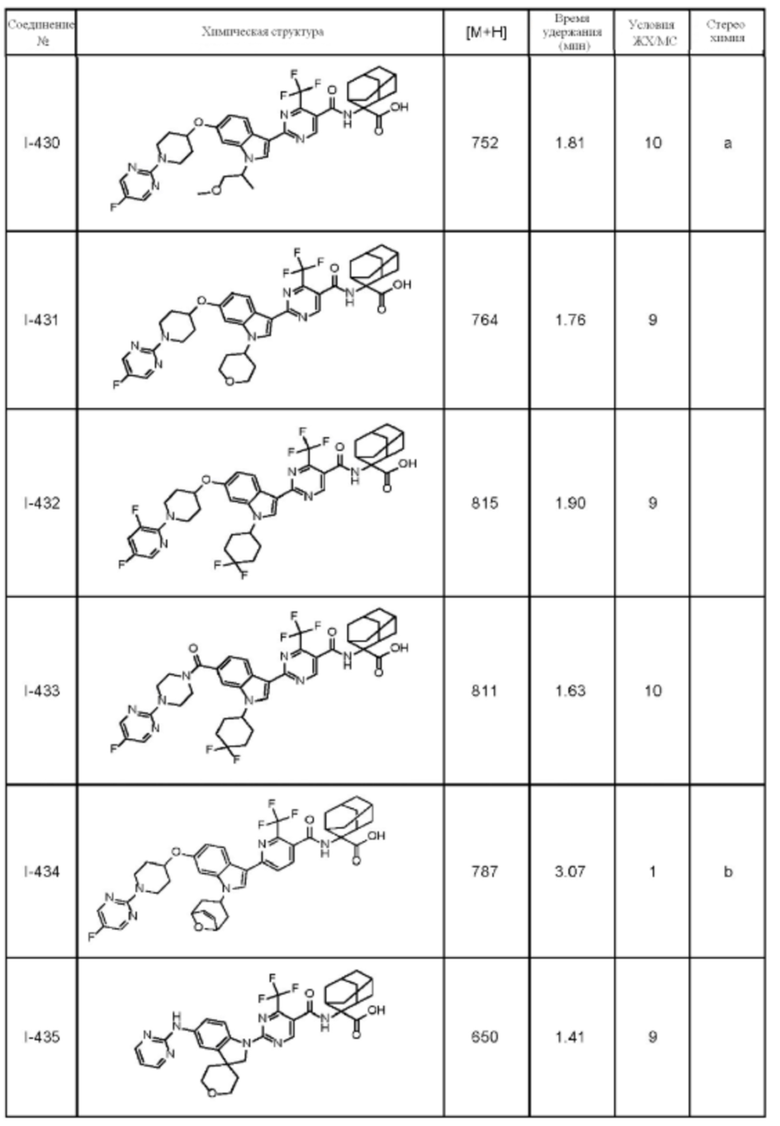
[0315]
[Таблица 76]
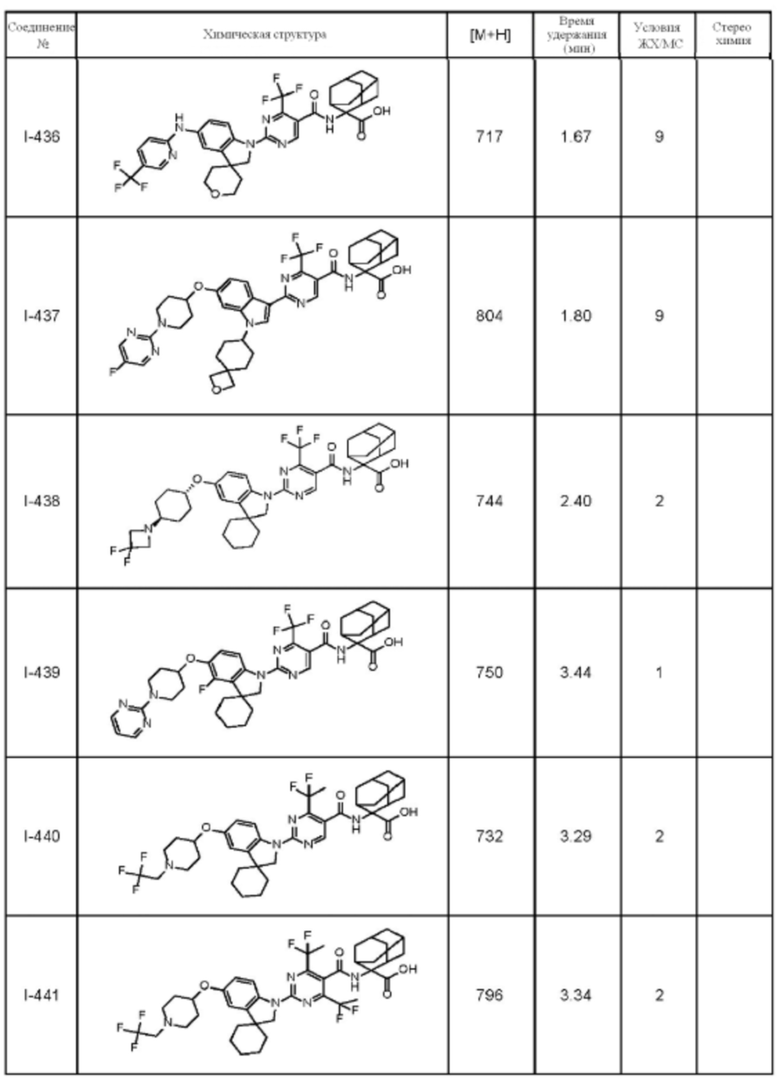
[0316]
[Таблица 77]
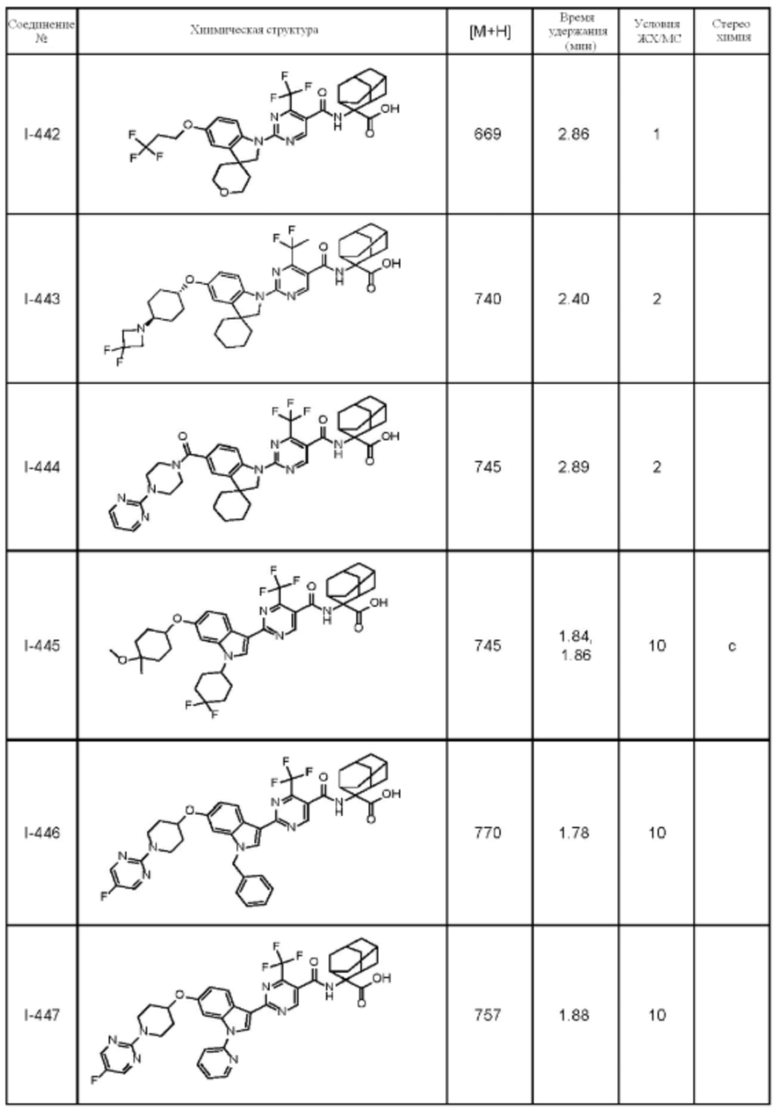
[0317]
[Таблица 78]
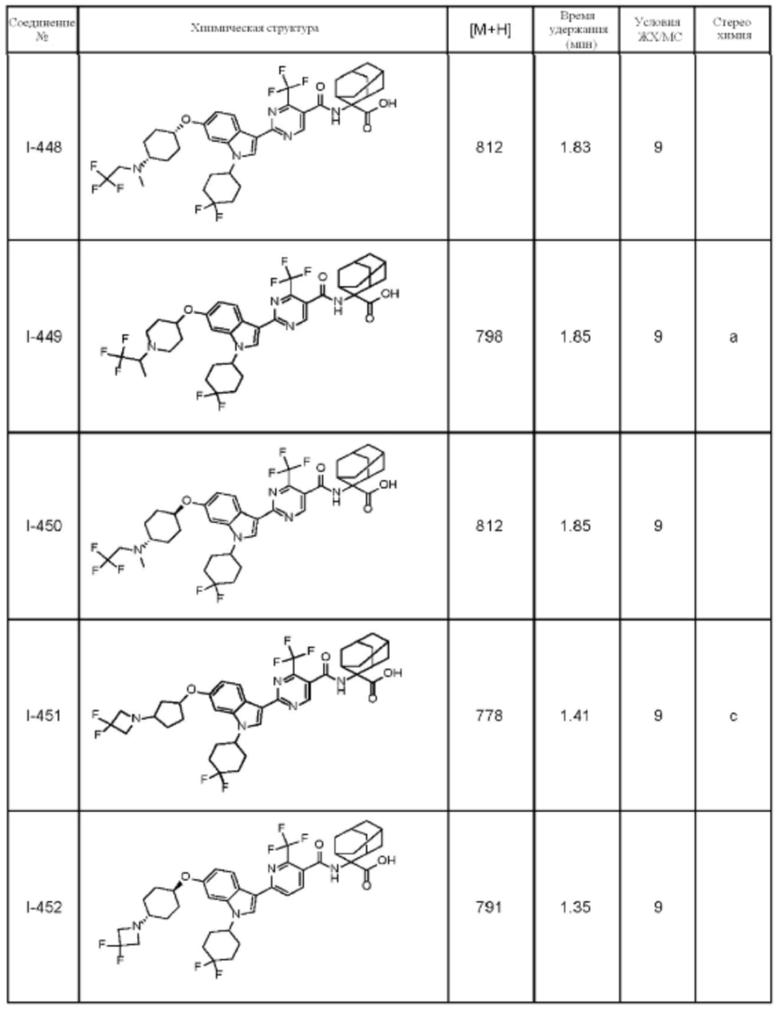
[0318]
[Таблица 79]
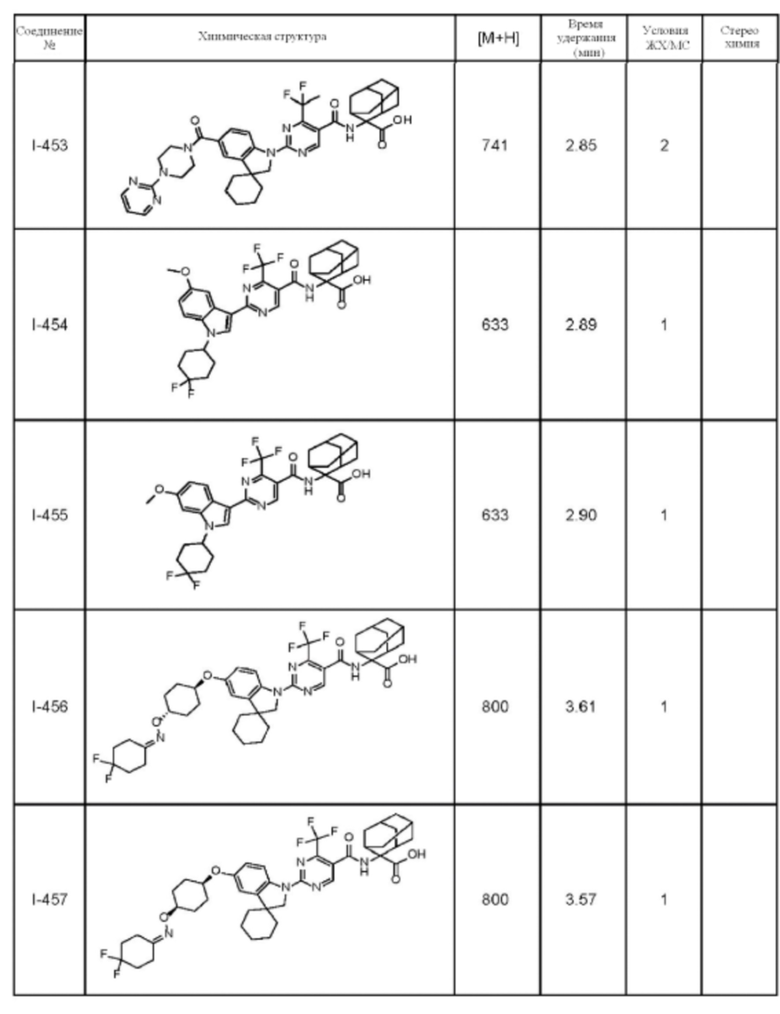
[0319]
[Таблица 80]
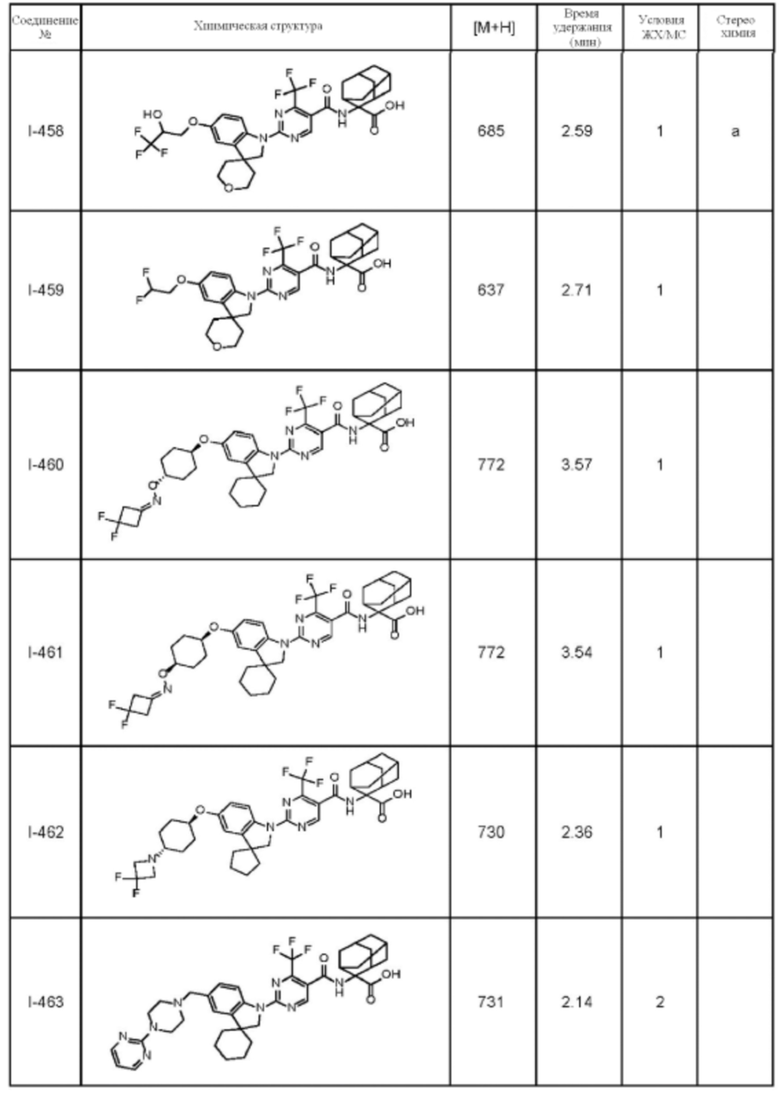
[0320]
[Таблица 81]
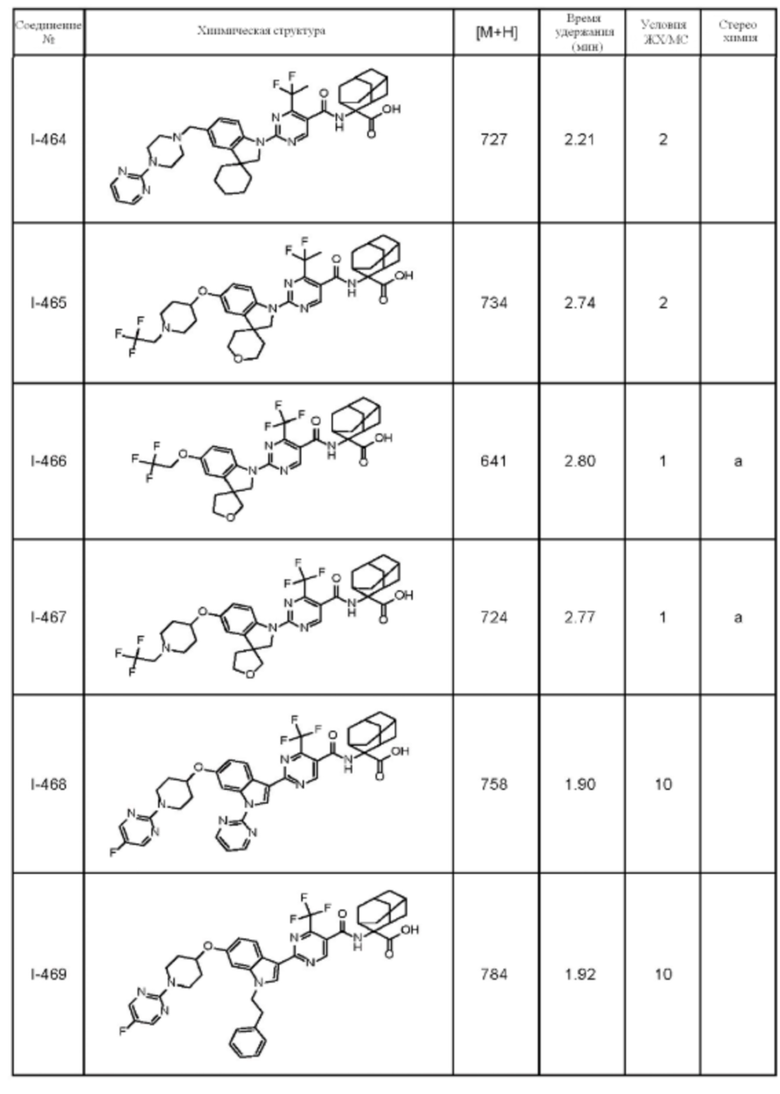
[0321]
[Таблица 82]
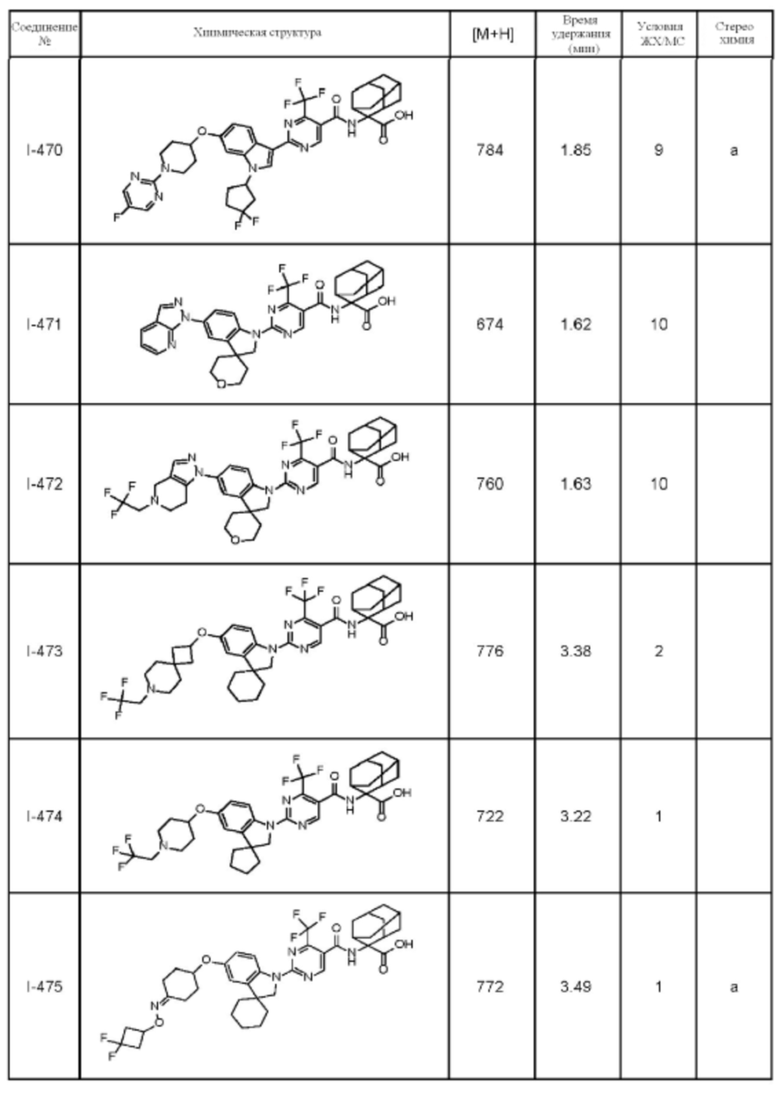
[0322]
[Таблица 83]
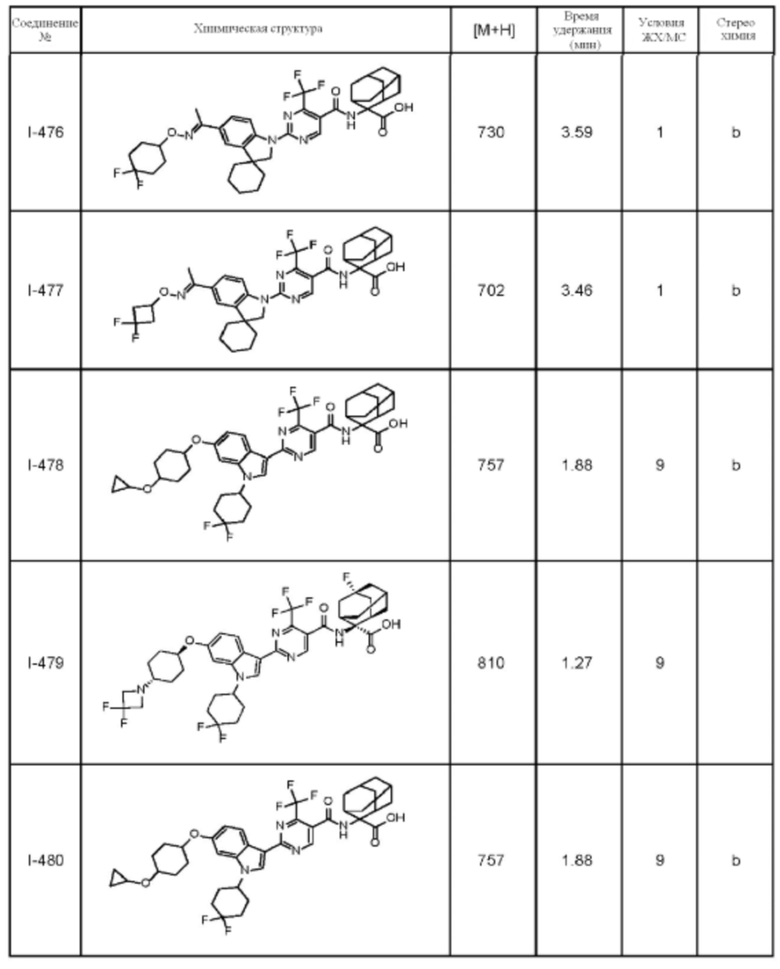
[0323]
[Таблица 84]
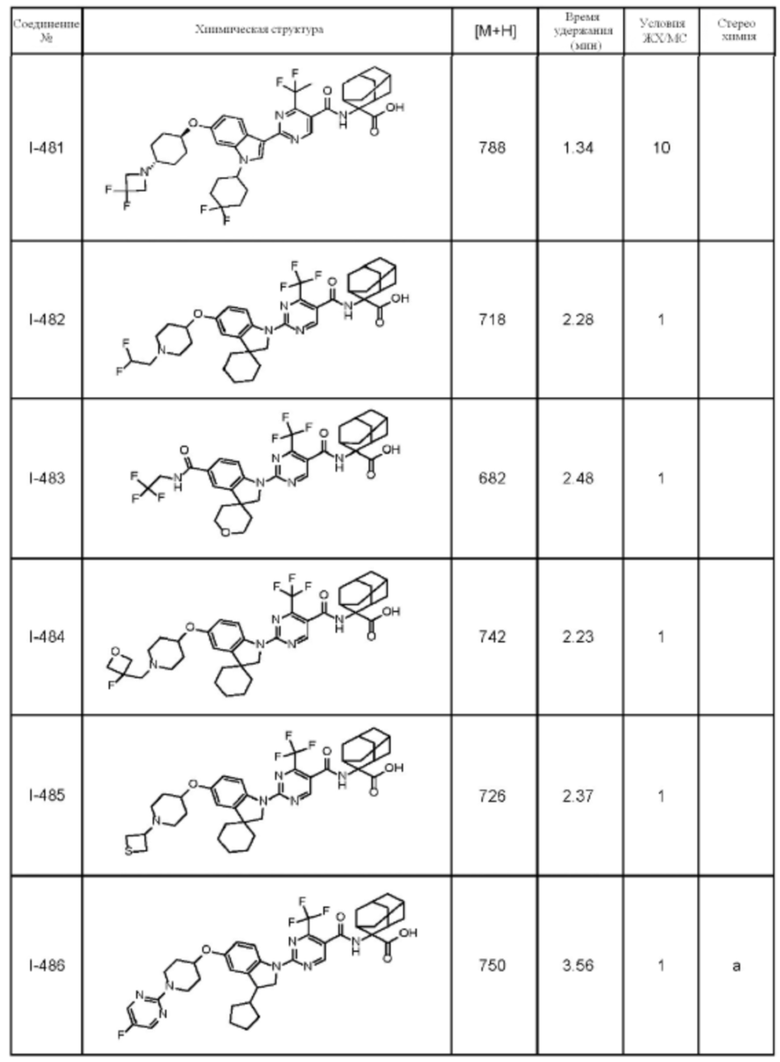
[0324]
[Таблица 85]
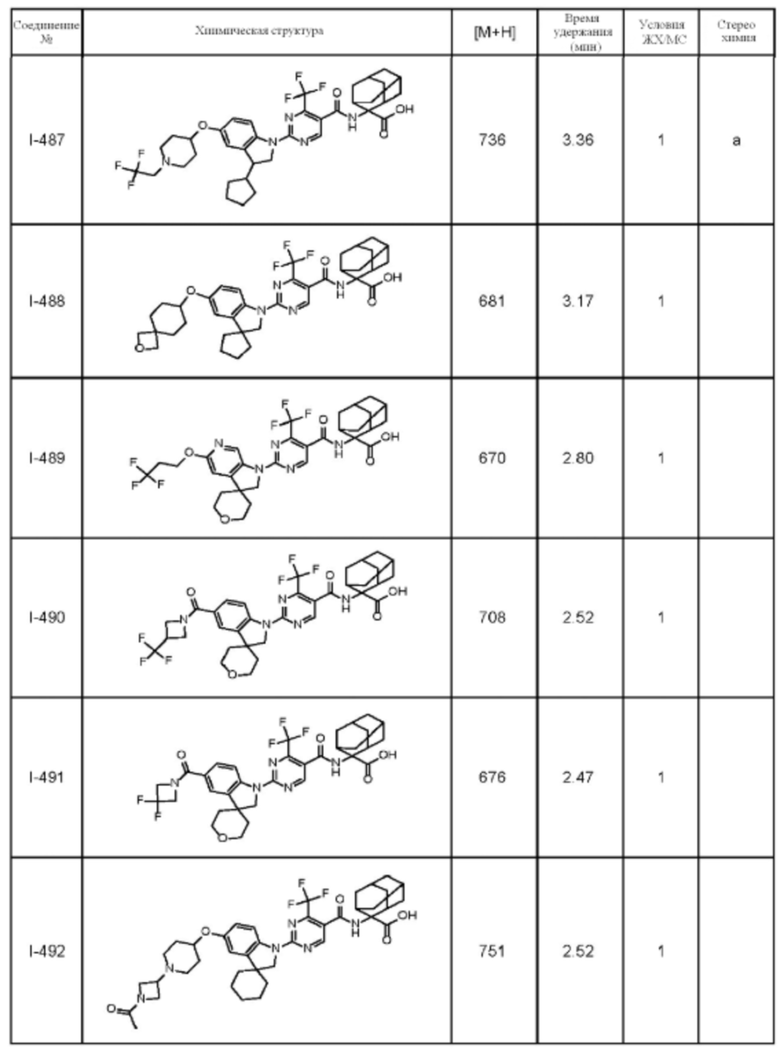
[0325]
[Таблица 86]
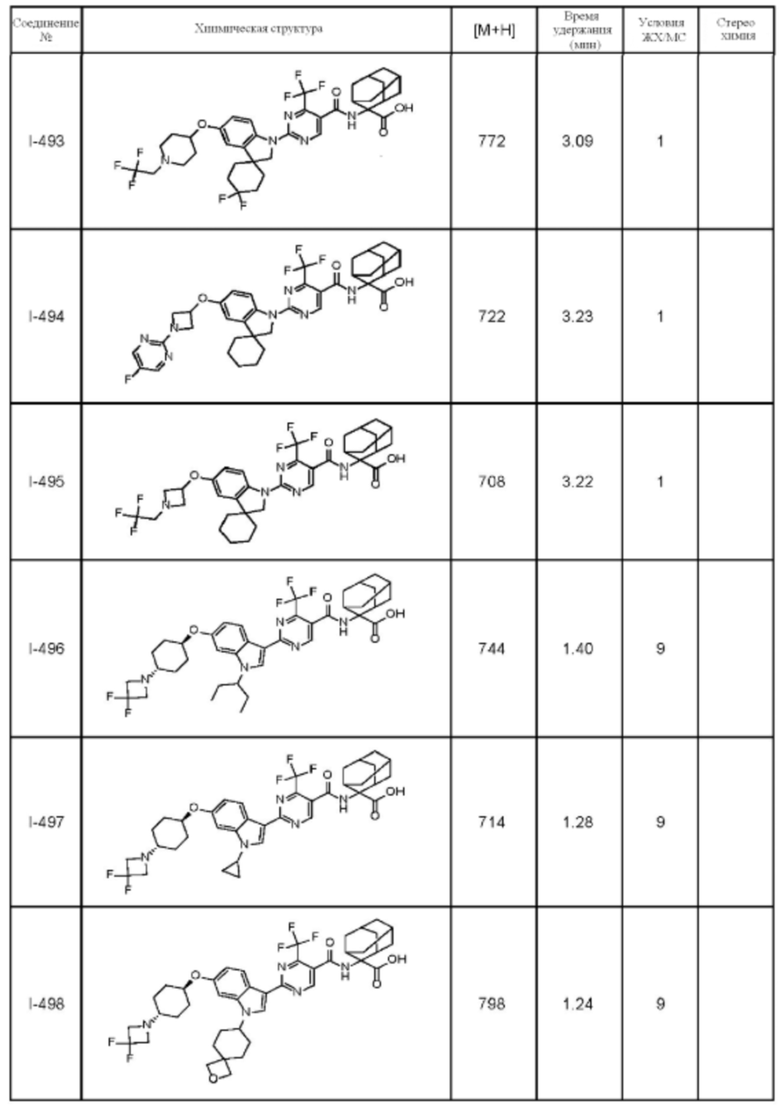
[0326]
[Таблица 87]
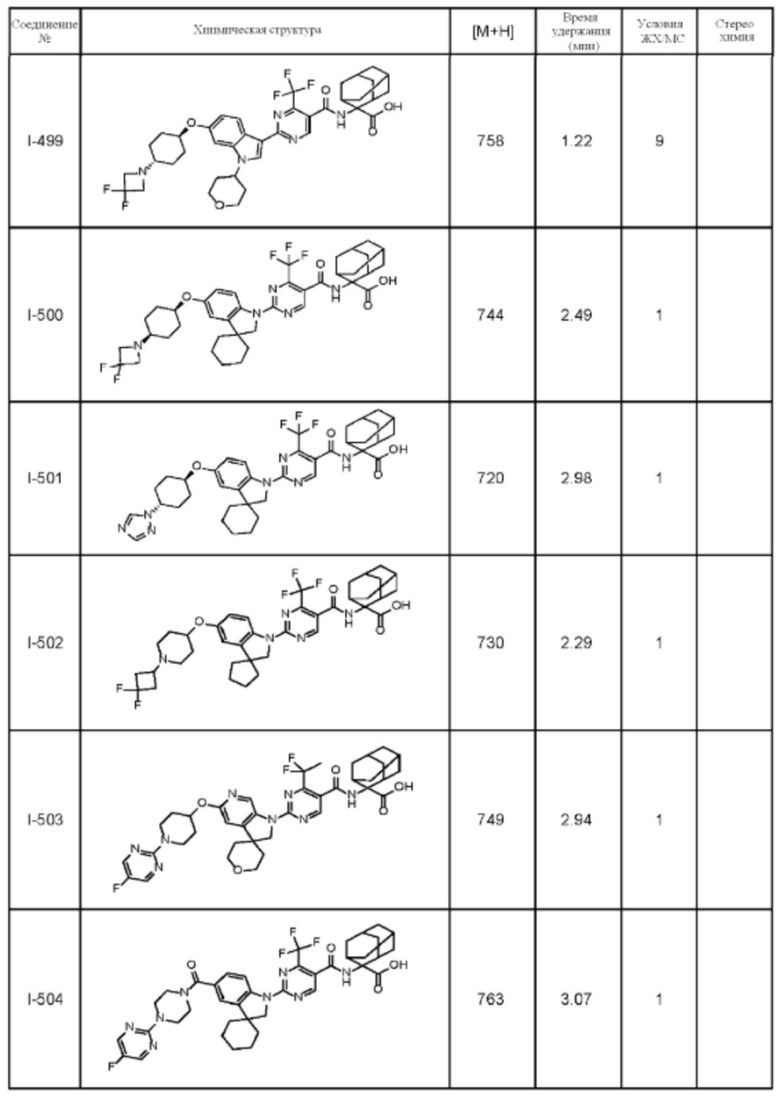
[0327]
[Таблица 88]
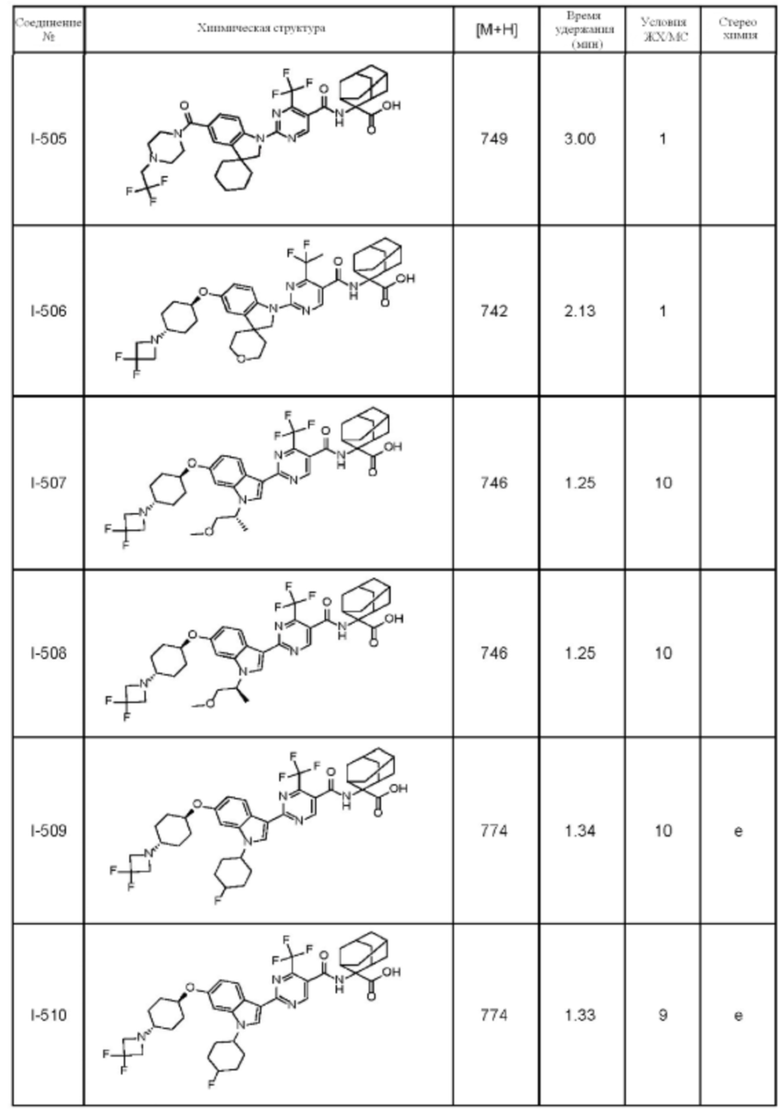
[0328]
[Таблица 89]
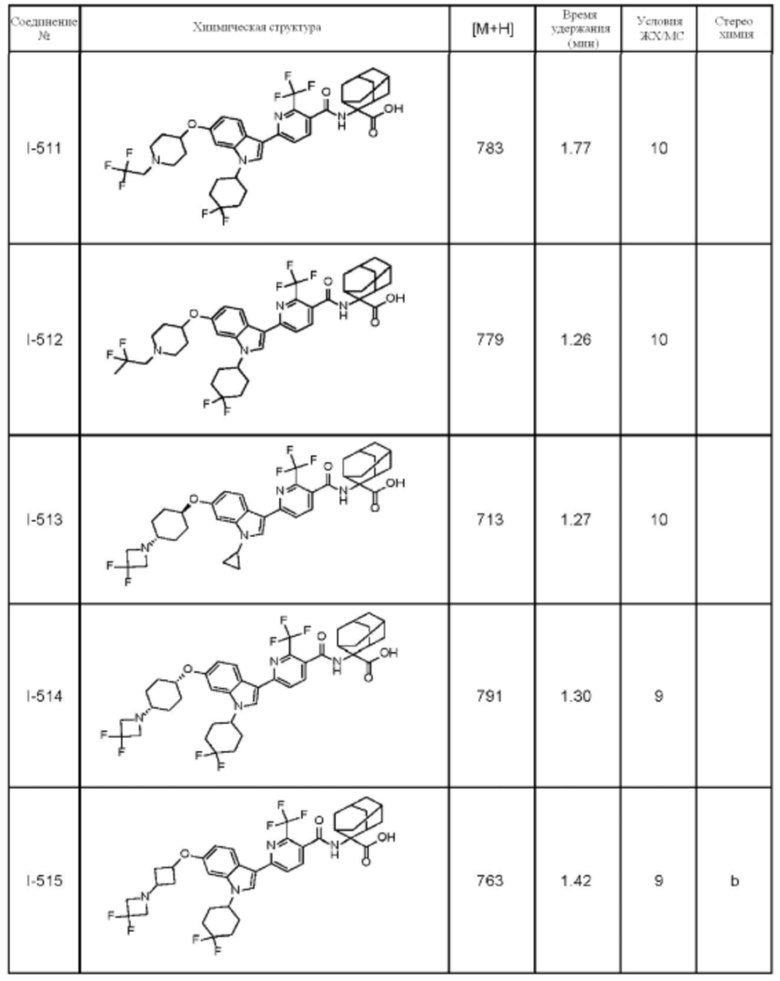
[0329]
[Таблица 90]
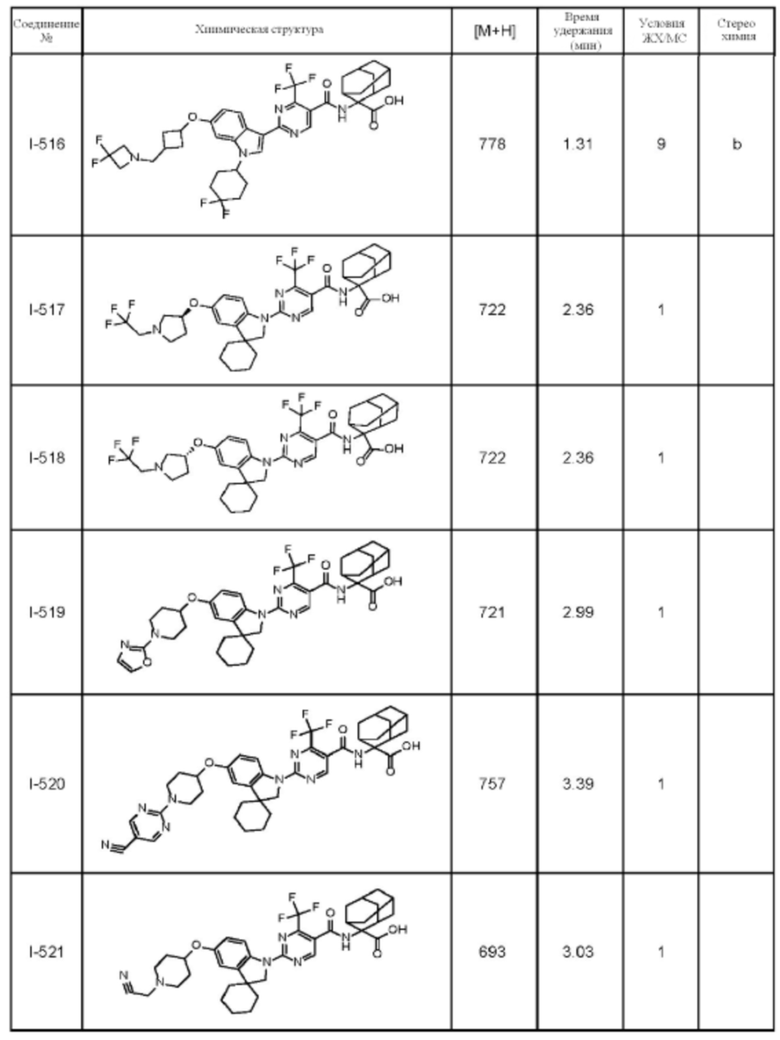
[0330]
[Таблица 91]
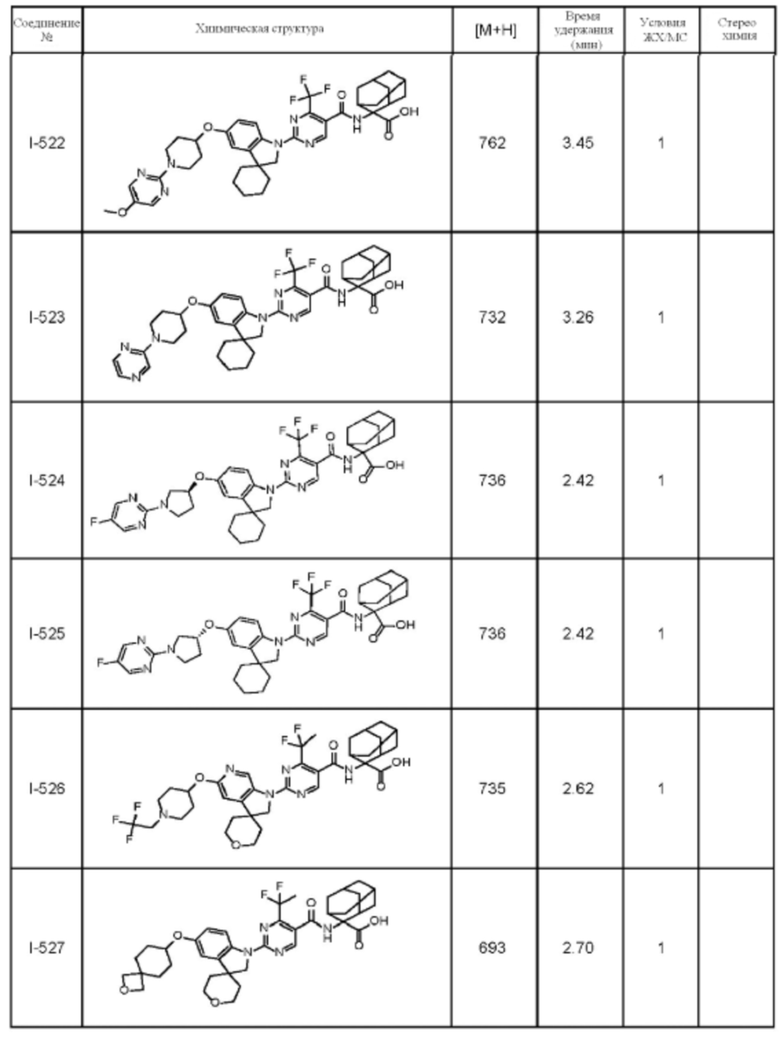
[0331]
[Таблица 92]
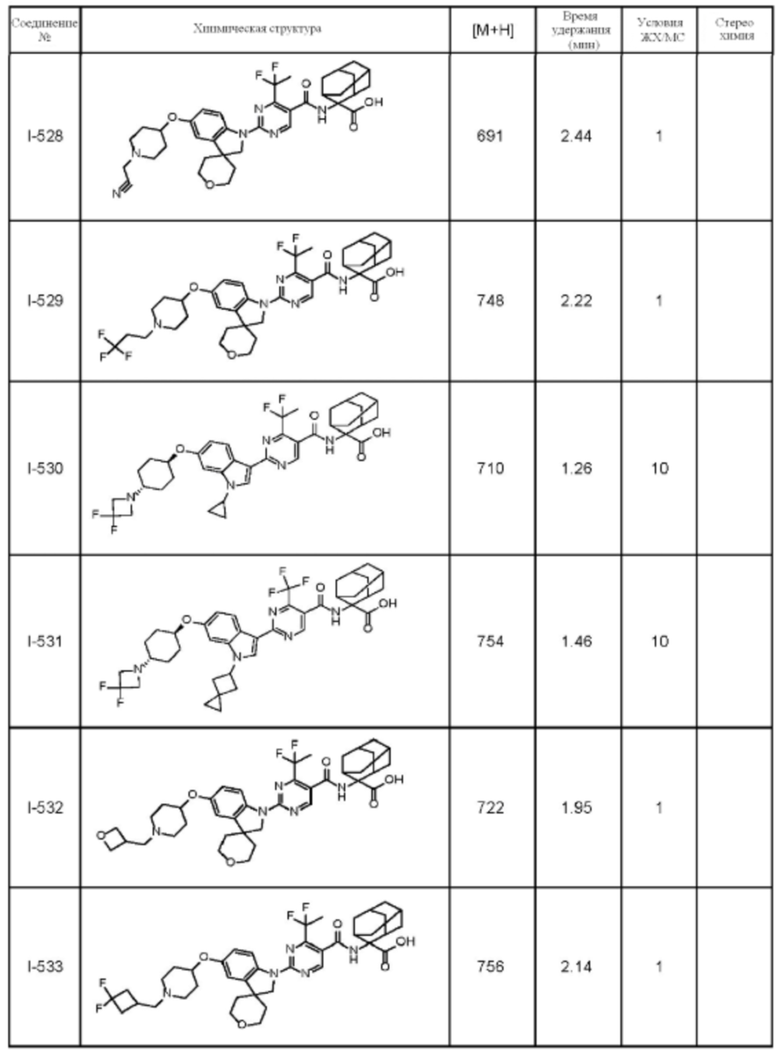
[0332]
[Таблица 93]
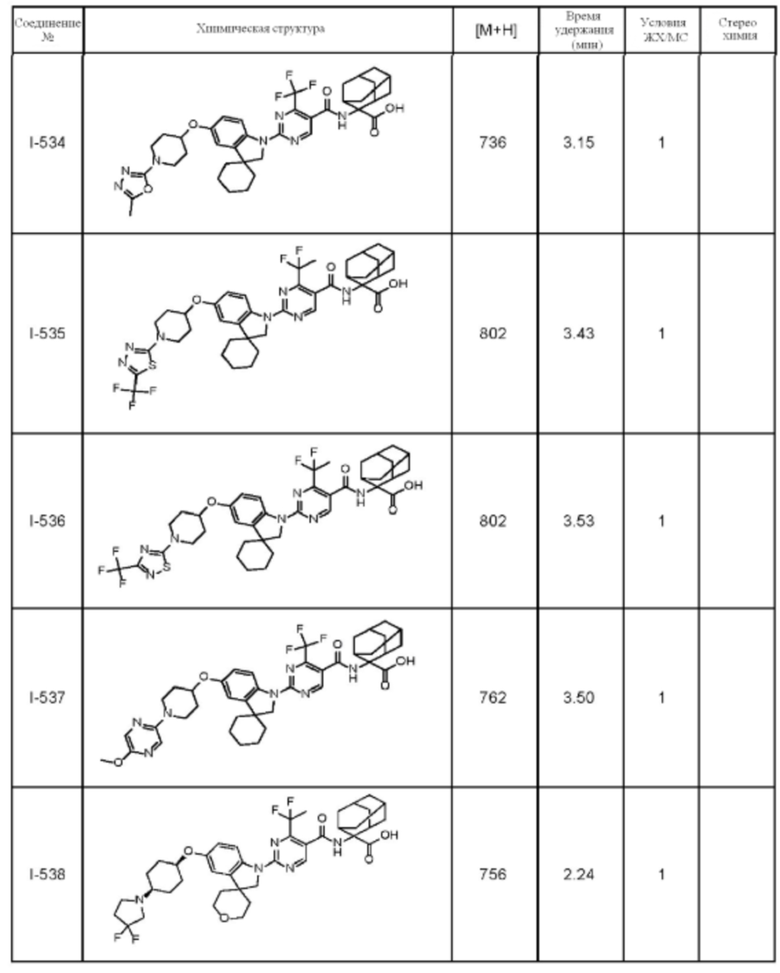
[0333]
[Таблица 94]
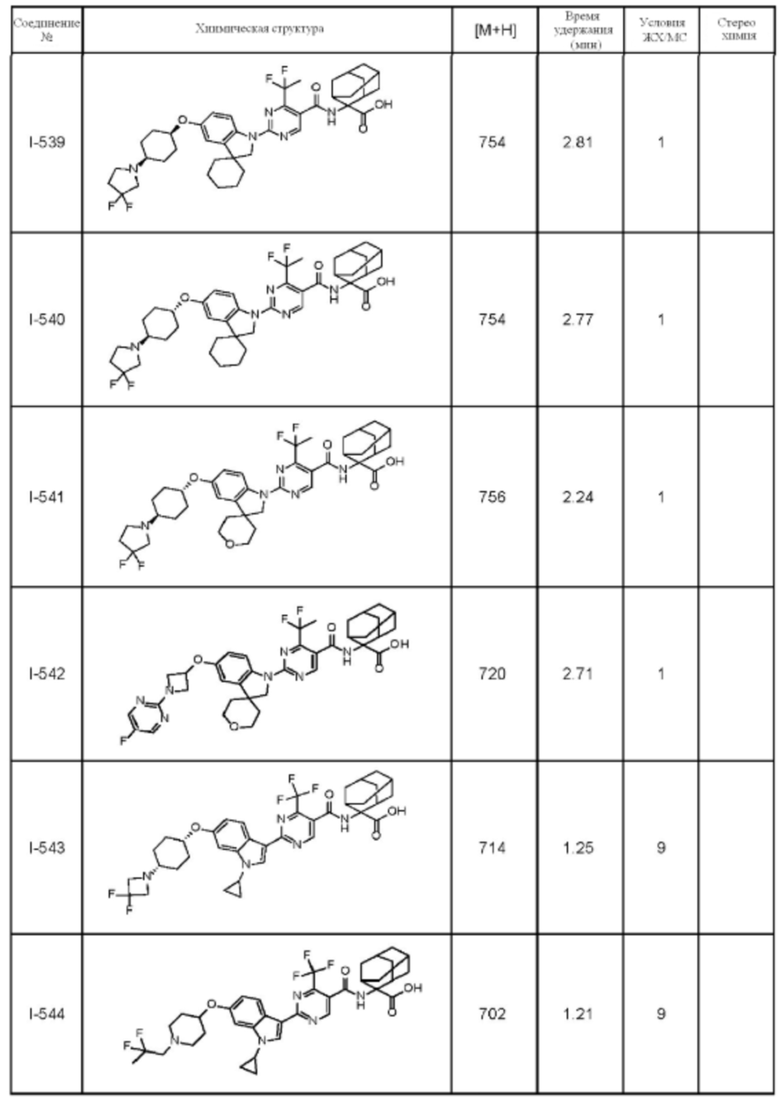
[0334]
[Таблица 95]
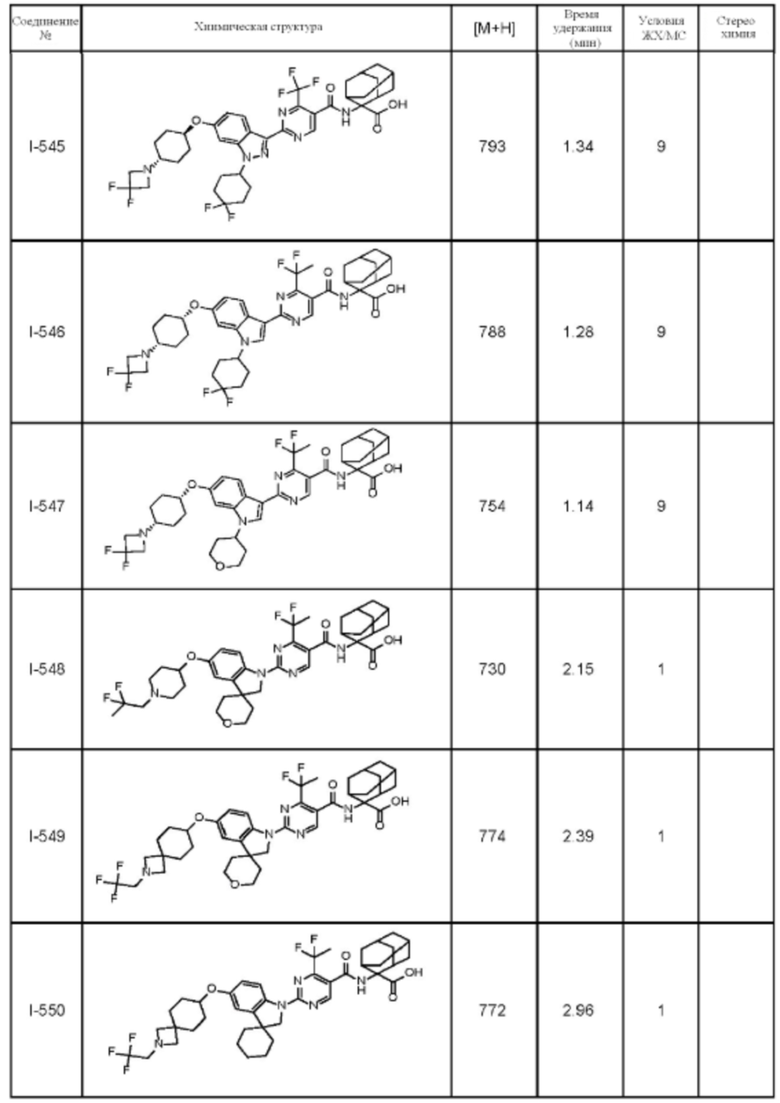
[0335]
[Таблица 96]
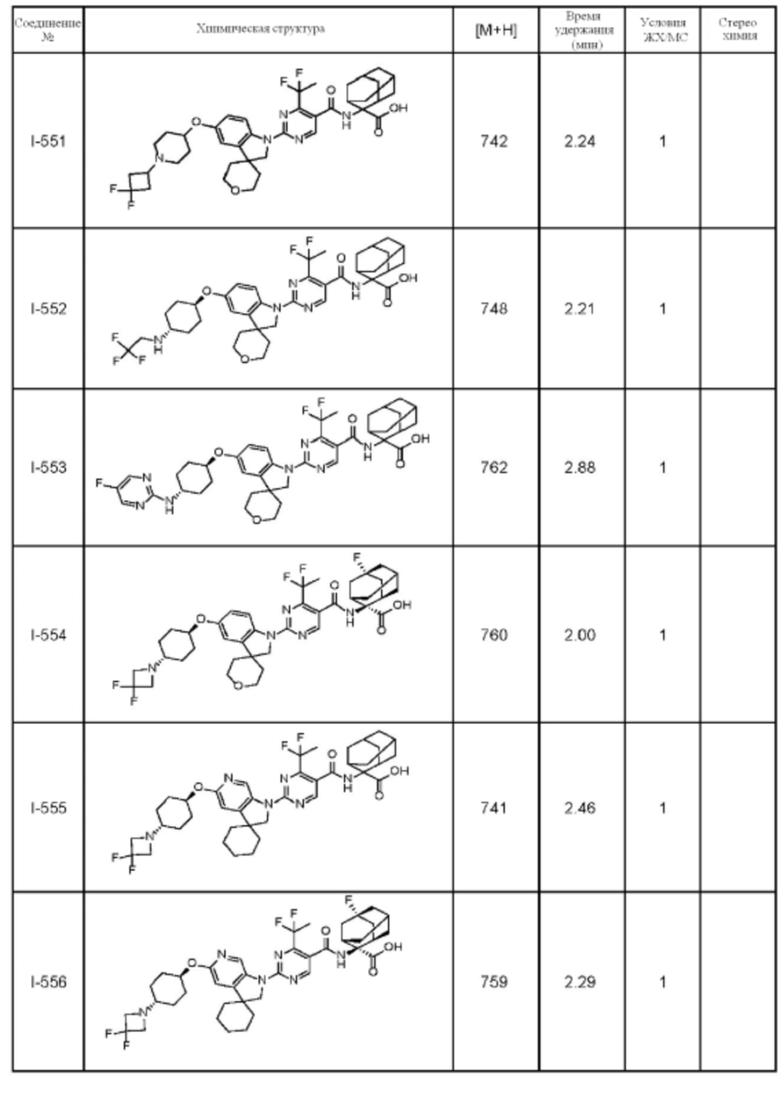
[0336]
[Таблица 97]
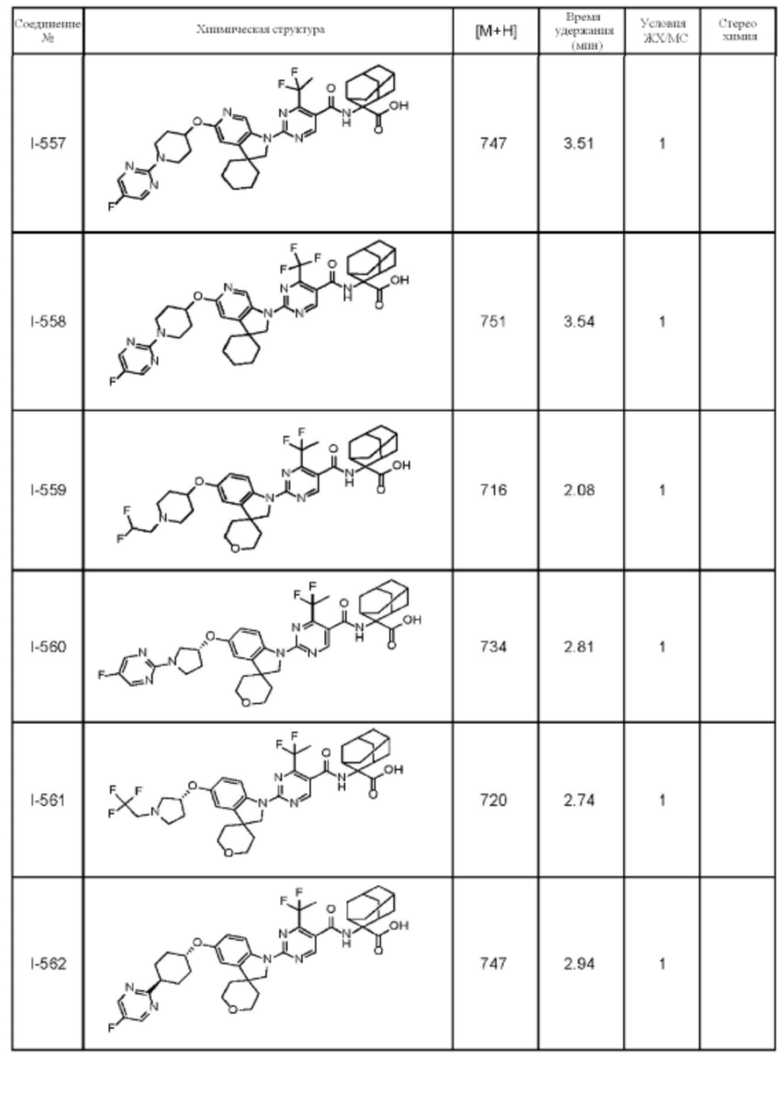
[0337]
[Таблица 98]
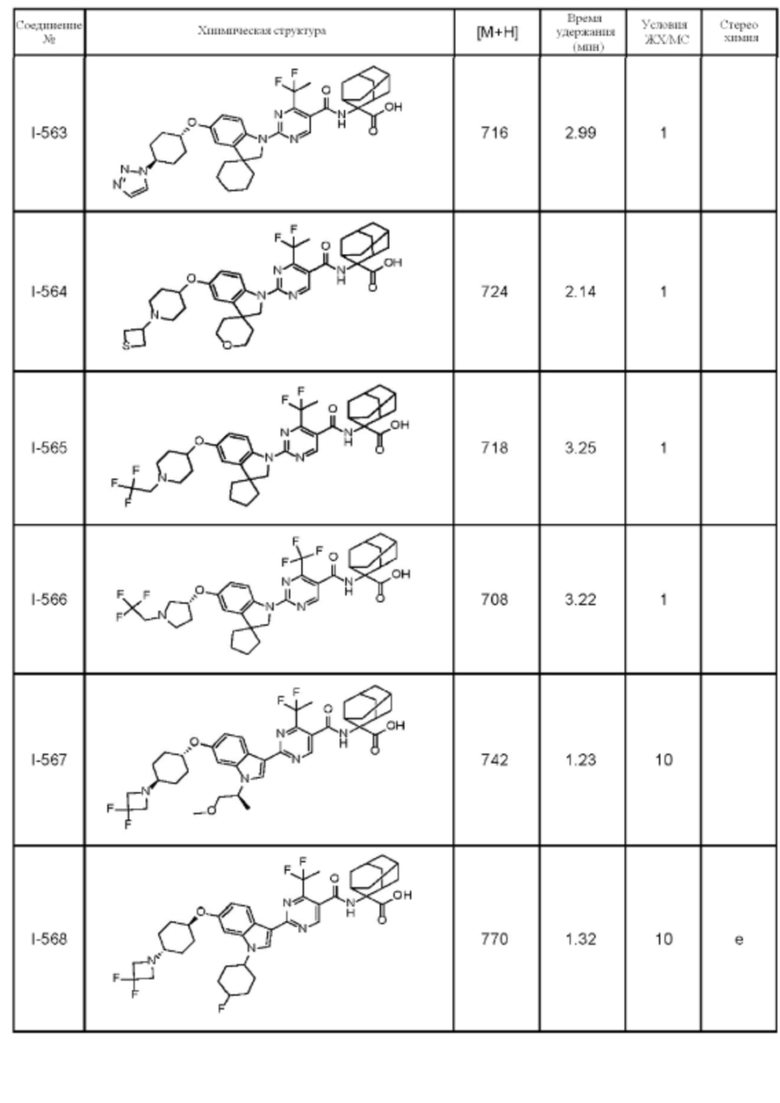
[0338]
[Таблица 99]
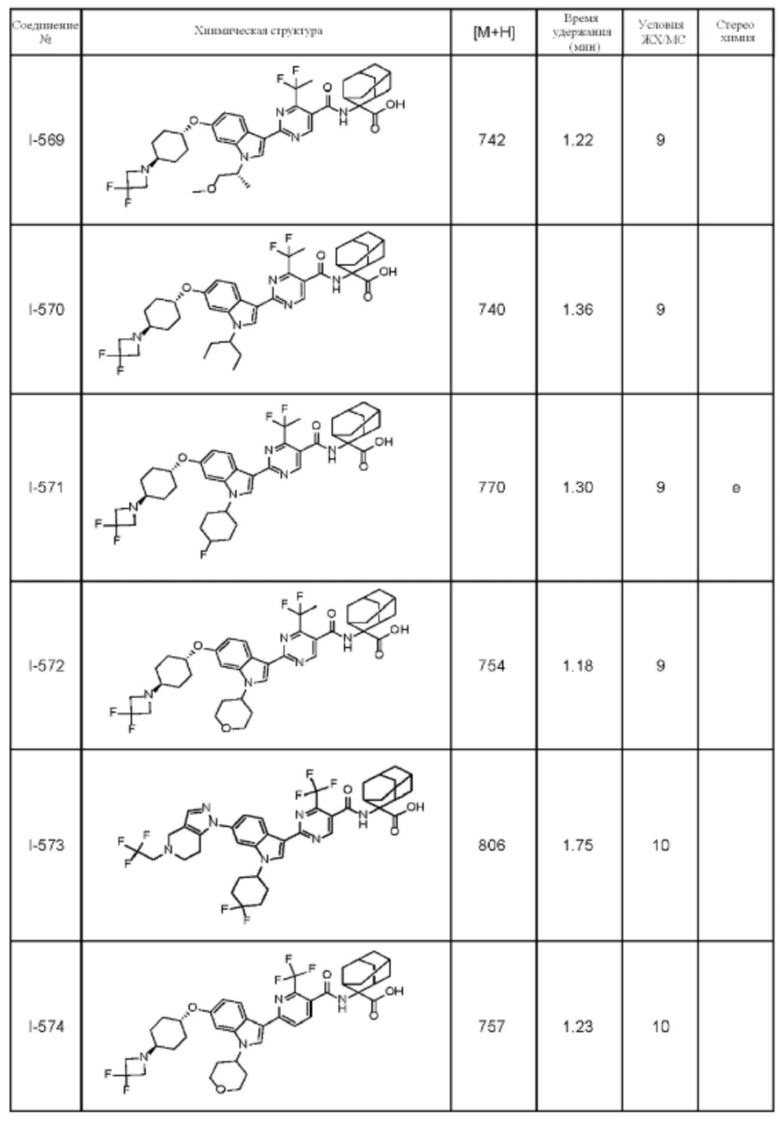
[0339]
[Таблица 100]
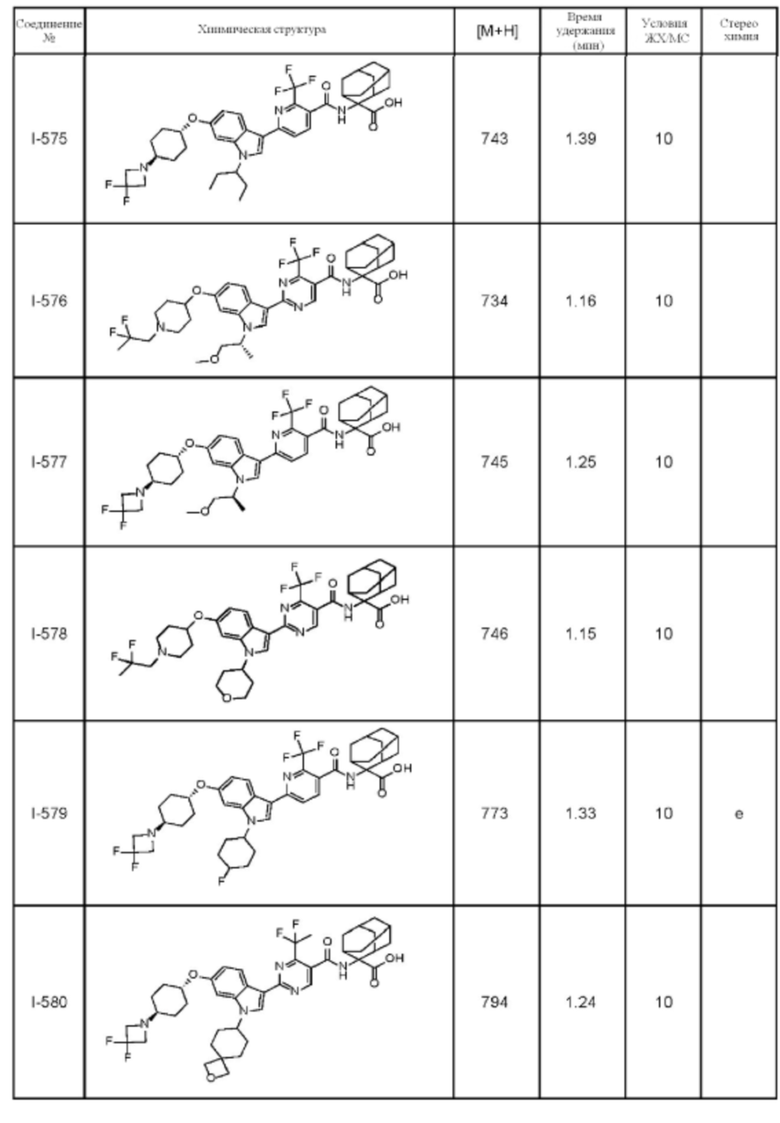
[0340]
[Таблица 101]
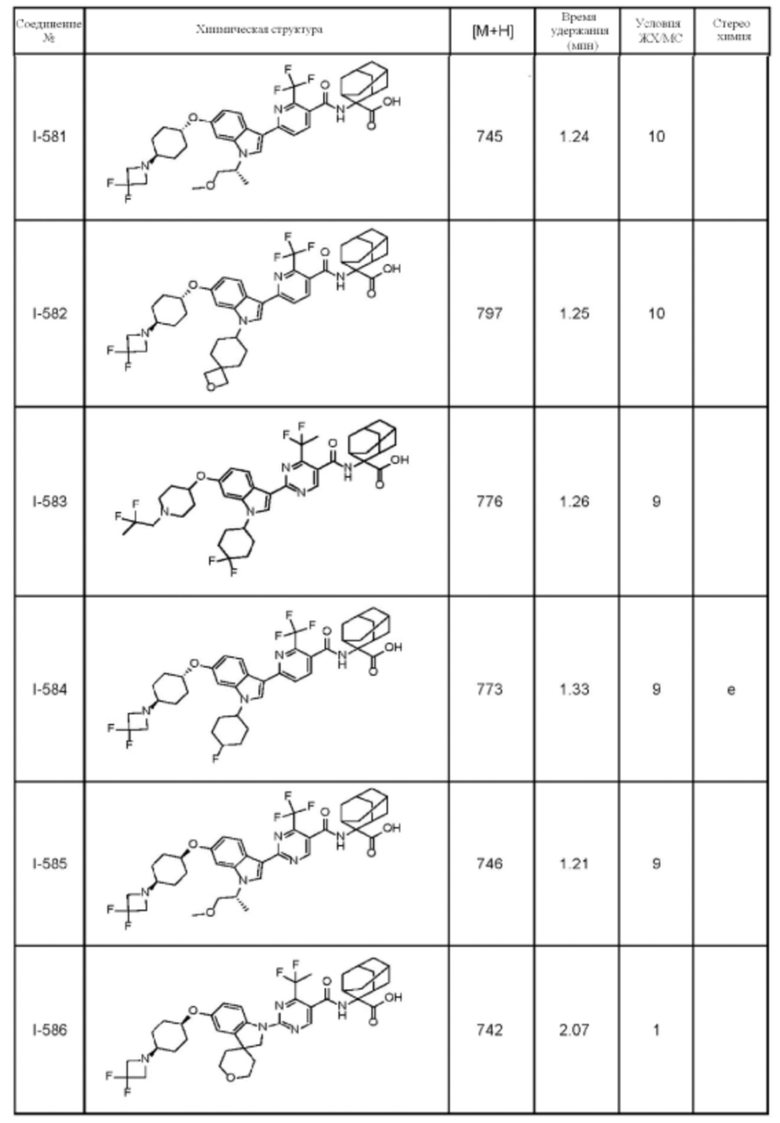
[0341]
[Таблица 102]
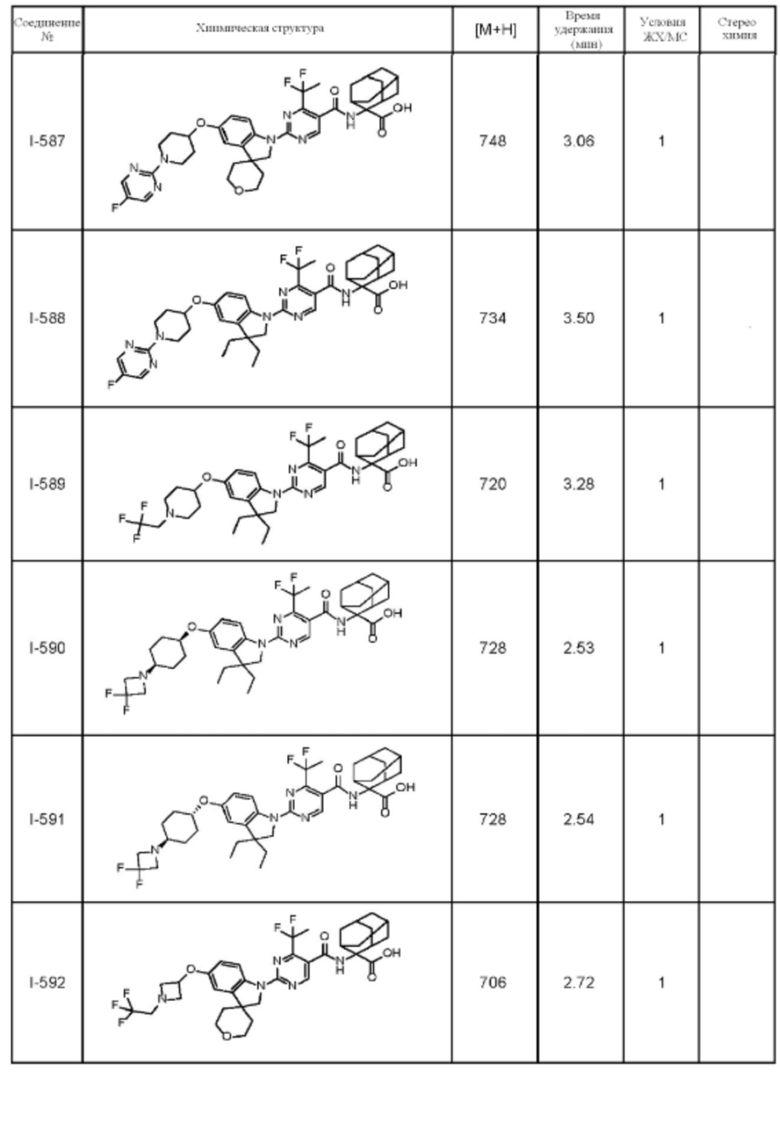
[0342]
[Таблица 103]
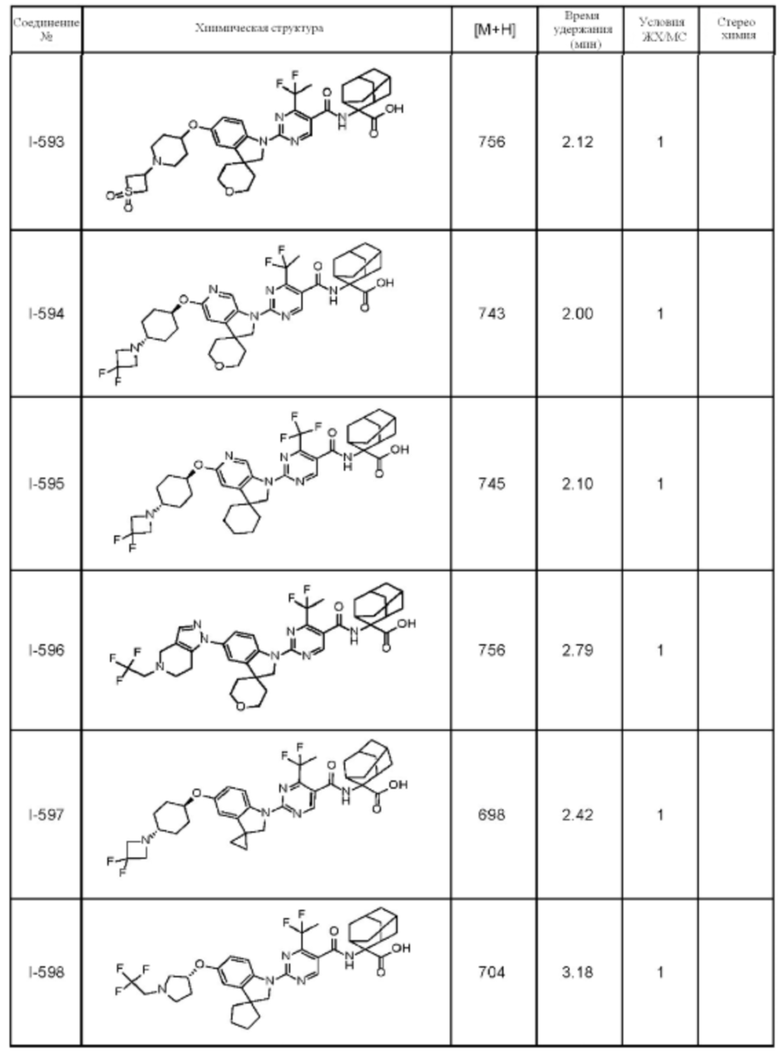
[0343]
[Таблица 104]
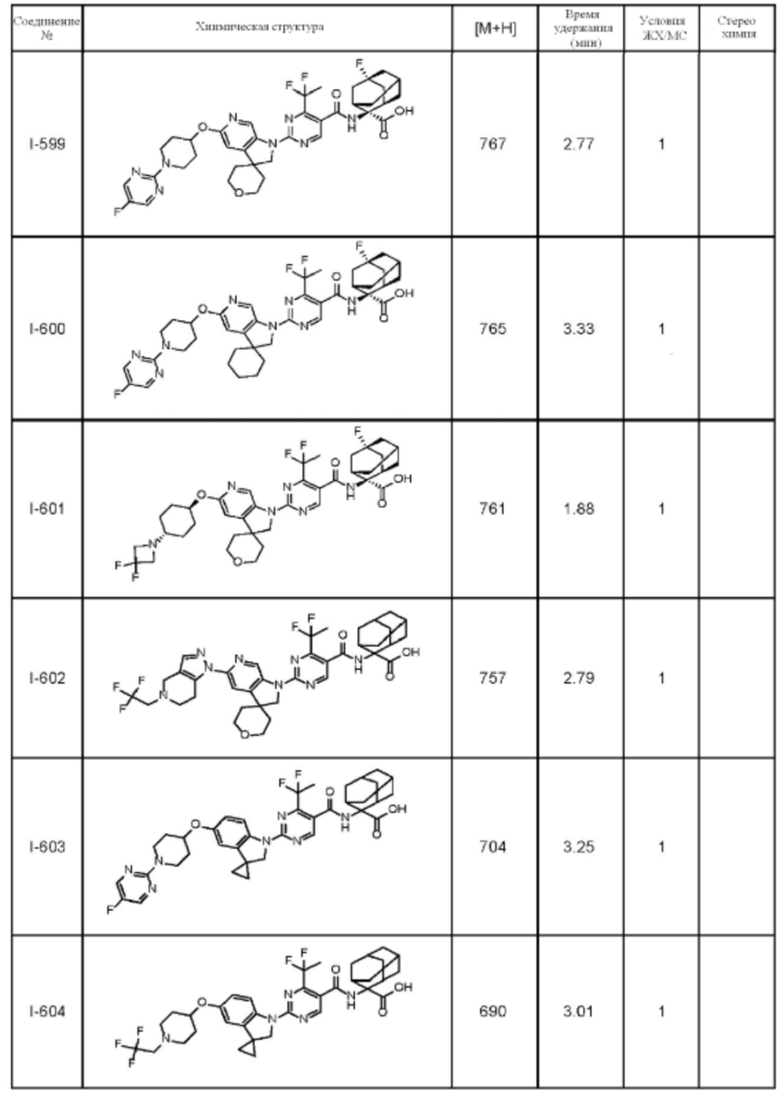
[0344]
[Таблица 105]
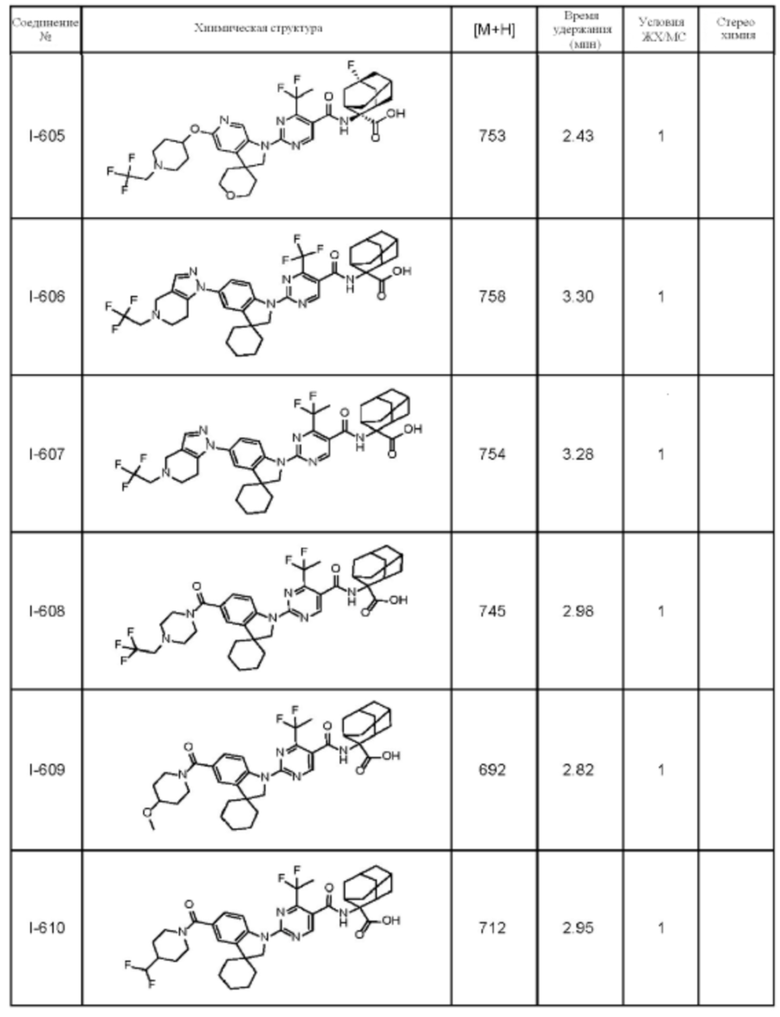
[0345]
[Таблица 106]
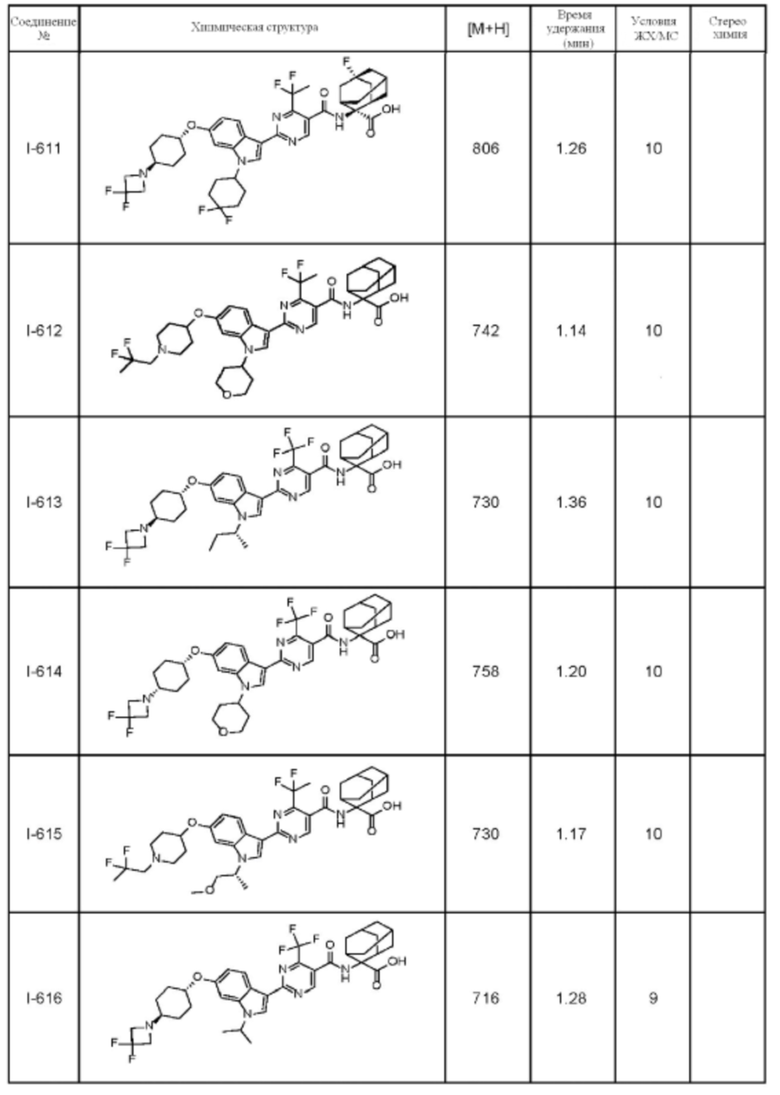
[0346]
[Таблица 107]
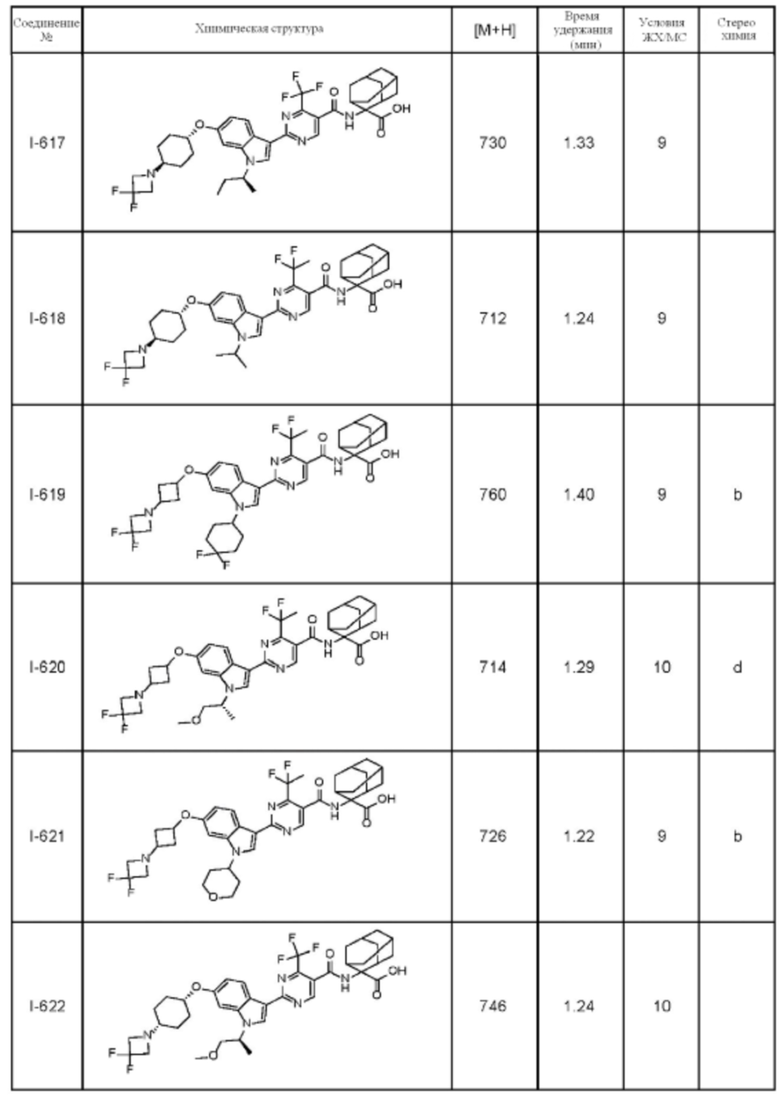
[0347]
Биологические Экспериментальные примеры для соединений по изобретению описаны ниже.
Соединение формулы (I) по настоящему изобретению оказывает ингибирующее действие на цитопатический эффект, вызываемый вирусом RS, и ингибирует цитопатический эффект у человека.
В частности, в способе оценки, описанном ниже, значение IC50 предпочтительно составляет 5000 нМ или менее, более предпочтительно, 1000 нМ или менее, и еще более предпочтительно, 100 нМ или менее.
[0348]
Экспериментальный пример 1: Испытание по оценке эффекта ингибирования CPE (CytoPathic Effect) in vitro
Исследуемый образец предварительно разводят ДМСО до соответствующей концентрации и готовят 3-кратные серии серийных разведений на 384-луночном планшете (0,32 мкл/лунку). Клетки HEp-2 (CCL-23; ATCC), доведенные до соответствующего количества (2,4×105 клеток/мл) в 2% FBS E-MEM (полученные путем добавления канамицина и FBS в питательную среду Игла; Invitrogen), добавляют по 12,5 мкл/лунку в 384-луночный планшет, предварительно аликвотированный с тестируемыми образцами. Штамм RSV A2 разводят до соответствующей концентрации в культуральной среде и добавляют в 384-луночный планшет, содержащий тестируемый образец, в количестве 12,5 мкл/лунку. Культуральную среду дополнительно добавляют в 384-луночный планшет и начинают тест с 50 мкл/лунку. Контрольные лунки готовят только на безвирусной культуральной среде. Планшет инкубируют в инкубаторе с 5% CO2 при 37°C в течение 4 дней, и затем помещают на 30 минут при комнатной температуре. Анализ CellTiter-Glo (зарегистрированная торговая марка) 2.0 (Promega) добавляют по 15 мкл/лунку, перемешивают в течение 30 секунд и помещают планшет приблизительно на 1 час. Затем люминесцентный сигнал измеряют с помощью EnVision (PerkinElmer). Ингибирующее действие тестируемых агентов на RSV-индуцированный СРЕ, рассчитывают как степень ингибирования 0% и 100% для каждой концентрации образца на основе уровня оставшихся жизнеспособных клеток с помощью CellTiter-Glo (зарегистрированная торговая марка) 2,0 со значением EC50 для каждого соединения, рассчитанным с помощью нелинейной регрессии как концентрация, которая ингибирует RSV-индуцированный СРЕ на 50%. В случае оценки против RSV типа B, RSV B (штамм Wash/18537) инфицируют таким же образом, как тип A, культивируют в течение 5 дней и количественно определяют таким же образом, как для штамма A2.
(Результат)
Соединения по изобретению тестируют в основном так, как описано выше. Ингибирующее действие соединений против RSV типа А показано ниже. Значения ЕС50 менее 10 нМ, 10 нМ или более и менее 100 нМ, и 100 нМ или более и 5000 нМ или менее обозначены как «А», «В» и «С», соответственно.
Соединение № I-23: 0,96 нМ
Соединение № I-33: 7,5 нМ
Соединение № I-82: 0,27 нМ
Соединение № I-148: 1,5 нМ
Соединение № I-159: 0,88 нМ
Соединение № I-162: 0,88 нМ
Соединение № I-165: 0,37 нМ
Соединение № I-182: 0,39 нМ
Соединение № I-228: 1,3 нМ
Соединение № I-268: 1,4 нМ
Соединение № I-269: 1,3 нМ
Соединение № I-270: 37 нМ
Соединение № I-486: 3 нМ
Соединение № I-570: 0,70 нМ
Соединение № I-591: 0,61 нМ
Соединение № I-594: 0,38 нМ
[0349]
[Таблица 108]
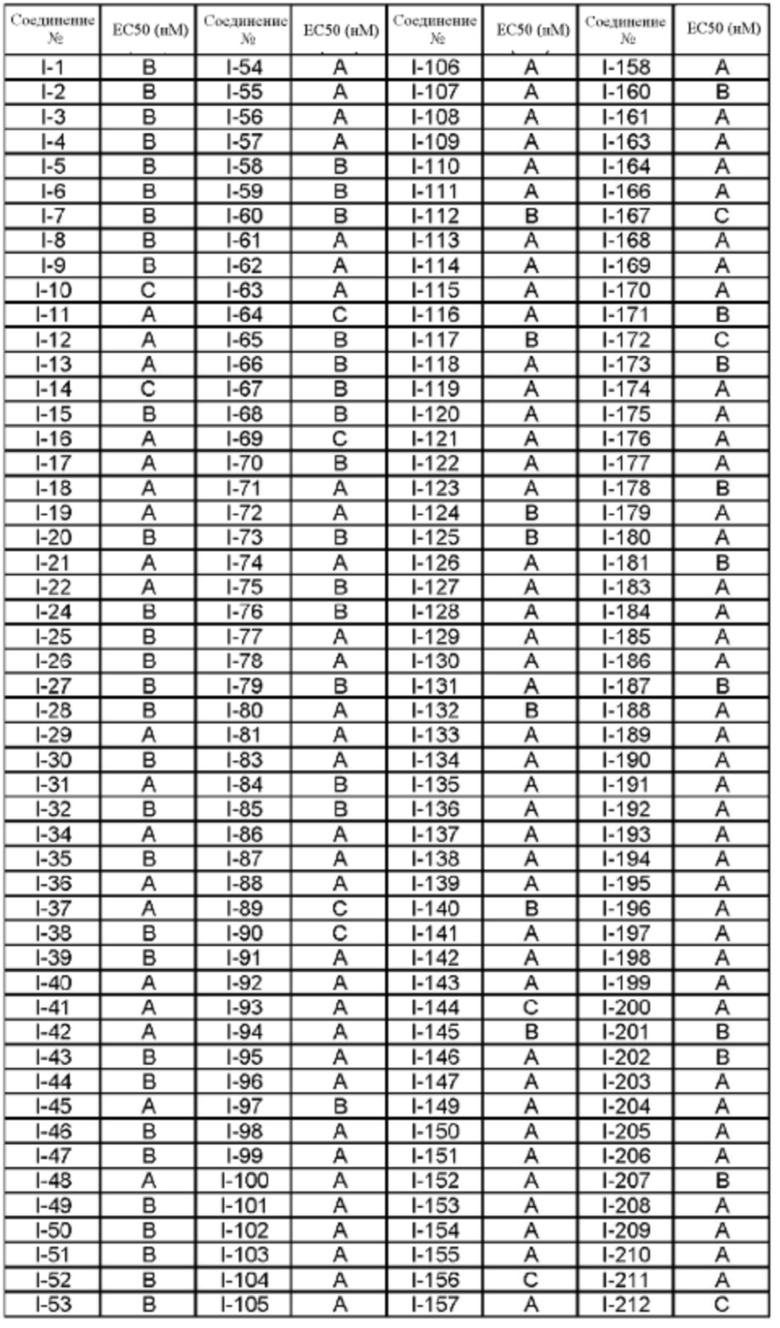
[0350]
[Таблица 109]
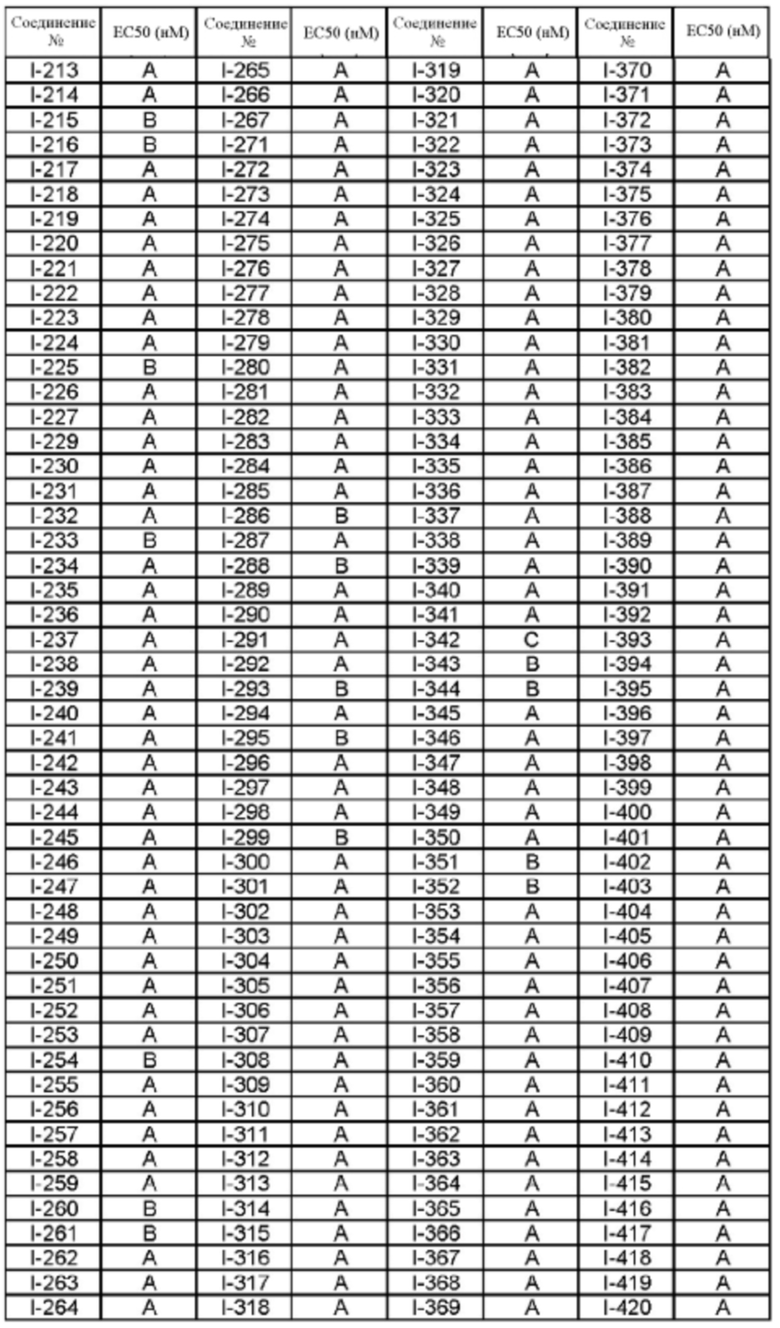
[0351]
[Таблица 110]
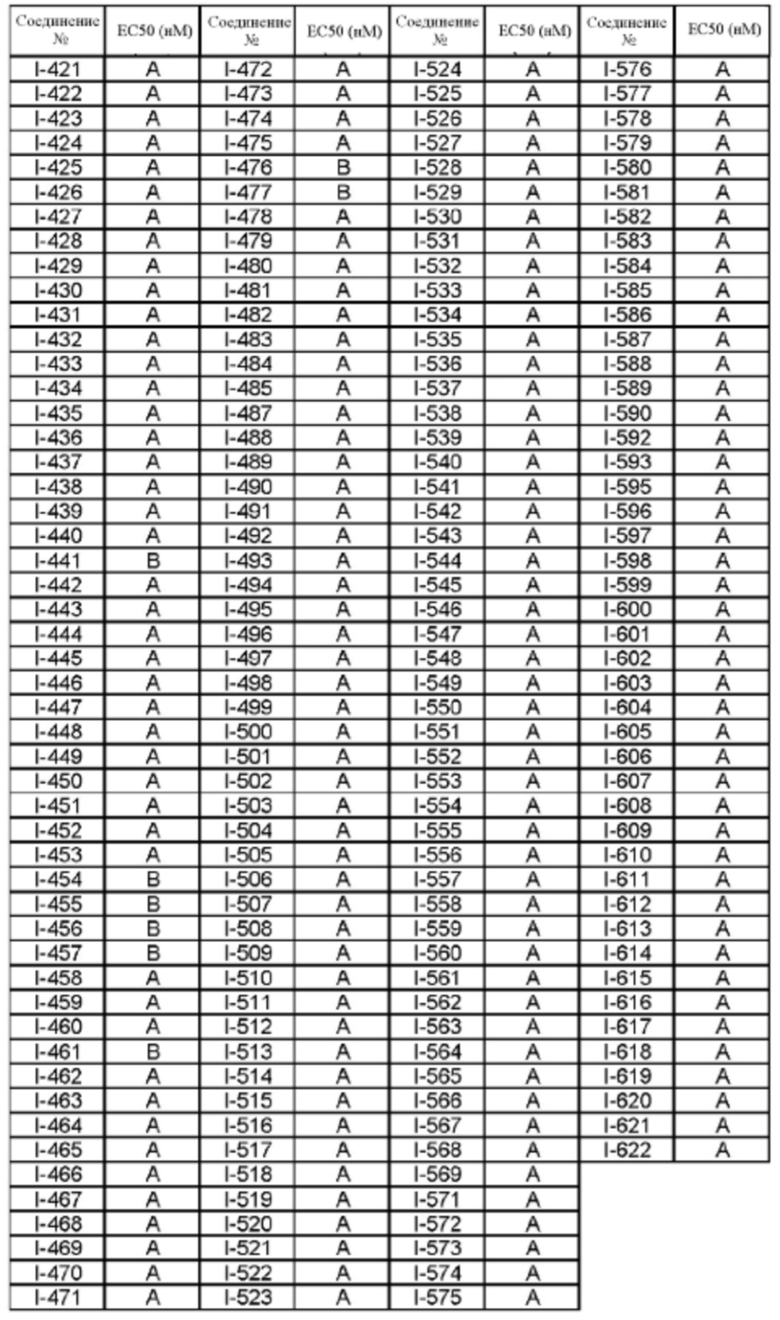
[0352]
Соединения по изобретению тестируют по существу как описано выше. Ингибирующее действие соединений против RSV типа B показано ниже. Значения EC50 менее 10 нМ, 10 нМ или более и менее 100 нМ, и 100 нМ или более и 5000 нМ или менее обозначены как «A», «B» и «C», соответственно.
Соединение № I-23: 16 нМ
Соединение № I-33: 110 нМ
Соединение № I-82: 0,34 нМ
Соединение № I-148: 2,8 нМ
Соединение № I-159: 3 нМ
Соединение № I-162: 3,3 нМ
Соединение № I-165: 0,62 нМ
Соединение № I-182: 2,1 нМ
Соединение № I-228: 36 нМ
Соединение № I-268: 4,3 нМ
Соединение № I-486: 28 нМ
Соединение № I-570: 2,1 нМ
Соединение № I-591: 2,2 нМ
Соединение № I-594: 4,2 нМ
[0353]
[Таблица 111]
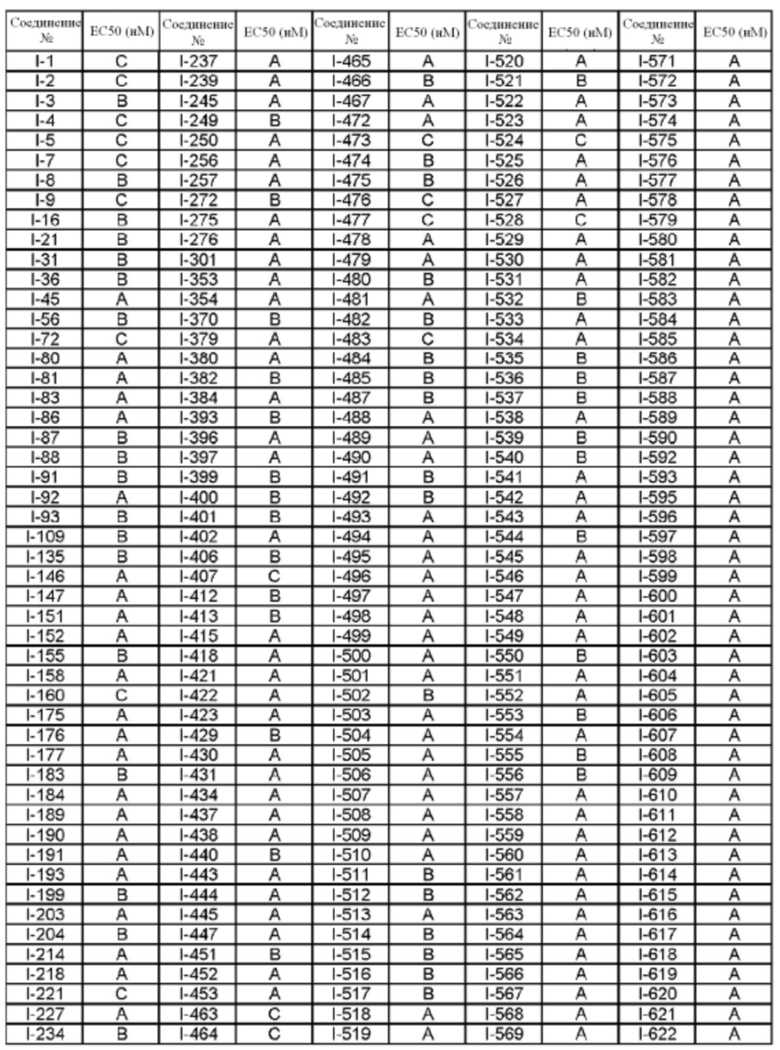
[0354]
Экспериментальный пример 2: Тестирование эффективности лекарственного средства на мышах in vivo
Хотя мыши являются полупермиссивными для репликации RSV человека, их часто используют в качестве модели в доклинических скрининговых тестах терапевтических агентов против RSV. Эффективность лекарственного средства in vivo оценивают с использованием мышей Balb/c, которые подходят для размножения штамма RSV A2. Мышей BALB/c (самки, возраст 6 недель) инокулируют интраназально штаммом RSV A2 в дозе 5х106 БОЕ/мышь. После инфицирования, тестируемый образец вводят в фиксированной дозе два раза в день (с интервалом 8 ч/16 ч), и легкое удаляют на 4 или 5 день. Легкое гомогенизируют в PBS, быстро замораживают и хранят при -80°C. Вирусные титры в супернатантах гомогенатов легких количественно определяют способом полуинфицирующей дозы культуры ткани (TCID50) с использованием иммуноблоттинга.
[0355]
Экспериментальный пример 3: Тестирование ингибирования CYP
Используя коммерчески доступные объединенные микросомы печени человека, а также, в качестве маркерных реакций пяти основных изоформ ферментов CYP человека (CYP1A2, 2C9, 2C19, 2D6, 3A4), О-деэтилирования 7-этоксирезоруфина (CYP1A2), метил-гидроксилирования толбутамида (CYP2C9), 4'-гидроксилирования мефенитоина (CYP2C19), О-деметилирования декстрометорфана (CYP2D6) и гидроксилирования терфенадина (CYP3A4), оценивают степень ингибирования продуцирования количества каждого метаболита соединением по настоящему изобретению.
[0356]
Условия реакции следующие: субстрат, 0,5 мкмоль/л этоксирезоруфина (CYP1A2), 100 мкмоль/л толбутамида (CYP2C9), 50 мкмоль/л S-мефенитоина (CYP2C19), 5 мкмоль/л декстрометорфана (CYP2D6), 1 мкмоль/л L-терфенадина (CYP3A4); время реакции 15 минут; температура реакции 37°С; фермент, объединенные микросомы печени человека 0,2 мг белка/мл; концентрации соединения по настоящему изобретению 1, 5, 10, 20 мкмоль/л (четыре точки).
[0357]
Каждые пять видов субстратов, микросомы печени человека или соединение по настоящему изобретению в 50 ммоль/л буфера Hepes добавляют в 96-луночный планшет в композиции, как описано выше, в качестве реакционного раствора, добавляют NADPH в качестве кофактора для инициации реакций метаболизма. После инкубации при 37°С в течение 15 минут, раствор метанол/ацетонитрил=1/1 (об./об.) добавляют для остановки реакции. После центрифугирования при 3000 об/мин в течение 15 минут, резоруфин (метаболит CYP1A2) в супернатанте определяют количественно с помощью флуоресцентного многоканального ридера или ЖХ/МС/МС, и гидрокситолбутамид (метаболит CYP2C9), 4'-гидроксимефенитоин (метаболит CYP2C19), декстрорфан (метаболит CYP2D6) и метаболит терфенадинового спирта (метаболит CYP3A4) количественно определяют с помощью ЖХ/МС/МС.
Концентрацию разведения и растворитель для разведения меняют по мере необходимости.
[0358]
Добавление только ДМСО, являющегося растворителем, растворяющим соединение по настоящему изобретению, в реакционную систему принимают в качестве контроля (100%), остаточную активность (%) рассчитывают для каждой концентрации соединения по настоящему изобретению, добавленного в виде раствора, и IC50 рассчитывают путем обратной презумпции с помощью логистической модели с использованием концентрации и скорости ингибирования.
[0359]
Экспериментальный пример 4: Тест CYP3A4 (MDZ) MBI
Тест CYP3A4 (MDZ) MBI представляет собой тест исследования потенциала суицидного ингибирования (MBI) на ингибирование CYP3A4 соединением. Ингибирование CYP3A4 оценивают с использованием реакции 1-гидроксилирования мидазолама (MDZ) объединенными микросомами печени человека в качестве маркерной реакции.
[0360]
Условия реакции следующие: субстрат, 10 мкмоль/л MDZ; время предварительной реакции, 0 или 30 минут; время реакции субстрата 2 минуты; температура реакции 37°С; содержание белка в объединенных микросомах печени человека до реакции 0,5 мг/мл, во время реакции 0,05 мг/мл (при 10-кратном разведении); концентрации соединения по настоящему изобретению во время предварительной реакции 1, 5, 10, 20 мкмоль/л или 0,83, 5, 10, 20 мкмоль/л (четыре точки).
[0361]
Объединенные микросомы печени человека и раствор соединения по настоящему изобретению в буфере K-Pi (рН 7,4) в качестве раствора для предварительной реакции добавляют в 96-луночный планшет в композиции для предварительной реакции. Часть раствора предварительной реакции переносят в другой 96-луночный планшет и разводят 10-кратно буфером K-Pi, содержащим субстрат. Добавляют NADPH в качестве кофактора для инициации маркерной реакции (предварительная инкубация 0 мин). По истечении заданного времени реакции, добавляют раствор метанол/ацетонитрил=1/1 (об./об.) для остановки реакции. С другой стороны, NADPH также добавляют к оставшемуся раствору предварительной реакции, чтобы инициировать предварительную реакцию (предварительная инкубация 30 мин). По истечении заданного времени предварительной реакции, часть переносят в другой 96-луночный планшет и 10-кратно разводят субстратом в буфере K-Pi, содержащем субстрат, для инициации маркерной реакции. По истечении заданного времени реакции, раствор метанол/ацетонитрил=1/1 (об./об.) добавляют для остановки реакции. После центрифугирования при 3000 об/мин в течение 15 минут, 1-гидроксимидазолам в супернатанте количественно определяют с помощью ЖХ/МС/МС.
Концентрацию и растворитель для разведения меняют по мере необходимости.
[0362]
Образец с добавлением ДМСО в реакционную систему вместо раствора соединения по настоящему изобретению принимают в качестве контроля (100%), так как ДМСО используют в качестве растворителя для растворения соединения по настоящему изобретению. Оставшуюся активность (%) рассчитывают при каждой концентрации соединения по настоящему изобретению по сравнению с контролем, и значение IC рассчитывают путем обратной презумпции с помощью логистической модели с использованием концентрации и степени ингибирования. IC при предварительной инкубации 0 мин/IC при предварительной инкубации 30 мин определяют как значение сдвинутой IC, и случай, когда сдвинутая IC составляет 1,5 или более, считается положительным, и случай, когда сдвинутая IC составляет 1,0 или менее, считается отрицательным.
[0363]
Экспериментальный пример 5: Тест BA
Материалы и способы для экспериментов по оценке перорального всасывания
(1) Животные: используют мышей или крыс.
(2) Условия разведения: мышам или крысам разрешают свободно принимать твердую пищу и стерилизованную водопроводную воду.
(3) Уставка дозы и деление на группы: пероральное введение и внутривенное введение осуществляют с заранее определенной дозировкой. Группы устанавливают как показано ниже (дозировка изменена для каждого соединения):
Пероральное введение: от 2 до 60 мкмоль/кг или от 1 до 30 мг/кг (n=от 2 до 3)
Внутривенное введение: от 1 до 30 мкмоль/кг или от 0,5 до 10 мг/кг (n=2 или 3)
(4) Приготовление дозированного состава: пероральное введение осуществляют в форме суспензии или раствора. Внутривенное введение осуществляют после солюбилизации.
(5) Пути введения: пероральное введение в желудок осуществляют через зонд для кормления. Внутривенное введение в хвостовую вену осуществляют с помощью шприца, оснащенного инъекционной иглой.
(6) Элементы оценки: кровь собирают с течением времени и измеряют концентрацию соединения по изобретению в плазме с помощью ЖХ/МС/МС.
(7) Статистический анализ: что касается профиля концентрации в плазме соединения по изобретению, площадь под кривой зависимости концентрации от времени (AUC) рассчитывают способом моментного анализа, и рассчитывают биодоступность (BA) соединения по изобретению из соотношения доз и отношения AUC в группе перорального введения и в группе внутривенного введения.
При необходимости следует изменить концентрацию разведения и растворитель для разведения.
Экспериментальный пример 6: Тест оценки клиренса
Материал и способ
(1) Животное: используют крыс SD.
(2) Условия разведения: крысам разрешают свободно принимать твердую пищу и стерилизованную водопроводную воду.
(3) Дозировка и деление на группы: внутривенное введение осуществляют в заранее определенной дозе. Деление на группы проводят следующим образом:
Внутривенное введение: 1 мкмоль/кг (n=2)
(4) Приготовление дозированного состава: Исследуемый образец солюбилизируют, используя растворитель диметилсульфоксид/пропиленгликоль=1/1, и вводят.
(5) Путь введения: введение в хвостовую вену осуществляют с помощью шприца, оснащенного инъекционной иглой.
(6) Элементы оценки. Кровь собирают с течением времени и измеряют концентрацию соединения по изобретению в плазме с помощью ЖХ/МС/МС.
(7) Статистический анализ: относительно профиля концентрации соединения в плазме, общий клиренс организма (CLtot) рассчитывают способом моментального анализа. При необходимости следует изменить концентрацию разведения и растворитель для разведения.
Экспериментальный пример 7: Тест на метаболическую стабильность
Используя объединенные микросомы печени человека и объединенные микросомы печени крысы, соединение по настоящему изобретению подвергают реакции в течение постоянного времени, и оставшуюся скорость рассчитывают путем сравнения прореагировавшего образца и непрореагировавшего образца, тем самым оценивая степень метаболизма в печени.
Реакцию проводят (окислительная реакция) при 37°С в течение 0 или 30 минут в присутствии 1 ммоль/л NADPH в 0,2 мл буфера (50 ммоль/л Tris-HCl pH 7,4, 150 ммоль/л хлорида калия, 10 ммоль/л хлорида магния), содержащего 0,5 мг белка/мл микросом печени человека или крысы. После реакции, 50 мкл реакционного раствора добавляют к 100 мкл раствора метанол/ацетонитрил=1/1 (об/об), перемешивают и центрифугируют при 3000 об/мин в течение 15 минут. Соединение по изобретению в центрифугированном супернатанте определяют количественно с помощью ЖХ/МС/МС или твердофазной экстракции (ТФЭ)/МС. Количество соединения по изобретению, остающееся после реакции, рассчитывают по количеству соединения в 0 минут реакции, определенному как 100%. Реакцию гидролиза проводят в отсутствие NADPH, и реакцию глюкуронирования проводят в присутствии 5 ммоль/л UDP-глюкуроновой кислоты вместо NADPH с последующими аналогичными процедурами. При необходимости изменяют концентрации разведения и растворители для разведения.
Экспериментальный пример 8: Тест на метаболическую стабильность (гепатоциты)
Используя гепатоциты человека, крысы, собаки или обезьяны, соединение по изобретению подвергают реакции в течение постоянного времени, и оставшуюся скорость рассчитывают путем сравнения прореагировавшего образца и непрореагировавшего образца, тем самым оценивая степень метаболизма в печени. Чтобы учесть влияние связывания белков сыворотки на метаболизм, в среду можно добавлять до 10% сыворотки видов, соответствующих каждому гепатоциту.
Гепатоцит человека, крысы, собаки или обезьяны суспендируют в среде Вильяма Е при 1х106 клеток/мл и подвергают реакции с соединением по изобретению при 37°С в течение 0, 1 или 2 часов. При добавлении сыворотки, до 10% сыворотки добавляют в среду Вильяма Е заранее, и затем гепатоциты суспендируют. После реакции, добавляют 120 мкл раствора метанол/ацетонитрил=1/1 (об./об.) к 30 мкл реакционного раствора, смешивают и центрифугируют при 3000 об/мин в течение 15 минут. Соединение по изобретению в центрифугированном супернатанте определяют количественно с помощью ЖХ/МС/МС или твердофазной экстракции (ТФЭ)/МС. Количество соединения по изобретению, остающееся после реакции, рассчитывают по количеству соединения в 0 минут реакции, определенному как 100%. При необходимости изменяют концентрации разведения и растворители для разведения.
Промышленная применимость
Соединение по изобретению оказывает ингибирующее действие на RSV и может быть использовано для лечения и/или профилактики инфекции RSV и родственных заболеваний, вызванных инфекцией.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЗОТСОДЕРЖАЩИЕ ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ ВИЧ | 2016 |
|
RU2720145C2 |
| 6-ЧЛЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2016 |
|
RU2683245C1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА ИЛИ ИМИДАЗОПИРИДИНА, ПОЛЕЗНЫЕ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ БОЛЕЗНЕЙ, АССОЦИИРОВАННЫХ С АСС2 | 2016 |
|
RU2702637C2 |
| БИЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ И ВКЛЮЧАЮЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2017 |
|
RU2753524C2 |
| С17-, С20- И С21-ЗАМЕЩЕННЫЕ НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2828261C2 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ГРИППА, ХАРАКТЕРИЗУЮЩИЙСЯ ТЕМ, ЧТО В НЕМ ОБЪЕДИНЕНЫ ИНГИБИТОР КЭП-ЗАВИСИМОЙ ЭНДОНУКЛЕАЗЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО ПРОТИВ ГРИППА | 2016 |
|
RU2745071C2 |
| ЗАМЕЩЕННЫЕ ПОЛИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ПИРИДОНА И ИХ ПРОЛЕКАРСТВА | 2016 |
|
RU2712275C2 |
| ПРОИЗВОДНОЕ ДИГИДРОПИРАЗОЛОПИРАЗИНОНА, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ MGAT-2 | 2020 |
|
RU2803743C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, ЗАМЕЩЕННЫЕ В ПОЛОЖЕНИИ 10 ЦИКЛИЧЕСКОЙ ГРУППОЙ, ДЛЯ ИСПОЛЬЗОВАНИЯ ПРИ ЛЕЧЕНИИ РАССТРОЙСТВ ЦНС | 2019 |
|
RU2796006C2 |
| ПРОТИВОВИРУСНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2552533C2 |
Группа изобретений относится к области химии и фармацевтики, а именно раскрывается соединение формулы (I) или его фармацевтически приемлемая соль фармацевтическая композиция на их основе, обладающие активностью против респираторно-синцитиального вируса (вируса RS). В общей формуле (I) пунктирная линия показывает присутствие или отсутствие связи; R1 представляет собой карбокси, тетразолил или оксадиазолинил; L представляет собой замещенный или незамещенный 3-20-членный неароматический карбоциклилдиил, включающий одно кольцо или два или более колец, где замещающая группа выбрана из C1-С6 алкила; гидрокси; циано; C1-С6 алкилокси и галогена; замещенный или незамещенный 5- или 6-членный неароматический гетероциклилдиил, включающий один или два атома кислорода или атома азота, где замещающая группа выбрана из C1-С6 алкиклоксикарбонила; или замещенный или незамещенный C1-С6 алкилен, где замещающая группа выбрана из C1-С6 алкила и С3-С6 членного неароматического карбоциклила; R2 представляет собой замещенный или незамещенный C1-С6 алкил, где замещающая группа выбрана из галогена и гидрокси; R3 представляет собой атом водорода; замещенный или незамещенный C1-С6 алкил, где замещающая группа выбрана из амино, C1-С6 алкиламино, гидрокси и галогена; незамещенный С1-С6 алкилокси; или замещенный или незамещенный амино, где замещающая группа выбрана из C1-С6 алкила; V представляет собой -CRV= или -N=; W представляет собой =CRW- или =N-; 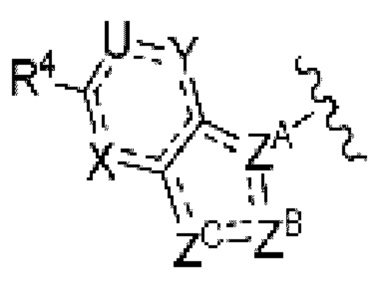 представляет собой структуры, указанные ниже. Остальные значения радикалов указаны в формуле изобретения. 2 н. и 18 з.п. ф-лы, 111 табл., 23 пр.
представляет собой структуры, указанные ниже. Остальные значения радикалов указаны в формуле изобретения. 2 н. и 18 з.п. ф-лы, 111 табл., 23 пр.
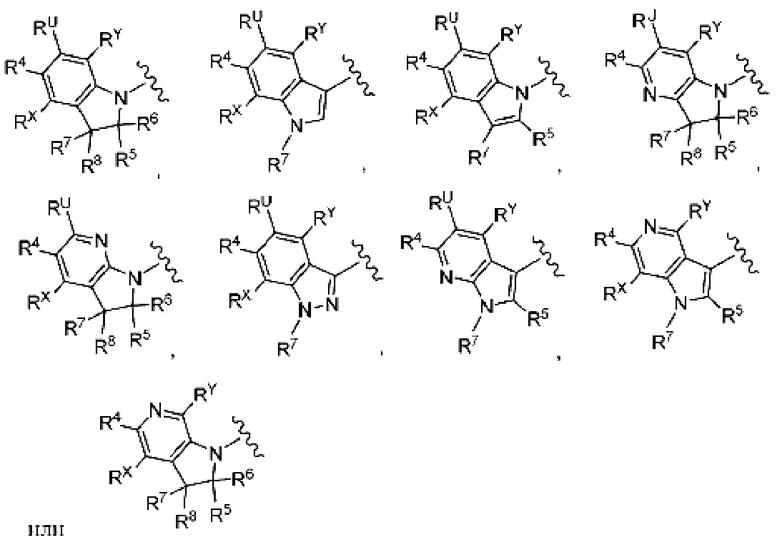
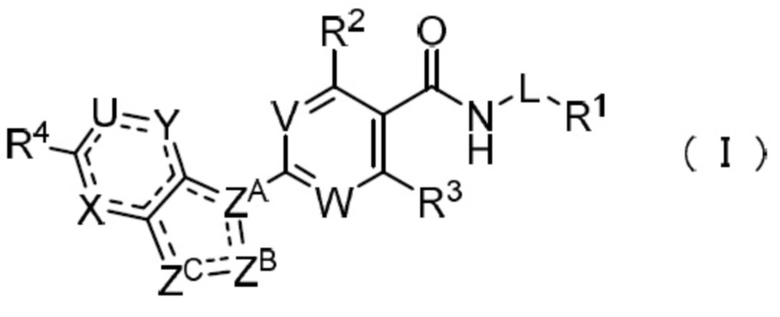
1. Соединение формулы (I):
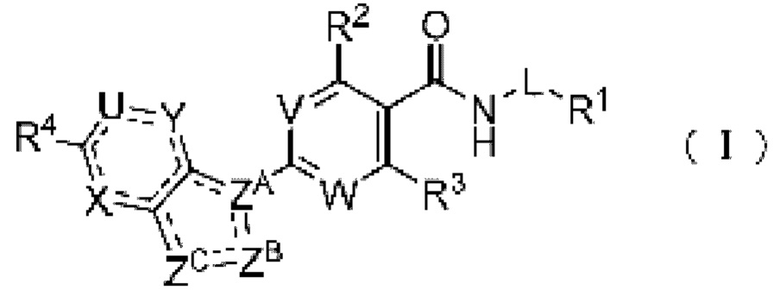
где:
пунктирная линия показывает присутствие или отсутствие связи;
R1 представляет собой карбокси, тетразолил или оксадиазолинил;
L представляет собой замещенный или незамещенный 3-20-членный неароматический карбоциклилдиил, включающий одно кольцо или два или более колец, где замещающая группа выбрана из C1-С6 алкила; гидрокси; циано; C1-С6 алкилокси и галогена;
замещенный или незамещенный 5- или 6-членный неароматический гетероциклилдиил, включающий один или два атома кислорода или атома азота, где замещающая группа выбрана из C1-С6 алкиклоксикарбонила; или
замещенный или незамещенный C1-С6 алкилен, где замещающая группа выбрана из C1-С6 алкила и С3-С6 членного неароматического карбоциклила;
R2 представляет собой замещенный или незамещенный C1-С6 алкил, где замещающая группа выбрана из галогена и гидрокси;
R3 представляет собой атом водорода; замещенный или незамещенный C1-С6 алкил, где замещающая группа выбрана из амино, C1-С6 алкиламино, гидрокси и галогена; незамещенный С1-С6 алкилокси; или замещенный или незамещенный амино, где замещающая группа выбрана из C1-С6 алкила;
V представляет собой -CRV= или -N=;
W представляет собой =CRW- или =N-;
RV и RW каждый независимо представляет собой атом водорода, циано или незамещенный карбамоил; группа формулы:
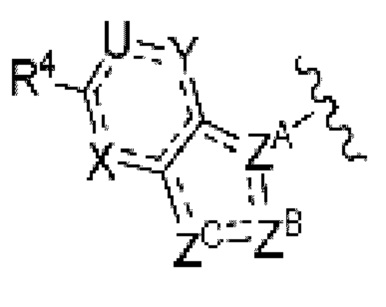
представляет собой
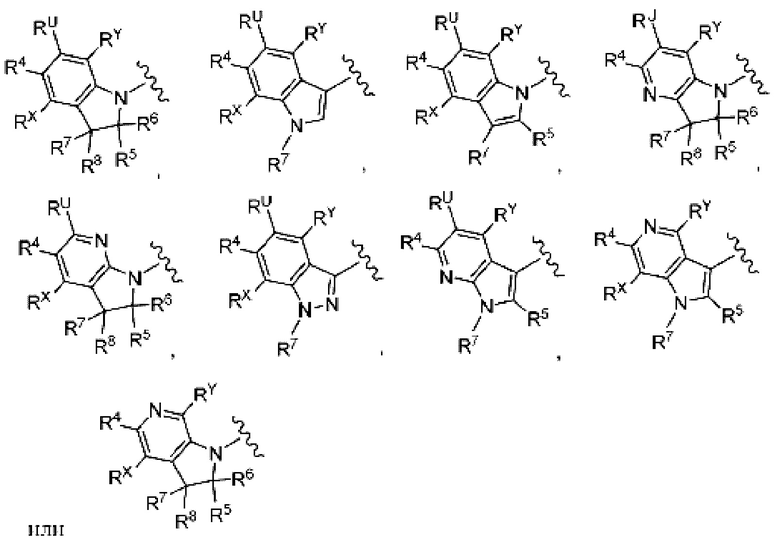
где RX и RY каждый независимо представляет собой атом водорода, галоген или незамещенный C1-С6 алкил;
RU представляет собой атом водорода; незамещенный C1-С6 алкилокси;
замещенный или незамещенный 6-членный неароматический гетероциклилокси, включающий один атом азота, где замещающая группа выбрана из 3-6-членного неароматического гетероциклила, включающего один атом кислорода;
замещенный или незамещенный 6-членный неароматический карбоциклилокси, где замещающая группа выбрана из 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; или
галоген;
R5 и R6 каждый независимо представляет собой атом водорода; или незамещенный 6-членный неароматический гетероциклил, включающий один атом кислорода;
или R5 и R6 взяты вместе с образованием оксо;
R7 и R8 каждый независимо представляет собой атом водорода;
замещенный или незамещенный С1-С6 алкил, где замещающая группа выбрана из С1-С6 алкилокси, галогена, гидрокси, 6-членного ароматического карбоциклила, 3-6-членного неароматического карбоциклила, 3-6-членного неароматического карбоциклила, замещенного галогеном, 3-6-членного неароматического гетероциклилкарбонила, включающего один атом азота и один атом кислорода, и 3-6-членного неароматического гетероциклила, включающего один атом кислорода;
замещенный или незамещенный 3-6-членный неароматический карбоциклил, где замещающая группа выбрана из галогена, циано, 6-членного ароматического карбоциклил-С1-С6-алкилокси, гидрокси, С1-С6 алкиклокси, С1-С6 алкила, С1-С6 алкила, замещенного галогеном;
замещенный или незамещенный 3-6-членный неароматический гетероциклил, включающий один атом кислорода, один атом серы или один атом азота, где замещающая группа выбрана из оксо или С1-С6 алкила, замещенного галогеном;
замещенный или незамещенный 6-членный ароматический карбоциклил, где замещающая группа выбрана из галогена, С1-С6 алкила, С1-С6 алкила, замещенного галогеном, С1-С6 алкилокси и циано;
замещенный или незамещенный 5- или 6-членный ароматический гетероциклил, включающий один или два атома азота, где замещающая группа выбрана из С1-С6 алкила, С1-С6 алкила, замещенного галогеном, галогена, С1-С6 алкилокси, гидрокси и циано;
незамещенный 3-6-членный неароматический карбоциклилоксикарбонил;
незамещенный 3-6-членный неароматический гетероциклилоксикарбонил, включающий один атом кислорода; или
незамещенный 3-6-членный неароматический карбоциклилсульфонил;
или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного 3-6-членного неароматического углеродного кольца, где замещающая группа выбрана из галогена;
замещенного или незамещенного 5- или 6-членного неароматического гетероциклического кольца, включающего один атом азота или один атом серы, где замещающая группа выбрана из С1-С6 алкила, С1-С6 алкила, замещенного галогеном, С1-С6 алкилкарбонила, С1-С6 алкилоксикарбонила, 3-6-членного неароматического гетероциклила, включающего один атом кислорода, С1-С6 алкилкарбамоила, 3-6-членного неароматического
карбоциклила, 5- или 6-членного ароматического гетероциклила, включающего два атома азота, 5- или 6-членного ароматического гетероциклила, включающего два атома азота, замещенного галогеном, 6-членного ароматического карбоциклил-С1-С6-алкилоксикарбонила и оксо; или
R5 и R7 взяты вместе с атомом углерода, к которому они присоединены, с образованием незамещенного 3-8-членного неароматического углеродного кольца или незамещенного 6-членного ароматического углеродного кольца; или
R4 представляет собой:
атом водорода;
замещенный или незамещенный C1-С6 алкилокси, где замещающая группа выбрана из С1-С6 алкилокси; циано; галогена; гидрокси; С1-С6 алкилкарбонилокси; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота, замещенного галоген-С1-С6 алкилом; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота; 3-6-членного неароматического гетероциклила, включающего два атома азота, замещенного С1-С6 алкилом; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенный галогеном; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота и атома серы, замещенного С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один атом азота, замещенного С1-С6 алкилокси; 5- или 6-членного ароматического гетероциклила, включающего два атома азота; и амино, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота;
замещенный или незамещенный 3-10-членный неароматический гетероциклилокси, включающий один, два или три атома, выбранных из атома кислорода, атома азота и атома серы, где замещающая группа выбрана из С1-С6 алкила; C1-С6 алкила, замещенного галогеном; С1-С6 алкила, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота, замещенным C1-С6 алкилом; С1-С6 алкила, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом кислорода; С1-С6 алкила, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом кислорода, замещенным галогеном; С1-С6 алкила, замещенного 3-6-членным неароматическим карбоциклилом, замещенным галогеном; C1-С6 алкила, замещенного С1-С6 алкилсульфонилом; С1-С6 алкила, замещенного С1-С6 алкокси; С1-С6 алкила, замещенного циано; С1-С6 алкилкарбонила; С1-С6 алкилоксикарбонила; C1-С6 алкилоксикарбонила, замещенного 6-членным ароматическим карбоциклилом; С1-С6 алкилкарбамоила; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома азота и атома серы, замещенного оксо; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного C1-С6 алкилкарьбонилом; 3-6-членного неароматического гетероциклилкарбонила, включающего один атом кислорода; 5- или 6-членного ароматического гетероциклила, включающего один или два атома, выбранных из атома азота и атома серы; 5- или 6-членного ароматического гетероциклилкарбонила, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота, атома кислорода и атома серы, замещенного С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота, атома кислорода и атома серы, замещенного галоген-С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного С1-С6 алкилокси; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного циано; 3-6-членного неароматического карбоциклила; 3-6-членного неароматического карбоциклила, замещенного галогеном; 3-6-членного неароматического карбоциклилкарбонила; 3-6-членного неароматического карбоциклилкарбонила; 3-6-членного неароматического карбоциклилсульфонила; оксо; и галогена;
замещенный или незамещенный 3-10-членный неароматический карбоциклилокси, где замещающая группа выбрана из 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; С1-С6 алкилсульфонила; С1-С6 алкилокси; 3-6-членного неароматического гетероциклила, включающего один атом кислорода и один атом азота; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного галогеном; 3-6-членного неароматического карбоциклилиминокси, замещенного галогеном; 3-6-членного неароматического карбоциклилоксиимино, замещенного галогеном; 3-6-членного неароматического гетероциклил-С1-С6 алкила, включающего один атом азота, замещенного галогеном; С1-С6 алкила; С1-С6 алкила, замещенного галогеном; галогена; амино, замещенного галоген-С1-С6 алкилом; амино, замещенного C1-С6 алкилом; 5- или 6-членного ароматического гетероциклиламино, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома азота; и 3-6-членного неароматического карбоциклилокси;
незамещенный 6-членный ароматический карбоциклилокси; замещенный или незамещенный C1-С6 алкил; где замещающая группа выбрана из галогена; 3-10-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила включающего один или два атома азота, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота; 3-10-членного неароматического гетероциклила, включающего три атомами азота, замещенного С1-С6 алкилом; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом азота, где указанный гетероциклил замещен галогеном; 6-членного ароматического карбоциклила; 6-членного ароматического карбоциклила, замещенного C1-С6 алкилокси; и 3-6-членного неароматического карбоциклилоксиимино, замещенного галогеном;
замещенный или незамещенный С2-С6 алкенил, где замещающая группа выбрана из 6-членного ароматического карбоциклила, замещенного С1-С6 алкилокси; и 3-6-членного неароматического гетероциклила, включающего один атом кислорода;
замещенный или незамещенный амино, где замещающая группа выбрана из 6-членного ароматического карбоциклилкарбонила; 6-членного ароматического карбоциклилкарбонила, замещенного С1-С6 алкилокси; 6-членного ароматического карбоциклил-С1-С6-алкила, замещенного С1-С6 алкилокси; 6-членного ароматического карбоциклилсульфонила; 3-6-членного неароматического гетероциклила, включающего один атом азота и замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один атом азота и замещенного галоген-С1-С6 алкилом; и C1-С6 алкил;
замещенный или незамещенный карбамоил; где замещающая группа выбрана из С1-С6 алкила, замещенного галогеном;
гидрокси;
галоген;
замещенный или незамещенный 6-членный ароматический карбоциклил; где замещающая группа выбрана из C1-С6 алкила, замещенного С1-С6 алкилокси;
незамещенный 9- или 10-членный неароматический гетероциклил, включающий три атома азота;
замещенный или незамещенный 3-10-членный неароматический гетероциклил; где замещающая группа выбрана из С1-С6 алкила, замещенного 6-членным ароматическим карбоциклом; С1-С6 алкила, замещенного 5- или 6-членным ароматическим гетероциклом, включающая один или два атомами азота; С1-С6 алкила, замещенного галогеном; и 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота;
замещенный или незамещенный 3-6-членный неароматический карбоциклил; где замещающая группа выбрана из карбамоила и С1-С6алкилкарбамоила; или
замещенный или незамещенный 3-6-членный неароматический гетероциклилкарбонил, включающий один или два атома азота; где замещающая группа выбрана из 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 3-6-членного неароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; С1-С6 алкила, замещенного галогеном; галогена; и С1-С6 алкилокси; или
R4 и RU взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного 5- или 6-членного неароматического гетероциклического кольца, включающего один или два атома кислорода; где замещающая группа выбрана из галогена;
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, где R1 представляет собой карбокси, или его фармацевтически приемлемая соль.
3. Соединение по п. 1 или 2, где L представляет собой замещенный или незамещенный 3-20-членный неароматический карбоциклилдиил, включающий одно кольцо или два или более колец, где замещающая группа выбрана из С1-С6 алкила; гидрокси; циано; С1-С6 алкилокси и галогена,
или его фармацевтически приемлемая соль.
4. Соединение по любому из пп. 1-3, где R3 представляет собой атом водорода,
или его фармацевтически приемлемая соль.
5. Соединение по любому из пп. 1-4, где V представляет собой -N= и W представляет собой =N-,
или его фармацевтически приемлемая соль.
6. Соединение по любому из пп. 1-5, где группа формулы:
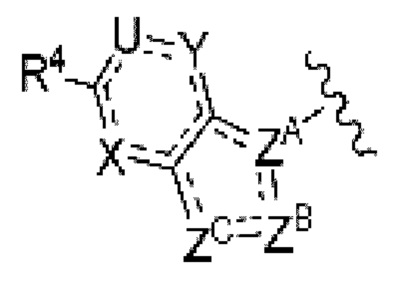
представляет собой
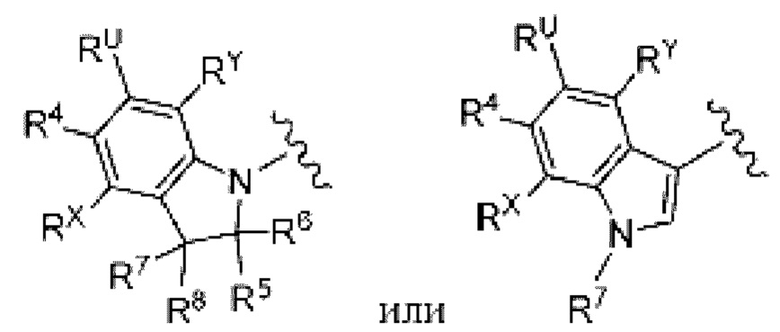
где каждый символ такой, как определен в п. 1,
или его фармацевтически приемлемая соль.
7. Соединение по любому из пп. 1-6, где группа формулы:
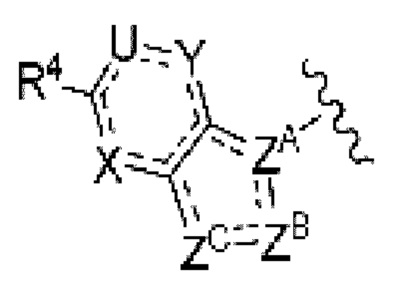
представляет собой
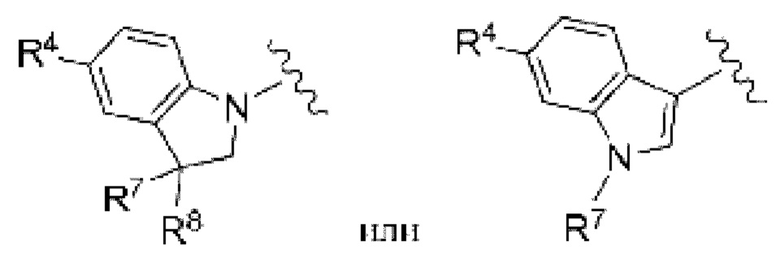
где каждый символ такой, как определен в п. 1, или его фармацевтически приемлемая соль.
8. Соединение по любому из пп. 1-7, где группа формулы: 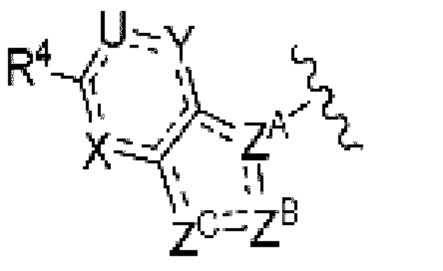 представляет собой
представляет собой 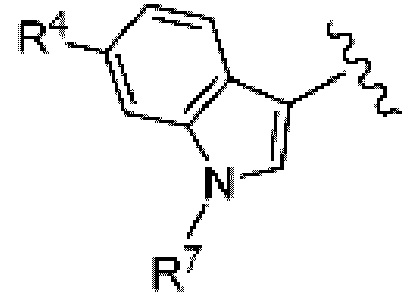
где
R4 такой, как определен в п. 1; и
R7 представляет собой замещенный или незамещенный C1-С6 алкил, где замещающая группа выбрана из C1-С6 алкилокси, галогена, гидрокси, 6-членного ароматического карбоциклила, 3-6-членного неароматического карбоциклила, 3-6-членного неароматического карбоциклила, замещенного галогеном, 3-6-членного неароматического гетероциклилкарбонила, включающего один атом азота и один атом кислорода, и 3-6-членного неароматического гетероциклила, включающего один атом кислорода;
замещенный или незамещенный 3-6-членный неароматический карбоциклил, где замещающая группа выбрана из галогена, циано, 6-членного ароматического карбоциклил-С1-С6-алкилокси, гидрокси, C1-С6 алкиклокси, C1-С6 алкила, C1-С6 алкила, замещенного галогеном;
замещенный или незамещенный 3-6-членный неароматический гетероциклил, включающий один атом кислорода, один атом серы или один атом азота, где замещающая группа выбрана из оксо или C1-С6 алкила, замещенного галогеном;
замещенный или незамещенный 6-членный ароматический карбоциклил, где замещающая группа выбрана из галогена, C1-С6 алкила, C1-С6 алкила, замещенного галогеном, C1-С6 алкилокси и циано;
замещенный или незамещенный 5- или 6-членный ароматический гетероциклил, включающий один или два атома азота, где замещающая группа выбрана из C1-С6 алкила, C1-С6 алкила, замещенного галогеном, галогена, C1-С6 алкилокси, гидрокси и циано;
незамещенный 3-6-членный неароматический карбоциклилоксикарбонил;
незамещенный 3-6-членный неароматический гетероциклилоксикарбонил, включающий один атом кислорода; или
незамещенный 3-6-членный неароматический карбоциклилсульфонил,
или его фармацевтически приемлемая соль.
9. Соединение по любому из пп. 1-7, где группа формулы:
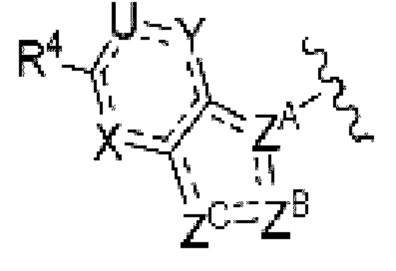
представляет собой
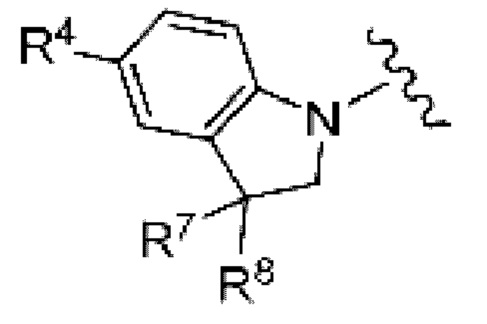
где
R4 такой, как определен в п. 1; и
R7 и R8 каждый независимо представляет собой атом водорода или замещенный или незамещенный C1-С6 алкил, где замещающая группа выбрана из C1-С6 алкилокси, галогена, гидрокси, 6-членного ароматического карбоциклила, 3-6-членного неароматического карбоциклила, 3-6-членного неароматического карбоциклила, замещенного галогеном, 3-6-членного неароматического гетероциклилкарбонила, включающего один атом азота и один атом кислорода, и 3-6-членного неароматического гетероциклила, включающего один атом кислорода; или R7 и R8 взяты вместе с атомом углерода, к которому они присоединены, с образованием замещенного или незамещенного 3-6-членного неароматического углеродного кольца, где замещающая группа выбрана из галогена,
или его фармацевтически приемлемая соль.
10. Соединение по любому из пп. 1-9, где R4 представляет собой замещенный или незамещенный C1-С6 алкилокси, где замещающая группа выбрана из C1-С6 алкилокси; циано; галогена; гидрокси; C1-С6 алкилкарбонилокси; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота, замещенного галоген-С1-С6 алкилом; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота; 3-6-членного неароматического гетероциклила, включающего два атома азота, замещенного C1-С6 алкилом; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенный галогеном; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота и атома серы, замещенного С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один атом азота, замещенного С1-С6 алкилокси; 5- или 6-членного ароматического гетероциклила, включающего два атома азота; и амино, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота;
замещенный или незамещенный 3-10-членный неароматический гетероциклилокси, включающий один, два или три атома, выбранных из атома кислорода, атома азота и атома серы, где замещающая группа выбрана из С1-С6 алкила; С1-С6 алкила, замещенного галогеном; С1-С6 алкила, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота, замещенным С1-С6 алкилом; С1-С6 алкила, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом кислорода; С1-С6 алкила, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом кислорода, замещенным галогеном; С1-С6 алкила, замещенного 3-6-членным неароматическим карбоциклилом, замещенным галогеном; C1-С6 алкила, замещенного С1-С6 алкилсульфонилом; С1-С6 алкила, замещенного C1-С6 алкокси; С1-С6 алкила, замещенного циано; С1-С6 алкилкарбонила; С1-С6 алкилоксикарбонила; С1-С6 алкилоксикарбонила, замещенного 6-членным ароматическим карбоциклилом; C1-С6 алкилкарбамоила; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома азота и атома серы, замещенного оксо; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного С1-С6 алкилкарбонилом; 3-6-членного неароматического гетероциклилкарбонила, включающего один атом кислорода; 5- или 6-членного ароматического гетероциклила, включающего один или два атома, выбранных из атома азота и атома серы; 5- или 6-членного ароматического гетероциклилкарбонила, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота, атома кислорода и атома серы, замещенного С1-С6 алкилом; 5- или 5-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота, атома кислорода и атома серы, замещенного галоген-С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного С1-С6 алкилокси; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного циано; 3-6-членного неароматического карбоциклила; 3-6-членного неароматического карбоциклила, замещенного галогеном; 3-6-членного неароматического карбоциклилкарбонила; 3-6-членного неароматического карбоциклилкарбонила; 3-6-членного неароматического карбоциклилсульфонила; оксо; и галогена;
замещенный или незамещенный 3-10-членный неароматический карбоциклилокси, где замещающая группа выбрана из 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; С1-С6 алкилсульфонила; С1-С6 алкилокси; 3-6-членного неароматического гетероциклила, включающего один атом кислорода и один атом азота; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного галогеном; 3-6-членного неароматического карбоциклилиминокси, замещенного галогеном; 3-6-членного неароматического карбоциклилоксиимино, замещенного галогеном; 3-6-членного неароматического гетероциклил-С1-С6 алкила, включающего один атом азота, замещенного галогеном; C1-С6 алкила; С1-С6 алкила, замещенного галогеном; галогена; амино, замещенного галоген-С1-С6 алкилом; амино, замещенного C1-С6 алкилом; 5- или 6-членного ароматического гетероциклиламино, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома азота; и 3-6-членного неароматического карбоциклилокси;
незамещенный 6-членный ароматический карбоциклилокси;
замещенный или незамещенный С1-С6 алкил; где замещающая группа выбрана из галогена; 3-10-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила включающего один или два атома азота, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота; 3-10-членного неароматического гетероциклила, включающего три атомами азота, замещенного С1-С6 алкилом; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом азота, где указанный гетероциклил замещен галогеном; 6-членного ароматического карбоциклила; 6-членного ароматического карбоциклила, замещенного C1-С6 алкилокси; и 3-6-членного неароматического карбоциклилоксиимино, замещенного галогеном;
замещенный или незамещенный С2-С6 алкенил, где замещающая группа выбрана из 6-членного ароматического карбоциклила, замещенного С1-С6 алкилокси; и 3-6-членного неароматического гетероциклила, включающего один атом кислорода;
замещенный или незамещенный амино, где замещающая группа выбрана из 6-членного ароматического карбоциклилкарбонила; 6-членного ароматического карбоциклилкарбонила, замещенного С1-С6 алкилокси; 6-членного ароматического карбоциклил-С1-С6-алкила, замещенного C1-С6 алкилокси; 6-членного ароматического карбоциклилсульфонила; 3-6-членного неароматического гетероциклила, включающего один атом азота и замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один атом азота и замещенного галоген-С1-С6 алкилом; и С1-С6 алкил;
замещенный или незамещенный карбамоил; где замещающая группа выбрана из С1-С6 алкила, замещенного галогеном;
гидрокси;
галоген;
замещенный или незамещенный 6-членный ароматический карбоциклил; где замещающая группа выбрана из С1-С6 алкила, замещенного С1-С6 алкилокси;
незамещенный 9- или 10-членный ароматический гетероциклил, включающий три атома азота;
замещенный или незамещенный 3-10-членный неароматический гетероциклил; где замещающая группа выбрана из С1-С6 алкила, замещенного 6-членным ароматическим карбоциклом; C1-С6 алкила, замещенного 5- или 6-членным ароматическим гетероциклом, включающая один или два атомами азота; С1-С6 алкила, замещенного галогеном; и 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота;
замещенный или незамещенный 3-6-членный неароматический карбоциклил; где замещающая группа выбрана из карбамоила и С1-С6 алкилкарбамоила;
или его фармацевтически приемлемая соль.
11. Соединение по любому из пп. 1-10, где R4 представляет собой замещенный или незамещенный 3-10-членный неароматический гетероциклилокси, включающий один, два или три атома, выбранных из атома кислорода, атома азота и атома серы, где замещающая группа выбрана из С1-С6 алкила; C1-С6 алкила, замещенного галогеном; С1-С6 алкила, замещенного 5- или 6-членным ароматическим гетероциклилом, включающим два атома азота, замещенным С1-С6 алкилом; С1-С6 алкила, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом кислорода; С1-С6 алкила, замещенного 3-6-членным неароматическим гетероциклилом, включающим один атом кислорода, замещенным галогеном; С1-С6 алкила, замещенного 3-6-членным неароматическим карбоциклилом, замещенным галогеном; С1-С6 алкила, замещенного С1-С6 алкилсульфонилом; С1-С6 алкила, замещенного С1-С6 алкокси; С1-С6 алкила, замещенного циано; С1-С6 алкилкарбонила; С1-С6 алкилоксикарбонила; С1-С6 алкилоксикарбонила, замещенного 6-членным ароматическим карбоциклилом; С1-С6 алкилкарбамоила; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома кислорода и атома азота; 3-6-членного неароматического гетероциклила, включающего один или два атома, выбранных из атома азота и атома серы, замещенного оксо; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного C1-С6 алкилкарьбонилом; 3-6-членного неароматического гетероциклилкарбонила, включающего один атом кислорода; 5- или 6-членного ароматического гетероциклила, включающего один или два атома, выбранных из атома азота и атома серы; 5- или 6-членного ароматического гетероциклилкарбонила, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота, атома кислорода и атома серы, замещенного С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома, выбранных из атома азота, атома кислорода и атома серы, замещенного галоген-С1-С6 алкилом; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного С1-С6 алкилокси; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного циано; 3-6-членного неароматического карбоциклила; 3-6-членного неароматического карбоциклила, замещенного галогеном; 3-6-членного неароматического карбоциклилкарбонила; 3-6-членного неароматического карбоциклилкарбонила; 3-6-членного неароматического карбоциклилсульфонила; оксо; и галогена;
замещенный или незамещенный 3-10-членный неароматический карбоциклилокси, где замещающая группа выбрана из 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота; C1-С6 алкилсульфонила; C1-С6 алкилокси; 3-6-членного неароматического гетероциклила, включающего один атом кислорода и один атом азота; 3-6-членного неароматического гетероциклила, включающего один атом азота, замещенного галогеном; 3-6-членного неароматического карбоциклилиминокси, замещенного галогеном; 3-6-членного неароматического карбоциклилоксиимино, замещенного галогеном; 3-6-членного неароматического гетероциклил-С1-С6 алкила, включающего один атом азота, замещенного галогеном; C1-С6 алкила; С1-С6 алкила, замещенного галогеном; галогена; амино, замещенного галоген-С1-С6 алкилом; амино, замещенного С1-С6 алкилом; 5- или 6-членного ароматического гетероциклиламино, включающего один или два атома азота; 5- или 6-членного ароматического гетероциклила, включающего один или два атома азота, замещенного галогеном; 5- или 6-членного ароматического гетероциклила, включающего один, два или три атома азота; и 3-6-членного неароматического карбоциклилокси,
или его фармацевтически приемлемая соль.
12. Соединение по п. 1, выбранное из группы, состоящей из соединений:
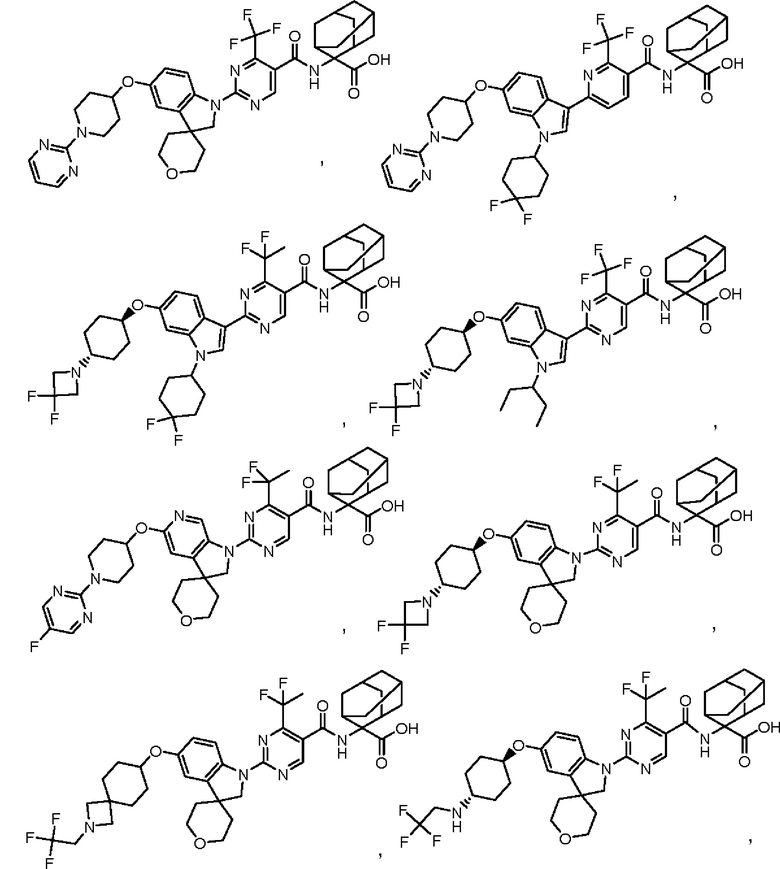
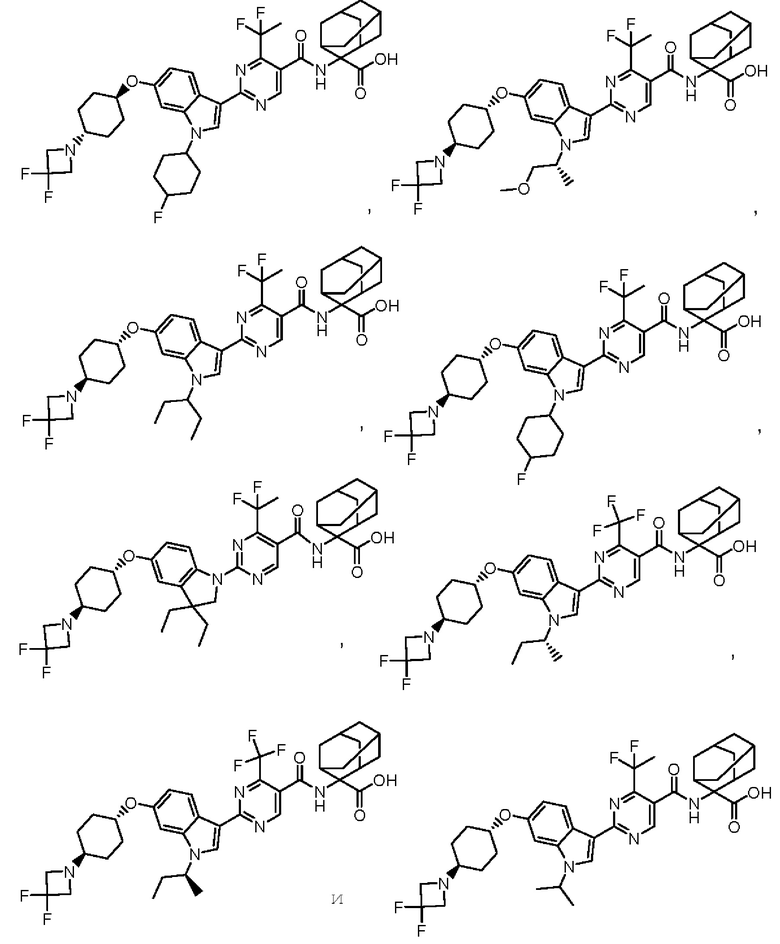
или его фармацевтически приемлемая соль.
13. Соединение по п. 1, представляющее собой:
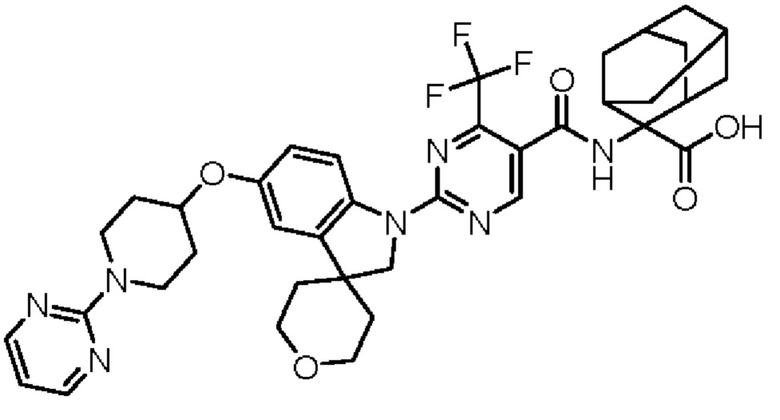
или его фармацевтически приемлемая соль.
14. Соединение по п. 1, представляющее собой:
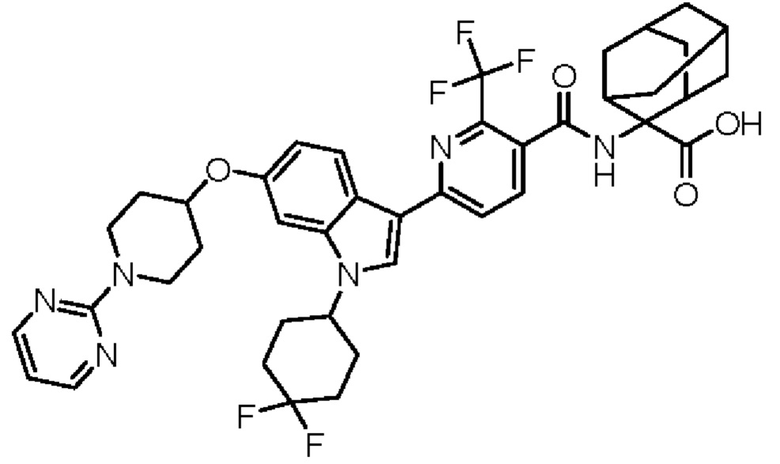
или его фармацевтически приемлемая соль.
15. Соединение по п. 1, представляющее собой:
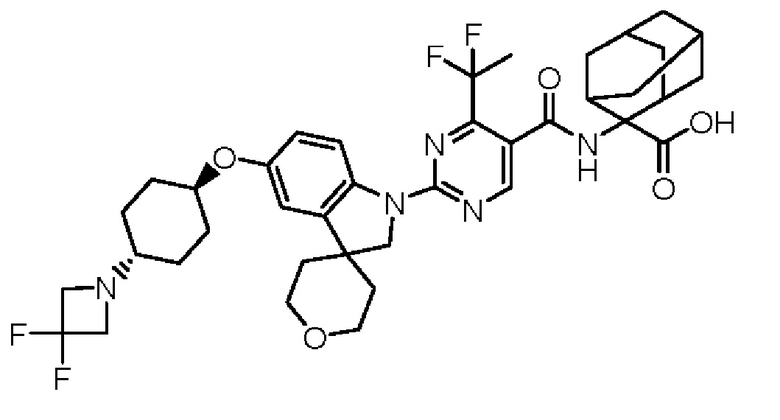
или его фармацевтически приемлемая соль.
16. Соединение по п. 1, представляющее собой:
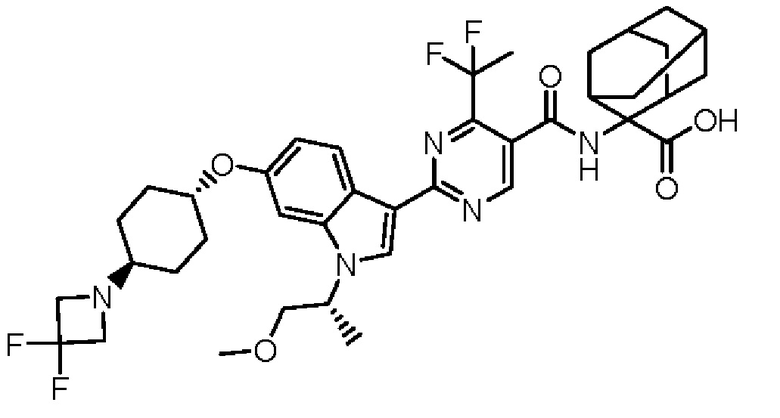
или его фармацевтически приемлемая соль.
17. Соединение по п. 1, представляющее собой:
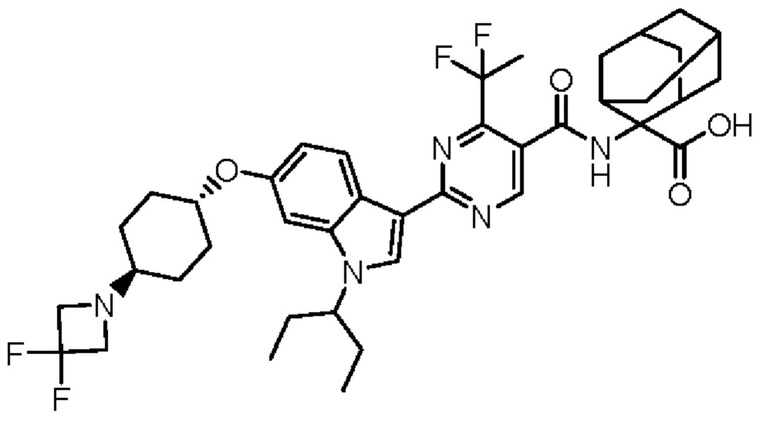
или его фармацевтически приемлемая соль.
18. Соединение по п. 1, представляющее собой:
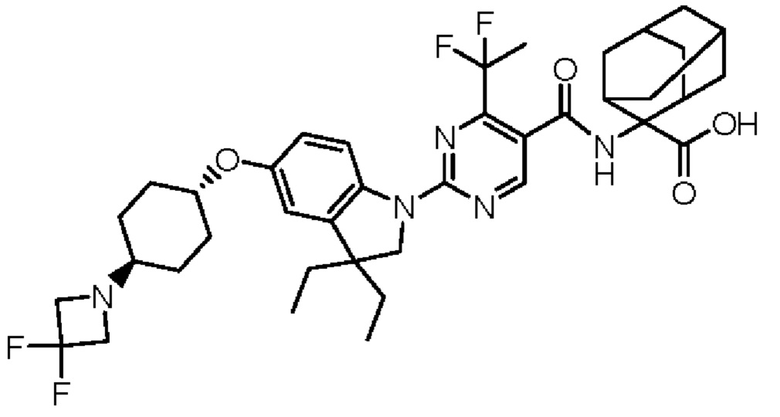
или его фармацевтически приемлемая соль.
19. Соединение по п. 1, представляющее собой:
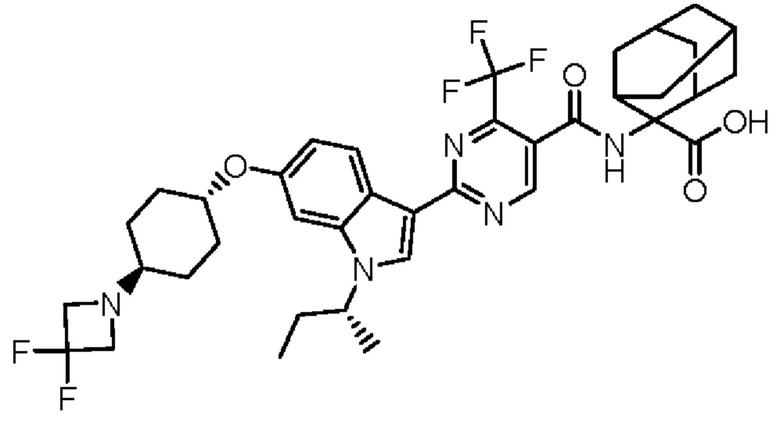
или его фармацевтически приемлемая соль.
20. Фармацевтическая композиция, обладающая активностью против вируса RS, содержащая эффективное количество соединения по любому из пп. 1-19 или его фармацевтически приемлемой соли.
| WO 2016148145 A1, 22.09.2016 | |||
| JP 2015516976 A, 18.06.2015 | |||
| WO 2012130905 A1, 04.10.2012 | |||
| RU 2008143557 A, 20.06.2010. |
Авторы
Даты
2025-03-20—Публикация
2021-10-27—Подача