Изобретение относится к области химической промышленности, а именно к способам получения производных фталонитрилов - 4,5-бис(4'-пропилфенокси)фталонитрила, который может быть использован в качестве полупродукта в синтезе окта-4,5-(4'-пропилфенокси)фталоцианина и его комплексов с алюминием (III), галлием (III) и индием (III), проявляющими флуоресцентные свойства.
Известен окта-(4,5-(фенокси)фталоцианин магния [Znoiko S.A. et al. Synthesis of Magnesium Octa-4,5-phenoxyphthalocyanine and Sulfo- and Alkylsulfamoyl Derivatives on Its Basis // Russian Journal of General Chemistry. - 2018. - V. 88. - P. 1148-1153].
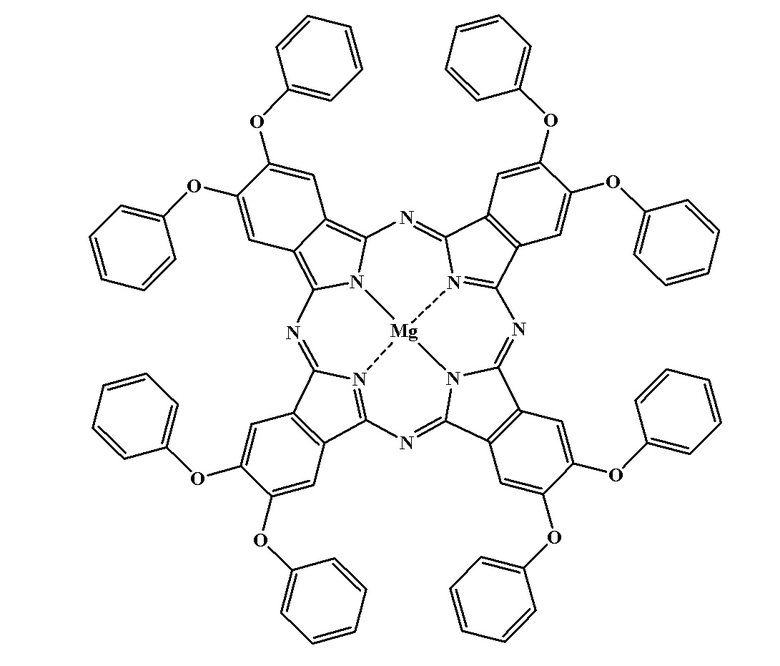
Однако сведения о наличии у него флуоресцентных свойств отсутствуют.
Известен окта-4,5-(4'-метоксифенокси)фталоцианин меди [Miho Yoshioka, Kazuchika Ohta, Mikio Yasutake Flying-seed-like liquid crystals. Part 4:† a novel series of bulky substituents inducing mesomorphism instead of using long alkyl chains // The Royal Society of Chemistry. - 2015 - V. 5. - P. 13828-13839].
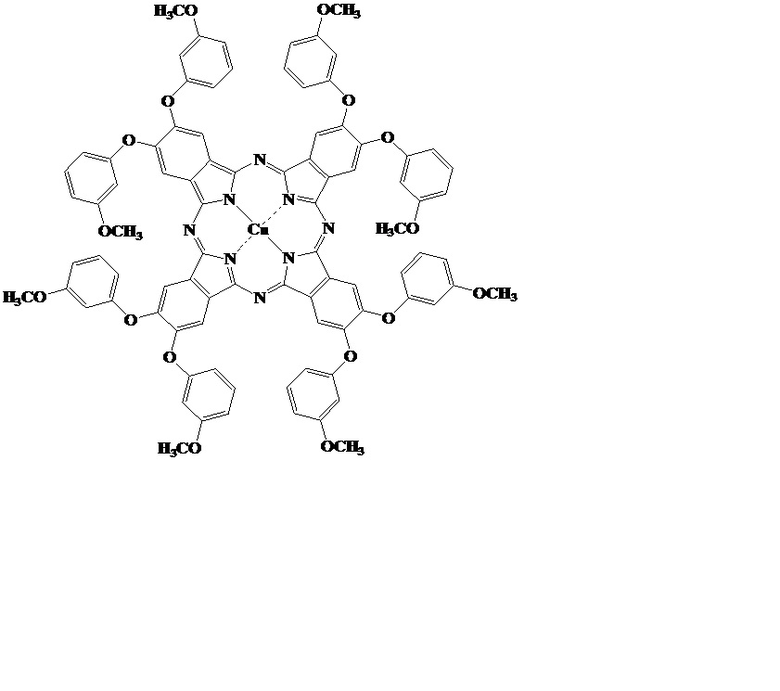
При этом в научно-технической литературе отсутствуют сведения о проявлении окта-4,5-бис(4'-метоксифенокси)фталоцианином меди флуоресцентных свойств.
Изобретательская задача состоит в поиске новых соединений, обладающих флуоресцентными свойствами.
Поставленная задача решена синтезом окта-4,5-(4'-пропилфенокси)фталоцианина и его комплексов с алюминием (III), галлием (III) и индием (III) общей формулы:
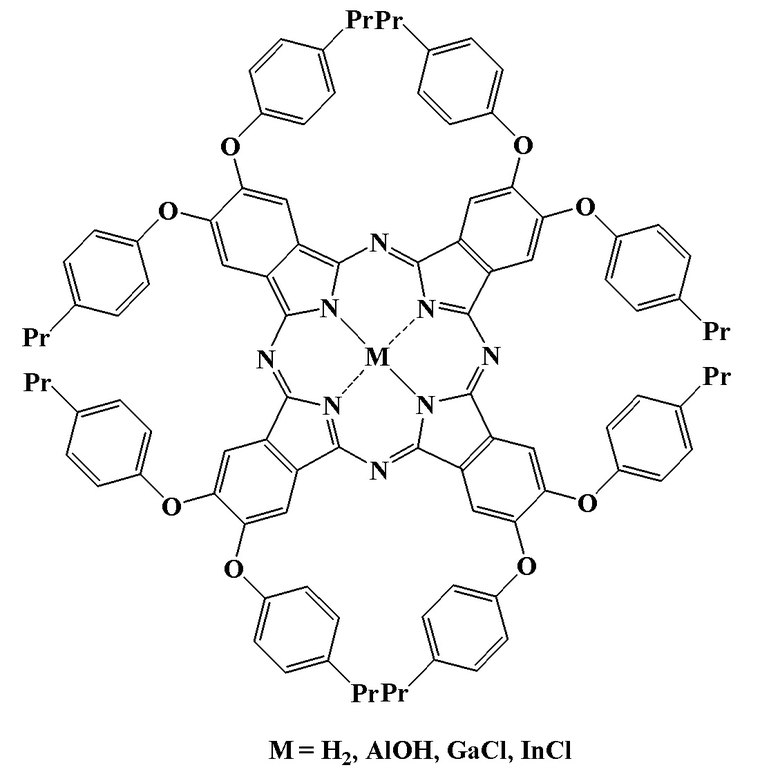
Структура этих соединений доказана данными элементного анализа, масс-спектрометрии (MALDI-TOF), электронной, ИК и ЯМР спектроскопии.
В качестве промежуточных соединений для синтеза фталоцианинов используются фталонитрилы.
Известен 4,5-бисфеноксифталонитрил [Koptyaev A.I., Galanin N.E., Shaposhnikov G.P. Synthesis and association in dichloromethane solution of low-symmetry phenoxy (fluoro)-substituted nickel phthalocyaninates // Russian Journal of General Chemistry. - 2016. - Т. 86. - С. 854-858; Znoiko S. A. et.al. Synthesis of Magnesium Octa- 4, 5-phenoxyphthalocyanine and Sulfo- and Alkylsulfamoyl Derivatives on Its Basis //Russian Journal of General Chemistry. - 2018. - V. 88. - P. 1148-1153].
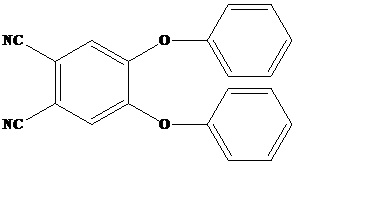
Однако сведения о наличии флуоресцентных свойств полученных на его основе металлокомплексов фталоцианина отсутствуют.
Одним из наиболее близких структурных аналогов заявляемого соединения является 4,5-бис(4'-метоксифенокси)фталонитрил [Miho Yoshioka, Kazuchika Ohta, Mikio Yasutake Flying-seed-like liquid crystals. Part 4:† a novel series of bulky substituents inducing mesomorphism instead of using long alkyl chains // The Royal Society of Chemistry. - 2015 - V. 5. - P. 13828-13839].
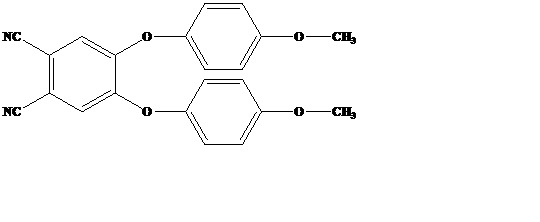
Однако сведения о получении на основе 4,5-бис-(4'-метоксифенокси)фталонитрила соответствующих комплексов фталоцианина и об их флуоресцентных свойствах в научно-технической литературе отсутствуют.
Изобретательская задача состоит в поиске нового соединения, которое является промежуточным в синтезе окта-4,5-(4'-пропилфенокси)фталоцианина и его комплексов с алюминием (III), галлием (III) и индием (III).
Поставленная задача решена синтезом 4,5-бис(4'-пропилфенокси)фталонитрила формулы:
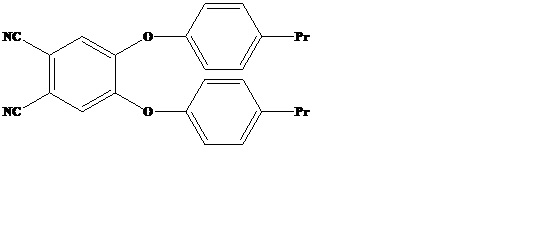
Структура соединения доказана данными элементного анализа, ИК, ЯМР спектроскопии, хромато-масс спектрометрии.
Изобретение поясняется чертежами.
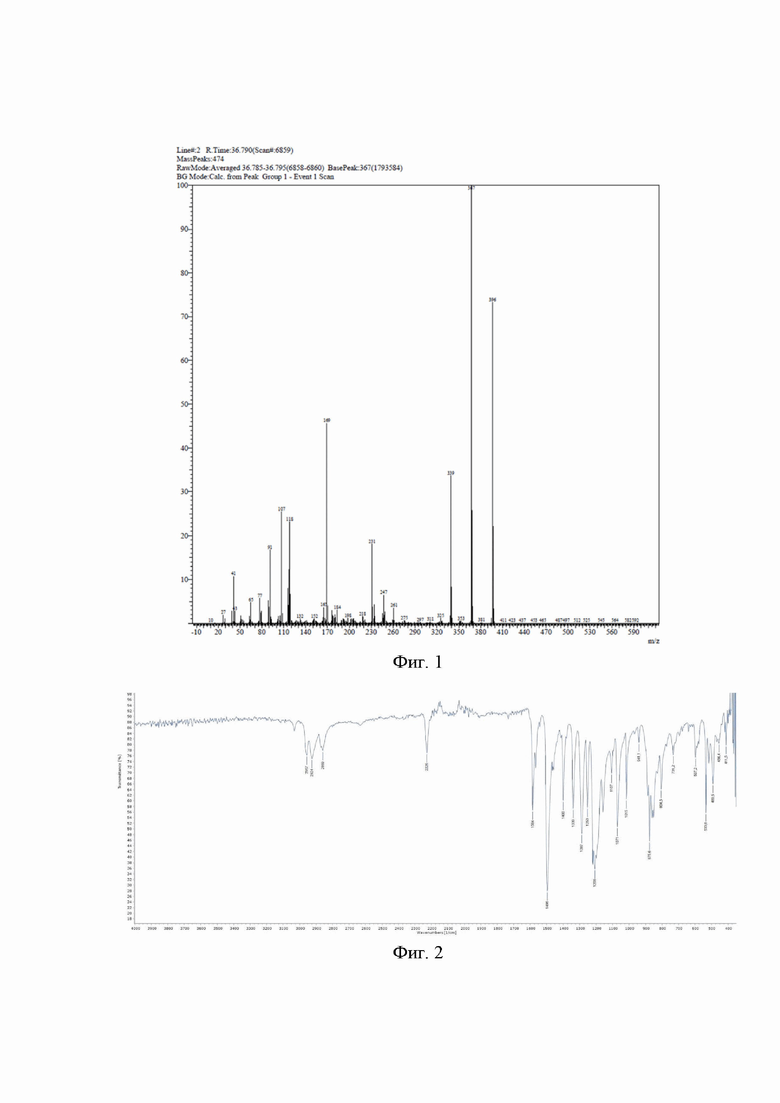
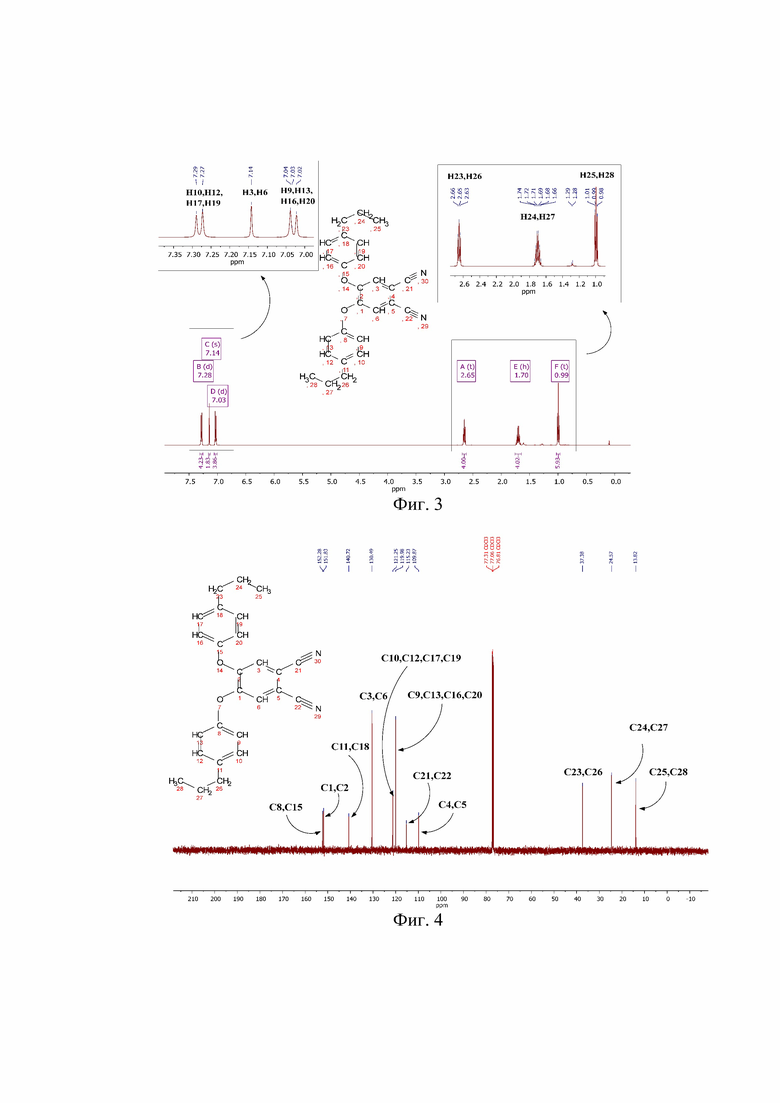
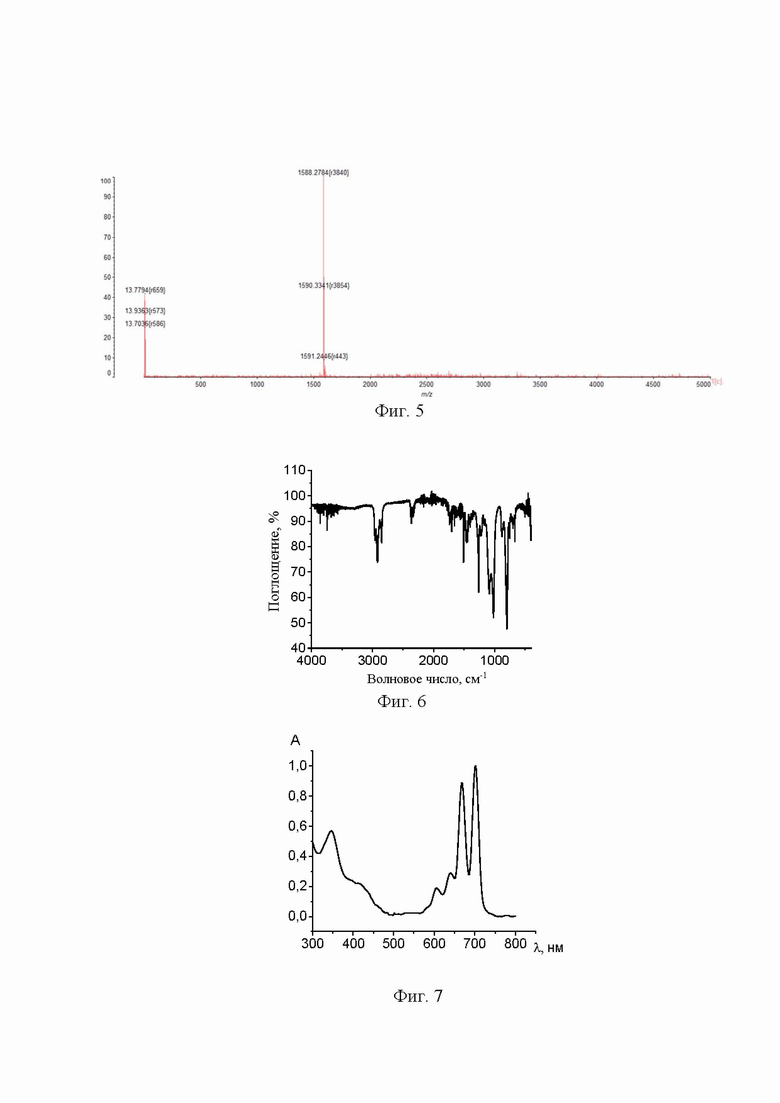
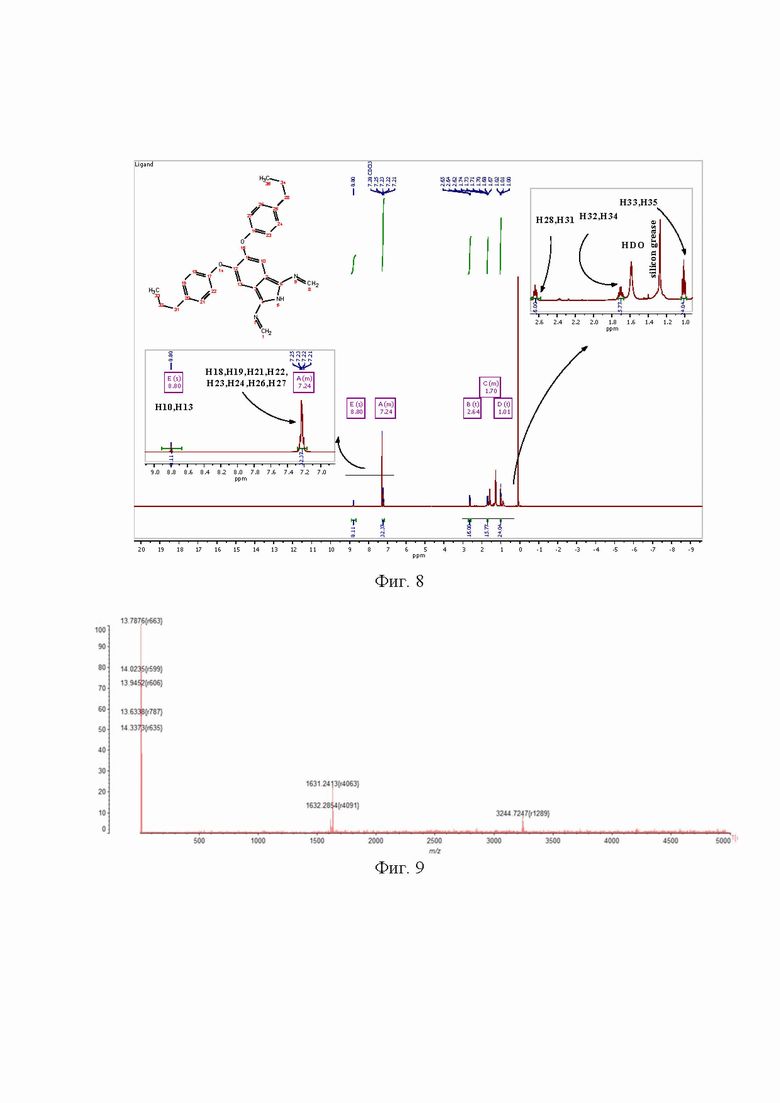
На фиг. 1 изображен хромато-масс-спектр 4,5-бис(4'-пропилфенокси)фталонитрила; на фиг. 2 - ИК спектр 4,5-бис(4'-пропилфенокси)фталонитрила; на фиг. 3 - 1Н ЯМР спектр 4,5-бис(4'-пропилфенокси)фталонитрила; на фиг. 4 - 13С ЯМР спектр 4,5-бис(4'-пропилфенокси)фталонитрила; на фиг. 5 - MALDI-TOF масс-спектр окта-4,5-(4'-пропилфенокси)фталоцианина; на фиг. 6 - ИК спектр окта-4,5-(4'-пропилфенокси)фталоцианина на фиг. 7 - ЭСП окта-4,5-(4'-пропилфенокси)фталоцианина; на фиг. 8 - 1Н ЯМР спектр окта-4,5-(4'-пропилфенокси)фталоцианина; на фиг. 9 - MALDI-TOF масс-спектр окта-4,5-(4'-пропилфенокси)фталоцианина алюминия (III); на фиг. 10 - ИК спектр окта-4,5-(4'-пропилфенокси)фталоцианина алюминия (III); на фиг. 11 - ЭСП окта-4,5-(4'-пропилфенокси)фталоцианина алюминия (III); на фиг. 12 - 1Н ЯМР спектр окта-4,5-(4'-пропилфенокси)фталоцианина алюминия (III); на фиг. 13 - MALDI-TOF масс-спектр окта-4,5-(4'-пропилфенокси)фталоцианина галлия (III); на фиг. 14 - ИК спектр окта-4,5-(4'-пропилфенокси)фталоцианина галлия (III);на фиг. 15 - ЭСП окта-4,5-(4'-пропилфенокси)фталоцианина галлия (III); на фиг. 16 - 1Н ЯМР спектр окта-4,5-(4'-пропилфенокси)фталоцианина галлия (III); на фиг. 17 - MALDI-TOF масс-спектр окта-4,5-(4'-пропилфенокси)фталоцианина индия (III); на фиг. 18 - ИК спектр окта-4,5-(4'-пропилфенокси)фталоцианина индия (III); на фиг. 19 - ЭСП окта-4,5-(4'-пропилфенокси)фталоцианина индия (III); на фиг. 20 - 1Н ЯМР спектр окта-4,5-(4'-пропилфенокси)фталоцианина индия (III).
Для синтеза заявляемых соединений используют следующие вещества:
- 4-бром-5-нитрофталонитрил - не является коммерчески доступным, его получали по известной методике [Шишкина О. В., Майзлиш В. Е., Шапошников Г. П., Смирнов Р. П., Бараньски А. Галогенонитрофталимиды и фталодинитрилы на их основе // Журн. общ. химии - 1997. - Т. 67, вып. 5. - С. 842-845];
- ДМФА - ГОСТ 20289-74;
- 4-пропилфенол - Alfa Aesar CAS 645-56-7;
- K2CO3 - ГОСТ 4221-76;
- ацетат магния тетрагидрат - Ареолаб CAS 16674-78-5;
- хлорид алюминия - ГОСТ 3759-75;
- хлорид галлия - ПКП-РМС CAS 13450-90-3;
- хлорид индия - ТУ 6-09-04-124-74;
- соляная кислота - ГОСТ 12.1.007-76;
- гидроксид натрия - ГОСТ 4328-77;
- молибдат аммония тетрагидрат - Sisco Reseach Laboratories CAS 12054-85-1;
- трифторуксусная кислота - ООО «Кемикал Лайн» CAS RN 76-05-1;
- вода дистиллированная (κ = 3,6 мкС/см, pH = 6,6);
- этанол - ГОСТ 5962-2013;
- дихлорметан - ТУ 2412-426-05763441-2004;
- карбамид - ГОСТ 2081-2010.
Заявляемые соединения могут быть получены следующим образом.
Пример 1. Синтез 4,5-бис(4'-пропилфенокси)фталонитрила:
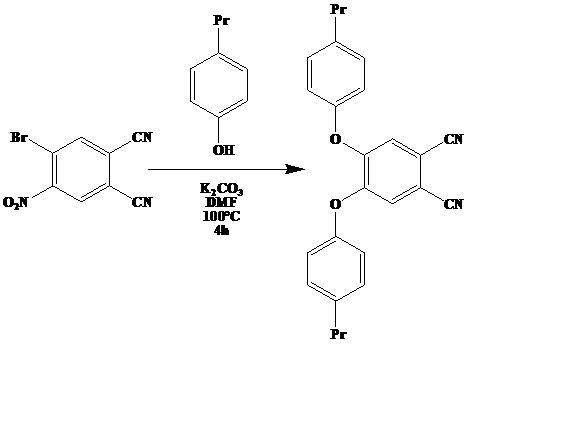
Смесь, состоящую из 5 г (0,02 моль) 4-бром-5-нитрофталонитрила (0,02 моль), 6 г (0,044 моль) 4-пропилфенола и 6 г (0,044 моль) K2CO3 растворяют в 20 мл ДМФА и перемешивают при 100°С в течение 4 часов. Полученный раствор разбавляют 60 мл дистиллированной воды и подкисляют соляной кислотой до слабокислой реакции (pH = 4). Образующийся осадок темно-коричневого цвета отфильтровывают, промывают водой (90 мл) до нейтральной реакции промывных вод и перекристаллизовывают из этанола.
Выход: 6,6 г (85%).
Найдено, %: C -77,96; H - 6,18; N - 7,00; C26H24N2O2.
Вычислено, %: C -78,76; H - 6,10; N - 7,07.
Масс-спектр, m/z = 396 [M], вычислено - 396,48 (Фиг. 1).
ИК спектр, см-1: 2957(C-H), 2924(C-H), 2860(C-H), 2226 (CN), 1584, 1496, 1400, 1339, 1287, 1252, 1208, 1159, 1107(-C-O-C-), 1071(-C-O-C-), 1015, 941, 876, 805, 731, 597, 534, 490, 456, 412 (Фиг. 2).
Спектр 1H ЯМР (500 МГц; CDCl3), δ, м.д.: δ 7,28 (d, 3J = 8,3 Гц, 4H), 7,14 (s, 2H), 7,03 (d, 3J = 8,2 Гц, 4H), 2,65 (t, 3J = 7,7 Гц, 4H), 1,70 (h, 3J = 7,4 Гц, 4H), 0,99 (t, 3J = 7,3 Гц, 6H) (Фиг. 3).
Спектр 13C ЯМР (126 МГц, CDCl3) δ 152,28, 151,83, 140,72, 130,49, 121,25, 119,98, 115,23, 109,87, 77,31, 77,06, 76,81, 37,38(Ar-CH2), 24,57(-CH2-), 13,82(-CH3) (Фиг. 4).
Пример 2. Использование 4,5-бис(4'-пропилфенокси)фталонитрила как промежуточного продукта для синтеза окта-4,5-(4'-пропилфенокси)фталоцианина:
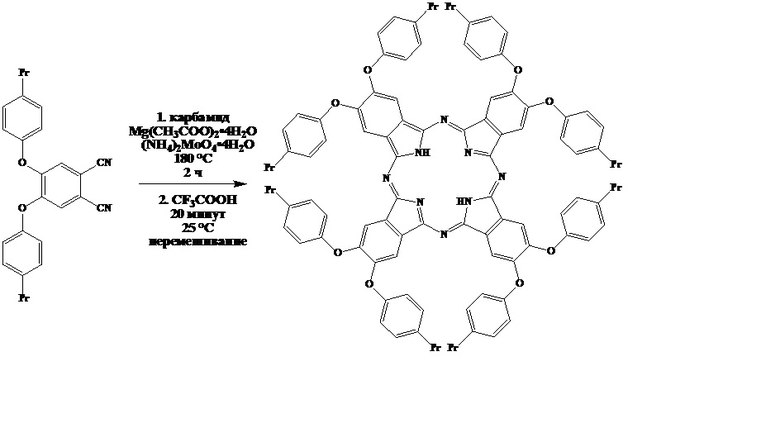
Смесь 0,100 г (0,00025 моль) 4,5-бис(4'-пропил)фталонитрила, 0,100 г (0,0017 моль) карбамида, 0,030 г (0,000024 моль) тетрагидрата молибдата аммония и 0,017 г (0,00008 моль) тетрагидрата ацетата магния нагревают при 180°C в течение 2 часов. Неочищенный темно-зеленый осадок помещают в коническую колбу с 4 мл CF3COOH, закрывают пробкой и перемешивают при комнатной температуре в течение 20 минут. Темно-коричневый раствор разбавляют 10 мл воды, полученный темно-зеленый осадок отфильтровывают, промывают горячим этанолом (40 мл), 5 %-ным раствором NaOH (20 мл) и горячей водой до нейтральной среды. Осадок высушивают на воздухе при 70°С, после чего очищают при помощи колоночной хроматографии на силикагеле, используя дихлорметан в качестве элюента.
Выход: 31 мг (37%).
Найдено, %: С - 57,02, H - 3,01, N - 13,22; C104H98N8O8.
Вычислено, %: C - 57,90, H - 2,92, N - 13,51.
Масс-спектр, m/z = 1588,19[M]; 1589,18[M+H], вычислено - 1587,94 (Фиг. 5).
ИК спектр, см-1: 795, 879, 1015 (NH), 1086, 1260 (Ar-O-Ar), 1507, 2358, 2849 (C-H), 2918(C-H), 2960 (C-H) (Фиг. 6).
ЭСП в дихлорметане, λmax , нм: 668; 701,5 (Фиг. 7).
Спектр 1H ЯМР (500 МГц, CDCl3) δ: 8,80 (s, 8H), 7,28-7,17 (m, 32H), 2,64 (t, 3J = 7,6 Гц, 16H), 1,73-1,67 (m, 16H), 1,01 (t, 3J = 7,3 Гц, 24H) (Фиг. 8).
Пример 3. Использование 4,5-бис(4'-пропилфенокси)фталонитрила как промежуточного продукта для синтеза окта-4,5-(4'-пропилфенокси)-фталоцианина алюминия (III):
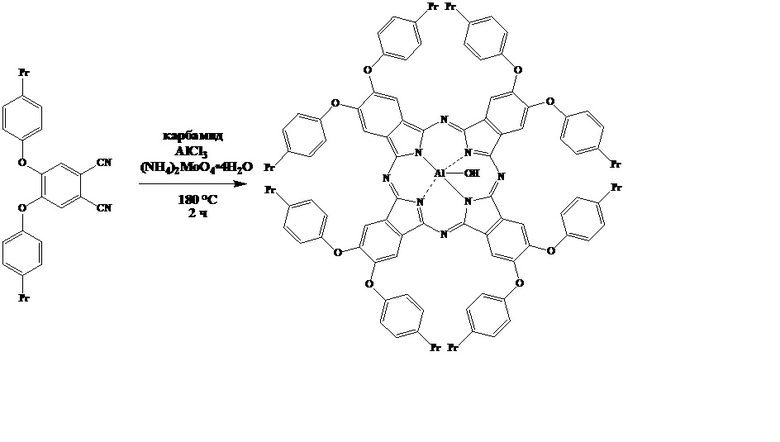
Смесь 0,100 г (0,00025 моль) 4,5-бис(4'-пропилфенокси)фталонитрила, 0,100 г (0,0017 моль) карбамида, 0,030 г (0,000024 моль) тетрагидрата молибдата аммония и 0,011 г (0,00008 моль) AlCl3 нагревают при 180°C в течение 2 часов. Полученный осадок темно-зеленого цвета промывают горячим этанолом (40 мл), 5 %-ным раствором NaOH (20 мл) и горячей водой до нейтральной среды. Осадок высушивают на воздухе при 70°С, после чего очищают при помощи колоночной хроматографии на силикагеле, используя дихлорметан в качестве элюента.
Выход: 19 мг (19%).
Найдено, %: C - 76,02; H - 6,16; N - 6,95; C104H97AlN8O9.
Вычислено, %: C - 76,64; H - 6,00; N - 6,87.
Масс-спектр, m/z = 1631,24 [M+H]; 1614,26 [M-OH], вычислено - 1629,91 (Фиг. 9).
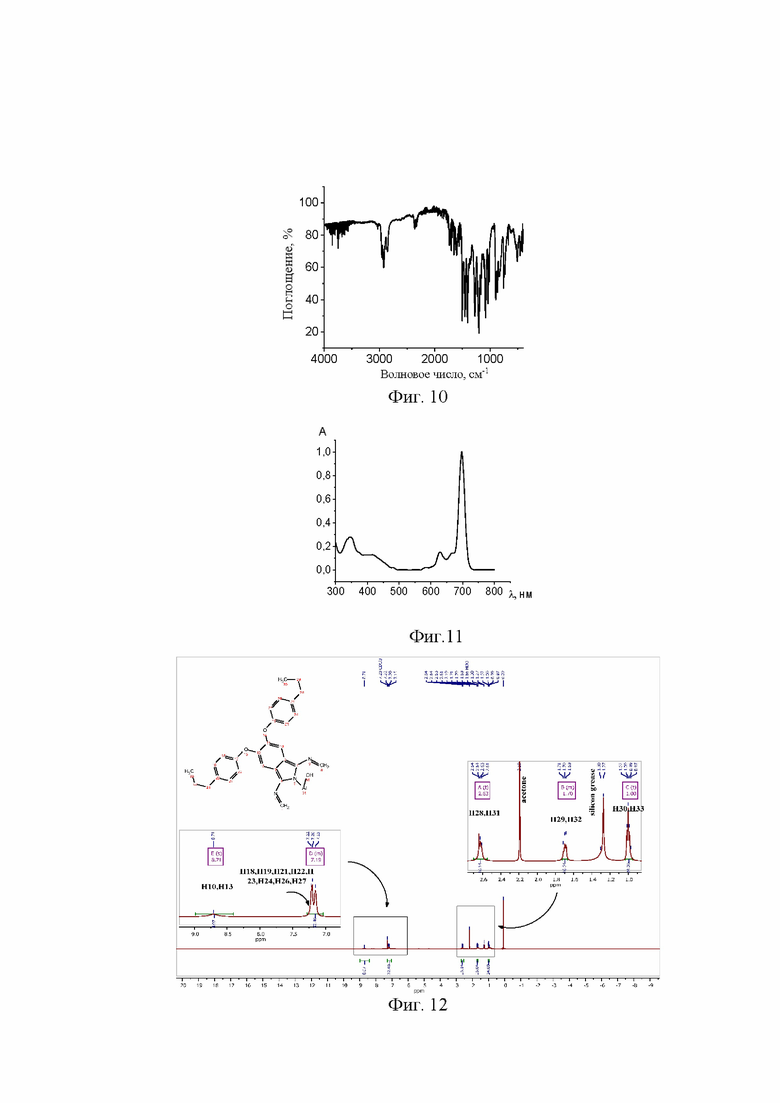
ИК спектр, см-1: 754, 865, 897, 1036, 1081, 1164, 1200 (C-O-C), 1274 (Ar-O-Ar), 1407, 1455(C-H), 1504, 1603, 1654, 1700, 2852(C-H), 2926(C-H), 2956(C-H) (Фиг. 10).
ЭСП в дихлорметане, λmax, нм: 697 (Фиг. 11).
Спектр 1H ЯМР (500 МГц, CDCl3) δ 8,71 (s, 8H), 7,28-7,03 (m, 32H), 2,63 (t, 3J = 7,8 Гц, 16H), 1,72-1,67 (m, 16H), 1,00 (t, 3J = 7,3 Гц, 24H) (Фиг. 12).
Пример 4. Использование 4,5-бис(4'-пропилфенокси)фталонитрила как промежуточного продукта для синтеза окта-4,5-(4'-пропилфенокси)-фталоцианина галлия (III):
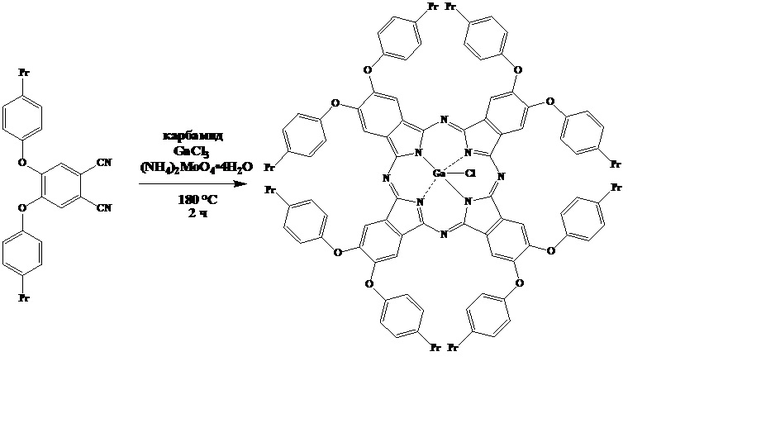
Смесь 0,100 г (0,00025 моль) 4,5-бис(4'-пропилфенокси)фталонитрила, 0,100 г (0,0017 моль) карбамида, 0,030 г (0,000024 моль) тетрагидрата молибдата аммония и 0,014 г (0,00008 моль) GaCl3 нагревают при 180°C в течение 2 часов. Полученный осадок темно-зеленого цвета промывают горячим этанолом (40 мл), 5 %-ным раствором NaOH (20 мл) и горячей водой до нейтральной среды. Осадок высушивают на воздухе при 70°С, после чего очищают при помощи колоночной хроматографии на силикагеле, используя дихлорметан в качестве элюента.
Выход: 25 мг (24%).
Найдено, %: C - 73,04; H - 5,68; N - 6,72; C104H96ClGaN8O8.
Вычислено, %: C - 73,86; H - 5,72; N - 6,63.
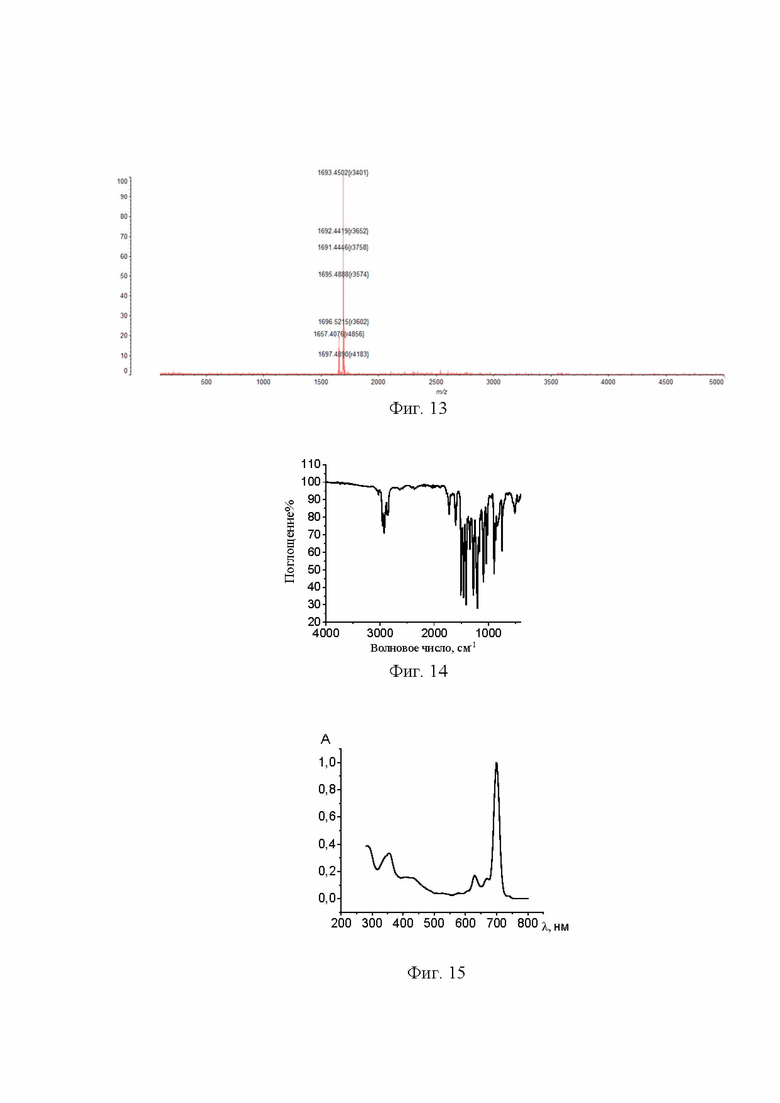
Масс-спектр, m/z = 1693,45 [M+2H], 1659,42 [M-Cl+4H], вычислено - 1691,1 (Фиг. 13).
ИК спектр, см-1: 746, 893, 1036, 1090, 1200(C-O-C), 1275(Ar-O-Ar), 1337, 1410, 1456(C-H), 1504, 1601, 1724, 2851(C-H), 2924(C-H), 2957(C-H) (Фиг. 14).
ЭСП в дихлорметане, λmax, нм: 700 (Фиг. 15).
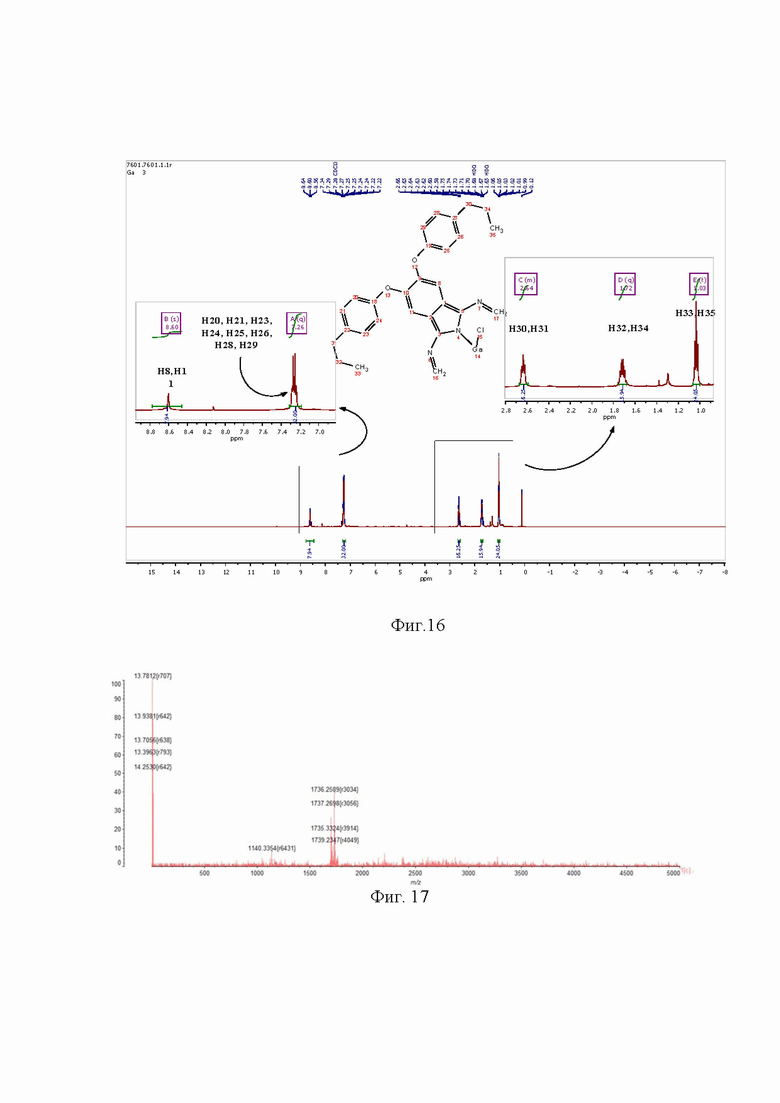
Спектр 1H ЯМР (500 МГц, CDCl3) δ 8,60 (s, 8H), 7,26 (q, 3J = 8,7 Гц, 32H), 2,67-2,59 (m, 16H), 1,72 (q, 3J = 7,4 Гц, 16H), 1,03 (t, 3J = 7,3 Гц, 24H) (Фиг. 16).
Пример 5. Использование 4,5-бис(4'-пропилфенокси)фталонитрила как промежуточного продукта для синтеза окта-4,5-(4'-пропилфенокси)-фталоцианина индия (III):
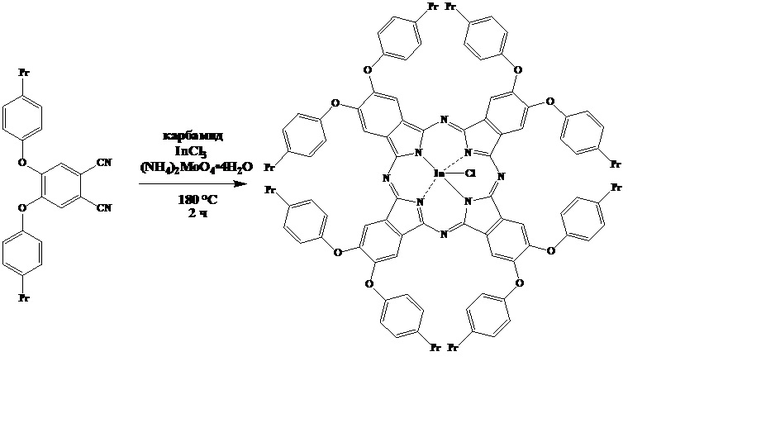
Смесь 0,100 г (0,00025 моль) 4,5-бис(4'-пропилфенокси)фталонитрила, 0,100 г (0,0017 моль) карбамида, 0,030 г (0,000024 моль) тетрагидрата молибдата аммония и 0,018 г (0,00008 моль) InCl3 нагревают при 180°C в течение 2 часов. Полученный осадок темно-зеленого цвета промывают горячим этанолом (40 мл), 5 %-ным раствором NaOH (20 мл) и горячей водой до нейтральной среды. Осадок высушивают на воздухе при 70°С, после чего очищают при помощи колоночной хроматографии на силикагеле, используя дихлорметан в качестве элюента.
Выход: 27 мг (29%).
Найдено, %: C - 72,05; H - 5,7; N - 6,57; C104H96ClInN8O8.
Вычислено, %: C - 71,95; H - 5,57; N - 6,45.
Масс-спектр, m/z = 1738,36[M+2H], 1703,66 [M-Cl], вычислено - 1736,19 (Фиг. 17).
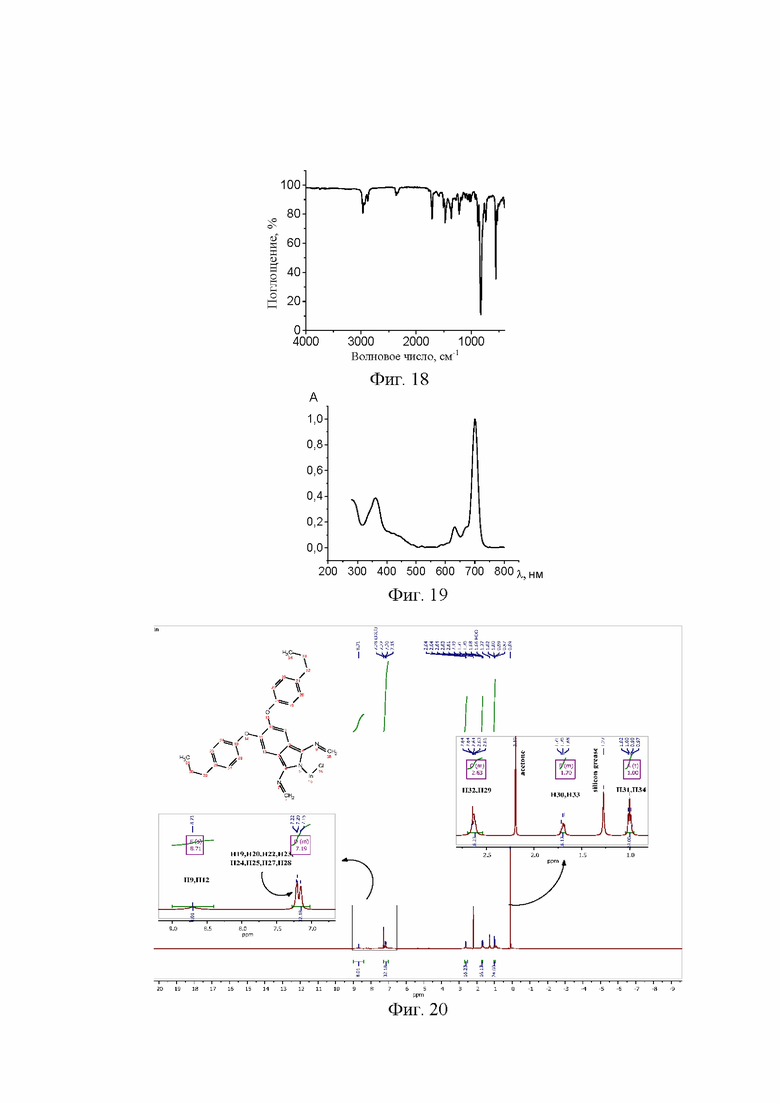
ИК спектр, см-1: 556, 737, 829, 1219 (Ar-O-Ar), 1362, 1474(C-H), 1713, 2874(C-H), 2967(C-H) (Фиг. 18).
ЭСП в дихлорметане, λmax , нм: 700,5 (Фиг. 19).
Спектр 1H ЯМР (500 МГц, CDCl3) δ 8,71 (s, 8H), 7,28-7,02 (m, 32H), 2,63 (t, 3J = 7,8 Гц, 16H), 1,73-1,67 (m, 16H), 1,00 (t, 3J = 7,3 Гц, 24H) (Фиг. 20).
Пример 6. Возможность использования окта-4,5-(4'-пропилфенокси)фталоцианина и его комплексов с алюминием (III), галлием (III) и индием (III) в качестве материалов, проявляющих флуоресцентные свойства:
Квантовые выходы флуоресценции соединений в дихлорметане оценивали путем сравнения со стандартом с известным квантовым выходом с использованием уравнения (1). В качестве стандарта использовали раствор фталоцианина цинка в бензоле (Φ = 0.30) [Brouwer A.M. Standards for photoluminescence quantum yield measurements in solution (IUPAC Technical Report // Pure Appl. Chem. - 2011. - Т. 83. - С. 2213-2228].
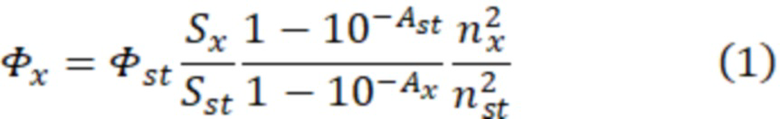
Где Φ - квантовый выход флуоресценции, S - интегральная площадь под спектром флуоресценции, A - оптическая плотность на длине волны возбуждения, n - показатель преломления растворителя. Индексы x и st относятся к измеряемому образцу и стандарту соответственно.
Результаты определения квантового выхода флуоресценции для соединений представлены в таблице 1.
Таблица 1
| название | год | авторы | номер документа |
|---|---|---|---|
| 4,5-БИС-(1',2':3',4'-ДИ-О-ИЗОПРОПИЛИДЕН-α-D-ГАЛАКТОПИРАНОЗО-6'-ИЛ)ФТАЛОНИТРИЛ | 2009 |
|
RU2409585C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ОКТА-4,5-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ФТАЛОЦИАНИНА В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНЫХ МАТЕРИАЛОВ И КРАСИТЕЛЕЙ ДЛЯ ПОЛИМЕРНЫХ МАТЕРИАЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2641743C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ОКТА-4,5-(4-СУЛЬФОФЕНИЛСУЛЬФАНИЛ)ФТАЛОЦИАНИНА С МЕДЬЮ, ЦИНКОМ И КОБАЛЬТОМ | 2017 |
|
RU2640303C1 |
| 4-(4-МЕТОКСИФЕНОКСИ)-5-НИТРОФТАЛОНИТРИЛ И ТЕТРА-4-[(4-МЕТОКСИФЕНОКСИ)-5-НИТРО]ФТАЛОЦИАНИНЫ МЕДИ, КОБАЛЬТА И ЦИНКА НА ЕГО ОСНОВЕ | 2023 |
|
RU2830011C1 |
| 5,6-БИС-(1',2':3',4'-ДИ-О-ИЗОПРОПИЛИДЕН-α-D-ГАЛАКТОПИРАНОЗО-6'-ИЛ)-1,3-ДИИМИНОИЗОИНДОЛИН | 2009 |
|
RU2409586C1 |
| 4-ТРЕТ-БУТИЛ-5-НИТРОФТАЛОНИТРИЛ | 2012 |
|
RU2495025C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(2,4,5-ТРИХЛОРФЕНОКСИ)ФТАЛОНИТРИЛА | 2017 |
|
RU2684113C1 |
| 4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]-5-НИТРОФТАЛОНИТРИЛ | 2016 |
|
RU2620381C1 |
| ТЕТРА-4-[4-(2,4,5-ТРИХЛОР-3,6-ДИСУЛЬФОФЕНОКСИ)]-ФТАЛОЦИАНИНЫ МЕДИ И КОБАЛЬТА | 2017 |
|
RU2659224C1 |
| ТЕТРА-4-[4-(2,4,5-ТРИХЛОРФЕНОКСИ)]ФТАЛОЦИАНИН МЕДИ | 2017 |
|
RU2667915C1 |
Изобретение относится к области химической промышленности, а именно к производному фталонитрила - 4,5-бис(4'-пропилфенокси)фталонитрилу, который может быть использован в качестве полупродукта в синтезе окта-4,5-(4'-пропилфенокси)фталоцианина и его комплексов с алюминием (III), галлием (III) и индием (III), проявляющих флуоресцентные свойства. Заявлены окта-4,5-(4'-пропилфенокси)фталоцианин и его комплексы с алюминием (III), галлием (III) и индием (III) общей формулы: 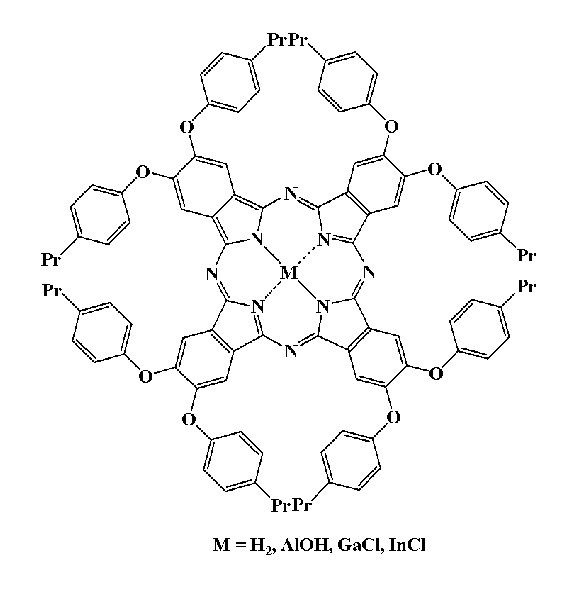 и 4,5-бис(4'-пропилфенокси)фталонитрил формулы:
и 4,5-бис(4'-пропилфенокси)фталонитрил формулы: 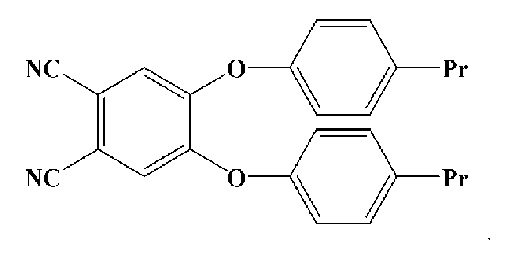 Изобретение позволяет получить новые соединения, обладающие флуоресцентными свойствами, и промежуточный продукт для синтеза таких соединений. 2 н.п. ф-лы, 20 ил., 1 табл., 6 пр.
Изобретение позволяет получить новые соединения, обладающие флуоресцентными свойствами, и промежуточный продукт для синтеза таких соединений. 2 н.п. ф-лы, 20 ил., 1 табл., 6 пр.
1. Окта-4,5-(4'-пропилфенокси)фталоцианин и его комплексы с алюминием (III), галлием (III) и индием (III) общей формулы:
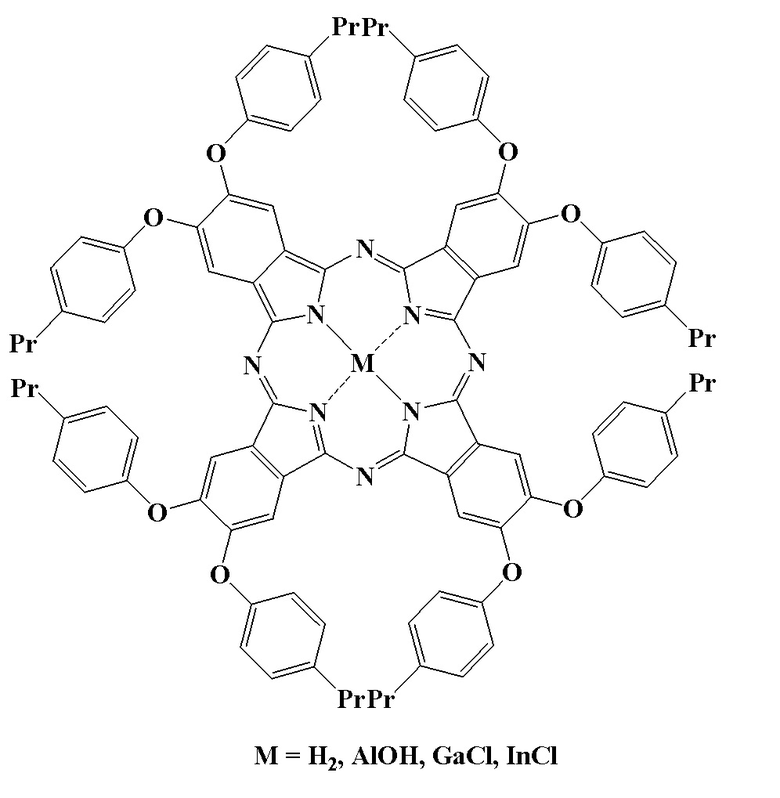
2. 4,5-Бис(4'-пропилфенокси)фталонитрил формулы:
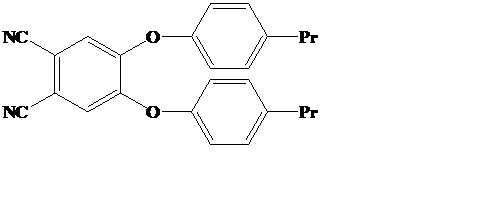
| МЕТАЛЛОКОМПЛЕКСЫ ОКТА-4,5-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ФТАЛОЦИАНИНА В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНЫХ МАТЕРИАЛОВ И КРАСИТЕЛЕЙ ДЛЯ ПОЛИМЕРНЫХ МАТЕРИАЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2641743C1 |
| JAMOUSSI B | |||
| et al | |||
| Hybrid Zinc Phthalocyanine/PVDF-HFP System for Reducing Biofouling in Water Desalination: DFT Theoretical and MolDock Investigations, Polymers, 19.06.2024, v | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| ZIMCIK P | |||
| et al | |||
| Magnesium Azaphthalocyanines: As Emerging Family of Excellent Red-Emittimg Fluorophores, Inorganic Chemistry, 2012, | |||
Авторы
Даты
2025-03-24—Публикация
2024-11-25—Подача