Изобретение относится к химической промышленности, а именно к получению новых производных фталоцианина, конкретно, металлокомплексов тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианины меди и кобальта, которые:
1) Обладают красящей способностью по отношению к полистиролу, вискозе и капрону;
2) Могут быть использованы в качестве исходных соединений для синтеза металлокомплекса сульфокислот тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианинов с кобальтом, проявляющего каталитическую активность при окислении серосодержащих органических соединений.
Известен тетра-4-феноксифталоцианин [Быкова В.В., Усольцева Н.В., Ананьева Г.А., Майзлиш В.Е., Шапошников Г.П. Мезоморфизм тетра-4-арилоксизамещенных фталоцианина меди // Изв. АН. Серия физическая. 1998. Т. 62. №8. С. 1647-1651.]
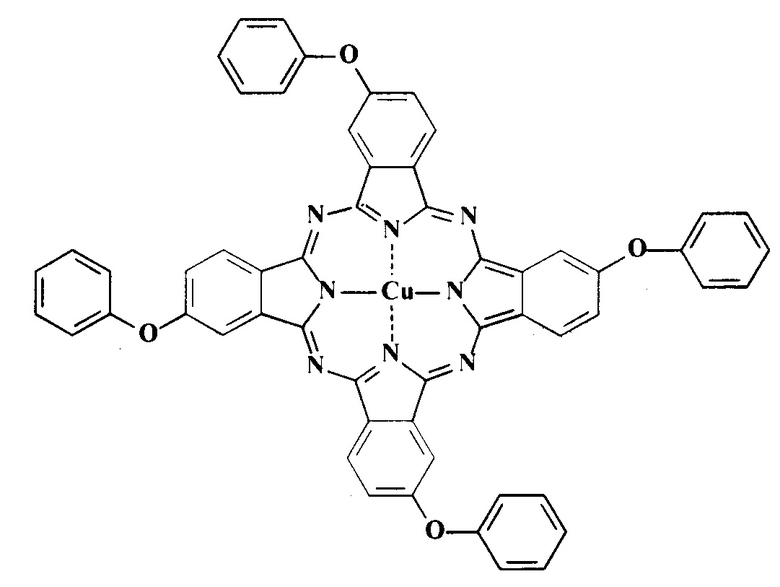
Однако тетра-4-феноксифталоцианин меди, который обладает ограниченной растворимостью в органических растворителях, и при крашении полимерных материалов не позволяет получить насыщенный цвет и равномерные окраски, независимо от количества красителя.
Кроме того, ничего не известно о возможности использования данного соединения в качестве исходных для получения металлокомплексов фталоцианина, обладающих красящей способностью по отношению к шерстяным волокнам и проявляющих каталитическую активность при окислении серосодержащих органических соединений.
Кроме того, известен тетра-3-(2,4-дихлорфенокси)фталоцианин палладия [Hai-Tao Xu, Wen-Wei Xie, Yan-Chuan Guo, Ying Ci, Li-Juan Chen, Bi-Xian Peng. The Synthesis of Tetra-α-phenoxyphthalocyanines and Research of their Physical and Chemical // Properties Journal of the Chinese Chemical Society. 2007, V. 54, pp. 211-217].
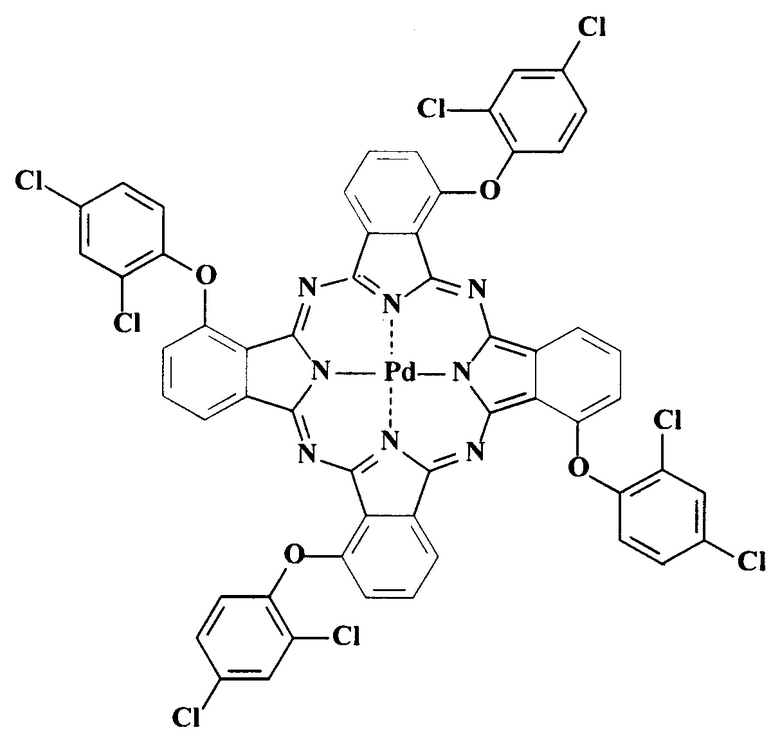
При этом в литературе отсутствуют сведения о проявлении тетра-3-(2,4-дихлорфенокси)фталоцианин палладия красящей способностью по отношению к полистиролу, вискозе и капрону.
Кроме того, данные соединения не могут быть использованы в качестве исходных для получения металлокомплексов фталоцианина с медью, обладающего красящей способностью по отношению к шерстяным волокнам и хлопку, и с кобальтом, проявляющего каталитическую активность при окислении серосодержащих органических соединений.
Изобретательская задача состояла в поиске нового соединения, обладающего красящей способностью по отношению к полистиролу, вискозе и капрону, которое является исходным соединением в синтезе металлокомплекса фталоцианина с кобальтом, проявляющего каталитическую активность при окислении серосодержащих органических соединений.
Поставленная задача решена синтезом тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианины меди и кобальта общей формулы:
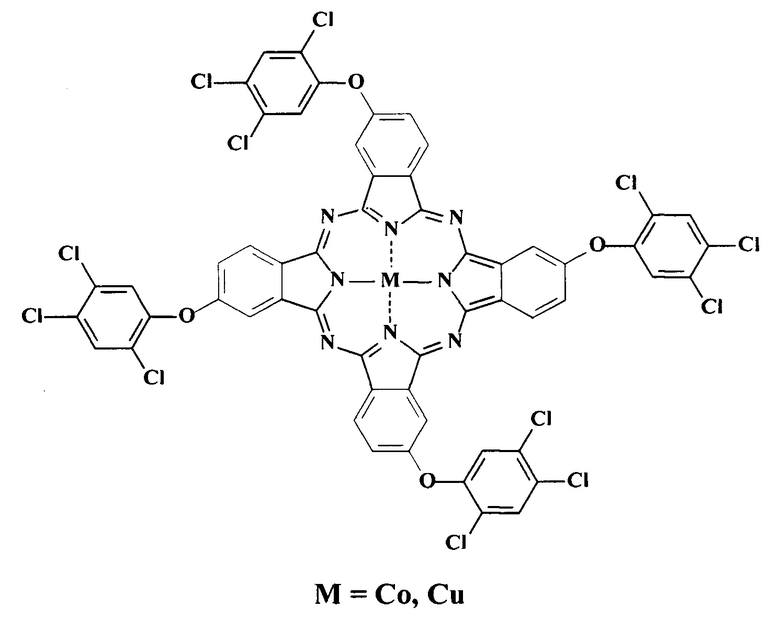
Структура этих соединений доказана данными элементного анализа, ИК и электронной спектроскопии, MALDI-TOF спектрометрии.
Так, в ИК-спектрах заявляемых соединений присутствуют полосы, характерные для валентных колебаний соответствующих функциональных групп: 752-755 см-1 (С-Cl), 1249 см-1 (Ar-O-Ar) [Дайер Дж. Р. Приложение абсорбционной спектроскопии органических соединений / Пер. с англ. Иванова В.Т. М.: Химия. 1970. 164 с]. В масс-спектрах синтезированных металлокомплексов фталоцианинов с кобальтом и медью обнаружены сигналы целевых молекулярных ионов с m/z=1352; 1358, 1374 соответственно.
Краткое описание чертежей
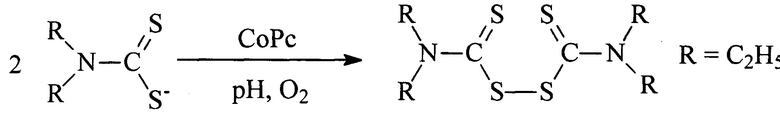
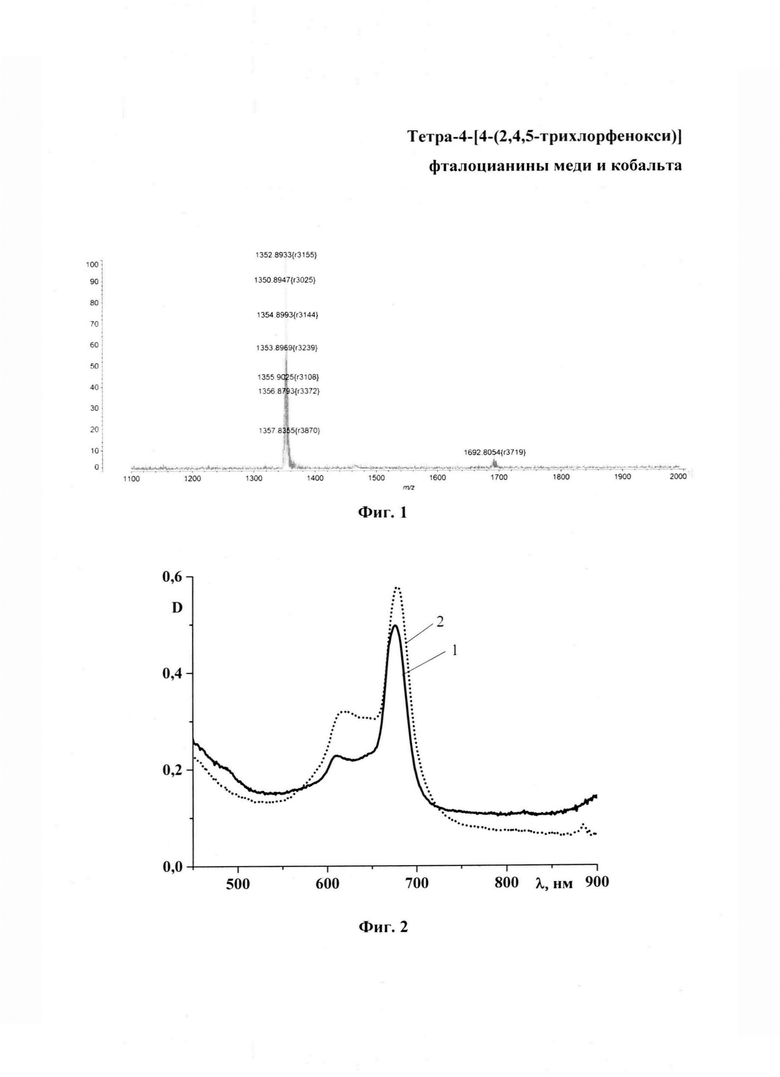
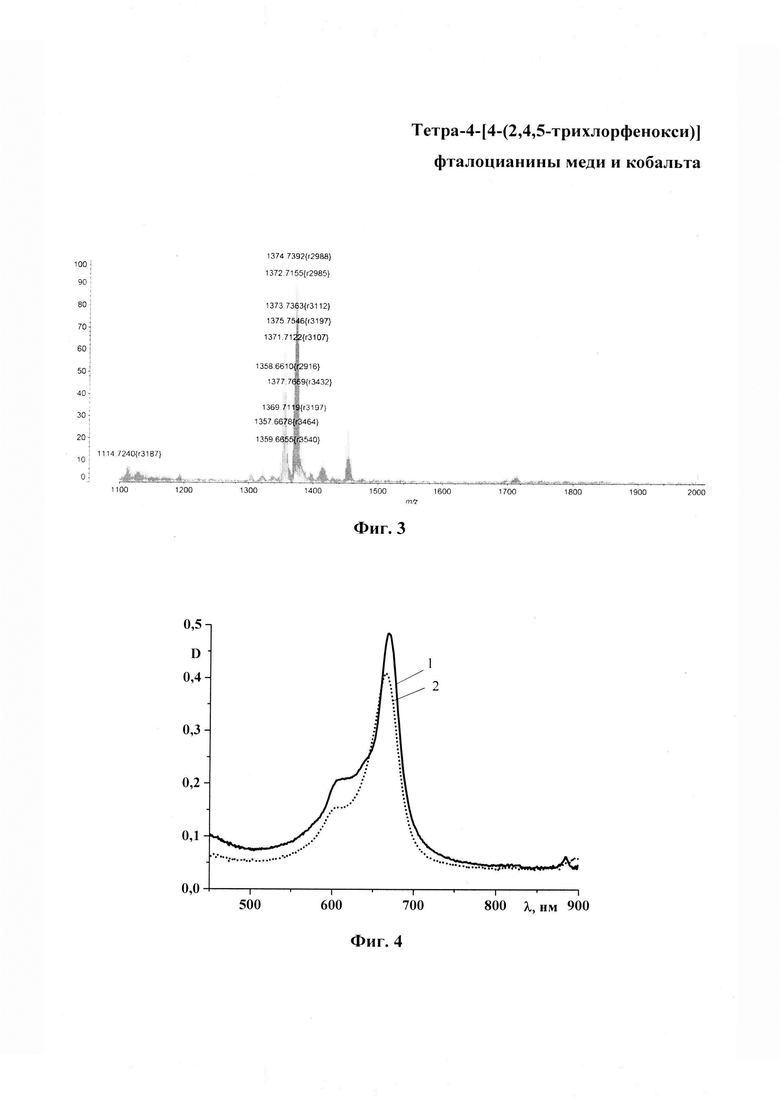
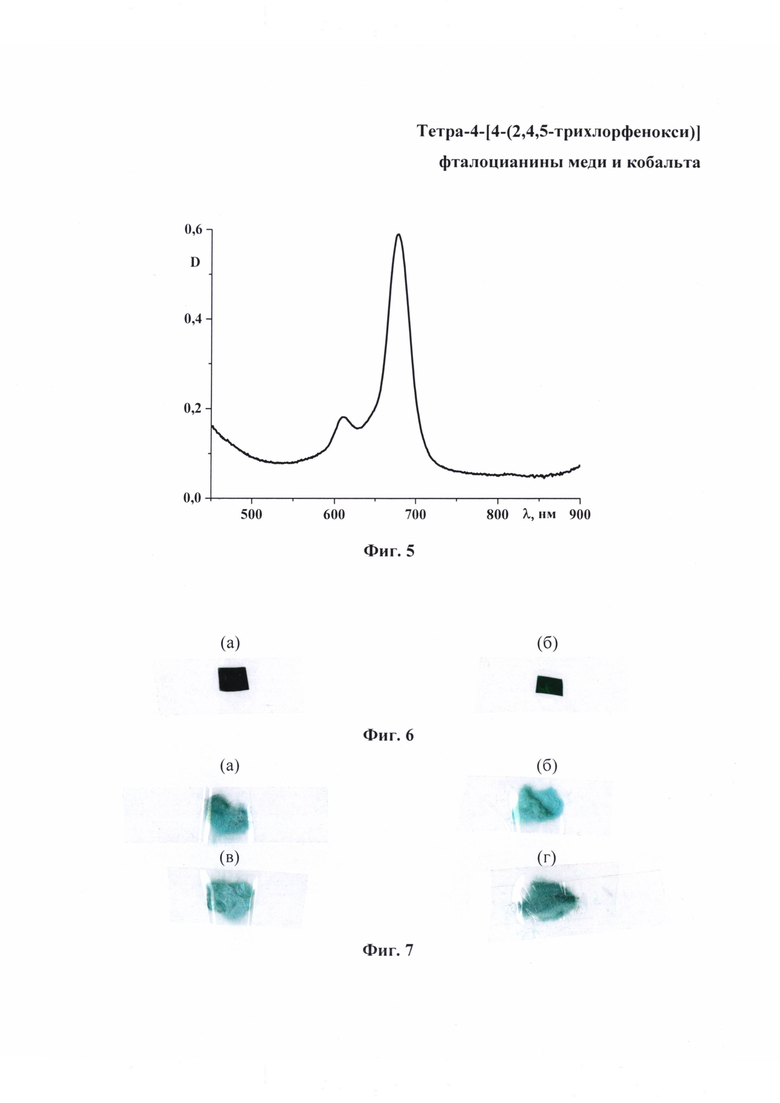
На фиг. 1 изображен MALDI-TOF масс-спектр тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина кобальта; на фиг. 2 - ЭСП тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина меди в ДМФА (кривая 1) и хлороформе (кривая 2); на фиг. 3 - MALDI-TOF масс-спектр тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина меди; на фиг. 4 - ЭСП тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина кобальта в ДМФА (кривая 1) и хлороформе (кривая 2); на фиг. 5 - ЭСП тетра-4-[4-(2,4,5-трихлор-3,6-дисульфофенокси)]фталоцианина кобальта в ДМФА; на фиг. 6 - образцы полистирола, полученные по примеру 4, окрашенные (а) - тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианином кобальта, (б) - тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианином меди; на фиг. 7 - образцы полимерных волокон, полученные по примеру 5, окрашенных тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианином меди, где (а) - образец вискозы; (б) - образец капрона и тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианином кобальта, где (в) - образец вискозы; (г) - образец капрона.
Изобретение позволяет получить следующие преимущества:
1) Обладают красящей способностью по отношению к полистиролу, вискозе и капрону;
2) Применяемость заявляемых соединений для синтеза водорасторимого фталоцианина иллюстрируется получением металлокомплекса тетра-4-[4-(2,4,5-трихлор-3,6-дисульфофенокси)]фталоцианина кобальта с выходом 70%, проявляющего каталитическую активность при окислении серосодержащих органических соединений.
Для синтеза заявляемого соединения используют следующие вещества:
- ацетат кобальта - ГОСТ 5861 - 79;
- ацетат меди - ГОСТ 5852-79
- 4-(2,4,5-трихлорфенокси)фталонитрил, однако, поскольку это соединение является новым и не выпускается промышленностью, оно было получено следующим способом: из 4-нитрофталодинитрила [31643-49-9 ACROS ORGANICS (Китай)] путем нуклеофильного замещения нитрогруппы на 2,4,5-трихлорфеноксигруппу, синтезируют целевой фталонитрил. Синтез осуществлялся следующим способом:
Синтез 4-(2,4,5-трихлорфенокси)фталонитрила:
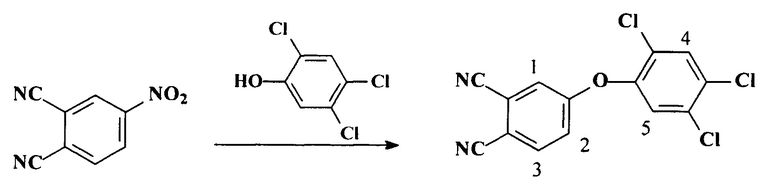
В 30 мл ДМФА растворяют 1.73 г (0.01 моль) 4-нитрофталонитрила и 1.97 г (0.01 моль) 2,4,5-трихлорфенола, к полученному раствору прибавляют раствор 2.76 г (0.02 моль) K2CO3 в 5 мл воды и перемешивают при 100°С в течение 3 часов. Полученный осадок отфильтровывают, промывают водой до рН=7 и высушивают на воздухе при 70-80°С.
Выход: 2.43 г (75%).
Найдено, %: С - 51.15, Н - 2.00, N - 8.74; C14H5Cl3N2O;
Вычислено: С - 51.97, Н - 1.56, N - 8.66.
Масс-спектр, m/z=362 [М+K]+, вычислено - 323.
ИК спектр, см-1: 2231 (C≡N), 1250 (Ar-O-Ar), 772 (С-Cl).
ЯМР 1Н спектр, δ, м.д.: 7.80 д (1Н; Н3), 7.69 с (1Н; H1), 7.33 с (1Н; Н2), 7.28 м (1Н; Н4), 7.24-7.22 м (1Н; Н5).
Заявляемое соединение может быть получено следующим образом.
Пример 1. Синтез тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина меди
Тщательно растертую смесь 0.32 г (1 ммоль) 4-(2,4,5-трихлорфенокси)фталонитрила и 0.036 г (0.17 моль) (СН3СОО)2Cu *2H2O нагревают при 190°С в течение 10 часов. По окончании процесса реакционную массу охлаждают, растирают в ступке и растворяют в концентрированной серной кислоте. Полученный раствор выливают на лед, образовавшийся осадок отфильтровывают и промывают водой до рН 7, высушивают на воздухе при 70-70°С. Целевой продукт экстрагируют хлороформом и подвергают колоночной хроматографии на силикагеле М60, элюируя хлороформом. Получено твердое вещество темно-зеленого цвета, не растворимое в воде, хорошо растворимое в хлороформе и ДМФА.
Выход: 0.29 г. (85%).
Найдено, %: С - 49.10, Н - 1.74 N - 8.12; C56H20Cl12CuN8O4;
Вычислено: С - 49.54, Н - 1.48, N - 8.25.
Масс-спектр, m/z=1358 [М+Н]+, 1374 [М+Na]+, вычислено - 1357 (Фиг. 1)
ИК спектр, (KBr)/см-1: 752 (С-Cl), 1249 (Ar-О-Ar).
ЭСП в ДМФА, λmax, нм, 676 (Фиг. 2, кривая 1); ЭСП в хлороформе, λmax, нм, 620, 678 (Фиг. 2, кривая 2).
Пример 2. Синтез тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина кобальта
Тщательно растертую смесь 0.32 г (1 ммоль) 4-(2,4,5-трихлорфенокси)фталонитрила и 0.033 г (0.17 моль) (СН3СОО)2Со *2H2O нагревают при 190°С в течение 10 часов. По окончании процесса реакционную массу охлаждают, растирают в ступке и растворяют в концентрированной серной кислоте. Полученный раствор выливают на лед, образовавшийся осадок отфильтровывают и промывают водой до рН 7, высушивают на воздухе при 70°С. Целевой продукт экстрагируют хлороформом и подвергают колоночной хроматографии на силикагеле М60, элюируя хлороформом. Получено твердое вещество темно-зеленого цвета, не растворимое в воде, хорошо растворимое в хлороформе и ДМФА.
Выход: 0.26 г. (78%).
Найдено, %: С - 49.41, Н - 1.75, N - 8.02; C56H20Cl12CoN8O4;
Вычислено: С - 49.71, Н - 1.49, N - 8.28.
Масс-спектр, m/z=1352 [М]+, вычислено - 1353 (Фиг. 3).
ИК спектр, (KBr)/см-1: 755 (С-Cl), 1249 (Ar-О-Ar).
ЭСП в ДМФА, λmax, нм, 665 (Фиг. 4, кривая 1); ЭСП в хлороформе, λmax, нм, 668 (Фиг. 4, кривая 2).
Пример 3. Использование тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина кобальта в качестве исходного соединения для синтеза тетра-4-[4-(2,4,5-трихлор-3,6-дисульфофенокси)]фталоцианина кобальта
Тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианин кобальта (405 мг, 0.3 ммоль) подвергают взаимодействию с 10 мл (24 ммоль) 26% олеума при температуре 90°С в течение 6 часов. По окончании перемешивания реакционную смесь выливают на лед, обработанный хлористым натрием. Выпавший осадок собирают на фильтре Шотта, промывают концентрированной соляной кислотой до бесцветных фильтратов и высушивают в эксикаторе над серной кислотой в течение 3 суток. Окончательная очистка осуществляется колоночной хроматографией: элюент - ДМФА, сорбент - силикагель М 60.
Полученные продукты - твердые вещества темно-зеленого цвета, растворимые в воде, аммиаке, водно-щелочных растворах, ДМФА.
Выход: 420 мг (70%).
Найдено, %: С 33.41, Н 1.10, N 5.56, S 12.38; C56H20Cl12CoN8O28S8.
Вычислено: С 33.74, Н 1.01, N 5.62, S 12.86.
ИК спектр (KBr)/см-1: 742 (С-Cl), 1167, 1042 (S=O), 1069 (C-S), 1240 (Ar-О-Ar).
ЭСП в ДМФА, λmax, нм, 678 (Фиг. 5).
Пример 4. Использование тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианинов меди и кобальта в качестве жирорастворимого красителя для крашения полистирола.
0.1 г полистирола растворяли при нагревании в 1 мл хлороформа и добавляли 1 мл хлороформа, в котором растворено 0.002 г тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина меди и кобальта. Раствор кипятили в течение 3 минут и полученную массу выливали в форму.
Образцы прилагаются (Фиг. 6).
Пример 5. Использование тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианинов меди и кобальта в качестве красителя для капрона и вискозы
0.002 г Тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианина меди или кобальта растворяли при нагревании в 5 мл хлороформа и добавляли 25 мг синтетического волокна (капрон, вискоза). Раствор кипятили в течение 3 минут, окрашенное волокно отжимали и сушили на воздухе.
Образцы прилагаются (Фиг. 7).
Пример 6. Использование тетра-4-[4-(2,4,5-трихлор-3,6-дисульфофенокси)]фталоцианина кобальта в качестве гомогенного катализатора окисления соединений серы
 i
i
Каталитическую активность оценивают по величине эффективной константы скорости окисления N,N-диэтилдитиокарбамата натрия (ГОСТ 8864-71) кислородом воздуха при рН 7.6 и температуре 30°С (kэф). Окисление ведут при нормальном давлении в металлическом реакторе периодического действия объемом 650 мл, снабженном термометром, обратным холодильником, отводом для отбора проб и барботером для подачи воздуха со скоростью - 2 л/мин, обеспечивающей протекание процесса в кинетическом режиме. В реактор загружают 600 мл раствора N,N-диэтилдитиокарбамата натрия с концентрацией 0.1 г/л. Для определения текущей концентрации диэтилдитиокарбамата натрия пробу объемом 2 мл переносят в колбу на 25 мл и добавляют 4 мл 0,02 н CuSO4. Раствор сульфата меди готовят, используя реактив в соответствии с ГОСТ 19347-99. При добавлении сульфата меди к отобранной пробе образуется густой темно-коричневый осадок медного комплекса. Смесь перемешивают одну минуту. Затем к полученному раствору добавляют 5 мл хлороформа, 3 капли 50% уксусной кислоты и взбалтывают 1.5 минуты. Медный комплекс диэтилдитиокарбамата экстрагируют в слой хлороформа. Органический слой переносят в мерную колбу объемом 25 мл, а из оставшегося водного раствора комплекс экстрагируют повторно для повышения точности анализа. Собранный раствор медного комплекса доводят до метки хлороформом. Из этой колбы отбирают 2 мл раствора, переносят в другую мерную колбу объемом 25 мл и снова доводят до метки хлороформом. На спектрофотометре при длине волны 436 нм определяют оптическую плотность раствора и рассчитывают концентрацию N,N-диэтилдитиокарбамата на основании калибровочной прямой.
Каталитическая активность тетра-4-[4-(2,4,5-трихлор-3,6-дисульфофенокси)]фталоцианина кобальта измеренная при концентрации катализатора 6*10-5 моль/л и субстрата 0,00203 моль/л может быть оценена с помощью эффективной константы скорости окисления диэтилдитиокарбамата натрия, измеренная при рН=7.6, которая составляет 41.97 10-3 л/(моль с).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 4-(2,4,5-ТРИХЛОРФЕНОКСИ)ФТАЛОНИТРИЛА | 2017 |
|
RU2684113C1 |
| ТЕТРА-4-[4-(2,4,5-ТРИХЛОР-3,6-ДИСУЛЬФОФЕНОКСИ)]-ФТАЛОЦИАНИНЫ МЕДИ И КОБАЛЬТА | 2017 |
|
RU2659224C1 |
| 4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]-5-НИТРОФТАЛОНИТРИЛ | 2016 |
|
RU2620381C1 |
| ТЕТРА-4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ТЕТРА-5-НИТРОФТАЛОЦИАНИНЫ КОБАЛЬТА И НИКЕЛЯ | 2016 |
|
RU2620270C1 |
| ТЕТРА-4-{ 4-[1-МЕТИЛ-1-(4-СУЛЬФОФЕНИЛ)ЭТИЛ]ФЕНОКСИ} -ТЕТРА-5-НИТРОФТАЛОЦИАНИН КОБАЛЬТА | 2016 |
|
RU2622290C1 |
| 4-(4-МЕТОКСИФЕНОКСИ)-5-НИТРОФТАЛОНИТРИЛ И ТЕТРА-4-[(4-МЕТОКСИФЕНОКСИ)-5-НИТРО]ФТАЛОЦИАНИНЫ МЕДИ, КОБАЛЬТА И ЦИНКА НА ЕГО ОСНОВЕ | 2023 |
|
RU2830011C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ОКТА-4,5-(4-СУЛЬФОФЕНИЛСУЛЬФАНИЛ)ФТАЛОЦИАНИНА С МЕДЬЮ, ЦИНКОМ И КОБАЛЬТОМ | 2017 |
|
RU2640303C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ОКТА-4,5-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ФТАЛОЦИАНИНА В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНЫХ МАТЕРИАЛОВ И КРАСИТЕЛЕЙ ДЛЯ ПОЛИМЕРНЫХ МАТЕРИАЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2641743C1 |
| 4-ТРЕТ-БУТИЛ-5-НИТРОФТАЛОНИТРИЛ | 2012 |
|
RU2495025C1 |
| 4-(3'-МЕТОКСИФЕНОКСИ)-5-ХЛОРФТАЛОНИТРИЛ И ТЕТРА-[4-(3'-МЕТОКСИФЕНОКСИ)-5-ХЛОР]ФТАЛОЦИАНИНЫ МЕДИ, КОБАЛЬТА НА ЕГО ОСНОВЕ | 2024 |
|
RU2839463C1 |
Изобретение относится к тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианину меди общей формулы:
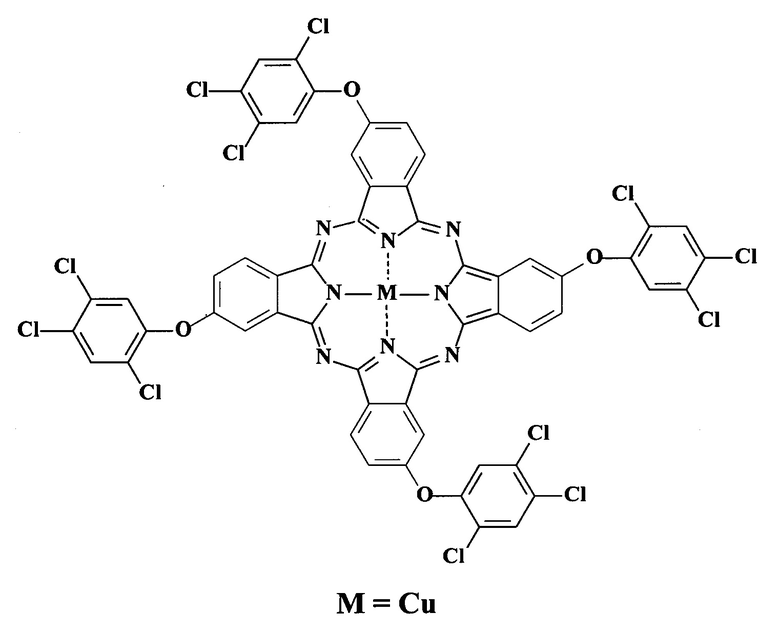 .
.
Тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианин меди обладает красящей способностью по отношению к полистиролу, вискозе и капрону. 6 пр., 7 ил.
Тетра-4-[4-(2,4,5-трихлорфенокси)]фталоцианин меди общей формулы:
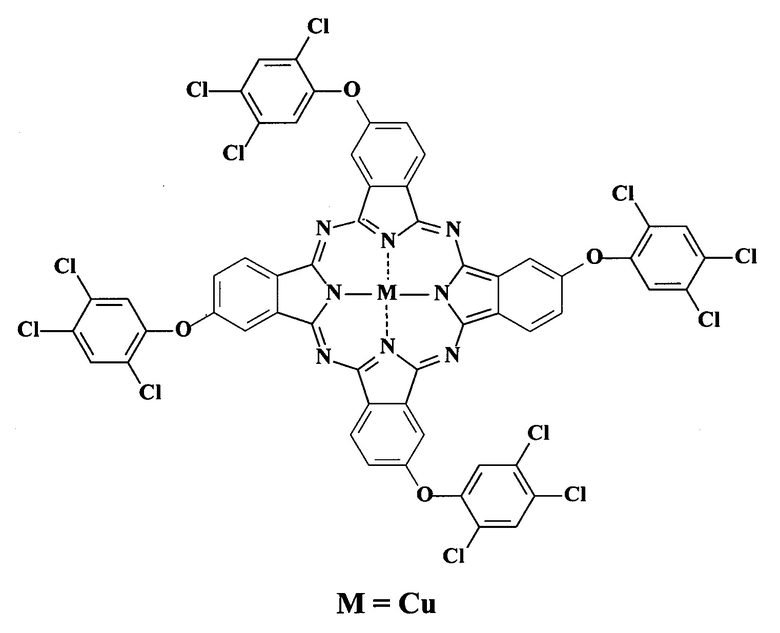
| ЧЕСНОВ А.А., 4-(2,4,5-трихлорфенокси)фталонитрил и фталоцианин на его основе, Молодая наука в классическом университете: тезисы докладов научных конференций фестиваля студентов, аспирантов и молодых ученых, Иваново, Иван | |||
| гос | |||
| ун-т, 17.04.2017, с | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| KR 101478296 B1, 31.12.2014 | |||
| XU Hai-Tao et al, The Synthesis of Tetra-alpha-phenoxyphthalocyanines and Research of their Physical and Chemical Properties, Journal of the Chinese Chemical Society, 2007, v | |||
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| Способ добывания бензина и иных продуктов из нефти, нефтяных остатков и пр. | 0 |
|
SU211A1 |
Авторы
Даты
2018-09-25—Публикация
2017-12-20—Подача