Способ получения 3-метилсульфолана относится к способам получения органических растворителей и может быть использован для извлечения ароматических соединений из углеводородных смесей в нефтехимической и нефтеперерабатывающей промышленности.
Сульфолан и алкилсульфоланы используются в качестве растворителей в процессах экстракции и экстрактивной ректификации при выделении бензола, толуола и ксилолов из смесей углеводородов, растворителей четвертичных аммониевых оснований, нитроцеллюлозы и некоторых полимерных соединений, выступают в качестве промежуточных продуктов для производства средств борьбы с вредителями и т.д.
Фирма Glitch Technology Corporation (GTC) в 1990-е годы разработала процесс, в котором предложено выделять бензол и его гомологи экстрактивной ректификацией с использованием смесей сульфолана с алкилсульфоланами, содержащими до 8 атомов углерода, например, смеси 10-25 % мас. сульфолана и 90-75 % мас. 3-метилсульфолана. В качестве второго компонента, повышающего растворяющую способность сульфолана, целесообразно использовать именно 3-метилсульфолан, так как селективность алкилсульфоланов с более длинными алкильными заместителями быстро снижается [А.А. Гайле, И.А. Соловых. Снижение содержания бензола в автомобильных бензинах методом экстрактивной ректификации. Известия СПбГТИ (ТУ), выпуск № 18 (44), 2013, с. 32-42].
Известно, что 3-метилсульфолан (3-метил-1,1-тетрагидротиофен) может быть получен аналогично сульфолану по реакции Дильса-Альдера с использованием изопрена и представляет собой апротонный, сильно полярный, водорастворимый органический растворитель многих органических соединений, обладает высокой химической и термической стабильностью, способностью к восстановлению, высокой селективностью, относительно слабой коррозионной активностью и низкой токсичностью. Область применения 3-метилсульфолана преимущественно связана с использованием в качестве растворителя в промышленных процессах выделения ароматических соединений, например, из риформата бензина, что обеспечивает высокий рыночный потенциал.
Известен способ получения 3-метилсульфолана, включающий следующие стадии: 1) используя изопрен и серосодержащие соединения в качестве сырья, соли металлов в качестве катализаторов и ароматические кетоны в качестве сокатализаторов, проводят реакцию циклизации с получением реакционного раствора, содержащего 3-метилциклобутенилсульфон; 2) после десульфурации и нейтрализации вышеуказанной реакционной жидкости проводят реакцию гидрирования под действием катализатора гидрирования с получением 3-метилсульфолана (патент CN116283898, МПК C07D 333/48, заявлен 07.12.2022, опубликован 23.06.2023). Недостатками изобретения являются:
- использование в качестве растворителя гексафторизопропанол, который является дорогостоящим и труднодоступным компонентом;
- применение катализатора металлата (пированадат калия, бисульфат калия, ванадат висмута и др.) и сокатализатора (бензантрон, тимохинон, бензофенон и др.) на стадии взаимодействия пиросульфита натрия с изопренсодержащей жидкостью, образующейся в ходе проведения реакции Сауси-Марбе (содержание изопрена 80-94 %), что неизбежно приводит к удорожанию процесса;
- применение катализатора и сокатализатора на стадии синтеза 3-метилсульфолена обуславливает необходимость дополнительных операций промывки в вакууме этанолом от 3 до 5 раз, нейтрализации избытком щелочи, а также стадий фильтрации и перегонки для извлечения катализатора и сокатализатора. Таким образом, в способе необходимо использовать довольно сложную систему разделения, что повлечет потери ценного целевого продукта.
Известен способ получения сульфоланового соединения, включающий на первой стадии взаимодействие сопряженного диенового соединения, представленного следующей формулой (1), с диоксидом серы с получением сульфоленового соединения, представленного следующей формулой (2). На второй стадии остаточный диоксид серы удаляют путем подачи воздуха со скоростью от 2500 мл/мин. Температура жидкости при введении воздуха в раствор сульфоленового соединения составляет от 20 до 150°С. Способ получения сульфоланового соединения, представленного следующей формулой (3), по настоящему изобретению включает стадию 3 гидрирования сульфоленового соединения, представленного формулой (2), в присутствии катализатора гидрирования.
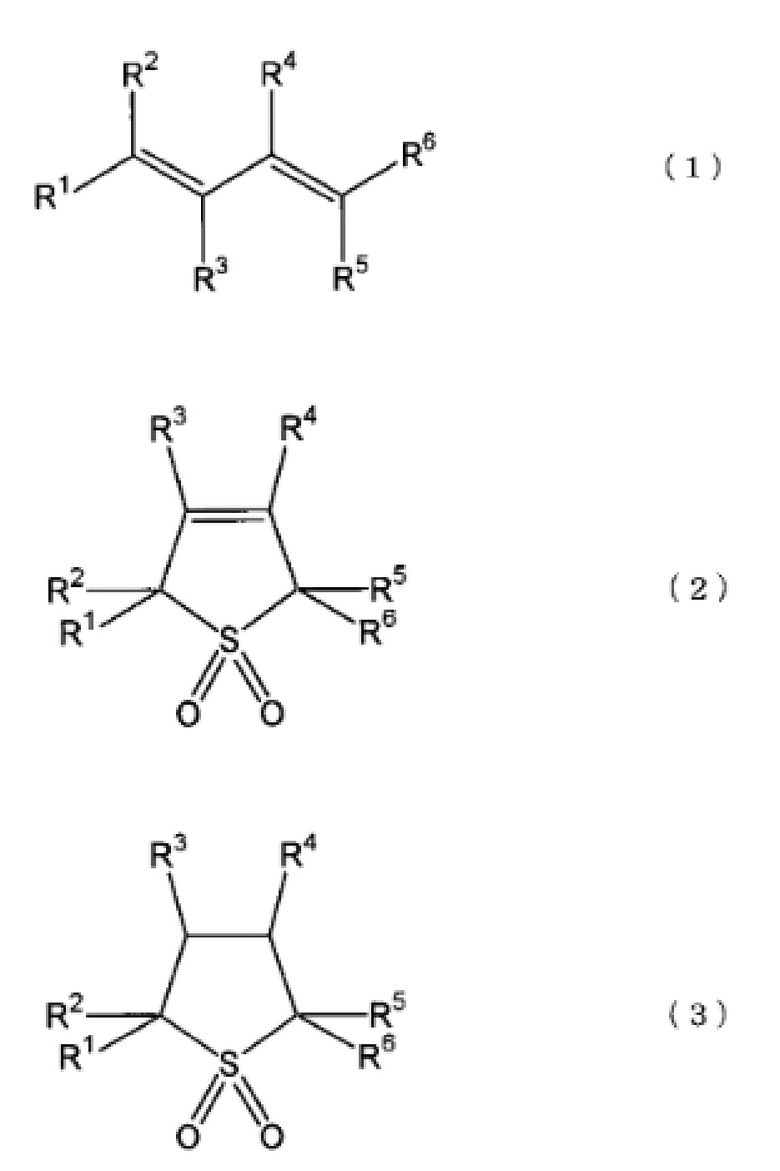
В формуле (1) каждый из R1-R6 независимо представляет собой атом водорода или алкильную группу, имеющую от 1 до 6 атомов углерода. В формуле (2) от R1 до R6 представляют те же группы, что и от R1 до R6 в формуле (1). В формуле (3) от R1 до R6 представляют те же группы, что и от R1 до R6 в формуле (1) (патент JP2012158543, МПК C07D 333/48, заявлен 31.01.2011, опубликован 23.08.2012). Недостатками данного изобретения являются условия подачи исходных реагентов в газообразном виде и условия реакции синтеза сульфолена в автоклаве (температура 100°С и высокое давление 2,7-0,7 МПа), которые обуславливают высокую энергоемкость способа.
Известен также наиболее близкий к заявляемому изобретению способ получения 3-метилсульфолана, отличающийся тем, что в реактор вводится гидрохинон в качестве ингибитора полимеризации в условиях защиты азота, затем последовательно добавляют жидкий диоксид серы и изопрен, при этом молярное отношение жидкой двуокиси серы к изопрену составляет 1,2 : 1,0 и нагревают до температуры 80°С, по достижении температуры 80°С нагрев прекращают, при этом температура реакции циклизации продолжает подниматься при медленном перемешивании в течение 20 минут без охлаждения водой, и в это время в реакционную зону подается вода в качестве растворителя для регулирования температуры путем охлаждения реакционной системы до температуры от 90°С до 100°С и перемешивание продолжается в течение 20 минут для получения сырого сульфолена; добавляют воду для разбавления сырого сульфолена, флоккулированный осадок отфильтровывают и затем флоккулированный осадок переносят в реактор гидрирования, работающий под азотной подушкой, добавляют никелевый катализатор Ренея, перемешивают и вводят водород высокой чистоты в реактор для осуществления реакции для реакции гидрирования; при этом давление водорода составляет 2,0 МПа, температура в зоне реакции гидрирования ниже 70°С для поддержания температуры используется охлаждающая вода, когда давление подачи водорода достигает 3,0 МПа подачу воды прекращают, реакция завершается, продукт фильтруют, обезвоживают и выделяют в концентрированном виде (патент CN101875651, МПК C07D 333/48, заявлен 28.04.2009, опубликован 03.11.2010). Недостатками изобретения являются:
- жесткие условия реакции, когда давление в реакционном аппарате поддерживается на уровне 2,5-3,0 МПа, обуславливая высокую энергозатратность способа;
- использование в качестве растворителя воды в значительном объеме требует поддержания в реакционной системе высокого давления, усложняет процесс проведения реакции и разделения продуктов в связи с образованием гетерогенной системы «вода-изопрен», при этом SO2 растворяется в воде с образованием сернистой кислоты, интенсифицируя коррозию аппаратуры;
- существенные потери дорогостоящего катализатора никеля Ренея, приводящие к росту себестоимости продукта.
Целью настоящего изобретения является разработка способа получения 3-метилсульфолана на основе изопрена в результате реакции циклизации изопрена с диоксидом серы с последующим гидрированием соответствующего 3-метилсульфолена до 3-метилсульфолана с обеспечением высокого выхода и высокой чистоты целевого продукта, при этом предлагаемый способ позволяет исключить генерацию большого количества органических отходов, потерь растворителя, повысить эффективность использования серы и является подходящим для промышленного производства.
Поставленная задача решается за счет того, что разработан способ получения 3-метилсульфолана, включающий стадии:
а) сжигают серу в среде концентрированного кислорода в блоке окисления серы с получением диоксида серы, который далее охлаждают в холодильнике до минус 10°С с получением диоксида серы в жидкой фазе;
б) подготавливают жидкий раствор диоксида серы со стадии (а) в первой части растворителя при температуре не выше минус 10 и атмосферном давлении;
в) жидкий диоксид серы в среде растворителя с температурой минус 10°С со стадии (б) под атмосферным давлением вводят в избытке против стехиометрического соотношения с изопреном по реакции Дильса-Альдера в реакционный аппарат, смешивают с ингибитором полимеризации изопрена и изопреном с температурой минус 10°С, подаваемым под атмосферным давлением, подогревают теплоносителем через рубашку реакционного аппарата до 40°С и осуществляют при перемешивании химическую реакцию при температуре 60-80°С и давлении до 1,0 МПа в течение 1-2 часов с получением первого раствора 3-метилсульфолена;
г) нагревают первый раствор 3-метилсульфолена стадии (в) теплоносителем до 90-100°С и испаряют посредством теплоносителя остаточный диоксид серы и избыток растворителя, получая второй раствор 3-метилсульфолена;
д) смешивают второй раствор 3-метилсульфолена стадии (г) со второй частью растворителя, получая третий раствор 3-метилсульфолена;
е) третий раствор 3-метилсульфолена охлаждают до 20°С, при этом 3-метилсульфолен кристаллизуется и осаждается, а маточный раствор растворителя декантируется;
ж) кристаллический 3-метилсульфолен стадии (е) растворяют третьей частью растворителя и гидрируют в реакторе гидрирования при 40-60°С под давлением газообразного водорода до 1,0 МПа в течении 1-2 часов в присутствии катализатора гидрирования с получением раствора 3-метилсульфолана;
з) раствор 3-метилсульфолана стадии (ж) продувают, фильтруют и перегоняют при пониженном давлении с получением отработанного растворителя и товарного 3-метилсульфолана;
и) избыток растворителя со стадии (г) с остаточным диоксидом серы направляют в блок регенерации растворителя на стадию регенерации растворителя в испаритель, где отделяют диоксид серы и очищенный растворитель направляют в первую емкость-накопитель блока регенерации растворителя;
к) маточный раствор растворителя стадии (е) направляют в вакуумно-роторный испаритель блока регенерации растворителя, после чего очищенный растворитель охлаждают и направляют во вторую емкость-накопитель блока регенерации растворителя, откуда подают на стадию (ж) в качестве третьей части растворителя;
л) кубовый остаток вакуумно-роторного испарителя, содержащий 3-метилсульфолен, подают в блок перекристаллизации, где отделяют остатки растворителя, которые возвращают в первую емкость-накопитель блока регенерации растворителя, очищенный 3-метилсульфолен возвращают на стадию (е);
м) отработанный растворитель со стадии (з), выделенный при перегонке 3-метилсульфолана направляют в блок регенерации растворителя на стадию регенерации растворителя в испаритель и далее в первую емкость-накопитель;
н) очищенный растворитель из первой емкости-накопителя направляют на стадии (б), (в) и (д) соответственно в качестве первой и второй части растворителя; при этом стадии (а) и (б) выполняют в блоке окисления серы, стадии (в), (г) и (д) выполняют последовательно в одном реакционном аппарате в реакционном блоке, стадию (е) выполняют в блоке фильтрации, стадию (ж) выполняют в блоке гидрирования, стадию (з) - в блоке разделения, стадии (и), (к), (м) и (н) - в блоке регенерации растворителя, стадию (л) - в блоке перекристаллизации.
При разработке изобретения рассмотрен вариант синтеза диоксида серы из отработанной серы, направляемой на утилизацию. Основным промышленным способом получения SО2 является способ обжига железного колчедана FeS2 или других сульфидов с целью дальнейшего производства SO3 и H2SO4. В настоящее время в России диоксид серы получают преимущественно в виде промышленных отходов, например, как побочный продукт обжига медных и цинковых сульфидных руд. Так как диоксид серы токсичен, утилизация его выбросов является одной из серьезных промышленных проблем. Так предприятие «Норникель» в 2023 году запустило масштабный экологический проект, предусматривающий улавливание и утилизацию диоксида серы путем переработки в серную кислоту H2SO4. В свою очередь для синтеза сульфоланов необходим химически чистый диоксид серы, который может быть получен при сжигании отработанной серы в потоке концентрированного кислорода. При этом в качестве отработанной серы можно использовать гранулированную, элементарную серу высокой чистоты, а также порошок или суспензию. Путем сжигания чистой серы в потоке концентрированного кислорода возможно получать чистый диоксид серы, пригодный для реакции циклизации с участием изопрена для синтеза ценных сульфоланов. Важным фактором для дальнейшего процесса является отсутствие в SO2 примесей влаги, так как при охлаждении до минус 10°С будут образовываться кристаллы, а сам SO2 растворяется в воде с образованием кислоты средней силы, способной к реакциям согласно формуле (4) со многими органическими соединениями, такими как аммиак, акролеин, щелочные металлы, амины, бутадиен и другими:
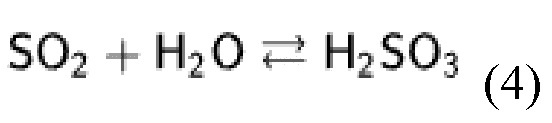
Диоксид серы агрессивен в отношении многих металлов, включая алюминий, железо, сталь, бронзу, медь и никель в присутствии воды.
Стадию сжигания серы ведут в недостатке кислорода, так как его избыток способен привести к образованию серного ангидрида, который при наличии воды в системе приведет к образованию серной кислоты, как представлено в формулах (5)-(7):
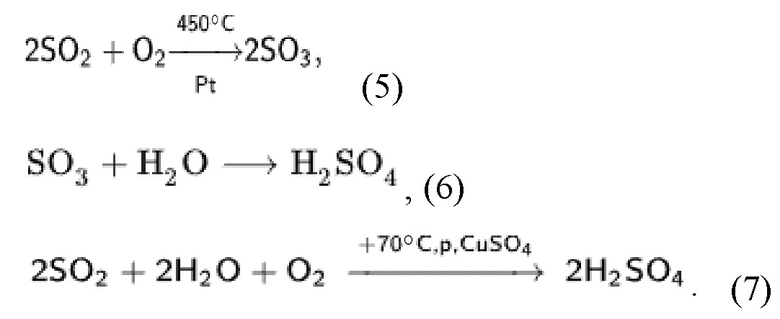
В способе предлагается охлаждать в холодильнике с использованием хладагентов полученный диоксид серы до минус 10°С для поддержания в жидком состоянии при атмосферном давлении, что позволит подавать в реакционный аппарат путем перекачивания насосом без привлечения компрессорного оборудования, а также позволит снизить его коррозионную активность. Кроме того, диоксид серы перед подачей в реакционный аппарат предварительно подготавливают в виде жидкого раствора диоксида серы в растворителе при температуре минус 10°С и атмосферном давлении.
В реакционном блоке в качестве реакционного аппарата используется реактор периодического действия с возможностью переключения с одной стадии на другую. Реакционный аппарат предварительно подготавливается путем очистки, осушки и продувки азотом перед использованием. Реакционный аппарат представляет собой вертикальный цилиндрический аппарат, выполненный из нержавеющей стали, оснащенный мешалкой для эффективного перемешивания реакционной смеси и одетый в рубашку для осуществления подвода или съема тепла в ходе всего процесса.
Известно, что изопрен способен к самопроизвольной полимеризации при повышении температуры, и во избежание потери сырья на побочную продукцию предварительно в реакционный аппарат подается ингибитор полимеризации изопрена, в качестве которого может применяться гидрохинон в количестве 0,1-0,3 % от суммарного количества изопрена и диоксида серы. В качестве сырья используют изопрен с чистотой не менее 99 %, диоксид серы с чистотой не менее 99,5 %. При этом изопрен перед подачей в реакционный аппарат хранится при минус 10°С и атмосферном давлении и подается в процесс при данных параметрах. Это позволяет эффективно перемешивать реакционную массу и проводить процесс получения 3-метилсульфолена в гомогенной фазе, обеспечивая максимальный контакт реагентов друг с другом.
Жидкий диоксид серы готовят предварительно, смешивая с растворителем, в качестве которого предпочтительно использовать изопропиловый спирт, отличающийся высокой степенью растворимости. Изопропиловый спирт позволяет работать в среде жидкого диоксида серы при отрицательных температурах и не требует создания высоких давлений, при этом гидрохинон, изопрен и 3-метилсульфолен при температуре процесса также растворяются в изопропиловом спирте. Мольное соотношение жидкого диоксида серы и изопрена составляет предпочтительно 1,2 : 1,0. При недостатке диоксида серы снижается выход сульфоленового соединения, а при существенном избытке возникает необходимость дополнительной очистки и утилизации избыточного диоксида серы, что приведет к неоправданному удорожанию себестоимости продукта. Изопропиловый спирт используется в избытке, количество используемого растворителя не ограничено, но предпочтительно соотношение растворителя и изопрена поддерживать равным 2 : 1. Если количество используемого растворителя недостаточно, то существует риск того, что реакция не будет протекать из-за осаждения сырья, что приведет к снижению выхода. Если количество используемого растворителя избыточно, то это повлечет за собой большие потери растворителя и увеличение нагрузки на блок регенерации растворителя, что экономически неоправданно.
Предварительно подготовленный в избытке жидкий диоксид серы в среде растворителя с температурой минус 10°С и под атмосферным давлением подают в реакционный аппарат на первую стадию в жидком виде, что позволяет осуществлять процесс при относительно низких давлениях, не превышающих 1,0 МПа, затем загружают ингибитор полимеризации изопрена, изопрен с температурой минус 10°С, подаваемый под атмосферным давлением, и осуществляют подогрев теплоносителем через рубашку до 40°С. В результате химического взаимодействия происходит образование 3-метилсульфолена в растворе, и по мере полного превращения изопрена в продукт за счет теплового эффекта химической реакции температура в реакторе начинает возрастать до 60-80°С. Таким образом, процесс осуществляется при температурах 60-80°С и давлении не выше 1,0 МПа, активном перемешивании в течение 1-2 часов до полного превращения изопрена.
На следующем этапе осуществляют нагрев реакционной смеси до 90-100°С посредством теплоносителя, циркулирующего в рубашке реакционного аппарата, и начинает происходить испарение остаточного диоксида серы и растворителя, которые отводятся в блок регенерации растворителя.
После завершения реакции циклизации, полного удаления диоксида серы на третьей стадии в реакционный аппарат подают свежий растворитель, путем перемешивания промывают реакционную массу и направляют в блок фильтрации. В блоке фильтрации раствор 3-метилсульфолена охлаждают до 40°С, при этом 3-метилсульфолен кристаллизуется из раствора, так как температура плавления 3-метилсульфолена составляет 67-68°С, а маточный раствор с остаточными примесями направляют в блок регенерации растворителя.
В реактор гидрирования блока гидрирования направляется 3-метилсульфолен в смеси с растворителем, куда под давлением азота вводится катализатор, содержащий никель, в частном случае может использоваться катализатор никель Ренея в количестве 3-4 % от общего количества сырья, смесь эффективно перемешивается. После перемешивания в реактор поступает высокочистый газообразный водород с чистотой не менее 99,9 % под давлением 2,0 МПа. При температурах 40-60°С осуществляется процесс селективного гидрирования с получением 3-метилсульфолана. При достижении давления в реакторе 0,6-1,0 МПа процесс гидрирования завершается.
Реакционную массу гидрирования, содержащую 3-метилсульфолан направляют в блок разделения, где продувают азотом от остаточных газообразных примесей, в частности, от водорода. После продувки реакционная масса поступает на стадию фильтрации, затем на ректификацию для отделения остатков растворителя. Так как синтезированный 3-метилсульфолан начинает медленно разлагаться при температурах выше 200°С, то перегонку целесообразно осуществлять при пониженном давлении в вакуум-ректификационном аппарате. На данном этапе можно также использовать отпарку растворителя путем нагрева 3-метилсульфолана до 90-100°С.
В качестве растворителя в предлагаемом изобретении используется изопропиловый спирт, отличающийся доступностью, дешевизной и при этом хорошей растворимостью. Помимо этого, так как температура испарения изопропилового спирта составляет 82,4°С это позволяет работать в процессе при температурах не выше 100°С. Потери растворителя могут существенно ухудшить экономический эффект изобретения. Для решения данной проблемы в способе предусмотрен блок регенерации растворителя. Таким образом, отработанный растворитель с остаточным диоксидом серы со второй стадии из реакционного аппарата и отработанный растворитель, выделенный при перегонке 3-метилсульфолана из блока разделения, направляют в блок регенерации растворителя на стадию регенерации растворителя в испаритель, где отделяют диоксид серы и очищенный растворитель направляют в сборную емкость блока регенерации растворителя, откуда возможна подача растворителя снова в процесс. Отделенный диоксид серы выводят в блок регенерации диоксида серы, откуда после стадий очистки и нейтрализации диоксид серы может снова использоваться в процессе. Маточный раствор растворителя из блока фильтрации направляют в вакуумно-роторный испаритель блока регенерации растворителя, после чего очищенный растворитель охлаждают, сепарируют и направляют на третью стадию в реакционный аппарат на смешение с реакционной массой, содержащей 3-метилсульфолен, или в сборную емкость стадии регенерации растворителя. Кубовый остаток из вакуум-роторного испарителя, как правило, содержит загрязненный 3-метилсульфолен, который целесообразно подвергнуть процессу перекристаллизации, чтобы вернуть в процесс. С этой целью 3-метилсульфолен подают в блок перекристаллизации, где отделяют остатки растворителя, которые возвращают в блок регенерации растворителя, а очищенный 3-метилсульфолен возвращают в блок фильтрации.
Возможно использовать для проведения первой стадии процесса готовый диоксид серы из баллонов.
Возможно подавать изопрен в реакционный аппарат порционно с температурой 25-30°С под давлением азота для интенсификации химического взаимодействия.
Целесообразно использовать в качестве растворителя изопропиловый спирт, обладающий хорошей растворимостью по отношению ко всем исходным реагентам в процессе, что позволяет осуществлять синтез 3-метилсульфолена в одной фазе, но при этом изопропиловый спирт имеет низкую температуру кипения 82,4°С, что позволяет легко отделять 3-метилсульфолен и 3-метилсульфолан из среды растворителя.
Возможно в качестве ингибитора полимеризации изопрена использовать гидрохинон, отличающийся высокой эффективностью, дешевизной и доступностью по сравнению с другими ингибиторами полимеризации. При этом использование ингибитора позволяет практически полностью исключить образование полиизопрена, который снижает показатели процесса и приводит к снижению выхода продукта за счет потери части сырья.
Рационально использовать в качестве катализатора гидрирования 3-метилсульфолена катализатор никель Ренея или никель Урушибара.
Целесообразно каждую из стадий (в), (г) и (д), протекающих в реакционном аппарате, реализовывать по крайней мере в трех отдельных реакторах, что позволит разработать непрерывный процесс получения 3-метилсульфолана для промышленных целей, что является особенно актуальным в условиях роста спроса на данный продукт.
Рационально для организации непрерывного процесса получения 3-метилсульфолана стадии (в), (г) и (д), выполняемые по крайней мере в трех разных реакционных аппаратах реакционного блока, выполнять последовательно.
Целесообразно стадии (в), (г) и (д) выполнять последовательно в каждом из трех реакционных аппаратов реакционного блока со смещением во времени в каждом из реакторов, которое обеспечивается при помощи циклограммы.
Возможно стадию гидрирования 3-метилсульфолена осуществлять в реакционном аппарате реакционного блока после очистки и продувки азотом после завершения стадии (д) получения 3-метилсульфолана, исключая при этом необходимость использования реактора гидрирования в периодическом процессе.
Целесообразно в качестве хладагента и теплоносителя, циркулирующего в рубашке реакционного аппарата реакционного блока, использовать один компонент, обеспечивающий рабочий диапазон температур от минус 20 до плюс 120°С. В качестве такого компонента можно использовать охлаждающую жидкость «Тасол» или раствор этиленгликоля. Использование одного и того же теплоносителя для охлаждения и подогрева реакционной смеси существенно упрощает систему теплообмена и позволяет реализовать все стадии процесса в одном аппарате при реализации периодической схемы процесса.
Целесообразно также в качестве хладагента и теплоносителя использовать н-октан, или н-нонан, или октан-нонановую фракцию, что позволяет уменьшить число компонентов, необходимых для реализации процесса.
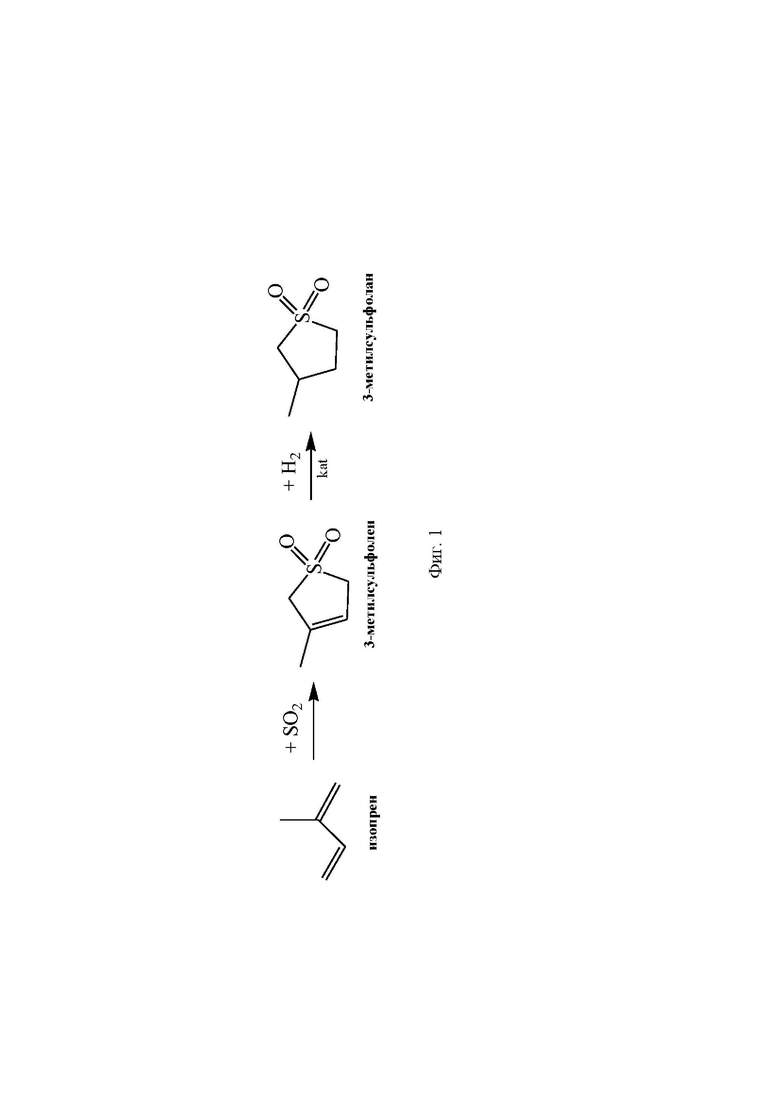
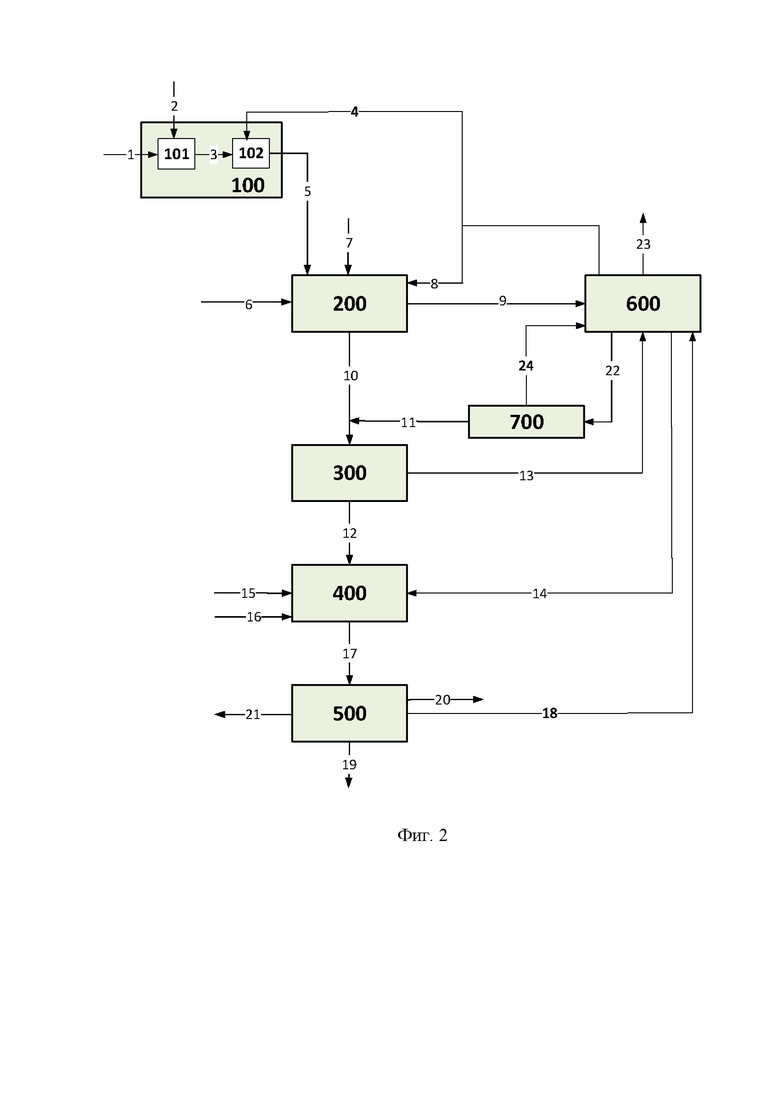
Реакционный механизм получения 3-метилсульфолана на основе изопрена с использованием способа по настоящему изобретению представлен на фигуре 1. На фигуре 2 представлена принципиальная схема основных стадий реализации используемого способа получения 3-метилсульфолана на основе изопрена с использованием следующих обозначений:
1-24 - потоки,
100 - блок окисления серы,
101 - реакционный узел блока окисления серы,
102 - узел подготовки жидкого раствора диоксида серы,
200 - реакционный блок,
300 - блок фильтрации,
400 - блок гидрирования,
500 - блок разделения,
600 - блок регенерации растворителя,
700 - блок перекристаллизации.
В одном из вариантов реализации способа получения 3-метилсульфолана на основе изопрена на стадии (а) в блок окисления серы 100 в реакционный узел блока окисления серы 101 подают серу потоком 1 и концентрированный кислород потоком 2. В результате сжигания серы в среде концентрированного кислорода образуется диоксид серы, подаваемый далее в холодильник, где охлаждается до минус 10°С (на схеме не показан) и поступает в виде жидкого диоксида серы по потоку 3 на стадию (б) в узел подготовки жидкого раствора диоксида серы 102 блока окисления серы 100, в котором при смешении с первой частью растворителя, который подают потоком 4, подготавливается жидкий раствор диоксида серы в растворителе. Жидкий диоксид серы в среде растворителя потоком 5 с температурой минус 10°С со стадии (б) под атмосферным давлением вводят в избытке против стехиометрического соотношения с изопреном по реакции Дильса-Альдера в реакционный аппарат, оснащенный мешалкой и рубашкой, реакционного блока 200 на стадию (в). В реакционный аппарат реакционного блока 200 на стадии (в) также загружают ингибитор полимеризации изопрена потоком 6 и изопрен с температурой минус 10°С, подаваемый под атмосферным давлением азота потоком 7, после чего начинают подогрев теплоносителем через рубашку реакционного аппарата до 40°С и осуществляют при перемешивании химическую реакцию при температуре 60-80°С и давлении не выше 1,0 МПа в течение 1-2 часов с получением первого раствора 3-метилсульфолена. На стадии (г) первый раствор 3-метилсульфолена нагревают теплоносителем до 90-100°С и испаряют посредством теплоносителя, циркулирующего в рубашке реакционного аппарата, остаточный диоксид серы и избыток растворителя, которые одним потоком 9 выводят в блок регенерации растворителя 600, где впоследствии разделяют. Диоксид серы потоком 23 направляется на регенерацию, а растворитель проходит систему очистки и возвращается вновь в процесс потоком 4. При этом на стадии (г) получают второй раствор 3-метилсульфолена, который на следующей стадии (д), реализуемой в реакционном аппарате реакционного блока 200, смешивают со второй частью растворителя, подаваемой из блока регенерации растворителя 600 потоком 8, получая при этом третий раствор 3-метилсульфолена, который потоком 10 направляет в блок фильтрации 300 на стадию (е). В блоке фильтрации 300 третий раствор 3-метилсульфолена охлаждают до 20°С, при этом 3-метилсульфолен кристаллизуется и осаждается, а маточный раствор растворителя декантируется и потоком 13 направляется в блок регенерации растворителя 600. Кристаллический 3-метилсульфолен смешивают с потоком возвратного очищенного 3-метилсульфолена, подаваемого потоком 11 со стадии (л) из блока перекристаллизации 700, подают потоком 12 на стадию (ж) в блок гидрирования 400, чтобы затем растворить третьей частью растворителя, подаваемой потоком 14. В реакторе гидрирования блока гидрирования 400 осуществляют процесс гидрирования 3-метилсульфолена при 40-60°С под давлением газообразного водорода, подаваемого потоком 15, до 1,0 МПа в течение 1-2 часов в присутствии катализатора гидрирования, подаваемого потоком 16, с получением 3-метилсульфолана. При этом процесс происходит до полного гидрирования 3-метилсульфолена, а в качестве катализаторов гидрирования используют катализатор никель Ренея или никель Урушибара.
Полученный раствор 3-метилсульфолана потоком 17 направляют в блок разделения 500 на стадию (з), где продувают от остатков водорода, отводимых потоком 20, фильтруют для отделения отработанного катализатора потоком 21, отделяют путем перегонки при пониженном давлении от отработанного растворителя, отводимого потоком 18, и в результате получают товарный 3-метилсульфолан, направляемый потоком 19 в систему хранения (на схеме не показана).
В способе по изобретению предусмотрен блок регенерации растворителя 600, предназначенный для сокращения расхода свежего растворителя и потерь отработанного растворителя. Таким образом, отработанный избыток растворителя со стадии (г) с остаточным диоксидом серы потоком 9 из реакционного аппарата направляют в блок регенерации растворителя 600 на стадию (и) регенерации растворителя, которую осуществляют в испарителе с целью отделения диоксида серы, отводимого потоком 23 на дальнейшую очистку. Также в испаритель поступает отработанный растворитель, выделенный при перегонке 3-метилсульфолана на стадии (м) потоком 18. После испарителя очищенный растворитель направляют в первую емкость-накопитель блока регенерации растворителя 600. На стадии (к) происходит очистка в вакуумно-роторном испарителе блока регенерации растворителя 600 маточного раствора растворителя, поступающего потоком 13 из блока фильтрации 300, затем очищенный растворитель охлаждают и направляют во вторую емкость-накопитель блока регенерации растворителя 600. При этом полученный кубовый остаток вакуумно-роторного испарителя, содержащий 3-метилсульфолен, поступает потоком 22 в блок перекристаллизации 700, где на стадии (л) в результате перекристаллизации происходит отделение остатков растворителя от очищенного 3-метилсульфолена, возвращаемого потоком 11 на стадию (е) в блок фильтрации 300, а отделившиеся остатки растворителя потоком 24 возвращают в первую емкость-накопитель блока регенерации растворителя 600. После очистки и сбора отработанного растворителя в первой и второй емкостях-накопителях растворитель вновь используют в процессе, подавая на соответствующие стадии способа в качестве первой части растворителя потоком 4, второй части растворителя потоком 8 и третьей части растворителя потоком 14.
Пример. Согласно вышеизложенному способу получения 3-метилсульфолана были произведены расчеты реализации изобретения. В реакционный аппарат объемом 500 мл, оснащенный мешалкой, термометром, манометром и охлаждающей рубашкой загружают 0,34 г гидрохинона, 132 г изопропилового спирта и 76,9 г сернистого ангидрида. Реакционный аппарат нагревается до 80°С, включается перемешивание и дозировочным насосом загружается 68,12 г свежеперегнанного изопрена со скоростью 1,5 г/мин. После реакционная масса выдерживается при этой температуре 1,5 часа. Давление 0,6-0,8 МПа, в конце реакции снижается до 0,4 МПа.
Далее давление дросселируется и в реакционный аппарат через барботер подается азот со скоростью 300 мл/мин. Пары изопропилового спирта конденсируются в прямом холодильнике и впоследствии используются при следующих загрузках. Нагрев прекращается и в реакционный аппарат подается 132 г изопропилового спирта. Реакционная масса перемешивается в течение 15 минут при охлаждении до 50°С и выгружается в емкость для кристаллизации. После охлаждения до температуры плюс 5°С выпадают кристаллы 3-метилсульфолена, которые отфильтровывают и высушивают. Выход составляет 115 г. Фильтрат упаривается и используется при следующих загрузках. При упаривании образуется дополнительное количество 3-метилсульфолена, которое собирается и перекристаллизовывается. Выход составляет 5 г. Суммарный выход 3-метилсульфолена 90,9 % от стехиометрически возможного.
Осадок 3-метилсульфолена в количестве 120 г помещается в реакционный аппарат объемом 500 мл, туда же загружается 280 г изопропилового спирта и 6 г свежеприготовленного никеля Ренея или никеля Урушибара. Реакционный аппарат герметизируется, включается перемешивание и подается водород под давлением 0,6 МПа. Температура реакции устанавливается 40-50°С. Давление поддерживается в течение 180 мин, после чего водород дросселируется, а реакционная масса фильтруется. Отфильтрованный катализатор направляется на регенерацию. Растворитель упаривается и возвращается в реакцию. Выход 3-метилсульфолана на полученный ранее 3-метилсульфолен составил 119 г (97,7 % от стехиометрически возможного). Чистота 3-метилсульфолана методом газожидкостной хроматографии составила 99,6 % масс.
По стехиометрии 68 г изопрена реагируют с 64 г ангидрида с получением 132 г 3-метилсульфолена, который реагирует с 2 г водорода. В таком случае по теории должны получить 134 г 3-метилсульфолана. На практике продукта получено 119 г. Таким образом, суммарный выход 3-метилсульфолана по двум стадиям составляет 88,81 % масс.
Таким образом, заявляемое изобретение решает задачу разработки способа получения 3-метилсульфолана в результате реакции циклизации изопрена с диоксидом серы с последующим гидрированием соответствующего 3-метилсульфолена до 3-метилсульфолана с обеспечением высокого выхода и высокой чистоты целевого продукта, при этом предлагаемый способ позволяет исключить генерацию большого количества органических отходов, потерь растворителя за счет его многократного использования после блока регенерации растворителя, повысить эффективность использования серы и является применимым для промышленного производства.
Изобретение относится к области технологии органических растворителей, конкретно к способу получения 3-метилсульфолана, который используют для извлечения ароматических соединений из углеводородных смесей в нефтехимической и нефтеперерабатывающей промышленности. Способ включает сжигание серы с получением диоксида серы, который далее охлаждают до жидкой фазы и подают на последующую реакцию с изопреном в среде первой части растворителя, в присутствии ингибитора полимеризации, при перемешивании при температуре 60-80°С и давлении до 1,0 МПа, в течение 1-2 ч с получением 3-метилсульфолена. Затем полученный раствор 3-метилсульфолена освобождают посредством испарения от остаточного диоксида серы и избытка растворителя, после чего смешивают со второй частью растворителя и при охлаждении кристаллизуют, а маточный раствор декантируют. Кристаллический 3-метилсульфолен гидрируют в среде третьей части растворителя при 40-60°С под давлением до 1,0 МПа в течение 1-2 ч в присутствии катализатора, с получением раствора 3-метилсульфолана, который затем продувают, фильтруют и перегоняют при пониженном давлении, с получением товарного 3-метилсульфолана. Остатки растворителя, полученные в ходе технологических операций, направляют в блок регенерации растворителя, откуда возвращают очищенный растворитель в емкость-накопитель и далее на стадии смешения. Технический результат – предложен эффективный способ получения целевого продукта с высоким выходом и высокой чистотой при сокращении отходов растворителя. 11 з.п. ф-лы, 2 ил., 1 пр.
1. Способ получения 3-метилсульфолана, включающий стадии:
а) сжигают серу в среде концентрированного кислорода в блоке окисления серы с получением диоксида серы, который далее охлаждают в холодильнике до минус 10°С с получением диоксида серы в жидкой фазе;
б) подготавливают жидкий раствор диоксида серы со стадии (а) в первой части растворителя при температуре не выше минус 10°С и атмосферном давлении;
в) жидкий диоксид серы в среде растворителя с температурой минус 10°С со стадии (б) под атмосферным давлением вводят в избытке против стехиометрического соотношения с изопреном по реакции Дильса-Альдера в реакционный аппарат, смешивают с ингибитором полимеризации изопрена и изопреном с температурой минус 10°С, подаваемым под атмосферным давлением, подогревают теплоносителем через рубашку реакционного аппарата до 40°С и осуществляют при перемешивании химическую реакцию при температуре 60-80°С и давлении до 1,0 МПа в течение 1-2 ч с получением первого раствора 3-метилсульфолена;
г) нагревают первый раствор 3-метилсульфолена стадии (в) теплоносителем до 90-100°С и испаряют посредством теплоносителя остаточный диоксид серы и избыток растворителя, получая второй раствор 3-метилсульфолена;
д) смешивают второй раствор 3-метилсульфолена стадии (г) со второй частью растворителя, получая третий раствор 3-метилсульфолена;
е) третий раствор 3-метилсульфолена охлаждают до 20°С, при этом 3-метилсульфолен кристаллизуют и осаждают, а маточный раствор растворителя декантируют;
ж) кристаллический 3-метилсульфолен стадии (е) растворяют третьей частью растворителя и гидрируют в реакторе гидрирования при 40-60°С под давлением газообразного водорода до 1,0 МПа в течение 1-2 ч в присутствии катализатора гидрирования с получением раствора 3-метилсульфолана;
з) раствор 3-метилсульфолана стадии (ж) продувают, фильтруют и перегоняют при пониженном давлении с получением отработанного растворителя и товарного 3-метилсульфолана;
и) избыток растворителя со стадии (г) с остаточным диоксидом серы направляют в блок регенерации растворителя на стадию регенерации растворителя, в испаритель, где отделяют диоксид серы и очищенный растворитель направляют в первую емкость-накопитель блока регенерации растворителя;
к) маточный раствор растворителя стадии (е) направляют в вакуумно-роторный испаритель блока регенерации растворителя, после чего очищенный растворитель охлаждают и направляют во вторую емкость-накопитель блока регенерации растворителя, откуда подают на стадию (ж) в качестве третьей части растворителя;
л) кубовый остаток вакуумно-роторного испарителя, содержащий 3-метилсульфолен, подают в блок перекристаллизации, где отделяют остатки растворителя, которые возвращают в первую емкость-накопитель блока регенерации растворителя, очищенный 3-метилсульфолен возвращают на стадию (е);
м) отработанный растворитель со стадии (з), выделенный при перегонке 3-метилсульфолана, направляют в блок регенерации растворителя на стадию регенерации растворителя в испаритель и далее в первую емкость-накопитель;
н) очищенный растворитель из первой емкости-накопителя направляют на стадии (б), (в) и (д) соответственно в качестве первой и второй частей растворителя; при этом стадии (а) и (б) выполняют в блоке окисления серы, стадии (в), (г) и (д) выполняют последовательно в одном реакционном аппарате в реакционном блоке, стадию (е) выполняют в блоке фильтрации, стадию (ж) выполняют в блоке гидрирования, стадию (з) – в блоке разделения, стадии (и), (к), (м) и (н) – в блоке регенерации растворителя, стадию (л) – в блоке перекристаллизации.
2. Способ по п. 1, отличающийся тем, что диоксид серы подают из баллонов.
3. Способ по п. 1, отличающийся тем, что изопрен подают в реакционный аппарат порционно с температурой 25-30°С под давлением азота.
4. Способ по п. 1, отличающийся тем, что в качестве растворителя используют изопропиловый спирт.
5. Способ по п. 1, отличающийся тем, что в качестве ингибитора полимеризации изопрена используют гидрохинон.
6. Способ по п. 1, отличающийся тем, что в качестве катализатора гидрирования 3-метилсульфолена используют катализатор никель Ренея или никель Урушибара.
7. Способ по п. 1, отличающийся тем, что каждую из трех стадий (в), (г) и (д), протекающих в реакционном аппарате реакционного блока, реализуют по крайней мере в трех отдельных реакторах.
8. Способ по п. 7, отличающийся тем, что стадии (в), (г) и (д) выполняют последовательно в каждом из трех реакционных аппаратов реакционного блока.
9. Способ по п. 7, отличающийся тем, что стадии (в), (г) и (д) выполняют последовательно в каждом из трех реакционных аппаратов реакционного блока со смещением во времени в каждом из реакторов, обеспечиваемом при помощи циклограммы.
10. Способ по п. 1, отличающийся тем, что стадию гидрирования 3-метилсульфолена осуществляют в реакционном аппарате реакционного блока после очистки и продувки азотом после завершения стадии (д) получения 3-метилсульфолена.
11. Способ по п. 1, отличающийся тем, что в качестве хладагента и теплоносителя, циркулирующего в рубашке реакционного аппарата реакционного блока, используют один компонент, обеспечивающий рабочий диапазон температур от минус 20 до плюс 120°С.
12. Способ по п. 11, отличающийся тем, что в качестве хладагента и теплоносителя используют н-октан, или н-нонан, или октан-нонановую фракцию.
| CN 101875651 A, 03.11.2010 | |||
| US 5347018 A1, 13.09.1994 | |||
| JP 2012158543 A, 23.08.2012 | |||
| US 8436193 B2, 07.05.2013 | |||
| CN 116283898 A, 23.06.2023. |
Авторы
Даты
2025-03-31—Публикация
2024-09-26—Подача