Изобретение относится к фармацевтической промышленности, а именно к способам выделения флавоноидов из компрессионной древесины осины европейской (Populus tremula), обладающих высокой биологической активностью.
Данные соединения могут рассматриваться в качестве перспективных биологически активных веществ, способных найти применение при создании новых фармацевтических, пищевых, косметических продуктов и препаратов.
Флавоноиды представляют собой класс полифенольных вторичных метаболитов растений [1-2]. В основном они характеризуются общей базовой структурой (C6-C3-C6), в которой два ароматических кольца (A и B) соединены 3-углеродным мостиком, образуя гетероциклическое кольцо (C) [2-4]. Большое разнообразие внутри этого класса определяется степенью насыщенности и окисления кольца C, а также числом, положением и типом заместителей в структуре [5]. Этим обусловлено наличие широкого спектра биологической активности флавоноидов: от антиоксидантных свойств до антимикробного, противовирусного, противовоспалительного действия. Кроме того, они проявляют профилактическое действие при опухолевых и сердечно-сосудистых заболеваниях [6-8]. Таким образом, флавоноиды вызывают интерес к поиску их новых источников, разделению и выделению в виде индивидуальных компонентов.
Флавоноиды обнаруживаются в различных частях растений, но наибольшее внимание уделяется тем, которые употребляются в пищу как простой источник биологически активных соединений. Помимо этого, важным промышленным источником флаваноидов этого класса являются отходы сельскохозяйственной и лесной промышленности (кора и смола деревьев, семена растений и т.д.). В данном аспекте, перспективным источником выступает осина (Populus tremula L.). Помимо своей распространенности и активного применения в качестве сырья в лесной и лесохимической промышленности [9-11], она содержит в составе компрессионной древесины (древесина сучков) до 10-15% масс. экстрактивных веществ, основная доля которых (более 80%) приходится на аромадендрин и нарингенин (в том числе в виде метоксилированных и гликозилированных производных) [12-13]. Использование такого сырья для получения ценных биологически активных флавоноидов подразумевает разработку эффективных процедур их выделения в виде высокоочищенных препаратов.
Подходы, основанные на простых процедурах, например, жидкость-жидкостной экстракции или перекристаллизации, возможны лишь при доминировании одного целевого флавоноида в исходном сырье [14]. В случае более сложных по составу экстрактов ключевыми методами выделения и очистки являются хроматографические [15]. В литературе приведены различные варианты применения колоночной хроматографии низкого давления на силикагеле или обращенно-фазовом сорбенте, эксклюзионной, высокоскоростной противоточной, высокоэффективной жидкостной и других типов хроматографии [16-17]. Тем не менее, примеров использования перечисленных подходов для получения чистых препаратов производных аромадендрида и нарингенина не приводится. Дополнительными недостатками применения жидкостной хроматографии зачастую являются низкая эффективность разделения, значительный расход токсичных органических растворителей, длительное время процесса и т. д.
В качестве альтернативы существующим хроматографическим методам выделения природных соединений можно рассматривать сверхкритическую флюидную хроматографию (СФХ). В современном варианте этого метода основным компонентом подвижной фазы является диоксид углерода, при этом его элюирующая сила варьируется путем изменения доли органического модификатора (например, метанола) в составе, а также противодавления и температуры в хроматографической системе. По сравнению с классическими элюентами сверхкритический СО2, помимо низкой вязкости, характеризуется малым расходом токсичных растворителей, что является важным атрибутом в технологиях, отвечающих принципам «зеленой» химии. Дополнительным преимуществом СФХ является сокращение объема собираемых фракций за счет удаления диоксида углерода из подвижной фазы при снижении давления в системе, что упрощает дальнейшие процедуры упаривания и сушки выделенных компонентов. В литературе имеются сведения об успешном использовании препаративной сверхкритической флюидной хроматографии не только для выделения неполярных природных метаболитов (жирорастворимых витаминов, стероидов, терпенов) [18], но и ряда представителей полифенолов, например, полиметоксифлавонов [19], лигнанов [20] и др. Однако сведения о выделении производных нарингенина и аромадендрина из растительных экстрактов сверхкритической флюидной хроматографией в литературе не упоминается.
Ближайшим аналогом предлагаемого изобретения является способ получения чистых препаратов лигнанов из экстрактов компрессионной древесины хвойных пород деревьев, основанный на применении метода препаративной СФХ [21]. По этому способу экстракты компрессионной древесины сосны (Pinus sylvestris), ели (Picea abies), пихты (Abies sibirica) и лиственницы (Larix sibirica) разделяют на подвижной фазе из силикагеля с привитыми диольными группами. Отобранные фракции при этом отличаются наличием того или иного лигнана с высокой чистотой (не менее 90%).
Поставленными задачами в настоящем изобретении являются: разработка подхода для быстрого, экологически безопасного и эффективного выделения флавоноидов из компрессионной древесины осины и получение на этой основе чистых препаратов флавоноидов.
Технический результат изобретения - получение чистых препаратов флавоноидов, обладающих высокой биологической активностью.
В качестве объекта исследования выбрана компрессионная древесина лиственной породы, характерной для Европейского Севера, - осины европейской (Populus tremula). Растительный материал получали с деревьев возрастом 40-60 лет, заготовленных в Архангельской области (Россия).
Сучки (внутренняя часть, находящаяся в стволе дерева) высверливали и подвергали сушке в вакуумном сушильном шкафе на протяжении 12 часов и температуре 40°С. Для повышения эффективности экстракции сухие опилки дополнительно измельчали до размера частиц менее 1 мм на центробежной мельнице. Экстракция по Сокслету проводилась в два этапа по 10 часов каждый: гексаном, для удаления смоляных кислот, терпенов. липидов и пр., а затем ацетоном. Полученный ацетоновый экстракт упаривали на роторном испарителе до минимального объема (5 мл), приливали к нему 150 мл воды и тщательно перемешивали. После чего полученную суспензию замораживали жидким азотом и сушили в лиофильной сушилке. Полученные экстракты были перенесены в стеклянные виалы и хранились при температуре 4°С. Выход экстрактивных веществ в ацетоновых экстрактах составлял 10-14% от массы абсолютно сухой древесины.
Определение оптимальных параметров для хроматографического разделения
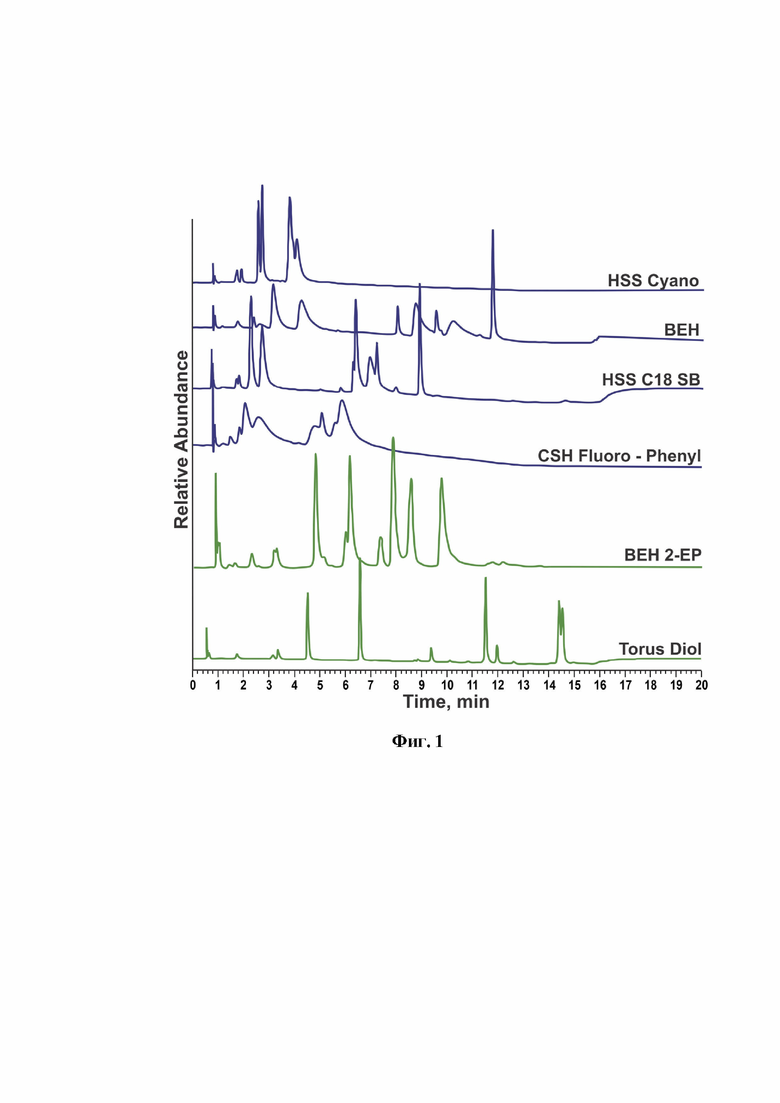
В связи с большим разнообразием сорбентов с различным химическим составом, используемых в СФХ, ключевым вопросом при разработке способа разделения является правильный выбор неподвижной фазы, обеспечивающей приемлемое удерживание и эффективное разделение аналитов. С этой целью был проведен скрининг важнейших неподвижных фаз, при этом в качестве подвижной фазы выступала смесь диоксида углерода с метанолом, содержащего 0,1 % муравьиной кислоты. Учитывая одинаковые геометрические характеристики колонок, использовали одинаковые условия элюирования (скорость подачи подвижной фазы, профиль градиента и т. д.) (фиг. 1), на основе результатов которого в качестве оптимальных были выбраны этилпиридиновая и диольная неподвижные фазы.
Установлено, что минимальная доля органического модификатора (метилового спирта), исключающая осаждение флавоноидов в хроматографической системе, должна составлять не менее 10%.
Для полупрепаративного выделения флавоноидов использовались хроматографическая колонки Shim - pack UC-Py (250 × 10 мм) и Shim-pack US Diol II (250 × 10 мм). Ключевым вопросом при масштабировании хроматографического метода является сохранение приемлемого разрешения целевых пиков в условиях экстремально высокого содержания соединений во вводимой пробе (концентрация и объемная перегрузка), что характерно для препаративных разделений. Максимально допустимое количество вводимой пробы в СФХ также ограничивается растворимостью ее компонентов в неполярном сверхкритическом диоксиде углерода. Предварительные опыты показали, что при объеме инжекции 100 мкл максимальная концентрация экстрактивных веществ компрессионной древесины не должна превышать 20 мг/мл. Концентрационные перегрузки приводят к значительному уширению хроматографических зон, что несколько снижает количество компонентов экстракта, которые можно выделить с достаточной степенью чистоты. Оптимизация режима градиентного элюирования позволила достичь продолжительности одного цикла выделения флавоноидов равной 30 минут.
Характеристика полученных фракций
Все полученные фракции накапливали в количествах от единиц до сотен миллиграммов при многократном полупрепаративном разделении и затем идентифицировали методами двумерной спектроскопии ядерного магнитного резонанса (2D-ЯМР) и высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием высокого разрешения (ВЭХЖ-МСВР), а также проверяли на их чистоту методом обращенно-фазовой ВЭЖХ со спектрофотометрическим детектированием. Выбор данной методики обусловлен «ортогональностью» разделения при реализации обращенно-фазового и адсорбционного механизмов, что позволяет разделять совместно элюирующиеся в условиях СФХ соединения. Полученные результаты показали (Shim - pack UC-Py (250 × 10 мм)), что 6 полученных фракций обладают высокими выходами, а еще одна фракция содержит 2 компонента (Таблица 1).
В случае другой колонки (Shim-pack US Diol II (250 × 10 мм)) показано, что 4 полученных фракции обладают высокими выходами, а еще одна фракция содержит 2 компонента (Таблица 2). Фракция №2 не охарактеризована, так как обладает большим набором компонентов.
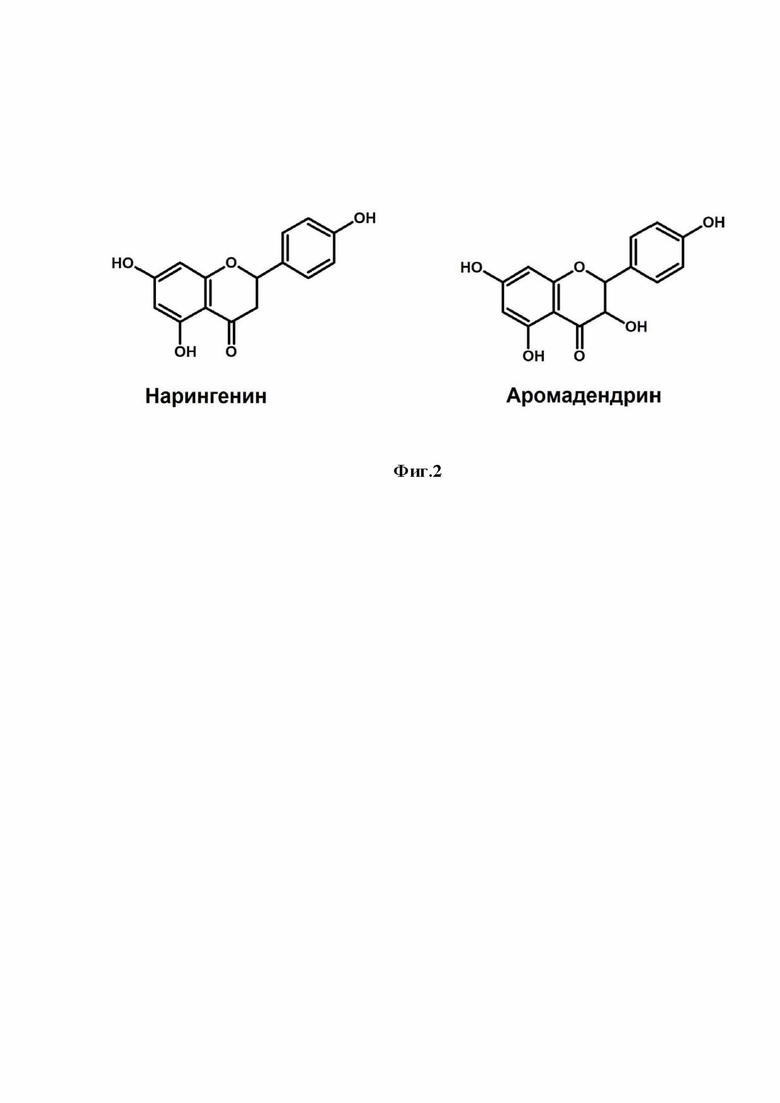
По данным таблиц видно, что преобладающие компоненты в компрессионной древесине Европейской осины (нарингенин и аромадендрин) (фиг. 2) были выделены в индивидуальном виде с чистотой более 90%. Также можно выделить наличие метиловых эфиров нарингенина и аромадендрина и их глюкозидов.
Выделенные в чистом виде компоненты обладают противомикробной, противовоспалительной, антиоксидантной, противогрибковой, а также противораковой активностью, что делает их перспективным сырьем для фармацевтической промышленности.
Вышеописанный способ выделения флавоноидов из компрессионной древесины осины поясняется следующими примерами:
Пример 1.
Компрессионную древесину осины (Populus tremula) высушивали, измельчали до размера частиц не более 1 мм, затем подвергали сушке в вакуумном сушильном шкафу при температуре 40°С. После чего полученные сухие опилки экстрагировали в аппарате Сокслета в две стадии: гексаном и ацетоном по 8 ч каждый. После этого, ацетоновый экстракт упаривали на роторном испарителе до минимального объема, добавляли пятикратный избыток деионизованной воды до получения суспензии и подвергали лиофильной сушке. Полученный экстракт в дальнейшем использовался для препаративного разделения.
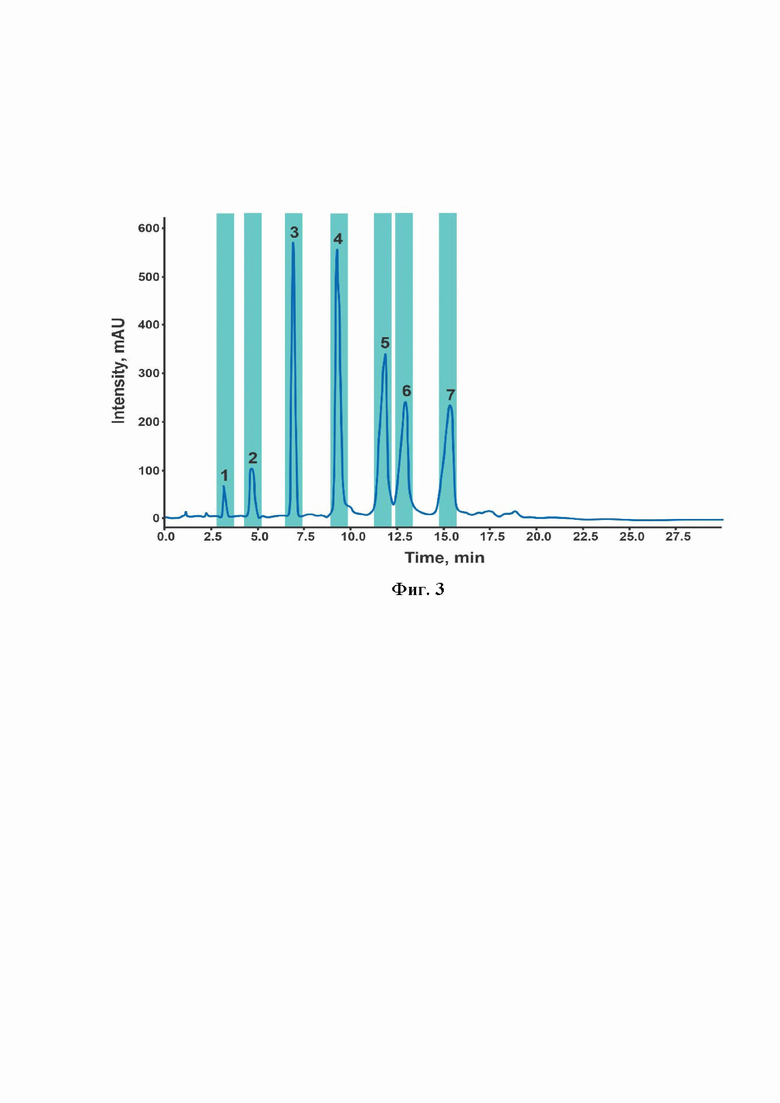
Выделение флавоноидов производили при помощи препаративной системы для сверхкритической флюидной хроматографии Nexera UC Prep (Shimadzu, Япония), оснащенная диодно-матричным детектором и автоматической системой сбора фракций. Использовалась колонка: Shim - pack UC-Py (250 × 10 мм), с градиентным режимом: 0-5 мин 10% метанола, 5-17 мин повышение до 30% метанола, 17-30 мин 30% метанола. Для этого готовили метанольный раствор ацетонового экстракта с концентрацией 20 мг/мл, 500 мкл из которого вводили в хроматограф. В течение 30-минутного анализа автоматически отбирались фракции, как показано на фиг. 3. Фракции упаривались на роторном испарителе до минимального объема и лиофильно высушивались, после чего анализировались методами ВЭЖХ-УФ, ВЭЖХ-МСВР и ЯМР для идентификации и оценки чистоты.
Пример 2.
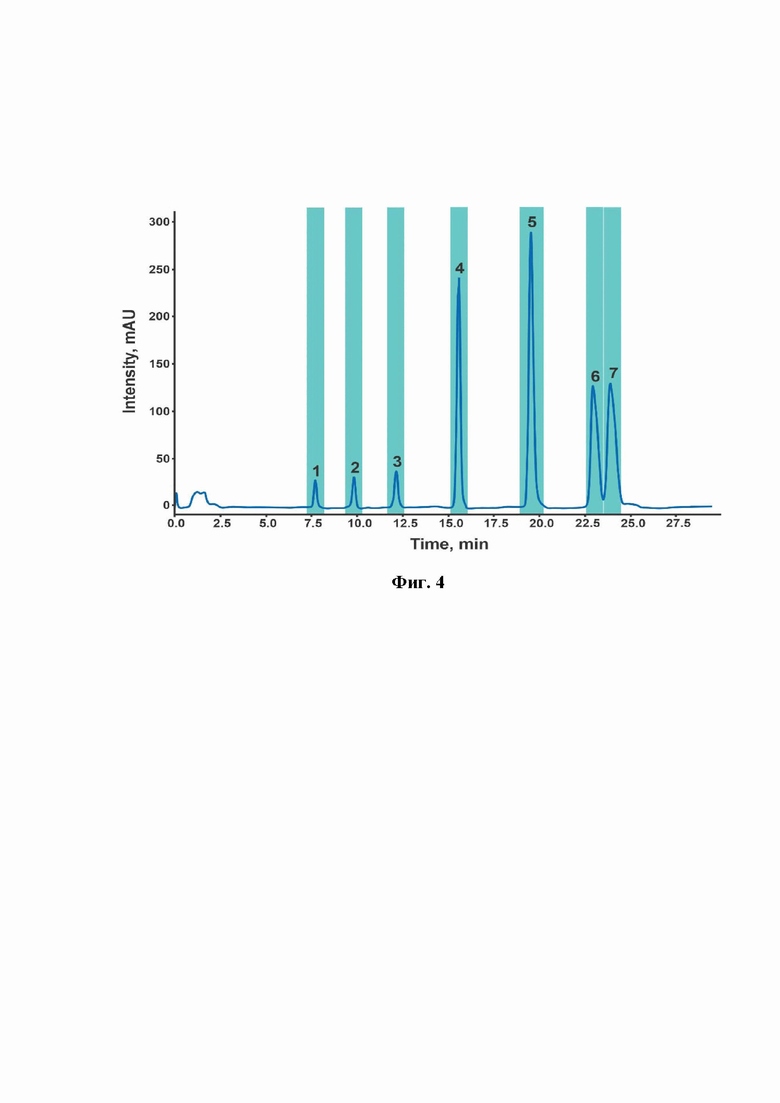
Эксперимент проводился на основе примера 1, отличаясь тем, что в качестве используемой колонки выступала Shim-pack US Diol II (250 × 10 мм), с градиентным режимом: 0 - 5 мин 10% метанола, 5 - 15 мин повышение до 30% метанола, 15 - 23 мин 30% метанола, 23 - 25 мин понижение до 10% метанола, 25 - 30 мин 10% метанола, а программа автоматического сбора фракций соответствовала представленной на фиг. 4.
На фиг.1 представлен скрининг неподвижных фаз. Условия: скорость потока 1,0 мл/мин (исключение - 0,8 мл/мин для Torus DIOL, ввиду меньшего внутреннего диаметра), температура термостата колонки 40°С, обратное давление 130 бар. В качестве сорастворителя В использовался метанол, содержащий 0,1% об. муравьиной кислоты, применялось градиентное элюирование: 0 мин - 10% В, 12-15 мин - 30% В, 16-20 мин - 10% В.
На фиг.2 представлены структурные формулы основных соединений, входящих в состав компрессионной древесины осины.
На фиг.3 представлена хроматограмма экстракта компрессионной древесины осины в режиме препаративной СФХ на этилпиридиновой неподвижной фазе. Цветом выделены области сбора фракций для дальнейшего исследования. (Градиент 0-5 мин 10% В, 5-17 мин повышение до 30% В, 17-30 30% В).
На фиг.4 представлена хроматограмма экстракта компрессионной древесины осины в режиме препаративной СФХ на диольной неподвижной фазе. Цветом выделены области сбора фракций для дальнейшего исследования. (Градиент 0-5 мин 10% В, 5-15 мин повышение до 30% В, 15-23 мин 30% В, 23-25 мин понижение до 10% В, 25-30 мин 10% В).
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Bhavabhuti Prasada, Sadhucharan Mallickb, Abinash Chand Bharatic, and Shivjeet Singhd. Flavonoids: Chemistry, biosynthesis, isolation, and biological function; Handbook of Biomolecules, 2023; 467 - 488.
2. A. N. Panchel, A. D. Diwan, and S. R. Chandra. Flavonoids: an overview; Journal of Nutritional Science, 2016; 1-15.
3. Mónica L. Chávez-González, Leonardo Sepúlveda, Deepak Kumar Verma, Hugo A. Luna-García, Luis V. Rodríguez-Durán, Anna Ilina, and Cristobal N. Aguilar. Conventional and Emerging Extraction Processes of Flavonoids; Processes 2020, 8, 434.
4. Weisheng Feng, Zhiyou Hao and Meng Li. Isolation and Structure Identification of Flavonoids. Flavonoids - From Biosynthesis to Human Health, 2017.
5. Raghad Yousef Ali Aljawarneh, Mohamad Shazeli Che Zain, Fauziahanim Zakaria. Macroporous polymeric resin for the purification of flavonoids from medicinal plants: A review; Journal of separation science, 2024, 47 (15).
6. Yogesh A. Bhadange, Jitendra Carpenter, Virendra Kumar Saharan. A Comprehensive Review on Advanced Extraction Techniques for Retrieving Bioactive Components from Natural Sources; ACS Omega, 2024.
7. Ioana Ignat, Irina Volf, Valentin I. Popa. A critical review of methods for characterisation of polyphenolic compounds in fruits and vegetables; Food Chemistry, 2011, 1821-1835 (126).
8. Bié, J., Sepodes, B., Fernandes, P.C.B., Ribeiro, M.H.L. Polyphenols in Health and Disease: Gut Microbiota, Bioaccessibility, and Bioavailability. Compounds 2023, 3, 40-72.
9. Tsarev A. Growth and breeding of aspen in Russia. Agric Food Sci 2013;62:153-160.
10. Liepiņš J, Ivanovs J, Lazdiņš A, Jansons J, Liepiņš K. Mapping of basic density within European aspen stems in Latvia. Silva Fenn 2017;51(5):7798.
11. Rogers PC, Pinno BD, Šebesta J, Albrectsen BR, Li G, Ivanova N, Kusbach A, Kuuluvainen T, Landhäusser SM, Liu H, Myking T, Pulkkinen P, Wen Z, Kulakowski D. A global view of aspen: Conservation science for widespread keystone systems. Glob Ecol Conserv 2020;21.
12. Anna V. Faleva, Danil I. Falev, Aleksandra A. Onuchina, Nikolay V. Ulyanovskii, Dmitry S. Kosyakov. Comprehensive identification of polyphenolic metabolites in aspen knotwood by combination of 2D NMR and HPLC-HRMS; Phytochemical Analysis. 2024;1-10.
13. Pietarinen SP, Willför SM, Vikström FA, Holmbom BR. Aspen knots, a rich source of flavonoids. J. Wood Chem Technol 2006; 26(3): 245-258.
14. Катасонова И.А.. Способ получения высокоочищенного дигидрокверцетина, патент № RU 2817996.
15. André de Villiers, Pieter Venter, Harald Pasch. Recent advances and trends in the liquid-chromatography-mass spectrometry analysis of flavonoids; Journal of Chromatography A, 2016, 16-78.
16. Lingxi Li, Jian Zhao, Tingting Yang, Baoshan Sun. High-speed countercurrent chromatography as an efficient technique for large separation of plant polyphenols: A review; Food Research International, 2022, 110956.
17. Yang Huanga, Ying Fenga, Guangyun Tanga, Minyi Li, Tingting Zhanga, Marianne Fillet, Jacques Crommena, Zhengjin Jianga. Development and validation of a fast SFC method for the analysis of flavonoids in plant extracts; Journal of Pharmaceutical and Biomedical Analysis, 2017, 384-391.
18. Anja Hartmann, Markus Ganzera. Supercritical Fluid Chromatography--Theoretical Background and Applications on Natural Products; Planta Med, 2015, 81(17):1570-81.
19.Shiming Li, Ted Lambros, Zhenyu Wang, Robert Goodnow, Chi-Tang Ho. Efficient and scalable method in isolation of polymethoxyflavones from orange peel extract by supercritical fluid chromatography; Journal of Chromatography B, 2007, 291-297.
20. Ul’yanovskii, N.V.; Onuchina, A.A.; Ovchinnikov, D.V.; Faleva, A.V.; Gorbova, N.S.;Kosyakov, D.S. Analytical and Preparative Separation of Softwood Lignans by Supercritical Fluid Chromatography. Separations 2023, 10, 449.
21. Онучина А.А., Фалёва А.В., Данилова Э.В., Ульяновский Н.В., Косяков Д.С. Способ получения чистых препаратов лигнанов из компрессионной древесины, патент №2827101.
ПОСОБ ПОЛУЧЕНИЯ ЧИСТЫХ ПРЕПАРАТОВ ФЛАВОНОИДОВ ИЗ КОМПРЕССИОННОЙ ДРЕВЕСИНЫ ОСИНЫ
* - соответствует номеру зоны сбора фракций, изображенной на фиг.2.
Таблица 1. Результаты исследования фракций экстракта компрессионной древесины осины на этилпиридиновой неподвижной фазе, выделенных методом СФХ.
СПОСОБ ПОЛУЧЕНИЯ ЧИСТЫХ ПРЕПАРАТОВ ФЛАВОНОИДОВ ИЗ КОМПРЕССИОННОЙ ДРЕВЕСИНЫ ОСИНЫ
* - соответствует номеру зоны сбора фракций, изображенной на фиг.3.
Таблица 2. Результаты исследования фракций экстракта компрессионной древесины осины на диольной неподвижной фазе, выделенных методом СФХ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЧИСТЫХ ПРЕПАРАТОВ ЛИГНАНОВ ИЗ КОМПРЕССИОННОЙ ДРЕВЕСИНЫ | 2024 |
|
RU2827101C1 |
| Биологически активная добавка к пище, обладающая антипаразитарной активностью | 2016 |
|
RU2621256C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2011 |
|
RU2456015C1 |
| Синтез сложных эфиров флавоноидов нарингенина, кверцетина, гесперетина | 2022 |
|
RU2800457C1 |
| ТРАНСГЕННОЕ РАСТЕНИЕ ОСИНЫ С ПОВЫШЕННОЙ ПРОДУКТИВНОСТЬЮ И МОДИФИЦИРОВАННОЙ ДРЕВЕСИНОЙ | 2013 |
|
RU2593722C2 |
| ТРАНСГЕННОЕ РАСТЕНИЕ ОСИНЫ С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ ЦЕЛЛЮЛОЗЫ В ДРЕВЕСИНЕ | 2014 |
|
RU2599445C2 |
| Региоселективный энзимный синтез производных кверцетина и мирицетина | 2022 |
|
RU2806073C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ОЛИГОСАХАРИДОВ | 2015 |
|
RU2600133C1 |
| Средство для лечения воспалительных заболеваний верхних и нижних дыхательных путей. | 2017 |
|
RU2688688C2 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ СИНЕРГЕТИЧЕСКАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2677030C2 |
Изобретение относится к фармацевтической промышленности, а именно к способам выделения флавоноидов. Способ получения чистых препаратов флавоноидов из компрессионной древесины включает подготовку сырья, выделение экстрактивных веществ с последующим получением индивидуальных компонентов, при этом в качестве сырья используют компрессионную древесину осины европейской Populus tremula, которую высушивают, измельчают до размера частиц не более 1 мм и далее сушат в вакуумном сушильном шкафу при температуре 40°С. Затем полученные сухие опилки экстрагируют в аппарате Сокслета в две стадии: гексаном и ацетоном по 10 ч каждая. Далее ацетоновый экстракт упаривают на роторном испарителе до минимального объема, добавляют пятикратный избыток деионизованной воды до получения суспензии и подвергают лиофильной сушке. Затем выделение чистых препаратов флавоноидов осуществляют методом сверхкритической флюидной хроматографии с разделением на модифицированных силикагелевых сорбентах, содержащих этилпиридиновые или диольные привитые группы, с получением препаратов флавоноидов с чистотой не менее 80%. Предлагаемый способ получения чистых препаратов флавоноидов из компрессионной древесины обеспечивает высокий выход чистых препаратов флавоноидов. 4 ил., 2 табл., 1 пр.
Способ получения чистых препаратов флавоноидов из компрессионной древесины, заключающийся в подготовке используемого сырья, выделении экстрактивных веществ с последующим получением индивидуальных компонентов, отличающийся тем, что в качестве сырья используют компрессионную древесину осины европейской Populus tremula, подготовку которой проводят высушиванием, измельчением до размера частиц не более 1 мм и последующей сушкой в вакуумном сушильном шкафу при температуре 40°С, после чего полученные сухие опилки экстрагируют в аппарате Сокслета в две стадии: гексаном и ацетоном по 10 ч каждая, далее ацетоновый экстракт упаривают на роторном испарителе до минимального объема, добавляют пятикратный избыток деионизованной воды до получения суспензии и подвергают лиофильной сушке, а для выделения чистых препаратов флавоноидов используют метод сверхкритической флюидной хроматографии с разделением на модифицированных силикагелевых сорбентах, содержащих этилпиридиновые или диольные привитые группы, позволяющих получать препараты флавоноидов с чистотой не менее 80%.
| СПОСОБ КОНЦЕНТРИРОВАНИЯ И РАЗДЕЛЕНИЯ ФЛАВОНОИДОВ | 2016 |
|
RU2646805C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЧИСТЫХ ПРЕПАРАТОВ ЛИГНАНОВ ИЗ КОМПРЕССИОННОЙ ДРЕВЕСИНЫ | 2024 |
|
RU2827101C1 |
| WO 2008121021 A1, 09.10.2008 | |||
| СПОСОБ ДИАГНОСТИКИ НАЧАЛЬНЫХ НАРУШЕНИЙ МАТОЧНОГО КРОВОТОКА ВО ВТОРОЙ ПОЛОВИНЕ БЕРЕМЕННОСТИ | 2006 |
|
RU2310379C1 |
| ОНУЧИНА А.А., ФАЛЁВА А.В., УЛЬЯНОВСКИЙ Н.В | |||
| "Компрессионная древесина - перспективный источник ценных биологически активных соединений", ХИМИЯ И ТЕХНОЛОГИЯ РАСТИТЕЛЬНЫХ ВЕЩЕСТВ, Тезисы докладов XII Всероссийской научной конференции с | |||
Авторы
Даты
2025-04-04—Публикация
2024-10-31—Подача