Область техники, к которой относится изобретение
[0001] Настоящее раскрытие сущности, в общем, относится к устройствам, способам и системам для доставки терапевтических агентов, таких как химические соединения, композиции, клетки или клеточные продукты, такие как экзосомы. В неограничивающем примере, устройства, предусмотренные в настоящем документе, имеют возможности дозируемой инфузии и выполнены с возможностью доставлять агенты внесосудисто в целевые местоположения внутри пациента при поддержании позиционной стабильности.
Уровень техники
[0002] Клеточная терапия представляет собой процесс терапии, в котором клеточный материал инъецируется в пациента для терапевтического эффекта для лечения множества различных заболеваний, в частности, чтобы нацеливаться на избранные органы в теле пациента. В некоторой клеточной терапии, клеточный материал может извлекаться из пациента, обработанного для терапевтического эффекта, и повторно инъецироваться в пациента в участке лечения или доставки. В определенных случаях, для успешной доставки клеток, инъецируемые клетки типично должны также представлять собой интактные живые клетки. Доставка клеточных терапий может осуществляться несколькими различными способами, к примеру, через внутрисосудистую доставку или внесосудистую доставку. Внутрисосудистая доставка заключает в себе клеточную терапию, которая инфузируется через сосудистый доступ. Нацеливание на определенные органы для лечения посредством этого процесса может осуществляться множеством способов. Тем не менее, эффективность может быть низкой, и время пребывания терапевтического клеточного материала, предоставленного в орган(ы), может быть коротким вследствие промывания, которое тело пациента выполняет естественно.
Сущность изобретения
[0003] В данном документе предусмотрены, в числе прочего, устройства, способы и системы для доставки терапевтических агентов, таких как химические соединения, композиции, клетки и клеточные продукты. В конкретных вариантах осуществления, устройства и системы, предусмотренные данном документе, выполнены с возможностью применения клеточной терапии. В конкретных вариантах осуществления, устройства и системы, предусмотренные в настоящем документе, включают в себя возможности дозируемой инфузии. В конкретных вариантах осуществления, устройства и системы, предусмотренные данном документе, выполнены с возможностью доставлять терапевтический агент внесосудисто в целевое местоположение внутри пациента, такое как внутренняя часть органа, при поддержании позиционной стабильности. Например, в одном примерном варианте осуществления, предусмотрено устройство доставки клеточной терапии, которое включает в себя корпус, имеющий актуатор, резервуар для текучей среды с текучей средой в нем и механизм доставки текучей среды. В конкретных вариантах осуществления, съемная инъекционная игла протягивается дистально из корпуса, и механизм доставки текучей среды выполнен с возможностью доставлять непрерывный поток или болюсы текучей среды через инъекционную иглу. В конкретных вариантах осуществления, орган представляет собой почки. В конкретных вариантах осуществления, у пациента рак, и орган содержит опухоль.
[0004] Устройство может иметь множество варьирований. В конкретных вариантах осуществления, механизм доставки текучей среды может включать в себя электромеханическую систему, имеющую центральный процессор и насос. В конкретных вариантах осуществления, устройство также может включать в себя клапан, который выполнен с возможностью перемещаться в пространстве проксимально и дистально параллельно инъекционной игле во время размещения устройства и доставки текучей среды. В конкретных вариантах осуществления, клапан может быть выполнен с возможностью перемещаться в пространстве приблизительно на 2 см дистально и проксимально. В конкретных вариантах осуществления, устройство может включать в себя приемное устройство для текучей среды, выполненное с возможностью съемно и с возможностью замены принимать резервуар для текучей среды. В конкретных вариантах осуществления, резервуар для текучей среды может включать в себя, по меньшей мере, один картридж, который включает в себя известную дозировку текучей среды. В конкретных вариантах осуществления, приемное устройство для текучей среды может быть выполнено с возможностью принимать один или более (например, 1, 2, 3, 4 или 5) картриджей асептически. В конкретных вариантах осуществления, приемное устройство для текучей среды может быть выполнено с возможностью принимать несколько картриджей последовательно (например, содержимое одного картриджа используется, картридж вынимается, и затем один или более дополнительных картриджей вставляются по мере необходимости, чтобы продолжать дозирование). В конкретных вариантах осуществления, приемное устройство для текучей среды может быть выполнено с возможностью принимать множество картриджей параллельно. В конкретных вариантах осуществления, текучая среда может включать в себя терапевтические клетки или клеточные продукты для лечения заболевания почек. В конкретных вариантах осуществления, текучая среда может включать в себя противораковый агент для лечения рака. В конкретных вариантах осуществления, устройство может включать в себя сенсорный дисплей, который может быть выполнен с возможностью управлять работой устройства. В конкретных вариантах осуществления, дисплей может быть выполнен с возможностью задавать одни или более параметров для доставки текучей среды, включающих в себя, по меньшей мере, одно из давления и объема. В конкретных вариантах осуществления, дисплей может быть выполнен с возможностью предоставлять информацию раздачи в реальном времени текучей среды во время доставки. В конкретных вариантах осуществления, актуатор может представлять собой одно из спусковой собачки, плунжера, переключателя или кнопки. В конкретных вариантах осуществления, устройство также может включать в себя зацепляющий признак на дистальном конце корпуса, выполненный с возможностью съемно зацеплять троакар.
[0005] В аспекте, предусмотрен троакар, который включает в себя удлиненный корпус с проскимальным и дистальным концами. В конкретных вариантах осуществления, корпус имеет головку на проксимальном конце, удлиненный вал, протягивающийся дистально из головки, и просвет, протягивающийся из проксимального конца к дистальному концу через него. В конкретных вариантах осуществления, средство стабилизации предоставляется на дистальной части удлиненного вала и выполнено с возможностью стабилизировать дистальный конец удлиненного корпуса относительно поверхности ткани.
[0006] Троакар может иметь множество варьирований. В конкретных вариантах осуществления, средство стабилизации может включать в себя один или более зацепляющих компонентов, которые выполнены с возможностью раскрываться, чтобы схватывать с возможностью расцепления поверхность ткани при приведении в действие. В конкретных вариантах осуществления, зацепляющие компоненты могут включать в себя множество ножек. В конкретных вариантах осуществления, ножки могут иметь микрокрючки. В конкретных вариантах осуществления, зацепляющие компоненты могут включать в себя, по меньшей мере, одно из адгезива, присоски и зажима. В конкретных вариантах осуществления, троакар может включать в себя съемный стилет, выполненный с возможностью протягиваться через просвет удлиненного корпуса. В конкретных вариантах осуществления, стилет выполнен с возможностью приводить в действие зацепляющие компоненты при вынимании. В конкретных вариантах осуществления, по меньшей мере, часть удлиненного вала может быть выполнена с возможностью перемещаться в пространстве дистально и проксимально параллельно продольной оси удлиненного вала. В конкретных вариантах осуществления, по меньшей мере, часть удлиненного вала может быть выполнена с возможностью перемещаться в пространстве приблизительно на 2 см дистально и проксимально.
[0007] В аспекте, предусмотрен способ доставки фармацевтического состава на основе текучей среды в ткань, который включает в себя присоединение инъекционного устройства в троакар. В конкретных вариантах осуществления, троакар имеет просвет через себя и стилет, позиционированный в нем. В конкретных вариантах осуществления, способ также включает в себя соединение источника текучей среды с инъекционным устройством и продвижение инъекционного устройства и троакара через внешнюю поверхность ткани пациента и обеспечение проникновения через внутренний целевой участок тканей. В конкретных вариантах осуществления, способ дополнительно включает в себя вынимание стилета из троакара и расцепление инъекционного устройства и троакара и присоединение инъекционной иглы к инъекционному устройству. В конкретных вариантах осуществления, способ также включает в себя вставку инъекционной иглы через троакар в целевой участок тканей и приведение в действие инъекционного устройства, чтобы доставлять непрерывный поток или болюсы текучей среды из источника текучей среды через инъекционную иглу и в целевой участок тканей. В конкретных вариантах осуществления, фармацевтический состав на основе текучей среды содержит, состоит по существу из или состоит из популяции клеток либо их продукта для фармацевтически приемлемого носителя текучей среды. В конкретных вариантах осуществления, клеточная терапия содержит стволовые клетки, клетки-предшественники, первичные клетки или клеточную линию. В конкретных вариантах осуществления, целевой участок тканей представляет собой почки. В конкретных вариантах осуществления, у пациента заболевание почек. В конкретных вариантах осуществления, заболевание почек представляет собой хроническое заболевание почек. В конкретных вариантах осуществления, клеточная терапия содержит биоактивные клетки почечного эпителия. В конкретных вариантах осуществления, клеточная терапия содержит выбранные клетки почечного эпителия. В конкретных вариантах осуществления, клеточная терапия содержит жидкий состав, содержащий клетки и температурочувствительный биоматериал. В конкретных вариантах осуществления, клеточная терапия представляет собой неопочечную аугментацию (NKA). В конкретных вариантах осуществления, клетки имеют форму сфероидов или клеточных кластеров. В конкретных вариантах осуществления, фармацевтический состав на основе текучей среды содержит клеточный продукт, к примеру, пузырек, например, микропузырек или экзосому. В конкретных вариантах осуществления, фармацевтический состав на основе текучей среды содержит химическое соединение. В конкретных вариантах осуществления, фармацевтический состав на основе текучей среды содержит противораковый агент. В конкретных вариантах осуществления, у пациента рак. В конкретных вариантах осуществления, целевой участок тканей представляет собой опухоль.
[0008] Способ может варьироваться множеством способов. Например, способ дополнительно может включать в себя, до вставки инъекционной иглы через троакар, раскрывание средства стабилизации на дистальной части троакара, с тем чтобы стабилизировать дистальный конец троакара относительно целевого участка тканей. В конкретных вариантах осуществления, раскрытие средства стабилизации может приводиться в действие посредством вынимания стилета. В конкретных вариантах осуществления, способ также может включать в себя убирание инъекционной иглы во время доставки текучей среды (например, ее непрерывного потока или болюсов). В конкретных вариантах осуществления, способ дополнительно может включать в себя, во время приведения в действие инъекционного устройства, стабилизацию инъекционного устройства с использованием перемещающегося в пространстве клапана и стабилизацию троакара с использованием сжимающей пружинной секции троакара.
Краткое описание чертежей
[0009] Изобретение должно лучше пониматься из нижеприведенного подробного описания, рассматриваемого в сочетании с прилагаемыми чертежами, на которых:
[0010] Фиг. 1 иллюстрирует вид пациента в позиции лежа;
[0011] Фиг. 2 иллюстрирует вид пациента в поперечной позиции;
[0012] Фиг. 3 иллюстрирует схему, подробно показывающую примерный процесс для применения предлагаемых на рынке устройств для лечения исследуемого объекта;
[0013] Фиг. 4A иллюстрирует вариант осуществления использования предлагаемых на рынке устройств, чтобы доставлять лечение в пациента в соответствии с процессом по фиг. 3;
[0014] Фиг. 4B и C иллюстрируют варианты осуществления предлагаемых на рынке устройств для доставки лечения в пациента в соответствии с процессом по фиг. 3;
[0015] Фиг. 5 иллюстрирует вид сбоку одного варианта осуществления троакара;
[0016] Фиг. 6 иллюстрирует вид сбоку одного варианта осуществления канюли;
[0017] Фиг. 7 иллюстрирует вид сбоку одного варианта осуществления инъекционного устройства с троакаром, присоединяемым к нему, который имеет вставленный стилет;
[0018] Фиг. 8 иллюстрирует упрощенную схему профиля болюсной доставки текучей среды;
[0019] Фиг. 9 иллюстрирует упрощенную схему профиля непрерывной доставки текучей среды;
[0020] Фиг. 10 иллюстрирует один вариант осуществления картриджа;
[0021] Фиг. 11 иллюстрирует вид сбоку троакара по фиг. 7;
[0022] Фиг. 12 иллюстрирует вид сбоку раскрывающегося троакара по фиг. 7;
[0023] Фиг. 13 иллюстрирует вид сбоку варианта осуществления вставляемого троакара;
[0024] Фиг. 14 иллюстрирует вид сбоку раскрывающегося троакара по фиг. 13;
[0025] Фиг. 15 иллюстрирует вид сбоку раскрывающегося троакара по фиг. 13;
[0026] Фиг. 16A иллюстрирует вид сбоку одного варианта осуществления раскрывающегося анкера для гипсокартона;
[0027] Фиг. 16B иллюстрирует вид сбоку раскрывающегося анкера для гипсокартона по фиг. 16A;
[0028] Фиг. 16C иллюстрирует вид сбоку раскрывающегося анкера для гипсокартона по фиг. 16B;
[0029] Фиг. 16D иллюстрирует вид сбоку раскрывающегося анкера для гипсокартона по фиг. 16C;
[0030] Фиг. 17 иллюстрирует дистальный вид одного варианта осуществления иглы с поверхностными признаками;
[0031] Фиг. 18A иллюстрирует вид со стороны дистального наконечника одного варианта осуществления стилета;
[0032] Фиг. 18B иллюстрирует вид со стороны дистального наконечника другого варианта осуществления стилета;
[0033] Фиг. 18C иллюстрирует вид со стороны дистального наконечника другого варианта осуществления стилета;
[0034] Фиг. 18D иллюстрирует вид со стороны дистального наконечника другого варианта осуществления стилета;
[0035] Фиг. 19 иллюстрирует упрощенную схему одного варианта осуществления инъекционной иглы;
[0036] Фиг. 20 иллюстрирует вид сбоку в сечении капсулы почечного тельца;
[0037] Фиг. 21 иллюстрирует схему, связанную с выявлением оптимального размера игл;
[0038] Фиг. 22 иллюстрирует дистальный конец инъекционной иглы с линейкой;
[0039] Фиг. 23 иллюстрирует дистальный конец инъекционной иглы по фиг. 22 с линейкой, четко указывающей размещение прорези в дистальном конце;
[0040] Фиг. 24 иллюстрирует примерный способ удерживания небольшого шприца для лучшего управления;
[0041] Фиг. 25 иллюстрирует упрощенный вид в поперечном сечении размещения троакара по фиг. 7 в почке;
[0042] Фиг. 26 иллюстрирует упрощенный вид в поперечном сечении размещения троакара по фиг. 7 в почке по фиг. 25;
[0043] Фиг. 27A-F иллюстрируют вариант осуществления доставки нескольких болюсов терапевтического агента в почку.
[0044] Следует понимать, что вышеуказанные чертежи необязательно должны быть нарисованы в масштабе, представляя в определенной степени упрощенное представление различных предпочтительных признаков, иллюстрирующих базовые принципы раскрытия сущности. Конкретные конструктивные признаки настоящего раскрытия сущности, включающие в себя, например, конкретные размеры, ориентации, местоположения и формы, должны определяться частично посредством конкретного намеченного варианта применения и окружения использования.
Подробное описание изобретения
[0045] Далее подробно описываются примерные варианты осуществления настоящего раскрытия сущности со ссылкой на прилагаемые чертежи. Специалисты в данной области техники должны осознавать, что описанные варианты осуществления могут модифицироваться различными способами без отступления от сущности или объема настоящего раскрытия сущности. Дополнительно, во всем подробном описании, аналогичные ссылки с номерами означают аналогичные элементы.
[0046] Терминология, используемая в данном документе, служит только для цели описания конкретных вариантов осуществления и не имеет намерение ограничивать раскрытия сущности. При использовании в данном документе, формы единственного числа "a", "an" и "the" служат для того, чтобы включать в себя также формы множественного числа, если контекст явно не указывает иное. Следует дополнительно понимать, что термины "содержит" и/или "содержащий" при использовании в данном подробном описании задают наличие изложенных признаков, целых частей, этапов, операций, элементов или компонентов, однако не препятствуют наличию или добавлению одного или более других признаков, целых частей, этапов, операций, элементов, компонентов или их групп. При использовании в данном документе, термин "и/или" включает в себя все без исключения комбинации одного или более из ассоциированных перечисленных элементов. Термины, обозначающие связывание, такие как "соединенный муфтовым способом", "зацепленный" и т.д., обозначают физическую взаимосвязь между двумя компонентами, за счет чего компоненты либо непосредственно соединяются между собой, либо косвенно соединяются через один или более промежуточных компонентов.
[0047] Следует понимать, что термин "пациент" или другой аналогичный термин при использовании в данном документе охватывает любой исследуемый объект (человека или животное), для которого может выполняться терапия, раскрытая в данном документе. Термин "пользователь" при использовании в данном документе охватывает любой объект, допускающий взаимодействие с или управление устройством. "Пользователь" также может представлять собой "пациента", либо "пользователь" и "пациент" могут представлять собой отдельные объекты, как описано в данном документе. В конкретных вариантах осуществления, исследуемый объект представляет собой живое животное. В конкретных вариантах осуществления, исследуемый объект представляет собой млекопитающее, такое как собака, кошка, лошадь, кролик, зоопарковое животное, корова, свинья, овца, коза, верблюд, мышь, крыса или морская свинка. В конкретных вариантах осуществления, исследуемый объект представляет собой примата, такого как человек, шимпанзе, орангутанг, обезьяна или бабуин. В конкретных вариантах осуществления, исследуемый объект представляет собой человека. В конкретных вариантах осуществления, исследуемый объект представляет собой пациента, подходящего для лечения, который испытывает либо испытывал один или более признаков, симптомов либо других индикаторов заболевания почек. Такие исследуемые объекты включают в себя, без ограничения, исследуемые объекты, которые диагностируются в первый раз или диагностируются ранее и теперь испытывают рецидив или обострение либо подвержены риску заболевания почек, вне зависимости от причины. В конкретных вариантах осуществления, исследуемый объект, возможно, ранее лечился от заболевания почек либо не лечился от него. В конкретных вариантах осуществления, исследуемый объект имеет диабет. В конкретных вариантах осуществления, исследуемый объект имеет диабет первого типа. В конкретных вариантах осуществления, исследуемый объект имеет диабет второго типа. В конкретных вариантах осуществления, исследуемый объект имеет хроническое заболевание почек. В конкретных вариантах осуществления, исследуемый объект имеет врожденную аномалию почки и/или мочевыводящего тракта. В конкретных вариантах осуществления, исследуемый объект представляет собой человека с врожденными аномалиями почки и мочевыводящего тракта. В конкретных вариантах осуществления, исследуемый объект испытывает либо испытывал один или более признаков, симптомов либо других индикаторов связанного с органом заболевания, такого как заболевание почек, анемия или недостаток эритропоэтина (EPO). В конкретных вариантах осуществления, исследуемый объект не имеет диабета. В конкретных вариантах осуществления, исследуемый объект не имеет диабета первого типа. В конкретных вариантах осуществления, исследуемый объект не имеет диабета второго типа. В конкретных вариантах осуществления, исследуемый объект не имеет заболевания почек. В конкретных вариантах осуществления, исследуемый объект имеет рак. В конкретных вариантах осуществления, рак содержит твердую опухоль.
[0048] В одном аспекте устройства, системы и способы, представленные в настоящем документе, применимы для введения пациенту противоракового агента или химиотерапии. В некоторых вариантах осуществления введение противоракового средства включает доставку противоракового средства или химиопрепарата во внутреннюю ткань или орган исследуемого объекта. В некоторых вариантах осуществления у пациента имеется солидная опухоль. В некоторых вариантах реализации солидная опухоль находится внутри, на, прорастает или является частью органа. В некоторых вариантах осуществления участок внутренней ткани или орган представляет собой почку, легкое, сердце, селезенку, желудок, поджелудочную железу, мочевой пузырь, головной мозг, тонкую кишку, толстую кишку, прямую кишку, аппендикс, яичник, матку, пищевод, печень, желчный пузырь, щитовидную железу, паращитовидную железу, надпочечник, грудь, лимфатический узел, мышцу, спинной мозг, яичко, простату, глотку, гортань, кость или трахею. В некоторых вариантах осуществления исследуемый объект болен раком. В некоторых вариантах осуществления рак представляет собой меланому (например, метастатическую меланому, распространившуюся во внутреннее местоположение, такое как орган), нейроэндокринную опухоль, карциному или саркому. В некоторых вариантах осуществления у пациента имеется саркома, рак мочевого пузыря, рак кости, опухоль головного мозга, рак шейки матки, рак толстой кишки, рак пищевода, рак желудка, рак головы и шеи, рак почки, миелома, рак щитовидной железы, лейкемия, рак предстательной железы, рак молочной железы (например, тройной негативный, эстроген-рецептор (ER) положительный, ER-отрицательный, устойчивый к химиотерапии, устойчивый к герцептину, HER2-положительный, устойчивый к доксорубицину, устойчивый к тамоксифену, протоковая карцинома, лобулярная карцинома, первичный или метастатический рак молочной железы), рак яичников, рак поджелудочной железы, рак печени (например, гепатоцеллюлярная карцинома), рак легкого (например, немелкоклеточная карцинома легкого, плоскоклеточная карцинома легкого, аденокарцинома, крупноклеточная карцинома легкого, мелкоклеточная карцинома легкого, карциноид или саркома), глиобластома multiforme, глиома, меланома, рак предстательной железы, резистентный к кастрации рак предстательной железы, глиобластома, рак яичников, рак легких, плоскоклеточный рак (например, головы, шеи или пищевода) или колоректальный рак. В некоторых вариантах реализации у исследуемого объекта имеется рак щитовидной железы, эндокринной системы, головного мозга, молочной железы, шейки матки, толстой кишки, головы и шеи, пищевода, печени, почки, легкого, немелкоклеточного легкого, меланомы, саркомы, желудка, медуллобластома матки, нейробластома, глиома, глиобластома multiforme, рак яичников, рабдомиосаркома, первичный тромбоцитоз, первичная макроглобулинемия, первичная опухоль головного мозга, злокачественная инсулинома поджелудочной железы, злокачественный карциноид, рак мочевого пузыря, рак яичка, рак щитовидной железы, рак пищевода, рак мочеполового тракта, злокачественная гиперкальциемия, рак эндометрия, рак надпочечников, медуллярный рак щитовидной железы, медуллярный рак щитовидной железы, метастатическая меланома (например, меланома, которая распространилась на внутреннее местоположение, такое как орган), колоректальный рак, папиллярный рак щитовидной железы, гепатоцеллюлярная карцинома, болезнь Педжета соска, филлодная опухоль, дольковая карцинома, протоковая карцинома, рак звездчатых клеток поджелудочной железы, рак звездчатых клеток печени или рак предстательной железы. Термин "саркома" обычно относится к опухоли, которая состоит из вещества, подобного эмбриональной соединительной ткани, и обычно состоит из плотно упакованных клеток, встроенных в фибриллярное или гомогенное вещество. Саркомы, которые можно лечить с помощью устройства, системы или способа, представленных в настоящем документе, включают в себя хондросаркому, фибросаркому, лимфосаркому, меланосаркому, миксосаркому, остеосаркому, саркому Абемети, жировую саркому, липосаркому, альвеолярную саркому мягких тканей, амелобластическую саркому, ботриоидную саркому, хлоромную саркому, хориокарциному, эмбриональную саркому, опухоль Вильмса, саркому эндометрии, стромальную саркому, саркому Юинга, фасциальную саркому, фибробластную саркому, гигантоклеточную саркому, гранулоцитарную саркому, саркому Ходжкина, идиопатическую множественную пигментную геморрагическую саркому, лимфобластную саркому В-клеток, иммунобластную саркому Т-клеток, саркому Дженсена, саркому Капоши, саркому клеток Купфера, ангиосаркому, лейкосаркому, злокачественную саркому мезенхимомы, паростальную саркому, ретикулоцитарную саркому, саркому Рауса, серокистозную саркому, синовиальную саркому или телеангиоэктальтическую саркому. Термин "меланома" обычно относится к опухоли, возникающей из меланоцитарной системы кожи и других органов. Меланомы, которые можно лечить с использованием устройства, системы или способа, представленных в настоящем документе, включают в себя, например, акрально-лентигинозную меланому, амеланотную меланому, доброкачественную ювенильную меланому, меланому Клаудмана, меланому S91, меланому Хардинга-Пасси, ювенильную меланому, меланома типа злокачественного лентиго, злокачественную меланому, узловую меланому, подногтевую меланому или поверхностно распространяющуюся меланому. В некоторых вариантах осуществления меланома представляет собой метастатическую меланому, распространившуюся во внутреннее местоположение (например, в орган или лимфатический узел) пациента. Термин "карцинома" относится к злокачественному новообразованию, состоящему из эпителиальных клеток, имеющих тенденцию инфильтрировать окружающие ткани и вызывать метастазы. Типичные карциномы, которые можно лечить с использованием устройства, системы или способа, представленных в настоящем документе, включают в себя, например, медуллярную карциному щитовидной железы, семейную медуллярную карциному щитовидной железы, ацинарную карциному, ацинозную карциному, аденокистозную карциному, аденоидно-кистозную карциному, аденоматозную карциному, карциному коры надпочечников, альвеолярную карциному, альвеолярно-клеточную карциному, базально-клеточную карциному, базально-клеточную карциному, базально-плоскоклеточную карциному, бронхиоальвеолярную карциному, бронхиолярную карциному, бронхогенную карциному, церебриформную карциному, холангиоцеллюлярную карциному, хорионическую карциному, коллоидную карциному, комедоновую карциному, корпусную карциному карцинома, рак в кирасе, рак кожи, цилиндрическую карциному, цилиндроклеточную карциному, протоковую карциному, протоковую карциному, карциному твердой оболочки, эмбриональную карциному, энцефалоидную карциному, эпидермоидную карциному, эпителиальную карциному аденоиды, экзофитную карциному, экс-язвенную карциному, фиброзную карциному, желатиниформную карциному, студенистую карциному, гигантоклеточную карциному, гигантоцеллюлярную карциному, железистую карциному, гранулезоклеточную карциному, карциному волосяного матрикса, гематоидную карциному, гепатоцеллюлярную карциному, карциному из клеток Гертла, гиалиновую карциному, гипернефроидную карциному, младенческая эмбриональную карциному, карциному in situ, внутриэпидермальную карциному, внутриэпителиальную карциному, карциному Кромпечера, карциному Кульчицкого, крупноклеточную карциному, лентикулярную карциному, лентикулярную карциному, липоматозную карциному, лобулярную карциному, лимфоэпителиальную карциному, карциному медуллярную, медуллярную карциному, меланотическую карциному, карциному неба, муцинозную карциному, карциному муципарум, карциному мукоцеллюлярную, мукоэпидермоидную карциному, карциному слизистой, слизистую карциному, миксоматозную карциному, назофарингеальную карциному, овсяноклеточную карциному, оссифицирующую карциному, остеоидную карциному, папиллярную карциному, перипортальную карциному, преинвазивную карциному, щипцово-клеточную карциному, пузырчатую карциному, почечно-клеточную карциному почки, резервно-клеточную карциному, саркоматодную карциному, Шнайдериан карциному, скиррозную карциному, карциному мошонки, перстневидно-клеточную карциному, простую карциному, мелкоклеточную карциному, соланоидную карциному, сфероидально-клеточную карциному, веретеноклеточную карциному, губчатую карциному, плоскоклеточный рак, плоскоклеточный рак, струнный рак, телеангиэктатическую карциному, карциному телеангиэктозы, переходно-клеточную карциному, бугорчатую карциному, тубулярную карциному, туберозную карциному, веррукозную карциному или ворсинчатую карциному.
[0049] "Противораковое средство" представляет собой терапевтическое средство, используемое для лечения или профилактики рака. В некоторых вариантах осуществления противораковое средство может представлять собой большую молекулу (например, белок или другое органическое соединение с молекулярной массой не менее 2000 дальтон) или малую молекулу (например, органическое соединение с молекулярной массой менее 2000 дальтон). Примеры противораковых средств включают в себя антитела, малые молекулы и большие молекулы или их комбинации. В некоторых вариантах осуществления противораковый агент содержит клетку, такую как иммунная клетка. В некоторых вариантах осуществления иммунная клетка была модифицирована (например, генетически и/или посредством воздействия опухолевого антигена) для атаки или стимуляции иммунного ответа на опухолевые клетки. В некоторых вариантах осуществления иммунная клетка представляет собой Т-клетку (такую как Т-клетка CD4, Т-клетка CD8 или их комбинация) или дендритную клетку (такую как плазмацитоидная дендритная клетка). В некоторых вариантах осуществления иммунная клетка была генетически модифицирована, например Т-клетка с химерным антигенным рецептором (CAR). В некоторых вариантах осуществления противораковый агент ингибирует рост или пролиферацию клеток. В некоторых вариантах осуществления противораковое средство представляет собой химиотерапевтическое средство. В некоторых вариантах осуществления противораковое средство представляет собой указанное в настоящем документе средство, применимое в способах лечения рака. В некоторых вариантах осуществления противораковое средство представляет собой средство, одобренное Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) или аналогичным регулирующим органом страны, отличной от США, для лечения рака. Примеры противораковых средств включают в себя, но не ограничиваются ими, ингибиторы MEK (например, MEK1, MEK2 или MEK1 и MEK2) (например, XL518, CI-1040, PD035901, селуметиниб/AZD6244, GSK1120212/траметиниб, GDC-0973, ARRY-162, ARRY-300, AZD8330, PD0325901, U0126, PD98059, TAK-733, PD318088, AS703026, BAY 869766), алкилирующие агенты (например, циклофосфамид, ифосфамид, хлорамбуцил, бусульфан, мелфалан, мехлорэтамин, тиоуроститемин, ураиомустин азотистые иприты (например, мехлорэтамин, циклофосфамид, хлорамбуцил, мейфалан), этиленимин и метилмеламины (например, гексаметилмеламин, тиотепа), алкилсульфонаты (например, бусульфан), нитрозомочевины (например, кармустин, ломуситне, семустин, стрептозоцин), триазены (декарбазин)), антиметаболиты (например, 5-азатиоприн, лейковорин, капецитабин, флударабин, гемцитабин, пеметрексед, ралтитрексед, аналог фолиевой кислоты (например, метотрексат) или аналоги пиримидина (например, фторурацил, флоксуридин, цитарабин), аналоги пуринов (например, меркаптопурин, тиогуанин, пентостатин) и т.д.), растительные алкалоиды (например, винкристин, винбластин, винорелбин, виндезин, подофиллотоксин, паклитаксел, доцетаксел и т.д.), ингибиторы топоизомеразы (например, иринотекан, топотекан, амсакрин, этопозид (VP16), этопозид фосфат, тенипозид и др.), противоопухолевые антибиотики (например, доксорубицин, адриамицин, даунорубицин, эпирубицин, актиномицин, блеомицин, митомицин, митоксантрон, пликамицин и др.), препараты на основе соединения платины или платиносодержащие агенты (например, цисплатин, оксалоплатин, карбоплатин), антрацендион (например, митоксантрон), замещенную мочевину (например, гидроксимочевина), производное метилгидразина (например, прокарбазин), адренокортикальный супрессант (например, митотан, аминоглютетимид), эпиподофиллотоксины (например, этопозид), антибиотики (например, даунорубицин, доксорубицин, блеомицин), ферменты (например, L-аспарагиназа), ингибиторы передачи сигналов митоген-активируемой протеинкиназы (например, U0126, PD98059, PD184352, PD0325901, ARRY-142886, SB239063, SP600125, BAY 43-9006 или вортманнин LY294002), ингибиторы Syk, ингибиторы mTOR, антитела (например, ритуксан), госсифол, генасенс, полифенол Е, хлорофузин, полностью транс-ретиноевую кислоту (ATRA), бриостатин, лиганд, индуцирующий апоптоз, связанный с фактором некроза опухоли (TRAIL), 5-аза-2'-дезоксицитидин, полностью транс-ретиноевую кислоту, доксорубицин, винкристин, этопозид, гемцитабин, иматиниб (Гливек®), гельданамицин, 17-N-аллиламино-17-деметоксигельданамицин (17-AAG), флавопиридол, LY294002, бортезомиб, трастузумаб, BAY 11-7082, PKC412, PD184352, 20-эпи-1, 25- дигидроксивитамин D3; 5-этинилурацил; абиратерон; акларубицин; ацилфульвен; адеципенол; адозелезин; альдеслейкин; антагонисты ALL-TK; альтретамин; кислоту; амрубицин; амсакрин; анагрелид; анастрозол; андрографолид; ингибиторы ангиогенеза; антагонист Д; антагонист G; антареликс; антидорсализирующий морфогенетический белок-1; антиандроген, карцинома предстательной железы; антиэстроген; антинеопластон; антисмысловые олигонуклеотиды; афидиколин глицинат; модуляторы гена апоптоза; регуляторы апоптоза; апуриновую кислоту; ара-CDP-DL-PTBA; аргининдезаминазу; асулакрин; атаместан; атримустин; аксинастатин 1; аксинастатин 2; аксинастатин 3; азасетрон; азатоксин; азатирозин; производные баккатина III; баланол; батимастат; антагонисты BCR/ABL; бензохлорины; бензоилстауроспорин; производные бета-лактаму; бета-алетин; беталамицин В; бетулиновую кислоту; ингибитор bFGF; бикалутамид; бисантрен; бисазиридинилспермин; биснафид; бистратен А; бизелезин; брефлат; бропиримин; будотитан; бутионин сульфоксимин; кальципотриол; кальфостин С; производные камптотецина; оспа канареек ИЛ-2; капецитабин; карбоксамид-аминотриазол; карбоксиамидотриазол; КаРест М3; ЦАРН 700; ингибитор хрящевого происхождения; карцелезин; ингибиторы казеинкиназы (ICOS); кастаноспермин; цекропин В; цетрореликс; хлорины; хлорхиноксалинсульфонамид; цикапрост; цис-порфирин; кладрибин; аналоги кломифена; клотримазол; коллизмицин А; коллизмицин В; комбретастатин А4; аналог комбретастатина; конагенин; крамбесцидин 816; криснатол; криптофицин 8; производные криптофицина А; курацин А; циклопентантрахиноны; циклоплатам; ципемицин; цитарабин окфосфат; цитолитический фактор; цитостатин; дакликсимаб; децитабин; дегидродидемнин В; дезлорелин; дексаметазон; дексифосфамид; дексразоксан; дексверапамил; диазиквон; дидемнин В; дидокс; диэтилнорспермин; дигидро-5-азацитидин; 9-диоксамицин; дифенил спиромустин; докозанол; доласетрон; доксифлуридин; дролоксифен; дронабинол; дуокармицин SA; эбселен; экомустин; эдельфозин; эдреколомаб; эфлорнитин; элемен; эмифур; эпирубицин; эпистерид; аналог эстрамустина; агонисты эстрогена; антагонисты эстрогена; этанидазол; этопозидфосфат; экземестан; фадрозол; фазарабин; фенретинид; филграстим; финастерид; флавопиридол; флезеластин; флуастерон; фударабин; гидрохлорид фтордауноруцина; форфенимекс; форместан; фостриецин; фотемустин; гадолиний тексафирин; нитрат галлия; галоцитабин; ганиреликс; ингибиторы желатиназы; гемцитабин; ингибиторы глутатиона; гепсульфам; херегулин; гексаметилен бисацетамид; гиперицин; ибандроновую кислоту; идарубицин; идоксифен; идрамантон; илмофозин; иломастат; имидазоакридоны; имихимод; иммуностимулирующие пептиды; ингибитор рецептора инсулиноподобного фактора роста-1; агонисты интерферона; интерфероны; интерлейкины; иобенгуан; йододоксорубицин; ипомеанол, 4-; иропласт; ирсогладин; изобенгазол; изогомогаликондрин В; итасетрон; джасплакинолид; кахалалид F; ламелларин-N триацетат; ланреотид; лейнамицин; ленограстим; лентинана сульфат; лептолстатин; летрозол; фактор ингибирования лейкемии; лейкоцитарный альфа-интерферон; лейпролид+эстроген+прогестерон; лейпрорелин; левамизол; лиарозол; аналог линейного полиамина; липофильный дисахаридный пептид; липофильные соединения платины; лиссоклинамид 7; лобаплатин; ломбрицин; лометрексол; лонидамин; лосоксантрон; ловастатин; локсорибин; лартотекан; лютеций тексафирин; Лисоф линия; литические пептиды; майтанзин; манностатин А; маримастат; масопрокол; маспин; ингибиторы матрилизина; ингибиторы матричных металлопротеиназ; меногарил; мербароне; метрелин; метиониназа; метоклопрамид; ингибитор МИФ; мифепристон; милтефозин; миримостим; несовпадающую двухцепочечную РНК; митогуазон; митолактол; аналоги митомицина; митонафид; митотоксин фактор роста фибробластов - сапорин; митоксантрон; мофаротен; молграмостим; моноклональное антитело, хорионический гонадотропин человека; монофосфориловый липид А+клеточную стенку миобактерий sk; мопидамол; ингибитор гена множественной лекарственной устойчивости; терапию на основе множественного опухолевого супрессора 1; горчичное противораковое средство; микапероксид В; экстракт клеточной стенки микобактерий; мириапорон; N-ацетилдиналин; N-замещенные бензамиды; нафарелин; нагрестип; налоксон+пентазоцин; напавин; нафтерпин; нартограстим; недаплатин; неморубицин; неридроновую кислоту; нейтральную эндопептидазу; нилутамид; низамицин; модуляторы оксида азота; нитроксидный антиоксидант; нитрулин; 06-бензилгуанин; октреотид; окиценон; олигонуклеотиды; онапристон; ондансетрон; ондансетрон; орацин; пероральный индуктор цитокинов; ормаплатин; осатерон; оксалиплатин; оксауномицин; палауамин; пальмитоилризоксин; памидроновую кислоту; панакситриол; паномифен; парабактин; пазеллиптин; пегаспаргазу; пельдезин; пентозан полисульфат натрия; пентостатин; пентрозол; перфлуброн; перфосфамид; периллиловый спирт; феназиномицин; фенилацетат; ингибиторы фосфатазы; пицибанил; пилокарпина гидрохлорид; пирарубицин; пиритрексим; плацетин А; плацетин В; ингибитор активатора плазминогена; комплекс платины; соединения платины; платино-триаминовый комплекс; порфимер натрия; порфиромицин; преднизолон; пропил-бис-акридон; простагландин J2; ингибиторы протеасом; иммуномодулятор на основе белка А; ингибитор протеинкиназы С; ингибиторы протеинкиназы С, микроводоросли; ингибиторы протеинтирозинфосфатазы; ингибиторы пуриннуклеозидфосфорилазы; пурпурины; пиразолоакридин; конъюгат полиоксиэтилированного пиридоксилированного гемоглобина; антагонисты раф; ралтитрексед; рамосетрон; рас ингибиторы фарнезилпротеинтрансферазы; ингибиторы ras; ингибитор ras-GAP; ретеллиптин деметилированный; этидронат рения Re 186; ризоксин; рибозимы; RII ретинамид; роглетимид; рохитукин; ромертид; роквинимекс; рубигинон В 1; рубоксил; сафингол; сентопин; СарЧНУ; саркофитол А; сарграммостим; миметики Sdi-1; семустин; ингибитор старения 1; смысловые олигонуклеотиды; ингибиторы сигнальной трансдукции; модуляторы передачи сигнала; одноцепочечный антигенсвязывающий белок; сизофуран; собузоксан; борокаптат натрия; фенилацетат натрия; солвероль; белок, связывающий соматомедин; сонермин; спарфозиновую кислоту; спамицин D; спиромустин; спленентин; спонгистатин 1; скваламин; ингибитор стволовых клеток; ингибиторы деления стволовых клеток; стипиамид; ингибиторы стромелизина; сульфинозин; суперактивный антагонист вазоактивных интестинальных пептидов; сурадисту; сурамин; свайнсонин; синтетические гликозаминогликаны; таллимустин; тамоксифен метиодид; тавромустин; тазаротен; текогалан натрия; тегафур; теллурапирилий; ингибиторы теломеразы; темопорфин; темозоломид; тенипозид; тетрахлордекаоксид; тетразомин; талибластин; тиокоралин; тромбопоэтин; миметик тромбопоэтина; тималфазин; агонист рецептора тимопоэтина; тимотринан; тиреотропный гормон; этилэтиопурпурин олова; тирапазамин; титаноцен бихлорид; топсентин; торемифен; тотипотентный фактор стволовых клеток; ингибиторы трансляции; третиноин; триацетилуридин; трицирибин; триметрексат; трипторелин; трописетрон; туростерид; ингибиторы тирозинкиназы; тирфостины; ингибиторы UBC; убенимекс; фактор ингибирования роста урогенитального синуса; антагонисты урокиназного рецептора; вапреотид; вариолин В; векторную систему, генную терапию эритроцитов; веларезол; верамин; вердены; вертепорфин; винорелбин; винксалтин; витамин; ворозол; занотерон; зениплатин; зиласкорб; зиностатин стимулямер; адриамицин; дактиномицин; блеомицин; винбластин; цисплатин; ацивицин; акларубицин; акодазола гидрохлорид; акронин; адозелезин; альдеслейкин; альтретамин; амбомицин; ацетат аметантрона; аминоглютетимид; амсакрин; анастрозол; антрамицин; аспарагиназу; асперлин; азацитидин; азетепу; азотомицин; батимастат; бензодепу; бикалутамид; бисантрена гидрохлорид; биснафиде димезилат; бизелезин; блеомицина сульфат; бреквинар натрия; бропиримин; бусульфан; кактиномицин; калустерон; карацемид; карбетаймер; карбоплатин; кармустин; гидрохлорид карубицина; карцелезин; цедефингол; хлорамбуцил; циролемицин; кладрибин; криснатол мезилат; циклофосфамид; цитарабин; дакарбазин; даунорубицина гидрохлорид; децитабин; дексормаплатин; дезагуанин; дезагуанин мезилат; диазиквон; доксорубицин; доксорубицина гидрохлорид; дролоксифен; дролоксифена цитрат; дромостанолона пропионат; дуазомицин; эдатрексат; эфлорнитина гидрохлорид; эльсамитруцин; энлоплатин; энпромат; эпипропидин; эпирубицина гидрохлорид; эрбулозол; эзорубицина гидрохлорид; эстрамустин; эстрамустинфосфат натрия; этанидазол; этопозид; этопозидфосфат; этоприн; фадрозола гидрохлорид; фазарабин; фенретинид; флоксуридин; флударабин фосфат; фторурацил; фторцитабин; фосквидон; фостриецин натрия; гемцитабин; гемцитабина гидрохлорид; гидроксимочевину; идарубицина гидрохлорид; ифосфамид; имифозин; интерлейкин II (включая рекомбинантный интерлейкин II или rIL 2), интерферон альфа-2а; интерферон альфа-2b; интерферон альфа-nl; интерферон альфа-n3; интерферон бета-la; интерферон гамма-lb; ипроплатин; иринотекана гидрохлорид; ланреотида ацетат; летрозол; ацетат лейпролида; лиарозола гидрохлорид; лометрексол натрия; ломустин; лосоксантрона гидрохлорид; масопрокол; майтанзин; мехлорэтамина гидрохлорид; мегестрола ацетат; меленгестрола ацетат; мелфалан; меногарил; меркаптопурин; метотрексат; метотрексат натрия; метоприн; метуредепу; митиндомид; митокарцин; митокромин; митогиллин; митомальцин; митомицин; митоспир; митотан; митоксантрона гидрохлорид; микофеноловую кислоту; нокодазои; ногаламицин; ормаплатин; оксисуран; пегаспаргазу; пелиомицин; пентамустин; пепломицина сульфат; перфосфамид; пипоброман; пипосульфан; пироксантрона гидрохлорид; пликамицин; пломестан; порфимер натрия; порфиромицин; преднимустин; прокарбазина гидрохлорид; пуромицин; пуромицина гидрохлорид; пиразофурин; рибоприн; роглетимид; сафингол; сафингола гидрохлорид; семустин; симтразен; спарфосат натрия; спарсомицин; гидрохлорид спирогермания; спиромустин; спироплатин; стрептонигрин; стрептозоцин; сулофенур; талисомицин; текогалан натрия; тегафур; телоксантрона гидрохлорид; темопорфин; тенипозид; тероксирон; тестолактон; тиамиприн; тиогуанин; тиотепу; тиазофурин; тирапазамин; цитрат торемифена; ацетат трестолона; трицирибинфосфат; триметрексат; триметрексат глюкуронат; трипторелин; тубулозола гидрохлорид; урациловый иприт; уредепу; вапреотид; вертепорфин; винбластина сульфат; винкристина сульфат; виндезин; сульфат виндезина; винэпидина сульфат; винглицинат сульфат; винлейрозина сульфат; винорелбина тартрат; винрозидина сульфат; винзолидина сульфат; ворозол; зениплатин; зиностатин; гидрохлорид зорубицина, агенты, которые останавливают клетки в фазах G2-M и/или модулируют образование или стабильность микротрубочек (например, Taxol™ (т.е., паклитаксел), Taxotere™, соединения, содержащие скелет таксана, эрбулозол (т.е., R-55104), Доластатин 10 (т.е., DLS-10 и NSC-376128), Мивобулин изетионат (т.е., как CI-980), винкристин, NSC-639829, дискодермолид (т.е., как NVP-XX-A-296), ABT-751 (Abbott, т.е. E-7010), алторхиртины (например, алторхиртин A и алторхиртин C), спонгистатины (например, спонгистатин 1, спонгистатин 2, спонгистатин 3, спонгистатин 4, спонгистатин 5, спонгистатин 6, спонгистатин 7, спонгистатин 8 и спонгистатин 9), гидрохлорид цемадотина (например, LU-103793 и NSC-D-669356), эпотилоны (например, эпотилон A, эпотилон B, эпотилон C (т.е., дезоксиэпотилон A или dEpoA), эпотилон D (т.е., KOS-862, dEpoB и дезоксиэпотилон B), эпотилон E, эпотилон F, эпотилон B N-оксид, эпотилон A N-оксид, 16-аза-эпотилон B, 21-аминоэпотилон B (т.е., BMS-310705), 21-гидроксиэпотилон D (т.е., дезоксиэпотилон F и dEpoF), 26-фторэпотилон, ауристатин PE (т.е., NSC-654663), соблидотин (т.е., TZT-1027), винкристина сульфат, криптофицин 52 (т.е., LY-355703), витилевамид, тубулизин А, канаденсол, кентауреидин (т.е., NSC-106969), онкоцидин А1 (т.е., BTO-956 и DF E), фиджианолид В, лаулимали de, наркозин (также известный как NSC-5366), наскапин, гемиастерлин, ацетилацетонат ванадоцена, монсатрол, линаноцин (например, NSC-698666), элеутеробины (такие как десметилелеутеробин, дезаэтилеутеробин, изоэлеутеробин A и Z-элеутеробин), карибеозид, карибеолин, галихондрин B, диазонамид A, таккалонолид A, диозостатин, (-)-фенилагистин (ieNSCL-96F037), миосеверин B, ресверастатина фосфат натрия, стероиды (например, дексаметазон), финастерид, ингибиторы ароматазы, агонисты гонадотропин-рилизинг-гормона (GnRH) такие как гозерелин или лейпролид, адренокортикостероиды (например, преднизолон), прогестины (например, гидроксипрогестерон капроат, мегестрола ацетат, медроксипрогестерона ацетат), эстрогены (например, диэтилстилбестрол, этинилэстрадиол), антиэстрогены (например, тамоксифен), андрогены (например, тестостерона пропионат, флуоксиместерон), антиандрогены (например, флутамид), иммуностимуляторы (например, бациллу Кальмета-Герена (BCG), левамизол, интерлейкин-2, альфа-интерферон и т.д.), моноклональные антитела (например, анти-CD20, анти-F£ER2, анти-CD52, анти-ULA-DR и анти-VEGF моноклональные антитела), иммунотоксины (например, моноклональное антитело анти-CD33-калихеамицин, конъюгат моноклонального антитела анти-CD22-экзотоксин псевдомонады и т.д.), радиоиммунотерапию (например, моноклональное антитело анти-CD20, конъюгированное с U1ln, 90 Y или mI, и т.д.), триптолид, гомохаррингтонин, дактиномицин, доксорубицин, эпирубицин, топотекан, итраконазол, виндезин, церивастатин, винкристин, дезоксиаденозин, сертралин, питавастатин, иринотекан, клофазимин, 5-нонилокситриптамин, вемурафениб, дабраферфитиб, ингибитор FR направленную на рецептор дермального фактора роста (EGFR) терапию или терапевтические средства (например, гефитиниб (Iressa™), эрлотиниб (Tarceva™), цетуксимаб (Erbitux™), лапатиниб (Tykerb™), панитумумаб (Vectibix™), вандетаниб (Caprelsa™), афатиниб/BIBW2992, CI-1033/канертиниб, нератиниб/HKI-272, CP-724714, TAK-285, AST-1306, ARRY334543, ARRY-380, AG-1478, дакомитиниб/PF299804, OSI-420/десметил эрлотиниб, AZD8931, AEE788, пелитиниб/EKB-569, CUDC-101, WZ8040, WZ4002, WZ3146, AG-490, XL647, PD153035, BMS-599626), сорафениб, иматиниб, сунитиниб, дазатиниб, гормональную терапию и т.п.
[0050] Переходный термин "содержащий (comprising)", который является синонимичным с "включающий в себя", "содержащий (containing)" или "отличающийся тем, что", является охватывающим или многовариантным и не исключает дополнительные неизложенные признаки, целые числа, этапы, операции, элементы и/или компоненты. В отличие от этого, переходная фраза "состоящий из" исключает любые признаки, целые числа, этапы, операции, элементы и/или компоненты, которые не указаны. Переходная фраза "по существу, состоящий из" ограничивает объем пункта формулы изобретения указанными признаками, целыми числами, этапами, операциями, элементами и/или компонентами "и признаками, целыми числами, этапами, операциями, элементами и/или компонентами, которые существенно не затрагивают базовую и новую характеристику(и)" заявленного изобретения.
[0051] При использовании в данном документе, термин "приблизительно" в контексте числового значения или диапазона означает ±10% от изложенного или заявленного числового значения или диапазона, если контекст не требует более ограниченного диапазона.
[0052] Термин "температура окружающей среды" означает температуру, при которой составы настоящего раскрытия сущности применятся к исследуемому объекту. В общем, температура окружающей среды представляет собой температуру температурно управляемой окружающей среды. Температура окружающей среды варьируется в диапазоне приблизительно от 18°C приблизительно до 30°C. В конкретных вариантах осуществления, температура окружающей среды составляет приблизительно 18°C, приблизительно 19°C, приблизительно 20°C, приблизительно 21°C, приблизительно 22°C, приблизительно 23°C, приблизительно 24°C, приблизительно 25°C, приблизительно 26°C, приблизительно 27°C, приблизительно 28°C, приблизительно 29°C или приблизительно 30°C.
[0053] "Фармацевтический состав на основе текучей среды" представляет собой фармацевтическую композицию, которая представляет собой жидкость в то время, когда она доставляется (т.е. применяется) пациенту. В конкретных вариантах осуществления, фармацевтический состав на основе текучей среды содержит активный агент, такой как химическое соединение, клетка или клеточный продукт, и фармацевтически приемлемый носитель. В конкретных вариантах осуществления, фармацевтически приемлемый носитель представляет собой температурочувствительный биоматериал.
[0054] Устройства, системы и способы, предусмотренные в настоящем документе, являются, в общем, полезными для доставки фармацевтических составов на основе текучей среды в участки тканей, к примеру, в органы (например, в твердые органы). В конкретных вариантах осуществления, участок тканей представляет собой опухоль (например, твердую или жесткую опухоль). В конкретных вариантах осуществления, участок тканей представляет собой орган, который содержит раковые клетки или опухоль. В конкретных вариантах осуществления, участок тканей содержит опухолевые клетки. В конкретных вариантах осуществления, участок тканей представляет собой лимфатический узел, который содержит опухолевые клетки. Тем не менее, в конкретных вариантах осуществления, настоящий предмет изобретения является, в частности, полезным для доставки биоактивных клеток почечного эпителия (к примеру, биоактивных клеток почечного эпителия, например, выбранных клеток почечного эпителия) в почки пациентов с заболеванием почек.
[0055] Термин "биоактивные клетки почечного эпителия" или "BRC" при использовании в данном документе означает клетки почечного эпителия, имеющие одно или более следующих свойств при применении к почке исследуемого объекта: способность уменьшать (например, замедлять или прекращать) ухудшение или развитие хронического заболевания почек либо его симптома, способность улучшать почечную функцию, способность влиять на (улучшать) почечный гомеостаз и способность ускорять заживление, восстановление и/или регенерацию почечной ткани или почек. В конкретных вариантах осуществления, эти клетки могут включать в себя функциональные тубулярные клетки (например, на основе улучшений экскреции креатинина и отложения белков), клубочковые клетки (например, на основе улучшения отложения белков), сосудистые клетки и другие клетки кортикомедуллярного перехода. В конкретных вариантах осуществления, BRC получаются из изоляции и растяжения клеток почечного эпителия из ткани почки. В конкретных вариантах осуществления, BRC получаются из изоляции и растяжения клеток почечного эпителия из ткани почки с использованием способов, которые выбирают биоактивные клетки. В конкретных вариантах осуществления, BRC оказывают регенеративный эффект на почку. В конкретных вариантах осуществления, BRC содержат, состоят по существу из или состоят из выбранных клеток почечного эпителия (SRC). В конкретных вариантах осуществления, BRC представляют собой SRC.
[0056] В конкретных вариантах осуществления, SRC представляют собой клетки, полученные из изоляции и растяжения клеток почечного эпителия из подходящего источника почечной ткани, при этом SRC содержат большую процентную долю одного или более типов клеток и не имеют либо имеют меньшую процентную долю одного или более других типов клеток, по сравнению с начальной популяцией почечных клеток. В конкретных вариантах осуществления, SRC содержат увеличенную пропорцию BRC по сравнению с начальной популяцией почечных клеток. В конкретных вариантах осуществления, SRC-популяция представляет собой изолированную популяцию почечных клеток, пополненных конкретными биоактивными компонентами и/или типами клеток и/или лишенных конкретных неактивных и/или неполезных компонентов или типов клеток для использования при лечении заболевания почек, т.е. при предоставлении стабилизации и/или улучшения, и/или регенерации функции почек. SRC предоставляют превосходные терапевтические и регенеративные результаты по сравнению с начальной популяцией. В конкретных вариантах осуществления, SRC получаются из почечной кортикальной ткани пациента через почечную биопсию. В конкретных вариантах осуществления, SRC выбираются (например, посредством сортировки люминесцентно-активированных клеток или "FACS") на основе их экспрессии одного или более маркеров. В конкретных вариантах осуществления, SRC лишаются (например, посредством сортировки люминесцентно-активированных клеток или "FACS") одного или более типов клеток на основе экспрессии одного или более маркеров относительно типов клеток. В конкретных вариантах осуществления, SRC выбираются из популяции биоактивных клеток почечного эпителия. В конкретных вариантах осуществления, SRC выбираются посредством градиентного разделения по плотности растянутых клеток почечного эпителия. В конкретных вариантах осуществления, SRC выбираются посредством разделения растянутых клеток почечного эпителия посредством центрифугирования по плотностной границе, барьеру или поверхности раздела либо посредством одноэтапного прерывистого ступенчатого градиентного разделения. В конкретных вариантах осуществления, SRC выбираются посредством непрерывного или прерывистого градиентного разделения по плотности растянутых клеток почечного эпителия, которые культивируются при гипоксических условиях. В конкретных вариантах осуществления, SRC выбираются посредством градиентного разделения по плотности растянутых клеток почечного эпителия, которые культивируются при гипоксических условиях, по меньшей мере, в течение приблизительно 8, 12, 16, 20 или 24 часа. В конкретных вариантах осуществления, SRC выбираются посредством разделения посредством центрифугирования по плотностной границе, барьеру или поверхности раздела растянутых клеток почечного эпителия, которые культивируются при гипоксических условиях. В конкретных вариантах осуществления, SRC выбираются посредством разделения растянутых клеток почечного эпителия, которые культивируются при гипоксических условиях, по меньшей мере, в течение приблизительно 8, 12, 16, 20 или 24 часа посредством центрифугирования по плотностной границе, барьеру или поверхности раздела (например, одноэтапного прерывистого градиентного разделения по плотности). В конкретных вариантах осуществления, SRC состоят главным образом из тубулярных клеток почечного эпителия. В конкретных вариантах осуществления, другие паренхимальные (например, сосудистые) и стромальные (например, собирательно-протоковые) клетки могут присутствовать в SRC. В конкретных вариантах осуществления, менее приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% клеток в популяции SRC представляют собой сосудистые клетки. В конкретных вариантах осуществления, менее приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% клеток в популяции SRC представляют собой собирательно-протоковые клетки. В конкретных вариантах осуществления, менее приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% клеток в популяции SRC представляют собой сосудистые или собирательно-протоковые клетки.
[0057] Термин "неопочечная аугментация (NKA)" означает биоактивный клеточный состав, который представляет собой инъекционный продукт, состоящий из аутологичных выбранных клеток почечного эпителия (SRC) в готовом составе биоматериала, содержащего желатиновый гидрогель.
[0058] Термин "заболевание почек" при использовании в данном документе означает расстройства, ассоциированные с любой стадией либо степенью острой или хронической почечной недостаточности, которая приводит к потере способности почки выполнять функцию фильтрации крови и избавления от избыточной жидкости, электролитов и шлаков из крови. Заболевание почек также может включать в себя эндокринные дисфункции, такие как анемия (недостаток эритропоэтина) и минеральный дисбаланс (недостаток витамина D). Заболевание почек может происходить в почке либо может быть вторичным по отношению ко множеству условий, включающих в себя (но не только) сердечную недостаточность, артериальную гипертензию, диабет, аутоимунное заболевание или заболевание печени. Заболевание почек может представлять собой условие хронической почечной недостаточности, которая развивается после острого повреждения почки. Например, повреждение почек в силу ишемии и/или подверженности воздействию токсикантов может вызывать острую почечную недостаточность; неполное восстановление после острого повреждения почек может приводить к развитию хронической почечной недостаточности.
[0059] Термин "сфероид" означает агрегат или узел клеток, культивированных с возможностью обеспечивать трехмерный рост, в противоположность росту в качестве монослоя. Следует отметить, что термин "сфероид" не подразумевает то, что агрегат представляет собой геометрическую сферу. В конкретных вариантах осуществления, агрегат может быть высокоорганизованным с четко определенной морфологией, либо агрегат может представлять собой неорганизованную массу. В конкретных вариантах осуществления, сфероид может включать в себя один тип клеток либо более одного типа клеток. В конкретных вариантах осуществления, клетки могут представлять собой первичные изоляты либо постоянную клеточную линию, либо комбинацию означенного. В конкретных вариантах осуществления, сфероиды (например, клеточные агрегаты или органоиды) формируются в центрифужной пробирке. В конкретных вариантах осуществления, сфероиды (например, клеточные агрегаты или органоиды) формируются в трехмерной матрице.
[0060] Относительно заболевания почек и в зависимости от контекста, "лечение" означает как терапевтическое лечение, так и профилактические или превентивные меры на предмет заболевания почек, недостатка транспортируемых тубулярных клеток или недостатка клубочковой фильтрации, при этом цель заключается в том, чтобы инвертировать течение, предотвращать или замедлять (уменьшать) целевое расстройство или симптом. Нуждающиеся в лечении включают в себя тех, кто уже имеет заболевание почек, недостаток транспортируемых тубулярных клеток или недостаток клубочковой фильтрации, а также склонных к заболеванию почек, недостатку транспортируемых тубулярных клеток или недостатку клубочковой фильтрации, либо тех, у которых должно предотвращаться заболевание почек, недостаток транспортируемых тубулярных клеток или недостаток клубочковой фильтрации. В конкретных вариантах осуществления, лечение включает в себя стабилизацию и/или улучшение функции почек. Относительно рака, лечение может включать в себя, например, уменьшенный объем опухоли, уменьшенный темп роста опухоли, увеличенную иммунную реакцию на опухолевый антиген, уменьшенный рост раковых клеток, уменьшенную пролиферацию раковых клеток или уменьшенную выживаемость раковых клеток (например, повышенное отмирание, к примеру, апоптоз или некроз опухолевых клеток).
[0061] Применение терапевтических агентов
[0062] Внесосудистая доставка может заключать в себе прямую инъекцию фармацевтического состава на основе текучей среды (например, фармацевтического состава на основе текучей среды, содержащего терапевтические клетки) в орган, к примеру, в строму органа, через одно или более устройств, таких как шприцы, катетеры, троакары и т.п. "Внесосудистая инъекция" означает доставку посредством инъекции за пределы кровеносных сосудов. При внесосудистой доставке, время пребывания терапевтических клеток может быть большим. Например, процесс очистки или промывания может основываться на процессах очистки, ассоциированных с локальной травмой и удалением отека в участке доставки. Эффективность доставки также может быть высокой. Тем не менее, успешная доставка терапевтических клеток либо их продуктов может быть затруднительной. Например, экстравазация терапевтического клеточного материала через входную прорезь устройства доставки может представлять собой сложность, вызываемую посредством множества различных проблем. Экстравазация может считаться утечкой (в частности, непреднамеренной утечкой) текучей среды из целевого участка инъекции. Например, естественное движение цели доставки вследствие перемещения пациента (и в силу этого перемещения целевого участка), к примеру, посредством дыхания может приводить к неустановившейся цели доставки. Неточная доставка терапевтического клеточного материала также может вызываться посредством травмы участка лечения вследствие ударного и режущего воздействия посредством инструментов доставки, вызываемого посредством перемещения во время применения. Дополнительно, доставка может быть затруднительной вследствие того, как возникает инфузия терапевтических клеток либо их продуктов, к примеру, посредством непрерывного потока с учетом дозировки в целевой участок.
[0063] В силу этого этих и других причин, требуются улучшенные устройства, способы и системы для доставки фармацевтических составов на основе текучей среды (к примеру, клеточной терапии). В данном документе предусмотрены, в числе прочего, улучшенные устройства, способы и системы для доставки терапевтических композиций, к примеру, композиций, содержащих химические соединения, клетки или клеточные продукты.
[0064] В аспекте, в данный документе включены устройства, способы и системы для доставки клеточной терапии, к примеру, с возможностями дозируемой инфузии, доставляемой внесосудисто в целевые местоположения внутри пациента при поддержании позиционной стабильности. Использование клеточной терапии представляет собой очень популярный и успешный подход к лечению множества различных заболеваний. Например, внесосудистая доставка клеточной терапии является успешной в предоставлении большого времени пребывания терапевтического клеточного материала в участке лечения и повышенной эффективности доставки. Тем не менее, внесосудистая доставка приводит к проблемам, таким как экстравазация терапевтического клеточного материала, вызываемым посредством таких факторов, как перемещение пациента (и в силу этого перемещение целевого участка), травма участка лечения вследствие ударного и режущего воздействия посредством инструментов доставки, вызываемого посредством перемещения пациента, и инфузия терапевтических клеточных материалов через непрерывный поток с учетом дозировки в участок лечения. Таким образом, предусмотрены устройства, способы и системы, которые выполнены с возможностью предоставлять стабильность доставки терапевтического агента (к примеру, клеточного материала, например, клеток либо их продукта, такого как экзосомы), например, посредством предоставления физически стабильного процесса доставки и прерывистых потоков с учетом дозировки терапевтического клеточного материала.
[0065] В аспекте, в данный документе включены устройства, способы и системы для доставки фармацевтического состава на основе текучей среды (например, клеточной терапии), к примеру, с возможностями дозируемой инфузии, доставляемого внесосудисто в целевые местоположения внутри пациента при поддержании позиционной стабильности. Устройства, системы и способы, предусмотренные в настоящем документе, могут использоваться для лечения множества различных заболеваний, в том числе, но не только, заболеваний почек и рака.
[0066] В конкретных вариантах осуществления, инъекционное устройство, предусмотренное в настоящем документе, выполнено с возможностью доставлять непрерывный поток текучей среды в целевой участок. В конкретных вариантах осуществления, инъекционное устройство, предусмотренное в настоящем документе, выполнено с возможностью доставлять прерывистый поток или болюс текучей среды в целевой участок. Примерное устройство, предусмотренное в настоящем документе, может быть выполнено с возможностью доставлять прерывистые потоки или болюсы текучей среды, такой как фармацевтический состав на основе текучей среды, содержащий клетки или клеточные продукты, в целевой участок. Болюс может считаться одной физической частью фармацевтической композиции (такой как фармацевтический состав на основе текучей среды). В конкретных вариантах осуществления, болюс представляет собой часть фармацевтической композиции (такой как фармацевтический состав на основе текучей среды), которая доставляется в качестве одного события. В конкретных вариантах осуществления, болюс представляет собой часть фармацевтической композиции (такой как фармацевтический состав на основе текучей среды), которая доставляется в качестве части нескольких частей (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более частей), которые доставляются один за другим, например, во время применения фармацевтической композиции. В конкретных вариантах осуществления, один болюс доставляется. В конкретных вариантах осуществления, фармацевтическая композиция не доставляется между несколькими дискретными болюсами. В конкретных вариантах осуществления, возникает некоторый непрерывный поток фармацевтической композиции. В конкретных вариантах осуществления, доставка является непрерывной, но количество фармацевтической композиции пульсирует (т.е. поток не прекращается, но увеличивается и уменьшается со временем). В конкретных вариантах осуществления, устройство, предусмотренное в настоящем документе, выполнено с возможностью обращения одной рукой. В конкретных вариантах осуществления, инъекционное устройство может зацепляться с примерным троакаром, который выполнен с возможностью иметь один или более стабилизирующих механизмов на валу, так что троакар предоставляет стабильный механизм доставки в инъекционное устройство. В конкретных вариантах осуществления, троакар выполнен с возможностью принимать инъекционную иглу, которая присоединяется к инъекционному устройству, и инъекционное устройство может доставлять дозу в качестве непрерывного потока текучей среды через нее в участок целевых тканей. В конкретных вариантах осуществления, троакар выполнен с возможностью принимать инъекционную иглу, которая присоединяется к инъекционному устройству, и инъекционное устройство может доставлять текучую среду через нее в болюсных дозах в участок целевых тканей. В конкретных вариантах осуществления, устройства, системы и способы, предусмотренные в настоящем документе, могут использоваться во множестве лечений, таких как предоставление измеренного дозирования терапевтических клеток или клеточных продуктов в почку (например, у пациента, который имеет заболевание почек, к примеру, хроническое заболевание почек) посредством непосредственной доставки текучей среды, содержащей терапевтические клетки или клеточные продукты, в несколько участков внесосудистой инъекции в почечных паренхимальных/стромальных отделах пациента. В конкретных вариантах осуществления, пациент позиционируется в позиции лежа лицом вниз или в поперечной позиции, как проиллюстрировано на фиг. 1 и 2. "Паренхима" представляет собой функциональную ткань органа, в отличие от соединительной и опорной ткани. "Строма" представляет собой опорную ткань эпителиального органа, опухоли, гонада и т.д., состоящего из соединительных тканей и кровеносных сосудов. В конкретных вариантах осуществления, исследуемый объект имеет недостаточность на поздней стадии. Тем не менее, хотя раскрытие сущности поясняет лечение почек в данном документе, устройства, системы и способы могут использоваться широко. В конкретных вариантах осуществления, устройства, системы и способы, предусмотренные в настоящем документе, могут использоваться во множестве лечений, к примеру, в предоставлении измеренного дозирования терапевтических клеток или клеточных продуктов в участок тканей, который имеет раковые клетки, к примеру, твердую опухоль. В конкретных вариантах осуществления, участок тканей представляет собой орган, который имеет или подозревается в наличии раковых клеток (например, метастазных раковых клеток или опухоли).
[0067] В конкретных вариантах осуществления, устройства, системы и способы, предусмотренные в настоящем документе, являются полезными для чрескожной инъекции фармацевтических составов на основе текучей среды в раковую клетку или твердую опухоль, содержащую орган, и/или непосредственно в опухоль. В конкретных вариантах осуществления, важно распределять состав в органе максимально возможно широко. В конкретных вариантах осуществления, распределение состава в органе или опухоли достигается посредством входа в орган или опухоль под углом, обеспечивающим осаждение состава в органе или опухоли максимально возможно широко. В конкретных вариантах осуществления, орган или опухоль визуализируется в продольном или поперечном подходе с использованием ультразвукового контроля направления либо с помощью осевой визуализации на основе компьютерной томографии (CT), в зависимости от индивидуальных характеристик пациента. В конкретных вариантах осуществления, инъекция заключает в себе несколько отложений по мере того, как инъекционная игла постепенно извлекается. В конкретных вариантах осуществления, полный объем состава может осаждаться в одной или в нескольких входных точках. В конкретных вариантах осуществления, вплоть до двух входных точек могут использоваться для того, чтобы осаждать полный объем терапевтического состава в орган или опухоль.
[0068] В конкретных вариантах осуществления, устройства, системы и способы, предусмотренные в настоящем документе, являются полезными для чрескожной инъекции фармацевтических составов на основе текучей среды в почечное корковое вещество для почки. В конкретных вариантах осуществления, важно распределять состав в почечном корковом веществе максимально возможно широко. В конкретных вариантах осуществления, распределение состава в почечном корковом веществе достигается посредством входа в почечное корковое вещество под углом, обеспечивающим осаждение состава в почечном корковом веществе максимально возможно широко. В конкретных вариантах осуществления, почка визуализируется в продольном или поперечном подходе с использованием ультразвукового контроля направления либо с помощь осевой CT-визуализации, в зависимости от индивидуальных характеристик пациента. В конкретных вариантах осуществления, инъекция заключает в себе несколько отложений по мере того, как инъекционная игла постепенно извлекается. В конкретных вариантах осуществления, полный объем состава может осаждаться в одной или в нескольких входных точках. В конкретных вариантах осуществления, вплоть до двух входных точек могут использоваться для того, чтобы осаждать полный объем терапевтического состава в почку. В конкретных вариантах осуществления, инъекция может применяться к одной почке, с использованием одной или более входных точек, например, одной или двух входных точек. В конкретных вариантах осуществления, инъекция осуществляется в обе почки, в каждой почке с использованием одной или более входных точек, например, одной или двух входных точек.
[0069] Устройства и системы, предусмотренные в настоящем документе, предоставляют преимущества по сравнению с предлагаемыми на рынке устройствами. Фиг. 3 и 4 приводят процесс для выполнения клеточной терапии с использованием типовых компонентов для почки пациента. Например, типовые части, такие как иглы, троакары/втулки, люэровские насадки, задвижки, система трубок, шприцы на 3 куб/см и шприцы на 10 куб/см, могут храниться в качестве запасов в месте, в котором терапевтический клеточный материал обрабатывается. Может подготавливаться комплект, который содержит вышеуказанные элементы в параллельных анализах, с диапазоном размеров для различных игл и троакаров/втулок. Диапазон размеров-калибров для игл может содержать диапазон длин: 10 см, 15 см и 20 см. Шприц на 10 куб/см, который может использоваться в упаковке, которая обеспечивает асептическое наполнение при клеточной терапии, может заполняться дозой. Шприц с дозой лекарства затем может поставляться отдельно в место проведения процедуры в упаковке с управлением температурой, которая поддерживает терапию приблизительно при 4-8°C в ходе перевозки. В месте проведения процедуры, может реализовываться протокол для того, чтобы нагревать шприц, собирать инъекционную систему и организовывать и подготавливать запасы для пользователя. Например, шприц может нагреваться приблизительно до 26-28°C в течение управляемого периода времени, к примеру, в течение приблизительно 30 минут. Пользователь затем может начинать процедуру в пределах выделенного окна для жизнеспособности продуктов, которое может составлять приблизительно 1,5 часа. Фиг. 4 иллюстрирует неограничивающую инъекционную систему, как пояснено выше, в которой шприц на 3 куб/см соединяется со шприцем на 10 куб/см через 3-стороннюю задвижку. Вывод из задвижки отправляется через систему трубок в люэровское соединение на инъекционной игле в троакаре/втулке, размещенном внутри пациента. Клеточная терапия может первоначально перемещаться в шприц на 3 куб/см через плунжер на 10 куб/см, и она может затем инъецироваться в почку пациента с управлением и простотой перемещения плунжера, обеспечиваемыми посредством меньшего шприца. Инъекция клеточной терапии может быть сложной задачей, которая может требовать минимум обеих рук ведущего пользователя и зачастую еще одной руки для помощи в действиях с плунжером при стабилизации троакара, иглы и инъекционной системы. Устройства и системы, включенные в данный документ, предоставляют преимущества по сравнению с процессами и компонентами, проиллюстрированными на фиг. 3 и 4, такие как повышенная стабильность (и меньшее повреждение) во время доставки терапевтического агента, а также более согласованная доставка терапевтического агента (например, по количеству и местоположению).
[0070] Фиг. 5 иллюстрирует один неограничивающий вариант осуществления троакара 20, который может использоваться в данном документе. В качестве неограничивающего примера, в простейшей форме, троакар приблизительно может представлять собой инструмент в форме пера, по меньшей мере, с в определенной степени острой треугольной точкой на одном конце, зачастую используемой внутри полой трубки, известной как канюля или втулка, для того, чтобы создавать отверстие в теле, через которое может вводиться втулка, чтобы предоставлять порт для доступа во время хирургического вмешательства. В конкретных вариантах осуществления, троакар представляет собой инструмент в форме пера с двумя частями, твердым обтуратором/стилетом с острой треугольной точкой на одном конце внутри полой трубки, известной как канюля или втулка (например, троакар используется для того, чтобы создавать отверстие в теле; стилет может выниматься, при этом втулка остается, чтобы предоставлять порт для доступа к внутренним структурам). Троакар 20, как проиллюстрировано на фиг. 5 может иметь ручку 22, удлиненный вал 24, экран 26 и расцепитель 28 экрана. Просвет может протягиваться через них. Фиг. 6 иллюстрирует один неограничивающий канюли 30, которая может использоваться в данном документе. Канюля 30 имеет ручку 32 и втулку 34, и она может иметь просвет, протягивающийся через них. Когда троакар, такой как троакар 20, размещается внутри пациента, крепление троакара осуществляется главным образом в двух точках. Фрикционный захват троакара возникает в сквозном проходе в коже, и аналогично, более слабое взаимодействие возникает в троакаре посредством внутренней ткани, к примеру, капсулы почки. Фрикционный захват во внутренней ткани является более слабым вследствие небольшой глубины проникновения троакара. Тем не менее, стабилизация глубины проникновения троакара в ткань, к примеру, в почку во время процедуры может быть преимущественной, чтобы избегать травмы ткани и помогать в более плавной инъекции терапевтического клеточного материала, и вредоносное перемещение дермальной анкерной точки относительно анкерной точки внутренних тканей, к примеру, в почке, может возникать.
[0071] Инъекционное устройство
[0072] Фиг. 7 иллюстрирует один неограничивающий пример инъекционного устройства 100, которое может быть выполнено с возможностью обращения одной рукой со съемным троакаром 200, который имеет стилет 300, и который протягивается дистально из устройства 100 вдоль продольной оси L1 устройства 100. Инъекционное устройство 100 имеет кожух 101, ручку 102, актуатор 104, приемное устройство 106 для текучей среды, дисплей 108 и зацепляющий механизм 110 троакара. В конкретных вариантах осуществления, дисплей 108 опускается. В конкретных вариантах осуществления, в устройстве 100, предусмотрены насос (не показан), один или более датчиков, выполненных с возможностью обнаруживать множество условий, таких как давление, расход, температура и т.д. (не показаны), источник мощности, такой как аккумулятор (не показан), и/или центральный процессор (CPU) (не показан). На фиг. 7, ручка 102 протягивается из кожуха 101 и имеет форму пистолетного захвата. Тем не менее, могут использоваться множество ручек, захватов, элементов управления и т.д.
[0073] Актуатор 104 представляет собой спусковую собачку, которая выполнена с возможностью приводить в действие доставку текучей среды из приемного устройства 106 для текучей среды и через клапан 120 на дистальном конце инъекционного устройства 100, подробнее поясненного ниже. Хотя актуатор 104 проиллюстрирован в качестве спусковой собачки, актуатор может иметь различные формы, такие как плунжеры, кнопки, переключатели, средства электронного приведения в действие, приводимые в действие с помощью CPU средства, включенные в дисплей 108, и т.д. Актуатор 104 выполнен с возможностью вручную нажиматься в направлении ручки 102. В конкретных вариантах осуществления, по мере того, как актуатор 104 нажимается, актуатор 104 может быть выполнен с возможностью предоставлять тактильную обратную связь пользователю. В конкретных вариантах осуществления, тактильная обратная связь может физически создаваться из ручного нажатия актуатора 104, либо она может моделироваться. Например, устройство 100 может иметь один или более механизмов тактильной обратной связи, встроенных в него, которые выполнены с возможностью моделировать механистическое действие актуатора 104, который фактически является электромеханическим и управляется посредством CPU. В конкретных вариантах осуществления, нажатие актуатора 104 выполнено с возможностью доставлять текучую среду из приемного устройства 106 для текучей среды в клапан 120 в импульсном шаблоне доставки, который включает в себя дискретные болюсы 122 доставки текучей среды в целевой участок, как проиллюстрировано на фиг. 8, и оно выполнено с возможностью убирать инъекционную иглу из целевого участка во время доставки текучей среды, с тем чтобы обеспечивать пространство для растягивания для доставляемой текучей среды. В конкретных вариантах осуществления, дискретные болюсы 122 текучей среды могут быть выполнены с возможностью не находиться в прямом контакте друг с другом, что позволяет предотвращать или уменьшать экстравазацию из участка целевых тканей. В конкретных вариантах осуществления, устройство альтернативно может быть выполнено с возможностью доставлять непрерывные потоки 123 текучей среды, как проиллюстрировано на фиг. 9, либо осуществлять комбинацию означенного. В конкретных вариантах осуществления, импульсный шаблон доставки и убирание иглы могут создаваться посредством электромеханической системы с механизмом накачки в устройстве 100, который может создаваться посредством насоса и CPU. Тем не менее, механизм накачки и убирания также может быть механическим по своему характеру, или все устройство 100 может быть исключительно механическим. В конкретных вариантах осуществления, текучая среда может вытягиваться из резервуара для текучей среды, зацепленного с приемным устройством 106 для текучей среды.
[0074] В конкретных вариантах осуществления, как показано на фиг. 7, приемное устройство 106 для текучей среды позиционируется на верхней поверхности устройства 100. Тем не менее, оно может содержаться в любом месте на устройстве 100. В конкретных вариантах осуществления, приемное устройство 106 для текучей среды выполнено с возможностью принимать текучую среду из резервуара для текучей среды, такого как картридж 130, показанный на фиг. 10, или шприц, и выполнено с возможностью доставлять текучую среду в клапан 120 при приведении в действие актуатора 104. В конкретных вариантах осуществления, приемное устройство 106 для текучей среды выполнено с возможностью принимать картридж 130, по меньшей мере, частично и протыкать картридж 130 с использованием асептического протыкающего септу элемента. Тем не менее, приемное устройство 106 для текучей среды альтернативно может быть выполнено с возможностью принимать один или более картриджей 130 полностью, соединяться с одной или более линий для текучей среды и т.д. Приемное устройство 106 для текучей среды также альтернативно может иметь один или более клапанов, насадок, зацеплений и т.д., чтобы соединяться с резервуаром(ами) для текучей среды. В конкретных вариантах осуществления, приемное устройство 106 для текучей среды также может иметь управление температурой, встроенное в кожух 101, чтобы управлять температурой картриджа 130. В конкретных вариантах осуществления, картридж 130 содержит гидрогель (например, желатиновый гидрогель), который нагревается до тех пор, пока гидрогель не расплавляется в жидкость. В конкретных вариантах осуществления, терапевтический агент (например, клеточная популяция или клеточный продукт, такой как экзосома) диспергирует (например, равномерно) по гидрогелю и/или текучей среде.
[0075] Резервуар для текучей среды, такой как картридж 130, выполнен с возможностью доставлять одну или более текучих сред через устройство 100 и в целевой участок при приведении в действие актуатора 104. Картридж 130, проиллюстрированный на фиг. 10, представляет собой картридж в форме стеклянной пробирки с резиновой диафрагменной поверхностью раздела, которая выполнена с возможностью доставлять текучую среду при протыкании посредством асептического протыкающего септу элемента приемного устройства 106 для текучей среды. В конкретных вариантах осуществления, картридж содержит характеристики материала, которые учитывают вязкость терапевтического агента (к примеру, клеточной терапии), в силу этого предотвращая потерю терапевтического агента, прилипающего к внутренним стенкам картриджа. В конкретных вариантах осуществления, картридж 130 может собираться с устройством 100 в стерильном поле, и аспирационная магистраль, которая входит в картридж для того, чтобы соединяться с магистралью для текучей среды через устройство 100, может быть выполнена с возможностью предотвращать потери текучей среды вследствие доступа в ориентациях в различных вариантах использования картриджа 130, например, если картридж 130 переворачивается. Картридж 130 также может быть выполнен с возможностью надежно удерживаться посредством устройства 100 в приемном устройстве 106 для текучей среды. В конкретных вариантах осуществления, резервуар для текучей среды может изготовлен из множества материалов, таких как полимеры, резина и т.д., и может иметь множество форм, таких как мешочки, линии для текучей среды, контейнеры и т.д., которые могут соединяться с резервуаром для текучей среды 106 множеством средств, таких как сквозные порты, клапаны и т.д. Картриджи 130 также могут быть выполнены с возможностью быть съемными и сменными, например, после доставки текучей среды в них. В конкретных вариантах осуществления, картриджи 130 могут предоставляться в предварительно выбранных дозах и/или конфигурациях таким образом, что пользователи могут использовать множество картриджей 130 в ходе одного лечения в зависимости от требуемого лечения. Альтернативно, устройство 100 может иметь встроенный резервуар для текучей среды, который предназначен для одного использования. В конкретных вариантах осуществления, устройство 100 также может иметь один или более механизмов для задания индивидуально настраиваемой дозы из картриджа 130, к примеру, посредством использования дисплея 108 (поясняется ниже). В конкретных вариантах осуществления, картриджи 130 могут иметь одну или более компьютерных микросхем, которые соединяются с устройством 100 при вставке и предоставляют подробную информацию относительно содержимого картриджа 130, рекомендуемых доз, расходов, распределения во времени и т.д. Компьютерные микросхемы могут соединяться с CPU устройства 100 через одно или более средств, к примеру, посредством проводных соединений, расположенных в приемном устройстве 106 для текучей среды, и/или в беспроводном режиме.
[0076] В конкретных вариантах осуществления, картридж 130 может быть выполнен с возможностью соединяться с устройством 100 таким образом, что минимальный мертвый объем формируется при соединении, и картридж 130 может быть выполнен с возможностью асептически наполняться в источнике изготовления текучей средой по мере необходимости для клеточной терапии и транспортироваться в место проведения хирургического вмешательства при поддержании температуры транспортировки приблизительно от 0°C приблизительно до 20 °C, а более конкретно, приблизительно от 2°C приблизительно до 8°C или приблизительно от 4°C приблизительно до 8 °C. В конкретных вариантах осуществления, устройство 100 может быть выполнено с возможностью принимать картридж 130, который может иметь пониженную температуру транспортировки, как подробно указано выше, чтобы нагревать картридж 130 до температуры для доставки в пациента в пределах выбираемого периода времени и поддерживать картридж 130 при температуре, которая является приемлемой для использования в течение другого выбираемого периода времени, и/или до тех пор, пока картридж 130 не используется. Например, устройство 100 может быть выполнено с возможностью принимать картридж 130, содержимое которого имеет температуру транспортировки, к примеру, приблизительно от 4°C приблизительно до 8 °C. Устройство 100 затем может нагревать картридж 130 до температуры для использования внутри пациента, к примеру, приблизительно от 20°C приблизительно до 40 °C, а более конкретно, приблизительно от 25°C приблизительно до 37 °C, в течение определенного периода времени, к примеру, в течение 15 минут, в течение 30 минут или в течение 45 минут. Устройство 100 затем может быть выполнено с возможностью удерживать температуру картриджа 130 приблизительно постоянной до тех пор, пока картридж 130 не используется, или в течение фиксированного периода времени, например, в течение приблизительно 1,5 часов. В некоторых неограничивающих примерах, устройство 100 может быть выполнено с возможностью указывать пользователю, если картридж 130 нагрет некорректно, и/или если картридж 130 не использован в пределах выделенного окна для жизнеспособности проб. В конкретных вариантах осуществления, устройство 100 может предотвращать использование пользователем картриджа 130, если устройство 100 определяет то, что жизнеспособность проб является неприемлемой, к примеру, предотвращать приведение в действие устройства 100. Объем картриджа 130 может варьироваться в зависимости от требуемого лечения. Например, диапазон объемов, используемых для клеточной терапии, может составлять приблизительно от 1 мл приблизительно до 15 мл, или более конкретно, приблизительно от 3 мл приблизительно до 8 мл. При использовании во время почечного лечения, объемы используемых картриджей 130 могут зависеть от почечной массы пациентов. Таблица 1 иллюстрирует примерные объемы дозировки, которые могут необязательно использоваться в данном документе при лечении почки.
Табл. 1
[0077] Фармацевтический состав на основе текучей среды может включать в себя множество терапевтических лечений, таких как терапевтические клетки и/или их продукты, к примеру, экзосомы), суспендированных в жидкости. Например, использование в почке может использовать текучую среду, включающую в себя терапевтические клетки и опорный гидрогель с вязкостью, например, приблизительно от 1,05 до 1,35 сП. Вязкость текучей среды может вводить дополнительные факторы при использовании компонентов, раскрытых в данном документе, таких как инъекционная игла и шприц с баррелем и плунжером. Например, чтобы инициировать поток из компонента, такого как инъекционная игла, требуется приложение силы к плунжеру шприца, которая больше силы, требуемой для того, чтобы поддерживать поток, когда он начинается. Дополнительно, может возникать начальный выброс текучей среды, такой как терапевтические клетки и опорный гидрогель, из иглы, который выходит за пределы управления вручную плунжером шприца. После того как поток начинается, удаление силы плунжера может не прекращать поток текучей среды. Может возникать гистерезис в нарастании давления в барреле шприца, и отток текучей среды может прекращаться только посредством убирания плунжера. Вследствие этих соображений, пользователи могут действовать с возможностью обеспечивать пульсацию плунжера, используемого для того, чтобы обеспечивать лучшее управление потоком из иглы.
[0078] В конкретных вариантах осуществления, вязкий характер терапевтического агента (к примеру, клеточной терапии, например, фармацевтического состава на основе текучей среды, содержащего клетки) может иметь тенденцию создавать ситуацию, когда часть терапевтического агента теряется, т.е. терапевтический агент (например, его часть) прилипает к внутренней части картриджа и не может удаляться через нормальный процесс устройства. В конкретных вариантах осуществления, внутренняя поверхность картриджа является гидрофобной. В конкретных вариантах осуществления, внутренняя поверхность картриджа является супергидрофобной. В конкретных вариантах осуществления, внутренняя поверхность картриджа является гидрофобной или супергидрофобной, чтобы уменьшать увлажнение и прилипание терапевтического агента (например, клеточной терапии) к картриджу. В конкретных вариантах осуществления, внутренняя поверхность картриджа является гидрофобной или супергидрофобной, чтобы предотвращать увлажнение и прилипание терапевтического агента (например, клеточной терапии) к картриджу.
[0079] Множество текучих сред может использоваться в данном документе, к примеру, текучие среды, поясненные в патенте (США) номер 8318484, выданном 27 ноября 2012 года; в международной PCT-публикации номер WO/2011/143499, опубликованной 17 ноября 2011 года; в патенте (США) номер 9724367, выданном 8 августа 2017 года; в публикации заявки на патент (США) номер 2017-0281684, опубликованной 5 октября 2017 года; и в публикации заявки на патент (США) номер 2016-0101133, опубликованной 14 апреля 2016 года, все из которых полностью содержатся в данном документе по ссылке. Приемное устройство 106 для текучей среды в силу этого выполнено с возможностью соединять с возможностью обмена текучей средой картридж 130 с клапаном 120, чтобы обеспечивать доставку текучей среды через него.
[0080] В примерном устройстве, проиллюстрированном на фиг. 7, клапан 120 позиционируется внутренне на дистальном конце устройства 100, на котором троакар 200 соединяется с устройством 100. В конкретных вариантах осуществления, клапан 120 представляет собой люэровский разъем, который выполнен с возможностью соединяться с инъекционной иглой для доставки текучей среды через нее. Тем не менее, могут использоваться множество клапанов, выполненных с возможностью соединяться с инъекционной иглой. В конкретных вариантах осуществления, клапан 120 зацепляется с кожухом 101 устройства 100 посредством гибкого монтажа, который выполнен с возможностью перемещаться в пространстве продольно дистально и проксимально вдоль оси L1 устройства 100, которая является приблизительно параллельной протоку для текучей среды через инъекционную иглу. В конкретных вариантах осуществления, клапан 120 может перемещаться в пространстве дистально и проксимально вплоть до приблизительно 5 см (например, вплоть до приблизительно 1, 2, 3, 4 или 5 см), а более конкретно, вплоть до приблизительно 2 см. Таким образом, клапан 120 выполнен с возможностью перемещаться в пространстве дистально и проксимально при приведении в действие устройства 100, чтобы раздавать текучую среду через себя, обеспечивая более устойчивую доставку текучей среды в целевой участок доставки и проксимальное убирание инъекционной иглы из целевого участка во время доставки текучей среды.
[0081] В конкретных вариантах осуществления, дисплей 108, такой как сенсорный экран ввода-вывода, позиционируется на проксимальном конце устройства 100, к примеру, как показано на фиг. 7. В конкретных вариантах осуществления, дисплей 108 выполнен с возможностью взаимодействовать с CPU, чтобы обеспечивать возможность пользователю управлять различными функциями и признаками на устройстве 100. Например, дисплей 108 может обеспечивать возможность пользователю задавать параметры инъекции, заливать инъекционную иглу, отслеживать различные уровни давления и доставляемые текучие среды, устранять взаимные блокировки между компонентами, предоставлять информацию дозирования в реальном времени и т.д. В примере, дисплей 108 представляет собой сенсорный экран с множеством элементов управления вводом, отображаемых на нем. Тем не менее, дисплей 108 альтернативно и/или дополнительно может иметь одну или более физических кнопок, элементов управления, переключателей, круговых ручек регулировки, измерителей, тумблеров и т.д. для управления одной или более функций устройства 100. Дисплей 108 также может позиционироваться в любом месте на устройстве 100, к примеру, сверху или по бокам от устройства 100.
[0082] В конкретных вариантах осуществления устройства 100, кожух 101 также может иметь просвет 140 для вынимания стилета, который протягивается вдоль оси L1, и он выполнен с возможностью разрешать вынимание стилета 300 через себя после размещения троакара 200 (поясняется ниже). Просвет 140 может обеспечивать вынимание вручную стилета 300, например, выполнен с возможностью позволять стилету 300 протягиваться проксимально из проксимального конца просвета 140, с тем чтобы обеспечивать схватывание вручную, или просвет 140 может включать один или более механических и/или электрических механизмов, чтобы предоставлять вынимание стилета 300, например, посредством использования одной или более шестерен, колес, крюков, перемещающихся гусеничных механизмов и т.д. В конкретных вариантах осуществления инъекционного устройства, глубины проникновения иглы могут регулируемо задаваться на самом устройстве.
[0083] Устройство 100 может иметь множество размеров по мере необходимости, например, оно может садиться внутри пространства с шириной приблизительно в 300 мм, глубиной приблизительно в 200 мм и высотой приблизительно в 100 мм, а более конкретно, оно может садиться внутри пространства с шириной приблизительно в 205 мм, глубиной приблизительно в 105 мм и высотой приблизительно в 70 мм. Устройство 100 может иметь множество весов и/или масс по мере необходимости. В конкретных вариантах осуществления, устройство 100 может иметь массу меньше приблизительно 2000 г, а более конкретно, массу меньше приблизительно 1400 г. Устройство 100 может изготовлено из множества материалов, таких как металл, смола и т.д., либо из комбинации материалов. Устройство 100 может быть выполнено с возможностью быть одноразовым или может быть выполнено с возможностью представлять собой многоразовое устройство, которое требует повторной стерилизации. В конкретных вариантах осуществления, контактирующие с клеткой материалы выполнены с возможностью удовлетворять определенным требованиям использования, таким как ISO10993, что разрешать такие проблемы, как риск выщелачиваемых продуктов и совместимость со стерилизацией (в нескольких циклах). Описания, связанные с ISO10993, предоставляются в Отраслевом руководстве для персонала Управления по контролю качества пищевых продуктов и лекарственных средств (документ выдан: 16 июня 2016 года), озаглавленном: Use of International Standard ISO 10993-1, "Biological evaluation of medical devices - Part 1: Evaluation and testing within the risk management process", Центр по контролю над оборудованием и радиационной безопасностью Управления по контролю качества пищевых продуктов и лекарственных средств Министерства здравоохранения и социального обеспечения США (доступен по адресу www.fda.gov/downloads/medicaldevices/deviceregulationandguidance/guidancedocuments/ucm348890.pdf), содержимое которого полностью содержится в данном документе по ссылке. Материалы, используемые для устройства 100, также могут быть согласованными с регулирующими нормами для устройств класса I/II, и устройство 100 необязательно может исключать использование смазывающих веществ, с тем чтобы исключать влияние на жизнеспособность терапевтического клеточного материала. Описания, связанные с устройствами класса I/II, предоставляются в документе Medical Devices "Classify Your Medical Device", обновленном 27 марта 2018 года, Управление по контролю качества пищевых продуктов и лекарственных средств США (доступна по адресу www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/Overview/ClassifyYourDevice/ucm2005371.htm), содержимое которого полностью содержится в данном документе по ссылке. В различных вариантах осуществления, устройство 100 может иметь взаимную блокировку, чтобы предотвращать случайное раскрытие любого картриджа 130 с дозой лекарства или терапевтического клеточного материала. Дополнительно, в других неограничивающих вариантах осуществления, оно включает динамическую инъекционную систему, чтобы помогать проникновению ткани, к примеру, почечной капсулы, взаимоблокировочная система может использоваться для того, чтобы предотвращать случайный спуск, когда устройство не находится в надлежащей позиции относительно ткани. В некоторых вариантах осуществления, устройство 100 может требовать источника мощности, и источник мощности может быть перезаряжаемым. Например, устройство может включать зарядный интерфейс, к примеру, USB-интерфейс. В конкретных вариантах осуществления, кнопочные интерфейсы с большой вероятностью должны соответствовать стандартам удобства и простоты использования, приведенным в документе IEC 62366; см., например, "International Electrotechnical Commission (2014). Application of usability engineering to medical devices", International IEC Standard 62366, редакция 1.1 2014-01, International Electrotechnical Commission, содержимое которого полностью содержится в данном документе по ссылке.
[0084] Устройство 100 может соединяться муфтовым способом со съемным троакаром 200 через зацепляющий механизм 110, который может включать в себя множество различных отверстий с фрикционной посадкой, защелок, крюков, рычагов и т.д.
[0085] Троакар со стилетом
[0086] Фиг. 11 иллюстрирует один неограничивающий пример троакара (который, например, может быть съемным по отношению к устройству, предусмотренному в данном документе). Троакар 200 выполнен с возможностью быть размещенным внутри пациента и предоставлять доступ к участку внутренних тканей, к примеру, к содержащему опухоль почки органу или к опухоли. Троакар 200 по фиг. 11 имеет расширяющуюся головку 202 и полый удлиненный цилиндрический вал 204, протягивающийся дистально из нее. Головка 202 выполнена с возможностью съемно и с возможностью замены присоединяться к устройству 100 вдоль оси L1 в зацепляющем механизме 110. Просвет протягивается через головку 202 и удлиненный вал 204, и он выполнен с возможностью принимать инструменты, такие как стилет 300 и инъекционная игла, через себя. Удлиненный вал 204 имеет клиновидный дистальный конец 206 и стабилизирующий механизм 220 на дистальной части. Вал 204 имеет сжимающую пружинную секцию 208 и сплошную секцию 210. Сжимающая пружинная секция 208 выполнена с возможностью сжиматься и растягиваться вместе с перемещением пациента и взаимодействием с устройством 100. Пружинная секция 208 в силу этого обеспечивает поступательное движение в пространстве проксимально и дистально вдоль оси L1, обеспечивая большее стационарное взаимодействие с тканью, более плавную доставку текучей среды в участок целевых тканей и проксимальное убирание инъекционной иглы из целевого участка во время доставки текучей среды. В конкретных вариантах осуществления, пружинная секция 208 может обеспечивать перемещение в пространстве дистально и проксимально вплоть до приблизительно 5 см (например, вплоть до приблизительно 1, 2, 3, 4 или 5 см), а более конкретно, вплоть до приблизительно 2 см. Сжимающая пружинная секция 208 проиллюстрирована в средней части на валу 204. Тем не менее, сжимающая пружинная секция 208 может позиционироваться в различных точках вдоль вала 204, например, в позиции, проксимальной по отношению к средней точке вала 204, или в позиции, дистальной по отношению к средней точке. Сплошная секция 210 позиционируется на дистальной части вала 204, и она имеет стабилизирующий механизм 220.
[0087] Стабилизирующий механизм 220 выполнен с возможностью помогать стабилизировать троакар 200 относительно внутреннего участка тканей внутри пациента, когда троакар 200 размещен через внешнюю поверхность ткани, к примеру, дерму пациента. Стабилизирующий механизм 220 в силу этого выполнен с возможностью обратимо удерживать троакар 200 в закрепленной позиции относительно ткани по мере того, как инструменты проходят через троакар 200. Например, когда троакар 200 используется во время лечения почки, стабилизирующий механизм 220 может быть выполнен с возможностью обратимо блокировать дистальный конец 206 троакара 200 в позиции относительно поверхности 250 почки. Проиллюстрированный стабилизирующий механизм 220 на фиг. 11 и 12 включает в себя три подножки 222 на валах 223, зацепленные с валом 204 в шарнирных точках 224. В конкретных вариантах осуществления, подножки 222 расположены радиально симметрично вокруг вала 204 и выполнены с возможностью раскрываться, чтобы обратимо зацеплять ткань в целевом участке. В конкретных вариантах осуществления, подножки 222 выполнены с возможностью перемещаться из утопленной позиции на валу 204, например, во время вставки троакара 200 в пациента, в растянутую позицию, например, во время стабилизации троакара 200 при использовании, посредством вращения в направлении от вала 204 вокруг шарнирных точек 224 в зацепленную позицию, как проиллюстрировано на фиг. 12. В утопленной позиции, подножки 222 могут приниматься в утопленных карманах 226 таким образом, что подножки 222 сидят заподлицо с внешней поверхностью вала 204. Во время раскрытия, подножки 222 могут быть выполнены с возможностью вращаться в направлении от вала 204 на 90-180 градусов, например, приблизительно на 100 градусов, с тем чтобы зацепляться с тканью.
[0088] Множество вращательных механизмов могут включаться в вал 204, чтобы вызывать вращение подножек 222, включающих в себя шестерни, пружины, электронные моторы, валы, электронагреваемые нитиноловые распорки и т.д. Например, небольшие кулачки (не показаны) могут включаться в вал 204 приблизительно в шарнирных точках 224, которые могут быть выполнены с возможностью зацеплять один или более признаков на стилете 300 при вынимании стилета 300, причем это вынимание может быть выполнено с возможностью приводить в действие кулачки и вызывать вращение подножек 222. Стабилизирующий механизм 220, в общем, может иметь одно или более средств раскрытия, которые приводятся в действие при вынимании стилета 300. В конкретных вариантах осуществления, подножки 222 могут иметь одно или более средств зацепления, например, биомиметических микрокрючков, выполненных с возможностью обратимо зацеплять ткань при начальном поверхностном контакте. Микрокрючки могут иметь множество размеров, к примеру, составляющих приблизительно от 100 до 500 мкм в масштабе. Троакар 200 в силу этого закрепляется на месте без вызывания существенной травмы до тех пор, пока пользователь не хочет извлекать троакар 200, так что подножки 222 расцепляются. Возможны множество других средств зацепления, например, биомиметические или другие крючки, временные клеящие материалы, активное всасывание, трение, сила сжатия пружины, механизм, аналогичный защелкивающему механизму миноги, и т.д. Средство зацепления также может быть расходуемым и/или биоразлагаемым. Хотя проиллюстрированы три подножки 222, могут предоставляться множество ножек. Дополнительно, стабилизирующий механизм 220 может иметь различные альтернативные и/или дополнительные варианты осуществления, отличные от подножек 222. Например, стабилизирующий механизм может включать в себя щипковые механизмы, крючки, различные адгезивные материалы и клеи, всасывание, фрикционную посадку и т.д.
[0089] Троакар 200 также может иметь один или более дополнительных либо альтернативных зацепляющих механизмов для зацепления ткани и дополнительной стабилизации троакара 200 при размещении внутри пациента, к примеру, во входной точке троакара 200 в дерме пациента. Например, троакар 200, как проиллюстрировано, выполнен с возможностью фрикционно захватываться посредством дермы пациента при размещении. Тем не менее, возможны дополнительные зацепляющие механизмы, такие как обратимо сплющиваемый растягивающийся элемент 500, который может включаться в вал 602 троакара 600, аналогично троакару 200. В конкретных вариантах осуществления, как проиллюстрировано на фиг. 13-15, растягивающийся элемент 500 может работать аналогично анкеру для гипсокартона (к примеру, аналогично примерной системе анкеровки для гипсокартона, как проиллюстрировано на фиг. 16A-16D, показывающих сверление прорези, забивание иллюстративного анкера для гипсокартона, использование шуруповерта для того, чтобы растягивать анкеровочные плечи, и, в завершение, завинчивание винта на месте). Растягивающийся элемент 500 выполнен с возможностью перемещаться между позицией размещения, как проиллюстрировано на фиг. 13, в которой вал 602 вставляется через дерму 620 пациента, в растянутую позицию, как проиллюстрировано на фиг. 14 и 15. Растягивающийся элемент 500 имеет одну или более ножек 502, которые являются шарнирными или сгибаемыми в аппроксимированной средней точке 504 вдоль ножек 502 (проиллюстрировано на фиг. 13 посредством пунктирной линии). В конкретных вариантах осуществления, один или более растягивающих механизмов могут включаться в вал 602 и выполнены с возможностью заставлять ножки 502 растягиваться наружу, таких как резьба, выполненная с возможностью убирать дистальную часть троакара 600 проксимально после того, как он позиционируется внутри дермы 620 таким образом, что ножки 502 растягиваются наружу (как показано посредством стрелок на фиг. 13) с возможностью прикрепляться к внутренней поверхности дермы 620 (как проиллюстрировано на фиг. 14 и 15). Растягивающийся элемент 500 выполнен с возможностью изменять направление на противоположное в позицию размещения пользователем, когда пользователь хочет вынимать троакар 600 из пациента.
[0090] Примерный троакар 200 в силу этого выполнен с возможностью стабилизироваться и/или крепиться в двух точках, когда троакар 200 размещается внутри пациента, на поверхности внутренней целевой ткани (к примеру, органа, такого как почка или твердая опухоль) и во входной точке через ткань в пациента (к примеру, в дерме) с использованием одного или более механизмов, поясненных выше. Стабилизация троакара 200 выполнена с возможностью обеспечивать стабильную глубину проникновения в ткани во время раскрытия, что предотвращает или уменьшает повреждение ткани и уменьшение потерь избыточных терапевтических клеток или клеточных продуктов во время инъекции в силу сдвига инструментов, вызываемого посредством сдвига ткани и перемещения пациента, к примеру, естественного перемещения органа и дыхания пациента. В конкретных вариантах осуществления, один или более поверхностных признаков также могут добавляться во внешнюю дистальную поверхность вала 204 троакара 200, таких как выпуклости, пазы, прорези, пометки и т.д., которые выполнены с возможностью предоставлять лучшую визуализацию местоположения троакара 200, к примеру, согласно ультразвуку, и в силу этого более точное размещение внутри пациента. Для иллюстрации, примерные эхогенные поверхностные признаки 272 проиллюстрированы в неограничивающем варианте осуществления ультразвуковой биопсийной иглы на фиг. 17. Можно считать, что "эхогенный" означает обладание свойством видимости при ультразвуковой визуализации. В качестве неограничивающего примера, проиллюстрированная игла представляет собой Cook Medical EchoTip®. Троакар 200 необязательно может использоваться с канюлей или втулкой троакара требуемым образом, к примеру, с втулкой троакара, которая имеет вес, по меньшей мере, в 20 г, и она может иметь такую размер и форму, что она может проникать через пациента на множество глубин, к примеру, приблизительно на 3-5 мм в участок целевых внутренних тканей, такой как почка пациента. Троакар 200 может иметь множество длин, к примеру, приблизительно в 5-25 см, более конкретно, в 10-20 см, и еще более конкретно, приблизительно в 15-20 см. Пружинная секция 208 может иметь множество длин, к примеру, приблизительно в 5-10 см.
[0091] Стилет 300 выполнен с возможностью приниматься в просвете троакара 200 вдоль оси L1 во время продвижения и размещения троакара 200 внутри пациента. Стилет 300 имеет удлиненный вал 302 стилета с дистальным наконечником 304. Вал 302 имеет такой размер и форму, что он принимается в троакаре 200 и протягивается дистально и проксимально из троакара 200. Например, дистальный наконечник 304 может быть выполнен с возможностью протягиваться дистально из клиновидного дистального конца 206 троакара 200 таким образом, что дистальный наконечник 304 может протыкать ткань, и проксимальный конец стилета 300 может протягиваться проксимально из троакара 200 для вынимания стилета 300. Примерный дистальный наконечник 304 имеет тупоконическую форму, как проиллюстрировано на фиг. 18A, но могут использоваться множество других форм, такие как пирамидальная, как проиллюстрировано на фиг. 18B, остроконическая, как проиллюстрировано на фиг. 18C, и тупая, как проиллюстрировано на фиг. 18D. Хотя могут использоваться множество наконечников, в конкретных вариантах осуществления, тупоконический наконечник может использоваться эффективно в ткани почки, поскольку тупоконический наконечник выполнен с возможностью минимизировать травму, вызываемую при первоначальной вставке троакара 200 со стилетом 300 в участок целевых тканей, к примеру, в почку. После размещения троакара 200 внутри пациента, стилет 300 может быть выполнен с возможностью выниматься. Стилет 300 может быть выполнен с возможностью вручную выниматься из троакара 200 непосредственно, когда устройство 100 не зацепляется с троакаром 200, либо он может быть выполнен с возможностью выниматься из троакара 200 через необязательный просвет 140 для вынимания устройства 100, вручную, механически, электрически либо через некоторую комбинацию, как пояснено выше. В конкретных вариантах осуществления, стилет 300 может иметь один или более признаков, выполненных с возможностью приводить в действие раскрытие стабилизирующего механизма 220 троакара 200 при вынимании стилета 300 из него. Например, стилет 300 может иметь один или более признаков зубьев шестерни, позиционированных в направлении дистального наконечника 304, которые выполнены с возможностью приводить в действие кулачки на троакаре 200 и вызывать вращение подножек 222.
[0092] Таким образом, в неограничивающем примере, троакар 200 (с или без втулки) может быть выполнен с возможностью протыкать кожу пациента за счет действия стилета 300. Примерная целевая глубина проникновения троакара 200 и/или втулки в ткань, к примеру, в орган (например, в почку) может составлять приблизительно 2-6 мм, или более предпочтительно, приблизительно 3-5 мм, когда стилет 300 вынимается. Когда стилет 300 вынимается, троакар 200 (т.е. втулка троакара) затем может закрепляться на месте. Крепление троакара 200 (т.е. втулки троакара) может осуществляться, по меньшей мере, в двух точках, как фрикционной захват в проходе для дермы и т.п., как более слабое взаимодействие в ткани, в которую проникает троакар 200 (т.е. втулка троакара), к примеру, в капсуле почки. Троакар (т.е. втулка троакара) 200 может быть выполнен с возможностью стабилизироваться на глубине проникновения в ткань, к примеру, в орган (например, в почку), во время процедуры. Тем не менее, размещение компонентов, проникающих через ткань, может быть динамическим вследствие потенциального сдвига ткани, к примеру, органа (например, почки) и по циклу дыхания пациента. Следовательно, вредоносное перемещение дермальной анкерной точки относительно анкерной точки внутренней ткани, к примеру, органа (например, почки) может возникать и в силу этого может минимизироваться с использованием компонентов, предусмотренных в данном документе, таких как стабилизирующий механизм 220. Минимизация травмы ткани, к примеру, органа (например, почки) также может быть преимущественной для общей успешности любого лечения. Например, травма может происходить, когда возникает непреднамеренное перемещение иглы 400 в троакаре 200, которое разрывает ткань, к примеру, орган (например, почку). Травма также может возникать при первоначальной вставке троакара 200 в ткань, к примеру, в орган (например, в почку), например, если дистальный наконечник 304 стилета 300 имеет любое действие резания (к примеру, острую точку, которая возникает в пирамидальных или остроконических конструкциях, поясненных выше). Таким образом, стабилизация троакара 200 может помогать уменьшать или исключать травму ткани за счет уменьшения или исключения непреднамеренного перемещения иглы 400, и тупоконический наконечник может использоваться для протыкания ткани, к примеру, органа (например, почки) и минимизации травмы.
[0093] В конкретных вариантах осуществления, травма может происходить в силу двух источников: 1) имеются морфологии стилета/наконечника иглы, которые наносят большие повреждения ткани, и 2) непреднамеренное перемещение троакара/иглы во время процедуры может разрывать почку. В конкретных вариантах осуществления, из точек стилета, показанных на фиг. 18A-D, рекомендуются тупоконические для протыкания почки и минимизации травмы. В конкретных вариантах осуществления, наконечник иглы является тупым и нережущим. Размер-калибр игл также может способствовать травме. В конкретных вариантах осуществления, меньшие иглы вызывают менее серьезную травму, при этом могут быть неэффективными при протыкании фиброзной капсулы. В конкретных вариантах осуществления, большие размеры игл являются проще видимыми посредством ультразвука с учетом размещения. Таким образом, в конкретных вариантах осуществления, в конструктивном решении, которое включает в себя динамический режим, чтобы протыкать капсулу эффективно с помощью небольшой иглы, обеспечивается возможность менее серьезных травм и меньший риск невозможности проникать через капсулу, но возникают потенциальные проблемы визуализации. В конкретных вариантах осуществления, существенные различия между втулкой и иглой могут приводить к изгибу небольшой иглы во втулке, и устройство выполнено с возможностью минимизировать изгиб иглы во втулке.
[0094] Инъекционная игла
[0095] Фиг. 19 иллюстрирует неограничивающий пример инъекционной иглы 400, которая выполнена с возможностью зацепляться с устройством 100 и вставляться через троакар 200, когда троакар 200 находится на месте внутри пациента. В конкретных вариантах осуществления, игла 400 выполнена с возможностью доставлять фармацевтический состав на основе текучей среды (к примеру, составы, содержащие клетки и/или их продукт) в целевой участок внутренних тканей, к примеру, в орган (например, в почку), из устройства 100. Проиллюстрированная игла 400 имеет зацепляющую головку 402 и удлиненный вал 404 с просветом через нее и дистальный наконечник 406 на ней. Дистальный наконечник 406 имеет прорезь, чтобы обеспечивать возможность текучей среде протекать дистально из иглы 400. Зацепляющая головка 402 выполнена с возможностью съемно и с возможностью замены присоединяться к устройству 100 вдоль оси L1 в зацепляющем механизме 110. Когда головка 402 присоединяется, она выполнена с возможностью зацепляться с клапаном 120. При приведении в действие устройства 100, головка 402 и просвет удлиненного вала 404 выполнены с возможностью создавать проток для текучей среды для текучей среды в резервуаре для текучей среды, соединенном с приемным устройством 106 для текучей среды из резервуара для текучей среды, через клапан 120, вдоль просвета вала 404 и из отверстия в дистальном наконечнике 406. Игла 400 также выполнена с возможностью убираться из своей позиции в целевой ткани по мере того, как текучая среда доставляется при приведении в действие. Размер, длина и калибр инъекционной иглы 400 могут варьироваться. Например, игла 400 может составлять приблизительно от 25 г приблизительно до 20 г. Размер-калибр игл может способствовать травме участка тканей, и большие размеры-калибры (которые являются меньшими иглами) могут вызывать менее серьезную травму.
[0096] При рассмотрении размера игл в применении к лечению органа (например, почки), может искаться баланс между проникновением в капсулу почечного тельца и потенциальной травмой ткани. Как проиллюстрировано на фиг. 20, капсула почечного тельца представляет собой жесткий фиброзный слой, который окружает почку. Таким образом, большая игла является более полезной для протыкания капсулы почечного тельца. Тем не менее, большая игла может вызывать более серьезную травму почки. В силу этого может искаться оптимальный размер игл, который учитывает взаимоисключающие факторы, как проиллюстрировано на фиг. 21.
[0097] Хотя меньшие иглы могут быть менее эффективными в протыкании ткани, игла 400, используемая в сочетании с троакаром 200 и стилетом 300 здесь, может быть выполнена с возможностью обеспечивать как успешное протыкание ткани, так и размещение меньшей иглы. Множество различных игл могут использоваться в данном документе. Таблица 2 иллюстрирует дополнительные примерные размеры-калибры игл, которые могут необязательно использоваться в данном документе.
Табл. 2
[0098] В конкретных вариантах осуществления, игла представляет собой иглу 18-30 калибра. В конкретных вариантах осуществления, игла меньше 20 калибра. В конкретных вариантах осуществления, игла меньше 21 калибра. В конкретных вариантах осуществления, игла меньше 22 калибра. В конкретных вариантах осуществления, игла меньше 23 калибра. В конкретных вариантах осуществления, игла меньше 24 калибра. В конкретных вариантах осуществления, игла меньше 25 калибра. В конкретных вариантах осуществления, игла меньше 26 калибра. В конкретных вариантах осуществления, игла меньше 27 калибра. В конкретных вариантах осуществления, игла меньше 28 калибра. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 20 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 21 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 22 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 23 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 24 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 25 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 26 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 27 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 28 калибр. В конкретных вариантах осуществления, игла меньше 29 калибра. В конкретных вариантах осуществления, игла имеет приблизительно 29 калибр.
[0099] В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,84 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,61 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,51 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,41 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,33 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,25 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,20 мм. В конкретных вариантах осуществления, внутренний диаметр иглы меньше 0,15 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 1,27 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,91 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,81 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,71 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,64 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,51 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,41 мм. В конкретных вариантах осуществления, внешний диаметр иглы меньше 0,30 мм. В конкретных вариантах осуществления, игла имеет один из размеров в следующей таблице:
[00100] Игла 400, например, может инъецироваться в участке внутренних тканей, который находится на относительно большом расстоянии от устройства 100, к примеру, на расстоянии приблизительно от 10 см до 20 см. В таком примере, троакар 200 также может механически поддерживать иглу 400 против скручивания, которое может развиваться в результате проникновения в участок внутренних тканей на относительно большом расстоянии. В конкретных вариантах осуществления, длина иглы 400 может иметь такую конфигурацию, в которой приблизительно от 5 см приблизительно до 6 см дистальной части иглы 400 протягивается за пределы самого дистального конца троакара 200. Например, приблизительно 5,3 см (например, приблизительно 5,5, 6 или 6,5 см) иглы 400 может быть выполнено с возможностью протягиваться дистально за пределы самого дистального конца троакара 200, как проиллюстрировано на фиг. 22. Длина может обеспечивать достаточную глубину проникновения иглы 400 в целевой ткани, к примеру, в органе (например, в почке), для осаждения терапевтических клеток или клеточных продуктов. В конкретных вариантах осуществления инъекционного устройства, глубины проникновения иглы могут регулируемо задаваться. В конкретных вариантах осуществления, при такой длине, прорезь в дистальном наконечнике 406 иглы 400 может позиционироваться приблизительно на 5,1 см позади самого дистального конца троакара 200, как проиллюстрировано на фиг. 23. В конкретных вариантах осуществления, прорезь иглы предпочтительно расположена поперечно приблизительно на 0,2 см от наконечника иглы, и прорезь расположена на 5,1 см позади троакара при длине в 5,3 см. В конкретных вариантах осуществления, связанных с удлинением приблизительно в 6 см, прорезь расположена приблизительно на 5,8 см позади троакара. В конкретных вариантах осуществления, поперечное позиционирование выходной прорези имеет преимущество касательно экструзии и размещения терапевтической клетки при обеспечении того, что игла является бескерновой. В конкретных вариантах осуществления, прорезь необязательно может быть расположена поперечно, что позволяет предоставлять преимущество касательно экструзии и размещения терапевтических клеток или клеточных продуктов в участке целевых тканей. В различных примерах, один или более поверхностных признаков также могут добавляться во внешнюю дистальную поверхность удлиненного вала 404 иглы 400, аналогично троакару 200, таких как выпуклости, пазы, пометки и т.д., которые выполнены с возможностью предоставлять лучшую визуализацию местоположения иглы 400, к примеру, согласно ультразвуку, и в силу этого более точное размещение внутри пациента. Более одной иглы 400 варьирующихся размеров также могут использоваться в зависимости от требуемого лечения. В некоторых примерах, размер-калибр игл может способствовать травме. Например, большие размеры-калибры (которые являются меньшими иглами) могут вызывать менее серьезную травму, при этом могут быть неэффективными в протыкании ткани, к примеру, фиброзной капсулы. Следовательно, в данном документе предусмотрены компоненты, такие как троакар 200, которые могут помогать через динамический режим и/или динамическое перемещение протыкать ткань, к примеру, капсулу, эффективно с помощью небольшой иглы. Это может приводить к менее серьезной травме и меньшему риску невозможности проникать через ткань, к примеру, через капсулу.
[00101] В конкретных вариантах осуществления, компоненты в данном документе могут конструироваться способом, который учитывает потребности пользователя, к примеру, хирурга с использованием устройства. При использовании, все компоненты в данном документе, к примеру, подвижные поверхности, предпочтительно могут быть удобными и помещаться в широком диапазоне размеров мужских и/или женских рук. Противоскользящие поверхности необязательно могут интегрироваться в один или более компонентов, поясненных в данном документе, например, предоставляющих поверхностные признаки, поверхности и/или материалы, которые хорошо взаимодействуют и предотвращают утечку в хирургических перчатках. В конкретных вариантах осуществления, интерфейсы ввода могут легко наблюдаться и легко активироваться пальцами в перчатках. В конкретных вариантах осуществления, один или более интерфейсов могут предоставлять тактильную обратную связь при активации, и если какая-либо часть процесса инъекции является механической, тактильная обратная связь может быть важной для успешного использования компонентов, раскрытых в данном документе, например, по мере того, как текучая среда, такая как терапевтический клеточный материал, инъецируется в ткань, к примеру, в почечное пространство. Пользователи зачастую отдают предпочтение меньшим шприцам, поскольку меньшие шприцы требуют меньшей силы для инфузии своего содержимого, и меньшие шприцы иногда удерживаются в атипичных позициях рук для лучшего управления, как проиллюстрировано в неограничивающем примере на фиг. 24. Таким образом, эргономика и удобство посадки компонентов в данном документе могут учитываться. В конкретных вариантах осуществления, могут предоставляться одна или более инструкций, инструкций по применению, руководств, видео, руководств по эксплуатации и т.д., и они могут индивидуально адаптироваться к потребностям конечного пользователя (к примеру, хирурга). Инструкции и т.д. могут быть выполнены с возможностью быть в соответствии с и/или задаваться посредством потребностей процесса конструирования подрядной инженерной организации.
[00102] Устройство 100, троакар 200 и игла 400 могут использоваться множеством различных способов. Например, инъекционное устройство 100 может присоединяться к троакару 200 со стилетом 300 на месте в троакаре 200. Картридж 130 или другой резервуар для текучей среды может зацепляться с устройством 100 в этот момент или до инъекции. Троакар 200 и стилет 300 затем могут маневрировать с возможностью проникать через внешнюю поверхность ткани, к примеру, через дерму и через внутренний целевой участок тканей, к примеру, через орган (например, почку) пациента на требуемой глубине (как пояснено выше). Стилет 300 затем может выниматься из троакара 200 через просвет 140 для вынимания. Вынимание стилета 300 может спускать собачку для приведения в действие стабилизирующего механизма 220 на троакаре 200. Как проиллюстрировано на фиг. 12, подножки 222 могут раскрываться, чтобы схватывать или зацеплять ткань. Троакар 200 может отсоединяться от устройства 100, и в этот момент во время использования, троакар 200 должен поддерживаться через фрикционное взаимодействие с дермой и через использование стабилизирующего механизма 220. В неограничивающем иллюстративном примере, фиг. 25 иллюстрирует упрощенную схему троакара 200, используемого для почки, в которой троакар 200 подвергается фрикционному взаимодействию с дермой и подвергается стабилизации через использование стабилизирующего механизма 220 относительно коркового вещества почки, которое представляет собой внешнюю часть почки между капсулой почечного тельца и мозговым веществом почки, которая может варьироваться по толщине в зависимости от пациента. Например, кортикальная толщина может составлять приблизительно 3-12 мм, а более конкретно, приблизительно 3,2-11 мм со средним значением приблизительно в 5,9 мм. Инъекционная игла 400 может зацепляться с устройством 100. Игла 400 затем может вставляться в троакар 200 до тех пор, пока игла 400 не проникает через целевую ткань через идентичную прорезь, созданную посредством стилета 300 на требуемой глубине (как пояснено выше), и актуатор 104 на устройстве 100 может приводиться в действие, чтобы доставлять текучую среду, к примеру, терапевтические клетки или клеточные продукты, в целевой участок. Стабилизирующий механизм 220 может работать в сочетании со сжимающей пружинной секцией 208 троакара 200 и гибким монтажом клапана 120, чтобы поглощать движение участка тканей, к примеру, органа (например, почки), относительно держания и приведения в действие, пользователем, устройства 100. По мере того, как текучая среда доставляется, игла 400 может убираться из своей позиции проникновения в участке целевых тканей. Спусковой рычаг активирует электромеханическую систему, которая доставляет импульсы терапевтического раствора в тракте движения иглы по мере того, как игла убирается. Могут выполняться несколько инъекций в идентичный участок тканей, к примеру, в орган.
[00103] Альтернативно, троакар 200 и стилет 300 могут маневрировать на место внутри пациента без присоединения к устройству 100, и стилет 300 может выниматься, чтобы приводить в действие стабилизирующий механизм 220 на троакаре 200. Игла 400 с зацепленным устройством 100 затем может вставляться в троакар 200 для доставки текучей среды. Троакар 200 со стилетом 300 также может позиционироваться внутри пациента при присоединении к устройству 100, и затем устройство 100 может отсоединяться от троакара 200, чтобы вручную вынимать стилет 300 до присоединения иглы 400 и ее вставки в троакар 200. Если троакар 200 имеет дополнительный зацепляющий механизм, такой как обратимо сплющиваемый растягивающийся элемент 500, инъекционное устройство 100 может присоединяться к троакару 200 со стилетом 300 на месте в троакаре 200. Троакар 200 и стилет 300 затем могут маневрировать с возможностью проникать через внешнюю поверхность ткани и внутренний целевой участок тканей. После вынимания стилета 300 и отсоединения устройства 100, но до вставки иглы 400, растягивающийся элемент 500 может раскрываться. Тем не менее, этот порядок может изменяться в зависимости от механизма использования различных зацепляющих механизмов. Когда устройство 100 используется конкретно для лечения почек, троакар 200, стилет 300 и игла 400 могут использоваться, как пояснено выше, для того, чтобы протыкать капсулу почки, область потенциально фиброзной ткани и доставлять запрещенный объем в почку при одновременном извлечении иглы 400, чтобы обеспечивать пространство для растягивания для доставляемого болюса терапевтических клеток или клеточных продуктов. При использовании в данном документе и в зависимости от контекста, "фиброзный" означает или обозначает осаждение фиброзной внеклеточной матрицы, которая обычно является более плотной, чем окружающая ткань. Плотная фиброзная ткань зачастую представляет собой результат состояния хронического заболевания. В конкретных вариантах осуществления, фиброзная ткань представляет собой результат состояния хронического заболевания. В конкретных вариантах осуществления, плотная фиброзная ткань представляет собой результат состояния хронического заболевания. В конкретных вариантах осуществления, фиброзная ткань присутствует в органе, проходящем лечение (например, представляет собой участок доставки композиции, доставляемой с использованием) с помощью устройства, системы или способа, предусмотренного в настоящем документе.
[00104] В конкретных вариантах осуществления, до использования картридж 130 может нагреваться приблизительно до 25-30 °C, а более конкретно, приблизительно до 26-28 °C. В конкретных вариантах осуществления, до использования картридж 130 может нагреваться приблизительно до 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 или 37°C. В конкретных вариантах осуществления, нагревание может возникать в течение управляемого периода времени, к примеру, приблизительно в течение 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55 или 60 минут или приблизительно от 15 приблизительно до 45 минут. В конкретных вариантах осуществления, после того как картридж 130 нагрет, доставка текучей среды в нем предпочтительно может возникать приблизительно в пределах 0,5, 1, 1,5, 2 или 2,5 часов, чтобы исключать выбрасывание картриджа 130.
[00105] В конкретных вариантах осуществления, после доставки текучей среды и вынимания инъекционной иглы 400 из участка целевых тканей и троакара 200, заглушка 700 (к примеру, гидрогелевая заглушка или тампон, такой как тампон Gelfoam®) может вручную вставляться в троакар 200 и выталкиваться и выдавливаться из дистального конца 206 троакара 200, чтобы закрывать проникающую рану. Устройство 100 и троакар 200 могут быть выполнены с возможностью приспосабливать доставку заглушки. В конкретных вариантах осуществления, тампон (такой как тампон Gelfoam®), который начинается приблизительно от 2 приблизительно до 4 мм приблизительно на 10 мм, сжимается, с тем чтобы обеспечивать вставку (например, вставку вручную) в троакар, и выталкивается и выдавливается из наконечника троакара, с тем чтобы закрывать рану в почечной капсуле. В конкретных вариантах осуществления, тампон представляет собой небольшой кусок поглощающей ваты или другого мягкого материала (к примеру, гидрогеля). В конкретных вариантах осуществления, тампон или заглушка используется для того, чтобы затыкать рану или другое отверстие в теле или органе. В конкретных вариантах осуществления, устройство выполнено с возможностью приспосабливать этот терминальный процесс закрытия раны. В неограничивающем иллюстративном примере, фиг. 26 иллюстрирует упрощенную схему троакара 200, используемого в почке, в котором заглушка 700 "заряжается по принципу мушкета" либо помещается на место вручную через троакар 200. Троакар 200 затем может выниматься из пациента. Таким образом, в течение процесса, раскрытого в данном документе, один или более компонентов могут помогать в ручном протыкании ткани, таких как фиброзные почечные капсулы, плавная управляемая доставка текучей среды, такой как терапевтический клеточный материал, и позиционная стабильность троакара в динамическом окружении пациента (что, в свою очередь, предоставляет стабильность при доставке терапевтического клеточного материала при минимизации травмы ткани), которые вызывают сложности в других подходах, но один или более текущих компонентов в данном документе могут быть выполнены с возможностью справляться с ними.
[00106] Хотя описание приводится с фокусировкой на почке в качестве участка целевых тканей и/или органа, компоненты в данном документе могут иметь широкое применение для множества органов и/или участков внутренних тканей и/или соответствующих методов терапии. В качестве неограничивающего примера, компоненты, поясненные в данном документе, в силу этого представляют собой карманные инъекционные компоненты, сконструированные с возможностью доставлять один или более инъецируемых объемов (к примеру, при клеточной терапии) в один или более участков целевых тканей, таких как паренхимальные и/или стромальные отделы больного участка, к примеру, органа (такого как почка или участок опухоли). В конкретных вариантах осуществления, компоненты в силу этого могут протыкать внешнюю поверхность участка тканей, к примеру, участка органа, такого как почечная капсула, область потенциально фиброзной ткани в почке и могут доставлять запрещенный объем вдоль инъекционного тракта при одновременном извлечении инъекционной иглы, чтобы обеспечивать пространство для растягивания для доставляемого объема, к примеру, болюса терапевтического клеточного материала. В конкретных вариантах осуществления, могут быть возможны несколько инъекций в идентичный целевой участок, к примеру, в орган. В конкретных вариантах осуществления, компоненты в данном документе могут иметь средство стабилизировать себя относительно поверхности участка целевой ткани, к примеру, органа, через раскрытие троакара, могут принимать предварительно наполненные асептические картриджи, содержащие объем, к примеру, раствор с терапевтическим клеточным материалом, и могут быть эргономичными для намеченного врача, к примеру, хирурга. В конкретных вариантах осуществления, компонент в данном документе может быть интуитивным и приспосабливать иглы для подкожных инъекций в пределах указанного диапазона размеров и может обладать способностью задавать переменные инъецируемые или раздаваемые объемы и глубины проникновения.
[00107] В конкретных вариантах осуществления, инъекционное устройство может состоять из одного физического устройства, которое может принимать терапевтические дозы на основе картриджа. В конкретных вариантах осуществления, стандартные комбинации троакара/втулки/иглы могут включаться в устройство из типовых, индивидуально упакованных и стерилизованных запасов. В таких примерах, целевые размеры могут меняться из различных стандартных размеров, к примеру, иглы для подкожных инъекций составляют в диапазоне приблизительно от 25 грамм минимум приблизительно до 20 грамм максимум, и комбинации троакара/втулки составляют, по меньшей мере, приблизительно 20 г. В конкретных вариантах осуществления, размер троакара/втулки составляет приблизительно от 21 г приблизительно до 18 г. В конкретных вариантах осуществления, исследуемый объект имеет высокий индекс массы тела (например, BMI, по меньшей мере, приблизительно в 35, 36, 37, 38, 39 или 40 кг/м2). BMI представляет собой показатель ожирения, и высокий BMI ассоциирован с сильным ожирением. В конкретных вариантах осуществления, размер втулки приблизительно от 20 г приблизительно до 18 г и игла приблизительно в 21 г и длина приблизительно от 20 приблизительно до 30 (например, 25 см) используется для пациентов с высоким BMI. В конкретных вариантах осуществления, в данном документе предусмотрено устройство или система, которое является полезным для лечения пациентов с нормальным и высоким BMI. В конкретных вариантах осуществления, инъекционный тракт инъекционной иглы в целевой участок, к примеру, в орган может предоставляться посредством спаривания с троакаром. В конкретных вариантах осуществления, троакар может служить для того, чтобы механически поддерживать инъекционную иглу против скручивания, которое может развиваться в некоторых случаях в результате проникновения в целевую ткань, к примеру, в орган, на относительно большом расстоянии, к примеру, приблизительно в 5-25 см, а более конкретно, приблизительно в 10-20 см от инъекционного устройства.
[00108] В конкретных вариантах осуществления одного или более компонентов в данном документе, компоненты могут помечаться ISO-совместимыми предупреждающими знаками в соответствии с надлежащей документацией регулирующего органа (например, США 21 C.F.R. § 801). В конкретных вариантах осуществления, компоненты в данном документе могут считаться безопасными для неуправляемого доступа, когда различные обшивки кожуха и продукта находятся на месте и закрепляются, и компоненты в данном документе необязательно могут не иметь доступных острых краев с радиусом менее приблизительно 0,5 мм, исключая различные компоненты троакара, втулки и иглы. В конкретных вариантах осуществления, компоненты могут не иметь внешне доступного электрического соединения, которое допускает снабжение питанием более чем приблизительно в 1,0 А приблизительно при 5,25 В постоянного тока. В конкретных вариантах осуществления, любые материалы, такие как пластмасса и/или отделочные материалы, могут иметь рейтинг воспламеняемости UL94 V-0 или лучше.
[00109] В конкретных вариантах осуществления, компоненты в данном документе могут быть выполнены с возможностью использоваться в температурно управляемых окружениях в помещениях, к примеру, в клиниках и больницах, и компоненты могут быть выполнены с возможностью удовлетворять требованиям по производительности в пределах диапазона изменения условий окружающей среды, предоставленных в таблице 3:
Табл. 3
[00110] В конкретных вариантах осуществления, компоненты, раскрытые в данном документе, могут быть выполнены с возможностью работать нормально после различных процессов стерилизации (например, стандартных процессов стерилизации), к примеру, через гамма-излучение, этиленоксид, E-пучок или газ. В конкретных вариантах осуществления, включающих одну или более пластмасс, пластмасса может быть выполнена с возможностью не становиться ломкой посредством процесса стерилизации, и обесцвечивание или изменение цвета может быть минимальным. В конкретных вариантах осуществления в данном документе, которые включают один или более электромеханических компонентов, могут использоваться процессы стерилизации, которые являются совместимыми с электронным оборудованием, которые могут включать различные этапы и дополнительные признаки, такие как вынимание съемных обшивок и/или поверхностей, которые могут стерилизоваться и асептически содержать рабочие элементы одного или более компонентов. Таблица 4 и таблица 5 предоставляют материалы на основе смолы, которые являются совместимыми с различными типами стерилизации.
Табл. 4
Табл. 5
2PVC, акриловые полимеры и PC требуют корректирующей раскраски, чтобы компенсировать обесцвечивание.
[00111] В конкретных вариантах осуществления, одни или более компонентов в данном документе, которые упакованы, могут быть выполнены с возможностью работать нормально при возврате в рабочий диапазон изменения условий окружающей среды после длительного периода времени. Например, таблица 6 иллюстрирует упаковывание с подверганием воздействию различных диапазонов изменения условий окружающей среды в течение 72 часов хранения, после чего компоненты работают нормально:
Табл. 6
[00112] В конкретных вариантах осуществления, которые упакованы, упакованные компоненты могут конфигурироваться и упаковываться таким образом, что они не получают функциональное или видимое косметическое повреждение при поставке коммерческими перевозчиками. Дополнительно, различные упакованные варианты осуществления компонентов в данном документе могут конфигурироваться и упаковываться таким образом, что они не получают функциональное или видимое косметическое повреждение при падении с высоты приблизительно в 1 метр.
[00113] Каждый компонент, поясненный выше, может использоваться независимо друг от друга, использоваться полностью вместе либо в любой комбинации означенного. Например, компоненты могут предоставляться независимо или могут предоставляться в различных комбинациях, системах и комплектах конечным пользователям. Различные комбинации картриджей 130 и/или диапазоны размеров и типы игл 400, троакаров 200 и/или стилетов 300 также могут содержать устройство 100. В конкретных вариантах осуществления, один или более компонентов либо все компоненты вместе могут упаковываться и поставляться в качестве полностью собранного блока, готового к действиям конечного пользователя после вынимания из упаковки. В конкретных вариантах осуществления, инструкции по сборке и/или применению могут предоставляться с любыми компонентами, например, с возможностью для конечного пользователя собирать или конфигурировать один или более из них для работы менее чем приблизительно за 10 минут.
[00114] Неограничивающие примеры инъекционных составов
[00115] Устройства и системы, предусмотренные в настоящем документе, могут быть выполнены с возможностью доставки различных фармацевтических составов на основе текучей среды. В конкретных вариантах осуществления, составы на основе текучей среды содержат активный агент (такой как клетка, клеточный продукт или химическое соединение) и температурочувствительный биоматериал. В конкретных вариантах осуществления, температурочувствительный биоматериал представляет собой фармацевтически приемлемый носитель для активного агента. В конкретных вариантах осуществления, состав включает биоматериалы, имеющие свойства, которые создают благоприятное окружение для активного агента, такого как биоактивные клетки почечного эпителия, который должен применяться к исследуемому объекту.
[00116] В конкретных вариантах осуществления, состав на основе текучей среды способен превращаться в гидрогель, например, состав представляет собой гидрогель, который имеет температуру, превышающую температуру плавления.
[00117] В конкретных вариантах осуществления, устройства и системы, предусмотренные данном документе, выполнены с возможностью доставлять состав (к примеру, NKA), который нагрет до температуры, достаточной для того, чтобы расплавлять или иным способом обеспечивать то, что композиция представляет собой жидкость. В конкретных вариантах осуществления, устройство выполнено с возможностью подогревать состав или поддерживать температуру, при которой состав представляет собой жидкость.
[00118] В конкретных вариантах осуществления, температурная чувствительность состава может варьироваться посредством регулирования процентной доли биоматериала в составе. Например, процентная доля желатина в растворе может регулироваться, чтобы модулировать температурную чувствительность желатина в конечном составе (например, жидкости, геле, бусинках и т.д.).
[00119] В конкретных вариантах осуществления, температурочувствительный биоматериал может иметь (i) практически твердое состояние приблизительно при 8°C или ниже и (ii) практически жидкое состояние при температуре окружающей среды или выше. В конкретных вариантах осуществления, температура окружающей среды составляет приблизительно комнатную температуру.
[00120] В конкретных вариантах осуществления, состояние температурочувствительного биоматериала представляет собой практически твердое состояние при температуре приблизительно 8°C или ниже. В конкретных вариантах осуществления, практически твердое состояние поддерживается приблизительно при 1°C, приблизительно при 2°C, приблизительно при 3°C, приблизительно при 4°C, приблизительно при 5°C, приблизительно при 6°C, приблизительно при 7°C или приблизительно при 8°C. В конкретных вариантах осуществления, практически твердое состояние имеет форму геля. В конкретных вариантах осуществления, состояние температурочувствительного биоматериала представляет собой практически жидкое состояние при температуре окружающей среды или выше. В конкретных вариантах осуществления, практически жидкое состояние поддерживается приблизительно при 25°C, приблизительно при 25,5°C, приблизительно при 26°C, приблизительно при 26,5°C, приблизительно при 27°C, приблизительно при 27,5°C, приблизительно при 28°C, приблизительно при 28,5°C, приблизительно при 29°C, приблизительно при 29,5°C, приблизительно при 30°C, приблизительно при 31°C, приблизительно при 32°C, приблизительно при 33°C, приблизительно при 34°C, приблизительно при 35°C, приблизительно при 36°C или приблизительно при 37°C. В конкретных вариантах осуществления, температура окружающей среды составляет приблизительно комнатную температуру.
[00121] В конкретных вариантах осуществления, состояние температурочувствительного биоматериала представляет собой практически твердое состояние при температуре приблизительно температуры окружающей среды или ниже. В конкретных вариантах осуществления, температура окружающей среды составляет приблизительно комнатную температуру. В конкретных вариантах осуществления, практически твердое состояние поддерживается приблизительно при 17°C, приблизительно при 16°C, приблизительно при 15°C, приблизительно при 14°C, приблизительно при 13°C, приблизительно при 12°C, приблизительно при 11°C, приблизительно при 10°C, приблизительно при 9°C, приблизительно при 8°C, приблизительно при 7°C, приблизительно при 6°C, приблизительно при 5°C, приблизительно при 4°C, приблизительно при 3°C, приблизительно при 2°C или приблизительно при 1°C.
[00122] В конкретных вариантах осуществления, клеточные популяции и препараты, которые должны доставляться, могут наноситься, осаждаться, заглубляться, присоединяться, сеяться, суспендировать или улавливаться в температурочувствительном биоматериале. В конкретных вариантах осуществления, клеточные популяции могут собираться в качестве трехмерных клеточных агрегатов или сфероидов либо трехмерных тубулярных структур в температурочувствительном биоматериале.
[00123] В конкретных вариантах осуществления, температурочувствительный биоматериал имеет переходное состояние между первым состоянием и вторым состоянием. В конкретных вариантах осуществления, переходное состояние представляет собой переходное из твердое в жидкое состояние между температурой приблизительно в 8°C и приблизительно температурой окружающей среды. В конкретных вариантах осуществления, температура окружающей среды составляет приблизительно комнатную температуру. В конкретных вариантах осуществления, переходное из твердое в жидкое состояние возникает при одной или более температур приблизительно в 8°C, приблизительно в 9°C, приблизительно в 10°C, приблизительно в 11°C, приблизительно в 12°C, приблизительно в 13°C, приблизительно в 14°C, приблизительно в 15°C, приблизительно в 16°C, приблизительно в 17°C и приблизительно в 18°C.
[00124] В конкретных вариантах осуществления, температурочувствительные биоматериалы имеют определенную вязкость при данной температуре, измеренную в сантипуазах (сП). В конкретных вариантах осуществления, биоматериал имеет вязкость при 25°C приблизительно от 1 сП приблизительно до 5 сП, приблизительно от 1,1 сП приблизительно до 4,5 сП, приблизительно от 1,2 сП приблизительно до 4 сП, приблизительно от 1,3 сП приблизительно до 3,5 сП, приблизительно от 1,4 сП приблизительно до 3,5 сП, приблизительно от 1,5 сП приблизительно до 3 сП, приблизительно от 1,55 сП приблизительно до 2,5 сП или приблизительно от 1,6 сП приблизительно до 2 сП. В конкретных вариантах осуществления, биоматериал имеет вязкость при 37°C приблизительно от 1,0 сП приблизительно до 1,15 сП. Вязкость при 37°C может составлять приблизительно 1,0 сП, приблизительно 1,01 сП, приблизительно 1,02 сП, приблизительно 1,03 сП, приблизительно 1,04 сП, приблизительно 1,05 сП, приблизительно 1,06 сП, приблизительно 1,07 сП, приблизительно 1,08 сП, приблизительно 1,09 сП, приблизительно 1,10 сП, приблизительно 1,11 сП, приблизительно 1,12 сП, приблизительно 1,13 сП, приблизительно 1,14 сП или приблизительно 1,15 сП. В конкретных вариантах осуществления, биоматериал представляет собой желатиновый раствор. Желатин присутствует приблизительно в 0,5%, приблизительно в 0,55%, приблизительно в 0,6%, приблизительно в 0,65%, приблизительно в 0,7%, приблизительно в 0,75%, приблизительно в 0,8%, приблизительно в 0,85%, приблизительно в 0,9%, приблизительно в 0,95% или приблизительно в 1% (вес/об) в растворе. В одном примере, биоматериал представляет собой 0,75%-ый (вес/об) желатиновый раствор в PBS. В конкретных вариантах осуществления, 0,75%-ый (вес/об) раствор имеет вязкость при 25°C приблизительно от 1,6 сП приблизительно до 2 сП. В конкретных вариантах осуществления, 0,75%-ый (вес/об) раствор имеет вязкость при 37°C приблизительно от 1,07 сП приблизительно до 1,08 сП. Желатиновый раствор может предоставляться в PBS, DMEM или другом подходящем растворителе.
[00125] В конкретных вариантах осуществления, состав на основе текучей среды является желатиновым. Желатин представляет собой нетоксичный, биоразлагаемый и водорастворимый белок, извлекаемый из коллагена, который представляет собой основной компонент внеклеточной матрицы (ECM) мезенхимальных тканей. Коллаген представляет собой основной структурный белок во внеклеточном пространстве в различных соединительных тканях в телах животных. В качестве основного компонента соединительной ткани, он представляет собой наиболее преобладающий белок у млекопитающих, что составляет от 25% до 35% содержания белка во всем теле. В зависимости от степени минерализации, коллагеновые ткани могут быть жесткими (кость), податливыми (сухожилие) или иметь градиент от жестких до податливых (хрящ). Коллаген, в форме продолговатых фибрилл, главным образом находится в фиброзных тканях, к примеру, в сухожилиях, связках и коже. Он также преобладает в роговицах, хряще, костях, кровеносных сосудах, пищеварительном тракте, межпозвоночных дисках и дентине в зубах. В мышечной ткани, он служит в качестве основного компонента эндомизий. Коллаген составляет один-два процента мышечной ткани и насчитывает 6% веса сильных, жилистых мышц. Коллаген возникает во многих местах во всем теле. Тем не менее, более 90% коллагена в человеческом теле имеет тип I.
[00126] К настоящему времени, 28 типов коллагена идентифицируются и описываются. Они могут разделяться на несколько групп согласно структуре, которую они формируют: Фибриллярные (тип I, II, III, v, XI). Нефибриллярные FACIT (ассоциированные с фибриллами коллагены с прерываемыми тройными спиралями) (тип IX, XII, XIV, XVI, XIX). Короткая цепочка (тип VIII, X). Базальная мембрана (тип IV). Мультиплексиновые (с несколькими областями тройных спиралей с прерываниями) (тип XV, XVIII). MACIT (ассоциированные с мембранами коллагены с прерываемыми тройными спиралями) (тип XIII, XVII). Другие (тип VI, VII). Пять наиболее распространенных типов являются следующими: Тип I: кожа, сухожилие, сосудистая лигатура, органы, кость (основной компонент органической части кости). Тип II: хрящ (основной коллагеновый компонент хряща). Тип III: ретикулярный (основной компонент ретикулярных волокон), обычно содержится вместе с типом I. Тип IV: формирует базальную пластинку, эпителиальный секретируемый слой базальной мембраны. Тип V: поверхности клеток, волосы и плацента.
[00127] Желатин сохраняет информационные сигналы, включающие в себя последовательность аргинилглициласпарагиновых кислот (RGD), которая ускоряет клеточную адгезию, пролиферацию и дифференциацию стволовых клеток. Характерное свойство желатина заключается в том, что он демонстрирует поведение в соответствии с верхней критической температурой растворения (UCST). Выше конкретного порогового значения температуры, желатин может растворяться в воде посредством формирования гибких случайных одиночных катушек. При охлаждении, возникают водородное связывание и ван-дер-ваальсовы взаимодействия, приводя к формированию тройных спиралей. Эти коллагеноподобные тройные спирали выступают в качестве зон перехода и в силу этого запускают золь-гель-переход. Желатин широко используется в фармацевтических и медицинских вариантах применения.
[00128] В конкретных вариантах осуществления, инъекционный клеточный состав на основе текучей среды основан на свином желатине, который может получаться из свиной кожи и предлагается на рынке, например, компанией Nitta Gelatin NA Inc (NC, США) либо компанией Gelita USA Inc. (IA, США). Желатин может растворяться, например, в фосфатно-буферном физиологическом растворе Дульбекко (DPBS), чтобы формировать термочувствительный гидрогель, который может загустевать и сжижаться при различных температурах. В конкретных вариантах осуществления, гидрогель, используемый для того, чтобы изготавливать состав инъекционных клеточных композиций, основан на рекомбинантном человеческом или животном желатине, экспрессированном и очищенном с использованием технологий, известных специалистам в данной области техники. В конкретных вариантах осуществления, экспрессионный вектор, содержащий всю или часть кДНК для человеческого коллагена типа I, альфа I, экспрессируется в дрожжах Pichia pastoris. Другие экспрессионные векторные системы и организмы должны быть известны для специалистов в данной области техники. В конкретных вариантах осуществления, желатиновый гидрогель настоящего раскрытия сущности представляет жидкость при и выше комнатной температуры (22-28°C) и (2-8°C) гели при охлаждении до температур охлаждения.
[00129] Специалисты в данной области техники должны принимать во внимание дополнительные признаки и преимущества изобретения на основе вышеописанных вариантов осуществления. Соответственно, изобретение не должно ограничиваться посредством того, что подробно показано и описано, за исключением того, что указывается посредством прилагаемой формулы изобретения. Все публикации и материалы, противопоставленные в данном документе, полностью содержатся в данном документе по ссылке в явном виде.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ КЛЕТОЧНЫЕ ВЕЗИКУЛЫ, И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2824136C2 |
| ИММУНОЛОГИЧЕСКИ ПРИВИЛЕГИРОВАННЫЕ БИОАКТИВНЫЕ ПОЧЕЧНЫЕ КЛЕТКИ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ПОЧЕК | 2018 |
|
RU2816753C2 |
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЯ ПОЧЕК У СУБЪЕКТОВ С АНОМАЛИЯМИ ПОЧЕК И/ИЛИ МОЧЕВЫВОДЯЩИХ ПУТЕЙ | 2020 |
|
RU2823980C2 |
| АППЛИКАТОР И СИСТЕМА ДЛЯ ЭЛЕКТРОПОРАЦИИ | 2019 |
|
RU2792194C2 |
| КОМБИНАЦИИ | 2015 |
|
RU2715236C2 |
| НОСИМОЕ УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОЙ ИНЪЕКЦИИ ДЛЯ УПРАВЛЯЕМОЙ ПОДАЧИ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2011 |
|
RU2695703C2 |
| ПОПУЛЯЦИИ КЛЕТОК ПОЧЕК И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2805243C2 |
| ПОДАВЛЕНИЕ РАКОВЫХ МЕТАСТАЗОВ | 2010 |
|
RU2571502C2 |
| ЦИСТЕАМИНДИОКСИГЕНАЗА-РЕЗИСТЕНТНЫЕ АНАЛОГИ ЦИСТЕАМИНА И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2766579C2 |
| КОМБИНАЦИИ ИНГИБИТОРА FGFR И ИНГИБИТОРА IGF1R | 2015 |
|
RU2715893C2 |
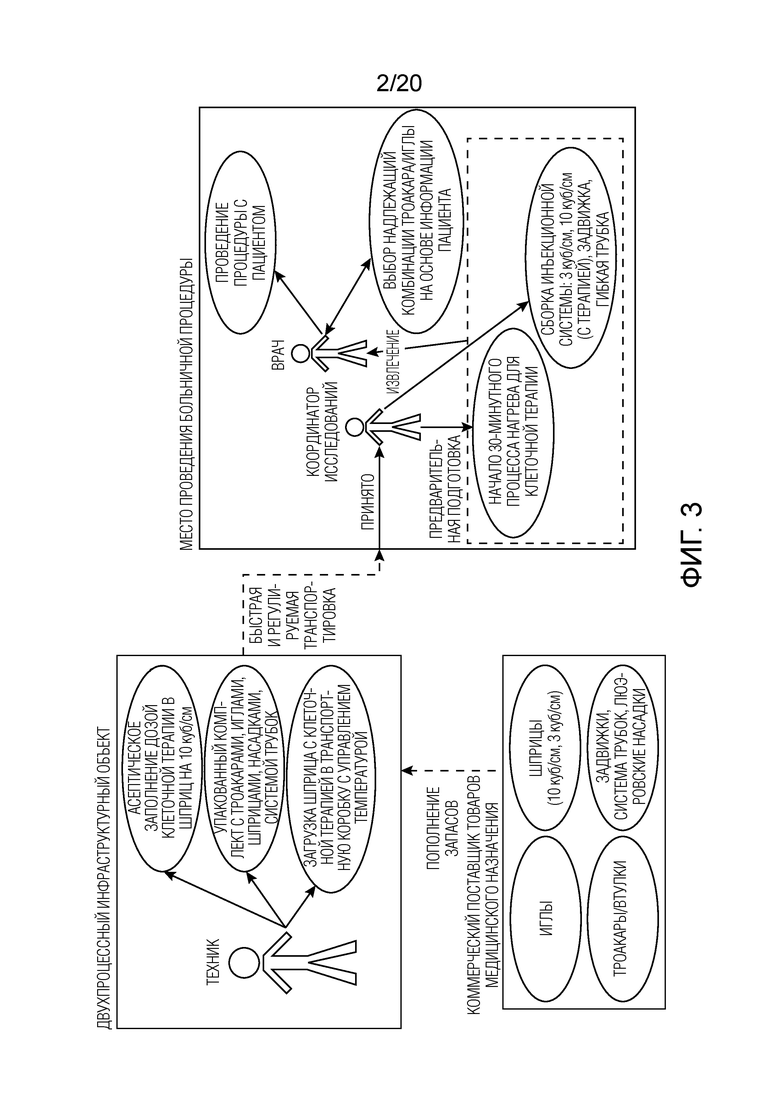
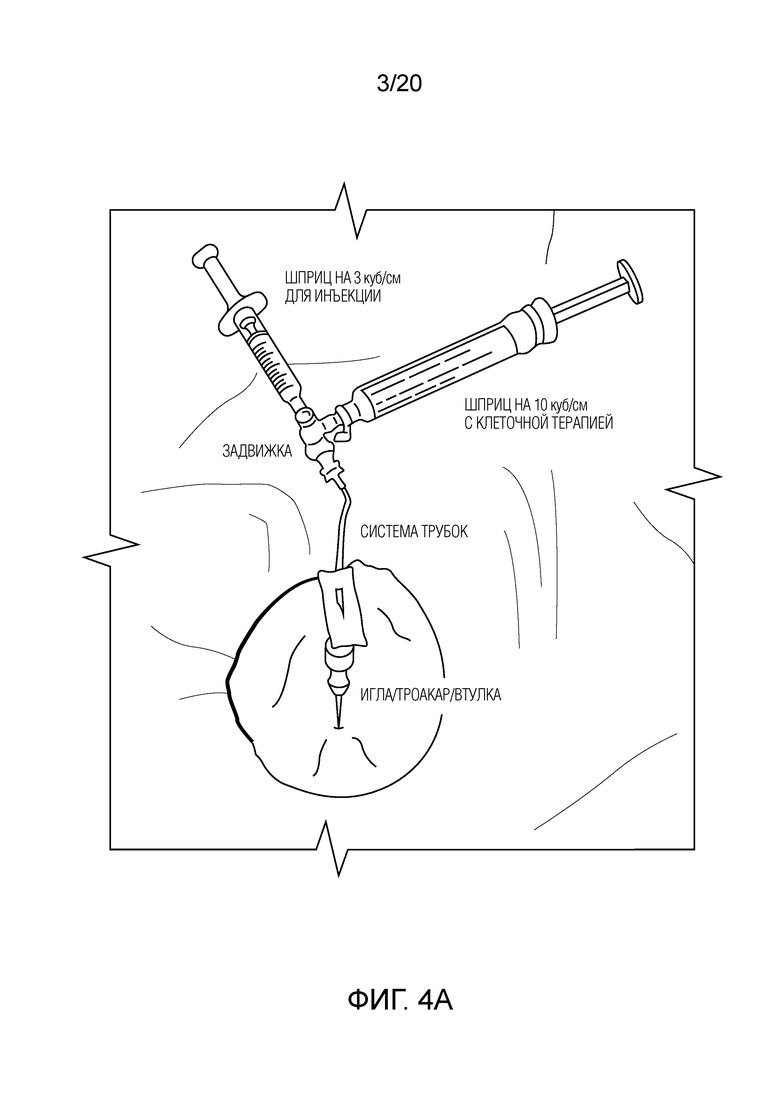
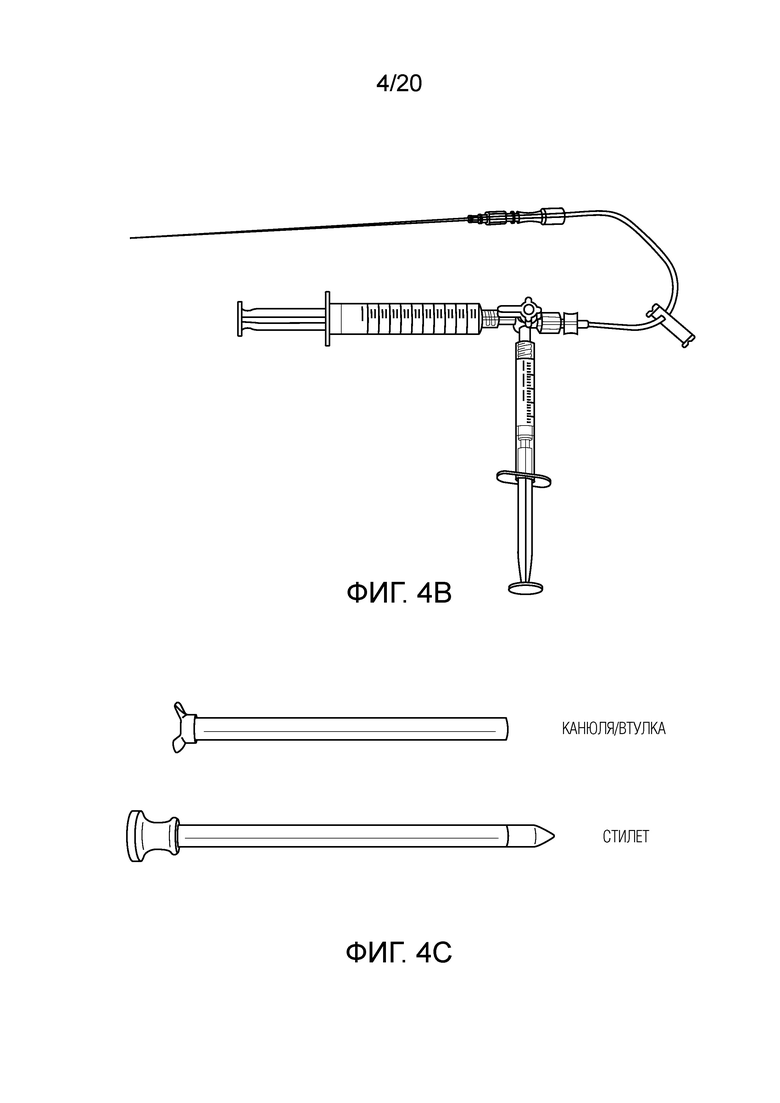
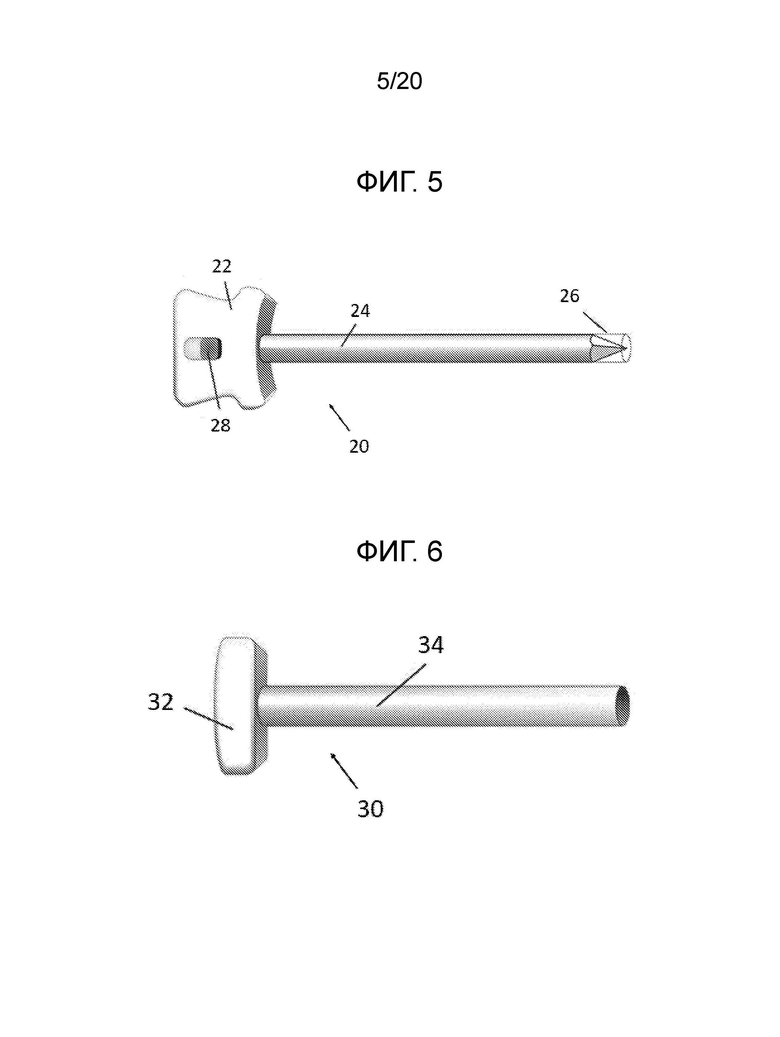
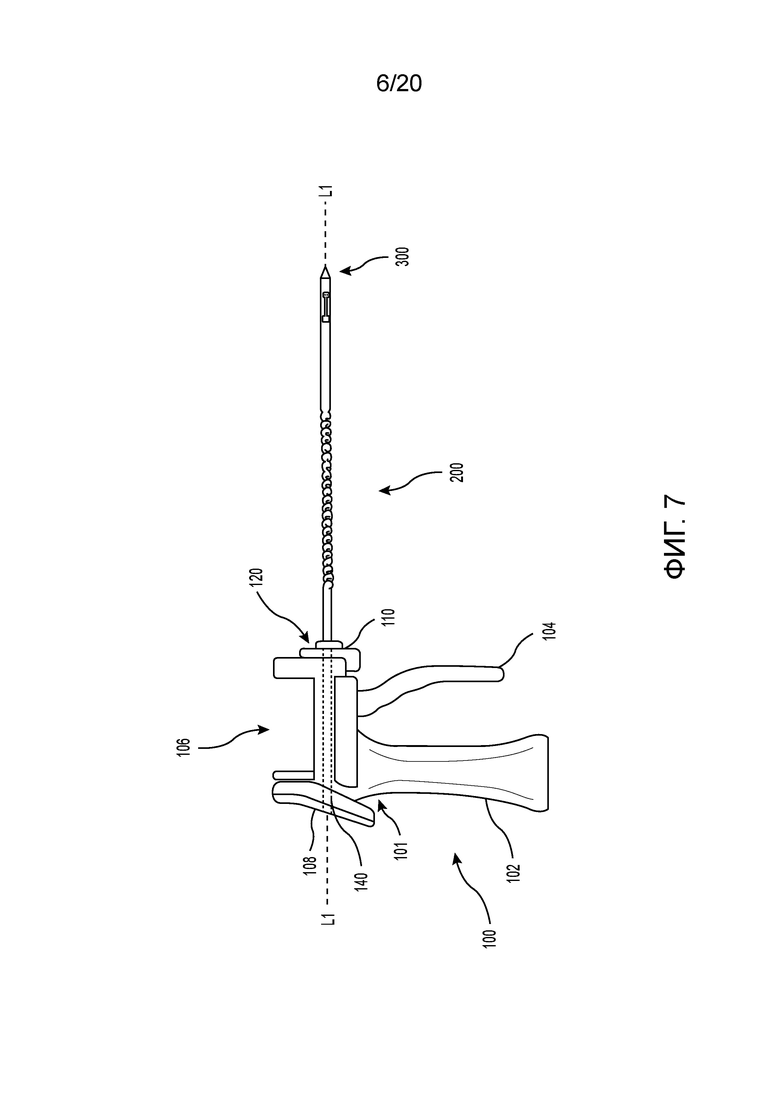
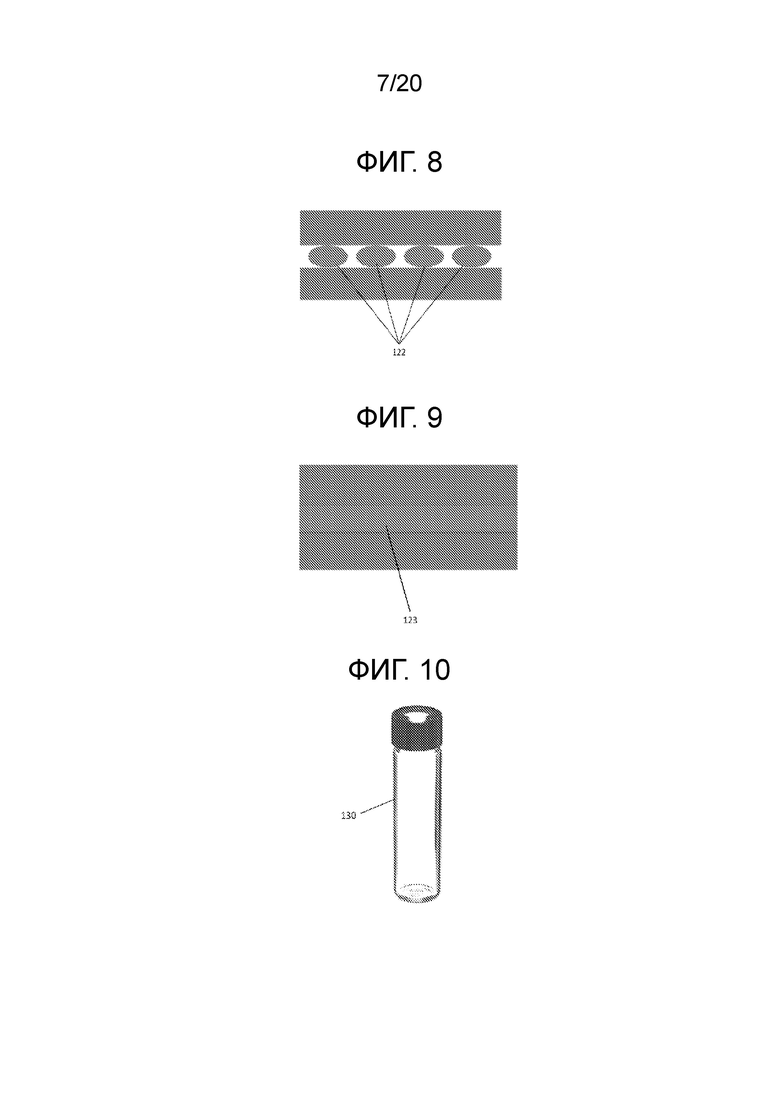
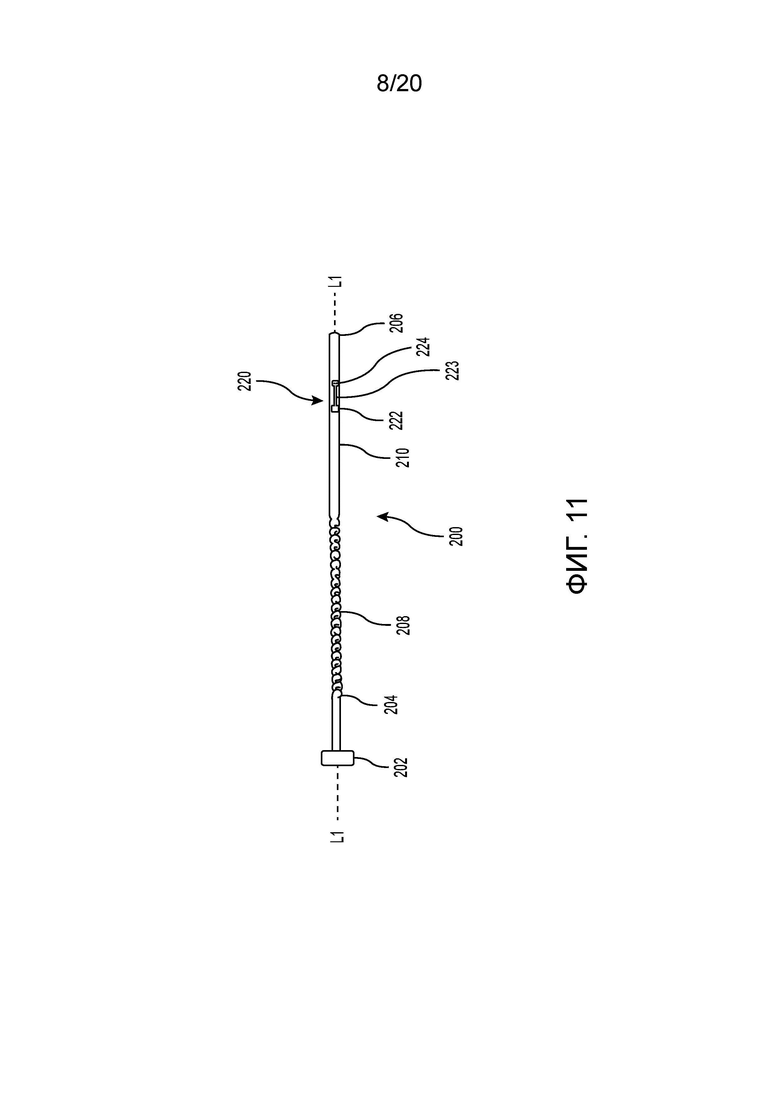
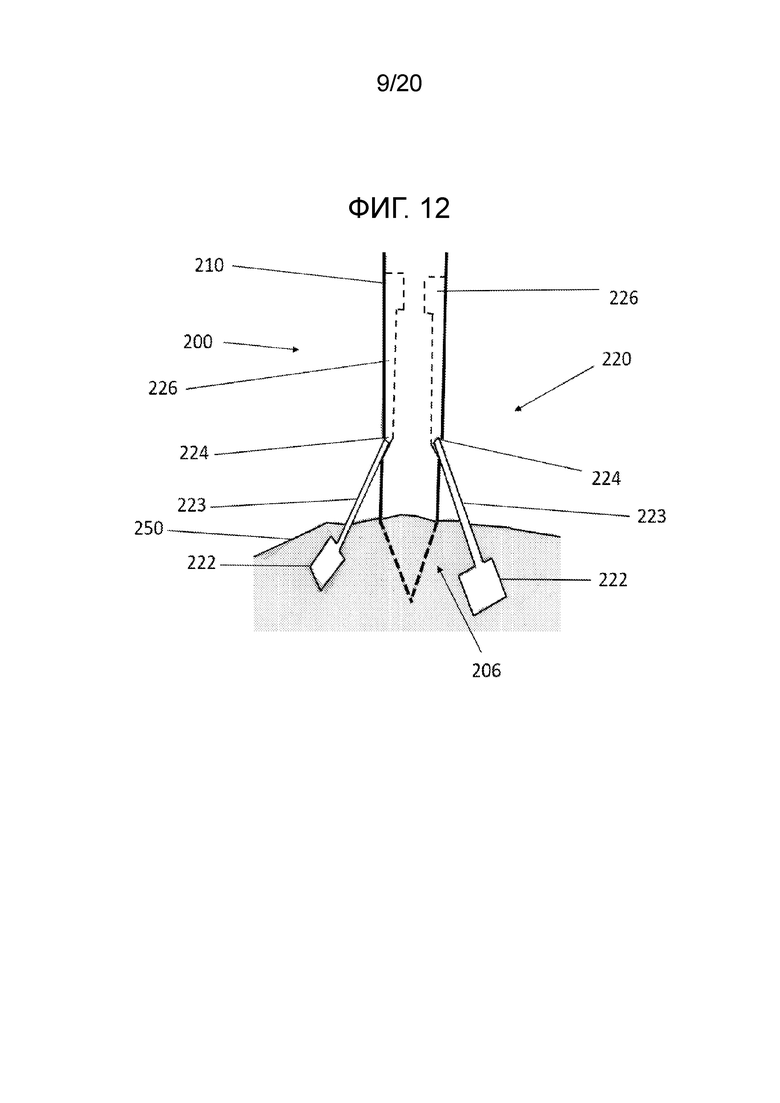
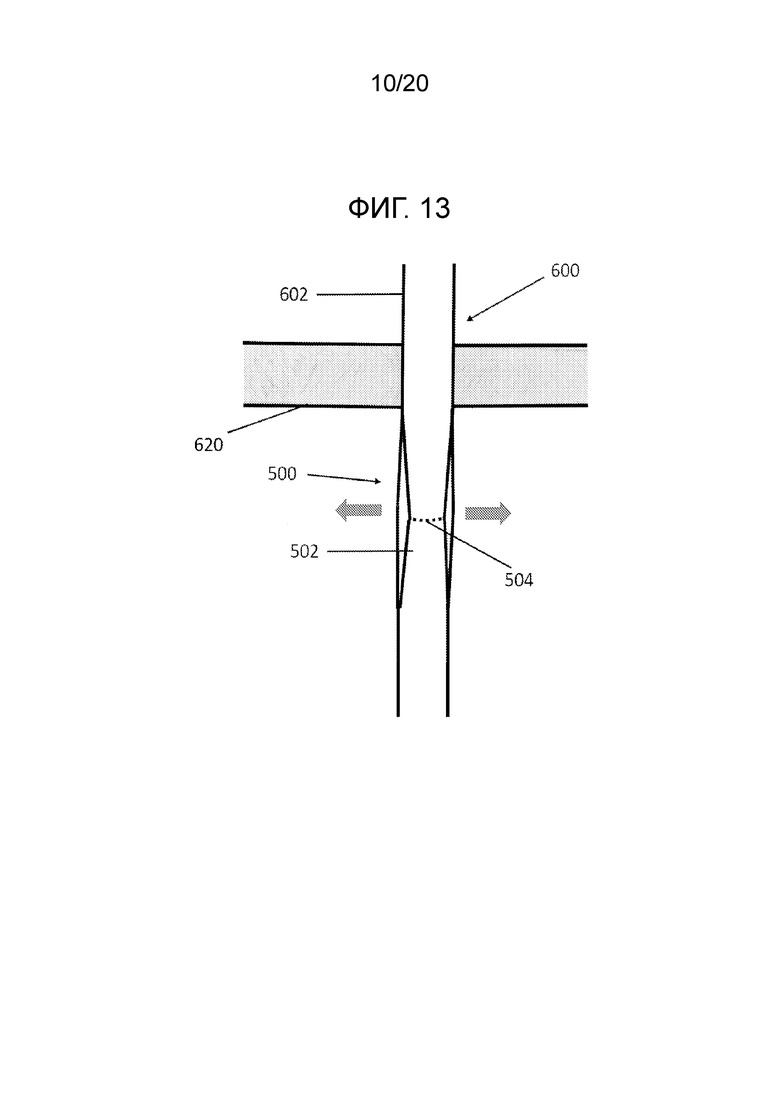
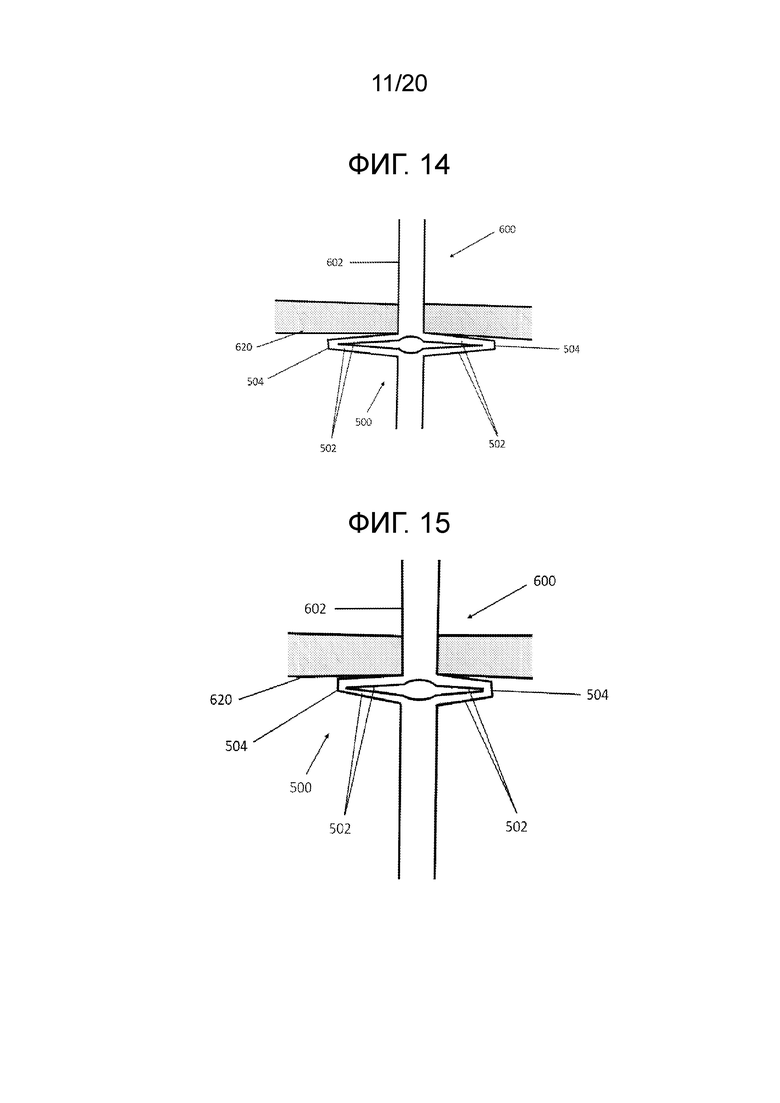
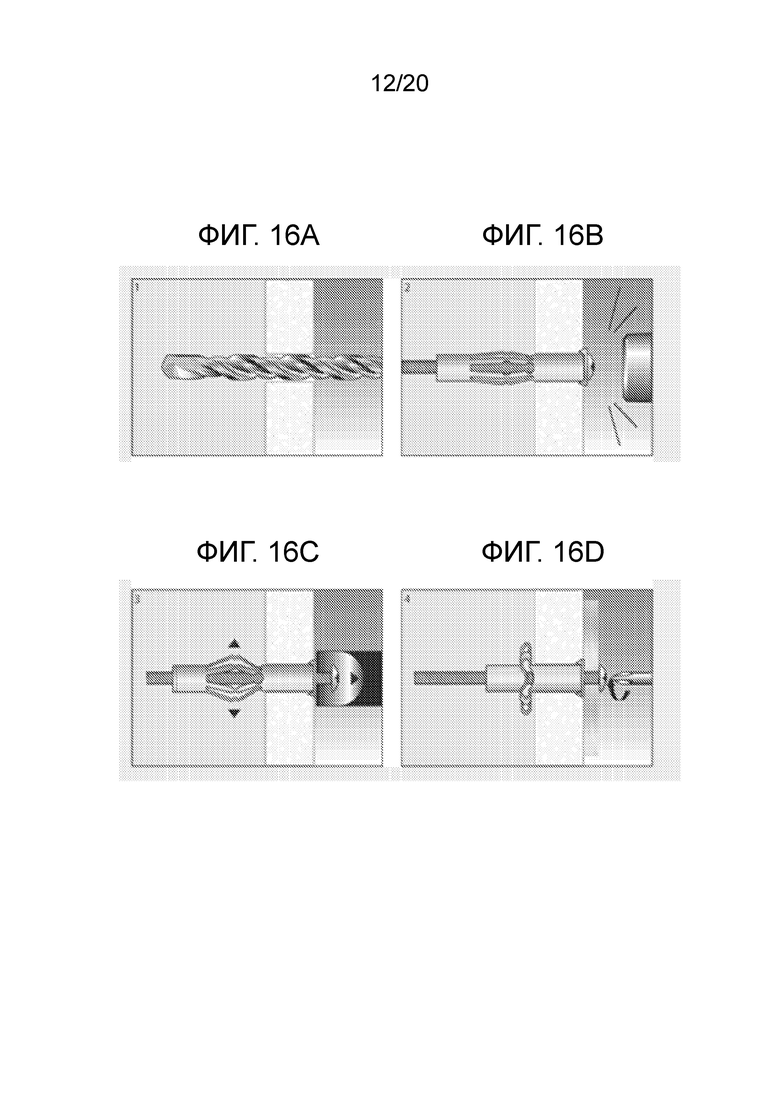
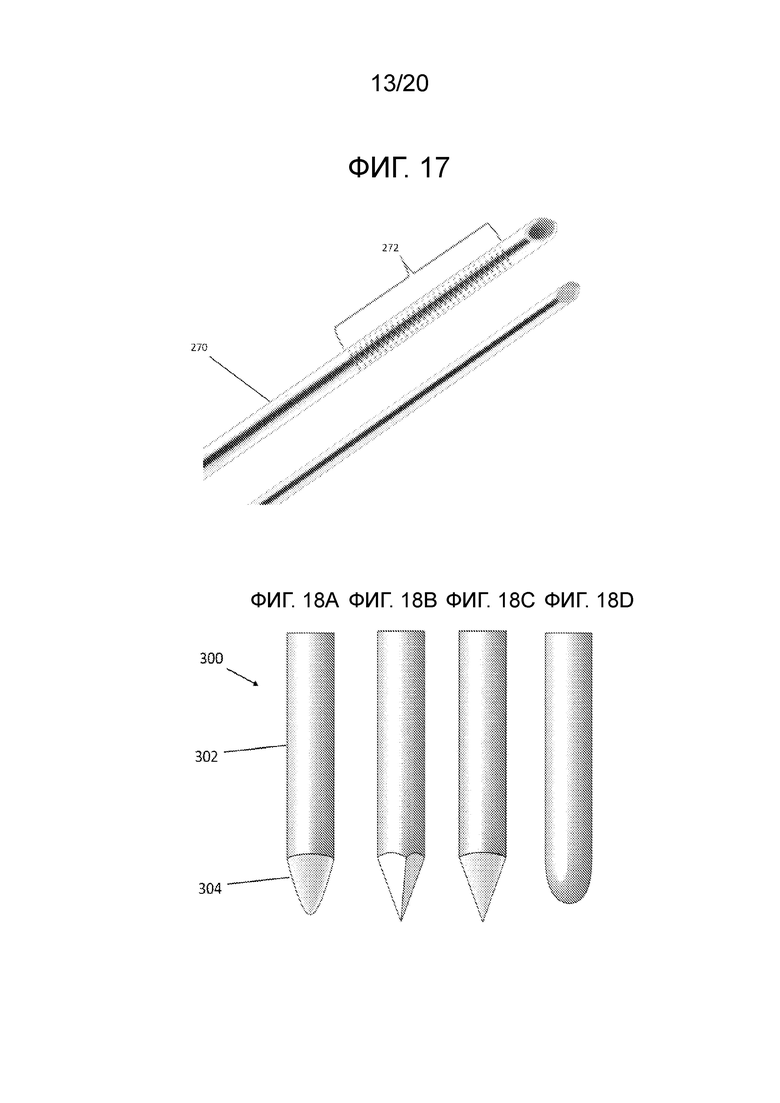
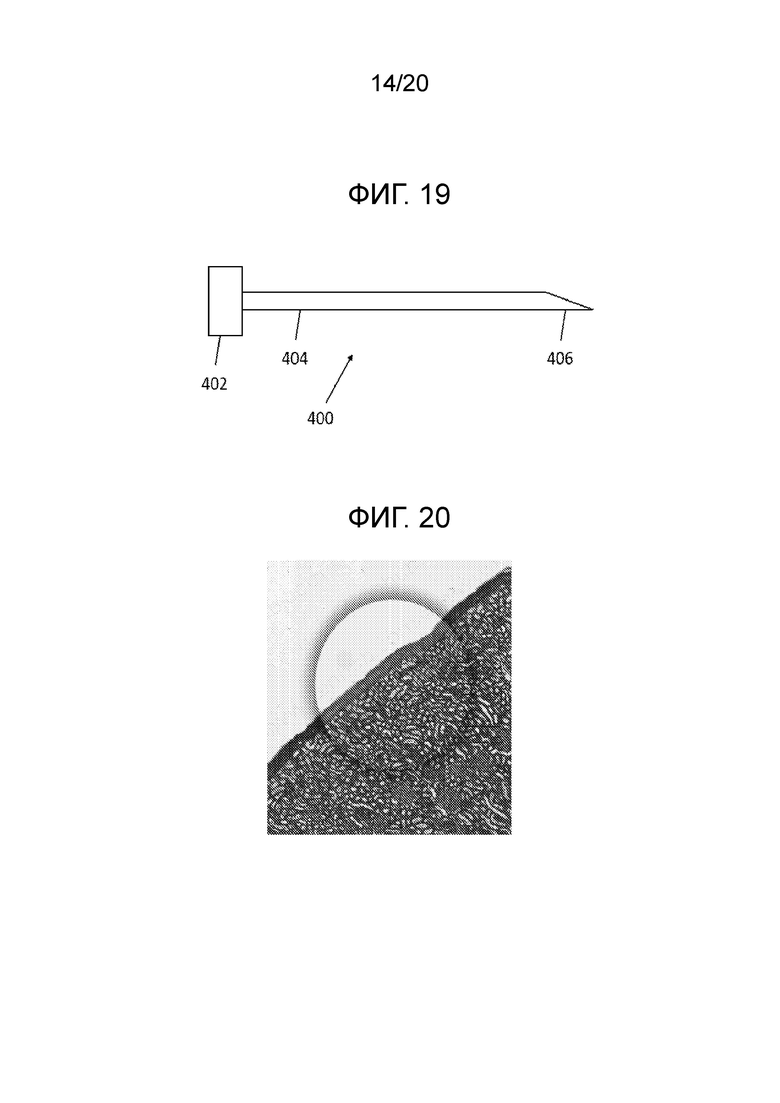
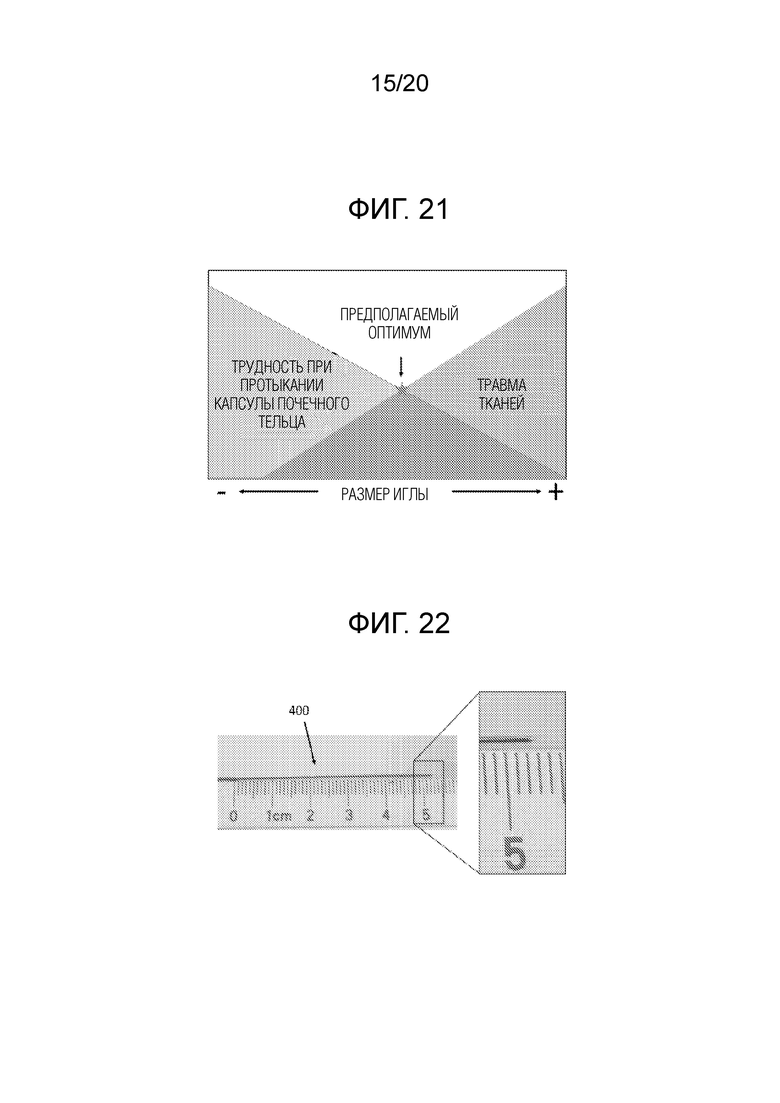
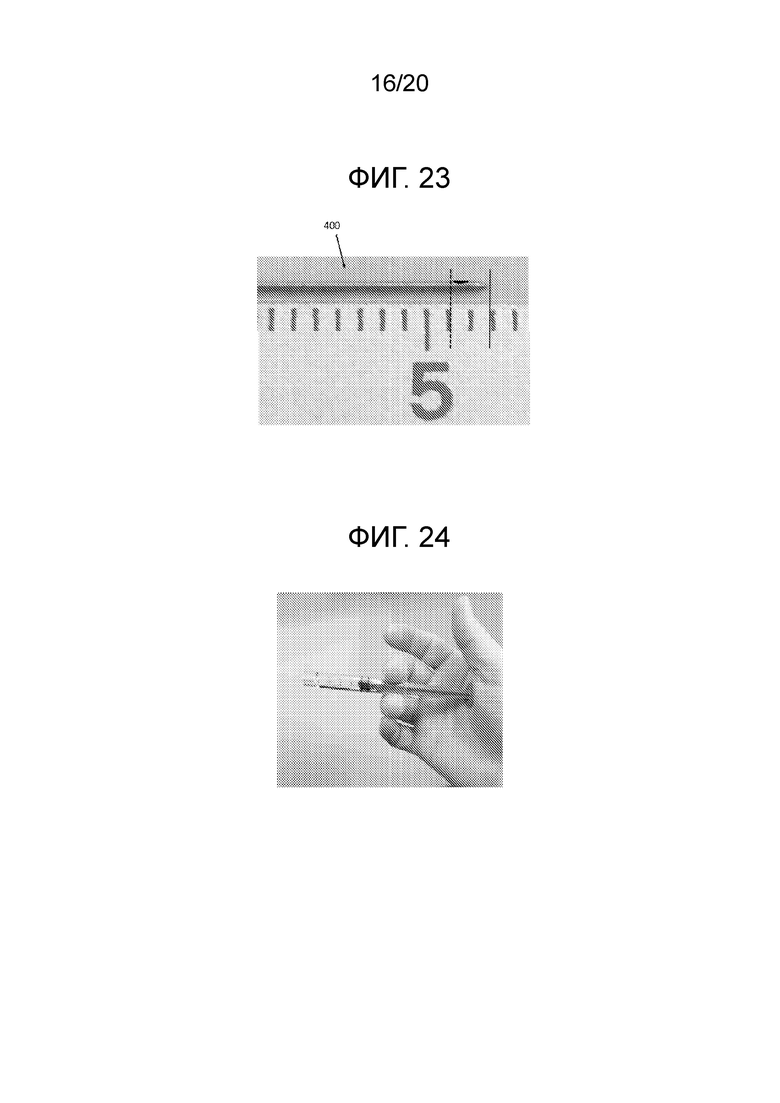
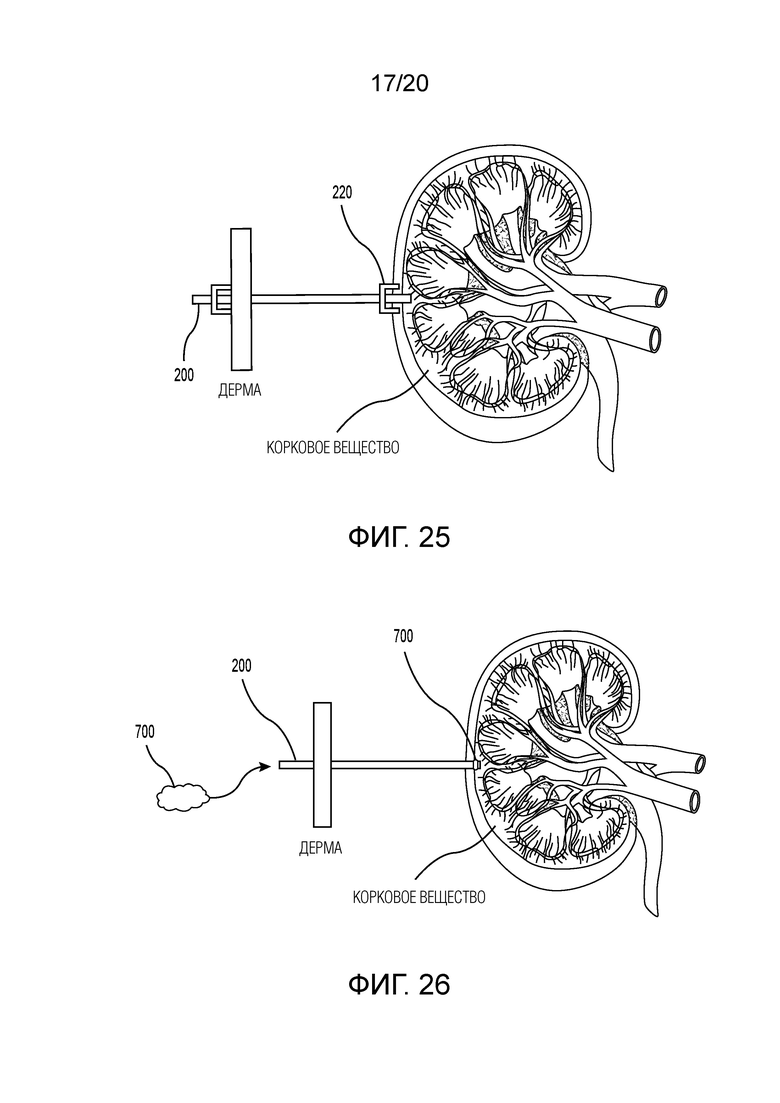
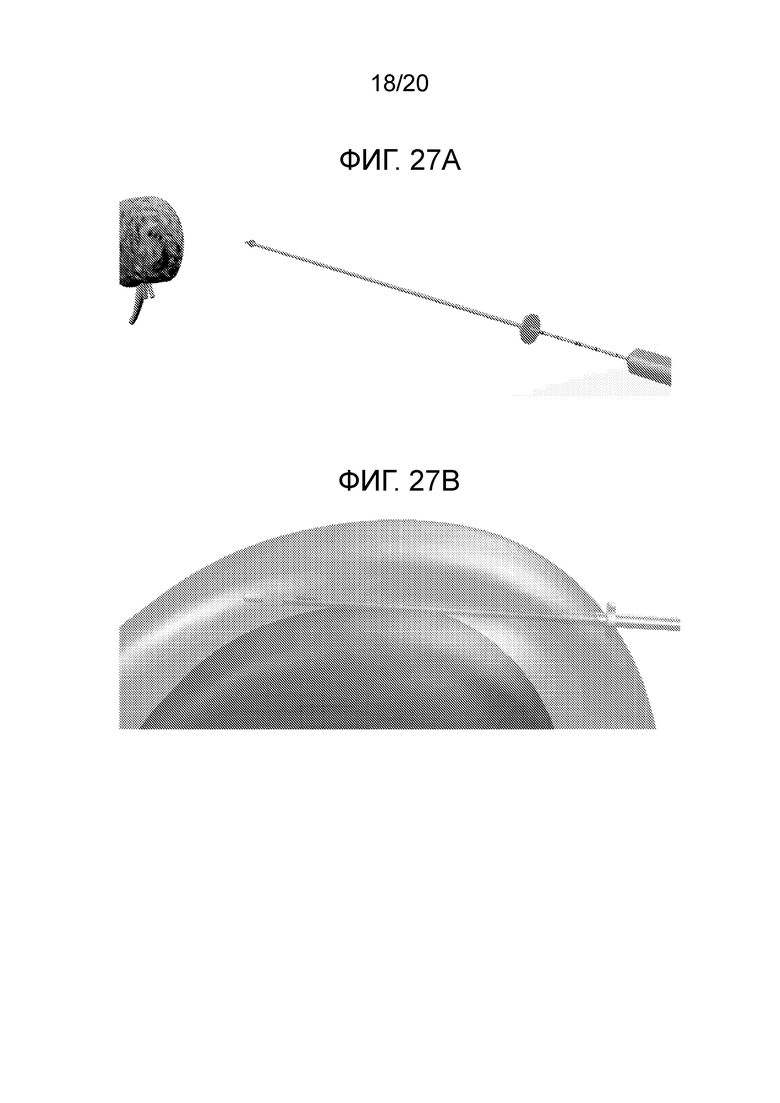
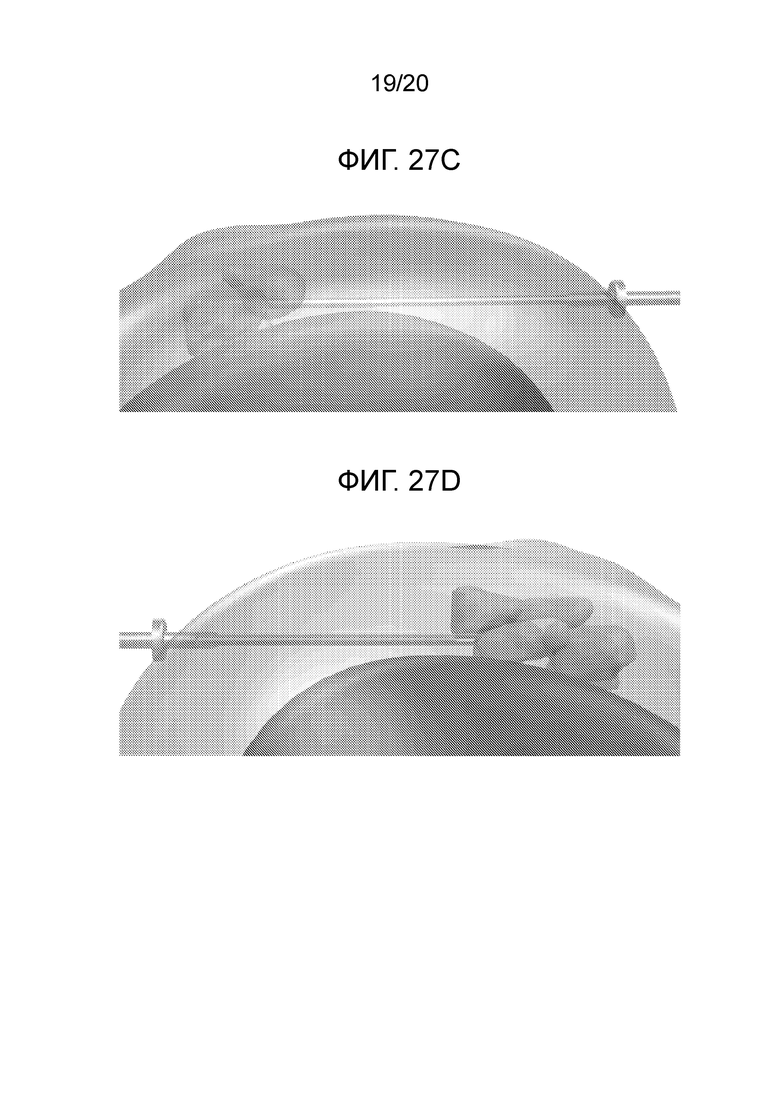
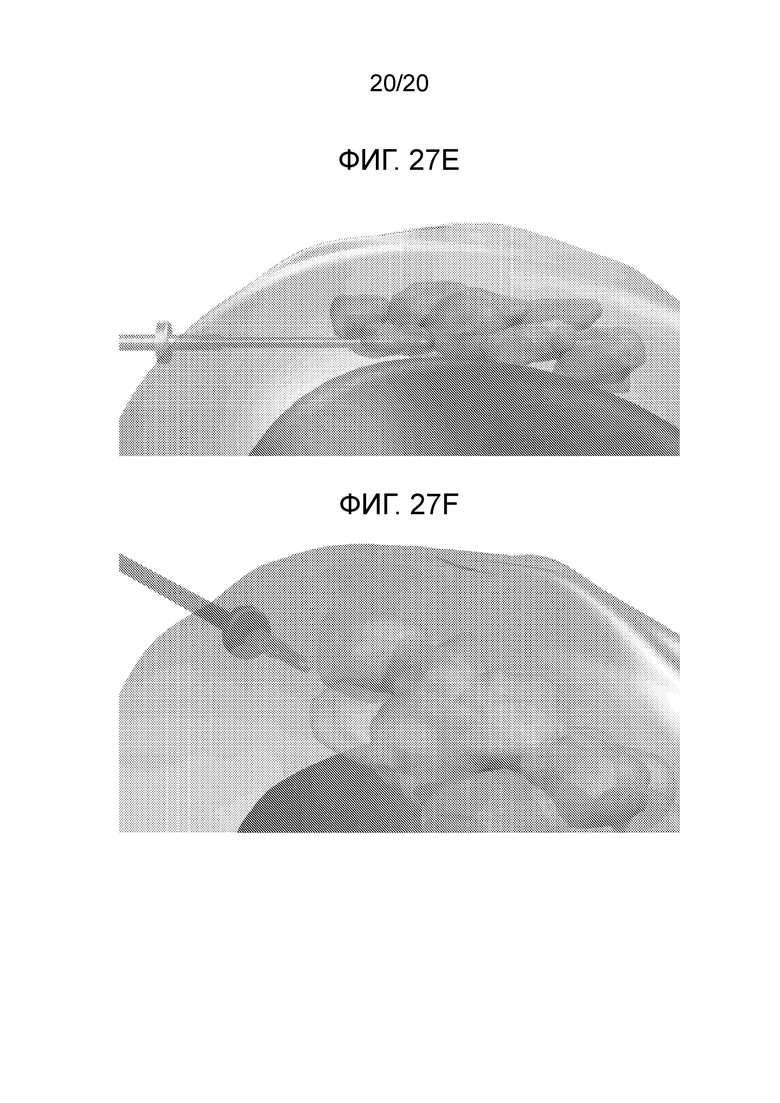
Изобретение относится к медицинской технике, а именно к устройству доставки фармацевтических составов. Устройство доставки фармацевтических составов на основе текучей среды содержит корпус, съемную инъекционную иглу и троакар. Корпус имеет актуатор, приемное устройство для текучей среды и механизм доставки текучей среды. Съемная инъекционная игла проходит дистально из корпуса. Механизм доставки текучей среды выполнен с возможностью доставлять болюсы или непрерывный поток текучей среды через инъекционную иглу. Троакар содержит удлиненный корпус, имеющий проксимальный и дистальный концы. Корпус имеет головку на его проксимальном конце, удлиненный вал, проходящий дистально из головки, и просвет, проходящий из проксимального конца к дистальному концу через него. Стабилизирующий механизм на дистальной части удлиненного вала выполнен с возможностью стабилизировать дистальный конец удлиненного корпуса относительно поверхности ткани. Стабилизирующий механизм содержит подножки и валы. Подножки расположены радиально симметрично вокруг удлиненного корпуса. Каждый вал соединен с соответствующей нижней частью подножек на первом конце и соединен с удлиненным корпусом посредством соответствующих шарнирных точек на другом конце. Подножка и вал выполнены с возможностью перемещения из утопленной позиции вдоль удлиненного корпуса в растянутую позицию, путем вращения в направлении от удлиненного корпуса посредством шарнирных точек, при использовании троакара. В растянутой позиции подножки схватывают поверхность ткани с возможностью расцепления. Использование изобретения позволяет обеспечить доставку терапевтических агентов внесосудисто в целевые местоположения внутри пациента при поддержании позиционной стабильности. 15 з.п. ф-лы, 27 ил.
1. Устройство доставки фармацевтических составов на основе текучей среды, содержащее:
- корпус, имеющий актуатор, приемное устройство для текучей среды и механизм доставки текучей среды; и
- съемную инъекционную иглу, проходящую дистально из корпуса,
- при этом механизм доставки текучей среды выполнен с возможностью доставлять болюсы или непрерывный поток текучей среды через инъекционную иглу; и
троакар, содержащий
удлиненный корпус, имеющий проксимальный и дистальный концы, причем корпус имеет головку на его проксимальном конце, удлиненный вал, проходящий дистально из головки, и просвет, проходящий из проксимального конца к дистальному концу через него; и
- стабилизирующий механизм на дистальной части удлиненного вала, выполненный с возможностью стабилизировать дистальный конец удлиненного корпуса относительно поверхности ткани, причем
стабилизирующий механизм содержит:
подножки, расположенные радиально симметрично вокруг удлиненного корпуса; и
валы, каждый из которых соединен с соответствующей нижней частью подножек на первом конце и соединен с удлиненным корпусом посредством соответствующих шарнирных точек на другом конце, причем подножка и вал выполнены с возможностью перемещения из утопленной позиции вдоль удлиненного корпуса в растянутую позицию, путем вращения в направлении от удлиненного корпуса посредством шарнирных точек, при использовании троакара, причем в растянутой позиции подножки схватывают поверхность ткани с возможностью расцепления.
2. Устройство по п. 1, в котором (а) механизм доставки текучей среды включает в себя электромеханическую систему, имеющую центральный процессор и насос; или (b) актуатор представляет собой одно из спусковой собачки, плунжера, переключателя или кнопки.
3. Устройство по п. 1, дополнительно содержащее клапан, выполненный с возможностью перемещаться в пространстве проксимально и дистально параллельно инъекционной игле во время размещения устройства и доставки текучей среды.
4. Устройство по п. 3, в котором клапан выполнен с возможностью перемещаться в пространстве на 2 см дистально и проксимально.
5. Устройство по п. 1, в котором приемное устройство для текучей среды выполнено с возможностью съемно и с возможностью замены принимать резервуар для текучей среды, и резервуар для текучей среды содержит по меньшей мере один картридж, который включает в себя дозировку текучей среды.
6. Устройство по п. 5, в котором приемное устройство для текучей среды выполнено с возможностью принимать картриджи параллельно.
7. Устройство по п. 1, в котором текучая среда включает в себя терапевтические клетки либо их продукты для лечения заболевания почек.
8. Устройство по п. 1, дополнительно содержащее сенсорный дисплей, выполненный с возможностью управлять работой устройства.
9. Устройство по п. 8, в котором дисплей выполнен с возможностью задавать один или более параметров для доставки текучей среды, включающих в себя по меньшей мере одно из давления и объема.
10. Устройство по п. 8, в котором дисплей выполнен с возможностью предоставлять информацию раздачи в реальном времени текучей среды во время доставки.
11. Устройство по п. 1, дополнительно содержащее зацепляющий элемент на дистальном конце корпуса, выполненный с возможностью съемно зацеплять троакар.
12. Устройство по п. 1, в котором подножки имеют микрокрючки на них.
13. Устройство по п. 1, в котором подножки включают по меньшей мере одно из адгезива, присоски и зажима.
14. Устройство по п. 1, дополнительно содержащее съемный стилет, выполненный с возможностью прохождения через просвет удлиненного корпуса, причем стилет выполнен с возможностью приводить в действие стабилизирующий механизм при вынимании.
15. Устройство по п. 1, в котором по меньшей мере часть удлиненного вала выполнена с возможностью перемещаться в пространстве дистально и проксимально параллельно продольной оси удлиненного вала.
16. Устройство по п. 15, в котором по меньшей мере часть удлиненного вала выполнена с возможностью перемещаться в пространстве на 2 см дистально и проксимально.
| US 2015224260 A1, 13.08.2015 | |||
| ГОРЕЛКА ДЛЯ УГОЛЬНОЙ ПЫЛИ | 1925 |
|
SU6694A1 |
| US 2015223977 A1, 13.08.2015 | |||
| US 2019030329 A1, 31.01.2019 | |||
| WO 2010129747 A1, 11.11.2010 | |||
| US 5817062 A, 06.10.1998 | |||
| US 2015342635 A1, 03.12.2015. | |||
Авторы
Даты
2025-04-28—Публикация
2021-04-21—Подача