Изобретение относится к экспериментальной медицине, а именно, к акушерству и гинекологии и может быть использовано при лечении эндометриоза.
Эндометриоз относится к группе социально-значимых заболеваний, затрагивая 10-15% женщин репродуктивного возраста по всему миру и являясь причиной от 30% до 70% случаев хронической боли в тазовой области и/или бесплодия [Wang Y, Nicholes К, Shih I-M The Origin and Pathogenesis of Endometriosis / Annu. Rev. Pathol. Mech. Dis. 2020.15:71-95; Ellis K. et al Endometriosis Is Undervalued: A Call to Action / Frontiers in Global Women's Health, 2022, V. 3, 902371]. Несмотря на применение различных стратегий лечения, включающих лекарственные препараты, физиотерапию и хирургическое вмешательство [Smolarz В. et al Endometriosis: Epidemiology, Classification, Pathogenesis, Treatment and Genetics (Review of Literature) / Int. J. Mol. Sci. 2021, 22, 10554], частота рецидивов заболеваний крайне высока [Леваков С.А., Громова Т.А. Прогнозирование рецидива эндометриоза яичников и его неопластической трансформации / Российский вестник акушера-гинеколога. 2019; 19(4): 17-21].
Последний аспект говорит о существующем сегодня недостаточном уровне понимания патогенеза эндометриоза. Недавние исследования показывают значительную роль митохондриальной дисфункции в развитии данного заболевания [Atkins H.M.et al Endometrium and endometriosis tissue mitochondrial energy metabolism in a nonhuman primate model / Reproductive Biology and Endocrinology, 2019, 17: 70; Chen C. et al Mitochondria and oxidative stress in ovarian endometriosis / Free Radical Biology and Medicine, 2019, 136, 22-34; Chou C.-H. et al Mitochondrial Dysfunction Induced by High Estradiol Concentrations in Endometrial Epithelial Cells / J Clin Endocrinol Metab, 2020, 105(1), 126-135; Hsu, A.H. et al Endometriosis may be associated with mitochondrial dysfunction in cumulus cells from subjects undergoing in vitro fertilization-intracytoplasmic sperm injection, as reflected by decreased adenosine triphosphate production / Fertility and Sterility, 2015, 103(2), 347-352]. Однако при этом отмечается отсутствие представления о механизмах ее возникновения. Указывается, что в патологичных клетках в значительной степени снижено содержание АТФ за счет нарушений окислительного фосфорилирования, что может быть связано с ассоциированным с гиперпродукцией АФК повреждением митохондриальной ДНК или мембранных структур, с изменениями клеточного метаболизма, недостатком митохондриальных субстратов. Однако механизм такой связи требует детального изучения, что позволит в дальнейшем выстроить эффективную стратегию лечения.
В исследованиях in vitro на первичных клеточных культурах показано, что в патологичных клетках, полученных от пациенток с подтвержденным эндометриозом, значительное увеличение производства АФК и обусловленное им развитие окислительного стресса связано не с утечкой электронов из электронтранспортной цепи (ЭТЦ) митохондрий, а с высоким уровнем активности и/или гиперэкспрессией ферментов семейства НАДФН-оксидаз. При этом нормализации функции митохондрий способствует обработка клеток ингибиторами данных ферментов [Погонялова М.Ю. и др. Механизм развития митохондриальной дисфункции в клетках пациентов с диагнозом "эндометриоз" // Сборник тезисов XXXV Зимней молодежной научной школы "перспективные направления физико-химической биологии и биотехнологии" - Москва, 7-10 февраля 2023 г. - С. 222].
С другой стороны, имеются данные о том, что восстановление нарушений в работе митохондрий патологичных клеток происходит также в присутствии высоких концентраций пирувата натрия [Погонялова М.Ю. и др. Восстановление функции митохондрий в клетках пациентов с диагнозом «эндометриоз» // Сборник тезисов 25-ой Пущинской школы-конференции молодых ученых с международным участием «Биология - наука XXI века». Пущино: ФИЦ ПНЦБИ РАН, 2022. - 379 с]. В результате окислительного декарбоксилирования последнего в митохондриях происходит восстановление никотинамидадениндинуклеотида (НАД) с образованием НАДН, который является субстратом комплекса I - важнейшего участника ЭТЦ, обеспечивающего как перенос электронов, так и формирование необходимого уровня митохондриального мембранного потенциала (ΔΨm). Выявленное положительное влияние пирувата на состояние патологичных клеток говорит о том, что вызываемые гиперпродукцией АФК нарушения в работе митохондрий связаны с возникающим значительным дефицитом митохондриальных субстратов, в частности НАДН, что может быть следствием их потребления в ходе реализации других процессов.
К основным потребляющим НАДН внутриклеточным процессам можно отнести функционирование ферментов семейства поли(АДФ-рибоза)-полимераз (PARP), активация которых существенно связана с репарацией повреждений как ядерной, так и митохондриальной ДНК, возникающих, в частности, при высокой продукции АФК в клетках. При этом в результате работы PARP происходит образование никотинамида (НАМ), что может привести к значительному снижению внутриклеточного содержания НАД. Причем вне зависимости от того, где происходит развитие связанной с PARP репарации повреждений ДНК, этот процесс может оказать существенное влияние на функции митохондрий, поскольку они не имеют собственной полноценной системы обратного перевода НАМ в НАД и зависят от образования прекурсоров НАД, в частности, никотинамидмононуклеотида, в цитозоле [Hurtado-Bages S. et al The taming of PARP 1 and its impact on NADH metabolism / Molecular Metabolism, 2020,38,100950]. Это объясняет тот факт, что потребление НАД ферментами семейства PARP может оказывать значительное влияние на клеточный, в частности, митохондриальный метаболизм [Murata М.М. et al NAD+ consumption by PARP1 in response to DNA damage triggers metabolic shift critical for damaged cell survival / Molecular Biology of the Cell, 2019, 30, 2584-2597], а применение ингибиторов PARP может выступать эффективным инструментом зашиты митохондрий [Gailyas Jr.F., Sumegi В. Mitochondrial Protection by PARP Inhibition / Int. J. Mol. Sci. 2020, 21, 2767].
Необходимо отметить, что изменение уровня экспрессии и активности PARP показано в развитии ряда процессов, протекающих в женской репродуктивной системе. В частности, повышенные концентрации PARP обнаружены в плазме крови женщин с бесплодием [Kacperczyk-Bartnik J. et al Plasma and Peritoneal Poly (ADP-Ribose) Polymerase Levels in Patients with Endometriosis / Biomedicines 2022, 10, 2451]. Помимо этого ферменты семейства PARP играет значительную роль в развитии дуцидуализации и имплантации эмбриона в матку [Kelleher A.M. Deficiency of PARP-1 and PARP-2 in the mouse uterus results in decidualization failure and pregnancy loss / PNAS 2021 Vol.118 No. 40 e2109252118; Soni U. K. et al Poly(ADP-ribose) polymerase-2 is essential for endometrial receptivity and blastocyst implantation, and regulated by caspase-8 / Molecular and Cellular Endocrinology 518 (2020) 110946; Joshi A. et al PARPl during embryo implantation and its upregulation by oestradiol in mice / Reproduction (2014) 147 765-780]. Увеличение экспрессии PARP и применение ингибиторов данных ферментов для терапии показано в случае ряда злокачественных патологий, таких как, например, рак эндометрия или рак яичников [Lawrence L.M. et al Expression of poly-ADP-ribose polymerase (PARP) in endometrial adenocarcinoma: Prognostic potential / Pathology - Research and Practice 216 (2020) 152965; Musacchio L. et al PARP Inhibitors in Endometrial Cancer: Current Status and Perspectives / Cancer Management and Research 2020:12]. С учетом того, что эндометриоз характеризуется рядом признаков рака (клеточная инвазия, неконтролируемый рост, стимуляция неоангиогенеза, резистенция к апоптозу, хронический воспалительный процесс, способность к метастазированию) [Пучков К.В. и др. Эндометриоз-ассоциированные злокачественные опухоли, связанные с глубоким инфильтративным эндометриозом: обзор литературы и клинические наблюдения / Российский вестник акушера-гинеколога, 2019, Т. 19, №4], который к тому же относится к списку развивающихся при эндометриозе осложнений [Dawson A. et al Endometriosis and endometriosis-associated cancers: new insights into the molecular mechanisms of ovarian cancer development / ecancer 2018, 12:803], фармакологическая регуляция работы PARP может быть использована в качестве инструмента для лечения данной патологии. Однако анализ доступной научной литературы, а также баз данных патентов показал отсутствие разработки такого рода решений.
Наиболее близкие к предлагаемому способу подходы предполагают применение антиоксидантов или регулирующих клеточный ответ на окислительный стресс соединений [Патент РФ №2549433, МПК А61К З1/198, А61Р 15/00, публ. 2015 г.; Патент РФ №2605287, МПК А61КЗ 1/095,198,4045, А61К 8/23,44,49. А61Р 17/00,31/00,35/00, публ. 2016 г.; Патент Канады №2811456, МПК А61К 31/565,57,585; А61Р 15/00, публ. 2015 г.; Патент США №9707239, МПК А61К 31/426,427,428,4709,56; А61К 38/43; C12Q 1/68, публ. 2017 г. ]. Однако механизм их действия опосредован нейтрализацией избыточной продукции АФК, приводящей к возможному повреждению ДНК и активации PARP, и не учитывает возможность конститутивной активации PARP, характерной для многих неопластических процессов. При таком подходе возможно облегчение течения патологического процесса с последующим развитием рецидива после отмены приема препаратов.
Технической задачей настоящего изобретения является разработка основы для нового класса лекарственных препаратов для лечения эндометриоза, действие которых основано на адресном подавлении развития внутриклеточных процессов, приводящих к пролиферации патологичных клеток вне полости матки.
Техническая задача достигается применением ингибиторов ферментов семейства PARP в качестве лекарственного средства для нормализации метаболизма клеток репродуктивной системы женщин при лечении эндометриоза.
Технический результат заключается в нормализации функции митохондрий патологичных клеток, участвующих в развитии эндометриоза.
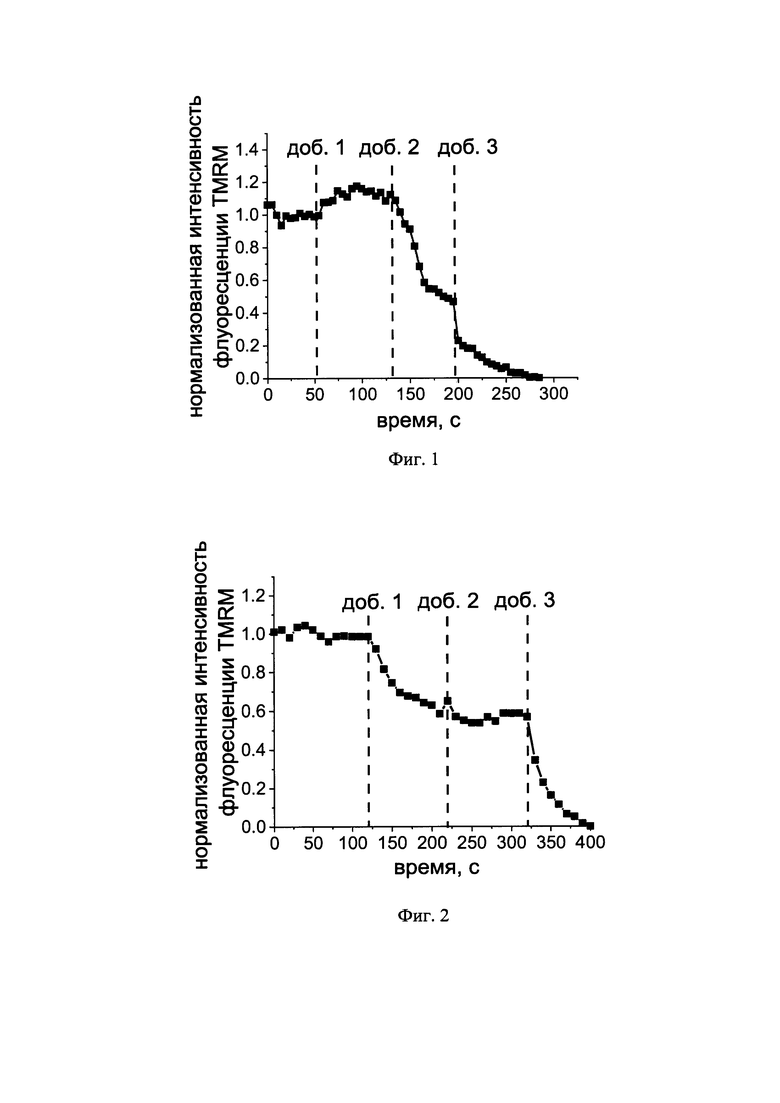
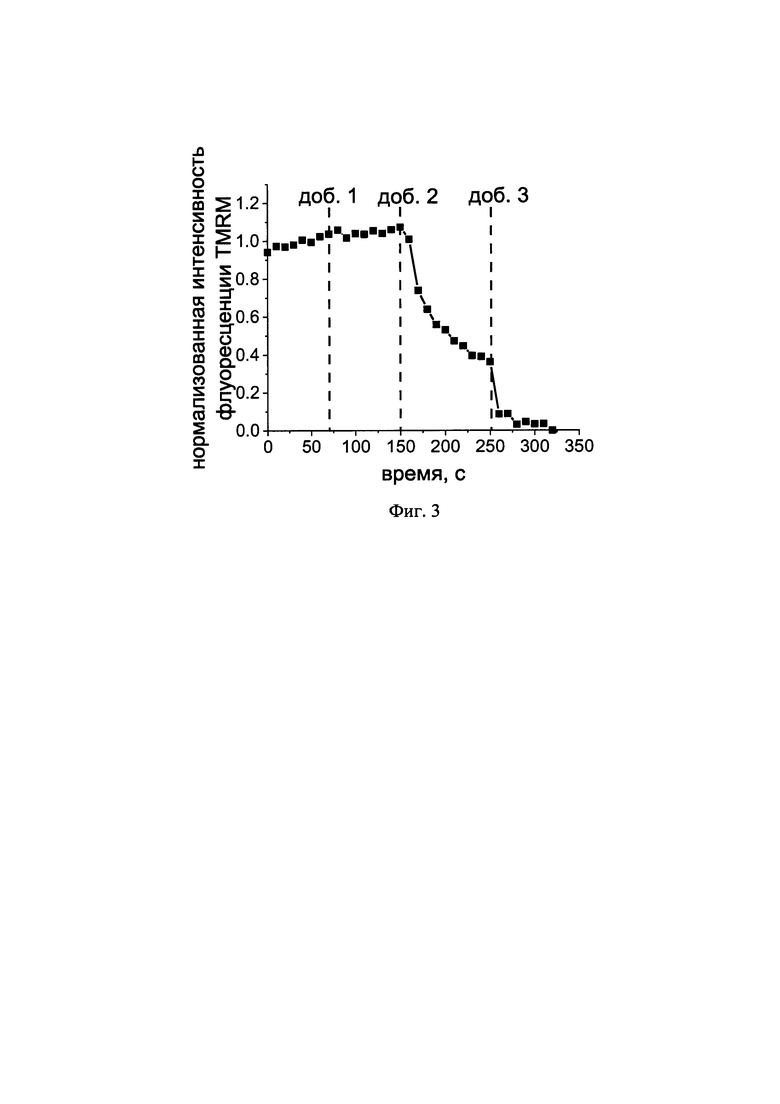
На фиг. 1 представлен график зависимости нормализованной интенсивности флуоресценции TMRM от продолжительности эксперимента для клеток контроля; на фиг. 2 - график зависимости нормализованной интенсивности флуоресценции TMRM от продолжительности эксперимента для клеток эндометриомы без обработки; на фиг. 3 - график зависимости нормализованной интенсивности флуоресценции TMRM от продолжительности эксперимента для клеток эндометриомы после обработки №-АВ в течение 0,5 ч. Обозначения «доб. 1», «доб. 2» и «доб. 3» на графиках соответствуют моментам внесения олигомицина А, ротенона и митохондриального разобщителя FCCP соответственно.
Изобретение осуществляется следующим образом.
Пример 1. Применение ингибитора PARP 3-аминобензамида (3-АВ).
Образец патологичной ткани (биоптат эндометриомы) отобран у пациентки с диагнозом «эндометриоз яичников». Для выделения клеток использовали ферментативную обработку. Для этого образец ткани поместили в 0,2%-ный раствор трипсина в среде RPMI-1640 и выдержали в течение 16 часов при температуре 0-4°С.Затем ткань трижды отмыли от фермента средой DMEM и инкубировали в 0,2%-ном растворе коллагеназы при температуре 37°С с последующей трехкратной отмывкой средой DMEM и механическим диспергированием. Клетки культивировали в ростовой среде на основе DMEM, содержащей 10% фетальной бычьей сыворотки, 1 мМ пирувата натрия, 2 мМ L-аланил-L-глутамина, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина. После достижения 80%-ного уровня конфлюэнтности клетки были разделены на две группы. Первую группу клеток далее культивировали без дополнительного воздействия, вторую - при добавлении ингибитора PARP 3-АВ до рабочей концентрации 0,5 мкМ. Время культивирования обеих групп составило 0,5 ч. После этого клетки отмыли от ростовой среды с помощью сбалансированного солевого раствора Хэнкса, выдержали в течение 45 минут при 37°С в 25 нМ растворе тетраметилродамина (TMRM) в сбалансированном солевом растворе Хенкса и исследовали методом конфокальной лазерной сканирующей микроскопии (длина волны возбуждения флуоресценции - 561 нм, интервал длин волн детекции флуоресценции - 570-700 нм) с получением временной серии изображений с последовательным добавлением ингибиторов Fl-F0-АТФ-синтазы олигомицина (2 мкг/мл) (доб. 1 на графиках), комплекса I дыхательной цепи митохондрий ротенона (2 мкМ) (доб. 2 на графиках) и митохондриального разобщителя FCCP (2 мкМ) (доб. 3 на графиках). В качестве контроля использовали клетки аспирата полости матки, полученного у условно-здоровых добровольцев, которые выделили и культивировали аналогично указанной выше процедуре без внесения 3-АВ.
Сравнение полученных экспериментальных данных для клеток контрольного образца и клеток из ткани эндометриомы свидетельствует о том, что в патологичных клетках наблюдается нарушение функции митохондрий. Клетки условно-здоровых добровольцев характеризуются нормальным механизмом поддержания митохондриального мембранного потенциала, что подтверждается небольшим увеличением интенсивности флуоресценции TMRM после внесения олигомицина А, свидетельствующем о гиперполяризации митохондрий после блокирования комплекса V электронтранспортной цепи митохондрий (фиг. 1), После обработки ротеноном происходит существенное снижение сигнала, что свидетельствует о деполяризации митохондрий вследствие ингибирования нормально функционирующего комплекса I дыхательной цепи митохондрий. В случае клеток эндометриомы после внесения олигомицина А наблюдается аномальное снижение интенсивности флуоресценции TMRM, что является признаком функционирования комплекса V в инверсном режиме, при котором происходит транспорт протонов водорода в межмембранное пространство митохондрий за счет энергии АТФ. Последующее воздействие ротенона не привело к значительному изменению сигнала вследствие дисфункции комплекса I электронтранспортной цепи (фиг. 2). Инкубирование патологичных клеток в присутствии 3-АВ, который является ингибитором ферментов из семейства PARP, приводит к нормализация функции митохондрий. В ходе эксперимента введение олигомицина А либо не вызывает изменения интенсивности флуоресценции TMRM и, соответственно, величины митохондриального мембранного потенциала, либо вызывает небольшую гиперполяризацию митохондрий, а происходящее снижение потенциала в ответ на внесение ротенона говорит о нормальном функционировании комплекса I электронтранспортной цепи (фиг. 3).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА | 2022 |
|
RU2818816C1 |
| СПОСОБ СОЗДАНИЯ КЛЕТОЧНОЙ МОДЕЛИ ПРЕЖДЕВРЕМЕННОЙ НЕДОСТАТОЧНОСТИ ЯИЧНИКОВ НА КРЫСАХ ЛИНИИ WISTAR | 2023 |
|
RU2815539C1 |
| СПОСОБ ДИАГНОСТИКИ НАСЛЕДСТВЕННОЙ ОПТИЧЕСКОЙ НЕЙРОПАТИИ | 2014 |
|
RU2566271C9 |
| КОМБИНАЦИЯ СИРОСИНГОПИНА И МИТОХОНДРИАЛЬНЫХ ИНГИБИТОРОВ ДЛЯ ЛЕЧЕНИЯ РАКА И ДЛЯ ИММУНОСУПРЕССИИ | 2012 |
|
RU2602937C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2024 |
|
RU2839611C1 |
| ПРОИЗВОДНОЕ 7-ГИДРОКСИКУМАРИНА ДЛЯ ИНДУКЦИИ МИТОФАГИИ В КЛЕТКАХ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2819611C1 |
| НЕИММУНОСУПРЕССОРНЫЙ ЦИКЛОСПОРИН ДЛЯ ЛЕЧЕНИЯ ВРОЖДЕННОЙ МИОПАТИИ УЛЬРИХА | 2008 |
|
RU2462262C2 |
| СПОСОБ ВЫБОРА МИТОХОНДРИЙ ДЛЯ ЭКСПЕРИМЕНТАЛЬНОЙ ТЕРАПИИ МЕЛАНОМЫ В16-F10 | 2022 |
|
RU2794762C1 |
| Нуклеиновая кислота для аллотопической экспрессии гена MT-ND4 | 2023 |
|
RU2809065C1 |
| Пептид митохондриальной локализации, нуклеиновая кислота для аллотопической экспрессии гена MT-ND4, содержащий ее экспрессионный вектор и его применение | 2023 |
|
RU2817420C1 |
Изобретение относится к медицине и может быть использовано при лечении эндометриоза. Предложено применение ингибиторов PARP в качестве лекарственного средства для нормализации метаболизма клеток репродуктивной системы женщин при лечении эндометриоза. Изобретение обеспечивает нормализацию функции митохондрий патологичных клеток, участвующих в развитии эндометриоза. 3 ил., 1 пр.
Применение ингибиторов PARP в качестве лекарственного средства для нормализации метаболизма клеток репродуктивной системы женщин при лечении эндометриоза.
| N-АЦЕТИЛ-L-ЦИСТЕИН ДЛЯ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА | 2010 |
|
RU2549433C2 |
| EP 2965762 A1, 13.01.2016 | |||
| US 9707239 B2, 18.07.2017 | |||
| Силачев Д.Н | |||
| и др | |||
| Роль полиаминов в жизнедеятельности клеток репродуктивной системы | |||
| Цитология, 2018, т.60, N3, с.164-172 | |||
| Покатаев И.А | |||
| и др | |||
| PARP-ингибиторы при новообразованиях женской репродуктивной системы | |||
| Современная онкология | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Куликова | |||
Авторы
Даты
2025-04-29—Публикация
2024-03-19—Подача