Изобретение относится к медицине, области регенеративной медицины и тканевой инженерии, а именно к области разработки новых способов получения ингредиентов, пригодных для изготовления скаффолдов и их использования в регенеративной медицине для восстановления поврежденных или утраченных органов и тканей.
В том случае, если размер утраченной ткани больше, чем организм способен воссоздать (регенерировать) без привлечения грубоволокнистой рубцовой ткани, дефект, образующийся в результате травмы или хирургического вмешательства, должен быть заполнен биоматериалом-тканезаместителем, который может иметь различную природу. Сегодня для трансплантации все чаще используются материалы других биологических видов. Биоматериалы животной природы полностью отличаются от человеческих. Поэтому крайне важно чтобы материал прошел очистку от антигенов для того, чтобы устранить все элементы, которые иммунная система человека могла бы распознать как чужеродные.
Репарация тканей происходит благодаря механизмам клеточной миграции, пролиферации и дифференцировки, а также образованию новой внеклеточной матрицы. Эти процессы позволяют заменить поврежденные клетки новыми и восстановить функции тканей. Коллагеновая скаффолд-матрица играет ключевую роль в этом процессе, обеспечивая поддержку и структурную основу для роста новых клеток. В результате такого взаимодействия происходит регенерация и частичное восстановление тканей, что в конечном итоге способствует заживлению травмы и восстановлению их функций.
Скаффолд-матрицы играют ключевую роль в регенеративной медицине и инженерии тканей (Сергацкий К.И., Никольский В.И., Шеремет Д.П., Альджабр М., Мизонов Д.В., Шабров А.В. Характеристика скаффолдов и технологии их изготовления для использования в регенеративной хирургии. Известия высших учебных заведений. Поволжский регион. Медицинские науки. 2022; 3(63): 124-133) [1]. Они должны соответствовать нескольким основным требованиям:
1. Биодеградируемость: скаффолд-матрица должна обладать способностью биодеградировать (трансформироваться) внутри организма после того, как ткань полностью зажила, что позволяет избежать необходимости повторного хирургического вмешательства для удаления скаффолда и снижает риск воспалительных реакций.
2. Биосовместимость: скаффолд-матрица должна быть совместима с биологическим окружением и не вызывать токсических или иммунологических реакций.
3. Поддержка клеточной адгезии и миграции: скаффолд-матрица должна способствовать адгезии клеток и их миграции, обеспечивая оптимальные условия для роста и дифференцировки.
4. Механическая прочность: скаффолд-матрица должна обладать достаточной механической прочностью, чтобы поддерживать тургор ткани в процессе заживления, а затем уступить место новообразованной ткани.
5. Поддержка тканеобразования: скаффолд-матрица должна обеспечивать оптимальные условия для процессов клеточной пролиферации, дифференцировки и образования новой внеклеточной матрицы.
Скаффолд-матрицы должны сочетать в себе все эти характеристики, чтобы эффективно помогать в регенерации тканей и инженерии органов. Таким образом, биологические биодеградируемые скаффолды являются важным инструментом в тканевой инженерии и регенеративной медицине, поскольку предназначены для поддержки и стимуляции роста новых тканей и органов (Никольский В.И., Сергацкий К.И., Шеремет Д.П., Шабров А.В. Скаффолд-технологии в восстановительной медицине: история проблемы, современное состояние и перспективы применения. Хирургия. Журнал им. Н.И. Пирогова. 2022; 11: 36-41) [2]. Существует несколько типов биологических скаффолдов:
1. Природные скаффолды: включают коллаген, эластин, фибрин, гиалуронат и другие белковые материалы, которые обычно присутствуют в тканях организма. Эти материалы могут быть извлечены из тканей животных или человека, но также могут быть синтезированы в лаборатории.
2. Синтетические скаффолды: включают в себя полимерные материалы, такие как полигликолид, полиакрилат, полилактид и другие, которые специально созданы для применения в регенеративной медицине. Они могут обеспечить определенные свойства, такие как механическая прочность, пористость, биодеградируемость и способность поддерживать клеточное рост.
3. Гибридные скаффолды: представляют собой комбинацию природных и синтетических материалов, объединяющих преимущества обоих типов, например, смесь коллагена с полимером может сочетать биологическую совместимость с желаемыми свойствами структурной поддержки и длительной стабильности.
Независимо от типа, биологические скаффолды должны быть биораспадаемыми, обеспечивать подходящую пористую структуру для колонизации клетками, и быть совместимыми с окружающими тканями, чтобы обеспечить успешное интегрирование и рост новых тканей. Данным требованиям наилучшим образом отвечают именно гибридные скаффолды.
Сегодня известны следующие гибридные скаффолды:
- гибридные скаффолды из коллагена и гликозаминогликанов (сГАГ) - такие скаффолды используются для тканевой инженерии костей и хрящей;
- гибридные скаффолды из геля и биокерамики - такие скаффолды используются для регенерации тканей после травмы;
- гибридные скаффолды из полимеров и белков - такие скаффолды используются для регенерации кожи и других мягких тканей;
- гибридные скаффолды из полимеров и растительных экстрактов - такие скаффолды используются в косметологии и медицинской эстетике для улучшения состояния кожи (Зиядуллаева Н.С., Акбаров А.Н., Тулаганов Д.У. Новые возможности в регенеративной стоматологии с применением скаффолдов (обзор литературы). Re-Health Journal. 2021; №1 (9): 160-167) [3].
Наиболее оптимальные свойства для создания биодеградируемого гибридного скаффолда присущи полиакриламидному гидрогелю. При приложении небольшого давления такой гель легко фрагментируется на мелкие доли, а после снятия напряжения фрагменты снова объединяются. Это свойство гелей позволяет вводить их в очаги деструкции костной ткани инъекционным способом. После инъекции фрагменты геля снова должны образовывать агрегаты, заполняя всю имеющуюся полость. За счет высокой гидрофильности полиакриламидный гель после введения в дефект растворяется, вызывая тем самым ответную реакцию организма в виде асептического воспаления. Кроме этого, происходит дегидратация геля и, как следствие, потеря его объема, что вкупе с его низкой адгезионной способностью негативно сказывается на его эффективности.
Известны гибридный скаффолд из поликапролактона и липосом с аспирином, а также скаффолд на основе полиакриламида и сульфатированных гликозаминогликанов (Егорихина М.Н., Мухина П.А., Бронникова И.И. Скаффолды как системы доставки биологически активных и лекарственных веществ. Комплексные проблемы сердечно-сосудистых заболеваний. 2020; 9 (1):92-102. DOI: 10.17802/2306-1278-2020-9-1-92-102) [4]. Обозначенные скаффолды обладают выраженной остеоиндуктивностью, способствуют процессам регенерации биологических тканей.
Однако несмотря на разнообразие систем доставки веществ на базе скаффолд-матрицы, большинство из них не способны гарантировать точную дозировку лекарственных веществ, адресно отсылаемых с помощью скаффолда в биологические ткани. Кроме этого, существующие системы доставки не могут обеспечить пролонгированный эффект высвобождения доставляемых веществ и сохранить их биологическую активность из-за низкой адгезии к окружающим тканям и вследствие этого, быстро резорбируются (вымываются) из места введения.
В качестве прототипа выбран материал для замещения дефектов мягких тканей, содержащий полиакриламид, препарат Реамберин и воду, он повышает местный иммунитет и уменьшает количество осложнений (RU 2633490) [5].
По данным авторов, за счет компонентов материала для замещения мягких тканей, усиливаются защитные иммунные реакции и снижается число осложнений, в том числе в виде воспаления и отека окружающих тканей. Материал способствует повышению местного иммунитета, в результате чего вокруг трансплантируемого гидрогеля образуется очень тонкая соединительно-тканная капсула, препятствующая миграции геля, ограничивая его ранозаживляющее действие зоной введения.
Недостатками прототипа являются значительная резорбция материала после введения в зону дефекта из-за низкого уровня адгезии к биологическим тканям, что препятствует его использованию в качестве основы для скаффолд-матрицы, а также отсутствие пористости, препятствующее адгезии и прикреплению плюрипотентных клеток на поверхности прототипа, что снижает его репаративные свойства.
Поставлена задача: разработка адгезивного гидрогеля для скаффолд-матрицы, обладающего пористостью и высокими адгезивными свойствами к биологическим тканям, обеспечивающего репаративные процессы, а также способствующего ингибированию дистрофических посттравматических процессов и подавляющего воспаление в процессе интеграции скаффолд-матрицы.
Поставленная задача решена созданием адгезивного гидрогеля для скаффолд-матрицы на основе полиакриламида, отличающегося тем, что дополнительно содержит метиленбисакриламид, ферроцианурат калия, глюкозамина гидрохлорид, пектин, линкомицина гидрохлорид и доломитный кисловодский нарзан при следующем соотношении компонентов, мас. %:
Способ изготовления адгезивного гидрогеля для скаффолд-матрицы:
Шаг 1. Растворяется 15 частей пектина в 25 частях доломитного кисловодского нарзана. Полученная смесь разогревается на водяной бане при температуре 70°С до полного растворения пектина и дегазации нарзана. Затем смесь охлаждается при комнатной температуре.
Шаг 2. К 20 частям полиакриламида добавляют 10 частей метиленбисакриламида и 5 частей ферроцианурата калия для инициирования полимеризации, смесь интенсивно перемешивают пластмассовым шпателем.
Шаг 3. В стерильной стеклянной посуде к остывшей смеси пектина и кисловодского нарзана добавляют предварительно смешанные 20 частей полиакриламида, 10 частей метиленбисакриламида и 5 частей ферроцианурата калия и смешивают пластмассовым шпателем до получения однородной тягучей гелеобразной массы.
Шаг 4. К полученной однородной тягучей гелеобразной массе последовательно добавляют 10 частей линкомицина гидрохлорида и 15 частей глюкозамина гидрохлорида.
Шаг 5. Полученную гелеобразную массу помещают в форму, которая имеет нужный вид (пластина, блок, шарик или нить) для скаффолд-матрицы и охлаждают при температуре 4°С в течение 3 часов, после чего полученный гидрогель готов к использованию.
Описание компонентов адгезивного гидрогеля для скаффолд-матрицы.
Полиакриламид - прозрачное кристаллическое вещество без запаха, растворимое в воде, имеет характеристики, аналогичные характеристикам биологических тканей, молекулярная структура гидрогеля является контролируемой и регулируемой, обладает хорошей биосовместимостью и инертностью, не токсична для клеток, поэтому подходит для имплантации in vivo и в качестве подкожного наполнителя в пластической хирургии или в процессе производства контактных линз - то есть в области слизистых оболочек, являющихся самыми чувствительными барьерными биологическими структурами. Из этого видно, что в области биомедицины полиакриламид считают средством с вязкоупругим эффектом, его преимущества постепенно проявляются в применении в различных отраслях биомедицины.
Использование полиакриламида в качестве основы для заявляемого адгезивного гидрогеля обусловлено его идеальным носительством. В результате реакции полимеризации он приобретает свойства молекулярного сита с пористостью, позволяющей плюрипотентным клеткам задерживаться внутри матрицы и высвобождаться дозированно по мере растворения его компонентов in vivo.
Метиленбисакриламид, также известный как N,Nў-метилен-бисакриламид, относится к классу органических соединений, известных как акриловые кислоты и их производные, представляет собой сшивающий агент, который полимеризуется с акриламидом и создает сшивки внутри полиакриламидного геля. N-Nў-метиленбисакриламид способен образовывать сеть, а не линейные цепи, что способствует поддержанию прочности геля. Введение в состав композиции метиленбисакриламида способствует повышению пористости адгезивного гидрогеля, как важного элемента для репаративной регенерации тканей.
Ферроцианурат калия относится к группе стабилизаторов. Основная функция добавки - сохранять однородность смеси, не допустить слипания частиц и образования комков сыпучих веществ, широко применяется как в пищевой промышленности, так и в химической, легкой, сельскохозяйственной.
Глюкозамин (2-дезокси-2-амино-D-(+)-глюкоза) является активным хондропротекторным средством и используется, как правило, в виде солей серной или хлористоводородной кислот. Глюкозамина гидрохлорид оказывает стимулирующее влияние на репаративные процессы в структурах соединительнотканного происхождения, а также способствует ингибированию в них дистрофических посттравматических процессов. Механизмом репаративного действия глюкозамина является стимулирование синтеза гликозаминогликанов и коллагена.
Введение в состав глюкозамина гидрохлорида в количестве 10% от общей массы считается оптимальным для использования в стоматологии, поскольку соответствует рН среды полости рта (в среднем, при рН=7,2-7,4). Количество глюкозамина гидрохлорида, превышающее 10% может создавать более кислую среду (например, до рН=5,0-6,0) и оказывать раздражающее действие на слизистую полости рта и биологические ткани.
Пектин - загуститель и часто он выступает в роли гелеобразователя, стабилизатора и влагоудерживающего агента, является водорастворимым волокном, («свернутый» или «желатинизированный»), содержащимся в клеточных стенках фруктов и овощей, способствует адгезии («прилипаемости») к поверхности биологических тканей (например, к слизистой оболочке полости рта).
Линкомицина гидрохлорид - антибиотик из группы линкозамидов, в составе адгезивного гидрогеля используется в виде прозрачной бесцветной жидкости. Оказывает бактерицидное действие - угнетает синтез белка в микробной клетке, проявляет антибактериальную активность в отношении грамположительных бактерий (Staphylococcus spp. Streptococcus pneumoniae, Corynebacterium diphtheriae, Clostridium spp., Bacteroides spp., Mycoplasma spp.).
Доломитный Кисловодский нарзан или доломитный теплый нарзан (лечебно-столовая сульфатно-гидрокарбонатная натриево-магниево-кальциевая природная питьевая минеральная вода), получаемый из буровой 5/0-бис (г. Кисловодск) - относится к воде со средней степенью минерализации ионами натрия, магния и хлора (1,9-2,0 г/л), способствует выведению токсинов, ускоряет тканевой метаболизм, применяется для ванн, орошений, ингаляций. Опытным путем установлено, что при смешивании теплого кисловодского нарзана с пектином значительно усиливает его адгезивные свойства.
Адгезивный гидрогель можно использовать для скаффолд-матрицы при лечении воспалительных заболеваний пародонта (пародонтита), при травматическом повреждении слизистой оболочки (протезном стоматите), в том числе слизистой оболочки полости рта, губ (хейлит), при устранении очагов деструкции костной ткани и купирования воспаления вокруг дентального имплантата (периимплантит).
Преимущества разработанного адгезивного гидрогеля для скаффолд-матрицы перед прототипом заключаются в увеличении его пористости без потери свойств, необходимых для оптимизации процесса прикрепления (адгезии) плюрипотентных клеток или клеточных факторов роста и обеспечения последующей биодеградации с формированием замещающих тканей. Заявляемый адгезивный гидрогель для скаффолд-матрицы обладает высокими адгезивными свойствами к биологическим тканям, обеспечивает интенсификацию репаративных процессов, а также способствует ингибированию дистрофических посттравматических процессов и подавляет воспаление в процессе интеграции скаффолд-матрицы что подтверждено результатами лабораторных и клинических исследований.
Заявляемый адгезивный гидрогель для скаффолд-матрицы предоставляет широкие возможности использования в стоматологии в зависимости от типа повреждения тканей полости рта.
Разработанный адгезивный гидрогель может быть использован в качестве скаффолд-матрицы для подсадки предварительно прекультивированых плюрипотентных аутологичных клеток из субэпителиальных тканей мягкого неба при устранении дефектов костной ткани и пародонта при лечении хронического генерализованного пародонтита средней и/или тяжелой степеней, при устранении очагов деструкции костной ткани и купирования воспаления вокруг дентального имплантата (периимплантит).
При лечении протезного стоматита для ускорения эпителизации декубитальной язвы, как и при лечении хейлитов заявляемый адгезивный гидрогель может быть использован в качестве скаффолд-матрицы для подсадки клеточных факторов роста, например, обогащенной тромбоцитами плазмы (аутоплазмы), выделенной из образца собственной крови пациента центрифугированием.
Срок годности полученного адгезивного гидрогеля не менее 2 лет (в условиях хранения при температуре 2-4°С). Параметры адгезивного гидрогеля стабильны в процессе хранения. Адгезивный гидрогель представляет собой светло-желтую массу без запаха. Заявляемый адгезивный гидрогель очень пластичен, легко принимает форму дефекта биологических тканей (слизистой оболочки, костной ткани), легко наносится на десну и слизистую оболочку, обладает высокой адгезией и проникающей способностью в ткани.
Лечебное действие заявляемого адгезивного гидрогеля для скаффолд-матрицы апробировано в указанном диапазоне количественного содержания компонентов. Осложнений и побочных явлений при использовании данного адгезивного гидрогеля для скаффолд-матрицы выявлено не было.
Способ использования адгезивного гидрогеля для скаффолд-матрицы раскрывается в клинических примерах.
Примеры конкретного выполнения.
Пример №1. Пациентка К., 45 лет, обратилась с жалобами на неприятные ощущения в области нижней челюсти, невозможность пережевывания пищи и боль при разговоре. Со слов пациентки 2 месяца назад ей был изготовлен частичный съемный протез на нижней челюсти, после чего она не посещала стоматолога.
Объективно: в области альвеолярной части нижней челюсти на уровне переходной складки с вестибулярной стороны и с язычной стороны десны определяется элементы поражения в виде язв, окруженных ободком гиперемии, покрытых фибринозным налетом, кровоточащих и резко болезненных при касании пальцем или инструментом. Элементы поражения локализуются в местах наибольшего давления частичного съемного протеза.
Диагноз: декубитальные язвы на слизистой оболочке альвеолярной части нижней челюсти (К 12.04 - травматическое изъязвление, связанное с ношением зубного протеза).
Лечение. Произведена инструментальная коррекция базиса протеза. Кроме этого, на область элемента поражения нанесен адгезивный гидрогель для скаффолд-матрицы с предварительно подсаженными клеточными факторами роста из обогащенной тромбоцитами плазмы (аутоплазмы), выделенной из образца собственной крови пациентки центрифугированием. Слизистая оболочка альвеолярной части нижней челюсти в области нанесенного геля изолирована медицинской самоклеящейся пленкой с солкосерилом «Диплен» с целью предотвращения вымывания геля ротовой жидкостью.
Через сутки после начала лечения, со слов больной, отмечено уменьшение болезненности при приеме пищи и разговоре. Уже на 3-е сутки от начала лечения больная отмечает значительное улучшение общего состояния, слизистая оболочка альвеолярной части нижней челюсти полностью эпителизировалась.
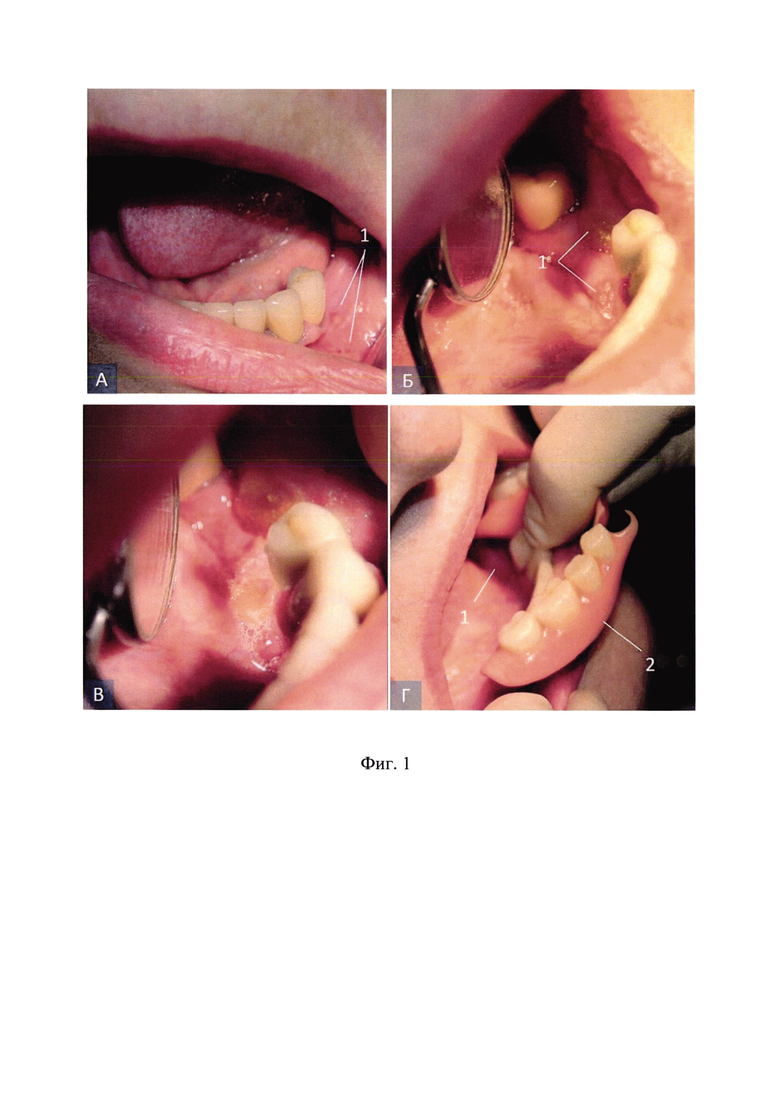
Результаты лечения изображены на фиг. 1, где представлены изображения слизистой оболочки полости рта больной К. до и после проведенного лечения с использованием разработанного адгезивного гидрогеля для скаффолд-матрицы.
Фиг. 1 (А) - декубитальные язвы (1) от ношения частичного съемного протеза на слизистой оболочке альвеолярной части нижней челюсти в области переходной складки с вестибулярной стороны.
Фиг. 1 (Б) - декубитальные язвы (1) от ношения частичного съемного протеза на слизистой оболочке альвеолярного отростка нижней челюсти в язычной области.
Фиг. 1 (В) - после нанесения на очаги изъязвления слизистой оболочки разработанного адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными клеточными факторами роста из обогащенной тромбоцитами плазмы (аутоплазмы), выделенной из образца собственной крови пациента центрифугированием.
Фиг. 1 (Г) - через 3 суток после начала лечения декубитальные язвы (1) полностью эпителизировались, произведена установка частичного съемного протеза с откорректированным базисом (2).
Пример №2. Пациентка С., 35 лет. Жалобы на кровоточивость и изъязвление поверхности красной каймы нижней губы, болезненность, кровоточивость и жжение при прикосновении, разговоре, улыбке, покраснение красной каймы нижней губы, наличие грязно-серого налета на поверхности красной каймы нижней губы.
Объективно: на красной кайме нижней губы имеется поражение, кровоточащее при прикосновении, имеющее вид широкой ленты, идущей от одного угла рта до другого, занимающее всю внутреннюю поверхность каймы, вплотную прилежащее к слизистой оболочке рта.
Диагноз: К13.0 Эксфолиативный хейлит.
Лечение. Пациентке назначено лечение в виде однократного нанесения на зону поражения нижней губы адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными клеточными факторами роста из обогащенной тромбоцитами плазмы (аутоплазмы), выделенной из образца собственной крови пациента центрифугированием. Вся зона поражения красной каймы нижней губы в области нанесения геля изолирована медицинской самоклеящейся пленкой с солкосерилом «Диплен». Через 2 суток после начала лечения у больной отмечено уменьшение размера очага гиперемии и полное исчезновение неприятных ощущений в виде жжения, при визуальном осмотре - слизистая оболочка и красная кайма губ с розовым оттенком, очаг поражения полностью эпителизирован, грязно-серого налета нет, отмечена легкая кровоточивость дефекта при пальпировании.
На фиг. 2 представлено изображение красной каймы нижней губы и слизистой оболочки рта пациентки С. до и после проведенного лечения с использованием адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными клеточными факторами роста из обогащенной тромбоцитами плазмы (аутоплазмы), выделенной из образца собственной крови пациентки центрифугированием.
Фиг 2 (А) - состояние слизистой оболочки и красной каймы нижней губы пациентки С.до начала лечения, грязно-серый налет (1), переходящий с красной каймы нижней губы на слизистую оболочку рта (2).
Фиг. 2 (Б) - состояние слизистой оболочки и красной каймы нижней губы пациентки С.через 2 суток после начала лечения, легкая кровоточивость в области дефекта (1) и остатки адгезивного гидрогеля для скаффолд-матрицы (2) на красной кайме нижней губы.
Пример №3. Пациент Ф., 29 лет, обратился с жалобами на кровоточивость при приеме пищи и чистке зубов, неприятный запах изо рта, зубной налет и подвижность зубов.
Объективно: слизистая оболочка в области зубов верхней и нижней челюстей гиперемирована, отечна, имеет цианотичный оттенок. Межзубные сосочки гипертрофированы, отечны до 1/3 высоты коронки зуба, при прикосновении кровоточат. При зондировании обнаружены пародонтальные карманы глубиной 3-5 мм.
При рентгенологическом обследовании: вертикальный неравномерный тип деструкции костной ткани альвеолярной части нижней челюсти и альвеолярного отростка верхней челюсти, сопровождающийся уменьшением высоты межальвеолярных перегородок от 1/4 до 1/2 длины корней зубов; наличие пародонтальных карманов глубиной от 3 до 5 мм. В области фронтальных зубов нижней челюсти (33, 32, 31, 41, 42, 43) определяются пародонтальные карманы глубиной до 5 мм с гноетечением и убылью костной ткани до 1/2 длины корня, подвижность указанных зубов - 2 степени. Индекс гигиены (ИГ) 2,48-3,75 (низкий).
Диагноз: хронический генерализованный пародонтит средней степени тяжести в стадии обострения.
Лечение. Назначена системная антибактериальная, противовоспалительная и общеукрепляющая терапия. Проведено снятие над- и поддесневых зубных отложений, кюретаж пародонтальных карманов в области 33, 32, 31, 41, 42, 43 зубов с последующим введением адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными прекультивироваными плюрипотентными аутологичными клетками из субэпителиальных тканей мягкого неба. Сразу после начала системной и местной терапии отмечено уменьшение боли и кровоточивости при приеме пищи. На 3-й сутки из пародонтальных карманов гноетечение и гиперемия десен не определялись, подвижность зубов значительно уменьшилась. Через 1 месяц на рентгенограмме в костных карманах в области 33, 32, 31, 41, 42, 43 зубов отмечено восстановление структуры костной ткани. В полости рта глубина патологических карманов сократилась до 2 мм, слизистая оболочка зубодесневого прикрепления плотная, бледно-розового цвета.
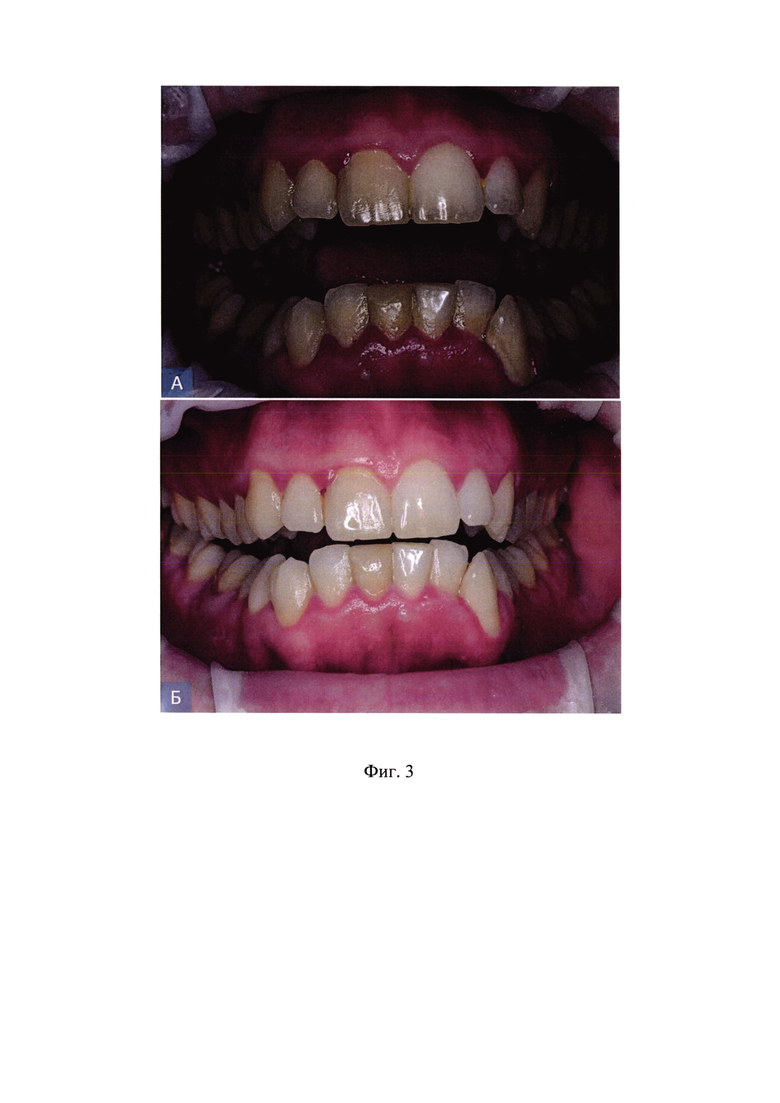
На фиг. 3 представлено изображение полости рта пациента Ф. до и после проведенного лечения с использованием адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными прекультивироваными плюрипотентными аутологичными клетками из субэпителиальных тканей мягкого неба.
Фиг 3 (А) - полость рта пациента Ф. до начала лечения.
Фиг. 3 (Б) - полость рта пациента Ф. через 1 месяц после начала лечения с использованием адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными прекультивироваными плюрипотентными аутологичными клетками из субэпителиальных тканей мягкого неба.
Пример №4.
Пациент С., 54 года, обратился с жалобами на воспалительные явления в области дентальных имплантатов, установленных на месте отсутствующих 45 и 46 зуба нижней челюсти, которые, со слов больного, ему установили более 2 лет назад.
При объективном осмотре в полости рта справа - слизистая вокруг дентальных имплантатов гиперемирована, отечна, при зондировании периимплантной борозды, глубиной более 5 мм, отмечалось кровотечение с гноетечением, неприятный запах.
На рентгенограмме - частично резорбированная щечная и язычная кортикальная пластинка (глубина резорбции костной ткани 7,5 мм) в периимплантной области дентального имплантата, установленного на месте отсутствующего 45 зуба нижней челюсти слева. Стабильность дентального имплантата не нарушена.
Диагноз: хронический периимплантит в области дентального имплантата, замещающего отсутствующий 45 зуб.
Лечение. Проведена операция по устранению периимплантатного дефекта в области имплантата, установленного на месте 45 зуба, с использованием адгезивного гидрогеля для скаффолд-матрицы с предварительно подсаженными прекультивироваными плюрипотентными аутологичными клетками из субэпителиальных тканей мягкого неба.
Результаты рентгенологического исследования периимплантной зоны пациента С. до и после начала лечения представлены на фиг. 4.
Фиг. 4 (А) - фрагмент обзорной рентгенограммы до ремоделирования периимплантной зоны челюстной кости, зона резорбции костной ткани глубиной 7,5 мм вокруг дентального имплантата на месте отсутствующего 45 зуба (1).
Фиг. 4 (Б) - фрагмент обзорной рентгенограммы через 3 месяца после операции по ремоделированию периимплантной зоны челюстной кости, восстановленная костная ткань вокруг дентального имплантата на месте отсутствующего 36 зуба (1), глубина зоны резорбции - 1,5 мм.
Как показали результаты исследования, разработанный адгезивный гидрогель для скаффолд-матрицы обладает пористостью и высокими адгезивными свойствами к биологическим тканям, обеспечивает репаративные процессы, а также способствует ингибированию дистрофических посттравматических процессов и подавляет воспаление в процессе интеграции скаффолд-матрицы.
Таким образом, полученные в клинике данные позволяют рекомендовать разработанный адгезивный гидрогель для скаффолд-матрицы как высокоэффективное средство терапии и профилактики пародонтита и/или периимплантита любой степени тяжести, травматические и воспалительные повреждения слизистой оболочки полости рта и красной каймы губ одонтогенной и неодонтогенной природы (язвы, ожоги, разрывы) обладающее выраженным клиническим эффектом и имеющее широкие функциональные возможности для практической медицины.
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Сергацкий К.И., Никольский В.И., Шеремет Д.П., Альджабр М., Мизонов Д.В., Шабров А.В. Характеристика скаффолдов и технологии их изготовления для использования в регенеративной хирургии. Известия высших учебных заведений. Поволжский регион. Медицинские науки. 2022; 3(63): 124-133.
2. Никольский В.И., Сергацкий К.И., Шеремет Д.П., Шабров А.В. Скаффолд-технологии в восстановительной медицине: история проблемы, современное состояние и перспективы применения. Хирургия. Журнал им. Н.И. Пирогова. 2022; 11: 36-41.
3. Зиядуллаева Н.С., Акбаров А.Н., Тулаганов Д.У. Новые возможности в регенеративной стоматологии с применением скаффолдов (обзор литературы). Re-Health Journal. 2021; №1 (9): 160-167.
4. Егорихина М.Н., Мухина П.А., Бронникова И.И. Скаффолды как системы доставки биологически активных и лекарственных веществ. Комплексные проблемы сердечно-сосудистых заболеваний. 2020; 9 (1):92-102. DOI: 10.17802/2306-1278-2020-9-1-92-102.
5. RU 2633490, заявка №2016146012,2016.11.23. Материал для замещения дефектов мягких тканей.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОЗОНИРОВАННЫЙ РАСТВОР КОЛЛОИДНОГО СЕРЕБРА ДЛЯ ЛЕЧЕНИЯ ПАРОДОНТИТА И ПЕРИИМПЛАНТИТА | 2023 |
|
RU2830653C1 |
| РАНОЗАЖИВЛЯЮЩИЙ ГЕЛЬ ДЛЯ ЛЕЧЕНИЯ ХЕЙЛИТОВ И ХРОНИЧЕСКИХ ТРЕЩИН ГУБ У ПАЦИЕНТОВ С ОРТОДОНТИЧЕСКОЙ ПАТОЛОГИЕЙ | 2023 |
|
RU2827882C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАРОДОНТИТА И ПЕРИИМПЛАНТИТА | 2023 |
|
RU2830655C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЙ ЭЛИКСИР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2355379C1 |
| КЛЕЕВАЯ КОМПОЗИЦИЯ ДЛЯ ПОЛОСТИ РТА ПРИ ЛЕЧЕНИИ ПАРОДОНТИТА И ПЕРИИМПЛАНТИТА | 2021 |
|
RU2791674C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ГЕНЕРАЛИЗОВАННОГО ПАРОДОНТИТА | 2014 |
|
RU2550957C1 |
| СПОСОБ ЛЕЧЕНИЯ ТРАВМЫ НИЖНЕГО АЛЬВЕОЛЯРНОГО НЕРВА ПРИ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ | 2011 |
|
RU2452429C1 |
| ПАСТА ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПЕРИИМПЛАНТИТА | 2022 |
|
RU2786136C1 |
| СПОСОБ КОСТНОЙ ПЛАСТИКИ ПРИ НЕПОСРЕДСТВЕННОЙ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ | 2008 |
|
RU2366378C1 |
| СПОСОБ ЛЕЧЕНИЯ РАДИКУЛЯРНОЙ КИСТЫ ЧЕЛЮСТИ | 2007 |
|
RU2326648C1 |


Настоящее изобретение относится к адгезивному гидрогелю для скаффолд-матрицы на основе полиакриламида, согласно изобретению дополнительно содержит метиленбисакриламид, ферроцианурат калия, глюкозамина гидрохлорид, пектин, линкомицина гидрохлорид и доломитный кисловодский нарзан при следующем соотношении компонентов, мас. %: полиакриламид 20, метиленбисакриламид 10, ферроцианурат калия 5, глюкозамина гидрохлорид 15, пектин 15, линкомицина гидрохлорид 10, доломитный кисловодский нарзан 25. Настоящее изобретение обеспечивает разработку адгезивного гидрогеля для скаффолд-матрицы, обладающего пористостью и высокими адгезивными свойствами к биологическим тканям, обеспечивающего репаративные процессы, а также способствующего ингибированию дистрофических посттравматических процессов и подавляющего воспаление в процессе интеграции скаффолд-матрицы. 4 ил., 4 пр.
Адгезивный гидрогель для скаффолд-матрицы на основе полиакриламида, отличающийся тем, что дополнительно содержит метиленбисакриламид, ферроцианурат калия, глюкозамина гидрохлорид, пектин, линкомицина гидрохлорид и доломитный кисловодский нарзан при следующем соотношении компонентов, мас. %:
| US 2017014550 A1, 19.01.2017 | |||
| ПОЛИФУНКЦИОНАЛЬНЫЙ БИОСОВМЕСТИМЫЙ ГИДРОГЕЛЬ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2205034C1 |
| ПОЛИМЕРНЫЙ ГИДРОГЕЛЬ АКРИЛАМИДНОГО СОПОЛИМЕРА ТЕРАПЕВТИЧЕСКОГО ПРИМЕНЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2198686C2 |
| Ibrahim M El-Sherbiny et al., Hydrogel scaffolds for tissue engineering: Progress and challenges / Glob Cardiol Sci Pract | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Способ получения полиакриламидного гидрогеля | 2020 |
|
RU2749268C1 |
Авторы
Даты
2025-05-07—Публикация
2024-04-26—Подача