Изобретение относится к области медицины, в частности к хирургии, как детской, так и общей абдоминальной хирургии, и колопроктологии, и предназначено для лапароскопического формирования неоаппендикостомы с антирефлюксным клапаном.
Недержание кала, в следствие недостаточности нервного или мышечного аппарата структур тазового дна, является сложной проблемой, ухудшающей социализацию человека и зачастую не имеет резерва для патогенетического лечения. Учитывая особенности физиологии толстой кишки, наряду со средствами личной гигиены активно применяются ежедневные очистительные клизмы, которые в большинстве случаев позволяют минимизировать непроизвольное подтекание стула. Но при использовании очистительных клизм помимо дискомфорта от регулярного введения катетера через анус, существуют обстоятельства, когда их эффективность снижается. Так при жидком стуле и метеоризме частота эпизодов каломазания значительно возрастает.
Для решения этой проблемы применяются технологии антеградного промывания толстой кишки. С этой цель пациенту накладывается континентная аппендикостома, которая используется для периодической катетеризации и не требует применения калоприемников. Данная операция была предложена английским хирургом Padraig S J. Malone (Malone, PS et al, Preliminary report: the antegrade continence enema, Lancet, 1990;336, p. 1217-1218) и показала свою эффективность и безопасность. В настоящий момент операция в литературе встречается под названием операция Малона. Войдя в клиническую практику, появились различные модификации как открытые, с лапароскопическим ассистированием / Lawal, ТА et al., Laparoscopic-assisted Malone appendicostomy in the management of fecal incontinence in children, J Laparoendosc Adv Surg Tech A. 2011; 21(5), p. 455-459) и лапароскопические (Lawal, ТА et al, Laparoscopic-assisted Malone appendicostomy in the management of fecal incontinence in children, J Laparoendosc Adv Surg Tech A. 2011;21(5), p.455-459; Lopez, JJ et al, Single institution review of Mini-ACE® low-profile appendicostomy button for antegrade continence enema administration, J Pediatr Surg. 2022; 57(10), p.359-364) методики для ее выведения. Варьируются и варианты локализации наружного отверстия стомы. Формирование клапана для предотвращения попадания кишечного содержимого в аппендикс, является важным компонентом операции для профилактики выделения кала через стому, воспалительных осложнений и неприятных ощущений у пациента и окружающих.
В случае, когда аппендикулярный отросток был утрачен к моменту наложения аппендикостомы, предложены варианты формирования неоаппендикостомы (Hensle, TW et al, The Malone antegrade continence enema procedure in the management of patients with spina bifida, J Am Coll Surg. 1998; 186(6), p.669-674). При данном вмешательстве из стенки слепой или восходящей (Chatoorgoon, К et al, Neoappendicostomy in the management of pediatric fecal incontinence, J Pediatr Surg. 2011; 46(6), p. 1243-1249; Acker, S et al, Transition of care: a growing concern in adult patients born with colorectal anomalies, Pediatr Surg Int. 2019; 35(2), p.233-237), а иногда и нисходящей ободочной кишки (Anselmo, СВ et al, Left-colon antegrade enema (LACE): Long-term experience with the Macedo-Malone approach, Neurourol Urodyn. 2017;36(1), p.111-115) выкраивается лоскут, из которого формируется тубулярная структура, замещающая аппендикс при формировании континентной стомы. Также некоторые хирурги использовали для этих целей тонкую кишку с баугиниевой заслонкой в виде клапана (Abildgaaard, НА et al, Ileal Neoappendicostomy in the Treatment of Fecal Incontinence in Children, Eur J Pediatr Surg. 2021; 31(5), p.427-431) или кондуита, выкроенного из сегмента тонкой кишки (Schell, SR et al, Control of fecal incontinence: continued success with the Malone procedure, Surgery, 1997; 122(3), p.626-631). При анализе доступной литературы вариантов лапароскопического формирования неоаппендикостомы обнаружено не было. Данные операции выполняются открытым способом в основном с применением ручного шва. В некоторых публикациях описано применение сшивающего аппарата для обуживания тонкокишечного кондуита и дистального сегмента подвздошной кишки, а также для выкраивания лоскута из стенки толстой кишки (Kastenberg, ZJ et al, Stapled neoappendicostomy: A novel technique, J Pediatr Surg. 2022; 57(12), p. 1029-1030).
Предложенные методики невозможно безопасно выполнить лапароскопическим доступом, в связи с чем нами был разработан описываемый способ. Анализ имеющихся методик позволил выявить ряд недостатков, которые ограничивают их применение в лапароскопическом варианте, а также обуславливают риск развития осложнений, такие как необходимость вскрывать просвет кишки, выкраивание лоскута с основанием, развернутым к противобрыжеечному краю, ввиду риска ишемизации лоскута, отказ от формирования клапанной антирефлюксной защиты неоаппендикса, а некоторые предложенные варианты создания клапана сокращают значительную часть длины неоаппендикса, с выведением стомы в косметически не выгодном положении.
В патентной литературе методик формирования аппедикостом и неоаппендикостом не найдено. Также отсутствует информация о наличии способов антеградного промывания толстой кишки. В отечественной литературе имеются единичные публикации о выполнении аппендикостомии у детей, при этом данные об опыте формирования неоаппендикостом отсутствуют.
Из всех описанных методик наш способ наиболее близок к технологии формирования неоаппендикса из стенки толстой кишки при помощи сшивающего аппарата, предложенной Kastenberg Z.J. с соавторами (Kastenberg, ZJ et al, Stapled neoappendicostomy: A novel technique, J Pediatr Surg. 2022; 57(12), p.1029-1030)., выбранный нами за прототип. В предлагаемом авторами методе лоскут формируется на питающем сосуде, в месте планируемого конца лоскута делают отверстие, через которое заводят катетер. При помощи зажимов Элисона отграничивают участок стенки вместе с заведенным катетером, моделируя диаметр будущего неоаппендикса. Затем сшивающим аппаратом отсекают смоделиванный неоаппендикс. Затем накладывают серо-серозные швы на основную кишку, укрывая основание отростка, при этом отросток ориентирован в латеральном направлении. Неоаппендикостому выводят в разрез.
К недостаткам упомянутых выше методик, в том числе и прототипа, следует отнести необходимость вскрытия просвета толстой кишки, открытую методику его формирования с отсутствием перспектив для выполнения данной операции в ограниченном пространстве брюшной полости при лапароскопическом доступе.
Таким образом, существует потребность в способе лапароскопического формирования неоаппендикостомы с антирефлюксным клапаном, лишенном вышеуказанных недостатков.
Технический результат состоит в снижении объема оперативного вмешательства и рисков интра- и послеоперационных осложнений при формировании неоаппендикостомы для обеспечения возможности проведения антеградной континентной клизмы пациентам с недержанием кала и утраченным аппендикулярным отростком. После применения предлагаемого способа обеспечивается адекватное удержание кала за счет тотального антеградного промывания толстой кишки с удалением содержимого как из правых, так и из левых отделов толстой кишки при помощи лапароскопически сформированного неоаппендикса. В связи с физиологическим заполнением толстой кишки до появления каловых масс в ампуле прямой кишке требуется около суток, что позволяет проводить необходимые гигиенические процедуры в комфортных домашних условиях без необходимости применения гигиенических средств в течение дня и без риска эпизодов каломазания, недержания жидкого стула и даже газов. Косметический эффект от данной операции позволяет пациентам вести активный образ жизни и адекватно социализироваться.
Для достижения указанного технического результата в способе формирования неоаппендикостомы с антирефлюксным клапаном, включающем формирование неоаппендикостомы из стенки толстой кишки при помощи линейного сшивающего аппарата с формированием лоскута на питающем сосуде и наложением серо-серозных швов между основанием неоаппендикса и складкой стенки несущей кишки с формированием антирефлюксного клапана, предлагается осуществлять оперативное вмешательство лапароскопически, при этом устанавливают троакар для оптики в правом подреберье, а также троакары в эпигастральной области справа от средней линии и в правой подвздошной области для манипуляторов, определяют питающий сосуд на брыжеечной стороне восходящей ободочной кишки, возле питающего сосуда накладывают первый шов-держалку на глубину мышечного слоя, который проводят через переднюю брюшную стенку в проекции над питающим сосудом, и принимают первый шов-держалку как внешний ориентир основания неоаппендикса; определяют длину будущего неоаппендикса как расстояние от внутреннего края пупочной ямки до ости подвздошной кости; наносят маркерную метку, соответствующую полученному расстоянию, на рабочий конец лапароскопического диссектора, в брюшной полости прикладывают метку диссектора к первому шву-держалке поперек восходящей ободочной кишки, на уровне края диссектора накладывают второй шов-держалку на глубину мышечного слоя, который также проводят через переднюю брюшную стенку в проекции над прошитым участком кишки, и принимают второй шов-держалку как внешний ориентир слепого конца неоаппендикса, при этом формируют петли швов-держалок длиной, достаточной для свободного смещения восходящей кишки на всю высоту брюшной полости; укладывают с помощью швов-держалок восходящую ободочную кишку вниз до осуществления разведения бранш сшивающего аппарата в брюшной полости, в раскрытые бранши заводят швы-держалки и подтягивают их таким образом, что помещают стенку кишки между браншами сшивающего аппарата, при этом выводят над краем кассеты сшивающего аппарата дупликатуру стенки кишки шириной, равной диаметру диссектора; выделенную часть стенки отжимают, прошивают и отсекают с помощью аппарата, удаляют первый шов-держалку с основания неоаппендикса, за второй шов-держалку сформированный неоаппендикс переводят в медиальную сторону, открывая доступ к аппаратному шву, после формирования антирефлюксного клапана герметизируют стенку несущей кишки, продлевая серо-серозный шов над всем аппаратным швом; по нижнебоковой стенке пупочной ямки выполняют треугольный кожный разрез; при помощи зажима формируют туннель для выведения неоаппендикса, при этом зажим заводят под медиальный край прямой мышцы живота в предбрюшинную клетчатку, избегая попадания в толщу мышцы, проводят зажим до середины ширины прямой мышцы живота, на этом уровне тупым способом перфорируют париетальную брюшину, захватывают концы второго шва-держалки и выводят слепой конец неоаппендикса через сформированный канал в разрез в пупочной ямке, вскрывают просвет неоаппендикса в месте слепого конца и накладывают по окружности слизисто-кожные швы без эвагинации слизистой, через неоаппендикостому в толстую кишку заводят силиконовый катетер с его накожной фиксацией, затем выполняют экстракорпоральную фиксацию восходящей ободочной кишки в области несущей неоаппендикостому части тремя узловыми швами к передней брюшной стенке.
На фиг. 1 - внешний вид расстановки троакаров со схемой.
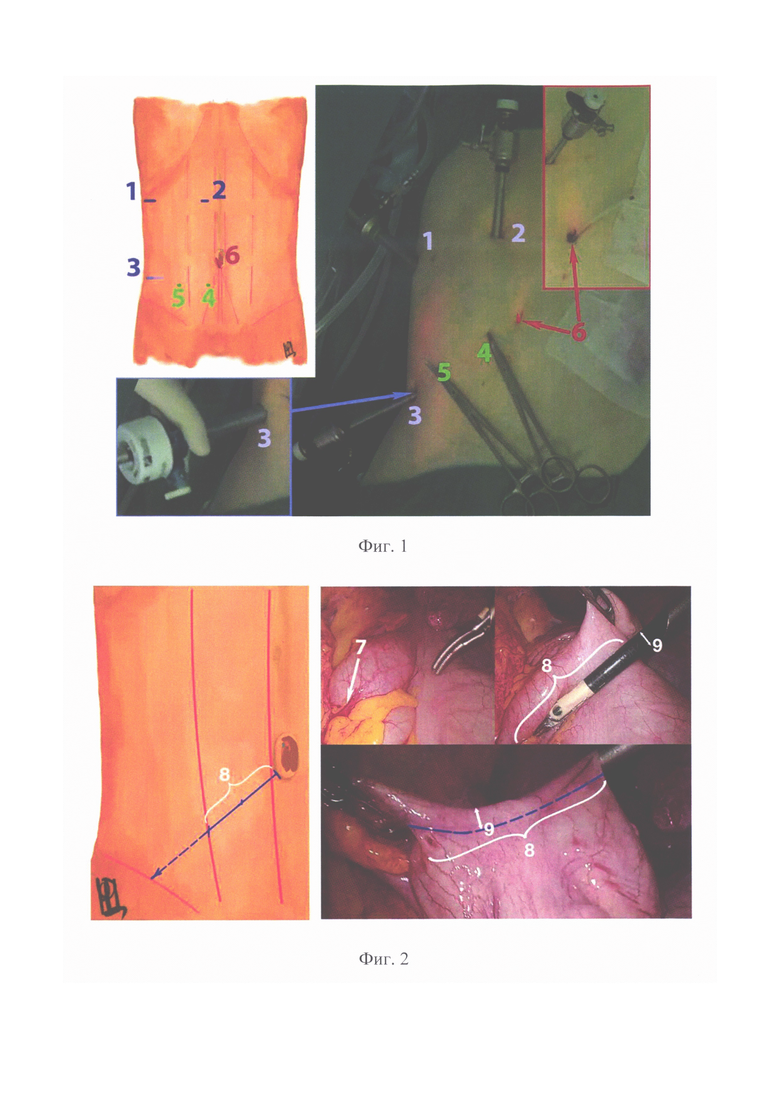
На фиг. 2-8 - последовательные этапы операции: определение питающего сосуда со схемой разметки лоскута, наложение швов-держалок на стенку кишки, расположение сшивающего аппарата в брюшной полости, адаптация стенки кишки в браншах сшивающего аппарата, сформированный неоаппендикс и внешний вид аппаратного шва, внешний вид неоаппендикса со сформированной манжетой и герметизированным швом основной кишки со схемой, внешний вид сформированной неоаппендикостомы со схемой, фиксация стенки восходящей ободочной кишки.
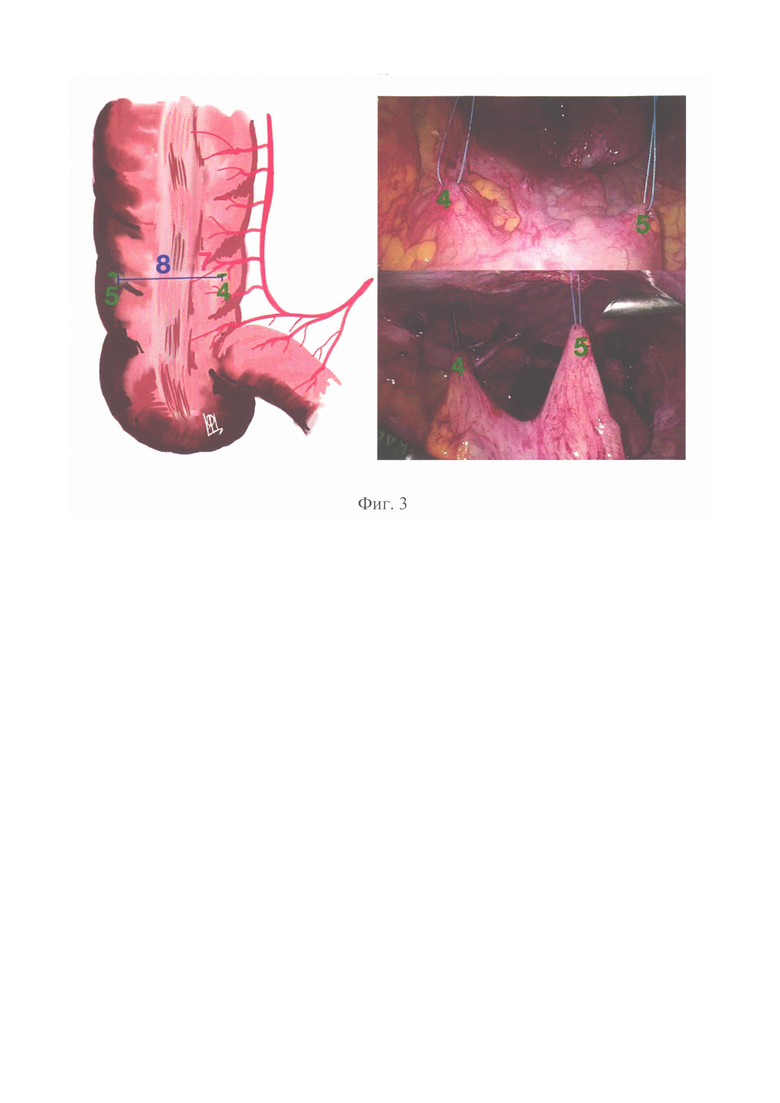
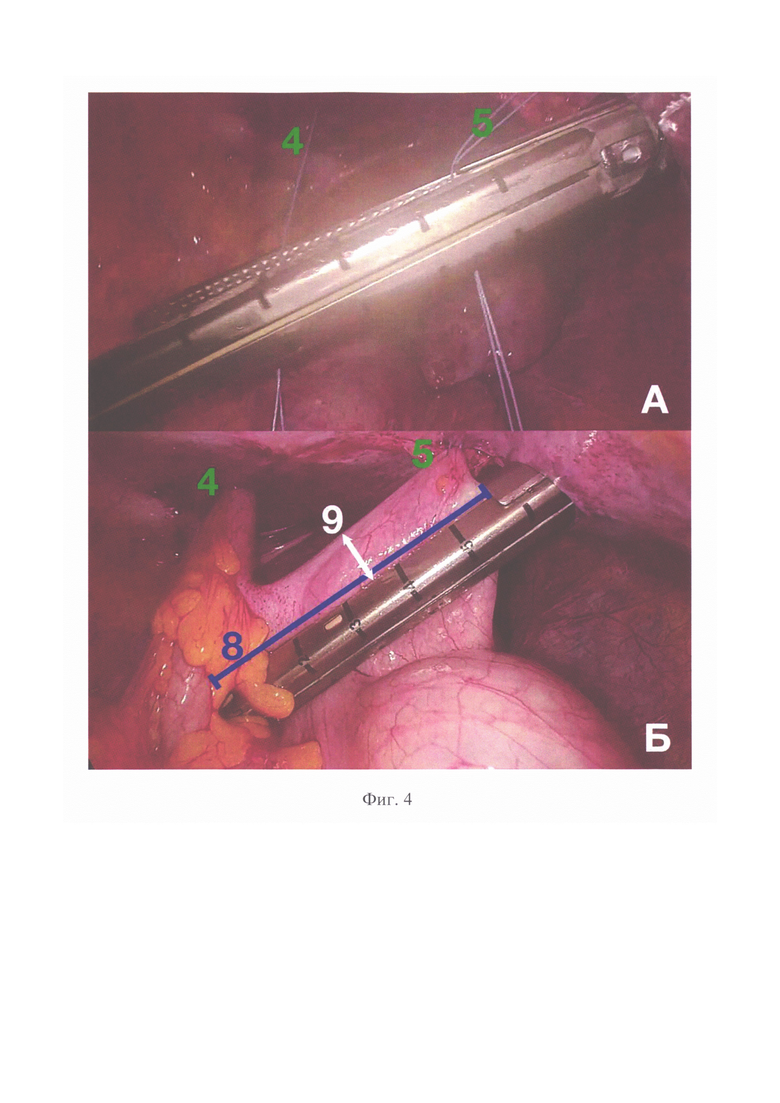
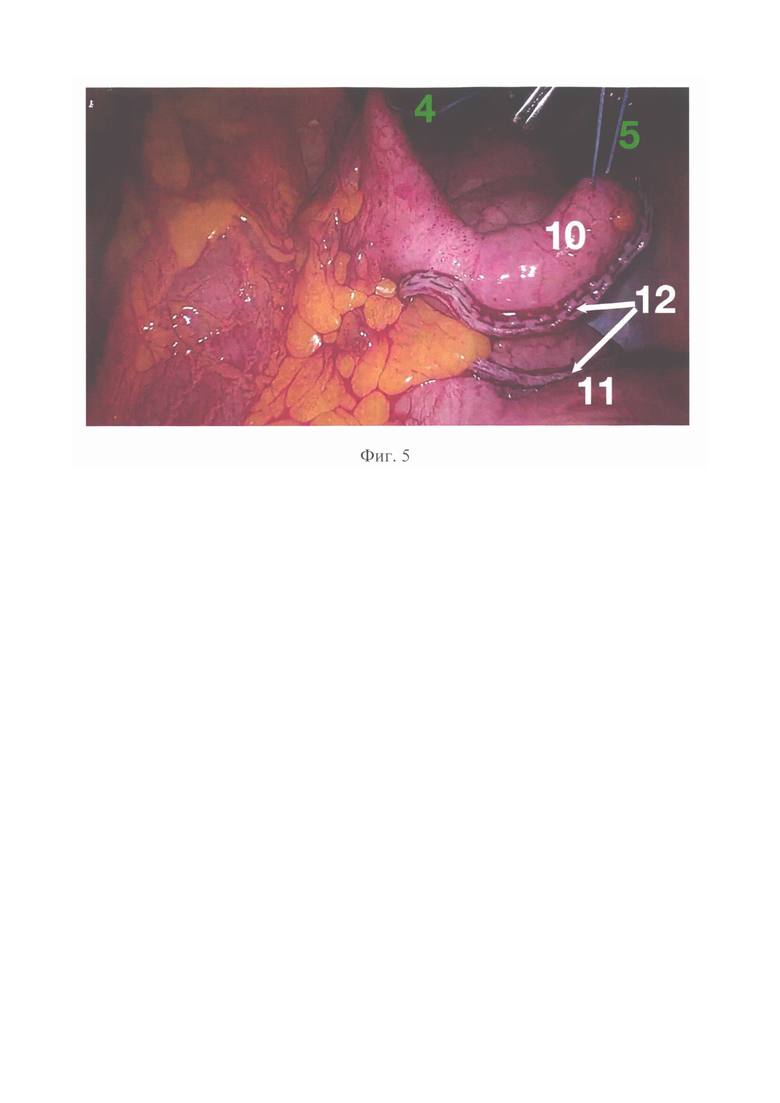
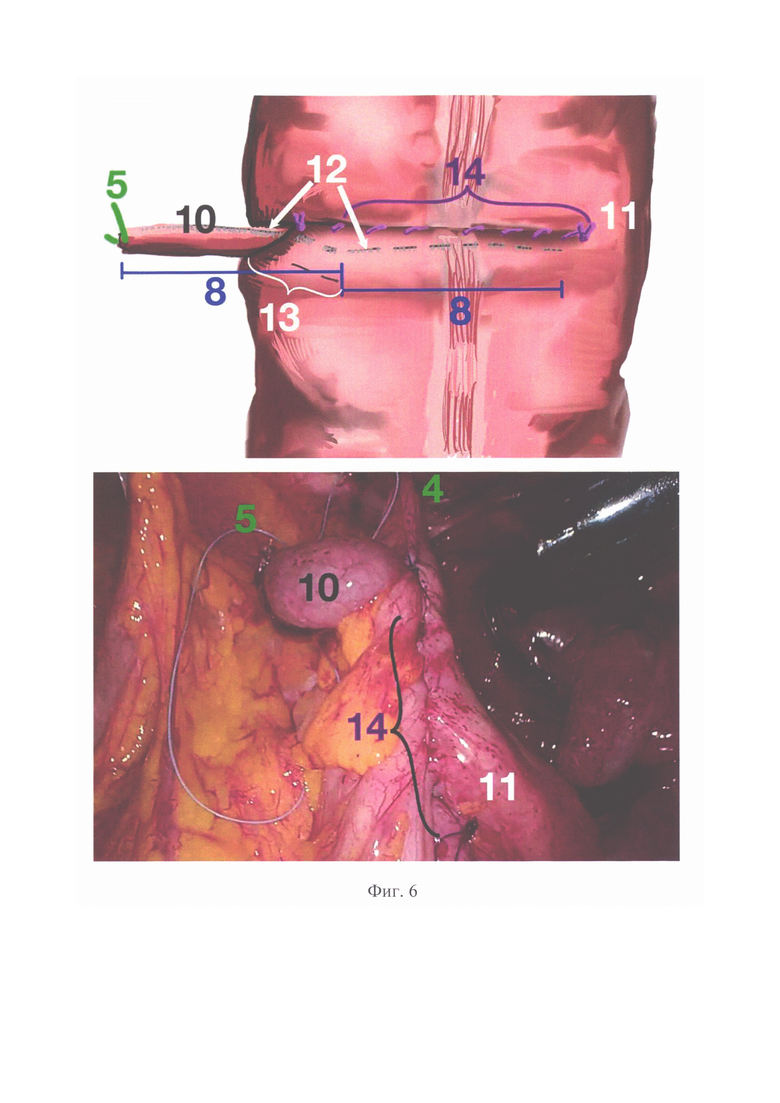
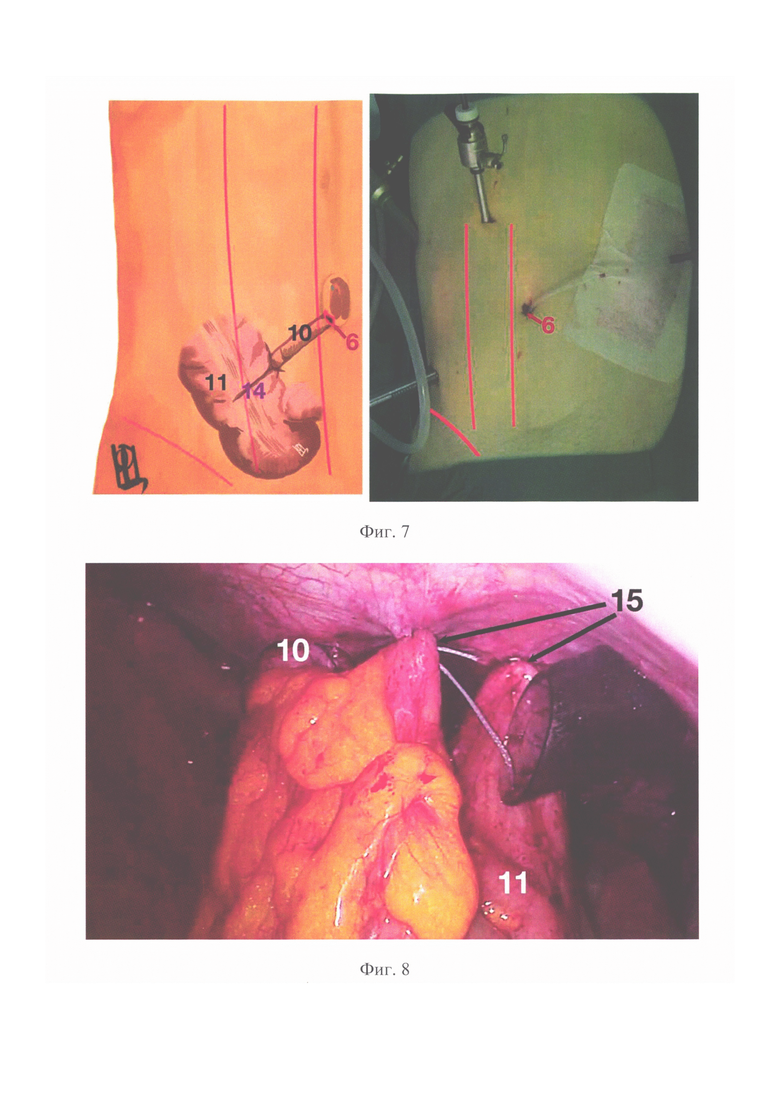
Способ осуществляют следующим образом. Выполняют лапароскопическую неоаппендикостомию как у детей, так и у взрослых пациентов. Оперативное вмешательство выполняют в плановом порядке в качестве самостоятельной операции или в сочетании с реконструктивным вмешательством по поводу порока развития или его осложнений. Под общей анестезией в положении на спине устанавливают лапаропорты. Расстановка лапоропортов проводится таким способом, чтобы было удобно манипулировать на восходящей ободочной кишке и области пупка (Фиг. 1, 1- троакар для оптики, 2 - троакар под манипулятор для левой руки, 3 - троакар под манипулятор для правой руки / троакар под линейный сшивающий аппарат, 4 - шов-держалка у основания неоаппедикса (питающий сосуд), 5 - шов-держалка у конца неоаппедикса, 6 - место разреза пупка для формирования неоаппендикостомы.). Первым устанавливают троакар для оптики (1) в правом подреберье. После наложения карбоксиперитонеума под контролем оптики устанавливают дополнительные троакары в эпигастральной области справа от средней линии (2) и в правой подвздошной области (3) для манипуляторов. Осматривают купол слепой кишки, при необходимости разделяя сращения, для адекватной визуализации илеоцекального угла и ревизии слепой кишки на предмет наличия аппендикса. Затем осматривают восходящую кишку с оценкой архитектоники сосудов брыжеечного края, определяют питающий сосуд, на котором будет сформирована неоаппендикостома (Фиг. 2, 7 -питающий сосуд на брыжеечном крае восходящей ободочной кишки, 8 -длина лоскута для формирования неоаппендикса, равная расстоянию от внутреннего края пупочной ямки до ости подвздошной кости, 9 - ширина дупликатуры стенки кишки, равная ширине рабочего конца диссектора). Возле питающего сосуда (7) накладывают первый шов-держалку (4), который проводят через переднюю брюшную стенку (вкол выполняется в проекции над питающим сосудом), затем при помощи лапароскопического иглодержателя прошивают стенку восходящей ободочной кишки на глубину мышечного слоя, после чего иглу выкалывают обратно на переднюю брюшную стенку в месте вкола. Данный первый шов-держалка обозначает основание будущего неоаппендикса. Длина петли должна быть достаточной для свободного смещения восходящей кишки на всю высоту брюшной полости. Второй шов-держалку (5) накладывают на проекцию слепого конца неоаппендикса, определяя направление выкраивания и длину лоскута. Длина определяется шириной прямой мышцы живота по линии, направленной от внутреннего края пупочной ямки по направлении к ости подвздошной кости (8). Для точного позиционирования второго шва-держалки (5) следует нанести маркерную метку на лапароскопический диссектор, приложив который к восходящей кишке, можно точно определить нужную длину лоскута (8) для будущего неоаппендикса. Это же значение используется для выбора длины кассеты сшивающего лапароскопического аппарата. После выбора места расположения слепого конца неоаппендикса второй шов-держалку (5) накладывают аналогично предыдущему, по описанной выше схеме (Фиг. 3 - наложение швов-держалок на стенку кишки: 4 - шов-держалка у основания неоаппедикса, 5 -шов-держалка у конца неоаппедикса, 7 - питающий сосуд на брыжеечном крае восходящей ободочной кишке, 8 - длина лоскута для формирования неоаппендикса). Выполняют смену троакара в правой подвздошной области на троакар, комплиментарный сшивающему аппарату, и заводят сам сшивающий аппарат, бранши которого располагают над размеченным участком восходящей кишки (Фиг. 4 -расположение сшивающего аппарата в брюшной полости (А) и адаптация стенки кишки в браншах сшивающего аппарата (Б): 4 - шов-держалка у основания неоаппедикса, 5 - шов-держалка у конца неоаппедикса, 8 - длина лоскута для формирования неоаппендикса, 9 - ширина дупликатуры стенки кишки). Подтягивая швы-держалки, помещают стенку кишки (11) между браншами сшивающего аппарата, адаптируя ее для формирования неоаппендикса (10) необходимого диаметра (Фиг. 5 - сформированный неоаппендикс и внешний вид аппаратного шва: 4 - шов-держалка у основания неоаппедикса, 5 - шов-держалка у конца неоаппедикса, 10 - неоаппендикс, 11 - несущая кишка, 12 - аппаратный шов). При помощи сшивающего аппарата часть стенки отжимают, аппаратно прошивают и отсекают (Фиг. 6 - внешний вид неоаппендикса со сформированной манжетой и герметизированным швом основной кишки со схемой: 4 - шов-держалка у основания неоаппедикса, 5 - шов-держалка у конца неоаппедикса, 8 - длина лоскута для формирования неоаппендикса, 10 - неоаппендикс, 11 - несущая кишка, 12 - аппаратный шов, 13 - манжета вокруг основания неоаппендикса, 14 - герметизирующий шов.). Сшивающий аппарат удаляют, удаляют шов-держалку (4) с основания неоаппендикса, а держалку (5) в области слепого конца неоаппендикса при помощи лапароскопического зажима полностью переводят в брюшную полость. За держалку сформированный неоаппендикс (10) переводят в медиальную сторону, накладывают серо-серозные швы, укрывая основание неоаппендикса и формируя таким образом антирефлюксный клапан. Серо-серозный шов продлевают над всем аппаратным швом, герметизируя его (Фиг. 7 - внешний вид сформированной неоаппендикостомы со схемой: 6 - разрез пупка для формирования неоаппендикостомы, 10 - неоаппендикс, 11 - несущая кишка, 14 - герметизирующий шов). По нижней или нижнелатеральной стенке пупочной ямки выполняют треугольный кожный разрез (6). При помощи зажима формируют туннель для выведения неоаппендикса (10) под контролем эндокамеры, на уровне середины ширины прямой мышцы живота перфорируют париетальную брюшину, захватывают концы шва-держалки (5) зажимом и выводят слепой конец неоаппендикса (10) в разрез в пупочной ямке (6). Вскрывают просвет неоаппендикса (10) и накладывают по окружности слизисто-кожные швы. Под контролем эндокамеры через неоаппендикс в толстую кишку заводят силиконовый катетер и выполняют фиксацию восходящей ободочной кишки к передней брюшной стенке экстракорпоральными узловыми швами (15) (Фиг. 8 - фиксация стенки восходящей ободочной кишки: 10 - неоаппендикс, 11 - несущая кишка, 15 - фиксирующие кишку швы). Проводят санацию и десуффляцию брюшной полости, ушивают троакарные раны.
Пример. Больная К. в возрасте 26 лет госпитализирована в хирургическое отделение Ильинской больницы. Пациентка перенесла серию реконструктивных оперативных вмешательств по поводу множественных врожденных пороков развития, ретроспективный анализ позволит верифицировать все компоненты порока: персистирующая клоака V тип по А. Рейа: короткий общий канал, полное удвоение влагалища и матки, эктопия правого мочеточника в шейку мочевого пузыря, вторичное сморщивание правой почки, рефлюксирующий мегауретер слева, нейрогенная дисфункция мочевого пузыря, агенезия копчика, гипоплазия крестца, гипоплазия нижней челюсти. После рождения порок развития был расценен как атрезия ануса с ректо-вагинальным свищем и для обеспечения адекватного отхождения кала пациентке начали проводить бужирование кишечной фистулы до трехлетнего возраста, когда ей была выведена колостома. В возрасте 9 месяцев в связи со вторичным сморщиванием правой почки была выполнена нефруретерэктомия справа. В возрасте 2 лет в связи с пузырно-мочеточниковым рефлюксом в единственную почку была выведена уретерокутанеостома слева. В возрасте 3 лет выполнена операция Грегуара с закрытием уретерокутанеостомы, однако, поскольку после операции сохранялся пузырно-мочеточниковый рефлюкс IV степени, была наложена нефростома симультанно с выведением колостомы. Через 6 месяцев после была выполнена заднесагиттальная аноректопластика по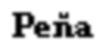 . Следующим этапом была выполнена расширяющая энтероцистопластика, наложен энтероуретероанастомоз слева с формированием цистоаппендикостомы. При закрытии колостомы была выполнена первая реконструкция промежности. В дальнейшем у пациентки сохранялось недержание кала, периодическое недержание мочи, произошла облитерация аппендикостомы. В возрасте 15 лет в связи с недержанием кала была выполнена повторная промежностная реконструкция - промежностная проктопластика с протезированием пуборектальной мышцы искусственным трансплантатом «Урослинг» и пластика промежности. После проведенной операции функция аноректальной зоны оставалась неудовлетворительной, адекватное опорожнение было возможно только на фоне применения клизмы. Без применения клизмы или слабительных отмечались длительные запоры, на фоне которых возникало повышенное газообразование. При незначительном размягчении каловых масс сопровождалось недержанием газов и порций каловых масс, постоянное каломазание. Пациентка обратился в Ильинскую больницу для решения вопроса о возможности восстановления половой функции. На момент обследования в клинике у пациентки имелась облитерация правого влагалища, внесфинктерное низведение прямой кишки, недержание кала, остаточная культя правого мочеточника после нефроуретерэктомии, нейрогенная дисфункция мочевого пузыря, состояние после энтероцистопластики цистоаппендикоцистостомии (облитерация аппендикостомы), состояние после оперативной коррекции гипоплазии нижней челюсти с ограничением ее выведения.
. Следующим этапом была выполнена расширяющая энтероцистопластика, наложен энтероуретероанастомоз слева с формированием цистоаппендикостомы. При закрытии колостомы была выполнена первая реконструкция промежности. В дальнейшем у пациентки сохранялось недержание кала, периодическое недержание мочи, произошла облитерация аппендикостомы. В возрасте 15 лет в связи с недержанием кала была выполнена повторная промежностная реконструкция - промежностная проктопластика с протезированием пуборектальной мышцы искусственным трансплантатом «Урослинг» и пластика промежности. После проведенной операции функция аноректальной зоны оставалась неудовлетворительной, адекватное опорожнение было возможно только на фоне применения клизмы. Без применения клизмы или слабительных отмечались длительные запоры, на фоне которых возникало повышенное газообразование. При незначительном размягчении каловых масс сопровождалось недержанием газов и порций каловых масс, постоянное каломазание. Пациентка обратился в Ильинскую больницу для решения вопроса о возможности восстановления половой функции. На момент обследования в клинике у пациентки имелась облитерация правого влагалища, внесфинктерное низведение прямой кишки, недержание кала, остаточная культя правого мочеточника после нефроуретерэктомии, нейрогенная дисфункция мочевого пузыря, состояние после энтероцистопластики цистоаппендикоцистостомии (облитерация аппендикостомы), состояние после оперативной коррекции гипоплазии нижней челюсти с ограничением ее выведения.
Учитывая основной запрос на восстановление половой функции, было принято решение о проведении реконструктивной операции с устранением всех компонентов порока развития, формирующих основные жалобы. Операция была разделена на два этапа: первым этапом выполнена лапароскопическая резекция культи правого мочеточника, видеоассистированное выведение защитной колостомы, заднесагиттальная перинеотомия с реконструкцией влагалища, ренизведением толстой кишки. Вторым этапом через 3 месяца была выполнена лабиопластика, гистероскопия с раздельным выскабливанием обеих маток, правосторонний лапароскопический сальпингоовариолизис с разделением адгезивных сращений малого таза и наложение межкишечного анастомоза. Лапароскопический этап был дополнен операцией по патентуемому способу. Под общей комбинированной анестезией с эндотрахеальным наркозом и эпидуральной аналгезией в положении на спине с разведенными ногами сначала был выполнен промежностный этап. По завершении промежностного этапа пациент переведен в положение на спине выполнена открытая лапароскопия, тупым способом в эпигастральной области справа от средней линии установлен 5 мм троакар. Наложен карбоксиперитонеум под давлением 12 mmHg, поток 6 л/мин. Под контролем оптики выполнена постановка дополнительных троакаров в правом подреберье 10 мм для оптики и в правой подвздошной области по старому рубцу 5 мм для манипулятора. Выполнена постепенное рассечение спаек между правым яичником, правой маточной трубой и правой половины матки.
Затем выполнена мобилизация купола слепой кишки из сращений, визуализирован илеоцекальный угол, аппендикс на слепой кишки отсутствует, общая брыжейка фиксирована в проекции дна мочевого пузыря (результат после цистоаппендикостомы по Митрофанову). Учитывая интраоперационную картину решено выполнить моделирование неоаппендикостомы из передней стенки восходящей ободочной кишки. Определен питающий сосуд, наложены держалки на переднюю стенку восходящей кишки: одна на проекцию слепого конца, вторая возле питающего сосуда. Выполнена смена 5 мм троакара в правой подвздошной области на 12 мм, через него заведен линейный сшивающий аппарат с кассетой 65 мм. При помощи сшивающего аппарата часть стенки между держалками отжата, прошита отсечена. Сшивающий аппарат удален. Сформированный неоаппендикс переведен в медиальную сторону, для формирования манжеты в области его основания и герметизации аппаратного шва наложен серо-серозный непрерывный шов монофиламентной биодеградируемой нитью диаметром 4/0. По нижнемедиальной стенке пупка выполнен треугольный разрез, через него при помощи зажима сформирован туннель в подбрюшинном пространстве, зажимом захвачены лигатуры на неоаппендиксе, конец последнего выведен на кожу. Вскрыт просвет неоаппендикса, наложены по окружности слизисто-кожные швы монофиламентной биодеградируемой нитью диаметром 4/0. Дополнительно выполнена фиксация восходящей ободочной кишки к передней брюшной стенке тремя узловыми швами полифиламентной небиодеградируемой нитью диаметром 2/0. Узлы сформированы экстракорпорально. Брюшная полость санирована, выполнена десуффляция. Троакарные раны ушиты послойно. Завершающим этапом выполнено наложение десцендо-сигмоанастомоза и иссечение келоидного рубца после параректальной лапаротомии. Операция прошла спокойно, после операции пробуждение на столе, переведена в ОРИТ. За время наблюдения в ОРИТ состояние с положительной динамикой, на фоне эпидуральной аналгезии болевой синдром не отмечался. По стабилизации состояния переведена в палату стационара на 1 п/о сутки. Самостоятельный стул получен на 2 п/о сутки. По восстановлении пассажа по кишечнику возобновлена энтеральная нагрузка щадящей диетой. Эпидуральный катетер удален через 48 часов после операции, уретральный катетер удален на 3 п/о суток, после удаления уретрального катетера мочилась самостоятельно, дизурии не отмечено. Также на 3 п/о сутки начато антеградное промывание толстой кишки, промывание эффективное без эпизодов каломазания в течение суток. Осложнений в послеоперационном периоде не отмечено, болевого синдрома не было, воспалительных изменений по анализам крови не выявлено. ЦВК и ПВК удалены на 3 п/о сутки. Для обеспечения адекватного опорожнения мочевого пузыря пациентка была обучена чистой периодической катетеризации. Также она была обучена выполнению антеградного промывания толстой кишки, после чего выписана на амбулаторный" этап лечения.
При наблюдении в катамнезе через 2 недели катетер из аппендикостомы был заменен, в течение месяца, катетер менялся раз в 2-3 дня, но находился в аппендикостоме постоянно. Затем катетер устанавливался только для проведения антеградного промывания. На этом фоне эпизодов каломазания и недержания кала или газов не отмечено.
Таким образом, патентуемый способ обладает следующими преимуществами: формирование неоаппендикостомы выполняется лапароскопическим способом, что позволяет сократить время операции, оценивать внутрибрюшинную синтопию органов максимально анатомично и функционально выгодно выполнять все компоненты операции. Также эта операция может быть выполнена симультанно с другими лапароскопическими вмешательствами. Предложенный вариант маркировки является воспроизводимым вне зависимости от опыта и пространственного ощущения хирурга. Используя лапароскопический инструмент и понятные анатомические ориентиры формирование лоскута и неоаппендикса возможно без значимых рисков ошибиться с пропорциями. Таким образом, предложенная методика позволяет наложить континентную аппендикостому из лапароскопического доступа с минимальными интраоперационными и послеоперационными рисками, даже при утраченном аппендикулярном отростке. Наш опыт позволяет говорить о том, что, применяя предложенные хирургические маневры, данная операция может быть выполнена у пациентов любого возраста.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ вагинопластики при аплазии влагалища у девочек | 2022 |
|
RU2778831C1 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОГО ЛЕЧЕНИЯ ПРОТЯЖЕННОЙ СТРИКТУРЫ ВЕРХНЕЙ ТРЕТИ МОЧЕТОЧНИКА С ФОРМИРОВАНИЕМ ИЛЕОКАЛИКОАНАСТОМОЗА | 2019 |
|
RU2724022C1 |
| Способ формирования интракорпорального лапароскопического термино-терминального инвагинационного илеотрансверзоанастомоза | 2018 |
|
RU2689870C1 |
| СПОСОБ РОБОТ-АССИСТИРОВАННОЙ РАДИКАЛЬНОЙ ЦИСТЭКТОМИИ У БОЛЬНЫХ С РАКОМ МОЧЕВОГО ПУЗЫРЯ | 2019 |
|
RU2718279C1 |
| Способ извлечения препарата толстой кишки через естественные отверстия организма человека | 2023 |
|
RU2814386C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО НЕРЕЗЕКТАБЕЛЬНОГО РАКА ТОЛСТОЙ КИШКИ | 2010 |
|
RU2445016C2 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОГО ИНТРАКОРПОРАЛЬНОГО РУЧНОГО ГАСТРОЭНТЕРОАНАСТОМОЗА | 2016 |
|
RU2645116C2 |
| СПОСОБ ФОРМИРОВАНИЯ КОМПРЕССИОННОГО АНТИРЕФЛЮКСНОГО МОЧЕТОЧНИКОВО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА НА ДРЕНАЖЕ | 2009 |
|
RU2392882C1 |
| СПОСОБ EN-BLOC РОБОТ-АССИСТИРОВАННОЙ РАДИКАЛЬНОЙ ЦИСТЭКТОМИИ У ПАЦИЕНТОВ С РАКОМ МОЧЕВОГО ПУЗЫРЯ | 2024 |
|
RU2825063C1 |
| СПОСОБ ЭКСПОЗИЦИИ ЧЕРВЕОБРАЗНОГО ОТРОСТКА ПРИ ЛАПАРОСКОПИЧЕСКОЙ АППЕНДЭКТОМИИ ЧЕРЕЗ МОНОДОСТУП | 2010 |
|
RU2427335C1 |
Изобретение относится к медицине, а именно к абдоминальной хирургии и колопроктологии, и может быть использовано для формирования неоаппендикостомы с антирефлюксным клапаном. Формируют неоаппендикостому из стенки толстой кишки при помощи линейного сшивающего аппарата с формированием лоскута на питающем сосуде и наложением серо-серозных швов между основанием неоаппендикса и складкой стенки несущей кишки с формированием антирефлюксного клапана. Оперативное вмешательство осуществляют лапароскопически. Определяют питающий сосуд на брыжеечной стороне восходящей oбодочной кишки. Накладывают и принимают первый шов-держалку как внешний ориентир основания неоаппендикса. На уровне края диссектора накладывают второй шов-держалку и принимают его как внешний ориентир слепого конца неоаппендикса. Укладывают с помощью швов-держалок восходящую ободочную кишку вниз до осуществления разведения бранш сшивающего аппарата в брюшной полости. Выводят над краем кассеты сшивающего аппарата дупликатуру стенки кишки шириной, равной диаметру диссектора. Удаляют первый шов-держалку с основания неоаппендикса, за второй шов-держалку сформированный неоаппендикс переводят в медиальную сторону. По нижнебоковой стенке пупочной ямки выполняют треугольный кожный разрез. Формируют туннель для выведения неоаппендикса. Вскрывают просвет неоаппендикса в месте слепого конца. Способ позволяет снизить объем оперативного вмешательства и риски интра- и послеоперационных осложнений при формировании неоаппендикостомы. 8 ил., 1 пр.
Способ формирования неоаппендикостомы с антирефлюксным клапаном, включающий формирование лоскута из стенки толстой кишки на питающем сосуде при помощи линейного сшивающего аппарата и наложение серо-серозных швов между основанием неоаппендикса и складкой стенки несущей кишки с формированием антирефлюксного клапана, отличающийся тем, что оперативное вмешательство осуществляют лапароскопически, устанавливают троакар для оптики в правом подреберье, троакары для манипуляторов - в эпигастральной области справа от средней линии и в правой подвздошной области, определяют питающий сосуд на брыжеечной стороне восходящей ободочной кишки, возле питающего сосуда накладывают первый шов-держалку на глубину мышечного слоя, который проводят через переднюю брюшную стенку в проекции над питающим сосудом, и принимают первый шов-держалку как внешний ориентир основания неоаппендикса; определяют длину будущего неоаппендикса как ширину прямой мышцы живота по линии, направленной от внутреннего края пупочной ямки по направлению к ости подвздошной кости; наносят маркерную метку, соответствующую полученному расстоянию, на рабочий конец лапароскопического диссектора, в брюшной полости прикладывают метку диссектора к первому шву-держалке поперек восходящей ободочной кишки, на уровне края диссектора накладывают второй шов-держалку на глубину мышечного слоя, который также проводят через переднюю брюшную стенку в проекции над прошитым участком кишки, и принимают второй шов-держалку как внешний ориентир слепого конца неоаппендикса; петли швов-держалок формируют длиной, достаточной для свободного смещения восходящей кишки на всю высоту брюшной полости; укладывают с помощью швов-держалок восходящую ободочную кишку вниз до осуществления разведения бранш сшивающего аппарата в брюшной полости, в раскрытые бранши заводят швы-держалки и подтягивают их таким образом, что помещают стенку кишки между браншами сшивающего аппарата, при этом выводят над краем кассеты сшивающего аппарата дупликатуру стенки кишки шириной, равной диаметру диссектора; выделенную часть стенки отжимают, прошивают и отсекают с помощью аппарата, удаляют первый шов-держалку с основания неоаппендикса, за второй шов-держалку сформированный неоаппендикс переводят в медиальную сторону, открывая доступ к аппаратному шву, после формирования антирефлюксного клапана герметизируют стенку несущей кишки, продлевая серо-серозный шов над всем аппаратным швом; по нижнебоковой или нижней стенке пупочной ямки выполняют треугольный кожный разрез; при помощи зажима формируют туннель для выведения неоаппендикса, при этом зажим заводят под медиальный край прямой мышцы живота в предбрюшинную клетчатку, избегая попадания в толщу мышцы, проводят зажим до середины ширины прямой мышцы живота, на этом уровне тупым способом перфорируют париетальную брюшину, захватывают концы второго шва-держалки и выводят слепой конец неоаппендикса через сформированный канал в разрез в пупочной ямке, вскрывают просвет неоаппендикса в месте слепого конца и накладывают по окружности слизисто-кожные швы без эвагинации слизистой, через неоаппендикостому в толстую кишку заводят силиконовый катетер с его накожной фиксацией, затем выполняют экстракорпоральную фиксацию восходящей ободочной кишки в области несущей неоаппендикостому части тремя узловыми швами к передней брюшной стенке.
| OSTERTAG-HILL C.A | |||
| et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Pediatr Surg Int | |||
| Двухосный автомобиль | 1924 |
|
SU2024A1 |
| СПОСОБ ЛЕЧЕНИЯ ОБТУРАЦИОННОЙ ТОЛСТОКИШЕЧНОЙ НЕПРОХОДИМОСТИ | 2011 |
|
RU2452400C1 |
| СПОСОБ ДЕКОМПРЕССИИ ТОЛСТОЙ КИШКИ ПРИ ОБТУРАЦИОННОЙ НЕПРОХОДИМОСТИ | 2013 |
|
RU2549489C1 |
| Паровозная машина с изменяемым ходом поршня | 1928 |
|
SU23045A1 |
| CN 204618341 U, 09.09.2015 | |||
| CN 212439533 U, 02.02.2021 | |||
| ШУГИНА Ю.В | |||
| и др | |||
| Хирургическая коррекция нарушений кишечного транзита | |||
Авторы
Даты
2025-05-12—Публикация
2024-06-18—Подача