Область техники
В общем, настоящее изобретение относится к способу образования in situ из пипеколиновой кислоты соединений, имеющих приведенную в настоящем документе формулу (V), в частности, к образованию следующих охлаждающих средств: 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-она (включая (2S)-2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин- 1-ил)бутан-1-он или рацемическую смесь), 2-(метилтио)-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)пропан-1-она, 2-метил-2-(метилтио)-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)пропан-1-она и 2,2-диметил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бут-3-ен-1-она. Настоящее изобретение также относится к соединениям, получаемым рассмотренными способами, и/или к соединениям, которые могут быть получены рассмотренными способами, к применению указанных соединений в составе ароматических композиций, например, в качестве охлаждающих средств ароматических композиций, к применению указанных ароматических композиций в потребительских товарах, к ароматическим композициям, включающим указанные соединения, и к потребительским товарам, включающим указанные ароматические композиции.
Уровень техники
Пипеколиновую кислоту можно использовать в качестве исходного материала для получения различных соединений. В частности, пипеколиновую кислоту можно использовать в качестве исходного материала для получения соединений, имеющих формулу (V), приведенную в настоящем документе. Однако эти способы обычно включают ряд стадий выделения и очистки промежуточных соединений перед проведением последующей стадии. Поэтому желательно улучшить имеющиеся способы или разработать альтернативные способы, в которых, например, извлечение и очистка промежуточных соединений не являются обязательными.
Краткое описание изобретения Первый аспект настоящего изобретения относится к способу образования in situ из пипеколиновой кислоты соединения, имеющего формулу (V), где способ in situ выполняют в присутствии растворителя, и растворитель представляет собой органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С, воду или смесь указанных растворителей, включающему:
(a) осуществление реакции пипеколиновой кислоты с хлоридом кислоты, имеющим формулу (Ia), в присутствии основания, или реакции пипеколиновой кислоты с ангидридом кислоты, имеющим формулу (Ib), возможно в присутствии основания, приводящей к образованию соединения, имеющего формулу (II),
(b) осуществление реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV), и
(c) осуществление реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V),
где структуры соединений, имеющих формулу (Ia), (Ib), (II), (III), (IV) и (V), приведены ниже:
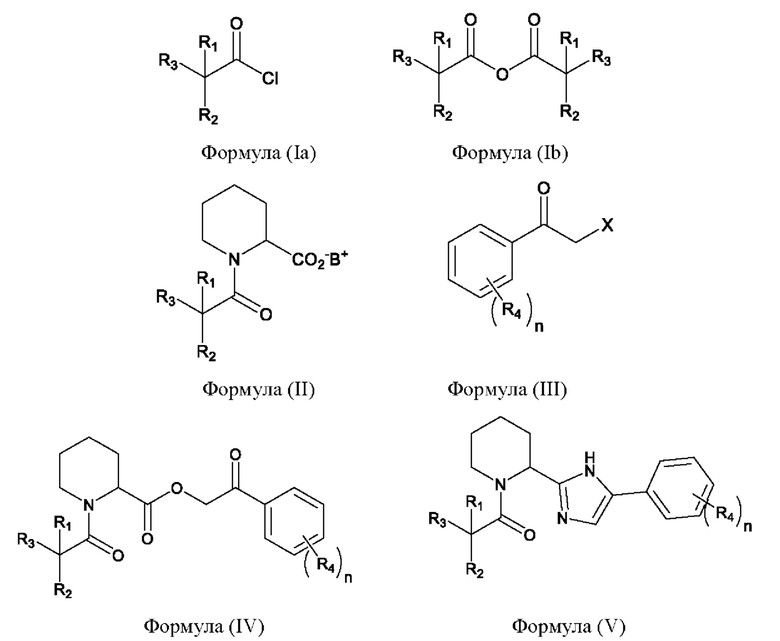
где
R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, образуют углеводородную группу, возможно включающую до 3 гетероатомов, независимо выбранных из О, S, N и F;
фенильная группа соединений, имеющих формулы (III), (IV) и (V), имеет n заместителей R4, где n равен нулю, единице, двум, трем, четырем или пяти;
каждый R4 независимо выбран из галогена, цианогруппы, нитрогруппы, C1-С6 алкила, возможно включающего до 5 атомов галогена, С2-С6 алкенила, C1-С6 алкоксигруппы, возможно включающей до 3 атомов галогена, С1-С3-алкокси-С1-С3-алкила и С3-С7 циклоалкила;
В+ представляет собой катион, предоставляемый основанием, и
X представляет собой галоген.
Второй аспект настоящего изобретения относится к соединению, имеющему формулу (V), получаемому и/или которое может быть получено способом согласно первому аспекту настоящего изобретения, включая любые его воплощения.
Третий аспект настоящего изобретения относится к применению соединения, имеющего формулу (V), согласно второму аспекту настоящего изобретения, включая любые его воплощения, в составе ароматической композиции. Например, соединение, имеющее формулу (V), можно применять в качестве охлаждающего средства ароматической композиции.
Четвертый аспект настоящего изобретения относится к ароматической композиции, включающей соединение, имеющее формулу (V), согласно второму аспекту настоящего изобретения, включая любые его воплощения.
Пятый аспект настоящего изобретения относится к потребительскому товару, включающему ароматическую композицию согласно четвертому аспекту настоящего изобретения, включая любые его воплощения.
Шестой аспект настоящего изобретения относится к применению ароматической композиции согласно четвертому аспекту настоящего изобретения, включая любые его воплощения, в потребительском товаре.
Некоторые воплощения настоящего изобретения могут обеспечивать одно или более из следующих преимуществ:
• способ получения in situ из пипеколиновой кислоты соединения, имеющего формулу (V);
• уменьшение количества стадий очистки и извлечения;
• применение одного и того же растворителя на протяжении всего способа;
• по окончании реакции растворитель может быть подвергнут рециркуляции;
• хиральность углеводородной группы, образованной радикалами R1, R2 и R3, остается неизменной в течение всей реакции;
• хлорангидрид и соединения, имеющие формулу (III), можно получать в лаборатории по месту синтеза и использовать неочищенными и в растворе, что снижает действие реагентов-лакриматоров на окружение;
• протекание такой побочной реакции, как гидролиз хлорангидрида, в меньшей степени;
• более мягкие условия реакции;
• снижение количества или числа требуемых реагентов (например, карбоновая кислота подвергается депротонированию на первой реакционной стадии, и, таким образом, на вторую реакционную стадию не нужно дополнительно добавлять основание);
• снижение количества источника иона аммония, требуемого для третьей реакционной стадии (например, благодаря добавлению порциями и/или определенной температуре реакции и/или удалению воды);
• приемлемый выход;
• приемлемая селективность.
Подробное изложение, примеры и предпочтительные варианты, приведенные при описании одного или более конкретных рассмотренных аспектов настоящего изобретения, дополнительно описаны в настоящей документе и равным образом применимы ко всем аспектам настоящего изобретения. Если не указано иное или иное не следует из контекста, то настоящее изобретение включает любую комбинацию всех возможных вариантов воплощений, примеров и предпочтительных воплощений, описанных в настоящей работе.
Подробное описание изобретения
Настоящее изобретение основано на неожиданном обнаружении того факта, что соединения, имеющие формулу (V), могут быть образованы из пипеколиновой кислоты in situ, и затем обработаны и извлечены.
Таким образом, изобретение относится к способу образования in situ из пипеколиновой кислоты соединения, имеющего формулу (V), где способ in situ выполняют в присутствии растворителя, и растворитель представляет собой органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С, воду или смесь указанных растворителей, где способ включает:
(а) осуществление реакции пипеколиновой кислоты с хлоридом кислоты, имеющим формулу (Ia), в присутствии основания, или реакции пипеколиновой кислоты с ангидридом кислоты, имеющим формулу (Ib), возможно в присутствии основания, приводящей к образованию соединения, имеющего формулу (II), 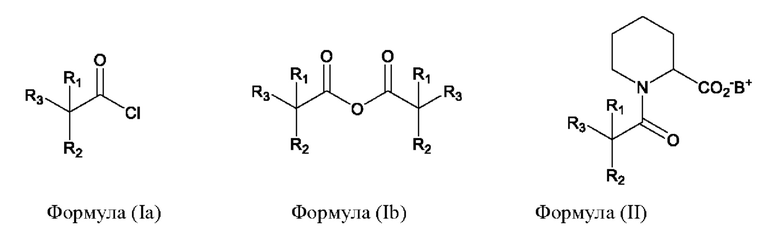
(b) осуществление реакции соединения, имеющего формулу (II) с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV),
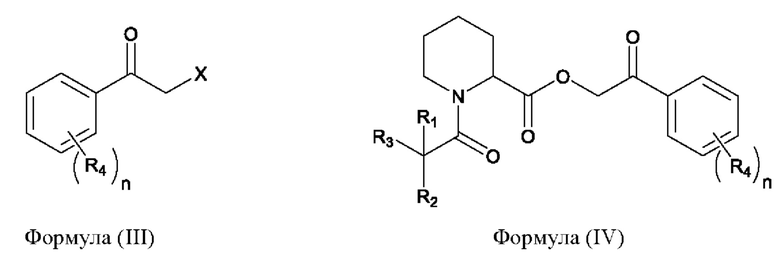
(c) осуществление реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V),
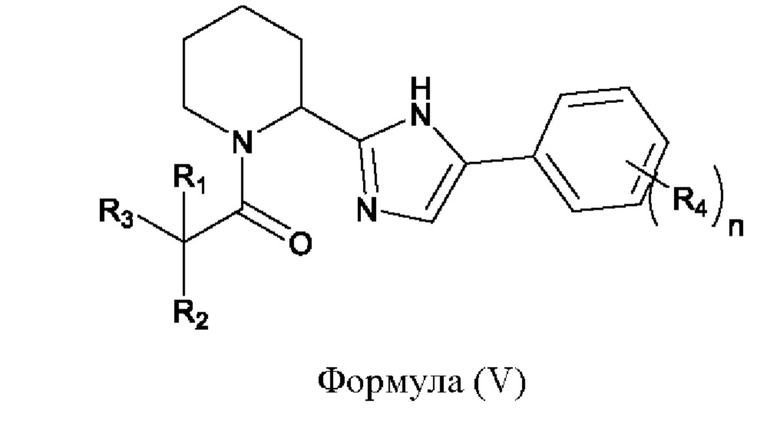
где
R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, образуют углеводородную группу, возможно включающую до 3 гетероатомов, независимо выбранных из О, S, N и F;
фенильная группа соединений, имеющих формулы (III), (IV) и (V), имеет n заместителей R4, где n равен нулю, единице, двум, трем, четырем или пяти;
каждый R4 независимо выбран из галогена, цианогруппы, нитргруппыо, C1-С6 алкила, возможно включающего до 5 атомов галогена, С2-С6 алкенила, C1-С6 алкоксигруппы, возможно включающей до 3 атомов галогена, С1-С3-алкокси-С1-С3-алкила и С3-С7 циклоалкила;
В+ представляет собой катион, предоставляемый основанием, и
X представляет собой галоген.
В настоящем описании фраза «образование in situ из пипеколиновой кислоты соединения, имеющего формулу (V)» относится к способу, в котором вся реакция протекает в одной реакционной смеси, и любые образующиеся промежуточные соединения (например, соединения, имеющие формулы (II) и (IV)) не выделяют или не очищают перед проведением стадий, выполняемых далее для получения готового продукта (т.е. соединения, имеющего формулу (V)). Другими словами, превращение пипеколиновой кислоты в соединение, имеющее формулу (II), превращение соединения, имеющего формулу (II), в соединение, имеющее формулу (IV), и превращение соединения, имеющего формулу (IV), в соединение, имеющее формулу (V), происходит в одной и той же реакционной смеси, без извлечения или очистки соединения, имеющего формулу (II), или соединения, имеющего формулу (IV). Такое образование in situ может происходить, например, в проточном реакторе или реакторе периодического действия.
Несмотря на то, что описанные в настоящей документе способы являются способами образования in situ из пипеколиновой кислоты соединения, имеющего формулу (V), следует понимать, что их выполнение не обязательно для получения соединения, имеющего формулу (V), и для получения соединения, имеющего формулу (V), можно выполнять одну или более стадий извлечения или очистки после каждой из стадий 1, 2 и 3, описанных в настоящем документе.
Превращение соединения, имеющего формулу (II), в соединение, имеющее формулу (IV), может быть произведено одновременно с превращением пипеколиновой кислоты в соединение, имеющее формулу (II), или после него.
Превращение соединения, имеющего формулу (IV), в соединение, имеющее формулу (V), может быть произведено одновременно с превращением соединения, имеющего формулу (II), в соединение, имеющее формулу (IV) или после него.
Определение «одновременно с» означает, что реагенты на каждой стадии превращения добавляют в реакционную смесь одновременно, так что оба реакционных превращения протекают в реакционной смеси в одно и то же время.
Определение «после» означает, что по меньшей мере некоторые из реагентов (например, хлорный ангидрид, имеющий формулу (Ia), ангидрид кислоты, имеющий формулу (Ib), соединение, имеющее формулу (III), и/или источник иона аммония) для следующей стадии реакции добавляют в реакционную смесь после частичного или полного завершения первой стадии реакции. Например, соединение, имеющее формулу (III), можно добавлять в реакционную смесь после полного или неполного превращения пипеколиновой кислоты в соединение, имеющее формулу (II). Например, источник иона аммония можно добавлять в реакционную смесь после полного или неполного превращения соединения, имеющего формулу (II), в соединение, имеющее формулу (IV). Если предыдущее превращение было неполным, то добавление реагентов для проведения последующей стадии может приводить к тому, что в течение некоторого времени оба реакционных превращения протекают в реакционной смеси в одно и то же время. Однако в начале процесса имеется период времени, в течение которого предыдущее превращение протекает в отсутствие последующего превращения. Последующее превращение протекает в той же реакционной смеси, и поэтому извлечение или очистка промежуточных соединений не требуются, и таким образом, последующее превращение представляет собой реакцию in situ в соответствии с настоящим изобретением.
В альтернативном варианте способ образования in situ соединения, имеющего формулу (V), описанный выше, включает:
(a) осуществление реакции пипеколиновой кислоты с соединением, имеющим формулу (III), в присутствии основания, которая приводит к образованию соединения, имеющего формулу (VI),
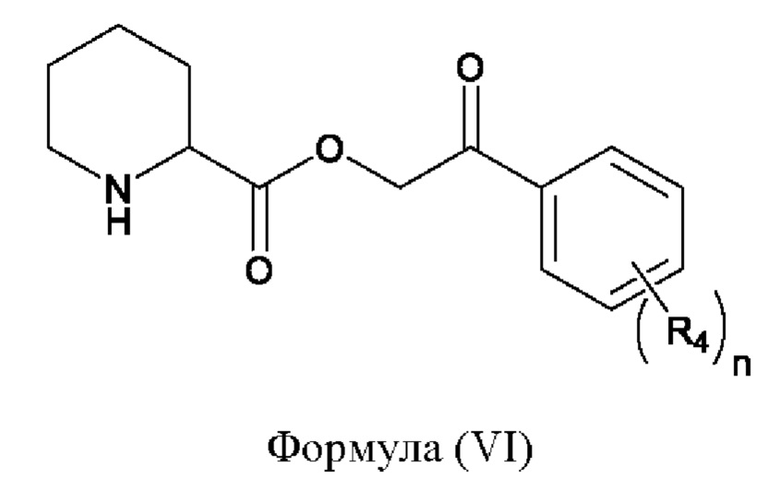
(b) осуществление реакции соединения, имеющего формулу (VI), с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящей к образованию соединения, имеющего формулу (IV), и
(c) осуществление реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V),
где структуры соединений, имеющих формулу (Ia), (Ib), (III), (IV) и (V) указаны выше.
В этом альтернативном способе реакционную стадию 3 с источником иона аммония можно необязательно проводить до осуществления реакции с хлорным ангидридом/ангидридом кислоты.
Однако при выполнении альтернативного способа пипеколиновая кислота должна быть селективно защищена защитной аминогруппой. Перед осуществлением последующей реакции с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), защитная группа должна быть удалена.
Описанный в настоящем документе способ in situ выполняют в присутствии растворителя, где растворитель представляет собой органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С, или растворитель представляет собой воду, или растворитель представляет собой смесь органического растворителя и воды. Другими словами, все стадии способа (включая все стадии 1, 2 и 3, описанные в настоящем документе) проводят в присутствии растворителя, который представляет собой органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С, или растворитель представляет собой воду, или растворитель представляет собой смесь органического растворителя и воды. Неожиданно было обнаружено, что выбор в качестве растворителя воды или органического растворителя с температурой кипения от приблизительно 50°С до приблизительно 160°С устраняет необходимость замены растворителя после каждой последующей стадии, что позволяет проводить весь способ в одной емкости как способ in situ. Применение в качестве растворителя воды или органического растворителя с температурой кипения от приблизительно 50°С до приблизительно 160°С также может способствовать уменьшению образования загрязняющих веществ и побочных продуктов. В некоторых воплощениях растворитель представляет собой органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С.
В некоторых воплощениях температура кипения органического растворителя больше или равна приблизительно 60°С, или больше или равна приблизительно 70°С, или больше или равна приблизительно 80°С, или больше или равна приблизительно 90°С, или больше или равна приблизительно 100°С, или больше или равна приблизительно 110°С.
В некоторых воплощениях температура кипения органического растворителя меньше или равна приблизительно 150°С, или меньше или равна приблизительно 140°С, или меньше или равна приблизительно 130°С, или меньше или равна приблизительно 120°С.
Например, температура кипения органического растворителя может составлять от приблизительно 60°С до приблизительно 150°С, или от приблизительно 70°С до приблизительно 120°С, или от приблизительно 80°С до приблизительно 140°С, или от приблизительно 90°С до приблизительно 130°С, или от приблизительно 100°С до приблизительно 120°С.
Одну или более стадий описанного в настоящем документе способа in situ (например, все стадии 1, 2 и 3, описанные в настоящем документе, или все стадии способа) могут быть проведены при температуре ниже температуры кипения растворителя, например, ниже температуры кипения органического растворителя, имеющего температуру кипения от приблизительно 50°С до приблизительно 160°С. В альтернативном варианте одну или более стадий описанного в настоящем документе способа in situ (например, все стадии 1, 2 и 3, описанные в настоящем документе, или все стадии способа) можно осуществлять посредством кипячения с обратным холодильником. Во время осуществления способа это может предотвращать испарение, приводящее к удалению растворителя из реакционной смеси.
Для предотвращения испарения растворителя из реакционной смеси при проведении реакции, одну или более стадий описанного в настоящем документе способа in situ (например, все стадии 1, 2 и 3, описанные в настоящем документе, или все стадии способа) можно осуществлять в запаянных трубках или в автоклаве. Это позволяет, например, использовать температуры, превышающие температуру кипения растворителя. Таким образом, можно использовать растворители, имеющие относительно низкие температуры кипения (например, МТБЭ).
Одну или более стадий описанного в настоящем документе способа in situ (например, все стадии 1, 2 и 3, описанные в настоящем документе, или все стадии способа) можно осуществлять при температуре ниже температуры разложения реагентов. Температура на всех стадиях способа может быть одинаковой или различной.
Например, может быть полезно подобрать растворитель (например, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С), который позволит проводить каждую стадию способа in situ при температуре, обеспечивающей максимальную скорость реакции, но достаточно низкой для предотвращения разложения реагентов.
Органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С может, например, представлять собой полярный или неполярный растворитель. Полярность растворителя может быть определена измерением диэлектрической постоянной растворителя (относительной проницаемости) при 0°С. Растворители, имеющие диэлектрическую постоянную менее 15, могут считаться неполярными растворителями. Растворители, имеющие диэлектрическую постоянную 15 или более, могут считаться полярными растворителями.
Органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С может, например, быть несмешиваемым с водой (т.е. смесь любых пропорций органического растворителя с температурой кипения от приблизительно 50°С до приблизительно 160°С с водой не может образовывать гомогенного раствора).
Органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С может, например, представлять собой ароматический растворитель или неароматический растворитель.
Ароматический растворитель может включать один или более гетероатомов, например, выбранных из азота, кислорода, серы и галогена, такого как фтор. Ароматический растворитель может, например, включать одну или более гетероароматических групп. Ароматический растворитель может, например, представлять собой ароматический растворитель, состоящий только из атомов углерода и водорода. Примерами ароматических растворителей, состоящих только из атомов углерода и водорода, являются алкилбензолы. Алкилбензольные растворители также являются примерами неполярных растворителей. Алкилбензольные растворители включают бензильную группу, в которой один или более атомов водорода бензольного цикла замещены алкильной группой. Каждая алкильная группа может, например, независимо включать от 1 до 5 атомов углерода, например, от 1 до 3 атомов углерода, например, 1 или 2 атома углерода. Примерами алкилбензольных растворителей являются толуол и ксилол. Примерами ароматических растворителей являются галогенобензольные (в которых в бензоле один или более атомов водорода замещены атомами галогена) растворители, такие как дихлорбензол.
Неароматический растворитель может включать один или более гетероатомов, например, выбранных из азота, кислорода, серы и галогена, такого как фтор. Неароматический растворитель может, например, включать одну или более неароматических гетероциклических групп. Примером неароматического растворителя, включающего гетероциклическую группу, является метилтетрагидрофуран, например, 2-метилтетрагидрофуран. Неароматический растворитель может, например, представлять собой простой эфир. Примером неароматического растворителя, представляющего собой простой эфир, является простой метил-трет-бутиловый эфир (МТБЭ). Неароматический растворитель может, например, представлять собой не ароматический растворитель, состоящий только из атомов углерода и водорода. Неароматический растворитель, состоящий только из атомов углерода и водорода, может, например, быть линейным (например, разветвленным или неразветвленным) или циклическим. Примером линейного неразветвленного не ароматического растворителя является гептан. Растворители-галогеноалканы (алканы, в которых один или более атомов водорода замещен атомом галогена), такие как дихлорметан, являются примерами неароматических растворителей. В частности, растворители-галогеноалканы можно использовать, например, если способ осуществляют в запаянной трубке или в автоклаве.
В некоторых воплощениях неароматический растворитель может включать один или более гетероатомов, выбранных из азота, кислорода и серы.
В частности, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С может представлять собой алкилбензольный растворитель. Например, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С может быть толуолом.
Стадия 1. Превращение пипеколиновой кислоты в соединение, имеющее формулу (II) Описанный в настоящем документе способ in situ может включать реакцию пипеколиновой кислоты с (a-i) хлорным ангидридом, имеющим формулу (Ia), в присутствии основания, или (a-ii) ангидридом кислоты, имеющим формулу (Ib), необязательно в присутствии основания, с образованием соединения, имеющего формулу (II). Например, описанный в настоящем документе способ in situ может включать реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), в присутствии основания, приводящую к образованию соединения, имеющего формулу (II).
Пипеколиновая кислота может быть получена промышленным способом. Она имеет следующую химическую структуру:
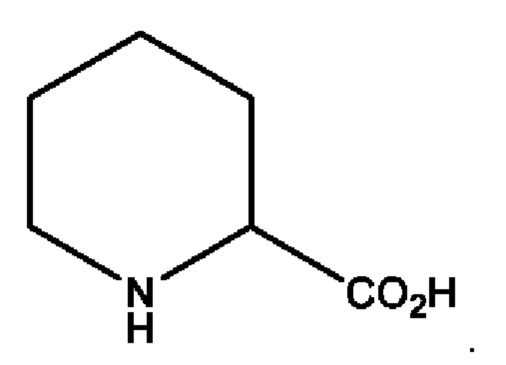
Хлорный ангидрид, имеющий формулу (Ia), имеет следующую химическую структуру:
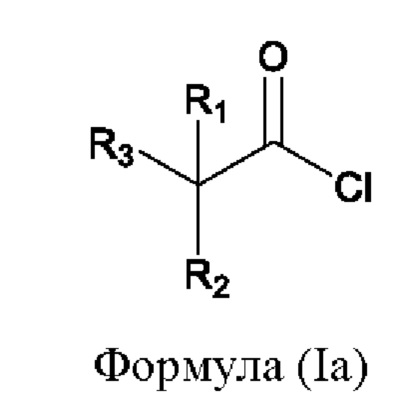
где R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, образуют углеводородную группу, необязательно включающую до 3 гетероатомов, независимо выбранных из О, S, N и F.
Хлорный ангидрид, имеющий формулу (Ia), может, например, быть получен промышленным способом или может, например, быть получен различными способами синтеза, такими как реакция карбоновой кислоты с тионилхлоридом (SOCl2), оксалилхлоридом (COCl2), трихлоридом фосфора (PCl3) или пентахлоридом фосфора (PCl5), или реакция тиомолочной кислоты с диметилсульфатом с последующим хлорированием, например, тионилхлоридом (SOCl2).
Ангидрид кислоты, имеющий формулу (Ib), имеет следующую химическую структуру:
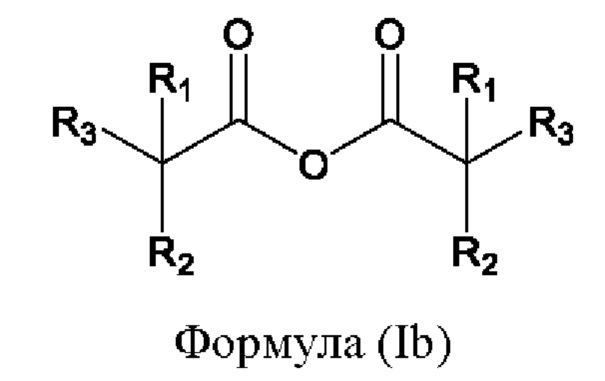
где определения R1, R2 и R3 приведены при описании хлорного ангидрида, имеющего формулу (Ia).
Ангидрид кислоты может, например, быть получен из промышленным способом или может, например, быть получен различными способами синтеза, такими как реакция хлорного ангидрида, имеющего формулу (Ia), с соответствующей карбоновой кислотой или реакция соответствующей карбоновой кислоты с уксусным ангидридом.
Термин «углеводородная группа, возможно включающая до 3 гетероатомов, выбранных из О, S, N и F» означает группу, включающую только атомы углерода и водорода и возможно атомы кислорода, серы, азота и фтора. Суммарное максимальное количество атомов кислорода, серы, азота и фтора составляет три.
R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, могут, например, образовывать углеводородную группу, возможно включающую до 3 гетероатомов, выбранных из О, S и F. R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, могут, например, образовывать углеводородную группу, необязательно включающую до 3 гетероатомов, которые представляют собой S.
R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, могут, например, образовывать углеводородную группу, не содержащую гетероатомов (т.е. образовывать углеводородную группу, включающую только атомы углерода и водорода).
R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, могут, например, образовывать углеводородную группу, включающую атомы углерода и водорода и один или два гетероатома, независимо выбранные из О, S, N и F. R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, могут, например, образовывать углеводородную группу, включающую атомы углерода и водорода и один или два гетероатома, независимо выбранные из О, S и F.
Атом углерода, к которому присоединены R1, R2 и R3, может, например, представлять собой хиральный центр. В некоторых воплощениях атом углерода, к которому присоединены R1, R2 и R3, представляет собой хиральный центр, и хиральность соединения не меняется на протяжении всей реакции.
«Углеводородная группа, возможно включающая до 3 гетероатомов, выбранных из О, S, N и F» может, например, включать от 1 до 15 атомов углерода. Например, «углеводородная группа, возможно включающая до 3 гетероатомов, выбранных из О, S, N и F» может включать от 2 до 15 атомов углерода. Например, «углеводородная группа, возможно включающая до 3 гетероатомов, выбранных из О, S, N и F» может включать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 атомов углерода.
R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, могут, например, образовывать углеводородную группу, выбранную из: 3-тиабут-2-ила, 2-метил-3-тиабут-2-ила, 3-тиапент-2-ила, 4-тиапент-2-ила, 2-тиапроп-1-ила, 2-метил-3-тиапент-2-ила, 3-оксо-3-тиабут-2-ила, 3-оксо-2-метил-3-тиабут-2-ила, 3-оксо-3-тиапент-2-ила, 4-оксо-4-тиапент-2-ила, 2-оксо-2-тиапроп-1-ила, 3-оксо-2-метил-3-тиапент-2-ила, бут-2-ила, пент-2-ила, бут-3-ен-2-ила, пент-3-ен-2-ила, бут-2-ен-2-ила, пент-2-ен-2-ила, бут-1-ен-2-ила, пент-1-ен-2-ила, 2-метилбут-2-ила, 2-метилпент-2-ила, 2-метилбут-3-ен-2-ила, 3-метилбут-2-ила, 3-метилбут-3-ен-2-ила, 3-метилбут-2-ен-2-ила, 2,3-диметилбут-2-ила, 2,3-диметилпент-2-ила, 2,3-диметилбут-3-ен-2-ила, 2,3-диметилпент-3-ен-2-ила, 2-метилпент-3-ен-2-ила, проп-2-ила, проп-1-ила, этила, циклопропила, 1,1-диметилциклопроп-2-ила, 1-метилциклопроп-2-ила, 1-метилциклопроп-1-ила, 3-тиагекс-5-ен-2-ила, 2-метил-3-тиагекс-5-ен-2-ила, 1-меркаптоэт-1-ила, 2-меркаптопроп-2-ила, 3,3,3-трифторпроп-2-ила, 2-метил-3,3,3-трифторпроп-2-ила, 1-(2-фурил)эт-1-ила, 1-(5-метилфур-2-ил)эт-1-ила, 2-(2-фурил)проп-2-ила, 1-(3-фурил)эт-1-ила, 1-(5-метилфур-3-ил)эт-1-ила, 2-(3-фурил)проп-2-ила, 1-(2-тетрагидрофурил)эт-1-ила, 2-(2-тетрагидрофурил)проп-2-ила, 1-(3-тетрагидрофурил)эт-1-ила, 2-(3-тетрагидрофурил)проп-2-ила, 1-циклопропилэт-1-ила, 2-циклопропилпроп-2-ила, 1-циклобутилэт-1-ила, 2-циклобутилпроп-2-ила, циклобутила, циклопентила, пент-2-ен-3-ила, 1-метоксипроп-1-ила, 1-метоксиэт-1-ила, 1,1,1-трифторбут-3-ила, 3-тиациклобут-1-ила, 1-(N-метиламино)эт-1-ила и 1-(N,N-диметиламино)эт-1-ила.
Например, каждый из R1, R2 и R3 может быть независимо выбран из водорода, алкила (включая линейные алкильные группы (неразветвленные и разветвленные) и циклоалкильные группы), алкенила, алкокси, алкил-С(О)-, алкил-S-, алкил-S-алкила (например, алкил-S-СН2-), алкенил-S-, алкил-S(O)-, алкил-S(O)2-, алкенил-S(O)-, алкенил-S(O)2-, -SH, CF3S-, фурила (например, 2-фурила или 3-фурила), возможно замещенного алкилом (например, фурила, возможно замещенного метилом) и фторалкила.
Например, каждый из R1, R2 и R3 может быть независимо выбран из водорода, линейного C1-C4-алкила, С3-С4-циклоалкила, С2-С5 алкенила, включающего одну или две двойные связи, C1-С3-алкокси, С1-С4-алкил-С(O)-, С1-С4-алкил-S-, С1-С4-алкил-S-С1-С4-алкила (например, С1-С4-алкил-S-СН2-), С1-С4-алкенил-8, С1-С4-алкил-S(O)-, С1-С4-алкил-S(O)2-, С1-С4-алкенил-S(O)-, С1-С4-алкенил-S(O)2-, -SH, CF3S-, фурила (например, 2-фурила или 3-фурила), необязательно замещенного С1-С4-алкилом (например, фурила, возможно замещенного метилом), и C1-С6-фтор-алкила (например, дифторметила, трифторметила, 2,2,2-трифторэтила или дифторэтила).
R1 может, например, быть выбран из водорода и С1-С4-алкила. Например, R1 может быть выбран из водорода и метила.
R2 может, например, быть выбран из водорода, С1-С4-алкила и С2-С5-алкенила, включающего одну или две двойные связи. Например, R2 может быть выбран из водорода, C1-С2-алкила и С2-С3-алкенила. Например, R2 может быть метилом.
R3 может, например, быть выбран из С1-С4 алкила, С2-С5 алкенила, включающего одну или две двойные связи, C1-С3-алкокси, C1-С4-алкил-С(O)-, C1-С4-алкил-S-, С1-С4-алкил-SCH2-, С1-С4-алкенил-S-, С1-С4-алкил-S(O)-, С1-С4-алкил-S(O)2-, С1-С4-алкенил-S(O)-, С1-С4-алкенил-S(O)2-, -SH, CF3S-, циклопропила, циклобутила, фурила (например, 2-фурила или 3-фурила), необязательно замещенного метилом, и C1-C6-фторалкила (например, дифторметила, трифторметила, 2,2,2-трифторэтила или дифторэтила). Например, R3 может быть выбран из С1-С4 алкила, С2-С5 алкенила, включающего одну или две двойные связи, и С1-С4-алкил-S-. Например, R3 может быть выбран из С1-С2 алкила, С2-С3 алкенила, включающего одну двойную связь, и С1-С2-алкил-S-. Например, R3 может быть выбран из этила, этенила и -SCH3.
Например, R1 может быть выбран из водорода и С1-С4-алкила, R2 может быть выбран из водорода, C1-С4-алкила и С2-С5-алкенила, включающего одну или две двойные связи, и R3 может быть выбран из С1-С4 алкила, С2-С5 алкенила, включающего одну или две двойные связи, C1-С3-алкокси, С1-С4-алкил-С(O)-, С1-С4-алкил-S-, С1-С4-алкил-SCH2-, С1-С4-алкенил-S-, С1-С4-алкил-S(O)-, С1-С4-алкил-S(O)2-, С1-С4-алкенил-S(O)-, С1-С4-алкенил-S(O)2-, -SH, CF3S-, циклопропила, циклобутила, фурила (например, 2-фурила или 3-фурила), необязательно замещенного метилом, и C1-C6-фторалкила (например, дифторметила, трифторметила, 2,2,2-трифторэтила или дифторэтила).
Например, R1 может быть выбран из водорода и метила, R2 может быть выбран из водорода, C1-С2-алкила и С2-С3-алкенила, и R3 может быть выбран из С1-С4 алкила, С2-С5 алкенила, включающего одну или две двойные связи, C1-С3-алкокси, С1-С4-алкил-С(O)-, С1-С4-алкил-S-, С1-С4-алкил-SCH2-, С1-С4-алкенил-S-, С1-С4-алкил-S(O)-, С1-С4-алкил-S(O)2-, С1-С4-алкенил-S(O)-, С1-С4-алкенил-S(O)2-, -SH, CF3S-, циклопропила, циклобутила, фурила (например, 2-фурила или 3-фурила), необязательно замещенного метилом, и C1-С6-фторалкила (например, дифторметила, трифторметила, 2,2,2-трифторэтила или дифторэтила).
Например, R1 может быть выбран из водорода и метила, R2 может представлять собой С1-С2-алкил, и R3 может быть выбран из С1-С4 алкила, С2-С5 алкенила, включающего одну или две двойные связи, и С1-С4-алкил-S-
Например, R1 может быть выбран из водорода и метила, R2 может представлять собой метил, и R3 может представлять собой этил, этенил или SCH3.
Хлорный ангидрид, имеющий формулу (Ia), или ангидрид кислоты, имеющий формулу (Ib) может, например, быть добавлен в реакционную смесь как таковой или в виде раствора в растворителе, например, в виде раствора в органическом растворителе, имеющем температуру кипения от приблизительно 50°С до приблизительно 160°С.
Соединение, имеющее формулу (III), может, например, быть добавлено в реакционную смесь как таковое или в виде раствора в растворителе (например, органическом растворителе, имеющем температуру кипения от приблизительно 50°С до приблизительно 160°С). Это может, например, снизить риск воздействия раздражающих веществ на окружение.
Реакция пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), предпочтительно может происходить в присутствии основания. Основание депротонирует карбоксильную кислотную группу пипеколиновой кислоты. Таким образом, можно использовать любое основание, подходящее для депротонирования пипеколиновой кислоты. Например, основание может представлять собой неорганическое или органическое основание.
Примеры неорганических оснований включают фосфаты металлов, гидроксиды металлов, карбонаты металлов, бикарбонаты металлов и комбинации перечисленных веществ.
Примеры органических оснований включают алкиламины, такие как трибутиламин, и алканоламины, такие как триэтаноламин, и комбинации перечисленных веществ.
Например, основание может представлять собой фосфат металла, гидроксид металла, карбонат металла, бикарбонат металл или комбинацию перечисленных веществ. Металл может, например, представлять собой щелочной металл или щелочноземельный металл. Ион В+, имеющий формулу (II), может, например, представлять собой катион металла, полученный из фосфата металла, гидроксида металла или карбоната металла.
В частности, основание может представлять собой гидроксид металла, например, выбранный из гидроксида натрия и гидроксида калия.
Дополнительно, основание также может нейтрализовать кислоту, образующуюся в результате реакции пипеколиновой кислоты с соединением, имеющим формулу (Ia) или (Ib), например, основание может нейтрализовать HCl, образующуюся в результате реакции пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia). Таким образом, может быть применено по меньшей мере приблизительно два эквивалента основания на один эквивалент хлорного ангидрида, имеющего формулу (Ia) (один эквивалент для депротонирования пипеколиновой кислоты и один эквивалент для нейтрализации образовавшейся кислоты (например, HCl, которая образуется в реакции пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia)). Например, может быть применено от приблизительно двух эквивалентов до приблизительно четырех эквивалентов или от приблизительно двух эквивалентов до приблизительно трех эквивалентов основания на один эквивалент хлорного ангидрида, имеющего формулу (Ia).
Например, можно использовать по меньшей мере приблизительно один эквивалент хлорного ангидрида, имеющего формулу (Ia), или ангидрида кислоты, имеющего формулу (Ib), на один эквивалент пипеколиновой кислоты.
Соединение, имеющее формулу (II), имеет следующую химическую структуру:
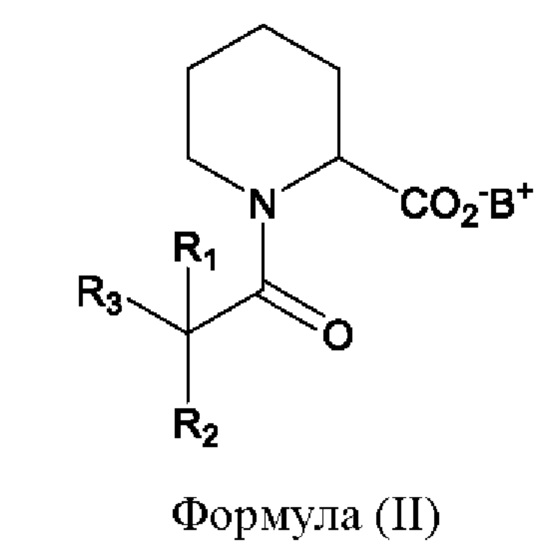
где определения R1, R2 и R3 приведены при описании хлорного ангидрида, имеющего формулу (Ia), и ангидрида кислоты, имеющего формулу (Ib), и В+ представляет собой катион, предоставляемый основанием. Например, В+ может представлять собой Na+ или K+, если в качестве основания применяют, соответственно, гидроксид натрия или гидроксид калия.
Реакция пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), может, например, протекать в присутствии катализатора межфазного переноса. В частности, реакция пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящая к образованию соединения, имеющего формулу (II), может протекать в присутствии катализатора межфазного переноса, если растворитель (например, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С) представляет собой неполярный растворитель, или если растворитель представляет собой смесь органического растворителя и воды. Применение катализатора межфазного переноса может, например, повышать выход реакции и/или снижать интенсивность гидролиза хлорного ангидрида, имеющего формулу (Ia), или ангидрида кислоты, имеющего формулу (Ib).
«Катализатором межфазного переноса» называется вещество, которое способствует миграции вещества из одной фазы в другую. Катализатор межфазного переноса может, например, способствовать миграции хлорного ангидрида, имеющего формулу (Ia), или ангидрида кислоты, имеющего формулу (Ib), в водную фазу, в которой он реагирует с пипеколиновой кислотой, в частности, если растворитель (например, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С) представляет собой неполярный растворитель.
Например, некоторые растворители или основания, используемые в реакции in situ, также могут действовать как катализаторы межфазного переноса. Например, частично растворимые в воде растворители, такие как метилтетрагидрофуран (Ме-ТГФ), могут действовать как катализаторы межфазного переноса. Например, фосфаты металлов или карбонаты металлов могут действовать как катализаторы межфазного переноса. Если растворитель или основание, применяемое в реакции in situ, действует как катализатор межфазного переноса, то использование дополнительного катализатора межфазного переноса может быть необязательным. Таким образом, если в качестве основания применяют фосфат металла или карбонат металла, то применение дополнительного катализатора межфазного переноса может быть необязательным.
Катализатор межфазного переноса может, например, представлять собой галогенид металла (например, йодид калия или йодид натрия).
Катализатор межфазного переноса может, например, представлять собой четвертичную аммонийную соль (NR4+, где R представляет собой алкильную или арильную группу) или органическую соль фосфония (PR4+, где R представляет собой водород, алкил, арил или галогенид).
Примеры четвертичных аммонийных солей, которые можно использовать в качестве катализаторов межфазного переноса, включают соли бензилтриэтиламмония (например, хлорид бензилтриэтиламмони), соли метилтрикапр ил аммония (например, хлорид метилтрикаприламмони), соли метилтрибутиламмония (например, хлорид метилтрибутиламмони), соли метилтриоктиламмония (например, хлорид метилтриоктиламмони) и соли тетра-н-бутиламмония. Примерами солей фосфония, которые можно использовать в качестве катализаторов межфазного переноса, являются соли гексадецилтрибутилфосфония (например, бромид гексадецилтрибутилфосфония).
Например, катализатор межфазного переноса может представлять собой соль тетра-н-бутиламмония, например, галогенид тетра-н-бутиламмония, например, тетра-н-бутиламмония бромид (ТБАБ).
Реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), с образованием соединения, имеющего формулу (II) можно осуществлять при любом подходящем рН, например, при рН от приблизительно 7,0 до приблизительно 15,0, или от приблизительно 8,0 до приблизительно 14,0, или от приблизительно 9,0 до приблизительно 14,0, или от приблизительно 10,0 до приблизительно 15,0.
Реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), которая приводит к образованию соединения, имеющего формулу (II) можно, например, осуществлять при рН, составляющем по меньшей мере приблизительно 12,5. Например, реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), можно осуществлять при рН, составляющем по меньшей мере приблизительно 13,0. Реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), которая приводит к образованию соединения, имеющего формулу (II) можно, например, осуществлять при рН, составляющем до приблизительно 14,5. Например, реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), которая приводит к образованию соединения, имеющего формулу (II) можно, например, осуществлять при рН, составляющем до приблизительно 14,0 или до приблизительно 13,5. Например, реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), которая приводит к образованию соединения, имеющего формулу (II) можно, например, осуществлять при рН от приблизительно 12,5 до приблизительно 14,5 или от приблизительно 12,5 до приблизительно 13,5. Величину рН реакционной смеси можно, например, поддерживать на протяжении всего периода протекания реакции пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящей к образованию соединения, имеющего формулу (II). Величину рН реакционной смеси можно, например, поддерживать посредством регулирования продолжительности добавления и количества основания, добавляемого в реакционную смесь. Это поддержание может, например, включать непрерывный мониторинг рН реакционной смеси с помощью рН-электрода. Регулирование величины рН реакционной смеси во время протекания реакции пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), позволяет, например, снижать степень гидролиза хлорного ангидрида или ангидрида кислоты.
Реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящую к образованию соединения, имеющего формулу (II), можно, например, осуществлять при температуре, составляющей по меньшей мере приблизительно -10°С. Например, реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящую к образованию соединения, имеющего формулу (II), можно осуществлять при температуре, составляющей по меньшей мере приблизительно -5°С или по меньшей мере приблизительно 0°С. Например, реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящую к образованию соединения, имеющего формулу (II), можно осуществлять при температуре, составляющей до приблизительно 40°С или до приблизительно 35°С, или до приблизительно 30°С, или до приблизительно 25°С, или до приблизительно 20°С, или до приблизительно 15°С, или до приблизительно 10°С. Например, реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящую к образованию соединения, имеющего формулу (II), можно осуществлять при температуре от приблизительно -10°С до приблизительно 40°С, или от приблизительно -5°С до приблизительно 30°С, или от приблизительно 0°С до приблизительно 20°С, или от приблизительно 0°С до приблизительно 15°С, или от приблизительно 0°С до приблизительно 5°С.
Реакцию пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящую к образованию соединения, имеющего формулу (II), можно, например, осуществлять при температуре ниже температуры разложения пипеколиновой кислоты и/или хлорного ангидрида, имеющего формулу (Ia), или ангидрида кислоты, имеющего формулу (Ib).
Продолжительность реакции пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящей к образованию соединения, имеющего формулу (II), может, например, составлять от приблизительно 30 секунд до приблизительно 5 часов. Например, продолжительность реакции пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящей к образованию соединения, имеющего формулу (II), может, например, составлять от приблизительно 30 секунд до приблизительно 1 часа, или от приблизительно 1 минуты до приблизительно 30 минут, или от приблизительно 1 минуты до приблизительно 15 минут, или от приблизительно 1 минуты до приблизительно 5 минут. Реакция пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящая к образованию соединения, имеющего формулу (II), может, например, продолжаться до полного завершения реакции.
Стадия 2. Превращение соединения, имеющего формулу (II), в соединение, имеющее формулу (IV)
Описанный в настоящем документе способ in situ может также включать реакцию описанного выше соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящую к образованию соединения, имеющего формулу (IV).
Соединение, имеющее формулу (III), имеет следующую химическую структуру:
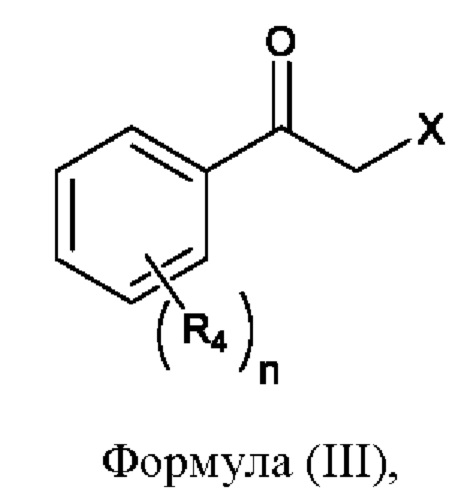
где фенильная группа соединения, имеющего формулу (III), имеет n заместителей R4, где n равен нулю, единице, двум, трем, четырем или пяти;
каждый заместитель R4 (если имеется) независимо выбран из галогена (например, F, О или Br), циано (C=N), нитро (-NO2), линейного C1-С6-алкила (неразветвленного или разветвленного), возможно включающего до 5 атомов галогена (например, до 5 атомов F) (например, СН3, CF3 или CHF2), С2-С6-алкенила (например, включающего одну или две двойные связи) (например, -СН=СН2), C1-С6-алкокси, возможно включающего до 3 атомов галогена (например, до 3 атомов F) (например, -ОСН3, -OCF3, -OCHF2, -OCH2F), С1-С3-алкокси-С1-С3-алкила (например, 2-метоксиэтила) и С3-С7-циклоалкила (например, циклопропила или циклобутила), и X представляет собой галоген.
Соединение, имеющее формулу (III), можно, например, получать промышленным образом или можно, например, получать ацилированием бензола или замещенного бензола по Фриделю-Крафтсу с использованием хлорацетилхлорида и катализатора хлорида алюминия, или хлорированием соответствующего ацетофенона сульфурилхлоридом (SO2Cl2) или 1,3-дихлор-5,5-диметилгидантоином или N-хлорсукцинимидом.
Например, R4 может представлять собой линейный C1-С6-алкил (неразветвленным или разветвленным), возможно включающий до 5 атомов галогена (например, до 5 атомов F) (например, CH3, CF3 или CHF2). Например, R4 может представлять собой метил.
Например, фенильная группа соединения, имеющего формулу (III), может иметь один или два заместителя R4. Например, фенильная группа соединения, имеющего формулу (III), может иметь один заместитель R4, который представляет собой метил.
Например, фенильная группа соединения, имеющего формулу (III), может иметь пять заместителей R4. Например, фенильная группа соединения, имеющего формулу (III), может иметь пять заместителей R4, которые все представляют собой метальные группы.
Например, X может представлять собой хлор, бром или йод. Например, X может представлять собой хлор.
Соединение, имеющее формулу (III), можно, например, добавлять в реакционную смесь как таковое или в виде раствора в растворителе (например, органическом растворителе с температурой кипения от приблизительно 50°С до приблизительно 160°С). Это, например, позволяет поддерживать смесь, в которой протекает реакция соединения, имеющего формулу (II), с соединением, имеющим формулу (III), с образованием соединения, имеющего формулу (IV), в перемешиваемом состоянии в течение всей реакции. Применение раствора позволяет, например, снижать риск воздействия раздражающих веществ на окружение.
Например, реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно осуществлять при температуре от приблизительно 50°С до приблизительно 160°С, например, от приблизительно 60°С до приблизительно 150°С, например, от приблизительно 80°С до приблизительно 130°С, например, от приблизительно 90°С до приблизительно 120°С, например, от приблизительно 100°С до приблизительно 110°С.
Соединение, имеющее формулу (IV), имеет следующую химическую структуру: 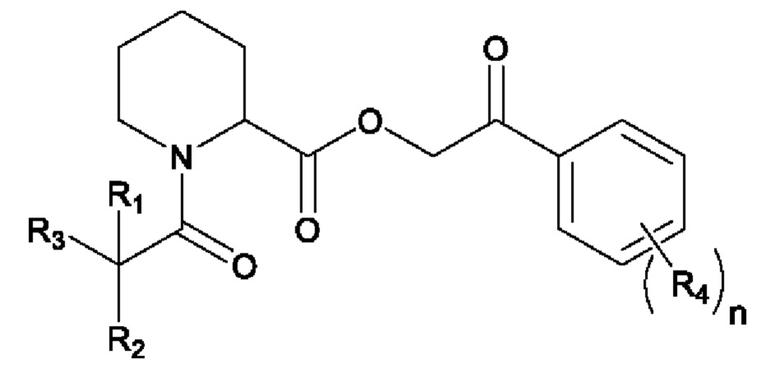
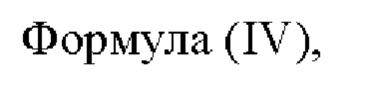
где определения R1, R2 и R3 приведены при описании соединений, имеющих формулу (Ia), (Ib) и (II), и определения R4 и n приведены при описании соединения, имеющего формулу (III).
Реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящую к образованию соединения, имеющего формулу (IV), можно, например, осуществлять в присутствии катализатора межфазного переноса. В частности, реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящую к образованию соединения, имеющего формулу (IV), можно осуществлять в присутствии катализатора межфазного переноса, если растворитель (например, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С) представляет собой неполярный растворитель.
Катализатор межфазного переноса может уже присутствовать в реакционной смеси, в которой протекает реакция пипеколиновой кислоты с хлорным ангидридом, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящая к образованию соединения, имеющего формулу (II), и протекающая в присутствии катализатора межфазного переноса. Таким образом, добавление дополнительного количества катализатора межфазного переноса в реакционную смесь, в которой протекает реакция соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящая к образованию соединения, имеющего формулу (IV), может быть необязательным.
Катализатор межфазного переноса может, например, способствовать миграции соединения, имеющего формулу (III), в водную фазу, в которой оно реагирует с соединением, имеющим формулу (II), с образованием соединения, имеющего формулу (IV). Соединение, имеющее формулу (IV), затем может мигрировать в органический слой (например, органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С).
Катализатор межфазного переноса может, например, быть катализатором, описанным в настоящем документе при рассмотрении стадии 1. Например, катализатор межфазного переноса может представлять собой соль аммония, такую как бромид тетра-н-бутиламмония (ТБАБ).
Например, добавление дополнительного количества основания в реакционную смесь, в которой протекает реакция соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящая к образованию соединения, имеющего формулу (IV), может быть необязательным. Это может, например, объясняться тем, что карбоксильная кислотная группа соединения, имеющего формулу (II), уже находится в депротонированном состоянии.
Реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно, например, осуществлять при температуре и давлении, соответствующих кипению реакционной смеси. Благодаря присутствию в смеси других компонентов, таких как вода, которые могут, например, образовывать азеотроп, температура кипения реакционной смеси может, например, отличаться (например, быть ниже) от температуры кипения растворителя (например, органического растворителя с температурой кипения от приблизительно 50°С до приблизительно 160°С).
Реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно, например, осуществлять при температуре ниже температуры разложения соединения, имеющего формулу (II), и/или соединения, имеющего формулу (III).
Например, реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно осуществлять при температуре, больше или равной приблизительно 50°С, например, больше или равной приблизительно 60°С, например, больше или равной приблизительно 70°С, например, больше или равной приблизительно 80°С.
Например, реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно осуществлять при температуре меньше или равной приблизительно 160°С, например, меньше или равной приблизительно 150°С, например, меньше или равной приблизительно 140°С, например, меньше или равной приблизительно 130°С, например, меньше или равной приблизительно 120°С, например, меньше или равной приблизительно 110°С, например, меньше или равной приблизительно 100°С.
Например, реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно осуществлять при температуре от приблизительно 50°С до приблизительно 160°С, например, от приблизительно 60°С до приблизительно 120°С, например, от приблизительно 70°С до приблизительно 100°С.
Реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно, например, осуществлять при любом подходящем рН, который обеспечивает депротонирование карбоновой кислоты, например, при рН больше или равном приблизительно 7,0 или больше или равном приблизительно 8,0 или больше или равном приблизительно 9,0 или больше или равном приблизительно 10,0.
Реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно, например, осуществлять при рН больше или равном приблизительно 12,0, например, больше или равном приблизительно 12,5. Реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно, например, осуществлять при рН меньше или равном приблизительно 14,0, например, меньше или равном приблизительно 13,5. Например, реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), можно осуществлять при рН, составляющем от приблизительно 12,0 до приблизительно 14,0 или от приблизительно 12,5 до приблизительно 13,5.
Продолжительность реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу
(IV), может, например, составлять от приблизительно 30 секунд до приблизительно 5 часов. Например, продолжительность реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV), может составлять от приблизительно 30 секунд до приблизительно 1 часа или от приблизительно 1 минуты до приблизительно 30 минут или от приблизительно 1 минуты до приблизительно 15 минут или от приблизительно 1 минуты до приблизительно 5 минут. Реакция соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящая к образованию соединения, имеющего формулу (IV), может, например, продолжаться до завершения реакции. Завершение реакции может быть определено, например, газохроматографическим анализом.
В случае использования органического растворителя, воду можно, например, удалять из реакционной смеси после проведения реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV), и до проведения реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V). Одним из преимуществ удаления воды является повышение температуры проведения реакции, что увеличивает скорость протекания реакции. Например, воду можно удалять из реакционной смеси после полного завершения реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV), и до проведения реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V). Воду можно, например, удалять любым подходящим способом. Например, воду можно удалять азеотропной отгонкой. Продукт реакции (соединение, имеющее формулу (IV)) может оставаться в органическом слое (например, включающем органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С). Это позволяет, например, проводить стадию 3 при более высокой температуре, например, при кипячении с обратным холодильником при более высокой температуре.
Стадия 3. Превращение соединения, имеющего формулу (IV), в соединение, имеющее формулу (V)
Описанный в настоящем документе способ in situ также включает реакцию описанного в настоящем документе соединения, имеющего формулу (IV), с источником иона аммония, что приводит к образованию соединения, имеющего формулу (V).
Соединение, имеющее формулу (V), имеет следующую химическую структуру:
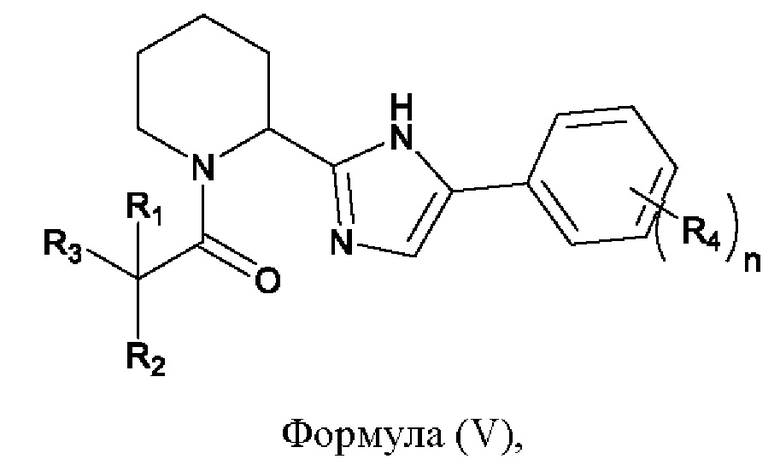
где определения R1, R2, R3, R4 и n приведены выше при описании соединений, имеющих формулы (Ia), (Ib), (II), (III), и (IV).
Соединение, имеющее формулу (V) может, например, представлять собой 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-он (включая (2S)-2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-он или рацемическую смесь), 2-(метилтио)-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)пропан-1-он, 2-метил-2-(метилтио)-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)пропан-1-он или 2,2-диметил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бут-3-ен-1-он.
Источник иона аммония может, например, представлять собой любой источник иона аммония, подходящий для превращения соединения, имеющего формулу (IV), в соединение, имеющее формулу (V).
Источник иона аммония может, например, представлять собой карбоксилат аммония, такой как ацетат аммония или формиат аммония. Источник иона аммония может, например, представлять собой смесь аммиака и карбоновой кислоты (RCO2H, где R представляет собой водород или алкильную группу). Например, источник иона аммония может представлять собой ацетат аммония или смесь аммиака и уксусной кислоты.
Подходящие источники иона аммония, такие как ацетат аммония, выпускаются в промышленности.
Источник иона аммония можно, например, добавлять в реакционную смесь в виде водного раствора. Например, пред добавлением в реакционную смесь, раствор можно нагревать для поддержания высокой концентрации растворенного источника иона аммония. Добавление источника иона аммония в виде водного раствора может, например, предотвратить накопление непрореагировавшего источника иона аммония.
Можно использовать, например, приблизительно пять или менее эквивалентов источника иона аммония на один эквивалент соединения, имеющего формулу (IV). Например, можно использовать приблизительно четыре или менее эквивалента источника иона аммония или приблизительно три или менее эквивалента источника иона аммония на один эквивалент соединения, имеющего формулу (IV). Например, можно использовать приблизительно один эквивалент или более или приблизительно два эквивалента или более источника иона аммония на один эквивалент соединения, имеющего формулу (IV).
Источник иона аммония можно, например, добавлять в реакционную смесь в водном растворе, или его можно добавлять в реакционную смесь в своем естественном виде (т.е. не в растворе), например, в виде твердого вещества. В некоторых воплощениях источник иона аммония можно добавлять в реакционную смесь в своем естественном виде, например, в виде твердого вещества, что может, например, способствовать минимизации количества воды, вводимой в реакцию.
Источник иона аммония можно, например, добавлять в реакционную смесь порциями (т.е. отдельными партиями, а не за один раз). Это позволяет, например, повысить эффективность реакции, например, благодаря снижению в реакционной смеси доли воды, поступающей с раствором источника иона аммония. Например, источник иона аммония можно добавлять в реакционную смесь по меньшей мере двумя или тремя или четырьмя порциями. Например, при добавлении источника иона аммония в реакционную смесь, его можно добавлять по меньшей мере двумя или по меньшей мере тремя порциями, например, в количестве от двух до шести порций или от трех до шести порций или от двух до четырех порций или от трех до четырех порций. Например, если источник иона аммония добавляют в реакционную смесь в виде водного раствора, то его можно добавлять по каплям.
Реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), можно, например, осуществлять при температуре и давлении, обеспечивающих кипячение с обратным холодильником реакционной смеси. Благодаря присутствию в смеси других компонентов, таких как вода, которые могут, например, образовывать азеотропную смесь, температура кипения реакционной смеси может, например, отличаться (например, быть ниже) температуры кипения растворителя (например, органического растворителя с температурой кипения от приблизительно 50°С до приблизительно 160°С).
Реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), можно, например, осуществлять при температуре ниже температуры разложения соединения, имеющего формулу (IV), и/или источника иона аммония.
Например, реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), можно осуществлять при температуре, которая больше или равна приблизительно 50°С, например, больше или равна приблизительно 60°С, например, больше или равна приблизительно 70°С, например, больше или равна приблизительно 80°С, например, больше или равна приблизительно 90°С, например, больше или равна приблизительно 100°С.
Например, реакция соединения, имеющего формулу (IV), с источником иона аммония, приводящая к образованию соединения, имеющего формулу (V), может быть проведена при температуре меньше или равной приблизительно 160°С, например, меньше или равной приблизительно 150°С, например, меньше или равной приблизительно 140°С, например, меньше или равной приблизительно 130°С, например, меньше или равной приблизительно 120°С, например, меньше или равной приблизительно 110°С.
Реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), можно, например, осуществлять при рН больше или равном приблизительно 1,0, например, больше или равном приблизительно 2,0. Реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), можно, например, осуществлять при рН меньше или равном приблизительно 14,0, например, меньше или равном приблизительно 12,0, или меньше или равном приблизительно 10,0, или меньше или равном приблизительно 8,0, или меньше или равном приблизительно 7,0, или меньше или равном приблизительно 6,0. Например, реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), можно осуществлять при рН от приблизительно 1,0 до приблизительно 14,0, или от приблизительно 1,0 до приблизительно 8,0, или от приблизительно 1,0 до приблизительно 7,0, или от приблизительно 2,0 до приблизительно 6,0. Это можно, например, осуществлять благодаря накоплению кислоты (например, уксусной кислоты), образующейся на реакционной стадии 3.
Продолжительность реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V), может, например, составлять от приблизительно 30 минут до приблизительно 10 часов.
Например, продолжительность реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V), может составлять от приблизительно 1 часа до приблизительно 8 часов или от приблизительно 2 часов до приблизительно 7 часов. Реакция соединения, имеющего формулу (IV), с источником иона аммония, приводящая к образованию соединения, имеющего формулу (V), например, может продолжаться до полного завершения реакции. Завершение реакции может быть определено, например, газохроматографическим анализом.
В случае использования органического растворителя, во время протекания реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V), можно, например, удалять воду из реакционной смеси. Например, удаление воды из реакционной смеси во время протекания реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V), может быть непрерывным. Воду может, например, удалять с помощью ловушки Дина-Старка. Продукт реакции (соединение, имеющее формулу (V)) может оставаться в органическом слое (например, включающем органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С).
Дополнительные стадии После проведения реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V), можно, например, осуществлять нейтрализацию слоя, включающего соединение, имеющее формулу (V) (например, органического слоя, который может включать органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С), и/или промывку водой. Промывку водой можно, например, осуществлять после нейтрализации слоя, включающего соединение, имеющее формулу (V) (например, органического слоя).
Соединение, имеющее формулу (V), можно, например, извлекать (например, извлекать из органического слоя, который может включать органический растворитель с температурой кипения от приблизительно 50°С до приблизительно 160°С) любым подходящим способом, например, кристаллизацией. Например, соединение, имеющее формулу (V), можно кристаллизовать непосредственно из растворителя (например, толуола или Ме-ТГФ), который можно использовать в качестве растворителя при проведении всего синтеза, что позволяет не менять растворитель на протяжении всех этапов синтеза и кристаллизации. В ином случае соединение, имеющее формулу (V), можно кристаллизовать из другого растворителя. Затем соединение, имеющее формулу (V), можно подвергать дальнейшей очистке.
В зависимости от растворителя, применяемого для проведения реакция, замена растворителя может приводить к таким полезным эффектам, как обонятельно чистое качество и/или более высокие выходы соединения, имеющего формулу (V). Подходящие растворители для кристаллизации могут быть выбраны, но не ограничены перечисленным, из этилацетата, бутилацетата, изопропилацетата, изо бутил ацетата, метилизобутилкетона и изопропанола, а также смесей, таких как гептан/изопропанол, гептан/этанол или простой метил-трет-бутиловый эфир/этилацетат.
Применение соединений, имеющих формулу (V)
Изобретение также относится к соединениям, имеющим формулу (V), которые, например, получают или которые могут быть получены способами, описанными в настоящем документе.
Соединения, имеющие формулу (V), могут, например, найти применение в ароматических композициях. В частности, соединения, имеющие формулу (V), можно использовать в качестве охлаждающих средств ароматической композиции.
Таким образом, изобретение также относится к ароматической композиции, включающей соединение, имеющее формулу (V), описанное в настоящем документе.
Ароматические композиции, описанные в настоящем документе, могут, например, быть включены в любой потребительский товар, который контактирует со слизистой оболочкой. Например, потребительский товар может представлять собой пищевой продукт, напиток, жевательную резинку, табачный продукт, продукт, заменяющий табак, средства по уходу за зубами, средства личной гигиены (включая средства по уходу за губами) или средства для сексуального здоровья и средства интимной гигиены.
Таким образом, изобретение также относится к потребительскому товару, включающему ароматическую композицию, описанную в настоящем документе.
Способы дополнительно раскрыты с помощью приведенных ниже неограничивающих примеров, которые относятся к конкретным воплощениям.
Примеры
Пример 1. Однореакторная процедура получения 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-она (соединения, имеющего формулу (V))
Реактор емкостью 10 литров продували азотом, и при комнатной температуре в реактор помещали пипеколиновую кислоту (DL-пипеколиновую кислоту, Xiamen Synress Import and Export Co., Ltd. (800 r, 6,2 моль)) и бромид тетрабутиламмония (100 г, 0,3 моль). К перемешиваемому раствору (102 об./мин.) последовательно добавляли воду (1630 г), толуол (1127 г) и гидроксид натрия (32%, 1664 г, 13,3 моль). Скорость перемешивания увеличивали (186 об./мин.), и смесь охлаждали до 5°С (Tj: -15°С). Затем в течение 2 часов по каплям добавляли 2-метилбутаноилхлорид (747 г, 6,2 моль), поддерживая температуру реакционной смеси в диапазоне от 3°С до 5°С. По завершении добавления, смесь перемешивали в течение одного часа, затем температуру повышали до 45°С, и порциями в течение 15 минут добавляли твердый 2-хлор-1-(пара-толил)этан-1-он (1077 г, 6,3 моль). Затем смесь нагревали до 90°С (Tj: 110°С) в течение 1 часа и 15 минут, после чего газохроматографический (ГХ) анализ смеси показал полное превращение 1-(2-метилбутаноил)пиперидин-2-карбоновой кислоты в 2-оксо-2-(пара-толил)этил-1-(2-метилбутаноил)пиперидин-2-карбоксилат.Затем реакционную смесь охлаждали до 50°С (Tj: 50°С), перемешивание прекращали, и водный слой отделяли от мутно-оранжевого органического слоя, сливая через нижний кран. К смеси, оставшейся в реакторе, добавляли толуол (607 г). Раствор перемешивали (160 об./мин.) и нагревали до кипения (89-114°С, Tj: 145°С) при одновременном удалении воды в виде азеотропной смеси. После удаления всей воды и достижения конечной температуры кипения (114°С), добавляли первую порцию ацетата аммония (477 г, 6,2 моль). Реакционную смесь перемешивали при кипячении с обратным холодильником в течение 45 минут, удаляя воду, образующуюся в реакции, в виде азеотропной смеси. Добавляли другую порцию ацетата аммония (477 г, 6,2 моль) и, наконец, спустя 3 часа проведения реакция, добавляли последнюю порцию ацетата аммония (477 г, 6,2 моль); перемешивание при кипячении с обратным холодильником продолжали в течение 70 минут до тех пор, пока ГХ анализ не показал завершение превращения. Реакционную смесь охлаждали до 50°С, и к перемешиваемой смеси добавляли воду (500 г) и гидроксид натрия (2 М, 1000 г). Затем рН смеси доводили до рН, составляющего 7, добавлением гидроксида натрия (2 М, 2700 г). Полученный раствор вновь нагревали до кипения для высушивания раствора за счет образования азеотропа (Tj: 145°С), затем раствор охлаждали до приблизительно 0°С (Tj: 0°С), и перемешивание (70 об./мин.) продолжали в течение 24 часов. Мелкие кристаллы, образовавшиеся в красной смеси, удаляли фильтрованием массы через воронку Бюхнера объемом 4 л и затем дважды промывали холодным простым метил-трет-бутиловым эфиром (4°С, 1000 мл).
Твердый продукт сушили в вакууме, получая 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-он (838 г, 2,5 моль, выход 40%) в виде твердого белого вещества. Т.пл.: 156.3°С. ГХ/МС (ЭИ) (то есть; газовая хроматография/масс-спектрометрия с электроионизацией): m/z (%): 325 (10) [М+], 268 (2), 240 (100), 224 (3), 185 (10), 159 (2), 142 (1), 84 (2), 57 (4). 1H ЯМР (500 МГц, ДМСО-d6, 413K, смесь стереомеров и таутомеров) δ=11,32 (br s, 1Н), 7,61 (br m, 2H), 7,28 (br s, 1H), 7,14 (br m, 2H), 5,63 (br m, 1H), 4,06 (br m, 1H), 3,29 (br m, 1H), 2,76 (m, 1H), 2,31 (s, 3H), 2,23 (br m, 1H), 1,83-1,60 (m, 5H), 1,49-1,33 (m, 2H), 1,09-1,05 (2d, J=6,8 Гц, 3Н), 0,91-0,85 (2t, J=7,4 Гц, 3Н) м.д (миллионные доли). 13С ЯМР (125 МГц, ДМСО-d6, 413K, смесь стереомеров и таутомеров; химические сдвиги получены способами гетероядерной спектроскопии с одноквантовым переносом когеренции и гетероядерной корреляционной спектроскопии через несколько связей (сокр. ГСОПК и ГКСНС)) δ 174,4 (s), 146,8 (s), 139,6 (s), 134,3 (s), 132,1 (s), 128,1 (2d), 123,7 (2d), 110,9 (d), 47,5 (d), 40,1 (t), 35,6 (d), 27,6 (t), 26,0 (t), 24,7 (t), 19,8 (q), 19,0 (t), 16,3 (q), 10,5 (q) м.д.
Обозначения: s-синглет; br s - уширенный синглет; m - мультиплет; br m - уширенный мультиплет; d - дублет; t - триплет; q - квадруплет
Кристаллическая форма 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-она была охарактеризована основными пиками порошковой рентгенограммы, которую получали под действием K-бета излучения меди при 2-тета (град.): 8,93, 9,59, 11,66, 12,44, 12,95, 14,53, 15,91, 17,13, 17,89, 18,43, 19,21, 19,51, 19,90, 20,76, 22,59, 25,06, 27,03, 27,77, 28,81, 29,79, 32,08.
Пример 2. (2S)-2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-он
Был получен из (S)-метилбутаноилхлорида в соответствии с раскрытой процедурой. 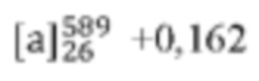 (с 1,114, EtOH). Данные спектроскопии идентичны данным рацемического продукта примера 1.
(с 1,114, EtOH). Данные спектроскопии идентичны данным рацемического продукта примера 1.
Пример 3. 2-(метилтио)-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)пропан-1-он
Был получен из 2-(метилтио)пропаноилхлорида в соответствии с раскрытой процедурой.
ГХ/МС (ЭИ): m/z (%): 357 (5) [М+], 342(7), 268 (11), 240 (100), 185 (11), 159 (5), 117 (4), 89 (10). 1Н ЯМР (500 МГц, ДМСО-d6, 413K, смесь стереомеров и таутомеров) δ 11,56-11,06 (br m, 1Н), 7,69-7,43 (br m, 2H), 7,34-7,24 (br m, 1H), 7,23-7,07 (br m, 2H), 5,69 и 5,58 (2 br m, 1H), 4,04 (br m, 1H), 3,91-3,87 (br m, 1H), 3,51-3,13 (br m, 1H), 2,37-2,27 (br m, 1H), 2,32 (br s, 3H), 2,09 и 2,08 (2 br s, 3H), 1,91-1,41 (br m, 5H), 1,44 и 1,42 (2 br d, J=6,7 Гц, 3Н) м.д. 13C ЯМР (125 МГц, ДМСО-d6, Т=413K, смесь стереомеров и таутомеров, химические сдвиги получены в анализах ГСОПК и ГКСНС) δ 169,7 (s), 146,4 (s), 137,7 (s), 134,2 (s), 131,4 (s), 128,0 (2d), 123,7 (2d), 110,9 (d), 47,5 (d), 40,8 (t), 37,7 (d), 27,4 (t), 24,3 (t), 19,7 (q), 18,8 (t), 17,0 (q), 11,0 (q) м.д.
Обозначения: s -синглет; br s - уширенный синглет; m - мультиплет; br m - уширенный мультиплет; d - дублет; t - триплет; q - квадруплет
Пример 4. Однореакторная процедура получения 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-он (соединения, имеющего формулу (V)) Реактор емкостью 5 литров продували азотом, и при комнатной температуре в реактор помещали пипеколиновую кислоту (DL-пипеколиновую кислоту, Xiamen Synress Import and Export Co., Ltd. (400 r, 3,1 моль)), фосфат калия (98%, 738 г, 3,4 моль) и гидроксид калия (85%, 184 г, 2,8 моль). Последовательно добавляли воду (1280 г) и 2-метилтетрагидрофурана (547 г), и смесь охлаждали до 4°С. В течение 1 часа по каплям добавляли 2-метилбутаноилхлорид (373 г, 3,1 моль), поддерживая температуру реакционной смеси ниже 15°С. По завершении добавления смесь перемешивали в течение одного часа, затем температуру повышали до 45°С, и в течение 15 минут порциями добавляли смесь твердого 2-хлор-1-(пара-толил)этан-1-она (97%, 571 г, 3,3 моль) и бромида тетрабутиламмония (9,98 г, 0,03 моль). Затем смесь в течение одного часа и 30 минут нагревали до 76°С (Tj: 95°С), после чего ГХ анализ смеси показал полное превращение 1-(2-метилбутаноил)пиперидин-2-карбоновой кислоты в 2-оксо-2-(пара-толил)этил-1-(2-метилбутаноил)пиперидин-2-карбоксилат. Реакционную смесь затем охлаждали до 60°С, перемешивание прекращали, и водный слой отделяли от мутного светло-оранжевого органического слоя, сливая через нижний кран. К смеси, оставшейся в реакторе, добавляли 2-метилтетрагидрофуран (1025 г). Раствор перемешивали (160 об./мин.), нагревали до кипения (85°С, Tj: 110°С), и порциями добавляли ацетат аммония (1462 г, 18,6 моль, 98%) при одновременном удалении воды в виде азеотропной смеси. Реакционную смесь перемешивали при кипячении с обратным холодильником в течение ночи до тех пор, пока ГХ анализ не показал завершение превращения, удаляя воду, образующуюся в реакции, в виде азеотропной смеси. Реакционную смесь охлаждали до 60°С и один раз промывали водой (1000 г), три раза-гидроксидом натрия (2 М, 1000 г) и четыре раза водой (1000 г) для достижения рН 7. Полученный раствор вновь нагревали до кипения для высушивания раствора за счет образования азеотропа (Tj: 115°С), затем раствор охлаждали до 0°С (Tj: 0°С), и перемешивание (50 об./мин.) продолжали в течение 24 часов. Мелкие кристаллы, образовавшиеся в оранжевой смеси, удаляли фильтрованием массы через воронку Бюхнера и затем дважды промывали холодным простым метил-трет-бутиловым эфиром (4°С, 400 мл).
Твердый продукт сушили в вакууме, получая 2-метил-1-(2-(5-(пара-толил)-1Н-имидазол-2-ил)пиперидин-1-ил)бутан-1-он (390 г, 1,2 моль, выход 39%) в виде твердого белого вещества. Т.пл.: 156,3°С. ГХ/МС (ЭИ): m/z (%): 325 (10) [М+], 268 (2), 240 (100), 224 (3), 185 (10), 159 (2), 142 (1), 84 (2), 57 (4). 1Н ЯМР (500 МГц, ДМСО-d6, 413K, смесь стереомеров и таутомеров) δ=11,32 (br s, 1H), 7,61(br m, 2Н), 7,28 (br s, 1H), 7,14 (br m, 2H), 5,63 (br m, 1H), 4,06 (br m, 1H), 3,29 (br m, 1H), 2,76 (m, 1H), 2,31 (s, 3H), 2,23 (br m, 1H), 1,83-1,60 (m, 5H), 1,49-1,33 (m, 2H), 1,09-1,05 (2d, J=6,8 Гц, 3Н), 0,91-0,85 (2t, J=7,4 Гц, 3Н) м.д. 13C ЯМР (125 МГц, ДМСО d6, 413K, смесь стереомеров и таутомеров, химические сдвиги получены в анализах ГСОПК и ГКСНС) δ 174,4 (s), 146,8 (s), 139,6 (s), 134,3 (s), 132,1 (s), 128,1 (2d), 123,7 (2d), 110,9 (d), 47,5 (d), 40,1 (t), 35,6 (d), 27,6 (t), 26,0 (t), 24,7 (t), 19,8 (q), 19,0 (t), 16,3 (q), 10,5 (q) м.д.
Обозначения: s синглет; br s - уширенный синглет; m мультиплет; br m - уширенный мультиплет; d - дублет; t - триплет; q - квадруплет
Выше приведено общее описание некоторых неограничивающих воплощений настоящего изобретения. Специалисты в данной области техники могут внести в воплощения модификации и изменения, не выходящие за пределы объема настоящего изобретения, определяемого прилагаемыми пунктами формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 3-ПИРИДИЛМЕТИЛ АММОНИЙ БРОМИДОВ | 2009 |
|
RU2549896C2 |
| СИНТЕЗ ПРЕДШЕСТВЕННИКА ИНГИБИТОРА ПРОТЕАЗЫ | 2006 |
|
RU2421459C2 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОФЕНИЛСУЛЬФОНИЛМОЧЕВИН (ВАРИАНТЫ), ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ | 1996 |
|
RU2177003C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАМАТ-КАРБОКСИЛАТНЫХ ПРОИЗВОДНЫХ | 2006 |
|
RU2403238C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ САЛИЦИЛАМИДОВ | 2005 |
|
RU2404158C2 |
| ПРОИЗВОДНЫЕ ГУАНИДИНАЛКИЛ-1,1-БИС-ФОСФОНОВЫХ КИСЛОТ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2114855C1 |
| СОЕДИНЕНИЯ С НЕМАТОЦИДНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2608217C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕРБИЦИДНЫХ СУЛЬФОНИЛМОЧЕВИН И N-(ПИРИМИДИНИЛ- ИЛИ ТРИАЗИНИЛ)-КАРБАМАТОВ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ | 1996 |
|
RU2177002C2 |
| ГАЛОГЕНИДЫ ГАЛОГЕНСУЛЬФОНИЛБЕНЗОЙНОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ФЕНИЛСУЛЬФОНИЛМОЧЕВИН | 2003 |
|
RU2330027C2 |
| СПОСОБ ПРОИЗВОДСТВА ПРОИЗВОДНЫХ ЗАМЕЩЁННОЙ 5-МЕТОКСИМЕТИЛПИРИДИН-2, 3-ДИКАРБОНОВОЙ КИСЛОТЫ | 2009 |
|
RU2549894C2 |
Изобретение относится к способу образования in situ из пипеколиновой кислоты соединения, имеющего формулу (V), где способ in situ выполняют в присутствии растворителя, и растворитель представляет собой органический растворитель с температурой кипения от 50°C до 160°C, воду или смесь указанных растворителей, где способ включает: (a) осуществление реакции пипеколиновой кислоты с хлорангидридом кислоты, имеющим формулу (Ia), в присутствии основания, или реакции пипеколиновой кислоты с ангидридом кислоты, имеющим формулу (Ib), возможно в присутствии основания, приводящей к образованию соединения, имеющего формулу (II)
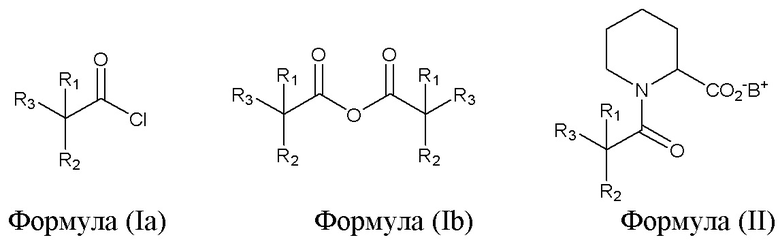
(b) осуществление реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV) 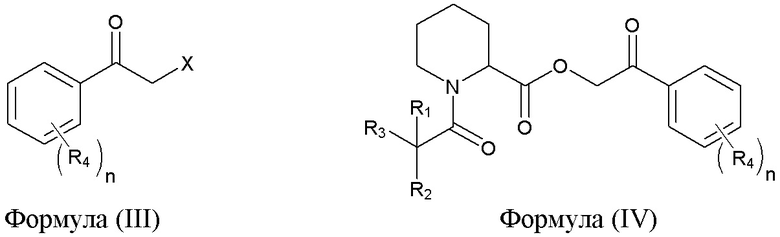
(c) осуществление реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V)
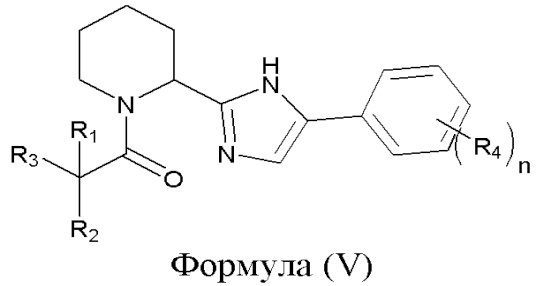
где R1 выбирают из водорода и метила, и/или R2 выбирают из водорода, C1-C2 алкила и C2-C3 алкенила, и R3 выбирают из C1-C3 алкила, C2-C5 алкенила, содержащего одну или две двойные связи, C1-C3-алкоксигруппы, C1-C4 алкил-C(O)-, C1-C4 алкил-S-, C1-C4 алкил-SCH2-, C1-C4 алкенил-S-, C1-C4 алкил-S(O)-, C1-C4 алкил-S(O)2-, C1-C4 алкенил-S(O)-, C1-C4 алкенил-S(O)2-, -SH, CF3S-, циклопропила, циклобутила, фурила, возможно замещенного метилом, и C1-C6 фторалкила; фенильная группа соединений, имеющих формулы (III), (IV) и (V), имеет n заместителей R4, где n равен нулю, единице, двум, трем, четырем или пяти; каждый R4 независимо выбран из линейного C1-C6 алкила, возможно включающего до 5 атомов F; B+ представляет собой катион, предоставляемый основанием, и X представляет собой хлор, бром или йод; при этом основание представляет собой фосфат металла, гидроксид металла, карбонат металла, бикарбонат металла или их комбинацию. Технический результат: получен новый способ получения in situ из пипеколиновой кислоты соединения, имеющего формулу (V), который позволяет уменьшить количество стадий очистки и извлечения; применять один и тот же растворитель на протяжении всего способа; по окончании реакции растворитель может быть подвергнут рециркуляции; хиральность углеводородной группы, образованной радикалами R1, R2 и R3, остается неизменной в течение всей реакции; хлорангидрид и соединения, имеющие формулу (III), можно получать в лаборатории по месту синтеза и использовать неочищенными и в растворе, что снижает действие реагентов-лакриматоров на окружение; протекание такой побочной реакции, как гидролиз хлорангидрида, в меньшей степени; более мягкие условия реакции; снизить количество или число требуемых реагентов; снизить количество источника иона аммония, требуемого для третьей реакционной стадии; получить приемлемый выход; получить приемлемую селективность. 12 з.п. ф-лы, 2 табл., 4 пр.
1. Способ образования in situ из пипеколиновой кислоты соединения, имеющего формулу (V), где способ in situ выполняют в присутствии растворителя, и растворитель представляет собой органический растворитель с температурой кипения от 50°C до 160°C, воду или смесь указанных растворителей, где способ включает:
(a) осуществление реакции пипеколиновой кислоты с хлорангидридом кислоты, имеющим формулу (Ia), в присутствии основания, или реакции пипеколиновой кислоты с ангидридом кислоты, имеющим формулу (Ib), возможно в присутствии основания, приводящей к образованию соединения, имеющего формулу (II)
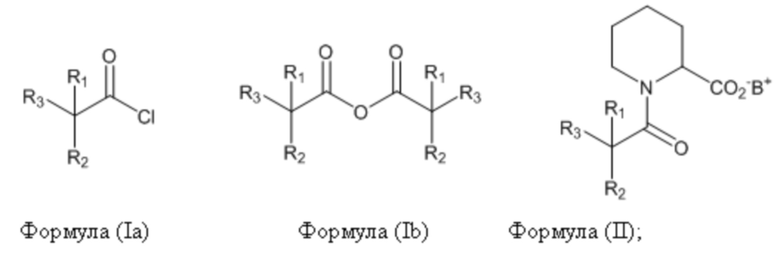
(b) осуществление реакции соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящей к образованию соединения, имеющего формулу (IV)
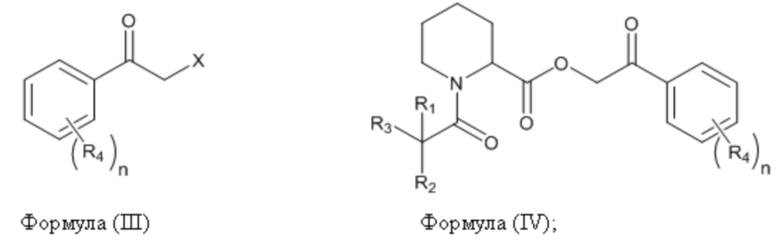
(c) осуществление реакции соединения, имеющего формулу (IV), с источником иона аммония, приводящей к образованию соединения, имеющего формулу (V)
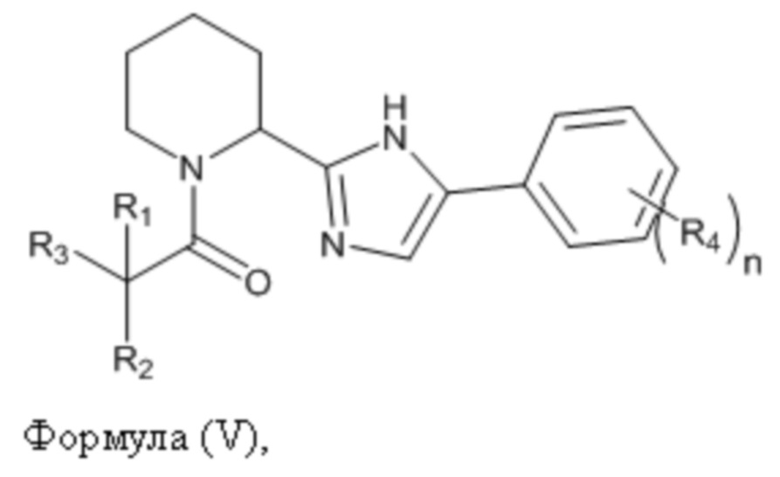
где R1 выбирают из водорода и метила, и/или
R2 выбирают из водорода, C1-C2 алкила и C2-C3 алкенила, и
R3 выбирают из C1-C3 алкила, C2-C5 алкенила, содержащего одну или две двойные связи, C1-C3-алкоксигруппы, C1-C4 алкил-C(O)-, C1-C4 алкил-S-, C1-C4 алкил-SCH2-, C1-C4 алкенил-S-, C1-C4 алкил-S(O)-, C1-C4 алкил-S(O)2-, C1-C4 алкенил-S(O)-, C1-C4 алкенил-S(O)2-, -SH, CF3S-, циклопропила, циклобутила, фурила, возможно замещенного метилом, и C1-C6 фторалкила;
фенильная группа соединений, имеющих формулы (III), (IV) и (V), имеет n заместителей R4, где n равен нулю, единице, двум, трем, четырем или пяти;
каждый R4 независимо выбран из линейного C1-C6 алкила, возможно включающего до 5 атомов F;
B+ представляет собой катион, предоставляемый основанием, и
X представляет собой хлор, бром или йод;
при этом основание представляет собой фосфат металла, гидроксид металла, карбонат металла, бикарбонат металла или их комбинацию.
2. Способ по п.1, в котором основание представляет собой гидроксид натрия или гидроксид калия.
3. Способ по любому из предшествующих пунктов, в котором применяют по меньшей мере два эквивалента основания на один эквивалент хлорангидрида кислоты, имеющего формулу (Ia), или ангидрида кислоты, имеющего формулу (Ib), или соединения, имеющего формулу (III).
4. Способ по любому из предшествующих пунктов, в котором реакцию пипеколиновой кислоты с хлорангидридом кислоты, имеющим формулу (Ia), или ангидридом кислоты, имеющим формулу (Ib), приводящую к образованию соединения, имеющего формулу (II), и/или реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящую к образованию соединения, имеющего формулу (IV), осуществляют в присутствии катализатора межфазного переноса.
5. Способ по п.4, где катализатор межфазного переноса представляет собой бромид тетрабутиламмония (ТБАБ).
6. Способ по любому из предшествующих пунктов, в котором растворитель представляет собой ароматический растворитель, например алкилбензольный растворитель, такой как толуол.
7. Способ по любому из пп.1-5, в котором растворитель представляет собой неароматический растворитель, например 2-метилтетрагидрофуран.
8. Способ по любому из предшествующих пунктов, в котором реакцию соединения, имеющего формулу (II), с соединением, имеющим формулу (III), приводящую к образованию соединения, имеющего формулу (IV), осуществляют при температуре, составляющей от 50°C до 120°C.
9. Способ по любому из предшествующих пунктов, в котором источником иона аммония является ацетат аммония или смесь аммиака и уксусной кислоты.
10. Способ по любому из предшествующих пунктов, в котором реакцию соединения, имеющего формулу (IV), с источником иона аммония, приводящую к образованию соединения, имеющего формулу (V), осуществляют при температуре, составляющей от 90°C до 120°C.
11. Способ по любому из предшествующих пунктов, в котором атом углерода, к которому присоединены R1, R2 и R3, является хиральным центром, и хиральность остается неизменной в течение всего периода протекания реакции.
12. Способ по любому из предшествующих пунктов, в котором R1, R2 и R3 совместно с атомом углерода, к которому они присоединены, образуют углеводородную группу, выбранную из: 3-тиабут-2-ила, 2-метил-3-тиабут-2-ила, 3-тиапент-2-ила, 4-тиапент-2-ила, 2-тиапроп-1-ила, 2-метил-3-тиапент-2-ила, 3-оксо-3-тиабут-2-ила, 3-оксо-2-метил-3-тиабут-2-ила, 3-оксо-3-тиапент-2-ила, 4-оксо-4-тиапент-2-ила, 2-оксо-2-тиапроп-1-ила, 3-оксо-2-метил-3-тиапент-2-ила, бут-2-ила, пент-2-ила, бут-3-ен-2-ила, пент-3-ен-2-ила, бут-2-ен-2-ила, пент-2-ен-2-ила, бут-1-ен-2-ила, пент-1-ен-2-ила, 2-метилбут-2-ила, 2-метилпент-2-ила, 2-метилбут-3-ен-2-ила, 3-метилбут-2-ила, 3-метилбут-3-ен-2-ила, 3-метилбут-2-ен-2-ила, 2,3-диметилбут-2-ила, 2,3-диметилпент-2-ила, 2,3-диметилбут-3-ен-2-ила, 2,3-диметилпент-3-ен-2-ила, 2-метилпент-3-ен-2-ила, проп-2-ила, проп-1-ила, этила, циклопропила, 1,1-диметилциклопроп-2-ила, 1-метилциклопроп-2-ила, 1-метилциклопроп-1-ила, 3-тиагекс-5-ен-2-ила, 2-метил-3-тиагекс-5-ен-2-ила, 1-меркаптоэт-1-ила, 2-меркаптопроп-2-ила, 3,3,3-трифторпроп-2-ила, 2-метил-3,3,3-трифторпроп-2-ила, 1-(2-фурил)эт-1-ила, 1-(5-метилфур-2-ил)эт-1-ила, 2-(2-фурил)проп-2-ила, 1-(3-фурил)эт-1-ила, 1-(5-метилфур-3-ил)эт-1-ила, 2-(3-фурил)проп-2-ила, 1-(2-тетрагидрофурил)эт-1-ила, 2-(2-тетрагидрофурил)проп-2-ила, 1-(3-тетрагидрофурил)эт-1-ила, 2-(3-тетрагидрофурил)проп-2-ила, 1-циклопропилэт-1-ила, 2-циклопропилпроп-2-ила, 1-циклобутилэт-1-ила, 2-циклобутилпроп-2-ила, циклобутила, циклопентила, пент-2-ен-3-ила, 1-метоксипроп-1-ила, 1-метоксиэт-1-ила, 1,1,1-трифторбут-3-ила и 3-тиациклобут-1-ила.
13. Способ по любому из предшествующих пунктов, в котором соединение, имеющее формулу (V), представляет собой 2-метил-1-(2-(5-(пара-толил)-1H-имидазол-2-ил)пиперидин-1-ил)бутан-1-он, 2-(метилтио)-1-(2-(5-(пара-толил)-1H-имидазол-2-ил)пиперидин-1-ил)пропан-1-он, 2-метил-2-(метилтио)-1-(2-(5-(пара-толил)-1H-имидазол-2-ил)пиперидин-1-ил)пропан-1-он или 2,2-диметил-1-(2-(5-(пара-толил)-1H-имидазол-2-ил)пиперидин-1-ил)бут-3-ен-1-он.
| WO 2013163270 A1, 31.10.2013 | |||
| WO 2015047973 A1, 02.04.2015 | |||
| АЛЛОСТЕРИЧЕСКИЕ МОДУЛЯТОРЫ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ | 2004 |
|
RU2360902C2 |
| Link J | |||
| O | |||
| et al | |||
| Отстойник для выделения взвешенных частиц из жидкостей | 1926 |
|
SU5885A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| - Т | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| - С | |||
| Способ радиопередачи | 1924 |
|
SU2033A1 |
Авторы
Даты
2025-05-14—Публикация
2021-08-24—Подача