Изобретение относится к технике защиты черных металлов от коррозии с помощью органических ингибиторов. Оно может быть использовано для защиты различного оборудования, изготовленного из стали, перспективно для применения в травильных растворах или в буровых растворах при реализации соляно-кислотных технологий в процессе нефтедобычи, предотвращении или замедлении атмосферной коррозии конструкционных материалов на основе стали за счет создания на их поверхности наноразмерных пассивирующих пленок или в составе различных защитных лаков и грунтовок.
Широкое применение в качестве ингибиторов коррозии цветных и черных металлов находят гетероциклические органические соединения класса азолов [Кузнецов Ю.И., Казанский Л.П. Физико-химические аспекты защиты металлов ингибиторами коррозии класса азолов // Успехи химии. - 2008. - Т. 77. - №3. - С. 227-242]. Так незамещенный аминотриазол ингибирует кислотную коррозию железа и других металлов [FR 2656630 (1991 г.), RU 2539129 (2015 г.)], а также в комплексе с производными аммиака - сероводородную коррозию черных металлов [RU 2539132 (2015 г.)].
Помимо этого, находят применение в качестве ингибиторов коррозии серосодержащие соединения класса меркаптанов. Так, известно использование ингибитора на основе 2-меркапто-1-метилимидазола для защиты печатных плат от атмосферной коррозии (CN 111472002 А (2020 г.)). Ингибирующая композиция с меркаптобензотиазолом и бензотриазолом в качестве действующих компонентов описана в патенте (CN 109652809 A (2019 г.)), сообщается, что данная смесь высокоэффективна в качестве добавки к теплоносителям на основе гликолей для защиты от коррозии цветного металла в теплообменниках. Известно о проявлении защитных свойств в отношении бронзы 1Н-бензо[d]имидазол-2,6-дитиолом (CN 106674126 А (2017 г.)). Среди соединений, содержащих меркаптановый фрагмент в своей структуре, широкое применение в качестве ингибиторов коррозии находят производные L-метионина [Khaled K.F. Monte Carlo simulations of corrosion inhibition of mild steel in 0.5 M sulphuric acid by some green corrosion inhibitors // Journal of Solid State Electrochemistry. - 2009. - Vol. 13, No. 11. - P. 1743-1756], [Khaled K.F. Corrosion control of copper in nitric acid solutions using some amino acids-a combined experimental and theoretical study // Corrosion Science. - 2010. - Vol. 52. - No. 10. - P. 3225-3234.]. Наряду с защитой цветных металлов производные класса меркаптанов находят применение и в защите железобетонных конструкций, например, 5-метилмеркапто-2-меркапто-1,3,4,-тиадиазол (CN 108002730 A (2018 г.)), 5-меркапто-1-тетразол ацетат натрия (CN 103820795 A (2014 г.)), производные 2-меркаптоэтанола (AU 2012329018 A1 (2014 г.)) и пр.
Аналогами предлагаемого ингибитора являются различные 1,3,5-триазины, применение которых в среде соляной кислоты ингибирует коррозию стали. Так тиотриазинонсульфонат, как компонент композиции, ингибирующей коррозию стали, может применяться в растворах для травления металлов [CN 110318059 A (2019)], недостатками данного изобретения является необходимость применения нескольких компонентов, включая 2-меркаптобензотиазол или 2-аминобензимидазола.
Производные триазинов, описанные в работе [Experimental and quantum chemical studies of synthesized triazine derivatives as an efficient corrosion inhibitor for N80 steel in acidic medium / M. Yadav, S. Kumar, N. Tiwari, I. Bahadur, E.E. Ebenso // Journal of Molecular Liquids. - 2015. - Vol. 212. - P. 151-167], ингибируют коррозию стали в растворах, содержащих до 15% соляной кислоты, но при этом максимальная степень защиты - 93%.
Восемь аналогов предлагаемых ингибиторов описано в обзоре [Coordination bonding and corrosion inhibition potential of nitrogen-rich heterocycles: Azoles and triazines as specific examples / Chandrabhan Verma, Abhinay Thakur, Richika Ganjoo, Shveta Sharma, Humira Assad, Ashish Kumar, M.A. Quraishi, Akram Alfantazi // Coordination Chemistry Reviews. - 2023. - Vol. 488. - 215177]. При этом шесть из них эффективно ингибируют коррозию стали в растворе с низким массовым (3,6-3,7%) содержанием соляной кислоты, а два в растворе с 15% кислоты проявляют степень защиты, не превышающую 93%.
Прототипом предлагаемых ингибиторов являются гетероциклические органические соединения класса 1,3,5-триазина, содержащие в качестве заместителя амино- и меркаптогруппу, обеспечивающие высокую степень защиты стальных материалов от коррозии в кислых средах [Synthesis, experimental and theoretical studies of triazine derivatives with surface activity as effective corrosion inhibitors for medium carbon steel in acid medium / Xuemei Ma, Jingbao Wang, Siyuan Yu, Xiaojie Chen, Jun Li, Hailin Zhu, Zhiyong Hu // Journal of Molecular Liquids. - 2020. - Vol. 315. - 113711]. Однако при этом прототип проявляет ингибирующее действие в растворе с массовой концентрацией соляной кислоты 3,6-3,7%, степень защитного действия прототипа не превышает 96,7% при использовании ингибитора в количестве 0,3-0,4 г/л. Отличительной особенностью предлагаемого изобретения является использование 4-алкилтио-1,3,5-триазин-2-аминов в качестве более эффективных ингибиторов коррозии стали, обеспечивающих степень защиты до 99,6% в растворах с массовым содержанием соляной кислоты 24%.
Задачей настоящего изобретения стало расширение арсенала ингибиторов коррозии для применения в травильных растворах или в буровых растворах при реализации соляно-кислотных технологий в процессе нефтедобычи, в том числе получение более эффективных ингибиторов коррозии, относящихся к классу производных аминотриазинов и обеспечивающих снижение скорости коррозии стали в кислой среде.
Технический результат заявленного изобретения состоит в высокой степени защиты стали, составляющей - 68,1-99,6% в соответствии с результатами потенциометрических методов для концентрации ингибитора 2 г/л в условиях кислотной коррозии - растворах с массовым содержанием соляной кислоты 24%.
Согласно гравиметрическим тестам максимальную степень защиты проявляют 4-пентилтио-1,3,5-триазин-2-амин (98%) и 4-гептилтио-1,3,5-триазин-2-амин (99,3%) в концентрации 1 г/л.
Технический результат достигается тем, что в качестве ингибитора кислотной коррозии стали используют серосодержащие производные 1,3,5-триазин-2-амина общей формулы:
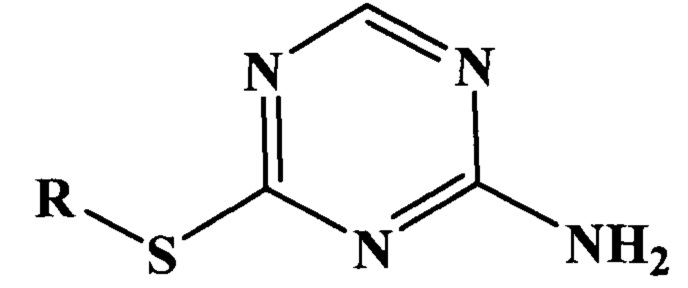 ,
,
где R представляет собой водород или CnH2n-1, где n=1-10.
Технический результат подтверждают проведенные исследования антикоррозионного действия для серосодержащих производных 1,3,5-триазин-2-амина с выявлением высокого значения ингибирующей активности.
Исследованные вещества были синтезированы на кафедре органической химии Федерального государственного бюджетного образовательного учреждения высшего образования «Воронежский государственный госуниверситет». 4-Меркапто-1,3,5-триазин-2-амин получали по известной методике [Weinreb, S.М. et al.: 2004 Science of Synthesis, 17: Category 2, Hetarenes and Related Ring Systems, ISBN 9783131836717 (17.2.3 Product Subclass 3: 1,3,5-Triazines and Phosphorus Analogues S. von Angerer)] взаимодействием амидинотиомочевины и триэтилортоформиата. 4-Алкилтио-1,3,5-триазин-2-амины получали взаимодействием эквимольных количеств 4-меркапто-1,3,5-триазин-2-амина и соответствующего алкилгалогенида в N,N-диметилформамиде в присутствии двукратного избытка триэтиламина при нагревании до 70-150°С в течение 2-4-х часов.

Для оценки защитного действия 4-меркапто-1,3,5-триазин-2-амина или 4-алкилтио-1,3,5-триазин-2-аминов использовали комплекс электрохимических и прямых коррозионных тестов.
Изобретение подтверждается проиллюстрированными чертежами, схемами, графиками, где:
на фиг. 1 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-меркапто-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-меркапто-1,3,5-триазин-2-амина.
на фиг. 2 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-метилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-метилтио-1,3,5-триазин-2-амина.
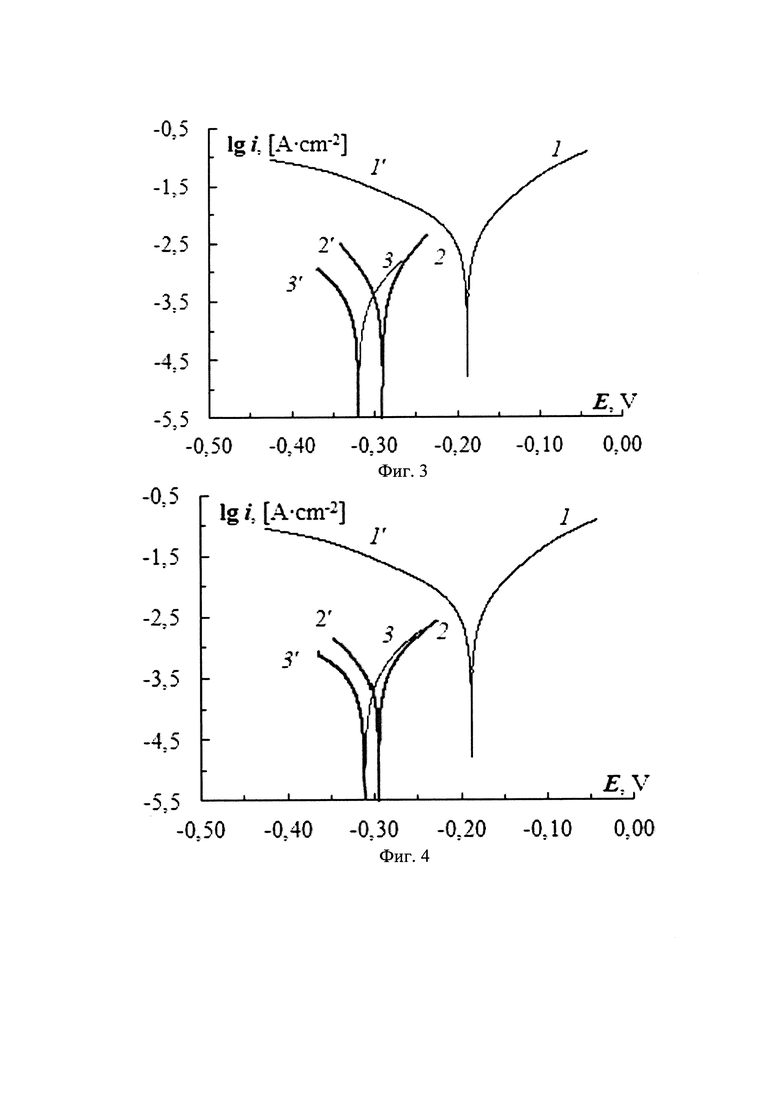
на фиг. 3 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-пропилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-пропилтио-1,3,5-триазин-2-амина.
на фиг. 4 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-бутилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-бутилтио-1,3,5-триазин-2-амина.
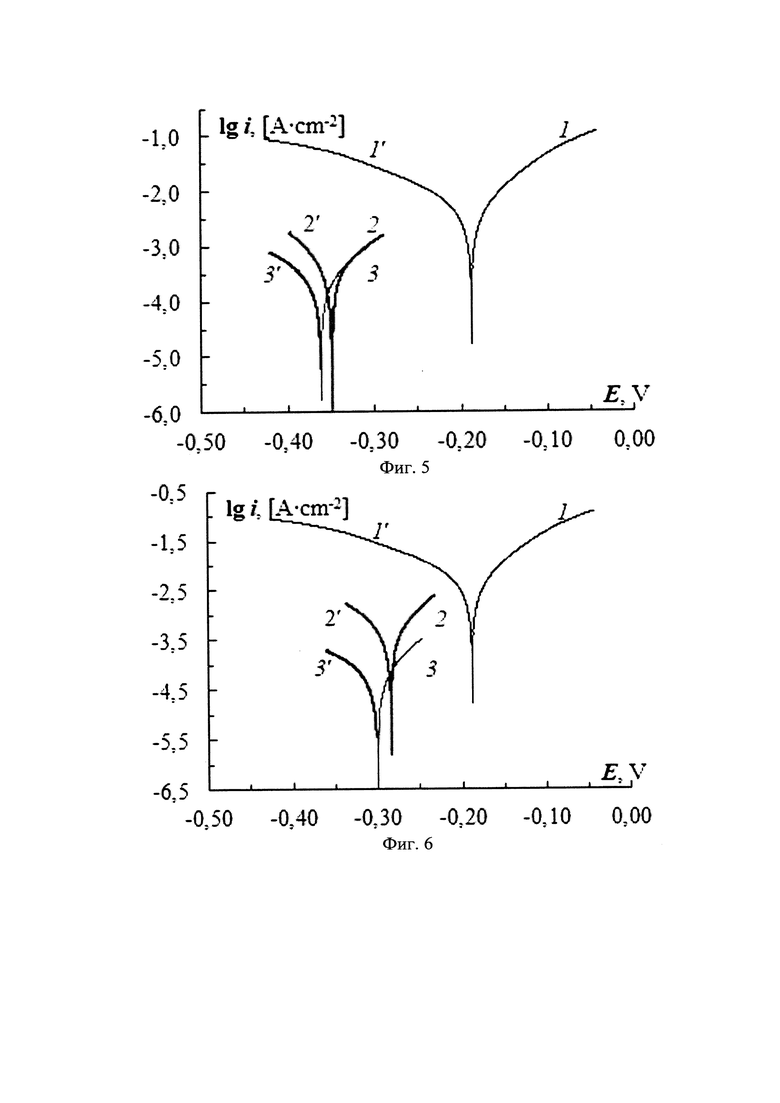
на фиг. 5 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-пентилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-пентилтио-1,3,5-триазин-2-амина.
на фиг. 6 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-изопентилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-изопентилтио-1,3,5-триазин-2-амина.
на фиг. 7 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-гептилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-гептилтио-1,3,5-триазин-2-амина.
на фиг. 8 показаны анодные (1-3) и катодные (1'-3') поляризационные кривые, полученные на низкоуглеродистой стали в 24% (масс.) растворе HCl и 1, 1' - без добавки; 2, 2' - 0,5 г/л 4-децилтио-1,3,5-триазин-2-амина; 3, 3' - 2 г/л 4-децилтио-1,3,5-триазин-2-амина.
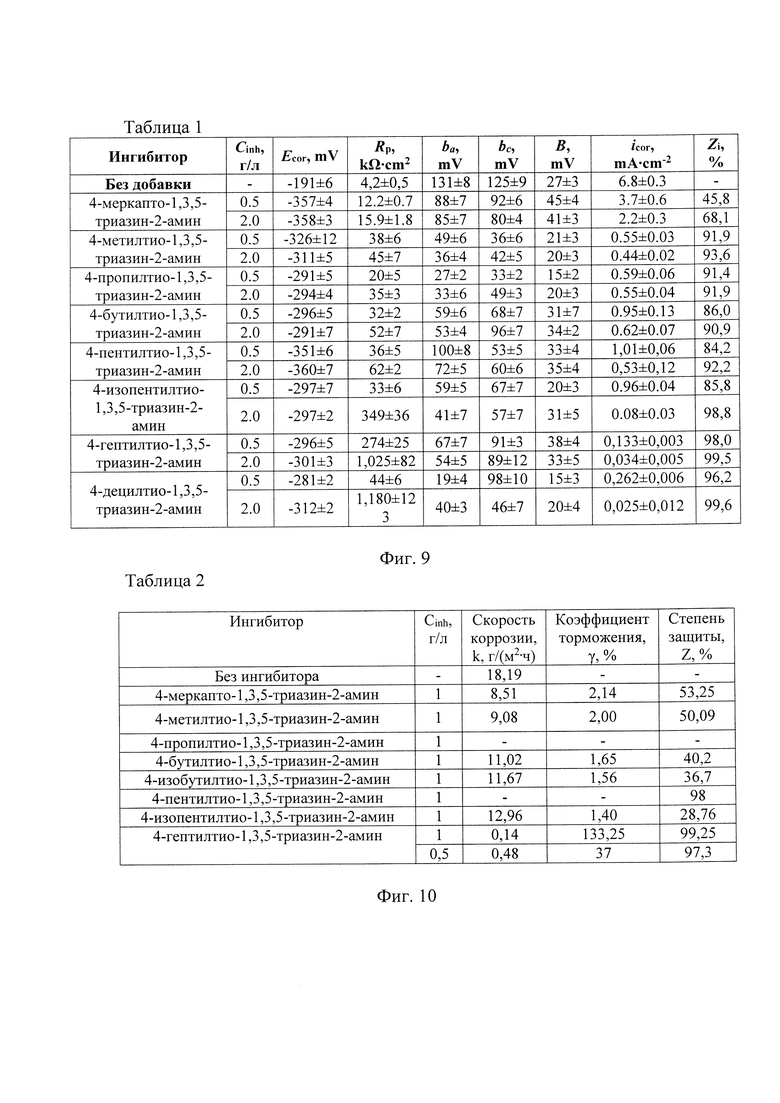
на фиг. 9 представлена таблица 1 с кинетическими параметрами коррозии электродов из низкоуглеродистой стали в 24%-ной HCl в присутствии 4-меркапто-1,3,5-триазин-2-амина или 4-алкилтио-1,3,5-триазин-2-аминов на основе данных поляризационных испытаний.
на фиг. 10 представлена таблица 2 с результатами расчетов степени защиты 4-меркапто-1,3,5-триазин-2-амина или 4-алкилтио-1,3,5-триазин-2-аминов на основе данных гравиметрических испытаний.
Ниже представлены конкретные примеры осуществления предлагаемого изобретения.
ПРИМЕР 1.
Методика синтеза 4-меркапто-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,18 г) амидинотиомочевины и 5 мл триэтилортоформиата. Смесь кипятили в течение 6 часов. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 15 мл ацетона. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 0.93 г. Выход 73%. Температура плавления 286-288°С; ЯМР 1Н (400.13 MHz, DMSO-d6), м.д.: 7.52 (1Н, с, NH); 7.74 (1Н, с, NH); 7.95 (1H, с, СН); 12.82 (1Н, с, SH). ВЭЖХ-МС, m/z ([М+Н]+), вычислено для C3H4N4S+H+ 129.0229, найдено 129.0232.
ПРИМЕР 2.
Методика синтеза 4-метилтио-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,28 г) 4-меркапто-1,3,5-триазин-2-амина, 15 мл N,N-диметилформамида, 0,02 моль (2,7 мл) триэтиламина и 0,01 моль (0,6 мл) метилйодида. Смесь перемешивали при температуре 70°С в течение 2 часов. Охлажденную смесь вылили в 100 мл холодной дистиллированной воды. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 25 мл дистиллированной воды. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 0.65 г. Выход 46%. Температура плавления 185-187°С; ЯМР 1Н (400.13 MHz, DMSO-d6): 2.39 (3Н, с, СН3); 7.51 (1H, с, NH); 7.53 (1Н, с, NH); 8.21 (1Н, с, СН). ВЭЖХ-МС, m/z ([М+Н]+), вычислено для C4H6N4S+H+ 143.0386, найдено 143.00388.
ПРИМЕР 3.
Методика синтеза 4-бутилтио-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,28 г) 4-меркапто-1,3,5-триазин-2-амина, 15 мл N,N-диметилформамида, 0,02 моль (2,7 мл) триэтиламина и 0,01 моль (1,08 мл) 1-бромбутана. Смесь перемешивали при температуре 70°С в течение 2 часов. Охлажденную смесь вылили в 100 мл холодной дистиллированной воды. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 25 мл дистиллированной воды. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 1.53 г. Выход 83%. Температура плавления 137-138°С; ЯМР 1Н (400.13 MHz, DMSO-d6): 0.86 (3Н, т, J=7.2 Гц, СН3); 1.30-1.40 (2Н, м, СН2); 1.57-1.60 (2Н, м, СН2); 3.00 (2Н, т, J=7.2 Гц, SCH2); 7.48 (1Н, с, NH); 7.51 (1Н, с, NH); 8.19 (1Н, с, СН). ВЭЖХ-МС, m/z ([М+Н]+), вычислено для C7H12N4S+H+ 185.0856, найдено 185.0861.
ПРИМЕР 4.
Методика синтеза 4-пентилтио-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,28 г) 4-меркапто-1,3,5-триазин-2-амина, 15 мл N,N-диметилформамида, 0,02 моль (2,7 мл) триэтиламина и 0,01 моль (0,87 мл) 1-йодпентана. Смесь перемешивали при температуре 70°С в течение 2 часов. Охлажденную смесь вылили в 100 мл холодной дистиллированной воды. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 25 мл дистиллированной воды. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 1.65 г. Выход 83%. Температура плавления 124-127°С; ЯМР 1Н (400.13 MHz, DMSO-d6), м.д.): 0.83 (3Н, т, J=6.8 Гц, СН3); 1.31-1.33 (4Н, м, 2СН2); 1.57-1.60 (2Н, м, СН2); 2.99 (2Н, т, J=7.2 Гц, SCH2); 7.48 (1H, с, NH); 7.51 (1H, c, NH); 8.19 (1H, с, СН). ВЭЖХ-МС, m/z ([M+H]+), вычислено для C8H14N4S+H+ 199.1012, найдено 199.1009.
ПРИМЕР 5.
Методика синтеза 4-изопентилтио-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,28 г) 4-меркапто-1,3,5-триазин-2-амина, 15 мл N,N-диметилформамида, 0,02 моль (2,7 мл) триэтиламина и 0,01 моль (1,64 мл) изопентилбромида. Смесь перемешивали при температуре 70°С в течение 2 часов. Охлажденную смесь вылили в 100 мл холодной дистиллированной воды. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 25 мл дистиллированной воды. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 1.71 г. Выход 86%. Температура плавления 144-146°С; ЯМР 1Н (400.13 MHz, DMSO-d6), м.д.): 0.90 (6Н, д, J=6.6 Гц, 2СН3); 1.49-1.54 (1Н, м, СН); 1.62-1.69 (2Н, м, СН2); 3.02-3.06 (2Н, м, SCH2); 7.45 (1Н, с, NH); 7.50 (1Н, с, NH); 8.22 (1Н, с, СН). ВЭЖХ-МС, m/z ([М+Н]+), вычислено для C8H14N4S+H+ 199.1012, найдено 199.1015.
ПРИМЕР 6.
Методика синтеза 4-гептилтио-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,28 г) 4-меркапто-1,3,5-триазин-2-амина, 15 мл N,N-диметилформамида, 0,02 моль (2,7 мл) триэтиламина и 0,01 моль (1,57 мл) 1-бромгептана. Смесь перемешивали при температуре 70°С в течение 2 часов. Охлажденную смесь вылили в 100 мл холодной дистиллированной воды. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 25 мл дистиллированной воды. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 1.79 г. Выход 79%. Температура плавления 122-124°С; ЯМР 1Н (400.13 MHz, DMSO-d6), м.д.): 0.82 (3Н, т, J=6.7 Гц, СН3); 1.22-1.27 (8Н, м, 4СН2); 1.58-1.61 (2Н, м, СН2); 2.99 (2Н, т, J=7.2 Гц, SCH2); 7.48 (1H, с, NH); 7.51 (1Н, с, NH); 8.19 (1Н, с, СН). ВЭЖХ-МС, m/z ([М+Н]+), вычислено для C10H18N4S+H+ 227.1326, найдено 227.1329.
ПРИМЕР 7.
Методика синтеза 4-децилтио-1,3,5-триазин-2-амина: в круглодонной колбе смешивали 0,01 моль (1,28 г) 4-меркапто-1,3,5-триазин-2-амина, 15 мл N,N-диметилформамида, 0,02 моль (2,7 мл) триэтиламина и 0,01 моль (2,11 мл) 1-йоддекана. Смесь выдерживали при температуре кипения растворителя (около 150°С) в течение 4 часов. Охлажденную смесь вылили в 100 мл холодной дистиллированной воды. Выпавший осадок отфильтровывали с помощью воронки фильтровальной лабораторной Шотта, промывали 25 мл дистиллированной воды. Высушивание продукта до постоянного веса проводили при температуре 40°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,005 кг/см2 (35±5 кПа).
Было выделено твердое вещество белого цвета массой 1.61 г. Выход 60%. Температура плавления 115-116°С; ЯМР 1Н (400.13 MHz, DMSO-d6), м.д.): 0.82 (3Н, т, J=6.7 Гц, СН3); 1.21-1.34 (14Н, м, 7СН2); 1.57-1.61 (2Н, м, СН2); 2.99 (2Н, т, J=7.2 Гц, SCH2); 7.47 (1Н, с, NH); 7.51 (1Н, с, NH); 8.19 (1H, с, СН). ВЭЖХ-МС, m/z ([М+Н]+), вычислено для C13H24N4S+H+ 269.1795, найдено 269.1799.
ПРИМЕР 8
Поляризационные кривые получали на электроде из стали марки Ст3 (площадью 1,0 см2) в электрохимической ячейке с неразделенными электродными пространствами на потенциостате IPC-PRO. Рабочий электрод предварительно зачищали на наждачной бумаге К2000 и обезжиривали этиловым спиртом. Потенциалы электрода (Е) измеряли относительно хлоридсеребряного электрода, соединяя пространство электрохимической ячейки и электрода сравнения посредством электролитического моста на основе агар-агара и нитрата натрия, и пересчитывали на шкалу стандартного водородного электрода (ст.в.э.) (потенциал +202 мВ относительно ст.в.э. Вспомогательный электрод - платиновая сетка.
Исследуемые вещества вводили в кислоту до получения необходимой концентрации. В готовый раствор помещали электроды и выдерживали до наступления стационарного состояния в течение 30 минут. После установления значения потенциала коррозии (Екор) получали поляризационные кривые со скоростью сканирования потенциала 0.2 мВ/с в анодном и катодном направлениях. Поляризационные кривые регистрировали до достижения плотности тока (i) 0.1 А⋅см-2.
Расчет скорости коррозии по методу поляризационного сопротивления
Скорость коррозии в токовых единицах определяли методом поляризационного сопротивления в соответствии с расчетной процедурой Ф. Мансфельда [F. Mansfeld, Tafel slopes and corrosion rates obtained in the pre-Tafel region of polarization curves, Corrosion Science, 2005, 47, no. 12, 3178-3186].
Исследования проводили с помощью трехэлектродной ячейки с неразделенным катодным и анодным пространствами без перемешивания в условиях естественной аэрации, электрод сравнения - хлоридсеребряный (потенциал +202 мВ относительно ст.в.э.), вспомогательный электрод - платиновая сетка. Электрод сравнения отделяли от ячейки электролитическим мостом, изготовленным на основе агар-агара и NaNO3.
Рабочий электрод предварительно зачищали на наждачной бумаге Р2000, обезжиривали этиловым спиртом (96%) и промывали дистиллированной водой. В готовый раствор помещали электроды и выдерживали до наступления стационарного состояния в течение 30 минут. По достижении стационарного состояния производили поляризацию электрода в интервале±30 мВ от значения Екор в потенциодинамическом режиме со скоростью сканирования 0.2 мВ/с.
Поляризационное сопротивление Rp определяли как наклон поляризационной кривой в точке Eкор в координатах ΔЕ - I, где ΔЕ - разница текущего потенциала электрода и потенциала коррозии (Е-Екор), I - сила электрического тока в измерительной цепи. Далее перестраивали зависимость в координатах 2.3⋅Rp⋅I - ΔЕ. Коэффициенты ba и bc (тафелевские наклоны катодного и анодного участков поляризационной кривой) определяли с помощью программы TableCurve 2D как параметры аппроксимации уравнения:

Ток коррозии рассчитывался с учетом полученных коэффициентов по уравнению:

где В - коэффициент Штерна-Гири, расчитывается по формуле:

Для возможности сравнения данных, получаемых в различных исследованиях, далее будут представлены значения плотности тока коррозии (icor), рассчитываемые по выражению:

где S - геометрическая площадь электрода. Для удобства дальнейшего сравнения полученных данных рассчитывали отношение плотности тока коррозии каждого исследованного образца к плотности тока фонового эксперимента 6.8 мА/см2):

Измерения для каждой концентрации вещества производили не менее 5 раз до получения воспроизводимых данных с их последующей статистической обработкой результатов измерения.
Введение всех исследованных веществ для всех концентраций Cinh=0.5-2.0 г/л приводит к смещению Ecor в область более отрицательных значений на 100-160 мВ (фиг 9, таблица 1). Можно предположить преимущественное влияние на катодную полуреакцию восстановления окислителя (Н+), которое связано с адсорбцией на поверхности стали посредством несвязанных электронных пар гетероатомов, а также π-электронов триазинового фрагмента [A. Singh, K.R. Ansari, D.S. Chauhan, M.A. Quraishi, H. Lgaz, I.-M. Chung, Comprehensive investigation of steel corrosion inhibition at macro/micro level by ecofriendly green corrosion inhibitor in 15% HCl medium, J. Colloid Interface Sci. 560 (2020) 225-236, https://doi.org/10.1016/j.jcis.2019.10.040].
При этом для всех случаев наблюдали снижение плотности тока не только на катодных, но и на анодных участках поляризационных кривых относительно контрольного эксперимента без добавки (фиг. 1-фиг. 8). В общем случае, значения плотности тока снижаются по мере увеличения длины алкильного радикала при заданной поляризации относительно Ecor. При увеличении концентрации добавки плотность тока также снижается.
На основании полученных поляризационных кривых рассчитали кинетические параметры в присутствии исследуемых веществ (фиг. 9, таблица 1). Для вещества 4-меркапто-1,3,5-триазин-2-амина, не имеющего алкильного заместителя у атома серы, получены наиболее низкие значения степени защиты Zi до 68% при Ginh=2.0 г/л. При включении в структуру алкильного заместителя для короткоцепочечного, например, метальной группы уже при Cinh - 0.5 г/л наблюдали увеличение степени защиты до 91%. Использование всех 4-алкилтио-1,3,5-триазин-2-аминов характеризуется значениями Zi в диапазоне 84,2-98,0% при Cinh=0.5 г/л и 90,9-99,6% при Cinh=2.0 г/л.
Для 4-гептилтио-1,3,5-триазин-2-амина и 4-децилтио-1,3,5-триазин-2-амина с наибольшей длиной алкильного заместителя получена наилучшая степень защиты до 99,5-99,6% при Cinh=2.0 г/л. При этом для получения раствора 4-децилтио-1,3,5-триазин-2-амина с концентрацией Cinh=2.0 г/л необходим дополнительный нагрев раствора. При его длительном хранении возможно выпадение осадка ингибитора. Такой эффект может представлять сложности при практическом использовании вещества 4-децилтио-1,3,5-триазин-2-амина.
Полученные значения степени ингибирования позволяют рассматривать данные соединения как потенциальные эффективные ингибиторы коррозии стали в кислой среде. При этом, наилучший эффект достигается при использовании 4-гептилтио-1,3,5-триазин-2-амина
ПРИМЕР 9
Гравиметрические прямые коррозионные испытания проводили на стальных пластинах (Ст3) (20×40 мм, толщина 1,2 мм). Каждый образец предварительно полировали мелкозернитой шлифовальной бумагой К 1000, после чего промывали дистиллированной водой, этанолом и сушили фильтровальной бумагой. Эксперименты проводили в 24%-ном растворе HCl (в течение 7 суток) при естественной аэрации без перемешивания для трех образцов параллельно (для каждой концентрации ингибитора). После испытаний пластины промывали дистиллированной водой и обрабатывали в соответствии с требованиями ГОСТ 9.907-83 «Методы утилизации изделий после коррозионных испытаний».
Скорость коррозии определяли по потере массы образцов и рассчитывали по формуле

где Δm=m0-m (m0 - масса образца до начала эксперимента, m - масса образца после испытаний,), S - суммарная площадь поверхности пластинки, м2, t - время, сут.
Для каждого раствора определяли скорость коррозии k0 без добавки ингибитора (k0(сред) ≈16.9±0.5 г/м2⋅сут - среднее значение скорости коррозии без добавки ингибитора, полученное в ходе проведенных исследований). Эффективность ингибирующего действия производных аминотриазола оценивали по величине коэффициента торможения:

и степени защиты:

где k0 и  - скорость коррозии в фоновом растворе и в растворе с ингибитором соответственно.
- скорость коррозии в фоновом растворе и в растворе с ингибитором соответственно.
Измерения для каждой концентрации вещества производили не менее 5 раз до получения воспроизводимых данных с их последующей статистической обработкой результатов измерения (фиг. 10, таблица 2).
Все синтезированные соединения проявляют хорошее антикоррозионное действие в концентрации 0,5-2 г/л. В целом эта группа ингибиторов позволяет добиться степени защиты выше 95%. Удлинение УВ-радикала до С10 снижает растворимость соединений и затрудняет получение раствора с нужной концентрацией. Короткоцепочечные заместители С1-С4 менее эффективны. Оптимальной длиной углеводородного радикала в алифатическом заместителе, позволяющей достичь степени защиты более 99,5% является С5-С7.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР КОРРОЗИИ МЕДИ И МЕДЬСОДЕРЖАЩИХ СПЛАВОВ | 2022 |
|
RU2813268C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРА КОРРОЗИИ СТАЛЬНОЙ АРМАТУРЫ В БЕТОНЕ | 2023 |
|
RU2839012C1 |
| ИНГИБИТОРЫ КОРРОЗИИ МЕДИ И МЕДЬСОДЕРЖАЩИХ СПЛАВОВ НА ОСНОВЕ 5-АЛКИЛСУЛЬФИНИЛ-3-АМИНО-1,2,4-ТРИАЗОЛОВ | 2018 |
|
RU2690124C1 |
| ИНГИБИТОРЫ КОРРОЗИИ МЕДИ И МЕДЬСОДЕРЖАЩИХ СПЛАВОВ НА ОСНОВЕ 5-АЛКИЛСУЛЬФОНИЛ-3-АМИНО-1,2,4-ТРИАЗОЛОВ | 2018 |
|
RU2689831C1 |
| ИНГИБИТОР КОРРОЗИИ МЕДИ И МЕДЬСОДЕРЖАЩИХ СПЛАВОВ В НЕЙТРАЛЬНЫХ РАСТВОРАХ ХЛОРИДОВ (ВАРИАНТЫ) | 2017 |
|
RU2679022C2 |
| КОНЦЕНТРАТ ИНГИБИТОРОВ КОРРОЗИИ | 2008 |
|
RU2362792C1 |
| Способ получения производных 1,2,4-триазолов с замещенными азагетероциклическими радикалами | 2024 |
|
RU2839001C1 |
| СПОСОБ ОЦЕНКИ ЗАЩИТНОЙ КОНЦЕНТРАЦИИ ЛЕТУЧИХ ИНГИБИТОРОВ КОРРОЗИИ В ФАЗОВОЙ ПЛЕНКЕ ВЛАГИ, ФОРМИРУЮЩЕЙСЯ НА ПОВЕРХНОСТИ МЕТАЛЛА | 2016 |
|
RU2619138C1 |
| Водный раствор ингибиторной композиции для формирования антикоррозионной ингибированной полимерной пленки на поверхности изделий из низкоуглеродистой стали и способ его применения для формирования антикоррозионной ингибированной полимерной пленки | 2023 |
|
RU2812428C1 |
| ИНГИБИТОР СОЛЯНОКИСЛОЙ КОРРОЗИИ СТАЛИ | 2021 |
|
RU2776118C1 |


Изобретение относится к технике защиты черных металлов от коррозии с помощью органических ингибиторов и может быть использовано для защиты различного оборудования, изготовленного из стали, перспективно для применения в травильных растворах или в буровых растворах при реализации соляно-кислотных технологий в процессе нефтедобычи, предотвращения или замедления атмосферной коррозии конструкционных материалов на основе стали за счет создания на их поверхности наноразмерных пассивирующих пленок или в составе различных защитных лаков и грунтовок. Предложено применение серосодержащих производных 1,3,5-триазин-2-амина общей формулы

в которой R представляет собой водород или CnH2n-1, где n=1-10, в качестве ингибитора кислотной коррозии стали. Изобретение позволяет расширить арсенал эффективных ингибиторов коррозии металлов. Технический результат состоит в высокой степени защиты стали - 68,1-99,6% в соответствии с результатами потенциометрических методов для концентрации ингибитора 2 г/л в условиях кислотной коррозии - растворах с массовым содержанием соляной кислоты 24%. 10 ил., 9 пр.
Применение серосодержащих производных 1,3,5-триазин-2-амина общей формулы
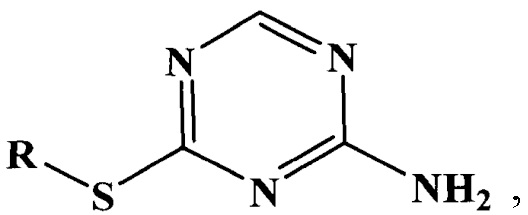
в которой R представляет собой водород или CnH2n-1, где n=1-10, в качестве ингибитора кислотной коррозии стали.
| XUEMEI MA et.al | |||
| Synthesis, experimental and theoretical studies of triazine derivatives with surface activity as effective corrosion inhibitors for medium carbon steel in acid medium | |||
| Journal of Molecular Liquids, 2020, Vol | |||
| Способ очищения амида ортотолуолсульфокислоты | 1921 |
|
SU315A1 |
| YADAV M | |||
| et.al | |||
| Experimental and quantum chemical studies of synthesized triazine derivatives as an efficient | |||
Авторы
Даты
2025-05-23—Публикация
2024-07-24—Подача