Изобретение относится к биотехнологии, а именно к биопрепаратам, предназначенным для перепрограммирования иммунитета в противоопухолевом направлении и используемого в комплексной терапии онкозаболеваний, способствующего уменьшению размеров первичного опухолевого очага и снижению количества метастазов.
В настоящее время противоопухолевая иммунотерапия - перспективный метод лечения злокачественных новообразований. Активная иммунотерапия включает использование цитокинов, некоторых бактериальных препаратов, синтетических молекул и гормонов тимуса, противовирусных и противоопухолевых вакцин [1]. Пассивная иммунотерапия основана на адаптивной иммунотерапии [2] и использовании моноклональных антител [3]. Сочетание методов активации специфического и неспецифического иммунитета можно считать перспективным направлением развития иммунотерапии опухолей. Такой подход помогает не только эффективно уничтожать опухолевые клетки в организме, в том числе метастазы, но и позволяет значительно снизить риск рецидива заболевания за счет развития иммунологической памяти [4].
Наиболее близким к изобретению является препарат субалин, основу которого составляет штамм Bacillus subtilis. Под действием интерферона, продуцируемого бактериями субалина в кишечнике и действующего локально на уровне иммунной системы слизистой кишечника, происходит активация иммунокомпетентных клеток крови к синтезу комплекса эндогенных цитокинов, представленного ФНО-α, ИФН-γ, ИФН-α, ИЛ-1β, ИЛ-2, ИЛ-4, который обеспечивает системные реакции организма. Введение субалина перорально повышает активность естественных киллеров и цитостатических эффекторов селезенки, цитостатическое действие перитонеальных макрофагов, стимулирует пролиферативную активность Т- и В-лимфоцитов, ускоряет формирование антиген - специфического клеточно-опосредованного иммунного ответа [5]. Субалин применяется для нормализации микрофлоры кишечника, предупреждению и коррекции дисбиоза, снижению уровня эндогенной интоксикации, повышает сопротивляемость организма вирусным инфекциям у животных и человека [6, 7].
Задачей изобретения является создание биопрепарата в виде лиофизизата для приготовления суспензии для приема внутрь в комбинированной терапии онкозаболеваний. Поставленная задача решается применением лиофилизата, который содержит в качестве основы культуру B.subtilis 2335 рВМВ105, характеризующуюся выраженной иммуномодулирующей активностью за счет продукции α-интерферона, что приводит к ингибированию роста и метастазирования злокачественных опухолей.
Лиофилизат содержит в качестве основы живые клетки B.subtilis 2335 рВМВ105 и наполнитель. Биомасса B.subtilis 2335 рВМВ105 составляет 1⋅109 живых микробных клеток. Необходимость наполнителя обусловлена его защитным действием для бактериальных клеток и повышением стабильности при хранении. В качестве наполнителя лиофилизат может содержать сыворотку крупного рогатого скота, молоко, сахарожелатиновую смесь в различных концентрациях и пропорциях.
Культура, составляющая основу лиофилизата, характеризуется следующими свойствами: B.subtilis 2335 рВМВ105 - грамположительные аэробные спорообразующие палочки, продуцирующие каталазу. На МПА, сусло-агаре, среде Громыко, картофельном агаре, а также на средах с добавлением 50 мкг/мл канамицина растет обильно, образуя матовые колонии телесного, сероватого цвета, легко снимаются петлей.
В мазках из колоний, выросших на картофельном агаре через 18 ч, обнаруживаются прямые палочковидные клетки размером 2,7×0,8 мкм, расположенные одиночно или в виде коротких и длинных цепочек. Клетки подвижны. Образуют аэробно споры овальной формы, которые располагаются в клетке центрально. При спорообразовании клетки не раздуваются. После роста на глюкозном агаре в протоплазме не обнаруживаются включения поли-β-оксимасляной кислоты. На МПБ культура образует пленку. Не растет в анаэробных условиях, не гидролизует мочевину. Дает положительную реакцию Фогес-Проскауэра. Растет в присутствии 7% NaCl. Гидролизует крахмал и казеин, разжижает желатину. При росте на МПБ образует Аммиак, не образует сероводород и индол. Ферментирует лактозу, глюкозу, арабинозу, ксилозу, маннит с образованием кислоты без газа. Редуцирует нитраты, обесцвечивает метиленовую синь. Коагулазной, гиалуронидазной, лецитиназной активностью не обладает.
Пример 1. На основе штамма B.subtilis 2335 рВМВ105 с типичными морфологическими, культурными, биохимическими свойствами приготовлены три варианта лиофилизата для приготовления суспензии для приема внутрь с одинаковым содержанием микробных клеток в составе и различным соотношением вспомогательных веществ.
Вариант 1. Лиофилизат, содержащий, г
Биомасса B.subtilis 2335 рВМВ105 в количестве 0,0020 (что соответствует 1⋅109 живых микробных клеток).
Наполнитель: желатин 0,0060, натрий хлористый 0,0017, сахароза 0,0200.
Вариант 2. Лиофилизат, содержащий, г
Биомасса B.subtilis 2335 рВМВ105 в количестве 0,0020 (что соответствует 1⋅109 живых микробных клеток).
Наполнитель: желатин 0,0060, натрий хлористый 0,0017, лактоза 0,0200. Вариант 3. Лиофилизат, содержащий, г
Биомасса B.subtilis 2335 рВМВ105 в количестве 0,0020 (что соответствует 1⋅109 живых микробных клеток).
Наполнитель: желатин 0,0080, сахароза 0,0300.
Изготовленные варианты препарата помещали в стерильные ампулы и запаивали.
Проверяли безопасность полученных вариантов препаратов (тест на аномальную токсичность), а также специфическую антибластомную и антиметатстатическую активность.
Для определения аномальной токсичности полученных вариантов смеси лиофилизата и наполнителей, содержимое ампулы растворяли в 0,5 мл воды дистиллированной и вводили полученный объем перорально мышам. Для каждого варианта использовали не менее 10 мышей массой 20-23 г. Биопрепарат считался безвредным, если все мыши выживали и не проявляли признаков неблагополучия в течение 5 суток наблюдения.
Для определения специфической активности исследовали антибластомную и антиметастатическую активность вариантов препарата на модели гематогеннометастазирующей карциномы легких Льюис (LLC).
Исследование выполнено на мышах самках SPF-категории, которых содержали в виварии при регулируемом световом режиме (12:12 ч), на стандартном рационе питания и со свободным доступом к воде. Использовано 80 мышей-самок линии С57 В1/6 массой 18-22 г, полученных из «SPF-виварий» ИЦиГ СО РАН. Для исследования использовали эпидермоидную LLC. Эта модель опухолевого роста мышей широко применяется в экспериментальной онкологии [8]. Для трансплантации опухолевую ткань рака легкого мыши LLC измельчали ножницами до гомогенной консистенции, помещали на клеточный фильтр (100 мкм), смешивали со средой 199 и производили гомогенизацию. Полученную суспензию опухолевых клеток в среде центрифугировали 1400 об/мин 10 минут, удаляли надосадочную жидкость, ресуспендировали клеточный осадок. Полученную суспензию клеток вводили подкожно в область правой боковой поверхности в количестве 4×106 клеток в объеме 0,5 мл всем группам животных.
Через 24 часа после перевивки опухолевых клеток животные были распределены на 8 экспериментальных групп (n=10):
Группа 1 (контроль) - внутрижелудочное введение растворителя исследуемого лиофилизата в течение 21 суток, резекция опухоли не проводилась;
Группа 2 - внутрижелудочное введение исследуемого лиофилизата состава Вариант 1 в течение 21 суток, резекция опухоли не проводилась;
Группа 3 - внутрижелудочное введение исследуемого лиофилизата состава Вариант 2 в течение 21 суток, резекция опухоли не проводилась;
Группа 4 - внутрижелудочное введение исследуемого лиофилизата состава Вариант 3 в течение 21 суток, резекция опухоли не проводилась;
Группа 5 (контроль) - внутрижелудочное введение растворителя исследуемого лиофилизата в течение 21 суток, резекция опухоли на 7 сутки;
Группа 6 - внутрижелудочное введение исследуемого лиофилизата состава Вариант 1 в течение 21 суток, резекция опухоли на 7 сутки;
Группа 7 - внутрижелудочное введение исследуемого лиофилизата состава Вариант 2 в течение 21 суток, резекция опухоли на 7 сутки;
Группа 8 - внутрижелудочное введение исследуемого лиофилизата состава Вариант 3 в течение 21 суток, резекция опухоли на 7 сутки;
На 7, 10, 14 и 18 сутки после перевивки опухоли у экспериментальных животных 1-4 групп определяли линейные размеры опухоли, такие как длина, ширина и высота с помощью электронного цифрового штангенциркуля.
Резекция опухоли всем животным 5-8 групп проводилась на 7 сутки от начала эксперимента под ингаляционным наркозом (изофлуран, Испания).
На 21 сутки от начала эксперимента всех животных подвергали эвтаназии передозировкой наркозного средства. После эвтаназии животных были собраны образцы легких, в которых подсчитывались субплевральные метастазы с помощью электронного цифрового штангенциркуля и операционного микроскопа (Carl Zeiss, Германия).
Противоопухолевое влияние оценивали по торможению роста опухоли (ТРО): ТРО=(Vo-Vk)/Vk×100%, где Vk - объем опухоли в контроле, Vo - объем опухоли в опыте. Для оценки антиметастатического действиявычисляли индекс ингибиции метастазирования (ИИМ, %) и индекс торможения роста метастазов (ТРМ, %) по формулам: ИИМ=(Ак*Вк-А*В)/Ак*Вк×100%, где Ак, А - процент мышей с метастазами в контрольной и опытной группах, Вк, В - количество метастатических колоний в легких. TPM=(Sk-So)/Sk×100%, где Sk, So - средняя площадь метастатических колоний в контрольной и опытной группах в мм2.
Статистическую обработку полученных результатов проводили в программе SPSS Statistics 23 (IBM). Для сравнения нескольких независимых групп применялся непараметрический критерий Краскела-Уоллиса с последующим использованием критерия Манна-Уитни для попарного сравнением групп. При сравнении нескольких групп исследования использовали поправку на множественное сравнение FDR. Данные представлены в виде медианы (Me) и квартилей (Q1-Q3). Статистически значимые считали различия при уровне значимости р<0,05.
Результаты исследований аномальной токсичности и специфической активности вариантов биопрепарата представлены в примерах 2-5.
Пример 2. Все исследуемые варианты биопрепарата не обладают аномальной токсичностью. Внутрижелудочное однократное введение всех исследуемых образцов не приводило к гибели экспериментальных животных в течение 5 суток. Признаков неблагополучия также не наблюдалось во всех испытуемых группах. Результаты исследования аномальной токсичности вариантов биопрепарата на основе лиофилизата B.subtilis 2335 рВМВ105 представлены в таблице 1.
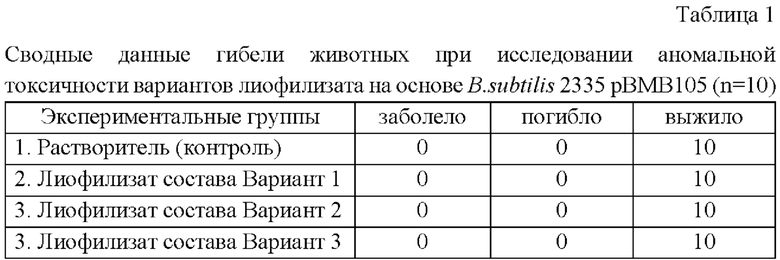
Пример 2.
Внутрижелудочное введение лиофилизата на основе B.subtilis 2335 рВМВ105 способствует уменьшению объема опухоли на 14 и 18 сутки после перевивки. Наибольшее уменьшение размера опухоли на 18 сутки регистрировалось при использовании лиофилизата состава Вариант 1 (0,43±0,07 см3) (таб. 2).
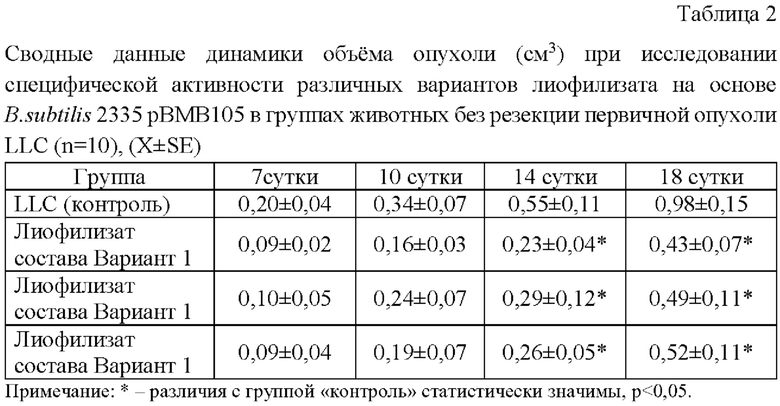
Пример 3.
Лиофилизат на основе B.subtilis 2335 рВМВ105 оказывал противоопухолевое действие в модели без резекции первичной опухоли LLC. Наибольшее торможение опухолевого процесса регистрировалось при использовании лиофилизата состава Вариант 1 (54%) (таб. 3).

Пример 4.
Лиофилизат на основе B.subtilis 2335 рВМВ105 оказывал противоопухолевое и антиметастатическое действие в модели с резекцией первичной опухоли LLC. Наибольшее ингибирование метастазирования торможение роста метастазов регистрировалось при использовании лиофилизата состава Вариант 1 (88,4% и 70,4%) соответственно) (таб. 4).
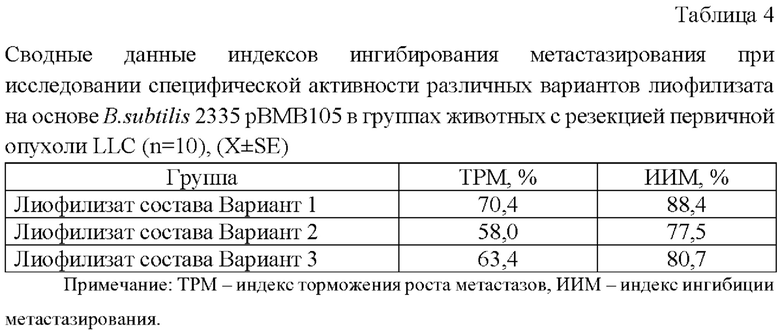
Таким образом, полученные данные свидетельствуют о том, что исследованные варианты биопрепарата в виде лиофилизата на основе B.subtilis 2335 рВМВ105 не обладают аномально токсичностью и характеризуются наличием противоопухолевой и антиметататической активностей.
Список используемых источников:
1. Baxevanis C.N., Perez S.A., Papamichail М. Cancer immunotherapy / Critical Reviews in Clinical Laboratory Sciences. - 2009. - Vol. 46, N. 4. - P. 167-189/
2. Prospects in adoptive cell transfer therapy for cancer / Li Y., Huang Q., Zhong Y. et all. // J. Immunol. Clin. Res. - 2013. - Vol. 1. - P. 1008.
3. Immunostimulatory monoclonal antibodies for cancer therapy / Melero I., Hervas-Stubbs S., Glennie M. et all. // Nat. Rev. Cancer - 2007. - Vol. 7., N. 2. - P. 95-106.
4. Immunotherapy of Cancer (Review) / Yuzhakova D.V., Shirmanova M.V., Sergeeva T.F. et all. // Modern technology in medicine. - 2016. - Vol. 8., N. 1. - P. 173-182
5. Чердынцева H.B., Литвяков H.B., Смольянинов E.C., Белявская В.А. Влияние рекомбинантного пробиотика субалина на функциональную активность иммунокомпетентных клеток // БЭБиМ. - 1999. - Т. 127. - Приложение 1. - С. 67-70.
6. В.В. Смирнов, С.Р. Резник, И.Б. Сорокулова, Л.С.Сандахчиев, В.А. Петренко, А.А. Ильичев, В.Н. Белявская, И.В. Тимофеев «Профилактический биопрепарат субалин», RU 2035185 C1, МПК A61K 35/66, публ. 20.05.1995.
7. Русакова Я.Л., Казаков О.В., Белявская В.А. Биомедицинский потенциал спорового рекомбинантного штамма Bacillus subtilis 2335/105 в составе субалина® как живой терапевтический системы доставки альфа-интерферона при вирусных лейкозах: оценка влияния на иммунные клетки и органы мышей в эксперименте вирусного лейкоза / Инновации и продовольственная безопасность. - 2019. - №2(24). - С. 85-93.
8. Трещалина Е.М., Жукова О.С., Герасимова Г.К. и др. Методические рекомендации по доклиническому изучению противоопухолевых лекарственных средств. В кн.: Руководство по проведению доклинических исследований лекарственных средств. Ч. 1. Под ред. А.Н. Миронова, И.Д. Бунятян, А.Н. Васильева и др. М.: Гриф и К, 2012. С. 642-57.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОБИОТИЧЕСКИЙ ПРЕПАРАТ КОМПЛЕКСНОГО ДЕЙСТВИЯ | 1999 |
|
RU2159625C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ИЗ БАКТЕРИЙ РОДА BACILLUS | 2001 |
|
RU2181596C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЙ БИОПРЕПАРАТ | 1999 |
|
RU2172175C1 |
| БИОПРЕПАРАТ БАЛИС ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ | 2010 |
|
RU2454238C1 |
| БИОПРЕПАРАТ "ИРИЛИС" НА ОСНОВЕ БАКТЕРИЙ РОДА BACILLUS ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ И ДИСБИОЗА РАЗЛИЧНОЙ ЭТИОЛОГИИ И ШТАММЫ БАКТЕРИЙ BACILLUS SUBTILIS И BACILLUS LICHENIFORMIS, ИСПОЛЬЗУЕМЫЕ ДЛЯ ИЗГОТОВЛЕНИЯ БИОПРЕПАРАТА | 2003 |
|
RU2264454C2 |
| БИОПРЕПАРАТ "ИРИЛИС" ВЕТЕРИНАРНОГО НАЗНАЧЕНИЯ | 2003 |
|
RU2264453C2 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЙ БИОПРЕПАРАТ ПРОТИВ БАКТЕРИАЛЬНЫХ И ГРИБКОВЫХ ИНФЕКЦИЙ, ОБЛАДАЮЩИЙ АНТИБИОТИКОУСТОЙЧИВОСТЬЮ | 2010 |
|
RU2444366C1 |
| СПОРОВЫЙ ПРОБИОТИК КОМПЛЕКСНОГО ДЕЙСТВИЯ | 2008 |
|
RU2388813C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЙ БИОПРЕПАРАТ "БАКТИСПОРИН" | 1997 |
|
RU2130316C1 |
| БИОПРЕПАРАТ ДЛЯ ЗАЩИТЫ РАСТЕНИЙ ОТ ГРИБНЫХ И БАКТЕРИАЛЬНЫХ БОЛЕЗНЕЙ | 2001 |
|
RU2201678C2 |
Изобретение относится к биотехнологии. Предложен лиофилизат на основе Bacillus subtilis 2335 pBMB105 для перепрограмирования иммунитета в противоопухолевом направлении при следующем составе компонентов, г: биомасса штамма бактерий B Bacillus subtilis 2335 рВМВ105 в количестве 0,0020, что соответствует 1⋅109 живых микробных клеток; наполнитель: желатин 0,0060, натрий хлористый 0,0017, сахароза 0,0200. Изобретение обеспечивает расширение арсенала средств, характеризующихся выраженной иммуномодулирующей активностью, для использования в комплексной терапии онкозаболеваний. 4 табл., 4 пр.
Лиофилизат на основе Bacillus subtilis для перепрограммирования иммунитета в противоопухолевом направлении, включающий живую биомассу Bacillus subtilis и наполнитель, отличающийся тем, что он содержит биомассу штамма бактерий B.subtilis 2335 рВМВ105 при следующем составе компонентов, г:
биомасса B.subtilis 2335 рВМВ105 в количестве 0,0020, что соответствует 1⋅109 живых микробных клеток;
наполнитель: желатин 0,0060, натрий хлористый 0,0017, сахароза 0,0200.
| ЧЕРДЫНЦЕВА Н.В | |||
| и др | |||
| "Влияние рекомбинантного пробиотика субалина на функциональную активность иммунокомпетентных клеток"; Бюллетень экспериментальной биологии и медицины, 1999, N S1, с.67-70 | |||
| ЛИТВЯКОВ Н.В | |||
| и др | |||
| "Роль макрофагов в реализации антибластного действия рекомбинантного пробиотика субалина"; Вопросы онкологии, 2001, том 47, N 1, |
Авторы
Даты
2024-06-17—Публикация
2023-12-15—Подача