Изобретение относится к химико-фармацевтической промышленности и представляет собой способ получения препарата для влажного ранозаживления на основе модифицированной гиалуроновой кислоты и активного йода.
Гиалуроновая кислота - природный полисахарид, состоящий из повторяющегося звена, представляющего собой остатки D-глюкуроновой кислоты и D-N-ацетилглюкозамина, соединенных поочередно β-1,4- и β-1,3-гликозидными связями. Гиалуроновая кислота широко распространена в природе, является основным компонентом синовиальной жидкости и хрящей человека, так как благодаря своей высокой молекулярной массе, достигающей 20000 кДа, образует растворы высокой вязкости. Ввиду своей низкой токсичности широко используется в медицине и косметологии. Например, получена инъекционная композиция для ухода за кожей лица, представляющая собой раствор гиалуроновой кислоты в водном изотоническом растворе хлорида натрия для коррекции лицевых изъянов в виде морщин и складок, а также для улучшения формы и объема губ и предотвращения процессов старения кожи [Патент №2159111 С1 Российская Федерация, МПК A61K 31/715, A61K 9/08, A61K 31/728. композиция для ухода за кожей лица: №99116548/14: заявл. 02.08.1999: опубл. 20.11.2000 / Е.М. Лебедева, И.А. Федорищев; заявитель Общество с ограниченной ответственностью "Новые медицинские технологии", Общество с ограниченной ответственностью Научно-производственное предприятие "Тульская индустрия LTD".].
Кроме нативных форм кислоты или соли в медицине используются и химически модифицированные производные полисахарида. Например, поперечно сшитые диаминами различного строения макромолекулы гиалуроновой кислоты применяются в качестве заменителей синовиальной жидкости, жидкой части стекловидного тела, в качестве матриц в формах с контролируемым высвобождением, в качестве заживляющих и противосклеивающих агентов, для получения протеза сосудов, биогибридных органов, заживляющих устройств, офтальмологических и отиатрических композиций, протеза, имплантатов и медицинских устройств [Патент №2230752 С2 Российская Федерация, МПК A61L 27/00, A61K 9/20, A61K 31/728. Поперечносшитые гиалуроновые кислоты и их применение в медицине: №2001112488/04: заявл. 08.11.1999: опубл. 20.06.2004 / Р. Барбуччи, Р. Рапуоли.]. Известен способ применения сульфатированной гиалуроновой кислоты в качестве регулятора цитокиновой активности для предупреждения и/или лечения астмы и дегенеративного суставного остеоартроза, связанных с активацией IL-1, IL-2, IL-6, IL-7, IL-8 и IL-12 [Патент №2552337 С2 Российская Федерация, МПК A61K 31/737, А61Р 11/06, А61Р 19/02. Сульфатированные гиалуроновые кислоты в качестве регуляторов цитокиновой активности: №2011146049/15: заявл. 11.05.2010: опубл. 10.06.2015 / Д. Галессо, А.М. Цанеллато; заявитель ФИДИА ФАРМАЧЕУТИЧИ С.П.А..].
Широкое применение нашли различные ранозаживляюшие композиции на основе гиалуроновой кислоты. Известен способ получения композиции для заживления ран, содержащей гиалуроновую кислоту, антисептик - смесь 1%-ного водного раствора сангвиритрина и настойки календулы на 70%-ном водном этиловом спирте, антиоксидант - витамин В6, анестетик - новокаин, эксципиент - дистиллированную воду или вазелин [Патент №2172168 С1 Российская Федерация, МПК A61K 9/08, A61K 9/06, A61K 31/728. Композиция для заживления ран на основе гиалуроновой кислоты: №2000111241/14: заявл. 11.05.2000: опубл. 20.08.2001 / Е.М. Лебедева, И.А. Федорищев.]. Недостатком предложенного способа является использование концентрированного раствора этанола, пересушивающего рану и таким образом замедляющего процессы регенерации тканей, а также вызывает дискомфорт у пациента при использовании.
Известна фармацевтическая композиция, содержащая фактор некроза опухоли-альфа, гиалуроновую кислоту, диметилсульфоксид и полиэтиленоксид при следующем соотношении компонентов, мас.%: фактор некроза опухоли-альфа 0,001-0,01; гиалуроновая кислота 0,1-1,0; диметилсульфоксид 5,0-15,0; полиэтиленоксид - остальное. Композицию используют для лечения инфекционно-воспалительных заболеваний, в том числе в комплексной терапии острых и хронических гинекологических воспалительных заболеваний, в комплексной терапии герпетической и иной вирусной инфекции, при лечении урогенитальной инфекции, а также при лечении долго не заживающих ран. Композиция обеспечивает повышенную терапевтическую эффективность и широкую область применения [Патент №2153352 С1 Российская Федерация, МПК A61K 38/19, A61K 31/728, А61Р 17/00. фармацевтическая композиция, обладающая ранозаживляющим и противовоспалительным действием: №99117224/14: заявл. 09.08.1999: опубл. 27.07.2000 / А.М. Гончар, С.Ф. Грачева, Г.А. Костина [и др.].]. Недостатком предложенного состава является наличие диметилсульфоксида, являющегося токсичным соединением четвертого класса опасности, вызывающего головную боль и тошноту.
Для придания препаратам гиалуроновой кислоты антибактериальной активности в них вносят антисептические компоненты, например, йод, его комплекс с йодидом калия, их смесь или хлоргексидин биглюконат [Патент №2153352 С1 Российская Федерация, МПК A61K 38/19, A61K 31/728, А61Р 17/00. фармацевтическая композиция, обладающая ранозаживляющим и противовоспалительным действием: №99117224/14: заявл. 09.08.1999: опубл. 27.07.2000 / А.М. Гончар, С.Ф. Грачева, Г.А. Костина [и др.].]. Однако и в этом случае из-за низкого содержания антисептика в составе композиции предлагается использовать токсичный трансмиттер диметилсульфоксид.
Наиболее близким по техническому решению является способ получения препарата для заживления ран, описанный в RU 2296569 [Патент №2296569 С2 Российская Федерация, МПК A61K 9/06, A61K 31/728, A61J 17/02. Препарат для заживления ран и предотвращения прилипания повязки к ране: №2004124041/15: заявл. 15.01.2003: опубл. 10.04.2007 / В. Велебни, Л. Соботка, С. Павек, Я. Ружичкова; заявитель СиПиЭн СПОЛ. С P.O..], содержащий физиологически приемлемую соль гиалуроновой кислоты (гиалуронат натрия или калия), имеющей молекулярную массу 200-2500 кДа, йод, йодистый калий и воду в количестве, мас.%: соль гиалуроновой кислоты - 0,05-10; йод - 0,05-2,5; йодистый калий - 0,05-5, вода - остальное. При этом препарат находится в виде стерильного водного раствора или геля. Препарат получают путем растворения йода в растворе йодистого калия в стерильной воде, отдельно растворяют соль или смесь солей гиалуроновой кислоты в стерильной воде для инъекций, после чего растворы стерилизуют и смешивают. Благодаря использованию комплекса йода с йодистым калием удается повысить растворимость йода в водной среде без использования этилового спирта или других побочных компонентов. Недостатком описанного способа является низкий процент содержания активного йода (до 2,5 мас.%) по сравнению с традиционным антисептическим спиртовым раствором йода с концентрацией 5 мас.%, а также низкая антибактериальная активность получаемого препарата.
Технической задачей настоящего изобретения является получение препарата на основе модифицированной гиалуроновой кислоты, содержащей не менее 5 мас.% активного йода.
Техническим результатом изобретения является препарат на основе привитого сополимера гиалуроната натрия и N-винилпирролидона, содержание йода в котором 5-7 мас.%, в виде геля с вязкостью 25-35 cps, обладающего повышенным содержанием активного йода более чем в два раза и повышенной антибактериальной активностью до 4 раз по сравнению с прототипом.
Технический результат достигается тем, что в способе получения препарата на основе гиалуроната натрия и N-винилпирролидона, обогащенного активным йодом, включающем растворение йода в растворе йодистого калия в стерильной воде для инъекций, последующее добавление полисахарида, согласно изобретению, растворяют 5-7 г йода в 30 г 10 мас.%-ного раствора йодида калия, приготовленного на стерильной воде для инъекций, после чего при постоянном перемешивании со скоростью 250 об/мин в приготовленный раствор вносят 1-5 г привитого сополимера гиалуроната натрия и N-винилпирролидона, полученного из гиалуроната натрия с молекулярной массой 400 кДа, при этом содержание привитых цепей TV-винилпирролидона в сополимере составляет 8 мас.%, а молекулярная масса привитых цепей равна 10 кДа, затем доводят объем полученного препарата в виде геля водой для инъекций до 100 г, фильтруют через мембрану из нейлона с диаметром пор 45 мкм.
Заявленный результат достигается за счет использования в составе препарата модифицированного гиалуроната натрия, а именно его привитого сополимера с N-винилпирролидоном. Поли-N-винилпирролидон - циклический биосовместимый низкотоксичный поли-N-виниламид с высокой комплексообразующей способностью по отношению к широкому спектру соединений, используемый в создании фармацевтических форм пролонгированного действия, в том числе содержащих йод, а также в качестве кровезаменителя. Введение боковых цепей из N-винилпирролидона повысит сродство гиалуроната к йоду, а также поспособствует образованию более стабильных и вязких гелей, что обуславливает более высокую антибактериальную активность.
Способ осуществляется следующим образом: в мерной посуде, снабженной перемешивающим устройством, растворяют 5-7 г йода в 30 г 10 мас.%-ного предварительно подготовленном растворе йодида калия (10 г йодида калия растворяют в 90 мл стерильной воды для инъекций), после чего при постоянном перемешивании со скоростью 250 об/мин в приготовленный раствор для получения препарата в виде геля вносят 1-5 г сополимера гиалуроната натрия и N-винилпирролидона, полученного из гиалуроната натрия с молекулярной массой 400 кДа, при этом содержание привитых цепей N-винилпирролидона в сополимере составляет 8 мас.%, а молекулярная масса привитых цепей равна 10 кДа, доводят объем полученного геля стерильной водой для инъекций до 100 г и фильтруют через мембрану из нейлона с диаметром пор 45 мкм.
Пример 1.
Получение привитого сополимера гиалуроната натрия и N-винилпирролидона с содержанием привитых цепей N-винилпирролидона в сополимере 8 мас.% и молекулярной массой привитых цепей, равной 10 кДа в трехгорлом реакторе: навеску гиалуроната натрия с молекулярной массой 400 кДа массой 0,5 г растворяли в 50 мл дистиллированной воды, после чего вносили водный раствор персульфата калия с концентрацией 0,01 г/мл в количестве 6,0 мл. Полученную смесь дегазировали трехкратным повторением циклов замораживание-вакуумирование-оттаивание, при этом заморозка осуществлялась путем погружения реактора в жидкий азот на 10 минут, после чего реактор вакуумировался в течение 10 минут при остаточном давлении 11 мм. рт.ст, после чего завакуумированный реактор для оттаивания помещался на водяную баню с температурой воды 25°С и выдерживался в течение 20 минут; затем в охлажденный до комнатной температуры реактор с полученной дегазированной смесью вносили против тока аргона, подающегося со скоростью 10 мл/мин, навеску безводного метабисульфита натрия массой 0,038 г через боковое горло реактора. Отдельно проводили вакуумную дегазацию N-винилпирролидона трехкратным повторением циклов замораживание-вакуумирование-оттаивание, исполненных как описано выше, после чего вносили мономер в реактор градуированной пипеткой против тока аргона, подающегося со скоростью 10 мл/мин, в количестве 5,3 мл. Реакцию в реакторе затем вели в течение 30 часов при температуре 40 °С. По завершении времени процесса продукт осаждали в 600 мл ацетона марки ч.д.а. и выдерживали при постоянном перемешивании со скоростью 250 об/мин при температуре 25°С в течение 30 минут, центрифугировали при скорости 4000 об/мин в течение 15 минут, осадок отделяли путем декантирования супернатанта и сушили в вакуумном шкафу в безвоздушном пространстве при 55°С до постоянной массы.
В мерной колбе на 100 мл, снабженной перемешивающим устройством, растворяют 5 г йода в 30 г 10 мас.%-ного предварительно подготовленном растворе йодида калия, полученного растворением 10 г йодида калия в 90 мл стерильной воды для инъекций, после чего при постоянном перемешивании со скоростью 250 об/мин вносят 1 г привитого сополимера гиалуроната натрия и N-винилпирролидона, полученного по методике, представленной выше, из гиалуроната натрия с молекулярной массой 400 кДа, при этом содержание привитых цепей N-винилпирролидона в сополимере составляет 8 мас.%, а молекулярная масса привитых цепей равна 10 кДа, доводят массу полученного геля стерильной водой для инъекций до 100 г и фильтруют через мембрану из нейлона с диаметром пор 45 мкм. Полученный препарат в виде геля содержит 5 мас.% йода, а его вязкость составляет 25 cps.
Для определения антибактериальной активности полученного препарата определяли его минимальную ингибирующую концентрацию (МИК) по отношению к S. aureus и Е. coli методом микроразведения в 96-луночных планшетах [Synthesis and Antimicrobial Activity of Sulfenimines Based on Pinane Hydroxythiols / N.O. Ilchenko, D.V. Sudarikov, R.V. Rumyantcev et al. // Antibiotics. 2022. Vol. 11, No 11. Article Number 1548.]. Для этого бактериальную суспензию, содержащую 108 КОЕ/мл и питательную среду следующего состава, на 100 г среды: дрожжевой экстракт - 0,5 г, пептон гороховый - 1 г, хлорид натрия - 1 г, глюкоза - 0,2 г, остальное - стерильная вода, в количестве 1 мкл вносили в лунку микролуночного планшета и добавляли 300 мкл питательной среды того же состава, получая в лунке суспензию, содержащую 106 клеток/мл, далее - рабочая суспензия. После этого планшеты инкубировали при 37°С в течение 24 часов.
В мерной колбе предварительно готовили из гелей водные растворы с концентрацией 2048 мг/мл с использованием стерильной воды, после чего помещали 100 мкл полученного раствора геля в лунку, содержащую 100 мкл питательной среды, описанной выше, получая раствор с концентрацией геля 1024 мкг/мл. Далее готовили растворы гелей в той же питательной среде методом последовательного разбавления непосредственно в лунках планшета, получая концентрацию гелей в диапазоне 1024-2 мкг/мл. После этого вносили в лунки, содержащие растворы геля с различной концентрацией, по 200 мкл рабочей суспензии, получая диапазон концентраций геля в лунках в интервале 1-512 мг/мл.
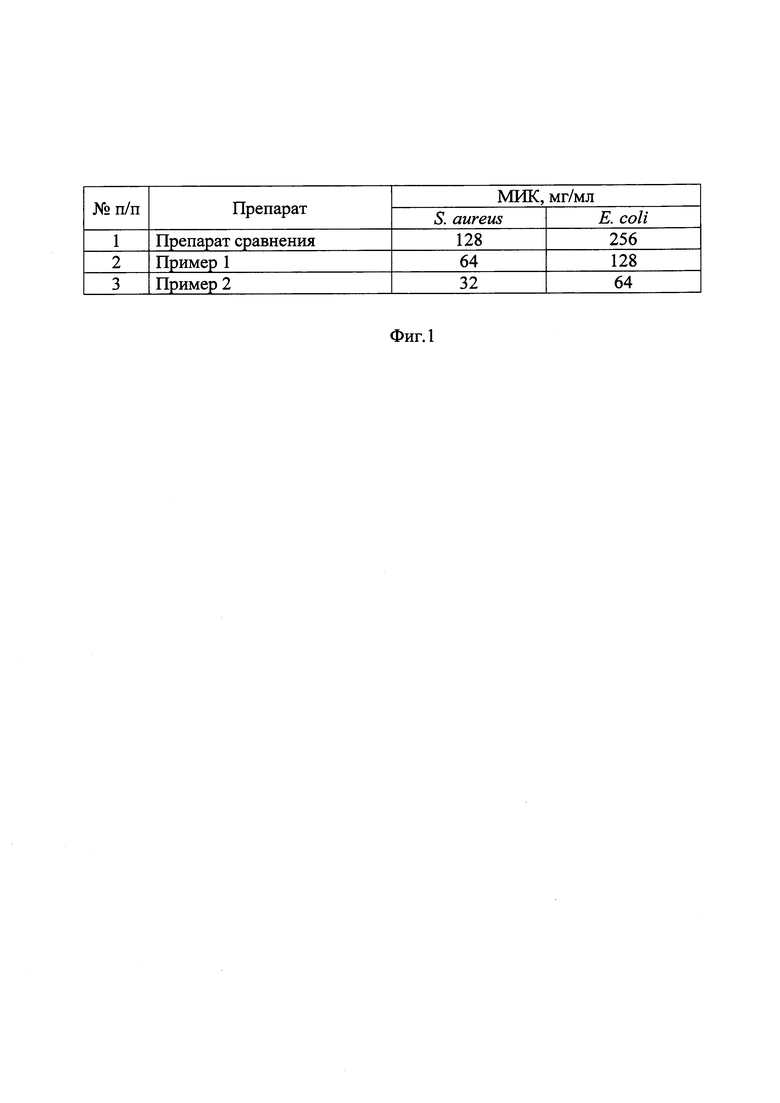
МИК определяли как самую низкую концентрацию препарата, при которой видимого роста бактерий не наблюдалось после 24 часов инкубации. Эксперимент выполнялся в пятикратной повторности, полученное среднее значение принимали за МИК. В качестве образца сравнения использовали препарат, полученный согласно прототипу и содержащий 10 мас.% гиалуроната натрия с молекулярной массой 400 кДа, 2,5 мас.% йода и 5 мас.% йодида калия, остальное - вода.
На фиг. 1 представлены данные по минимальной ингибирующей концентрации (МИК) препаратов.
Пример 2. Отличается от Примера 1 тем, что растворяют 7 г йода в 30 г 10 мас.%-ного предварительно подготовленном растворе йодида калия и используют 5 г сополимера гиалуроната натрия и N-винилпирролидона, Полученный препарат в виде геля с вязкостью 35 cps содержит 7 мас.% йода.
Предложенный способ обеспечивает получение препарата для влажного ранозаживления на основе модифицированной гиалуроновой кислоты и активного йода, с содержанием последнего 5-7 мас.% и повышенной актибактериальной активностью до 4 раз.
Изобретение относится к химико-фармацевтической промышленности и представляет собой способ получения препарата для влажного ранозаживления на основе модифицированной гиалуроновой кислоты и активного йода. Способ получения препарата на основе гиалуроната натрия и N-винилпирролидона, обогащенного активным йодом, включающий растворение йода в растворе йодистого калия в стерильной воде для инъекций, последующее добавление полисахарида, согласно изобретению, растворяют 5-7 г йода в 30 г 10 мас.%-ного раствора йодида калия, приготовленного на стерильной воде для инъекций, после чего при постоянном перемешивании со скоростью 250 об/мин в приготовленный раствор вносят 1-5 г привитого сополимера гиалуроната натрия и N-винилпирролидона, полученного из гиалуроната натрия с молекулярной массой 400 кДа, при этом содержание привитых цепей N-винилпирролидона в сополимере составляет 8 мас. %, а молекулярная масса привитых цепей равна 10 кДа, затем доводят полученный препарат в виде геля водой для инъекций до 100 г, фильтруют через мембрану из нейлона с диаметром пор 45 мкм. С помощью заявленного способа получен препарат на основе привитого сополимера гиалуроната натрия и N-винилпирролидона, содержание йода в котором 5-7 мас.%, в виде геля с вязкостью 25-35 cps, обладающего повышенным содержанием активного йода более чем в два раза и повышенной антибактериальной активностью до 4 раз. 1 ил., 2 пр.
Способ получения препарата на основе гиалуроната натрия и N-винилпирролидона, обогащенного активным йодом, включающий растворение йода в растворе йодистого калия в стерильной воде для инъекций, последующее добавление полисахарида, согласно изобретению, растворяют 5-7 г йода в 30 г 10 мас.%-ного раствора йодида калия, приготовленного на стерильной воде для инъекций, после чего при постоянном перемешивании со скоростью 250 об/мин в приготовленный раствор вносят 1-5 г привитого сополимера гиалуроната натрия и N-винилпирролидона, полученного из гиалуроната натрия с молекулярной массой 400 кДа, при этом содержание привитых цепей N-винилпирролидона в сополимере составляет 8 мас.%, а молекулярная масса привитых цепей равна 10 кДа, затем доводят полученный препарат в виде геля водой для инъекций до 100 г, фильтруют через мембрану из нейлона с диаметром пор 45 мкм.
| ПРЕПАРАТ ДЛЯ ЗАЖИВЛЕНИЯ РАН И ПРЕДОТВРАЩЕНИЯ ПРИЛИПАНИЯ ПОВЯЗКИ К РАНЕ | 2003 |
|
RU2296569C2 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ЛЕЧЕБНЫЙ ПРЕПАРАТ, ОБЛАДАЮЩИЙ БАКТЕРИЦИДНЫМ И ВИРУЛИЦИДНЫМ ДЕЙСТВИЕМ - ЙОДОМИДОЛ | 1996 |
|
RU2130312C1 |
| CN 116212008 A, 06.06.2023. | |||
Авторы
Даты
2025-06-05—Публикация
2024-04-18—Подача