ю го Изобретение относится к гидрометаллургии цветных металлов и може быть использовано при переработке окисленных никелевых руд, океанских конкреций на металлизированный продукт на основе железа. Известен способ переработки материалов на основе железа., содержащих цветные металлы 1 . Недостатком этого способа являетс то, что в процессе выщелачивания кислород, подаваемый на окисление железа, образовывает взрывоопасные смеси с выделяющимся водородом. Наиболее близким к .изобретению по технической сущности и достигаемому результату является способ обработки материалов на основе железа содержа1цих цветные металлы, включаю щий стадиальное выщелачивание их. раствором кислоть в присутствии кис лорода с одновременным или последую щим осаждением железа из растворов и извлечением из них цветных металлов Г 2 Ц . Недостатками известного способа являются; выделение водорода в процессе вы щелачивания в атмосферу кислорода с образованием взрывоопасных смесей; применение двух реагентов - кисл рода и соли щелочного металла суль фат натрия) для окисления железа в растворах выщелачивания с двух до трехвалентного состояния и осаждени его из растворов в виде ярозита Ма-ез(ЯОд;.(ОН загрязнение окружающей среды сул фато.м натрия, сбрасываемым с жидкой фазой пульпь в хвостохранилище; неприменимость способа к переработке бедного ферроникеля, требующего большого количества сульфата натрия для связывания всего железа в ярозит натрия. Целью изобретения является предо вращение образования взрывоопасной водородно-кислородной смеси газов в процессе выщелачивания и уменьшение расхода реагентов на осаждение железа. Поставленная цель достигается тем, что согласно способу обработки материалов на основе железа, содержащих цветные металлы, включающему стадиальное зыщелзчивание их раство ром кислоты в присутствии кислорода с одновременным или последующим осаж дением железа из растворов и извле112чением из них цветных металлов, выщелачивание сплава, на первой стадии ведут сернистой кислотой или смесью ее с серной при содержании сернистой кислоты в растворе в количестве Г20- t от общего расхода кислот , и процесс ведут до постоянного значения рН, а затем на второй стадии выщелачивание продолжают при 80-1 и прациальном давлении кислорода 315 атидо растворения цветных металлов и осаждения железа. По предлагаемому способу в качестве исходного сырья используют магнитный концентрат следующего химического состава, вес.%: Fe 75,2; N1 6,8; Со 0,71; Fe°73,3; Mi6,8; Со°0,68. Крупность концентрата (-) О, 16 мм, 1001. Загрузка в аппарат магнитного концентрата - 500 г, раствора кислот - 2,0 т. Общее количество кислоть, подаваемой в аппарат, рассчить1валось как 2-3-кратный избыток от стехиометрии на растворение цветных металлов. Первую стадию выщелачивания необходимо вести при 20-100 С до полной нейтрализации всего количества введенной кислоты, т.е. до постоянного значения рН. На данной стадии выщелачивания кислота расходуется в основном на растворение железа. Цветные металлы переходят при этом в раствор в незначительном количестве. На данной стадии выщелачивания растворение железа в присутствии сернистой кислоты не сопровождается выделением водорода в газовую фазу. Можно предположить, что растворение железа смесью кислот будет сопровождаться образованием тиосульфата железа, который реагирует с серной кислотой с образованием сульфата железа и элементарной серы. Затем элементарная сера соединяется с атомарным водородом, образуя сероводород который осаждает сульфатное железо в виде сульфида. При этом выделения водорода в газовую фазу также не происходит. Затем пульпа с первой стадии поступает на вторую и выщелачивание ее продолжают при 80-150 0 в присутствии кислорода ( или кислорода воздуха ) при парциальном давлении кислорода 3-15 ати. На второй стадии происходит окисление железа и термический его гидролиз, а цветные металлы при это переходят в раствор. При таком веде нии процесса выщелачивания водород в газовую фазу выделяется в незначительном количестве на второй стадии выщелачивания (табл. 1, 3 и k). После окончания выщелачивания производится отделение твердого от жидкого по известной технологии. П р и м е р 1 . Оптимальное соот ношение серной и сернистой кислоты при двухстадийном выщелачивании. Режим 1 стадии выщелачивания: температура 90°С, продолжительность 1 ч. Режим И стадии выщелачивания: температура , парциальное давл ние кислорода 7 ати, скорость страв ливания газовой фазы 2,D л/мин. Выщелачивание металлизированного продукта смесью серной и сернистой кислоты не сопровождается образованием взрывоопасной водородно-кислородной смеси газов при содержании не менее 20% сернистой кислоты от общего количества кислот (менее ,7° Нх). Выщелачив9н.ие металлизированных продуктов смесью кислот необходимо проводить в технологических схемах с регенерацией серной кислоты при электролитическом выделении металло из растворов. В этом случае потери кислоты в схеме можно компенсироват подачей на.выщелачивание сернистой кислоты. П р и м е р 2 . Температурный ин тервал и продолжительность 1 стадии выщелачивания металлизированного продукта смесью серной и сернистой кислот. Режим выщелачивания: исходная ко центрация серной кислоты +6,7 г/л, исходная концентрация сернистой кис лоты 40,5 г/л. В табл. 2 показано изменение кис лотности раствора на I стадии выщелачивания металлизированного продук та. В опыте № 2 в первые минуты пере мешивания пульпы, .температура самопроизвольно повысилась от 20 до 0° за счет тепла химических реакций. В дальнейшем она поддерживалась на эт уровне подогреванием пульпы. Процесс нейтрализации смеси кис лот на 1 стадии выщелачивания протекает быстро и заканчивается при 114 в течение 10 мин, при более высокой температуре - в процессе разогрева пульпы без подачи кислорода. Нейтрализация смеси кислот не сопровождается выделением водорода в газовую фазу. П р и м е р 3 . Температурный интервал процесса выщелачивания магнитного концентрата сернистой кислотой в две стадии без образования взрывоопасной водородно-кислород ной газовой фазы. 1 стадия выщелачивания проведена в период разогрева пульпы до требуемой температуры в отсутствие кислорода. Режим выщелачивания II стадии: парциальное давление кислорода 5 ати, исходная концентрация сернистой кислоты 58,3 г/л, скорость стравливания газовой фазы 2,0 л/мин. В табл. 3 представлено изменение состава газовой фазы на П стадии выщелачивания магнитного концентрата сернистой кислотой при различной температуре. В данном диапазоне температур применение сернистой кислоты с предварительной ее нейтрализацией перед выщелачиванием в отсутствие кислорода позволяет вести выщелачива- ние металлизированных продуктов без образования взрывоопасной смеси газов. Повышение температуры выщелачива.ния от 80 до ускоряет процесс растворения металлов и скорость гидролиза железа. При 80 С максимальное извлечение металлов в раствор - никеля 96%, кобальта - достигается в течение четырех часов выщелачивания магнитного концентрата, при - в течение двух часов, при 150°С - в течение 0,5 ч. Пример . Пределы парциального давления кислорода, обеспечивающие получение невзрывоопасной газовой фазы при двухстадийном выщелачивании магнитного концентрата сернистой кислотой. 1 стадия выщелачивания произведена без кислорода в период разогрева пульпы до 100°С. Режим II стадии выщелачивания: температура 100°С, скорость стравлиг вания газовой фазы 2,0 л/мин.
5
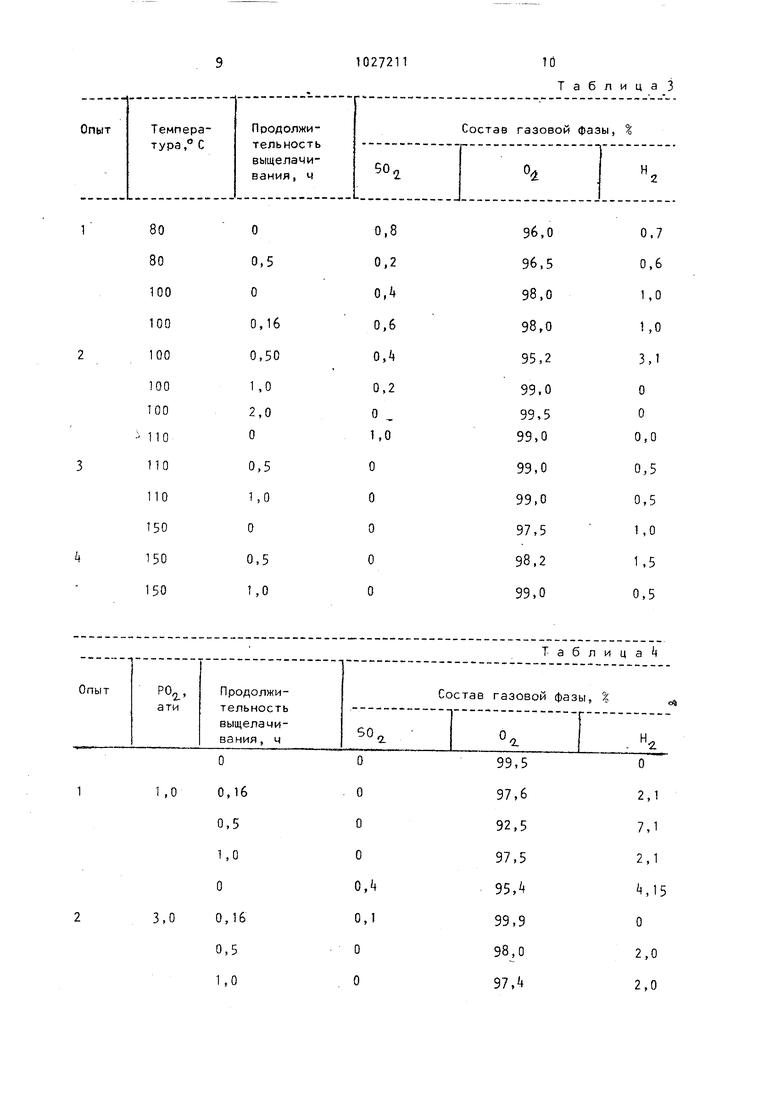
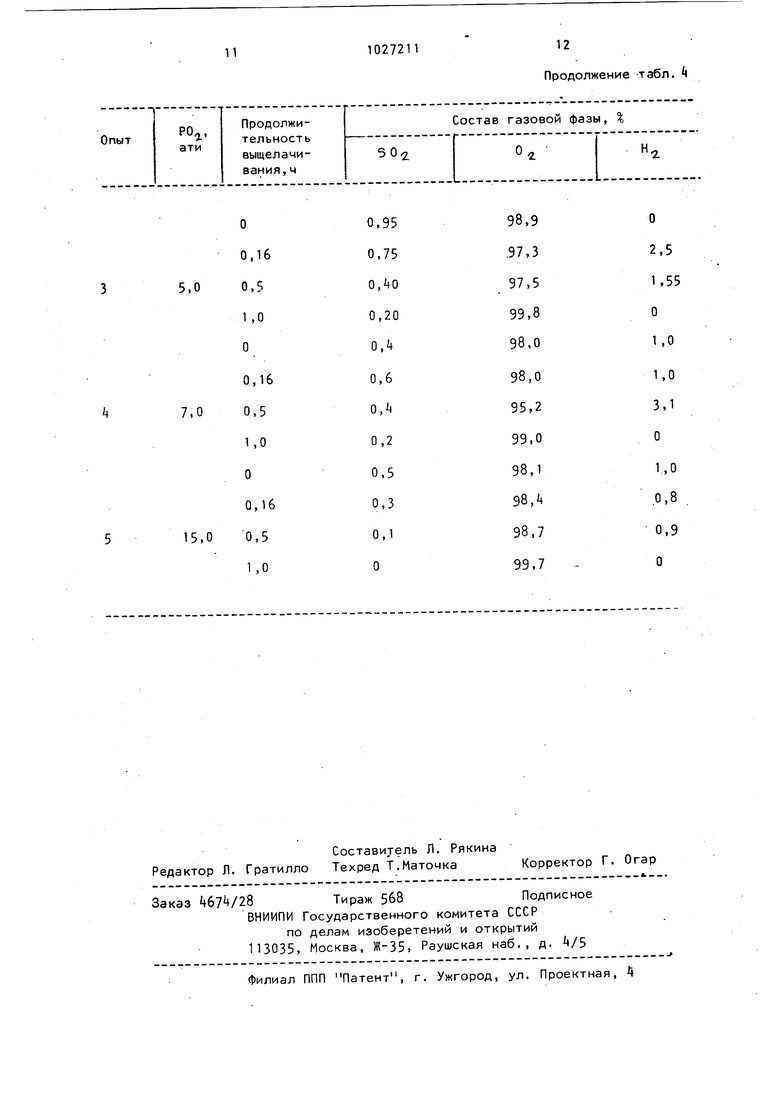
В табл. дано изменение состава газовой фазы на П стадии выщелачивания магнитного концентрата сернистой кислотой при различном парциальном давлении кислорода.
Выщелачивание металлизированного продукта сернистой кислотой предотвращает образование взрывоопасной ; водородно-кислородной смеси газов
(, H,j ,7%) при парциальном давлении кислорода не менее 3,0 ати.
При более низком парциальном давлении кислорода резко уменьшается скорость окисления железа и осажде ния его из растворов выщелачив.ания, а также происходит выделение водорода в газовую фазу больше ,1%
Процесс выщелачивания при парциальном давлении кислорода больше
272116
15 ати происходит без образования взрывоопасной газовой фазы, но скорость вь1щелачивания при этом увеличивается незначительно, поэтому повышать давление экономически нецелесообразно.
Таким образом, предложенный способ гидрометаллургической переработки металлизированного сПлава на основе железа позволяет;
получить невзрывоопасную водородно-кислородную смесь в процессе выщелачивания; уменьшить расход реагентов за счет того, что осаждение железа проводится без использования сульфата натрия; вовлечь в переработку бедные сплавы по содержанию цветных металлов.
Таблица 1

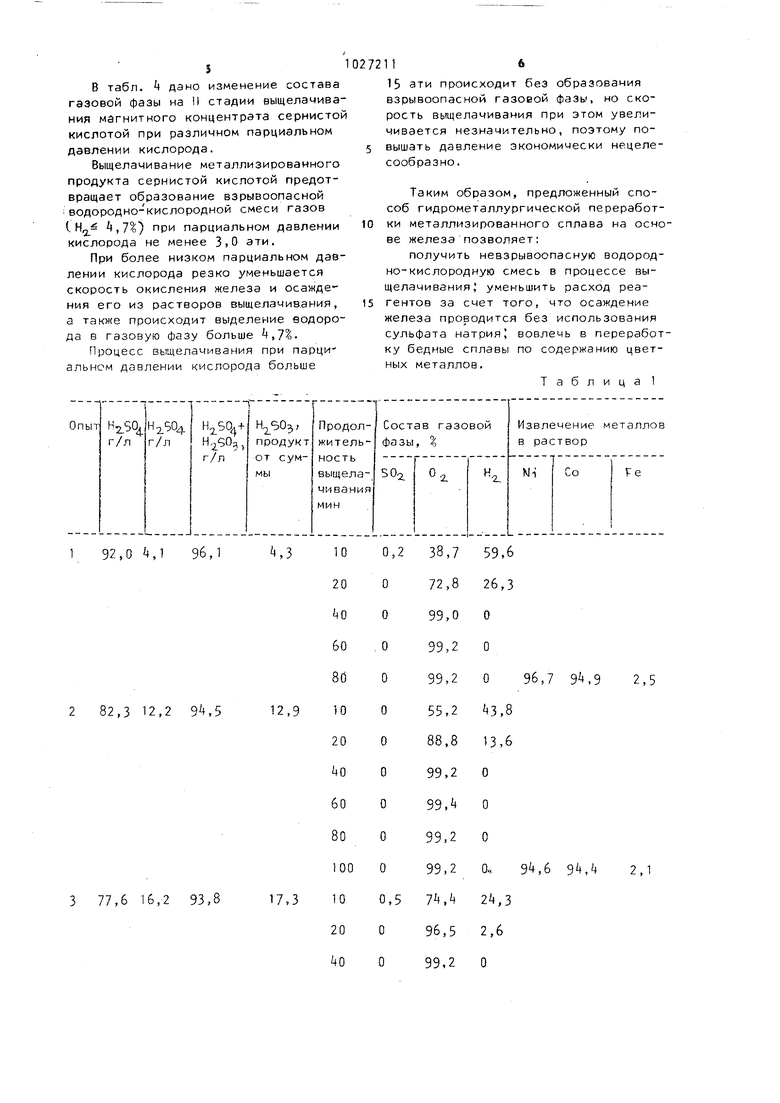
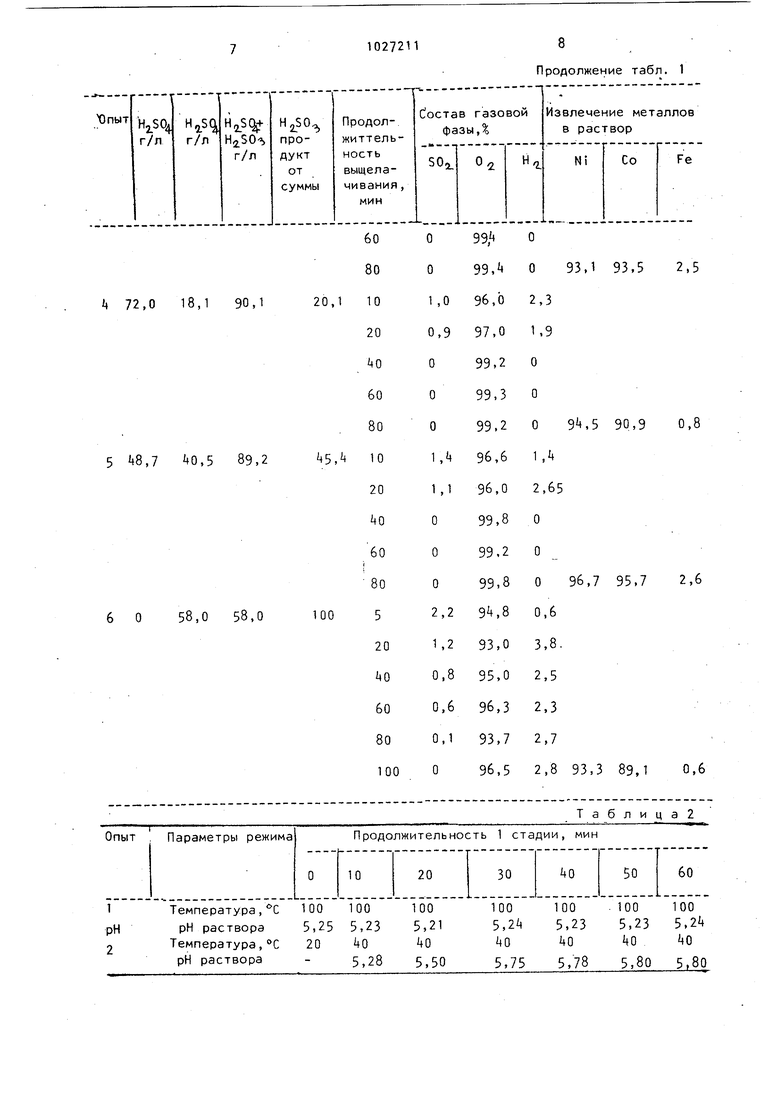
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ ПРОМПРОДУКТОВ МЕДНО-НИКЕЛЕВОГО ПРОИЗВОДСТВА | 2000 |
|
RU2160319C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПРОМПРОДУКТОВ МЕДНО-НИКЕЛЕВОГО ПРОИЗВОДСТВА, СОДЕРЖАЩИХ ДРАГОЦЕННЫЕ МЕТАЛЛЫ | 2000 |
|
RU2160785C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПРОМПРОДУКТОВ МЕДНО-НИКЕЛЕВОГО ПРОИЗВОДСТВА | 1999 |
|
RU2144091C1 |
| Способ переработки измельченного металлизированного медно-никелевого промпродукта, содержащего благородные металлы | 2022 |
|
RU2810029C1 |
| Способ переработки промпродуктов, содержащих драгоценные металлы, полученных при производстве катодного никеля (варианты) | 2022 |
|
RU2789528C1 |
| Способ переработки сульфидных концентратов, содержащих пирротин, пирит, халькопирит, пентландит и драгоценные металлы | 2019 |
|
RU2712160C1 |
| СПОСОБ ПЕРЕРАБОТКИ СВИНЦОВИСТЫХ ШЛАМОВ ЭЛЕКТРОРАФИНИРОВАНИЯ МЕДИ (ВАРИАНТЫ) | 2011 |
|
RU2451759C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕЛЕКТИВНЫХ КОНЦЕНТРАТОВ БЛАГОРОДНЫХ МЕТАЛЛОВ | 2001 |
|
RU2215801C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАЛЬЦИЕВОГО СУЛЬФИДИЗАТОРА ДЛЯ ОСАЖДЕНИЯ ТЯЖЕЛЫХ ЦВЕТНЫХ МЕТАЛЛОВ ИЗ КИСЛЫХ СУЛЬФАТНЫХ РАСТВОРОВ И ЖИДКОЙ ФАЗЫ ГИДРАТНЫХ ЖЕЛЕЗИСТЫХ ПУЛЬП | 1997 |
|
RU2120484C1 |
| СПОСОБ ПЕРЕРАБОТКИ СУЛЬФИДНЫХ МЕДНЫХ КОНЦЕНТРАТОВ, СОДЕРЖАЩИХ НИКЕЛЬ, КОБАЛЬТ И ЖЕЛЕЗО | 2001 |
|
RU2171856C1 |

,3
96,1
1 92,0
2 82,3 12,2 9,5
12,9
3 77,6 16,2 93,i
17,3
,2 38,759,6
72,826,3
99,0О
99,2О
99,2О 96,7 9,9
2,5
55,,8
88,813,6
99,2О
99,О
99,2О
99,2О,, 94,6 9,4
2,1
,5 7,24,3
96,52,6
99,2О i 72,0 18,1 90,1 20,1 10 kS, 10 5 tt8,7 0,5 89,2 1005 6 О 58,0 58,0
8
Продолжение табл. 1 60 80 20 40 60 Во 20 40 бО Во 20 i40 60 Во 100
Таблица2 О99/ О О99, 93,1 93,5 2,5 1,096,02,3 0,997,01,9 О99,2О О99,3О О99.2О 9,5 90,9 0,8 1,496,61,Д 1,196,02,65 О99,8О О99.2О о99,8О 96,7 95,7 2,6 2,,80,6 1,2Э3,03,8. 0,895,02,5 0,696,32,3 0,193,72,7 О96,52,В 93,3 89,1 0,6
О 0,5
О
0,16
0,50
1,0
2,0 О
0,5
1,0
О
0,5
1,0
ТаблицаЗ
9б,0
0,7
0,6 96,5 98,0 1,0 98,0 1,0 3,1 95,2
99,0
о
о
99,5 99,0
0,0 0,5
99,0 0,5 99,0 1,0
97,5 98,2 1,5 99,0 0,5
Таблица4
n
12
1027211
Продолжение табл. А
| Journal of Metals, 19Тб, 28, N It, p | |||
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент США № , кл | |||
| , 1977. | |||
Авторы
Даты
1983-07-07—Публикация
1982-01-22—Подача