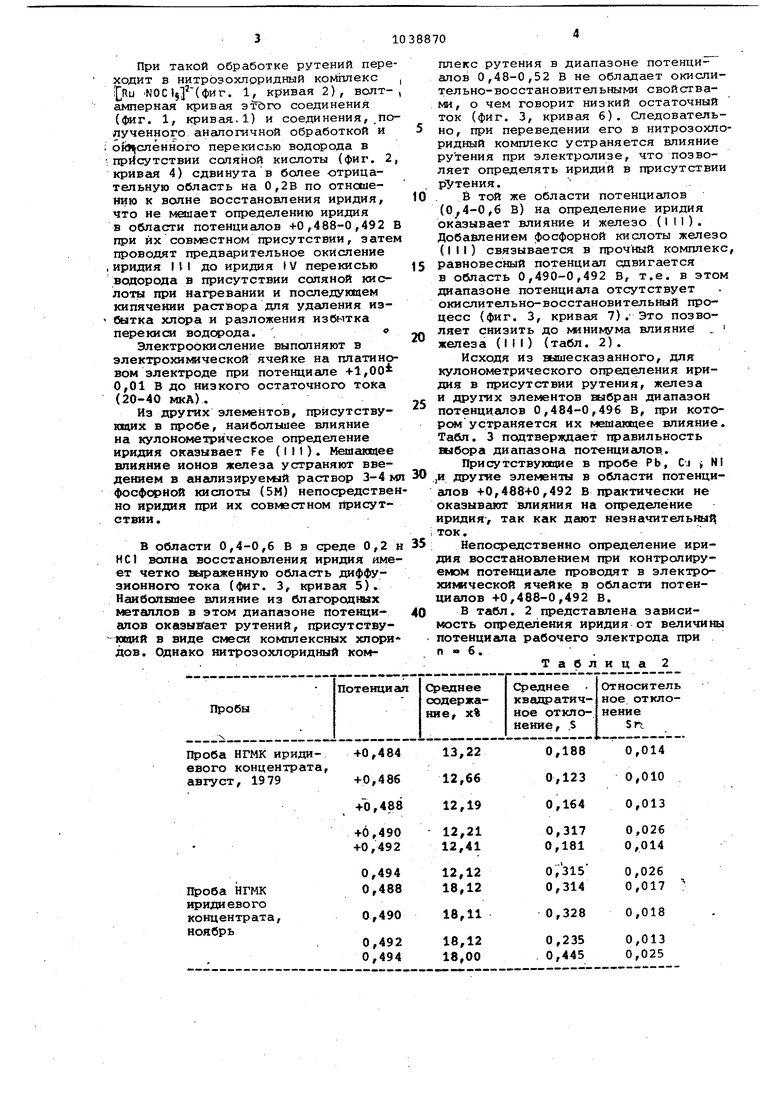
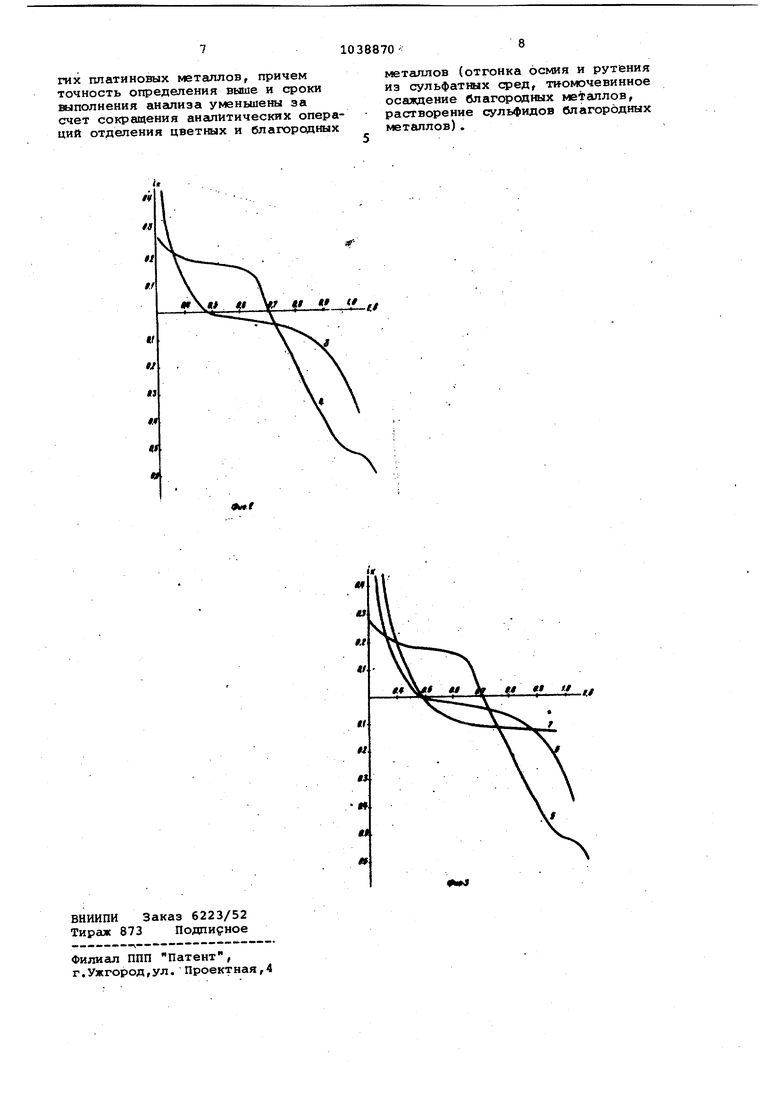
Изобретение относится к аналитической химии и может быть использовано при анализе промлшпенных проду тов, содеражщих платиновые металлы. Известен также способ кулонометрического определения иридия в потенциостатическом режиме в окрестности потенциала платинового катода +0g40 В (относительно насыщенного каломельного электрода) в синтетических растворах, содержащих миллиграммовые количества двух элементов иридия и палладия в двухкомпонентны системах 1 . Этот способ также применим для анализа растворов, не содержащих примеси цветных металлов и других металлов группы платины и золота. Недостатком способа является то, что процесс подготовки проб к анали зу длителен, так как иридий переводитсй в четырехвалентное состояние хлорированием (прсдхесс хлорирования длится 30-40 №1н) . Наиболее близким к предлагаемому является способ кулонометрического определения иридия путем восстановления при контролируемом потенциале заключаяадийся в предварительном окис лении перекисью в присутствии соляной 1;гислоты с последующим электроокислением при +1,004-0,018 иридия (Ml) в присутствии иридия ,(IV) на платиновом электроде И . Недостатком данного способа Является то, что определение иридия ведется в щзисутствии только родагя после отделения от цветных и осталь ных платиновых металлов. Требуется проведение дополнительных операций для переведения иридия в хлсч-фс му после дастилладии рутения и осмяя из сульфатных растворов, что увеличивает дпительноЪтъ анализ и понижает точность определения. Цель изобретения - повышение точности определения больших содержащий иридия в присутствии рутения и железа ( i И ). Поставленная цать достигается тем, что .в кулонометрическом способе определения иридия путем восстановления при контролируемом потенциале, заключающейся в предварительном окислении иридия до иридия (IV) перекисью водорода в присутствии соляной кислоты с последующим электродоокислением при величине на платиновом электроде потенциала +1,00+0,О1В раство- , ры перед окислением иридия в иридий (IV) обрабатывают смесью соляной и азотной кислот, взятых в соотношениях 1:1, а определение иридия. .(I t I ) проводят в присутствии 5М фосфсфной кислоты в области потенциалов платинового электрода +0,488-0,492 В от носительно наолщенного хлорсеребрянового электрода. Предварительную обработку растворов проводят смесью соляной и азотной кислот (1;1). Определение иридия выполняется предпочтительно при потенциеоте +0,492В относительно нормального каломельного электрода. На Фи.г. 1 представлены электронные спектры поглощения рутения без обработки (кривая I) и после обработки (кривая 2)J на фиг. 2 - вольтамперные кривые соединений рутения, представленных до обработки смесью кислот (кривая 3) и после обработки (кривая 4); на фиг. 3 - вольтамперные кривые соединений иридия. Способ осуществляется следукхцим образом. Растворы, приготовленные из промьтшенного концентрата состава, обрабатывают при нагревании смесью соляной и азотной кислот (1:1), В табл. 1 представлен состав анализируемого концентрата. При такой обработке рутений пере ходит в нитрозохлоридный комплекс НОС (фиг. 1, кривая 2), волтамперная кривая этйго соединения (фиг. 1, кривая.1) и соединения, по лученного аНсшогичной обработкой и ; О1в слённого перекисью водорода в присутствии соляной кислоты (фиг. 2 кривая 4} сдвинута в более отрицательную область на 0,2В по отношению к волне восстановления иридия, что не мешает определению иридия в области потенциалов +0,488-0,492 при их совместном присутствии, зате проводят предварительное окисление , иридия И1 до иридия tV перекисью водорода в присутствии соляной кислоты при нагревании и последующем кипячении раствора для удаления избытка хлора и разложения избытка перекиси водорода. .« Электроокисление выполняют в электрохимической ячейке на платино вом электроде при потенциале +1,00 0,01 В до низкого остаточного тока (20-40 мкА). Из других элементов, присутствующих в пробе, наибольшее влияние на кулонометрическое определение иридия оказывает Fe (III). Мешающее влияние ионов железа устраняют введением в аиализируекый раствор 3-4 м ФосфорИой кислоты (5М) непосредстве но иридия при их совместном йрисутствии. В области 0,4-0,6 В в среде 0,2 НС1 волна восстановления иридия име ет четко выраженную область диффузионного тока (фиг. 3, кривая 5). НаиболЕшее влияние из благородных металлов в этом диапазоне потеициапов оказывает рутений, присутству- ющий в виде смеси комплексных хлори дов. Однако нитрозохлоридный комплекс рутения в диапазоне потенциалов 0,48-0,52 В не обладает окислительно-восстановительными свойствами, о чем говорит низкий остаточный ток (фиг. 3, кривс1Я 6). Следовательно, при переведении его в нитрозохлоридный комплекс устраняется влияние рутения при электролизе, что позволяет определять иридий в присутствии рУтения. В той же области потенциалов (,б В) на определение иридия оказывает влияние и железо (III). Добавлением фосфорной кислоты железо (III) связывается в прочный комплекс, равновесный потенциал сдвигается в область 0,490-0,492 В, т.е. в этом диапазоне потенциала отсутствует окислительно-восстановительный процесс (фиг. 3, кривая 7). Это позволяет снизить до минил ма влияние , железа (III) (табл. 2). Исходя из вышесказанного, для кулонометрического определения иридия в присутствии рутения, железа и других элементов выбран диапазон потенциалов 0,484-0,496 В, при которе устраняется их мешающее влияние. Табя. 3 подтверждает правильность выбора диапазона потенциалов.. Присутствующие в пробе РЬ, Cj i N1 и другие элементы в области потенцигшов +0,488+0,492 В практически не оказывают влияния на определение иридия, так как дают незначительны ток. Непосредственно определение ириия восстановлением при контролируемом потенцигле проводят в электрохимической ячейке в области потениалов +0,488-0,492 В. В табл. 2 представлена зависимость определения иридия от величины потенцигла рабочего электрода при п - 6.. Таблица 2
Иэ данных таблицы видно, что для достижения поставленной цели необходимо использовать область потенциалов 0,488-0,492 В так как в этой области достигаются наиболее точные и воспроиэводимле результаты
Величина среднего квадратичного отклонения показывает, что наиболее воспроизводикие результаты получены при потенциале +0,492 В, в связи с чем предпочтительно определение в этой области.
Таким образом операции по переведению рутения в нитрозохлоридный
комплекс, устранение влияния железа и выбор определенной области потенцигшов позволяют ускорить проведение, анализа и улучшить точность результатов путем исключения операций по отделению цветных и благородных металлов.
Сравнительные данные по определению содержания иридия в пооь«шленных концентратах в присутст- ВИИ рутения предлагаемым способом и известным приведены в табл. 3.
Таблица 3

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ кулонометрического определения иридия в промышленных материалах | 1983 |
|
SU1187064A1 |
| Способ переработки концентратов на основе неблагородных элементов, содержащих редкие металлы платиновой группы | 2021 |
|
RU2773294C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ПЛАТИНОВОЙ ГРУППЫ ИЗ ПЛАТИНОСОДЕРЖАЩЕГО СЫРЬЯ | 2009 |
|
RU2415954C1 |
| Способ определения рутения | 1989 |
|
SU1673947A1 |
| СПОСОБ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ИРИДИЯ В НИТРИТНОЙ СРЕДЕ | 2010 |
|
RU2436079C1 |
| СПОСОБ ПЕРЕРАБОТКИ КОНЦЕНТРАТА БЛАГОРОДНЫХ МЕТАЛЛОВ | 1995 |
|
RU2094499C1 |
| СПОСОБ ВСКРЫТИЯ КОНЦЕНТРАТА СПУТНИКОВ ПЛАТИНЫ | 2004 |
|
RU2268315C1 |
| СПОСОБ ВСКРЫТИЯ РУТЕНИЕВОГО КОНЦЕНТРАТА | 2008 |
|
RU2378399C1 |
| СПОСОБ ПЕРЕРАБОТКИ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ПЛАТИНОВЫЕ МЕТАЛЛЫ И СЕРЕБРО | 2003 |
|
RU2256711C2 |
| Способ извлечения иридия и родия | 1977 |
|
SU698492A1 |


Конечная концентрация иридия
определяется расчетным методом Мак Невина-Беккера и Мейтса.
Пример, Опыты проводят в лабораторных условиях на синтетических растворах и промлшленных концентратах,содержаьщх платиновые и цветные металлы, количества которых указаны в табл. 1.
Навеску пробы проь«шленного концентрата массой 0,5 г сплавляют с пятикратным количеством перекиси натрия при 700°С в течение 30 NMH, После охлаяотения сплав выщелачивают смесью соляной и азотной кислот (3:1), упаривеиот до объема 40-50 см переводят бН соляной кислотой в колбу вместимостью 100 мл. Для определения иридия отбирают аликвотную часть (содержащую 1,5-5 мг иридия) в стакан емкостью 50 см , обрабатывают 20-25 см смесью соляной и азотной кислот (1:1) под крышкой при нагревании в течение 40-60 мин, упаривают на водяной бане до влажных солей, приливают 4-5 смНС бН (для получения в электрохимической ячейке кислотности по НС1 0,2-0,4Н) В электролизной ячейке ЯСЭ-2 объем доводят водой до 75-80 см. Рабочим электродом служит платиновая сетка, (d 31 мм, h 33 мм). Вспомогатель ным электродом служит спираль иэ платиновой проволоки (d 0,3 NW, Л 100 мм). Электрод сравнения насыщенный хпорсеребряный. Отделения для вспомогательного электрода и электрода сравнения заполняют 0,2Н соляной кислотой. Проводят электродоокисление анализируемого раствора для более полного переведения иридия 11 I в иридий IV, при постоянном потенциале рабочего электрода +1,0 + 0,01 В, используя потенциостат П-5827М, до остаточного тока 2040 мкА-. Затем потенциал рабочего электрода меняют на 0,492 В и проводят электролиз раствора в присутствии 3-4 мл 5М фосфсфной кислоты в течение 7-10 мин, регистрируя кривую ток - время на самописце ПДП-4.
Содержание иридия вычисляют по формуле, с учетом результата контрольного опыта, проведенного ангшогично пробам,
V - а 1,9918d 100 , - мМОбб
где Q- количество электричества
прошедшее на восстановление иридия IV, к; I,99i8 - электрохимический.эквивешент иридия, мг/к
М- масса навески пробы, г/
1000 - коэффициент перевода мг в г..
Количество электричества вычисляют по формуле
где i - начальная ордината графика. 1дЦ относительно t
К - тангенс угла наклона графика Igi относительно t, разделеннсш на 0,43i4 с-.
Щ едлагаекый способ позволяет проводить определение иридия в промяопенных концентратах и справах в присутствии рутения, является основным мешающим элементом а также в присутствии цветных и других платиновых металлов, причем точность определения выше и сроки выполнения анализа уменыиены за счет сокращения аналитических операций отделения цветных и благородных
металлов (отгонка осмия и рутения из сульфатных сред, тномочевинное осаждение благородных м6iPaллoв, растворение сульфидов благородных металлов).
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Наггаг J | |||
| Е., Shain А | |||
| Experiments as controlled patential | |||
| Analytical CheuiiJtry, 1966, t 8, p. | |||
| СПОСОБ ПОДВЕСА ТОВАРНЫХ ВАГОНОВ | 1920 |
|
SU1148A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Vallon J | |||
| W., Page J | |||
| Kulonometric delerflination of rodium and iriduum in, concetrates:, vol | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| АППАРАТ ДЛЯ РАЗРЕЗАНИЯ ПЕРЕДВИГАЮЩЕЙСЯ НА ПОДВИЖНОМ СТОЛЕ ТОРФЯНОЙ ПОЛОСЫ ПРИ ПОМОЩИ НОЖЕЙ, УКРЕПЛЕННЫХ НА ПОВЕРХНОСТИ БАРАБАНА | 1922 |
|
SU602A1 |
Авторы
Даты
1983-08-30—Публикация
1981-10-08—Подача