Изобретение относится к новым производным солей пиримидо 1,2-а бензимидазолия, а именно к перхлоратам пиримидо- l ,2-а1 бензимидазолия общей формулы
®Х9
е ciioy
R
в качестве флуоресцентных красителей (флуорохромов ) растительных тканей и микроорганизмов, которые могут быть использованы для изучения микробиологических объектов, их индикации и диагностики.
Известны флуоресцентные красители растительных тканей и микроорганизмов в различных классах соединений, а именно: акридиновые, азиновые, арилметиновые, ксантеновые ij 2J и 3.
Работа с Указанными флуорохромам требует соблюдения определенных условий: необходимой концентрации флуорохрома в растворе и окрашиваемого сусбтрата, рН раствора, времени флуорохромирования. Нарушение хотя бы одного из этих условий приводит к искажению результатов опыта Кроме того, описанные флуорохромы большей частью растворимы в воде, что создает некоторые трудности при приготовлении постоянных препаратов (при заключении окрсшенных объектов .в водные среды). Недостатком флуорохромов является также способность окргииенных ими объектов к выцветанию при воздействии ультрафиолетового или обычного света.
Например, как ядерный краситель общего значения используют флуорохром ряда ксантеновых красителей флуоресцеинат натрия (уранин А), обладающий характеристиками:
погл.ток 485-490 им; Anor.rla 527 ,33) растворимость 50 г в 100 г воды и 7 г в 100 г этанола 2 .
Указанный флуорохром имеет ряд недостатков: работает в относительно высоких концентрациях (0,00250,01%, разведение 1:40000-1:10000), его флуоресценция обратимо исчезает при , окрашенные препараты выцветают под действием ультрафиолетового (5-25 мин) и обычного (12 месяца) света. Кроме того, квантовый выход уранина А (в толуоле) составляет всего 0,33.
В ряду солей пиримидо l,2-a бензимидазолия не известны флуоресцентные крастители растительных тканей и микроорганизмов.
0 Цель изобретения - снижение концентрации рабочего раствора флуорохрома, расширение рабочего диапа3Oiia рН и повышение устойчивости к обычному и ультрафиолетовому све5 ту, а также повышение квантового выхода.
Поставленная цель достигается использованием предлагаемых перхлоратов пиримидо l,2-aj бензимидазолия общей формулы 1 в качестве флуоресцентных красителей растительных тканей и микроорганизмов. Указанные соединения получают путем взаимодействия перхлората
2,4,6-триарилипирилия с 1-алкил2-аминобензимидазолом, взятых в мольном соотношении 1:1,2, в кипящем диметилформамиде в течение 1ч.
Пример 1. Получение перхлората 1-(4-метоксифенил )--3-фенил5-нонилпиримидо l,2-aJ бензимидазолия (IB) .
0,88 г (2 ммоль) перхлората 2,6дифенил-4-(4-метоксифенил)-пирилия ди 0,63 г (2,4 ммоль) 2-амино-15 нонилбензимидазола кипятят 1 ч в 4 мл свёжелерегнанного диметилформамида. После охлаждения приливают 40 мл зфира и отфильтровывают «на плотном фильтре выпавший осадок.
0 Выход соединения 1в 0,77 г (66%), бледно-желтые кристаллы. Вещество перекристаллизовывают дважды из этанола, затем промывают небольшим количествам ацетона и эфиром.
5 Перхлораты 1,З-дифенил-5-октилпиримидо ,2-а бензимидазолия (I а), 1-(4-метоксифенил)-З-фенил-5-октилпиримидо- 1,2-аЗ бензимидазолия ( i б) , 1,З-дифенил-5-децилпиримидо l ,2- р, бензимидазолия (1г) и 1-(4-метоксифенил )-3-фенил-5-децилпиримидо 1,2-а бензимидазолия (1д) получают по аналогичной методике.
В табл. 1 приведены физико-хими5 ческие данные полученных соединений общей формулы I.
ИК-спектры полученных соединений общей I снимают на приборе Specord 71-1R в вазелиновом масле, 0 а УФ-спектры - на приборе Specord UV-vis с использованием ацетонитрила в качестве растворителя. Квантовые выходы флуоресценции (Ч{) при возбуждении светомА гпях З 5 ределяют по методу Паркера-Риса.
В качестве стандарта используют 9,10-дифенил-антрацен в этаноле ((,81).
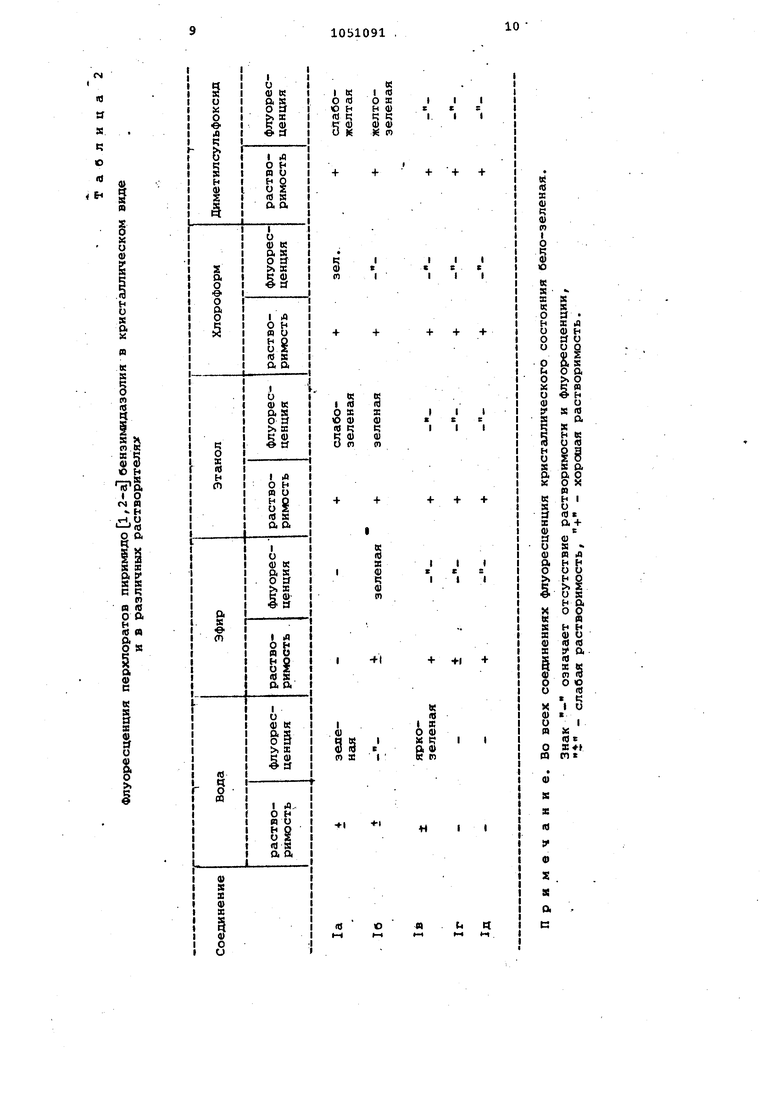
Изучают флуоресценцию полученных соединений )а-д в кристаллическом виде и в различных раст1ворителях. Исследования проводят с помощью установки для люминесцентного анализа Л-80, Результаты исследований приведены в табл. 2.
Как видно из та блицы, все соединения обладают отчетливой белозеленой флуоресценцией, яркой как в растворах, так и в сухом виде, что дает возможность использовать их в качестве флуорохромрв.
Для отработки методики флуорохромирования растительных тканей и грам-положительных микроорганизмов- проводят подбор ОПТИМёШЬНЫХ
концентраций флуорохрома и оптимального времени флуорохромирования (на -примере эпидермиса лука и Staphllococcus aureus).
Подбор оптимсшьных концентраций флуорохромов для окрашивания указанных объектов проводят следующим образом.
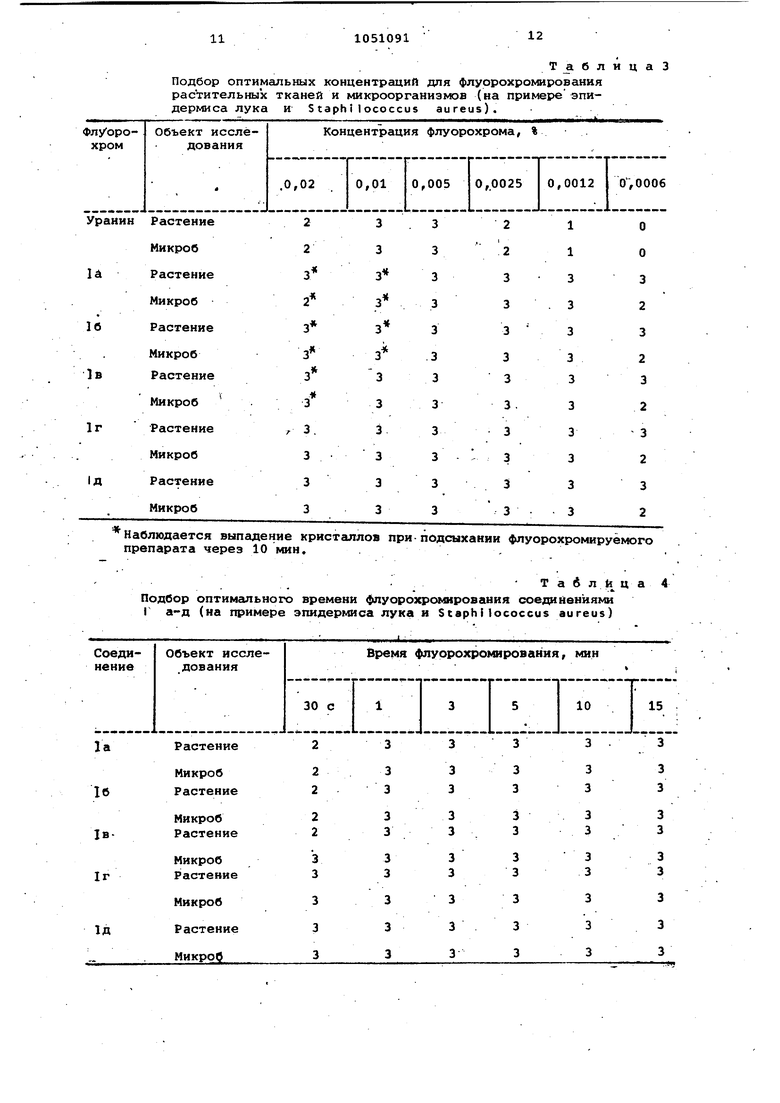
Готовят растворы соединений общей формулы 1 различных концентраций в 70%-ном этаноле и проводят флуорохромирование препаратов в течение 10 мин. Окрашенные препараты промывают дистиллированной водой и микроскопируют. Результаты приведены в табл. 3.
Интенсивность флуоресценции окрашенных объектов оценивают визуально по трехбалльной шкапе (О - отсутствие флуоресценции 1 - очень слабая флуоресценция; 2 - слабая, но отчетливая флуоресценция; 3 - интен.сивная флуоресценция.
Таким образом, предлагаемые в качестве флуорохромов соединений I а-д Окрашивают в 4-6 раз меньших по сравнению с уранином концентрациях. Оптимальная концентрация- рабочих растворов указанных соединений 0,0012, что соответствует разделени 1:80000. Увеличение концентрации не влияет на результаты окрагшвания выпадение кристаллов при подсыхании в процессе флуорохромирования легко предотвратить, используя закрнтые камеры для окрашивания препаратов.
Подбор оптимального времени флуорохроьшрования растительных тканей и микроорганизмов соединениями 1а-д на примере эпидермиса лука и StaphIlococcus aureus проводят еледующим образом.
Готовят растворы соединений Та-д в концентрациях 0,00125% (разведение 1:8000.0) и флуорохромируют препараты в течение различного времени Результаты исследований приведены в табл. 4.
Как видно из табл. 4, флуорохроирование препаратов наступает досаточно быстро и не ухудшается при величении времени окрашивания до 15 мин. За оптимальное время выбиают интервал 10 мин, так как за это время происходит почти полная фиксация микроорганизмов. Для растительных тканей достаточно 3-5 мин.
Свойства перзслоратов пиримидо l, 2aj бензимидазолия общей формулы Г как флуорохромов изучают по следующей етодике.
Для флуорохромирования готовят тонкий срез плотной растительной ткани или мазок культуры микроорганизмов. Приготовленный препарат заливают на предметном стекле 1-2 мл . спиртового раствора (на 70%-ном этаноле) перхлората пиримидо ,2 т а бензимидазолия (рабочее разведение 1:40000-1:80000, концентрация 0,0 0125-0,0025%). Время флуорохромирования 10 мин (для фиксации микроорганизмов). Окрашенные мазки или срезы промывают дистиллированной водой, накрывают покровным стеклом и микроскопируют с помощью люминесцентного микроскопа WI-2 в ультрафиолетовых лучах (Я 320-390 нм).
Выбо1р известных флуорохромов для сравнения с предлагаемыми соединениями производят как по общепринятым для УТИХ флуорохромов методикам, так и по описанной методике.
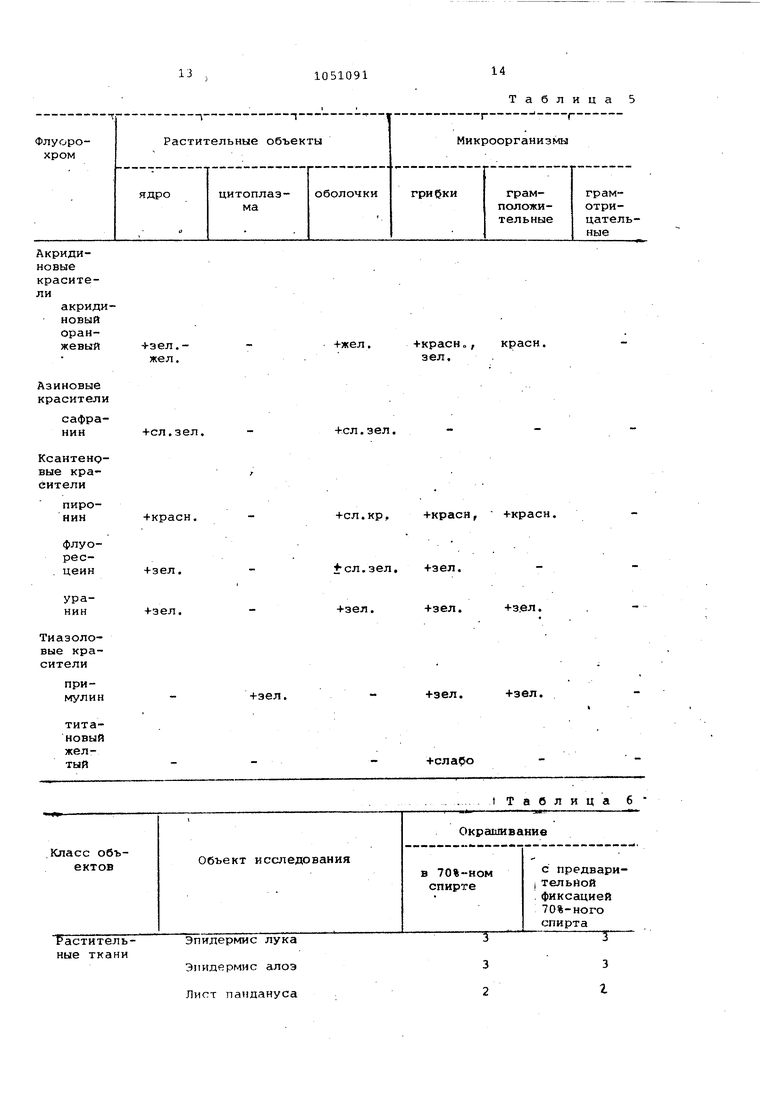
Результаты испатыний даны в табл. 5.
Как видно из данных табл. 5, наиболее близким к предла гаемым соединениям по окрашивающей способности, цвету и интенсивности флуоресценции является уранин.
Перече«ь изучаеь«лх объектов при- веден в табл. 6. Оценка интенсивности флуоресценции такая же, как в табл7 3.
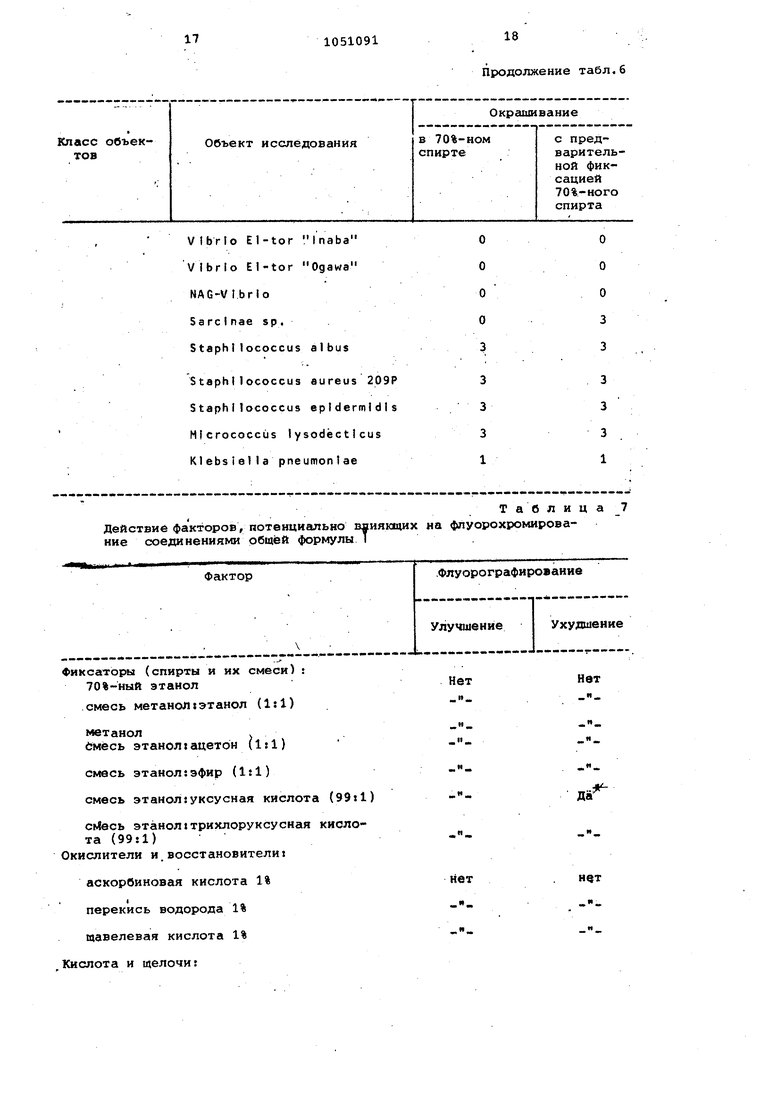
Как видно из табл. 6, предлагаемые соединения активно флуорохромируют растительные ткани, грибкиактиномицеты и .грам-положительные микроорганизмы. Для флуорохромирования грам-отридательных микроорганизмов необходим подбор специальных условий.
Полученные результаты подтверждают положение о том, что грам-поло.асительные бактерии связываются с флуорохромом энергичнее и прочнее, чем грам-отрицательные. ПоэтО1 1у данная методика может быть использована для быстрой предварительной идентификации микроорганизмов по Граму.
Кроме того, установлено, что предварительная фиксация в течение. 15 мин 70%-ным-этанолом и совмещение фиксации с флуорохромированием не влияют на люминесцентную картину объекта. Изучают действие различных фиксаторов, окислителей и восстановителей , а также различных кислот и щелочей в целях установления мешающих факторов и диапазона рН, оптимального для флуорохромирования (см. табл. 7). Таким обраэом, непродолжитёль ое действие (не более 5 мин) onHcaHHrijt факторов не оказывает отрицательного влияния на люминесцентную.картину препаратов„ Изучают также влияние ультрафиолетового и обычного света на качйство флуорохромированных препаратов. Длительное (в течение 2ч) УФ-облучение, а также продол житель ;ное (свыше 10 месяцев) хранение заключенных препаратов не приводят к ухудшению флуоресцентной картины, если таковая имеется после приготовления постоянного препарата. Таким образом, предлагаемые в качестве флуоресцентных красителей растительных тканей и микроорганизмов перхлораты пиримидо 1,2-а бензимидазолия общей формулы Т в низких концентрациях (0,006.-070012% ) имеют широкий рабочий диапазон рН (3-9), устойчивы к длительному воздействию ультрафиолетового (более 2 ч) и оейлчного (свыше 10 месяцев) света, обладают высоким квантовым выходом (до 0,56), а также устойчивы к воздействию факторов, потенциально влиянядих на флуорохромирование.
w cf
S R О
(d
M





| название | год | авторы | номер документа |
|---|---|---|---|
| Флуоресцентный краситель для микроорганизмов и растительных тканей | 1982 |
|
SU1124197A1 |
| СПОСОБ ОЦЕНКИ МОРФОЛОГИИ ПЫЛЬЦЕВЫХ ЗЕРЕН РАСТЕНИЙ | 2013 |
|
RU2563356C2 |
| ПРОИЗВОДНЫЕ 8,9-ДИГИДРОКСАНТЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2106350C1 |
| Способ диагностирования устойчивости сортообразцов хлопчатника к вилту ( ) | 1973 |
|
SU506623A1 |
| СПОСОБЫ РАЗДЕЛЕНИЯ И ХАРАКТЕРИСТИКИ МИКРООРГАНИЗМОВ С ПОМОЩЬЮ ИДЕНТИФИКАТОРА | 2009 |
|
RU2533252C2 |
| Способ определения эндотоксина бактерий в биологических жидкостях | 1977 |
|
SU657062A1 |
| НАБОР ДЛЯ ФЛУОРЕСЦЕНТНОГО ВЫЯВЛЕНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 1993 |
|
RU2102763C1 |
| Способ экспресс-диагностики биозаражения базальтопластиковой арматуры криофильными микроорганизмами | 2020 |
|
RU2757052C1 |
| СПОСОБЫ ХАРАКТЕРИЗАЦИИ МИКРООРГАНИЗМОВ НА ТВЕРДЫХ И ПОЛУТВЕРДЫХ СРЕДАХ | 2009 |
|
RU2523903C2 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2536966C1 |
Перхлораты пиримидо U 2-q бензим11дазапия общей формулы % 8% где 1а 16 R,.H; R.a R - СоН, 8 17 IB : R , ОСН. 1г R .1 , R -Н ; ОСИ |Д J. в качестве флусфесцентных красителей растительный тканей и микроорО ганизмов. :л
(М
I
ifl Я S
t;
о
Id
H
о
§
Подбор оптимальных концентраций для флуорохромирования растительных тканей и микроорганизмов (на примере эпидермиса лука и StaphiIOCOCCUS aureus).
Т 1блицаЗ Акридиновыекрасителиакридиновыйоран+эел. жевый жел. Азиновые красители сафра4-сл .зе нин Ксантеновые красителипиро+красннин флуорес+зел. . цеин
+зел.
4-зел.
+зел.
титановыйжелтый
Таблица 5
+зел. +з.ел.
+зел. +зел.
+слаОо
t Таблица 6 +сл.зел. +СЛ.КР, +красн, +красн. сл.зел. +зел. красн„, краен, зел.
Продолжение табл. б
Класс объекОбъект исследования тов
VIbrlo El-tor Inaba
Vibrio El-tor Ogawa
NAG-Vtbrlo
Sare I пае sp.
Staphllococcus albus
StaphIlococcus aureus 209 StaphIlococcus eptdermldls Mlcrococcus lysodectlcus Klebsiella pneumontae Действие факторов, потенциально влиякхцих на иие соединениями общей формулы I
фиксаторы (спирты и их смеси) t 70%-ный этанол
смесь метанол«этанол (1:1)
метанол.
ймёсь этанол«ацетои (1:1)
смесь этанол:эфир (1:1)
смесь этанол:уксусная кислот
сМесь этанол:трихлоруксусная та (99:1) Окислители и.восстановители:
аскорбиновая кислота 1%
. I
перекись водорода 1%
щавелевая кислота 1% Кислота и щелочи:
Продолжение табл.б
Окрашивание
с предварительной фиксацией70%-ного спирта
0 0 0 3 3
3 3 3
1
Нет
Нет 11 .-
Д
-1
HQT
нет
- Таблица Iшyopoxpo 4Иpoвa. П
Продолжение .табл.7 Действие фиксаторов осуществляют до флуорохромирования, остальных соединений - как до, так и после флуорохромирования. Результаты, помещенные , приведены для грамотрицательных микроорганизмов, в частности E.coli. Удается вызвать слабую .флуоресценцию грам-отрицательных микроорганизмов, заменив растворитель 70%-ный этанол диметилсульфоксидом, однако полученные данные нельзя считать удовлетворительными .
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Зеленин А.В | |||
| Взаимодействие аминопроизводных акридина с клеткой | |||
| М., 1971, с | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Метод люьлинесцентной микроскопии и микробиологии, вирусологии и иммунологии, л | |||
| , 1964, с | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Патогистологическая техника и практическая гистология | |||
| М | |||
| , 1969, с | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1983-10-30—Публикация
1982-07-01—Подача