Изобретение относится к хроматографии . а именно к способам разделения оптических изомеров аминосодержащих соединений,- и может быть использовано в различных областях химии, медицины.
Известен способ разделения оптических изомеров аминофенилуксусной кислоты, включающий элюирование изомеров через КОЛОНКУ с хиральной насадкой - ионитом 13.
Недостаток способа заключается в относительно слабом разделении оптических изомеров.
Наиболее близким по технической сущности к предлагаемому является способ разделения оптических изомеров аминокислот с помощью лигандообменной хроматографии на носителе с группировками оС-пролина в присутствии ионов двухвалентной меди. Сущность способа заключается в элюйровании изомеров через колонку, заполненную хиральнойкомплексообразующей насадкой. Взаимодействие оптических изомеров с хиральной насадкой осуществляется посредством образования координационных связей.
Лиганлообменная хроматография позволяет разделять оптические изомеры бидентатных и полидентатных аминосодержащих соединений, т.е. соединений, имеющих помимо аминогрупп дополнительные функциональные группы, способные к образованию координационных связей t2j.
Недостаток данного способа состоит в том, что с помощью лигандообМенной хроматографии разделить оптические изомеры монодентатных. аминосодержащих соединений не удается или удается лишь частично.
Цель изобретения - улучгчение разделения.
Цель достигаетця тем, что соглас но способу разделения оптических изомеров аминосодержащих соединений, включающему элюирование изомеров через колонку с хиральной насадкой с последующим детектированием, в качестве насадки используют носитель, содержащий на поверхности аминоалкиларилкетонные группировки Формулы
-NR- dH-CJ-Аг
R
.
где R и R - алкил, в том числе
(Ш) - -(CH;j)3 Ar - фенил или толил., Сущность предложенного способа состоит в элюировании оптических изомеров аминосодержащего соединения через КОЛОНКУ с хиральной насадкой, способной к взаимодействию
с изомерами с образованием ковалентных связей.
Хиральные карбонилсодержашие соединения могут быть получены следующим образом.
К 15,9 г хлорметилированного сополимера стирола с 0,5% дивинилбензола и 7% ксилилендихлорида добавляют раствор 4,5 г йодистого натрия в 54,5 мл абсолютного метанола. К
смеси приливают 230 мл абсолютного диоксана. После набухания сополимера в реакционную колбу засыпают 226 г бикаобоната натрия и 15 г хлорг.идрата метилового зфира L. -про-лина. Содержимс е колбы перемеьаивают медленным вращением в течение 15 ч при 50-55 С. Осадок отфильтровывают и промывают несколько раз водой. Высушенный продукт содержит 3,5%. N .
К полученному продукту приливают 200 мл 2 н.раствора NaOH в смеси вода:метанол:диоксан 1:1:2, выдерживают реакционную массу 6 сут при
5 комнатной температуре при периодическом встряхивании. Смолу отфильтровывают, промывают водой, слабым раствором НСЕ, водой, диоксаном и бензолом. После высуршвания смола содержит 4.2 % iN . В процессе гидро лиза происходит изменение ИК-спектра смолы: полоса 1730 см, соответствующая сложноэфирным группам исчезает, появляется новая полоса 1625 см , соответствующая ионизиро5 ванным карбоксильным группам.
К 5j8 г полученной смолы с группировками ь -пролина приливают 20 мл абсолютного диметилформамида. После набухания смолы к смеси приливают
0 по каплям мл свежеперегнанного SCCl.,Смесь кипятят на водяной бане 30 мин. Смола окрашивается в светлокоричневый цвет. После промывки толуолом, эфиром и высушивания в ва5 кууме над 2 смола содержит 4,25% Ми 22,2% сг, что соответствует 95%ному превращению карбоксильных групп.
к 6,2 г этой смолы приливают
0 100 мл абсолютно -о толуола и дают полимеру набухнуть. Затем при перемешивании приливают раствор 3,7 г в 50 мл нитробензола. Смесь нагревают на водяной бане 1 ч до
5 прекращения выделения ИСК охлаждают на ледяной бане и осторожно добавляют 100 мл воды. Смолу отфильтровывают , промывают водой, спиртом, толуолом, эфиром и выс1шивают в ваn кууме над . Смола содержит 3,6%
N .
«
Полученный носитель, модифицированный хиральным карбонилсодержащим соединением, представляет трехмер5 ный сополимер, содержардий 0,5% дивинилбензольных фрагментов, 7% бстатков ксилилендихлорида, 0,05 5,3%.аминоалкиларилкетонных лрагмен тов (в пересчете на азот/ и остальное (до 100% - остатки стирола.
Аналогичным образом получаются носители и с другими аминоалкиларилкетонными группировками.
Предложенный способ разделения оптических изомеров аминосодержащих соединений с использованием в качестве насадки колонки описанного носителя проверяется на примерах разделения конкретных смесей . примеры 1 и 2 .
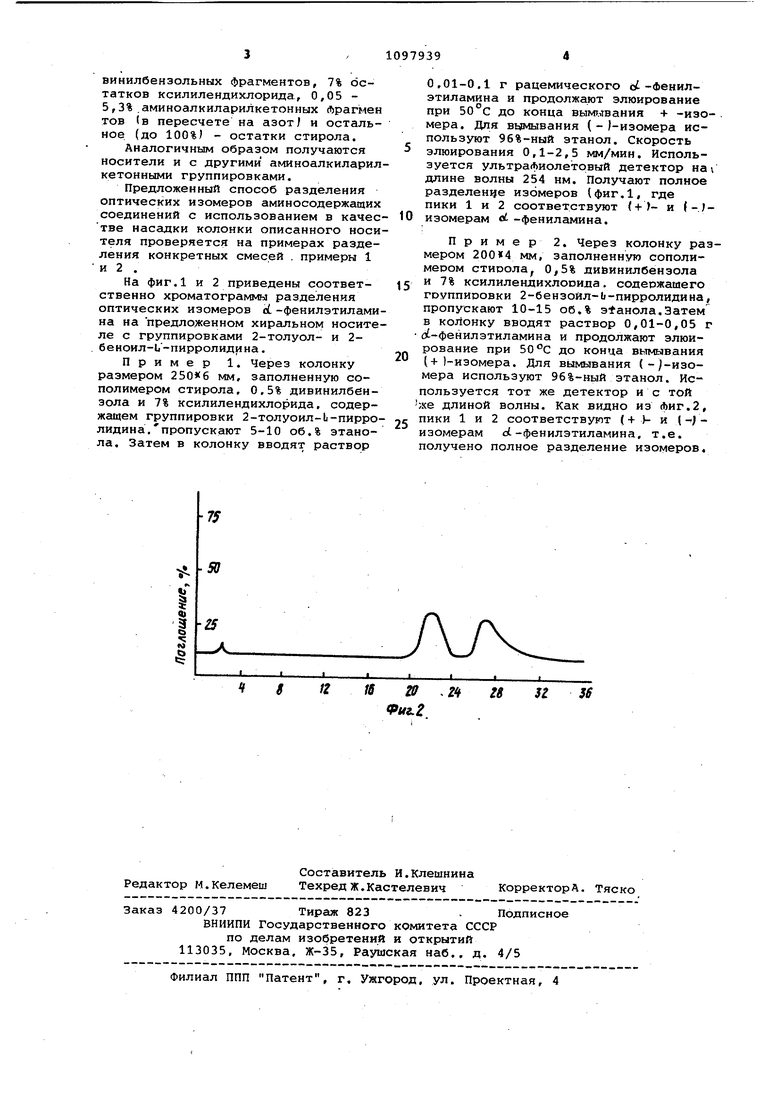
На фиг.1 и 2 приведены соответственно хроматограммы разделения оптических изомеров d. -фенилэтиламина на предложенном хиральном носителе с группировками 2-толуол- и 2беноил-1.-пирролидина.
Пример 1. Через колонку размером мм, заполненную сополимером стирола, 0,5% дивинилбёнзола и 7% ксилилендихлорида, содержащем группировки 2-толуоил-Ь-пирролидина.пропускают 5-10 об.% этанола. Затем в колонку вводят раствор
0,01-0.1 г рацемического ci-Фенилэтиламина и продолжают элюирование при 50°С до конца вымг.лвания + -изомера. Для вумывания (- 1-изомера используют 96%-ный этанол. Скорость элюирования 0,1-2,5 мм/мин. Используется ультрафиолетовый детектор на длине волны 254 им. Получают полное разделение изомеров (фиг.1, где пики 1 и 2 соответствуют ( и (-изомерам ti -фениламина.
0
Пример 2. Через колонку размером 200«4 мм, заполненную сополимером стирола, дийинилбензола И 7% ксилилендихлооида, содержашего ГРУППИРОВКИ 2-бензоил-Ь-пирролидина, пропускают 10-15 об.% этанола.Затем в колонку вводят раствор 0,01-0,05 г ot-фенилэтиламина и продолжают элюирование при 50 с до конца вьтмывания (+)-изомера. Для вымывания (-/-изомера используют 96%-ный этанол. Используется тот же детектор и с той же длиной волны. Как видно из фиг.2, пики 1 и 2 соответствуют (+ Ь и (; изомерам оС-фенилэтиламина, т.е. получено полное разделение изомеров.
| название | год | авторы | номер документа |
|---|---|---|---|
| Модифицированный кремнезем в качествеСОРбЕНТА для лигАНдООбМЕННОй XPO-МАТОгРАфии | 1979 |
|
SU833975A1 |
| СПОСОБ ВЫДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ИЗОМЕРОВ ДИГИДРОКВЕРЦЕТИНА | 2006 |
|
RU2317093C1 |
| Способ получения оптически активных L-аминокислот | 1979 |
|
SU895980A1 |
| Способ лигандообменного хроматографического разделения и анализа смеси энантиомеров аминокислот и способ получения алкилпроизводных оптических изомеров аминокислоты | 1981 |
|
SU1004876A1 |
| НОВОЕ СОЕДИНЕНИЕ САЛЬВИАНОЛОВОЙ КИСЛОТЫ Т, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2668955C2 |
| Способ разделения рацематов аминокислот на оптические изомеры | 1979 |
|
SU891641A1 |
| СПОСОБ ВЫДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ИЗОМЕРОВ ДИГИДРОКВЕРЦЕТИНА | 2006 |
|
RU2308267C1 |
| ОПТИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ 2-ИМИДАЗОЛИН-5-ОНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ ОБРАБОТКИ КУЛЬТУР | 1994 |
|
RU2126390C1 |
| ХИРАЛЬНЫЕ ОПТИЧЕСКИЕ АКТИВНЫЕ АДСОРБЕНТЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, СЕТЧАТЫЙ ПОЛИМЕР, ПРОИЗВОДНЫЕ ВИННОЙ КИСЛОТЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2121395C1 |
| СОПОЛИМЕРЫ ЭТИЛЕНА И СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ НА ОСНОВЕ ЭТИЛЕНА | 1995 |
|
RU2155776C2 |

СПОСОБ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ АМИНОСОДЕРЖАЩИХ СОЕДИНЕНИЙ, включающий элюиоование изомеров через КОЛОНКУ с хиральной насадкой с последующим детектированием, отличающийся тем, что с целью улучшения разделения, в качестве насадки используют носитель , содержащий на поверхности аминоалкилаоилкетонные группировки формулы -NR- dH- CJ -ЛР I.I где Ни . - алкил, в том числе , f (ККМ - -(CHj),-. -фенил или толил. Аг СО ;о :о :о го IS 19 117 30 3$ tfO 9in,1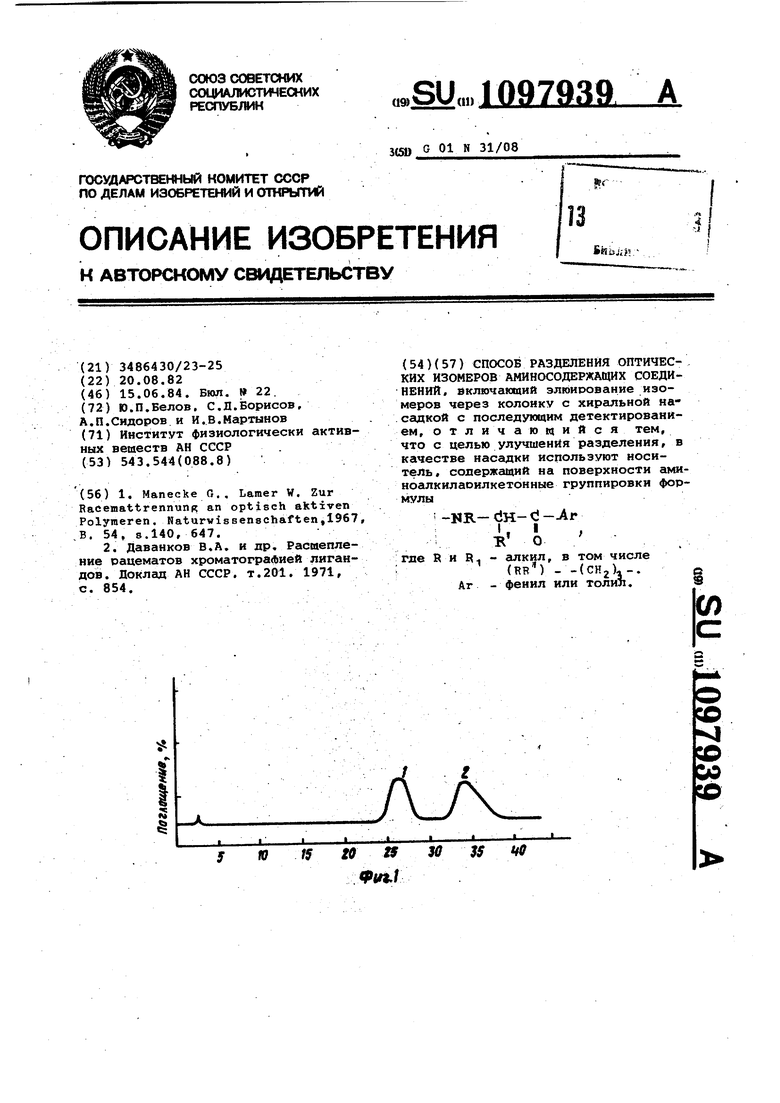
I
Z5
5
12 IS Iff ,Zf
Si 36
гв Pui.Z
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Manecke О,, Lamer W | |||
| Zur RacemattrennunR an optisch aktiven Polymeren | |||
| Naturwissenschaften,1967, ,B | |||
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Даванков В.A | |||
| и др | |||
| Расшепление рацематов хроматографией дигандов | |||
| Доклад АН СССР | |||
| Питательное приспособление к трепальным машинам для лубовых растений | 1922 |
|
SU201A1 |
| Устройство станционной централизации и блокировочной сигнализации | 1915 |
|
SU1971A1 |
| Перегонный куб | 1925 |
|
SU854A1 |
Авторы
Даты
1984-06-15—Публикация
1982-08-20—Подача