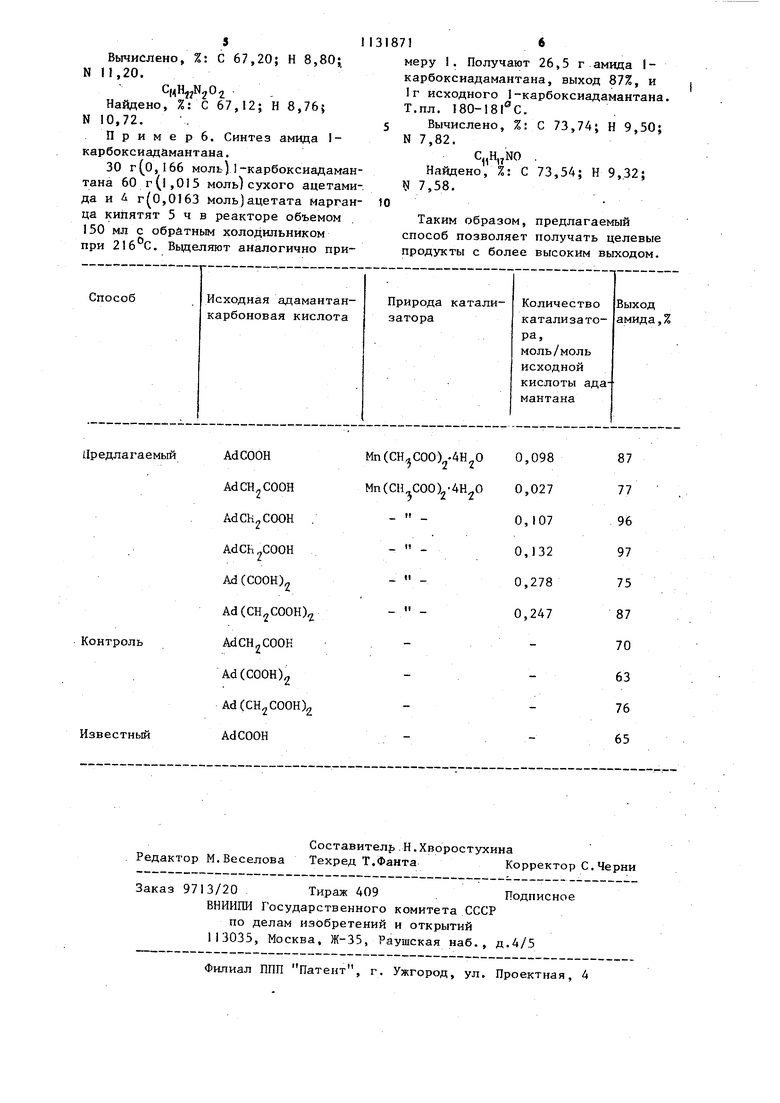
Изобретение относится к органичес кому синтезу, конкретно к усовершенствованному способу получения амидов ,адамантанкарбоновых кислот общей формулы: ГДЕ , Gf Ъ1Н2 R СВЯЗЬ, СН2 которые находят применение в качестве лекарственных препаратов, а также как промежуточные- соединения для . синтеза биологически активных веществ, пластификаторов, полимеров Известен способ получения амидов карбоновых кислот путем термической дегидратации аммонийных солей соответствующих кислот ij . Указанный метод неэффективен для производных адамантана вследстви того, что при нагревании до 200с реакция практически не идет, а при более высоких температурах разрушает ся ядро адамантана;. Известен способ получения амидов карбоновых кислот путем взаимодействия карбоновых кислот с хлорирующим агентом, например тионилхлоридом или пятихлористым фосфором, и последующей обработки образующегося хлорангидрида аммиаком 2 . Недостатком этого метода является использование высокотоксичных и огне опасных продуктов, таких как тионилхлорид, тетрагидрофуран. Кроме того хлорангидриды карбоновых кислот вещества высокотоксичные и разлагают ся при нагревании в присутствии влаги. Наиболее близким к предлагаемому по технической сущности и достигаемому результату является одностадийный способ получения амидов-адамантан-1-карбоновых кислот, заключающи ся во взаимодействии адамантан-1карбоновых кислот с избытком ацетам да при температуре кипения посхшднего(216 с)в течение 5 ч. Выход амида адамантан-1-карбоновых кислот составляет 63-69% 3j. Недостатком данного способа полу чения амидов адамантанкарбоновых кислот является сравнительно невысо кий выход целевых продуктов, что существенно, так как стоимость исходных адамантансодержащкх соединений довольно высока. Поэтому повышение выходов в реакциях получения производных адамантана, в частнбсти амидов адамантанкарбоновых кислот, является.важной задачей. Целью изобретения - повьшение выхода целевых продуктов - амидов адамантанкарбоновых кислот. Поставленная цель достигается способом получения амидов адамантанкарбоновых кислот общей формулы . ГДЕ , ее СНгС К связь, Ш., взаимодействием соответствующих карбоновых кислот адамантана с ацетамидом в присутствии ацетата марганца в качестве катализатора при мольном соотношении исходная кислота: катализатор 1:(0,027-0,278). По предлагаемому способу выход амидов адамантанкарбоновых кислот достигает 75-97% в зависимости от химической природы исходной адамантанкарбоновой кислоты. Как при меньшем, так и при большем указанного содержания катализатора в реакционной смеси выход целевых продуктов практически не повышается. В сравнении с известным способом 3j , где выход амида адамантан1-карбоновой кислоты составляет 65%, тот же амид в аналогичных условиях(температура, время, соотношение реагентовj, но в присутствии ацетата марганца в количестве 0,098 моль на 1 моль исходной кислоты получают с выходом 87%.(табл. l). В таблице приведены данные сравнения известного и предлагаемого способов получения амидов адамантанкарбоновых кислот при взаимодействии ацетамида с карбоновыми кислотами ряда адамантана продолжительность синтеза 5 ч, температура 216 С . Процессы получения моно- и диамидов адамантанкарбоновых кислот отличаются стадией выделения конечных продуктов. Как моно-, так и диамиды адамантанкарбоновык кислот, синтезируют при взаимодействии т-1збытка
ацетамида с соответствующей адамантанкарбоновой кислотой в присутствии в качестве катализатора ацетата марганца. Все реагенты загружаются в реактор с обратным холодильником. Реакционная смесь нагревается до температуры кипения ацетамида(216 С) и вьщерживается в этих условиях в течение 5 ч. Далее в случае моноамидов реакционную смесь после охлаждения до 80°С выливают в холодный раствор щелочи. При этом ацетамид и непрореагировавшая кислота переходит в.раствор, а амид адамантанкар оновой кислоты вьтадает в осадок Непрореагировавшую кислоту вьщеляют из щелочного раствора при подкислении, а амид адамантанкарбоновой кислоты перекристаллизовывают из этанола.
В случае диамидов кислот адаманта на вьщелецие целевых продуктов осуществляется следующим образом: после завершения реакции адамантансодержащей дикислоты с ацетамидом в присутствии ацетата марганца избыток ацетамида отгоняют под вакуумом, а кубовый остаток перекристаллизовьтают из смеси ацетона с водой (дйамид 1,3-дикарбоксиметиладамантанаДили этанола с водой диамид 1,3дикарбоксиадамантана .
Пример. Синтез амида 1карбоксиметиладамантана.
30 г (о, 154 моль) 1-карбоксиметил-. адамантана, 120 г(2,03 моль) сухого ацетамида и 1 г(0,00408 моль ацета-та марганца киЛятят 5 ч в реакторе объемом 250 мл с обратным холодильником при 216°С. После охлаждения не ниже 80 С выливают при перемешивании в 1,2 л холодного водного раствора 12 г едкого кали. После перемешивания образующейся суспензии в течение I ч осадок отфильтровывают промывают водой, сушат и переосаждают из этапола в воду. Получают 2 г амида 1-карбоксиметиладамантана выход 77%.
При подкислении водно-щелочного раствора, после отделения осадка амида, выделяется 7 г исходного 1-кйрбоксиметиладамантан. Температура плавления амида I-карбоксиадамантана 180-181°С.
С„Ы,,ЫО
Вычислено,%: С 74,62; Н 9,84; N 7,25.
Найдено,%: С 74,42; Н 9,84; N 7,25.
П р и м е р 2. Синтез амида 1карбоксиметиладамантана. ,
: 30 г 0.154 моль 1-карбоксиметиладамантана, 120 ,03 моль) сухого ацетамида и 4 г(0,0163 моль) ацетата марганца кипятят 5 ч в реакторе объемом 250 мл с обратнь1м холодштьНИКОМ при . Вьщеляют аналогично примеру 1. Получают 29 г амида 1-карбоксиметиладамантана, выход 96% и 1 г исходного 1-карбоксиметиладамантана.
5 ПримерЗ. Синтез амида 1-карбоксиметиладамантана.
30 г(0,154 моль) 1-карбоксиметил- адамантана, 120 г (2,03 .моль)сухого ацетамида .й-5 г (0,0204 моль)ацетата
0 марганца кипятят 5 ч в реакторе
объемом 250 мл с обратным холодильником при 216 С. Выделяют аналогично примеру 1 . Получают 25 г амида 1карбоксиметиладамантана, выход 97%
5 и 3 г исходного 1-карбоксиметиладамантана,
П р и м е р 4. Синтез диамида 1,3-дикарбоксиадамантана.
30 г(о,118 моль)1,3-дикарбоксиадамаптана, 120 г (2,03 моль)сухого .ацетамнда и 8 г (0,0326)моль ацетата марганца кипятят 5 ч в реакторе объемом 250 мл с обратным холодильником при 216 С. Затем под вакуумом ОТГОНЯ16Т избыток ацетамида, а кубовый остаток перекристаллизовывают из смеси этанола с водой. Выход диамида 1 ,3-дикарбоксиадамантана 22,4 г (75 %). 255-256°С.
Вычислено, %: С 64,86;.Н 8,11;
N 12,61 .
Cl2«lftN202
Найдено,%: С 64,58; Н 8,03; N 1,.51.
П р и м е р 5. Синтез диамида 1,3-д11карбоксиметиладамантана.
30 г(0,134 моль)1,3-дикарбоксиметиладамантана, 120 г(2,03 моль)
сухого ацетамида и 8 г 0,0326 моль ацетата марганца кипятят в реакторе объемом 250 мл с обратным холодильником при 216 С 5 ч, затем под вакуумом отгоняют избыток ацетамида, а кубовый остаток перекристаллизовывают из смеси ацетона с водой. Выход диамида 1,3-дикарбоксиметиладаманта на 25,9 г(87%). Т.пл. 169-170с.
5
Вычислено, %: С 67,20; Н 8,80; N 11,20.
Найдено, %: С 67,12; Н 8,76; N 10,72.
П р и м е р 6. Синтез амида Iкарбоксиадамантана.
30 г(0,166 моль)1-карбоксиадамантана 60 г(|,015 моль)сухого ацетамида и i г/0,0163 моль)ацетата марганца кипятят 5 ч в реакторе объемом 150 мл с обратным холодильником при 216 С. Вьщеляют аналогично при318716
меру I. Получают 26,5 г амида Iкарбоксиадамантана, выход 87%, и 1г исходного 1-карбоксиадамантана. Т.пл. 180-181 0.
5 Вычислено, %: С 73,74; Н 9,50; N 7,82.
С H,;NO .
Найдено, %: С73,54; Н 9,32; У 7,58. 10
Таким образом,предлагаемый
способ позволяетполучать целевые
продукты с болеевысоким выходом.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных N-фениладамантан-1-карбоксамида | 2016 |
|
RU2626237C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИЛА 1-АДАМАНТАНКАРБОНОВОЙ КИСЛОТЫ | 2006 |
|
RU2316540C1 |
| Способ получения ароматических амидов 1-адамантанкарбоновой кислоты | 2019 |
|
RU2698193C1 |
| 1-АМИНОМЕТИЛ-3-АМИНОЭТИЛАДАМАНТАН - МОНОМЕР ДЛЯ СИНТЕЗА СОПОЛИИМИДОВ С ПОВЫШЕННОЙ ГИДРОЛИТИЧЕСКОЙ УСТОЙЧИВОСТЬЮ | 1985 |
|
SU1317879A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТИЛ-3-ФОРМАМИДА (АМИДА 1-ХЛОРАДАМАНТИЛ-3-КАРБОНОВОЙ КИСЛОТЫ) | 2010 |
|
RU2455282C2 |
| Способ получения бензанилида | 2019 |
|
RU2712053C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ НИТРИЛОВ | 2003 |
|
RU2240310C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЗОЛОВ | 1969 |
|
SU428605A3 |
| Способ получения 1,3-бис/карбоксиметил/ адамантана | 1980 |
|
SU941348A1 |
| ПРОИЗВОДНЫЕ ЗАМЕЩЕННЫХ 1-(7-ХЛОРХИНОЛИН-4-ИЛ)ПИРАЗОЛ-3-КАРБОКСАМИД-N-ОКСИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2145323C1 |
СПОСОБ ПОЛУЧЕНИЯ АМИДОВ АДАМАНТАНКАРБОНОВЫХ КИСЛОТ общей формулы О 0 ,# ГДЕ ,С тш.. Н связь, СН2 5 взаимодейсгвием соотво.тствующих карбоновых кислот адамантана с ацетамидом при кипении реакционной среды, отличающийся (Л тем, что, с целью повышения выхода целевых продуктов, процесс веДут в присутствии ацетата марганца в качест ве катализатора при мольном соотношении исходная кислота: катализатор 1:(О,027-0,278).
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Бюлер Н., Пирон Д | |||
| Органические синтезы | |||
| Ч.П, М., Мир, 1973 | |||
| с | |||
| Переносный ветряный двигатель | 1922 |
|
SU384A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1984-12-30—Публикация
1983-09-14—Подача