1 22
2, Способ получения полиамидных мембран для хроматографии путем формования отливочного раствора, включающего поликапроамид,, муравьиную кислоту и воду, на по;1Д1Ожке с последующим экспонированием предсформован-- ной мембраны, о т л и ч а ю щ и и - с я тем, чтОэ с целью повышения производительности процесса формования мембран, в качестве подложки используют лавсан, а хроматографический слой формуют из раствора, содержаще- го,мас.%: поликапроамид 13-15; ацет- амид 24-26; fypaвьинyю кислоту
Изобретение относится к физической химии высокомолекулярных соединений, более конкретно к составам отливочного раствора для формования полиамидных мембран и к способам получения таких мембран, и может найти применение для производства мембран, необходимых для хроматографи- ческого разделения различных классов веществ, например, при анализе гербицидов, инсектицидов, пестицидов в сельском хозяйстве или при анализе антиоксидантов в пищевой промьшшен- ности, при определении содержания фе нольных соединений в сточных водах промышленных предприятий и т„ть
Цель изобретения - повыщенне производительности процесса формования полиамидных мембран, повьш1ение эффективности и скорости хроматографичес кого разделения на мембранах и придание лавсановой пленки шерохо затас- ти.
Пример 1, Лавсановую пленку толщиной 00 мкм размерами 8x15 см погружают в смесь, содержащую 80 мл 20%-ного водного раствора NaOH и 20 мл этиленгликоля (4:1 по об-ьему) Температура смеси 70 С, Через 15 Min пленка равномерно помутнеет. Ег извлекают, промывают водой и сушат, Сухую предобработанную пленку погружают в 100.мл отливочного раствора, содержащего, мас.%;
Промьшшенный поликапроамид
-
ii--52 и до 100, при температуре 60-80 С с последующим экспонированием мембраны на воздухе 30 - 60 с и обработкой в осадительной ванне, содержащей 30-40 мас.% водного раствора ацетамида, при 15-35 С.
3, Способ по по 2, о т л и ч а ю - щ и и с я тем, 4TOj с целью придания лавсановой пленке шероховатости, .ла1 сановую пленку предварительно обрабатывают смесью 20-25%-ного водного раствора едкого натра и этиленгли- коля г гри их объемном соотношении H -6t при 70-80 С в течение 12-20 мин
-
i 2Р
25
35
ПА-г с мол.м, в
интервале
20-30 10 13
Ацетамид ч ,,п , а 26
Вода9
Муравьиная кислота
(95%-ная)52
Пленку выдерживают до полного и разномерного смачивания поверхности, что занимает 35 мин, затем извлекают выдерживают ма воздухе 30 с к погружают на 5 мин в 200 мл 30%-но- го водного paciBopa ацетамида при zO С5 чог о гшенку отмывают во- дой npi- 60 С (5x300 мл) и сушат на воздухе,
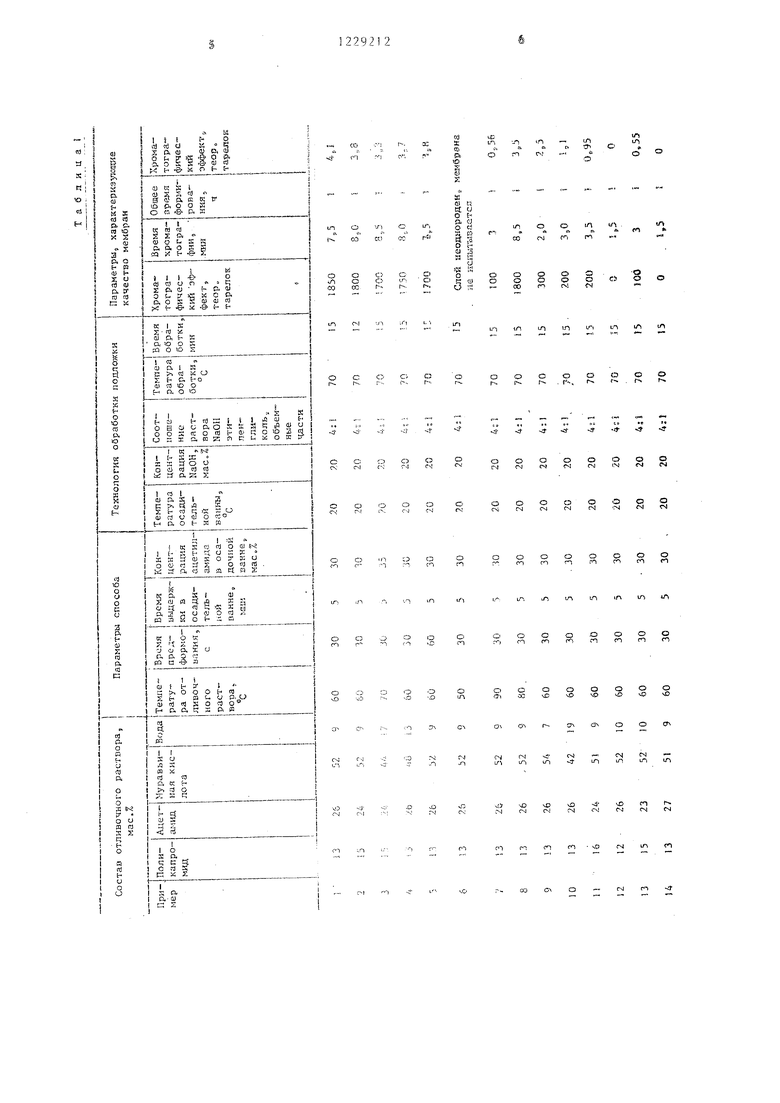
II р и м е р ы t-40 представлены в табл „ 1 ,
Для определения эффективности и других характеристик полученных мемб- pai на полиамидной мембране (2x5 см ) осущестЕ1Ляют хроматографию 1 мкл сме- С1- , вос1зми данзильных (DNS) производ- иь:х аминокислот: оксипролина, пролииа, триптофана, глицина, аланина, фе- ; илаланина 5 лейцина и изолейцина. Концентрация каждой аминокислоты в водном растворе составляет . При освещении УФ-лампой с - 365 нм все E -A-S-производные наблюдаются в виде желтсз-зеленых люминисцирующих зон. Хромагографию осуществляют восходящим способ(5м в системе бензол: ледяная уксусн.чя кисмота (8:2 по об7,5ему) „
31
Число теоретических т.арелок N определяют по ДНС-изолейцину, как
I N 16(-) 2, где 2 - расстояние от
центра-пятна до линии старта; D - диаметр пятна,
Время хроматографического разделения определяют по времени подъема фронта растворителя от стартовой до финишной черты (длина пробега 3,5 см). Воспроизводимость характеристик подтверждается многопробным (6-10 раз) получением мембран в идентичных условиях с воспроизведением хроматографической эффективности с относительной ошибкой не выше 12%. Значение времени хроматографии в параллельных идентичных условиях воспроизводится с относительной ошибкой не выше 10%,
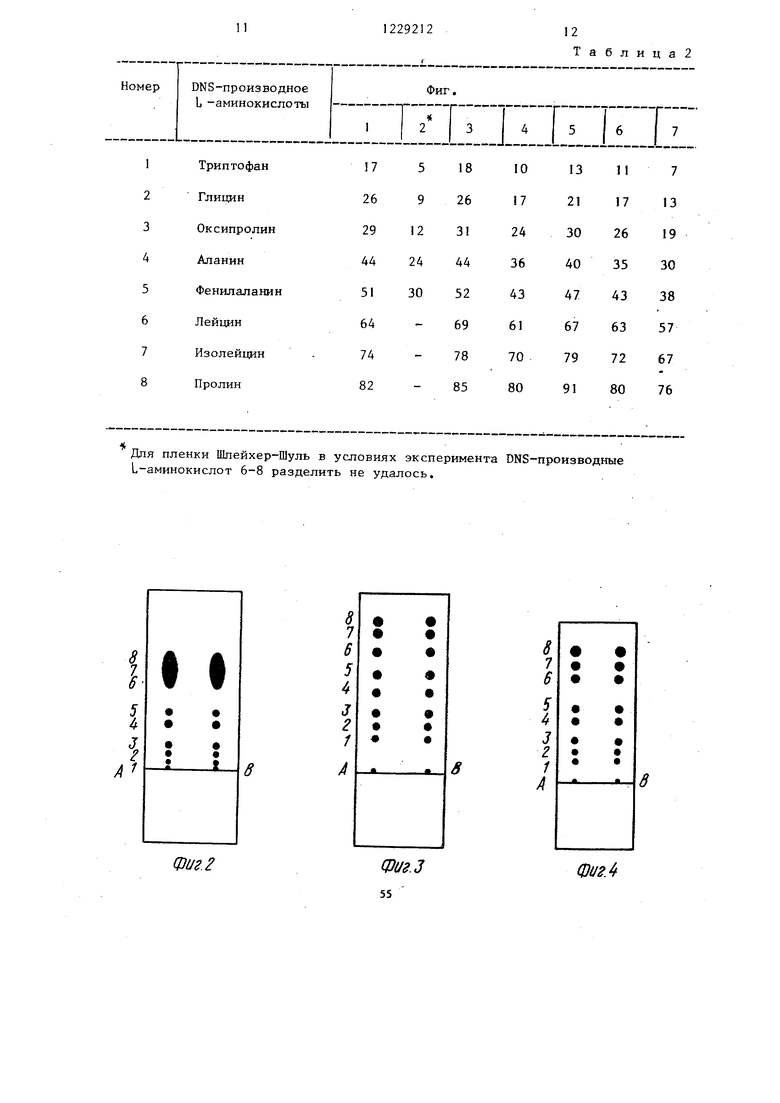
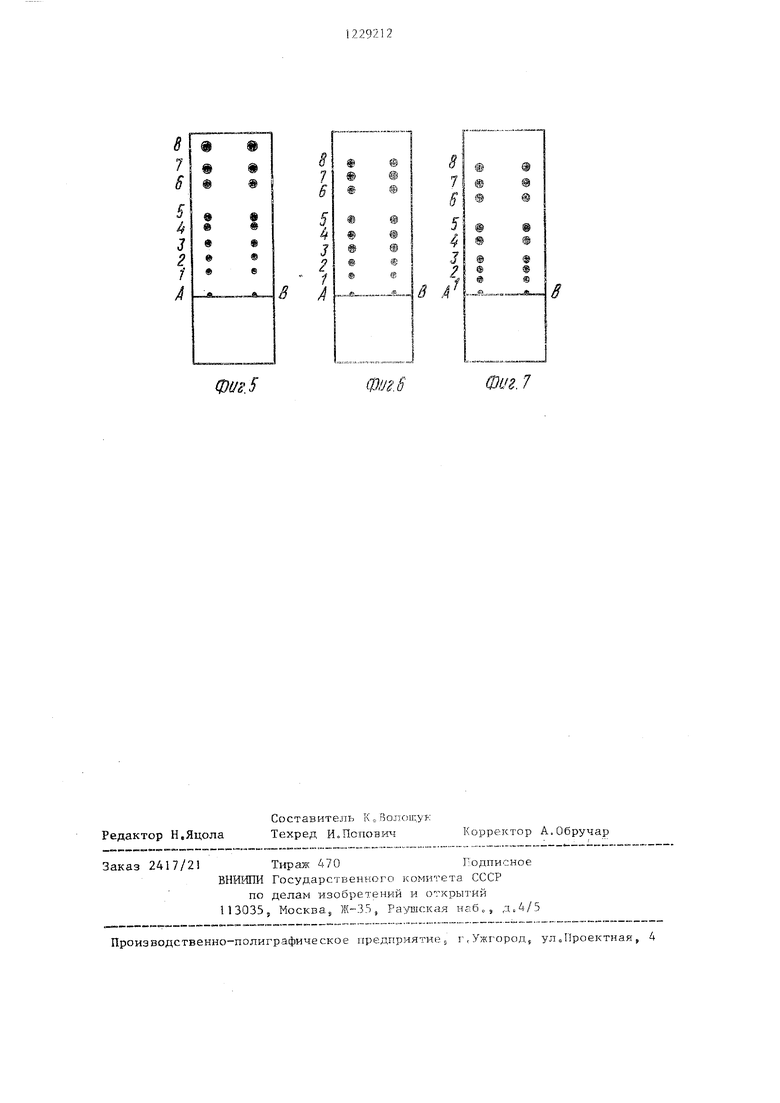
На фиг. 1 представлена фотокопия хроматограммы DNS-производных аминокислот на мембранах ВДН (Англия); на фиг, 2 - то же, на мембранах фирмы Шлейхер и Шуль (ФРГ); на фиг. 3 то же, на мембранах, полученных по известному способу, на фиг, 4 - 7 - то же, на мембранах полученных по примерам 1,8, 21 и 27 соответствен- но.
Электронно-микроскопические исследования предлагаемых мембран подтверждают изотропность структуры полимерного слоя. Средний радиус пор мембраны составляет 0,15+0,02 мкм, а пористость 65-80%.
Для хроматографии используют N-ка меру с насьщением. Толщина хроматографического слоя равна 37-40 мкм.
На копиях хроматограмм DNS-произ- водных аминокислот, АВ - линия старта. Идентификация пятен и значения R X 100 для индивидуальных пятен приведены (среднее из двух) в табл,2
Анализ таблицы позволяет дать обоснование предлагаемым интервальным значениям: увеличение концентрации поликапроамида выше 15 мас,% (пример 11, содержание поликапроамида 16 мас,%) приводит к снижению хроматографической эффективности, до 200 теор.тарелок; снижение концентрации ниже 13 мас,% (пример 12, содержание поликапроамида 12 мас,%) приводит к падению хроматографичес- кой эффективности до 0; увеличение
5
5 0
5 0
5
5
0
5
24
концентрации ацетамида выше 26 мас,%
(пример 14, содержание ацетамида 27 мас.%) приводит к снижению хроматографической эффективности до 0; снижение концентрации ацетамида ниже 24 мас,% (пример 13, содержание ацетамида 23 мас,%) сопровождается понижением хроматографической эффективности до 100 теор,тарелокJ повышение концентрации муравьиной кислоты выше 52 мас,% (пример 9, концентрация муравьиной кислоты 54 мас,%) приводит к падению хроматографической эффективности до 300 теор,тарелок; снижение концентрации муравьиной кислоты ниже 44% мас.% (пример 10, концентрация муравьиной кислоты 42мас,%) сопровождается снижением хроматографической эффективности до 200 теор, тарелок; снижение температуры отливочного раствора ниже 60 С (пример 6, температура отливочного раствора 50°С) приводит к визуально фиксируемой неоднородности хроматографического слоя; повышение температуры отливочного раствора выше 80 G (пример 7, температура отливочного раствора 90 С) сопровождается падением хроматографической эффективности до 100 теор, тарелок ; увеличение ни выдержки на воздухе до 70 с (пример 15) приводит к снижению хроматографической эффективности до 0; снижение времени выдержки до 20 с (пример 16) сопровождается фиксируе- . мой неоднородностью хроматографического слоя; повышение температуры оса- дительной ванны до 50 с (пример 25) или снижение до 10 С (пример 24) приводит к визуально фиксируемой неоднородности- хроматографического слоя; снижение концентрации щелочи до 17 мас,% или повышение до 28 мас,% при обработке лавсановой подложки (примеры 30 и 3I соответственно), изменение соотношения щелочной раствор: этиленгликоль до 3:1 (пример 32) или до 7:1 (пример 33) приводит к отслоению хроматографического слоя от лавсановой подложки; к отслоению хроматографического слоя приводит изменение температуры щелочной обработки лавсановой пленки до 65 С (пример 34) или до 85 С (пример 35); аналогично действует уменьшение времени щелочной обработки до 10 мин (пример 36) или увеличение до 23 мин (пример 37).
S о -.
о о
о ci
in CI
r-.
XI ttl
О
a
о
OJ
и
« о
c5
о о о о о о
- со гл
О
о
1Л
Sа (Пfc
оО
О С О О
LTiLn1Л1Л
о о с о
Г.Р-Г , f-.
о о о о
Г-ц{- ,
:i f- -tf
-If f
О О a О
(.МrsjСЧ
о о ca о
f4 Г4
oooooooo
r-, n) СЛ r гЛ o сЛ fO
vAlA1ЛminlA
О О О О О О О m (п rOf f-) fo ГО
с;:зoooooooo
LAО 1ССчС ОчОО чО
. ОCTN
CNi: jr4v r - cN|r4-
-f У inи 1- LTlLTiЮl/
-.15 -чО чо о -d- i: en t-. гч1 oj cN г сч fN
m m m m -,3 r%i m л
rsi m -оДля пленки Шлейхер-Шуль в условиях эксперимента DNS-производные Ь аминокислот 6-8 разделить не удалось.
в
Фиг. 2
Таблица2
8
8
Фиг.З
5
Редактор Н.Яцола
Составитель К,, Волощут : Техред И«Попович
Заказ 2417/2 Тираж 470Подписное
Государственного комитета СССР
по делам изобретений и от крытий П3035, Москва S Ж-ЗЗ, Ра ш1ская Нстбо д. 4/5
Производственно-полиграфическое предприятиеj г,Ужгород, 5 улс Проектная, 4
В
Фш.ё
Фиг. 7
Корректор А.Обручар



| название | год | авторы | номер документа |
|---|---|---|---|
| Состав для формования полиамидной ультрафильтрационной мембраны | 1990 |
|
SU1757726A1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОФИЛЬТРАЦИОННЫХ МЕМБРАН | 2000 |
|
RU2161530C1 |
| Способ получения микропористой полиамидной мембраны | 1987 |
|
SU1503841A1 |
| Способ получения микропористых полиамидных мембран | 1984 |
|
SU1281571A1 |
| ФУНКЦИОНАЛИЗИРОВАННЫЕ ТОНКОПЛЕНОЧНЫЕ ПОЛИАМИДНЫЕ МЕМБРАНЫ | 2009 |
|
RU2519377C9 |
| ПОЛИАМИДНАЯ УЛЬТРАФИЛЬТРАЦИОННАЯ МЕМБРАНА | 1989 |
|
RU2010594C1 |
| Полиамидная композиция для мембранного фильтра | 1989 |
|
SU1699490A1 |
| КОМПОЗИЦИЯ ПОЛИАМИДНОЙ СМОЛЫ | 2011 |
|
RU2572983C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРВАПОРАЦИОННОЙ КОМПОЗИЦИОННОЙ ПОЛИМЕРНОЙ МЕМБРАНЫ | 1994 |
|
RU2094105C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИАМИДНЫХ МЕМБРАН | 1989 |
|
RU2010595C1 |
1. Состав отливочного растйора для формования полиамидных мембран, включающий поликапроамид, воду, муравьиную кислоту,, отличающийся тем, что, с целью повышения эффективности и скорости хрома- тографического разделения на мембранах, состав дополнительно содержит ацетамид при следующем соотношении компонентов, мас.%: Поликапроамид 13-15 Ацетамид24-26 Муравьиная кислота44-52 Вода.до 100 с € (Л с: ьо ю со to ф{/г./



| Wang К.Т., Wang I S I.J.Chromat., 1976, 27, p.318. |
Авторы
Даты
1986-05-07—Публикация
1984-08-02—Подача