Изобретение относится к способу получения новых производных хиназо- яннона, которые проявляют актив.ность против кокковых инфекций и могут найти применение в ветеринарии.
Цель изобретения - синтез производных хиназолинона, обладающих пониженной токсичностью,
Пример 1 . Получение гидразона 6-хлор-7-бром-3- 3-(3-oкcи-2-пипe- pидил) -ацетонил - (ЗН)- хиназолин-4- она (соединение 1) формулы
1,8 г 6-хлор-7-бром-3- 3-(3-окси- 2-пиперидил) -ацетонил -(ЗН) -хиназо- лин-4-она нагревают в 200 мл этанола до получения чистого раствора, В этот раствор добавляют раствор 0,25 мл гидрата гидразина в 50 мл этанола -и 400-500 мг кислой сульфо- смолы (используют - Амберлист 15 Н), Реакционную смесь нагревают при температуре легкой дефлегмации в течение 40 ч. Через 30/40 мин можно наблюдать образование продукта в суспензии. После охлаждения смолу сливают и твердые частицы отделяют фильтрованием и промывают смесью Этанола с водой (1:1), После сушки получают П., 7 г целевого продук-та в виде белого твердого вещества (т,пл, 204-205°С),
Данные ИК-спектроскопии показывают исчезновение полосы при 1720 см (VC о) и наличие полосы при 1690 см (VC 11).
П р и м е р 2, Получение соединения этилгидразона 6-хлор-7 бром-3- ГЗ-(З-метокси-2-пиперидил)-ацетонил (ЗН)-хиназолин-4-она (соединение 2) формулы
ОСИ
В раствор 1 г 6-хлор-7-бром-3- 3-(3-метокси-2-пиперидил)-ацетонил - (ЗН)-хиназолин-4-она в 200 мл этанп
5
0
5
0
5
0
5
0
5
ла добавляют раствор 0,9 г дтилен- гидразиноксалата и 0,85 г ацетата натрия в 15 мл воды. Смесь нагревают при температуре дефлегмации, после чего осуществляют тонкослойную хроматографию (слой окиси алюминия, растворитель: смесь хлороформа с метанолом при объемном отношении 9:1) до тех пор, пока нЪ наблюдаются только следы исходного кетона (около 40 ч), Реакционную смесь, содержащую твердое вещество в суспензии, профильтровывают для отделения этого вещества, промывают его смесью этанола и воды в соотношении 1:1,
Таким образом, получают 0,3 г целевого продукта (белое твердое вещество, т,пл, 205-206°С),
Пример 3, Соединение получают по примеру 1 (соединение 1), а также и в соответствии со следующей процедурой,
5 г 6-хлор-7-бром-3- 3-(3-окси-2- пиперидил)-аиетонил -(ЗН)-хиназолин- 4-она растворяют в смеси 50 мл этанола и 50 мл буферного раствора уксусной кислоты и ацетата натрия (рН 6) ,
В этот раствор добавляют 2 мл гидрата гидразина. Спустя 48 ч после добавления растворители удаляют и остаток обрабатывают разбавленным водным раствором NaOH до получения основного рН,
Не растворившийся продукт собирают фильтрованием, получив 4,8 г целевого продукта, данные ИК-спектроскопии которого идентичны продукту 1 (пример 1), Образец, рекристаллизо- ванный из метанола, имеет т,пл, 214 С с разложением.
Пример 4, 11 ирокомасштабное . производство соединения (пример 1,
соединение 1) осуществляют следующим образом,
В эмалированный реактор емкостью 300 л, снабженный системой регулировки температуры и {механической мешалкой, загружают 100 л 95%-ного этанола, 10 кг 6-хлор-7-бром-3- 3-(З- окси-2-пиперидил)-ацетонил -(ЗН)- хиназолин-4-она, 100 л водного буферного раствора (уксусная кислота и ацетат натрия) при рН 4,3,
Смесь ,перемешивают до получения чистого раствора, к нему добавляют 2 л гидрата гидразина. Реакционную смесь перемешивают при 40°С, Реакцию сопровождают анализом (ГЖХ или ТПХ)
3129
образцов, периодически отбираемых из реактора. Через 17 ч наблюдают наличие только следов ксходного продукта (производного хиназолин-4-она). Летучие продукты (этанол, воду и часть уксусной кислоты) удаляют под вакуумом, их можно собрать и использовать в последующих операциях.
Остаток нейтрализовывают путем добавления 20 л воды и льда, содер- жащих 6 кг NaOH, в то время как реактор охлаждают снаружи. Твердый осадок собирают фильтрованием (фильтр-пресс), промывают умягченной водой (около 60 л) до достижения рН нейтральной среды и высушивают.
Таким образом, получают соединение 1 выходом 91,5% (в расчете на производное хиназолин-4-она), причем данные спектроскопического анализа этого соединения такие же, как для соединения, описанного по примерах 1 или 31
Соединения формулы
О Ш
J т
Ъ1Н
R.
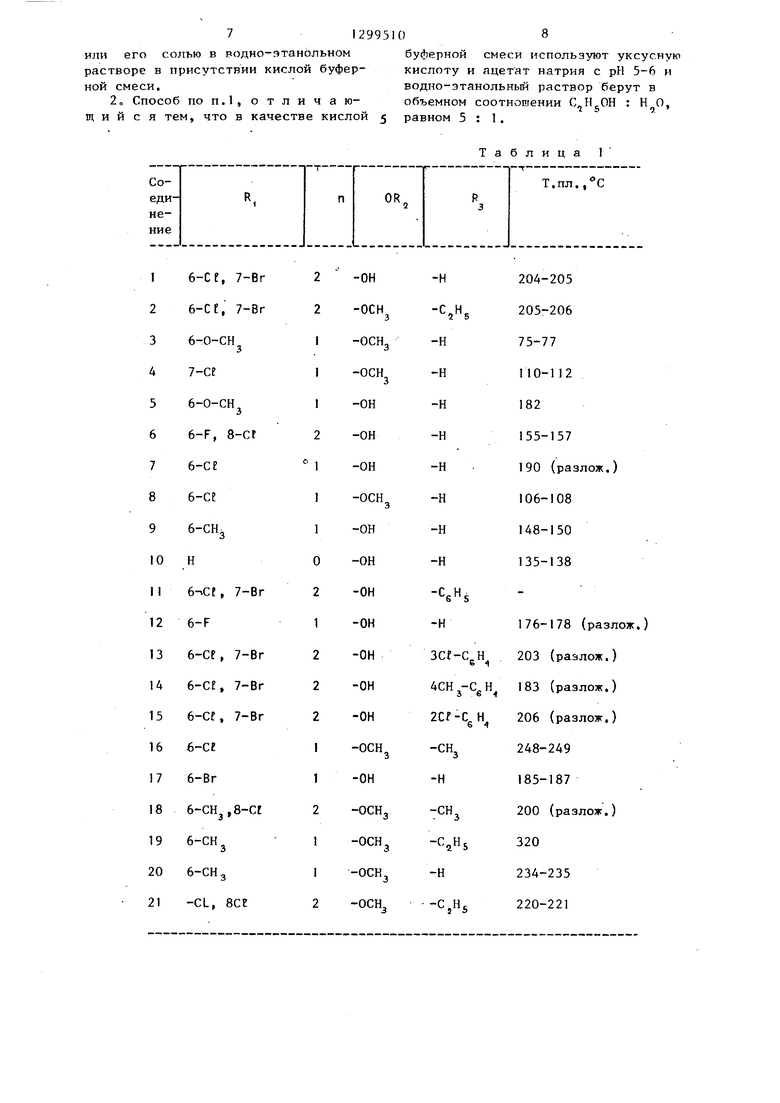
Данные элементного анализа и про- тонной ЯМР-спектроскопии всех соединений согласуются в присвоенной им структурной формулой. Температура плавления, при указанной температуре соединения разлагаются, Данные ИК- гГ:спектроскопии, указаны только значимые полосы. Получение соединения 1 подробно описано в примере 1 или 3. Получение соединения 2 подробно описано в примере 2 (табл.).
Пример 3. Соединение получают по примеру 3, но заменяют раствор уксусной кислоты и ацетата натрия одним из следующих буферов: гидроокись натрия + монокалиевая соль фталевой кислоты рН 5; гидроокись натрия + монокалиевая соль фосфорной кислоты рН 5,8-6; бензойная кислота + бензоат натрия рН 5,7;
монокалиевая соль винной кислоты + гидроокись натрия рН 5,5, и получают продукты и выходы такие же, как в примере 3.
O 5
0
5
0
5
5
0
104
Пример 6. По методике, описанной в примере 3, исходя из подходящего производного хиназолинона и производного гидразина, получают соединения формулы (1), представленные в табл.1
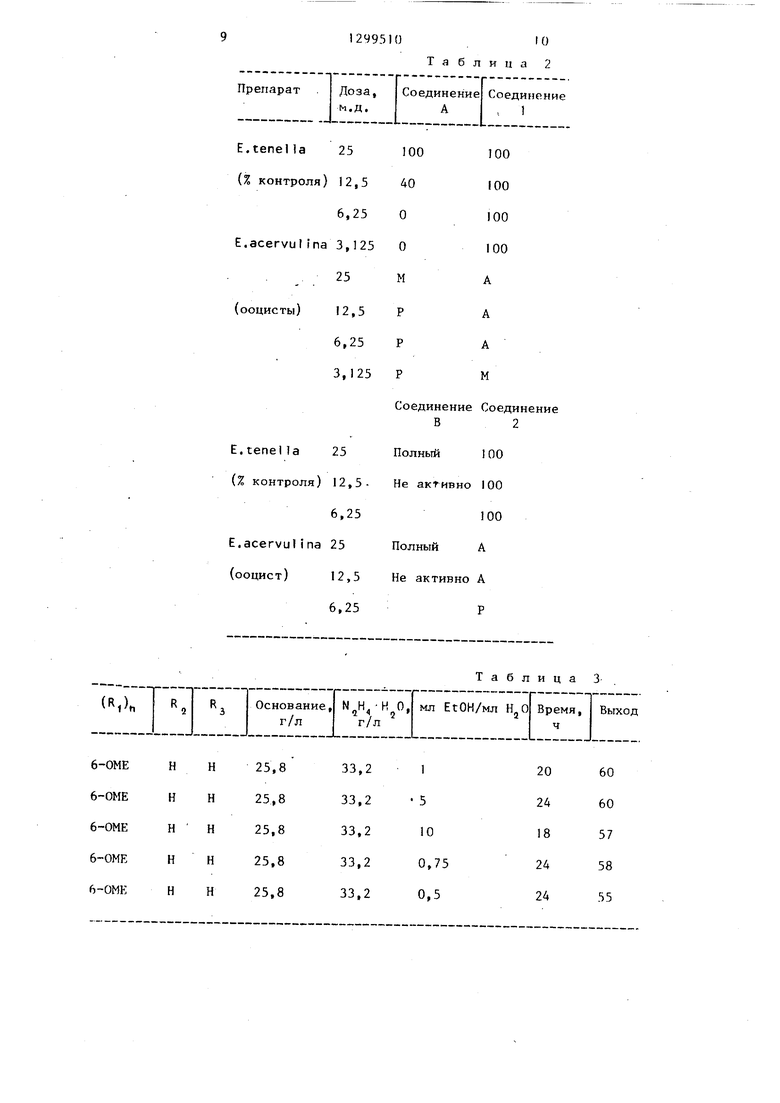
Определение противококковой активности in vivo.
Группы из пяти молодок (куры Рейнджер) в возрасте 1 нед. заражают смесью 5500 спорулированных оонист Eimeria tenella и 5000 спорулированных ооцист Eimeria acervulina. Испытуемое соединение вводят в предварительно выбранной дозе в смеси с кормом для домашней птицы (LD ), бедным витамином К и не содержащим других добавок. Молодкам скармливают по потребности приготовленный фураж, начиная за 1 день до заражения и продолжая в течение следующих пяти дней, В качестве контроля используют не зараженных не обработанных цьтлят и зараженных не обработанных цыплят.
Учет активности на Eimeria tenella осупхествляют, определяя поражение если оно было, через 5 дн после заражения, а активность на Eimeria vulina - определяя наличие ооцист, если они были, в экскрементах через. 5 дн после заражения. Предлагаемые сое- динения при испытаниях против Е. tenella иЕ.acervulina по описанной методике демонстрируют высокую активность даже при очень низких дозах,
Например, соединение 2 (пример 2) показывает высокую активность против Е. acervul ina при дозе 6,25 м.д. и высокую активность против Е,tenella при дозе 12,5 м.д. То же соединение при испытании на токсичность для домашней птицы показывает СД 100 мг/кг веса тела. Никаких симптомов отравления не наблюдается у цьтлят, которым скармливают корм для домашней птицы, содержащий 100 м.д, соединения 2, во время проведения испытания на активность.
Для сравнения противококковой активности берут соединения следую55
512
где а.Х - группа N-OH (соединение А)I что является свободнь1м основанием}
R ,j Н (оксимпрозводное галофугинона);
группа N-NH (соединение 1, табл,2); Hi
группа N-O-CjHj (соединение в), что является этилоксимпроизводным гало- фугинона;
Н;
ь.х
с.Х
d.X -.группа N-NH-C HE (соединение 2, табл.2); Rrt СН.
Указанные соединения испытьшают на про тивококковую активность против E.te nella HE.acervulina по вьшеописанной методике,
Активность против E.tenella вы- ражаю т как процент контроля инфекции
Коэффициент токсичности
(прирост веса незараженных необработанных)
100-100
(прирост веса зараженных обработанных)
5
0
О6
определенной дозе, а активность против E.acervulfna выражают на основе наличия, если они были, ооцист в экскрементах и классифицируют следующим образом: А отсутствуют, М присутствуют в минимальном коли- честве Р - присутствуют. .
Определение активности и токсичности соединений формулы I .
Токсичность оценивается параметром эффективность роста. Коэффициент токсичности определяется из допущения, что прирост веса незараженных ид 1плят по отношению к зараженным необработанным цыплятам равен 100, и оценивается весовой прирост обработанных и зараженных цыплят по отношению к той же величине для зараженных необработанных цыплят.
Коэффициент т дксичности определяется следующим образом.
(прирост веса зараженных необработанных)
(прирост веса зараженных необработанных)
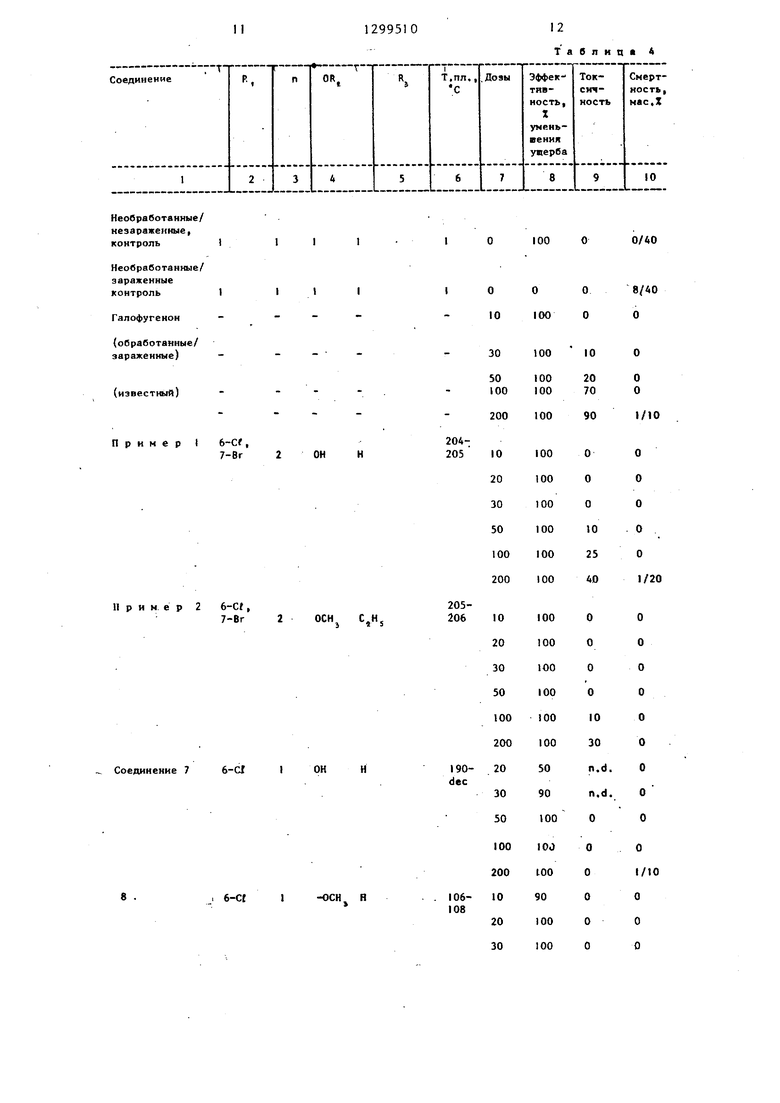
Эффективность против Coccidia Определяют как процент снижения внутренних повреждений у домашней птицы (табл,4),
В соответствии с методикой примера 3 проводят исследование, проводимое в водно-спиртовом растворе в присутствии кислотной буфферной системы.
Опыты проводят, изменяя в широких пределах отношение этанол/вода, к водной фазе добавляют СНоСООН и CH.COONa в таких количествах, чтобы достичь концентрации в воде уксусного буффера между 0,5-1 М (табл,3).
Диапазон отношения EtOH/H, находится между 10-0,5. Предпочтительный диапазон заключен между 5 и 1,
Формула изобретения
1, Способ получения производных хиназолинона формулы
40
где
R - галоген;
п 1 или 2j
R - водород или метил;
Rj - водород, этил, фенил, охлорфенил, п - метилфенил, отличающийся тем, что соединение формулы
где и п имеют указанные значения,
подвергают взаимодействию с эквимолярным количеством соединения общей
формулы NH j-NH-R-j,
где R: имеет указанные значения.
712995108
или его солью в родно-этанольном буферной смеси используют уксусную растворе в присутствии кислой буфер- кислоту и ацетат натрия с рН 5-6 и ной смеси,водно-этанольный раствор берут в
2о Способ по П.1, отличаю- объемном соотношении С, : Н О, щ и и с я тем, что в качестве кислой 5 равном 5:1.
Таблица 1
E.tenelia 25
(% контроля) 12,5
6,25
E.acervulina 3,125
25
(ооцисты) 12,5
6,25
3,125
СоединениеСоединение В 2
E.tenelia 25 Полный100
(% контроля) 12,5- Не активно100
6,25
E.acervulina 25 (ооцист) 12,5
6,25
Таблица 2
100
100
100
100
А
А
А
М
100
ПолныйА
Не активно А
Р
Таблица 3 .
1
t
It
II
(известный)
Пример I 6-Cf, 7-Вг
ОНН
II р и м. е р 2 6-Ct,
7-Вг2
ОСН С,Н,
Соединение 7 6-СГ I ОН Н
8 .
6-Ct I -ОСН Я
100
0/40
204- 205
205- 206
190- dec
106- 108
13129951014
Продолжение -табл.А



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных нафтиламина | 1983 |
|
SU1346041A3 |
| ВАКЦИНА ПРОТИВ Eimeria С УЛУЧШЕННОЙ ЭФФЕКТИВНОСТЬЮ | 2017 |
|
RU2764802C2 |
| Способ получения производных пиперидинилалкилхиназолина или их солей с фармацевтически приемлемыми кислотами | 1980 |
|
SU1041034A3 |
| ТРАНСДЕРМАЛЬНОЕ ПРИМЕНЕНИЕ ТРИАЗИНОВ ДЛЯ БОРЬБЫ С ИНФЕКЦИЯМИ КОКЦИДИЙ | 2007 |
|
RU2484825C9 |
| Способ получения гликозида | 1987 |
|
SU1590045A3 |
| ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО ДЛЯ БОРЬБЫ С ПАРАЗИТИЧЕСКИМИ ПРОСТЕЙШИМИ | 2006 |
|
RU2419287C2 |
| 5,6-ДИГИДРО-2-(ЗАМЕЩЕННЫЙ ФЕНИЛ)-1,2,4-ТРИАЗИН-3,5-(2Н,4Н)-ДИОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОКОКСИДИАЛЬНОЙ И КОКСИДИОСТАТИЧЕСКОЙ АКТИВНОСТЬЮ | 1987 |
|
RU2017736C1 |
| СПОСОБ ВАКЦИНАЦИИ IN OVO ПРОТИВ КОКЦИДИОЗА | 1996 |
|
RU2125890C1 |
| СПОСОБ ОЧИСТКИ, ВЫДЕЛЕНИЯ И СПОРУЛЯЦИИ ЦИСТ И ООЦИСТ | 2000 |
|
RU2260045C2 |
| ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ КОКЦИДИОЗА (ЭЙМЕРИОЗА) КУР | 2011 |
|
RU2465313C2 |
Изобретение касается -производных хиназолинона, в частности соединений обшей формулы (l): HN - СН„ СН, лой буферной смеси - СН СООН-CH COONa, рН 5-6 при соотиошении воды и этанола, равном 1:5, при кипячении с последующим выделением целевого (1) . Полученные (I) представляют собой кристаллические вещества с высокой температурой плавления. Противококко- вая активность (1) выше известных аналогичных веществ.; 1 з.п. ф-лы, 4 табл. СО ю ;о СП СМ

| Вейганд-Хильгетаг, Методы эксперимента в органической химии.- М.: Химия 1968, с.470, 481-482. |
Авторы
Даты
1987-03-23—Публикация
1983-07-14—Подача