Изобретение относится к способу получения алкоголятов металлов, яв ляющихся катализаторами и компонентами каталитических композиций, а также Сырьем для получения высокочистых и активньпс окисных материалов.
Целью изобретения является повышение выхода и качества целевых про- iiyKTOB, а также расвшрение их ассортимента .
Цель достигается введением хлорида или оксохлорида соответствующего металла в спиртовый раствор алкого-t лята натрия в виде его суспензии или раствора в диэтиловом эфире, алифатическом углеводороде или алкилгало- гениде при (-20.) - (+20)с, с последующим кипячением реакционной смеси.
Пример 1. В колбе.в атмосфере аргона растворяют 2,5 г (0,11 моль) металлического натрия в смеси 50 мл изопропилового спирта и 50 мл гексана Гспирт абсолютирзпот многочасовым кипячением над изопропи- латом алюминия с последующей отгонкой, а гексан - над металлическим натрием, а затем над цеолитом). Для доведения реакции до конца используют слабое нагревание. Синтез проводят в круглодонной колбе с мешалкой, капельной воронкой и обратным холодильником. Колбу помещают в охлажда- смесь. Через прибор пропускают ток сухого аргона. .
Суспензию 5,4 г (0,033 моль) све-. жевозогнанного хлорида железа .(HI) в 50 мл абсолютного гексана при 0°С и интенсивном перемешивании прикапывают в течение 1 ч к раствору изопро- пилата натрия. После полной гомогенизации реакционной смеси в результате образования биметаллического ал- коксохлорида натрия и железа (III)
15
Fe(ОРг-и о)амедленно возрастает п хранении препарата от 90-100 0 (в течение 1-х cyfoK) до 150°С (через год) ,
5 ИК-спектр этого соединения в об ласти колебаний OR-группы весьма б зок А1(ОРг-ИЭо)з: 2976с.; 2938 с. 2873 ср,; 2620 ел,; 1468 ср,; 1382 1332 ср,; 1165 о,с,; 1145 о.с,;
0 1128 с.пл,; 1056 ел.; 1010 с.; 956 897 ел.; 845 сл.пл,; 838 ср.; 603 о.с,; 555 ср.; 530 сл,пл,; 485 ср.; 473 ср.пл,; 433 ср,
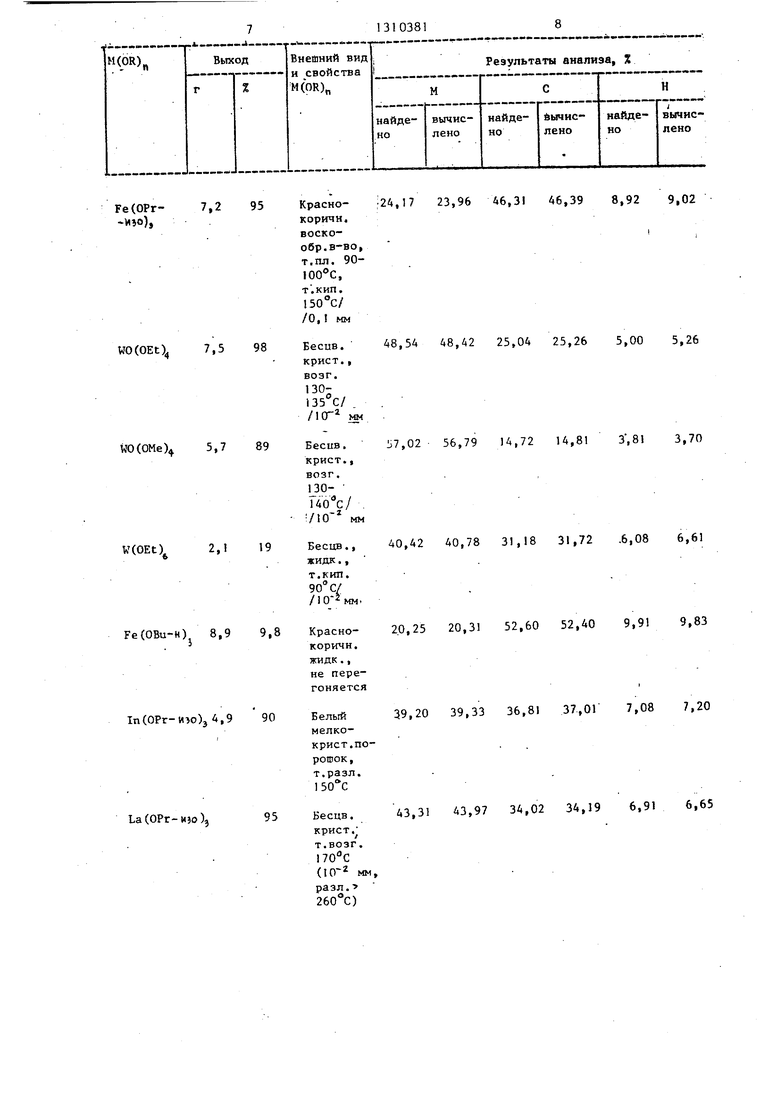
Данные анализа на Fe, С и Н пр ведены в таблице.
.Пример 2.К раствору 1,8 0,08 моль) натрия в 50 мл абс.эти лового спирта, охлажденному до -5 в течение 40 мин прикапывают из во ронки раствор 6,84 г (0,02 моль) WOC14 в 50 мл абс, диэтилового эфи ра. Затем к реакционной массе доба ляют еще 50 мл спирта (для полного растворения образовавшегося алкого лята и кипятят ее в течение 30 ми Раствор, полученный после центрифугирования NaCl, не содержит хлорид- ионов. После вакуумирования раствор теля остается кристаллический
WO(OEt), При перекристаллизации е из абс,спирта пол чают 7,5 г вещес ва (выход 98%), т,пл, (при быстром нагревании) 15-130°С, т.возг.130- 135°C/JO мм (с разл,).
35 ИК-спектрJ 2975 с.; 2935 с.;
2870 с,; 1460 ел,; 1380 ср.; 1140 ср ИЗО ср.; 1095 с,; 1070 е.; 922 с. 795 с,; 603 е,
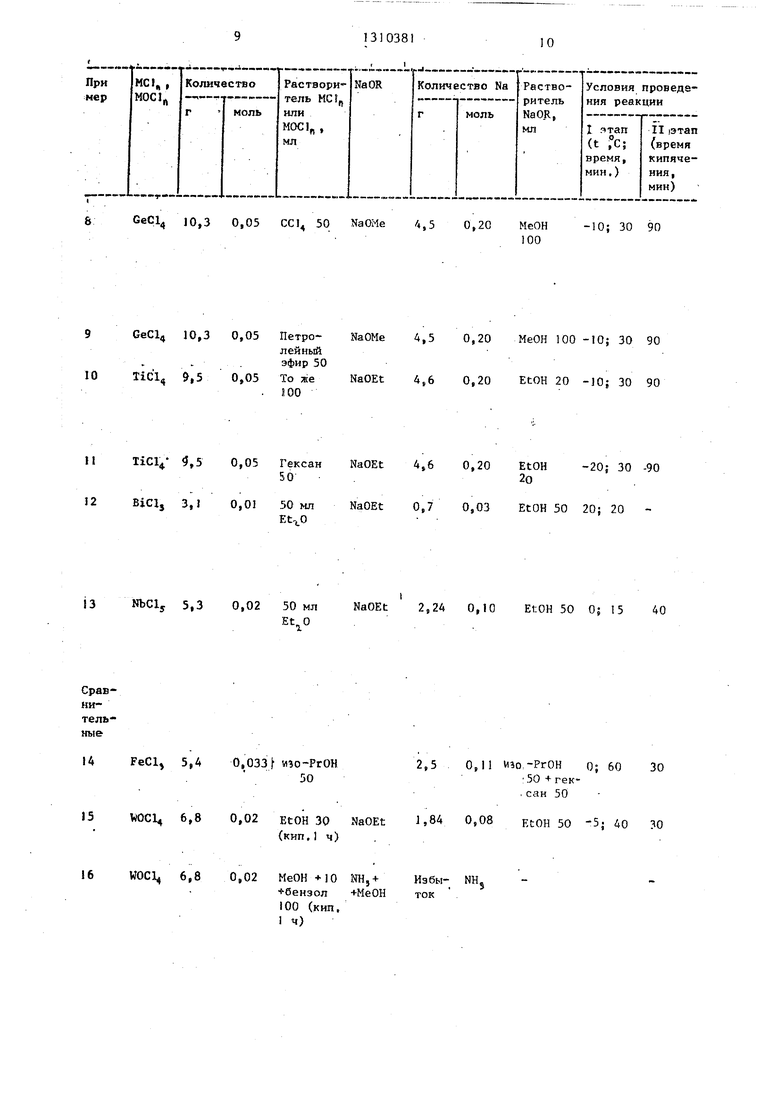
.Примеры 3-13, Синтезы сое динения (l) других производных пров дят аналогично примерам 1 и 2.
В таблице приведены количества и ходных веществ хлорида или оксохлорида, алкоголята натрия (в расчете
20
25
40
начинается выделение белого творожи- на вводимьй металлический натрий), стого осадка хлорида натрия. Реакционную смесь перемешивают еще в течение 30 мин при кипячении. Осадок NaCl отделяют центрифугированием, . Fe (ОРг- кзд ).-, частично адсорбирован- осадком, экстрагируют кипящим гексаном (3 раза по 20 мл), При ва- куумировании объединенного раствора образуется 7,2 г красно-коричневой жидкости, которая за 20-30 мин зас- тьшает, превращаясь в более светлое воекообразное вещество. Выход 95%, т,кип, 150°с(0,1 мм): т, пл.
объемы раетворителей для обоих реагентов, условия проведения реакций на стадии сливания реагентов (1 эта и дальнейшего взаимодействия в раст
50 воре (II этап) , а также свойства ц левого продукта и результаты его ор ганического микроорганизма.
Примеры 14-22 (сравнитель ные) .
55 Для сравнения приведены синтезы соединения (I) в условиях прототипа Использование спиртовых растворов хлоридов или оксохлоридов сопровож
Fe(ОРг-и о)амедленно возрастает при хранении препарата от 90-100 0 (в течение 1-х cyfoK) до 150°С (через год) ,
ИК-спектр этого соединения в области колебаний OR-группы весьма близок А1(ОРг-ИЭо)з: 2976с.; 2938 с.; 2873 ср,; 2620 ел,; 1468 ср,; 1382с,; 1332 ср,; 1165 о,с,; 1145 о.с,;
1128 с.пл,; 1056 ел.; 1010 с.; 956 с.; 897 ел.; 845 сл.пл,; 838 ср.; 603 о.с,; 555 ср.; 530 сл,пл,; 485 ср.; 473 ср.пл,; 433 ср,
Данные анализа на Fe, С и Н приведены в таблице.
.Пример 2.К раствору 1,8 г 0,08 моль) натрия в 50 мл абс.этилового спирта, охлажденному до -5 С в течение 40 мин прикапывают из воронки раствор 6,84 г (0,02 моль) WOC14 в 50 мл абс, диэтилового эфира. Затем к реакционной массе добавляют еще 50 мл спирта (для полного растворения образовавшегося алкого- лята и кипятят ее в течение 30 мин. Раствор, полученный после центрифугирования NaCl, не содержит хлорид- ионов. После вакуумирования растворителя остается кристаллический
WO(OEt), При перекристаллизации его из абс,спирта пол чают 7,5 г вещества (выход 98%), т,пл, (при быстром нагревании) 15-130°С, т.возг.130- 135°C/JO мм (с разл,).
ИК-спектрJ 2975 с.; 2935 с.;
2870 с,; 1460 ел,; 1380 ср.; 1140 ср.; ИЗО ср.; 1095 с,; 1070 е.; 922 с.; 795 с,; 603 е,
.Примеры 3-13, Синтезы соединения (l) других производных проводят аналогично примерам 1 и 2.
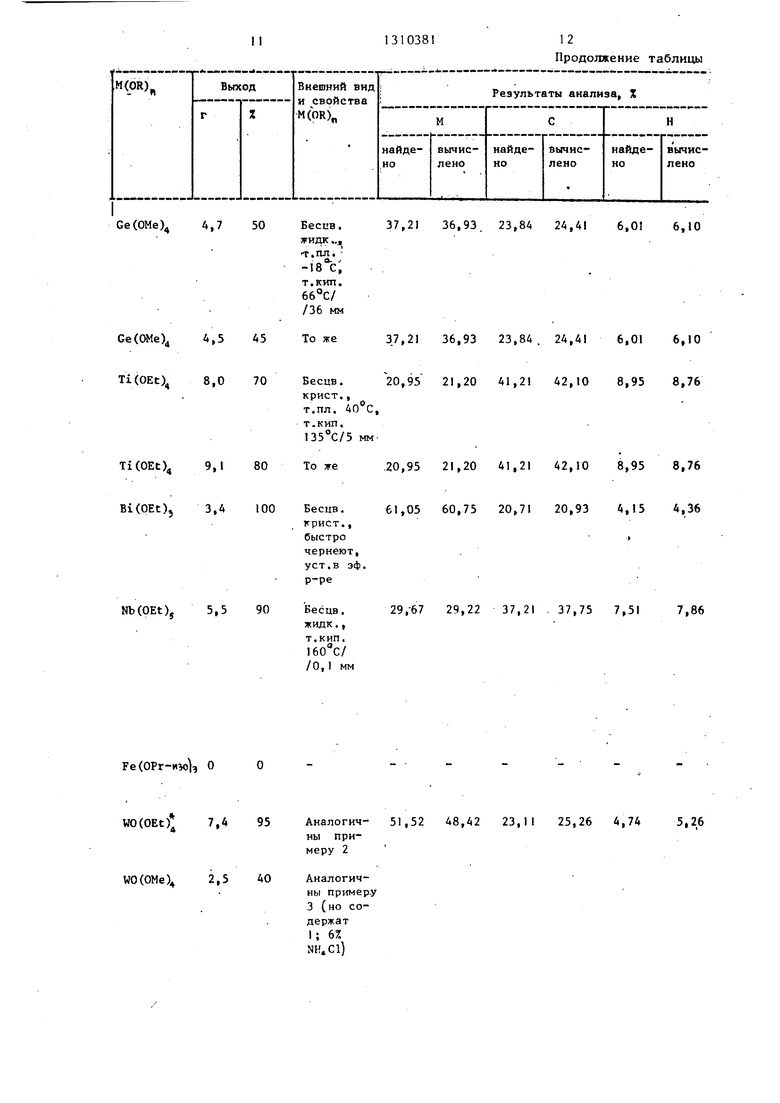
В таблице приведены количества исходных веществ хлорида или оксохлорида, алкоголята натрия (в расчете
на вводимьй металлический натрий),
на вводимьй металлический натрий),
объемы раетворителей для обоих реагентов, условия проведения реакций на стадии сливания реагентов (1 этап) и дальнейшего взаимодействия в раст50 воре (II этап) , а также свойства целевого продукта и результаты его органического микроорганизма.
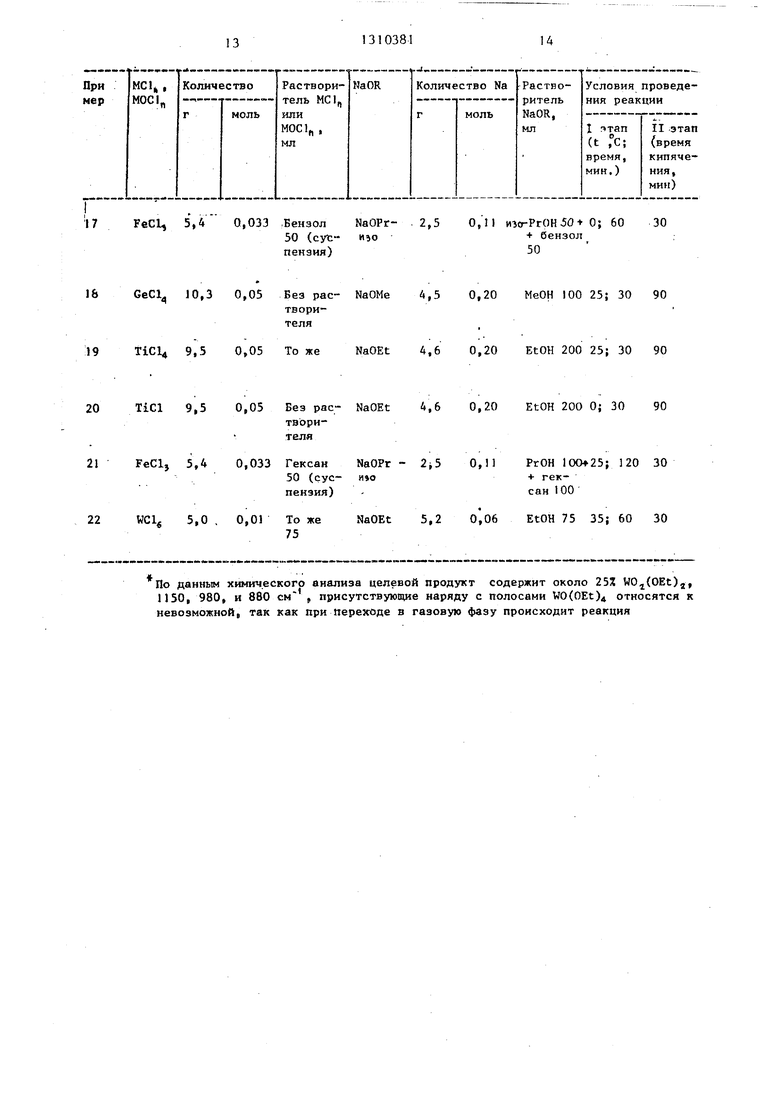
Примеры 14-22 (сравнительные) .
55 Для сравнения приведены синтезы соединения (I) в условиях прототипа. Использование спиртовых растворов хлоридов или оксохлоридов сопровож31
дается снижением выхода соединения I, особенно в случае предварительного кипячения растворов (до введения их в реакцию) в отсутствие инертных разбавителей. При отсутствии возможности очистки соединения (I) оказываются загрязненными продуктами гидролиза (примеры 14-16). К тем же результатам приводит использование бензола в качестве растворителя (пример 17) или повышение температ уры . первого этапа синтеза выше 20 С - вследствие образования в реакционной смеси воды (примеры 18 и 19), а также продуктов восстановления хлорида и алкоголята (пример 21) и , растворимого в спирте- значительно более, чем NaCl (примеры 16). При проведении синтезов соединений (I) при температурах ниже -20 С резко снижается растворимость NaOR ( а иногда и обоих компонентов) и вследствие этого скорость обменной реакции (пример 22).
Формула изобре тени
1. Способ получения алкоголя- тов металлов формулы I или II
14
M(OR) (1) или MO(OR)n (II), где М - атом металла, выбранного из группы: индий, лантан, германий, титан, висмут (III), ниобий,
вольфрам (VI) или железо (III), R - С ;|-С 4 - алкил нормального или изо- строения, п - целое число от 3 до 6, включающий введение хпорида или оксохлорида соответствующего металла в спиртовый раствор, соответствующего алкоголята натрия при охлажде НИИ, кипячение полученной реакционной смеси, отделение осадка хлористого натрия и отгонку растворителя, о тличающийся тем, что, с целью повьшения выхода и качества целевых продуктов, а также расширения их ассортимента, введение хлорида или оксохлорида металла осуществляют в виде его суспензии или раствора в диэтиловом эфире, алифатическом углеводороде или алкилгалоге- ниде при (-20) -() С.
2. Способ ПОП.1, о тличаю- щ и и с я тем, что в спиртовый ра- створ алкоголята натрия вводят алифатический углеводород.
FeClj 5,4 0,033 Гексан NaOPr50 (eye- - лъо пензия)
2 WOCL 6,8 0,02 То же NaOEt 1,8 0,08 EtOH
5050
«ОСЬ 6,8 0,02 Тоже NaOMe 1,8 0,08 МеОН 0;40 30 50.50
4WCL 10,0 0,025 Et...O
150
5 FeCl 5,4 0,033 EtjO
50
4,2 0,02
EtjO 100 (суспензия)
LaClj 4,9 0,02 Гептан NeOPr-«o1,
50 (суспензия)
0,11
изо- РтОН 50 + гек- сан 50
0; 6П 30
-5; АО мл EtOH)
NaOEt 3,5 0,15 EtOH--10; 90 30
150
NaOBu-H 2,5 0,11 j-BuOH 5; 30 30
70
NaOPr-nv)l,3 0,06 Mio-PrOH 50+ 0;15 30
50
0,06 «o-PrOH30+ 10; 30 40 f гептан 20
7,2
95
KpacHO- коричн,
BOCKOo6p.B-BO, Т.ПЛ. 90- , т .кип. 150°C/ /0,1 MM
7,5
98
Бесив.
крист.,
воэг.
130i35 c/
/(Г
мм
5,7
89
Бесив, крист., возг.
130-
, /10 мм
2,1
19
Бесцв., жидк., т.кип. 90 с/ ,
8,9
9,8
Красно- коричн. жидк., не перегоняется
)з 4,9
Mjo),
90
95
Белый мелко- крист.порошок , т.разл. 1 50 С
Бесцв. крист. т.возг. 170 С
(10-г разл. 260°С)
24,17 23,96 46,31 46,39 8,92 9,02
48,54 48,42 25,04 25,26 5,00 5,26
;7,02 56,79 14,72 14,81 3,81 3,70
40,42 40,78 31,18 31,72 .6,08 6,61
20,25 20,31 52,60 52,40 9,9 9,83
39,20 39,33 36,81 37,01 7,08
7,20
43,31 43,97 34,02 34,19 6,91 6,65
8СеСЦ 10,3 0,05 CCl 50 NaOMe 4,5 0,20
9GeCl, 10,3 0,05 Петро- NaOMe 4,5 0,20 МеОН 100 -10; 30 90
лейный
эфир 50
10liC l, 9,5 0,05 ТожеNaOEt 4,6 0,20 EtOH 20 -10; 30 90
.100
11liCl 9,5 0,05 ГексанNaOEt4,6 0,20 EtOH -20j 30 -90
50. 2o
12BiClj 3,J 0,01 50млNaOEt0,7 0,03 EtOH 50 20; 20
i3 NbCly 5,3 0,02 30мл NaOEt 2,2A 0,10 EtOH 50 0; 15 40
СравНИтельяые
14 FeCl. 5,A
0,033 иго-РгОН 50
15 ШСЦ 6,8 0,02 EtOH 30 NaOEt
(кип ,1ч)
WOCl 6,8
0,02 МеОН 0 NH, «бензол «-МеОН 100 (кип. 1 ч)
МсОН 100
-10; 30 90
2,5 0,11 .-РгОН 0; 60 30 ;50- -гек- . сан 30
1,84 0,08 KtOH 30 -5j 40 30
Избы- NHj ток
Ge(OMe)4,7 50
Бескв. жидк „л т.пл.; -18 С, т.кип.
37,21 36,93. 23,84 24,41 6,0 6,10
/36 мм Ge(,5 45Тоже3.7,21 36,93 23,84. 24,41 6,01 6,10
8,0 70
Бесцв. крист,, т,пл. 40 с, т.кип. 133°С/5 мм
Ti(OEt),9,1 80То же20,95 21,20 41,21 42,10 8,95 8,76
3,4 100
5,5
90
Бесцв. крист., быстро чернеют, уст.в эф. р-ре
Бесцв. жидк., т.кип, 160 С/ /О,1 мм
Fe(OPr-Hio), О О
7,4 95
2,5 40
Аналогич- 51,52 48,42 23,11 ны примеру 2
Аналогичны примеру 3 (но содержатI; 6% NK,Cl)
37,21 36,93. 23,84 24,41 6,0 6,10
20,95 21,20 41,2 42,10 8,93 8,76
61,05 60,75 20,71 20,93 4,15 4,36
29,-67 29,22 37,21 . 37,75 7,51 7,86
25,26 4,74 5,26
17FeCL, 5,4 0,033 ,Бензол NaOPr- .2,5 0, l 1 иэо-РгОН О 0; 60 30
50 (eye- И50- бензол
пензия)50
18GeCl 0,3 0,05 Без рас- NaOMe
твори- теля
19TiCl4 9,5 0,05 То жеNaOEt 4,6 0,20 EtOH 200 25; 30 90
20TiCl 9,5 0,05 Без рас- NaOEt 4,6 0,20 EtOH 200 0; 30 90
твори- теля
21FeClj 5,4 0,033 Гексан NaOPr - 0,11 PrOH 10О+25; 120 30
50 (eye- гекпенэия) -сан 100
22WCl 5,0, 0,01 ТожеNaOEt 5,2 0,06 EtOH 75 35; 60 30
75
По данным химического анализа целевой продукт содержит около 25% WOj(OEt)j, 1150, 980, и 880 см , присутствующие наряду с полосами WO(OEt)4 относятся к невозможной, так как при переходе в газовую фазу происходит реакция
4,5 0,20 МеОН 100 25; 30 90
что подтверждают и данные ИК-спектроскопии: полосы поглощения WOjCOEt). Очистка целевого продукта путем возгонки оказьтается диспропорционировання: WO(OR)(OR)g WOj(OR)j.
46,39 8,45
9,02



| название | год | авторы | номер документа |
|---|---|---|---|
| Биметаллические алкоголяты иттрия и циркония и способ их получения | 1980 |
|
SU902428A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,5-ДИАРИЛ-3-ЗАМЕЩЕННЫХ ПИРАЗОЛОВ | 2000 |
|
RU2243967C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ МЕТИЛАТОВ РЕНИЯ | 2011 |
|
RU2481418C1 |
| СПОСОБ ПОЛУЧЕНИЯ МНОГОСЛОЙНОГО ПОКРЫТИЯ | 2013 |
|
RU2534258C1 |
| Способ получения оксоалкоксопроизводных вольфрама (у1) | 1985 |
|
SU1306927A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТВЕРДОГО КОМПОНЕНТА КАТАЛИЗАТОРА (СО)ПОЛИМЕРИЗАЦИИ ЭТИЛЕНА, ТВЕРДЫЙ КОМПОНЕНТ КАТАЛИЗАТОРА (СО)ПОЛИМЕРИЗАЦИИ ЭТИЛЕНА, КАТАЛИЗАТОР (СО)ПОЛИМЕРИЗАЦИИ ЭТИЛЕНА И СПОСОБ ПОЛУЧЕНИЯ (СО)ПОЛИМЕРОВ ЭТИЛЕНА | 1992 |
|
RU2081884C1 |
| СПОСОБ ПОЛУЧЕНИЯ МНОГОСЛОЙНОГО ПОКРЫТИЯ НА ОСНОВЕ SiO-ZrO-PO-CaO | 2012 |
|
RU2497680C1 |
| СОЛИ 9-ЗАМЕЩЕННЫХ 2-ГАЛОГЕНФЕНИЛИМИДАЗО [1,2-a]БЕНЗИМИДАЗОЛОВ И ГАЛОГЕНИДЫ 1-ЗАМЕЩЕННЫХ 3-ГАЛОГЕНФЕНАЦИЛ-2-АМИНОБЕНЗИМИДАЗОЛИЯ, ОБЛАДАЮЩИЕ ГЕМОРЕОЛОГИЧЕСКИМИ СВОЙСТВАМИ | 2005 |
|
RU2290404C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛПИРИМИДИН-4,6-(3Н,5Н)-ДИОНА | 2012 |
|
RU2503665C1 |
| Способ получения производных пиразоло[3,4- @ ]хинолина или пиридо [2,3- @ ]хиназолина или их солей | 1987 |
|
SU1644718A3 |
Изобретение касается производных спиртов, в частности алкоголя- тов метсшлов общей формулы lMe(OR)n, где Me- атом металла: индий, лантан, германий, титан, висмут (III), ниобий, вольфрам (YI), железо (III); R - С,-С4-алкил нормального или изо- строения, п - целое число 3-6, кото- рые как катализаторы могут быть использованы в различных каталитических процессах. Повышение качества и выхода 1, расиирение ассортимента получаемых веществ достигается использованием другого растворителя для исходной соли металла. Процесс ведут в абсолютной среде из хлорида или оксохлорида в среде дизтилового эфира алифатического углеводорода или алкилгалогенида и спиртового раствора алкоголята натрия при (-20) - )(+20) с с последующим кипячением, отделением NaCl и отгонкой растворителя. Целесообразно в исходный спиртовый раствор добавлять алифатический углеводород, например гек- сан. Выход 1 70-100% против 0% (только в изопропаноле) или 76% (только в этаноле). В случае предварительного кипячения растворов до реакции в отсутствие инертных разбавителей снижается выход 1. 1 з.п,ф-лы, I табл. СЛ

| Bisehoff F, Adkins Н | |||
| Алкилти- танаты | |||
| I | |||
| Am, Chem | |||
| See | |||
| Устройство для приведения в действие электрического выключателя при отпирании дверного замка | 1925 |
|
SU1924A1 |
| I - . | |||
Авторы
Даты
1987-05-15—Публикация
1984-10-02—Подача