Изобретение относится к способу получения трициклических аналогов эрголина, применяемых в качестве ага- нистов дофамина
Цель изобретения - получение новых производных пиразоло 3,4-8 хино- лина или пиридоЈ2,3- 1хиназолина или их солей, превосходящих по своей биологической активности известные три- циклические аналоги эрголина.
Пример 1. 7-(5-Пропил-транс- 4,4а,5,6,8а,9-гексагидро-2Н пиразоло Ј3,4-§ |-хинолин)метанол
10
1,2 г (6,7 ммоль) гуанидинкарбоната в 75 мл этанола. Смесь кипятят с обратным холодильником в течение Зч, оставляют стоять на ночь при комнатной температуре, а затем выпивают в воду. Продукт экстрагируют из водной смеси СНС13/изо-РгОН(3:1). Органический растворитель отгоняют, получают коричневый полутвердый продукт, который оставляют на ночь в вакуумном эксикаторе. Масса полученного продукта составляет 1,9 г. Его пропускают через колонку с силикагеРаствор 1,8 г (15,7 ммоль) трет- 15 леи, используя 10% МеОН/СНг1г, со- бутилата калия в 20 мл ТГФ охлаждаютдержащий следы . Фракции, для
до 0°С0 К нему добавляют раствор 1,3 г (5,8 ммоль) аЗ-гидроксиметил-1которых ТСХ показывает наличие продукта, комбинируют с получением 0,5 г пропил-транс-1,2,4а,5,6,7,8а-октагид- желтого твердого вещества. Его отби- рохинолин-6-она, 1,7 г (23,3 ммоль) 20 Рают в смесь метанола и метиленхло- этилформиата и 40 мл ТГФ. СмесьРида. Раствор упаривают и добавляют
прогревают до комнатной температуры и перемешивают 3 ч, после чего добавляют 4 мл гидразина и концентрацию ионов водорода доводят до рН 9-10. 25 рают фильтрованием, сушат в вакуум- Смесь перемешивают в течение ночи при ном эксикаторе. Получают 0,4 г целе- комнатной температуре и затем выливают в воду. Продукт экстрагируют в раствор СНС13 /изо-РгОН (3:1), который затем упаривают с получением 1,3гзо коричневой камеди. Ее очищают на колонке с силикагелем, используя 10% МеОН/СН2С12, содержащий следы , что дает 400 мг материала, который растворяют в CHClj. Из раствора крис- 35 1030 см таллизуется твердое вещество и дляП р и м е р 3„ 8-МетОксиметил-6улучшения кристаллизации продукта, до- пропил-транс-5,5а,6,7,9а, 10-гексагид- бавляют гексан. После фильтрованияропиридо 2,3-з хиназолин-2-амик0
получают 390 мг кристаллов, идентифи-Целевой продукт получают с испольцированных как трихлорметановый ком- 40 зованием методики примера 2 из 3-ме- плекс целевого соединения, т.пл. 112- токсиметил-1-пропил-транс-1,2,4а,5,6,
7,8,8а-октагидрохинолин-6-она в качестве исходного материала.
Вычислено, %: С 66,64; Н 8,39; 45 N 19,43.
Найдено, %: С 66,76; Н 8,20; N 19,52.
Масс-спектр: 287, 259, 243, 198, 166, 136.
этилацетат до тех пор, пока не начнется образование кристаллов. Раствор охлаждают и твердое вещество собивого продукта.
Вычислено, %: С 65,67; Н 8,07; N 20,42,
Найдено, %: С 65,44; Н 7,80; N 20,29.
Масс-спектр: 287, 273, 245, 198, 166, 152, 122. ИК-спектр (КВг): 3380, 3316, 3192, 1642, 1593, 1562, 1476,
™
115°С,
Вычислено, %: С 49,08; Н 6,05; N 11,51; С1 29,00,
Найдено, %: С 49,46; Н 5,67; .N 11,53; С1 28,83.
Масс-спектр: 246,218,152,118.
Пример 2„ 8-(2-Амино-6-пропил- транс-5,5а,6,7,9а,10-гексагидропиридо
2, 3 хиназолин) метанол.JQ
К раствору 1,5 г (6,7 ммоль) 3-гид-пропил-4,4а,5,6,8а,9-транс-гексароксиметил-1-пропил-транс-1,2,4а,5,6,гидро-2Н-пира золо 3,4-g хинолин.
7,8,3а-октагидрохинолин-6-она в 100 мл
толуола добавляют 4,5 мл (16,9 ммоль)
трис(диметиламино)метана„ Смесь кипя- 556,7,8,8а-октагидрохинолин-6-она в
тят 1 ч с обратным холодильником.50 мл толуола добавляют 1,3 г
Толуол отгоняют и получают корич-(9,0 ммоль) трис(диметиламино)метана
невое масло. К раствору этого масла и греют с обратным холодильником в тев 75 мл этанола добавляют суспензиючение 2 ч, затем толуол отгоняют, осПример4„ 4-Метоксиметил-5К раствору 850 мг (3,6 ммоль) 3-ме- токсиметил-1-пропил-транс-1,2,4а,5,
1,2 г (6,7 ммоль) гуанидинкарбоната в 75 мл этанола. Смесь кипятят с обратным холодильником в течение Зч, оставляют стоять на ночь при комнатной температуре, а затем выпивают в воду. Продукт экстрагируют из водной смеси СНС13/изо-РгОН(3:1). Органический растворитель отгоняют, получают коричневый полутвердый продукт, который оставляют на ночь в вакуумном эксикаторе. Масса полученного продукта составляет 1,9 г. Его пропускают через колонку с силикагерают фильтрованием, сушат в вакуум- ном эксикаторе. Получают 0,4 г целе- 1030 см П р и м е р 3„ 8-МетОксиметил-6этилацетат до тех пор, пока не начнется образование кристаллов. Раствор охлаждают и твердое вещество соби рают фильтрованием, сушат в вакуум- ном эксикаторе. Получают 0,4 г целе- 1030 см П р и м е р 3„ 8-МетОксиметил-6вого продукта.
Вычислено, %: С 65,67; Н 8,07; N 20,42,
Найдено, %: С 65,44; Н 7,80; N 20,29.
Масс-спектр: 287, 273, 245, 198, 166, 152, 122. ИК-спектр (КВг): 3380 3316, 3192, 1642, 1593, 1562, 1476,
™
Пример4„ 4-Метоксиметил-5гидро-2Н-пира золо 3,4-g хинолин.
К раствору 850 мг (3,6 ммоль) 3-ме- токсиметил-1-пропил-транс-1,2,4а,5,
516
таток отбирают в 50 мл этанола, добавляют 2 ип гидразина и смесь перемешивают в течение ночи при комнатной температуре. Затем смесь выливают в воду и продукт экстрагируют метилен- хлоридом. Экстракт сушат сульфатом натрия и упаривают с получением 950 мг светло-коричневого масла. Его пропускают через колонку с сшшкагелем, ис- пользуя 5% MeOH/CH/ Clg f содержащий следы . Фракции, для которых ТСХ указывает на присутствие целевого соединения, комбинируют с получением желтого масла, которое кристаллизует- ся при стоянии. Его рекристаллизуют из EtOAc/гексана с получением 550 мг целевого соединения.
Вычислено, %: С 68,93; Н 8,87; N 16,08.
Найдено, %: С 68,99; Н 8,64; N 16,11.
Масс-спектр: 260, 232, 216, 166, 136.
П р и м е р 5. 7-Метилтиометил-5- пропил-транс-4,4а,5,6,8а,9-гексагид- ро-2Н-пиразолр,4- хинолин.
Целевое соединение получают по методике примера 1 из 3-метилтиометил-1 пропил-транс-1,2,4а,5,6,7,8,8а-окта- гидрохинолин-6-она в качестве исходного материала. Т.пл. 133-134°С.
Вычислено, %: С 64,94; Н 8,36; N 15,15; S 11,56.
Найдено, %: С 65,26; Н 8,26;
N 14,91; S 11,30.
Масс-спектр: 276, 248, 230. 182, 136, 94. ИК-спектр (СНС13): 3466, 3240, 2964, 1375, 1136. Протонный ЯМР-спектр (CDClj) 270 МГц: 7,34 (с, 1Н), 5,46 (с, 1Н), 2,02 (с, ЗН), 0,93 (т, ЗН),
П р и м е р 6. 7-Метилсульфинилме- тил-5-пропил-транс-4,4а,5,6,8а,9-гек- сагидро-2Н-пиразол ГЗ, 4-рЛ хинолин.
К раствору 480 мг (1,7 ммоль) 7- (метилтиометил)-5-пропил-транс-4,4а, 5,6,8а,9-гексагидро-2Н-пиразол 3,4-gl хинолина (пример 5) в 50 мл метанола добавляют раствор 740 мг (3,5 ммоль) метапериодата натрия в 20 мл воды. Смесь перемегаивают в течение 1 ч при комнатной температуре, а затем выливают в воду. Концентрацию ионов водорода доводят до рН 11, после чего продукт экстрагируют СНС1 /изо-РгОН (3:1). Растворитель упаривают с получением 0,47 г продукта, который пропускают через колонку с силикагелем,
186
используя 7-10% МеОН/СН2С12, содержащего следы NHjOH. Фракции, для которых ТСХ указывает на присутствие целевого соединения, комбинируют с получением 230 мг пени. Протонный ЯМР- спектр (CDC13) 270 МГц: 7,34 (с, 1Н); 5,72 (с, 1Н); 2,62 (с, ЗН); 0,93 (т, ЗН). Масс-спектр: 292, 261, 247, 230, 218, 200, 170, 152, 136.
Пример 7. 8-Метилтиометил-6- пропил-транс-5,5а,6,7,9а,10-гексагид- ропиридо 2,3-pfJ хиназолин-2-амин.
Целевое соединение получают по методике примера 2, используя соединение примера 5 в качестве исходного материала. Масс-спектр: 303,275,257, 227,313,198,182. ИК-спектр (СНСЦО : 3422, 2936, 1607, 1562, 1457. Протонный ЯМР-спектр (СПС13) 270 МГц: 8,08 (с, Ш), 5,48 (с, III), 4,89 (с, 2Н), 2,01 (с, ЗН), 0,94 (т, ЗН).
Соль малеиновой кислоты получают из 400 мг порции целевого соединения. Соль рекристаллизуют из МеОН/ /EtOAc, получая 270 мг продукта, который затем растворяют в теплом МеОН. Добавляют активированный уголь и смесь фильтруют в горячем состоянии о Остаток рекристаллизуют с получением 90 мг малеата целевого соединения в виде желтых кристаллов, Т.пл. 208°С.
Вычислено, %: С 57,12; Н 6,71; 13,32.
Найдено, %: С 57,35; Н 6,84; N 13,32.
П р ч м е р 8. 8-Метилсульфинилме- тил-6-пропил-транс-5,5а,6,7,9а,10-гек сагидропиридо 2,3-j jхиназолин-2-амин.
Целевое соединение получают по методике примера 6, используя соединени примера 7 в качестве исходного материала. Протонный ЯМР-спектр (ДМСО-с1б) 270 МГц: 8,02 (с, 1Н), 5,64 (с, 1Н), 2,32 (с, ЗН), 0,87 (т, ЗН)„ Масс- спектр: 273, 256, 245, 227, 152, 136.
П р и м е р 9. рац-(4а/3, 3/5, 8аб6)- 5-Пропил-4,4а,5,6,7,8,8а,9-октагидро- 2Н-пира зол рЗ, 4 хинолин-8-ол.
Готовят раствор 1,4 (12,8 ммоль) трет-бутилата калия в 20 мл тетрагид- рофурана и до О С. К раствору добавляют 1,0 г (4,7 ммоль) рац- (4 р, 4aoi, ) -4 -гидрокси-1 -пропил-де- кагидрохинолин-6-она, 1,4 г|
(19,0 ммоль) этилформиата и 20 мл тет- рагидрофурана. Смесь перемешивают 1 ч при комнатной температуре с образованием суспензии. Затем добавляют 3 мл
гидразина, концентрацию ионов водорода доводят до рН 9, и смесь перемешивают еще 2 ч„ Затем смесь выпивают на лед, продукт экстрагируют метиленхло- ридом, сушат сульфатом натрия и упаривают с получением 400 мг продукта. Оставшуюся в водном слое часть продукта экстрагируют СНС1 /изо-РгОН (3:1), сумат сульфатом натрия, после упаривания получают еще 680 мг продукта. Скомбинированные порции пропускают через колонку с силикагелем, используя 20% MeOH/CH Cl, содержащий (следы . Фракции, для которых ТСХ указывает на присутствие продукта, комбинируют с получением 850 мг. Свободное основание екристаллизуют из MeOH/EtOAc, получая 270 мг целевого продукта в виде белого порошка. Т.пл. ,153-154°С. Масс-спектр: 235, 219, 206, 159, 119, 107. УФ-спектр (EtOH): fltfQKo 222 нм. Протонный ЯМР-спектр (СВСЦ) 270 МГЦ: 7,34 (с, 1Н), 4,34 (д, 1Н), 0,88 (т, ЗН). ИК-спектр
(СНСЦ): 3450, 3225, 2947, 2875, 1078.
Пример 10. рац(4аЈ,8(/,8а«0- 5-Пропил-4,4а,,7,8,8а,9-октагндро- 2Н пиразол 3,4--}Лхинолин-8-ол„
Целевой продукт получают по методике примера 9, используя рац(4о(,4ай, 8а6)-4-гидрокси-1-пропилдекагидрохи- нолин-6-он. ИК-спектр (CHClj): 3570, 3234, 1084 . Протонный ЯМР-спектр (CDCLj) 270 МГц: 7,28 (д, 1Н), 0,89 (т, ЗН). Масс-спектр: 235, 206, 140, 124 о
Пример 11, Метансульфонат рац(4а|5, 8ft, 8аОО-2-амино-6-пропил- 5,5а,6,7,8,9а,10-октагидропиридо Ј2,З-gJ хиназолин-9-ола (1:2)„
К раствору 1,1 г (5,2 ммоль) рац- (4{J, 4ao(, 8а(Ь)-4-гидрокси-1-пропил- декагидрохинолин 6-она в 60 мл толуо- ла добавляют t,9 г (13,0 ммоль) трис- (диметиламино)метана. Смесь кипятят с обратным холодильником в течение 1 ч, а затем упаривают до коричневого остатка и добавляют 50 мл этанола Полученную смесь добавляют к суспензии 0,95 г (5,2 ммоль) гуанидинкарбо- ната в 50 мл этанола. Смесь кипятят с обратным холодильником в течение 4 ч, затем охлаждают и выливают в воду. Продукт экстрагируют СНС1з/ /изо-РгОН (3:1), сугаат сульфатом натрия, упаривают и получают 1,3 г темно-желтой камеди. Ее пропускают
через колонку с силикагелем, используя 10% МеОН/СН2С1г, содержащей следы . Фракции, для которых ТСХ указывает на присутствие целевого материала, комбинируют с получением 0,63 г желтого твердого вещества Соль получают добавлением ме- тансульфокислоты и рекристаллизацией из MeOH/EtOAc с получением 450 мг целевого продукта в виде желтого порошка, Т.пл. 238-239°Со ИК-спектр (КВг): 3304, 3165, 2954, 1661, 1602, 1569, 1496 . Масс-спектр: 261, 244, 234, 215, 153.
Пример 12. Дигидрохлорид рац(4а{3, 8, 8аоО-2-амино-6-пропил--5, 5а,6,7,8,9а, 10-октагидропиридо 2,З-pf хиназолин-9-ола.
Свободное основание целевого соединения получают по методике примера 11, используя соединение, полученное по примеру 10, в качестве исходного материала. Масс- спектр: 262, 244, 215, 153. ИК-спектр (КВг): 3380, 3320, 3166, 2980, 1653, 1599, 1565, 1487 . Протонный ЯМР-спектр (СПСЦ, ДМСО-е) 270 МГц: 8,00 (с, 1Н), 0,90 (т. ЗН). УФ-спектр (EtOH) :ftMClKC 229. Затем получают гидрохлоридную соль, т.пл. 29б-298°С.
Вычислено, %: С 50,15; Н 7,22; N 16,71; С1 21,15.
Найдено, %: С 50,36; Н 7,45; N 16,76; С1 21,15.
Пример 13. рац-(4а|$, 8tf, 8aoЈ)- 8-(Диметиламиносульфониламино)-5- пропил-4,4а,5,6,7,8,8а,9-октагидро- 2Н-пиразол 3,4 й хинолина этанолат.
К раствору 1,0 г (3,1 ммоль) рац- (4о(,4аоЈ, 8а6)-4-(диметиламиносульфо- ниламино)-1-пропил-транс-декагидро- хинолин-6-она в 100 мл толуола добавляют 1,1 г (7,9 ммоль) трис(диметил- амино)метанав Смесь кипятят с обратным холодильником в течение 45 мин, затем удаляют толуол и остаток отби- рают в 100 мл этанола. К нему добавляют 3 мл гидразина, смесь перемешивают в течение ночи при комнатной температуре, а затем выливают в .воду. Продукт экстрагируют метиленхлоридом, сушат сульфатом натрия, упаривают и получают t,1 г вещества. Его пропускают через колонку с скликагелем, используя 7-10% МеОН/СН2Г,12, содержащий следы . Фракции, для которых ТСХ указывает на то, что они являются продуктом, комбинируют с получением желтой пены. Масс-спектр: га/е 341. Ув -спектр: мчкс 219, Ј 6278,3
После перекристаллизации из EtOH/ /Et.O получают 360 мг целевого соль- ват. Т.пл. 154-156°С.
Вычислено, %: С 52,69; Н 8,58; N 18,07.
Найдено, %: С 52,44; Н 7,28; N 18,02.
Пример 14. рац-(5а, 8(Х, 8аоО 9-(Диметиламиносульфониламино)-6-про- пил-транс-5,5а,6,7,9,9а,10-октагидро- пиридор,3- 1хиназолин-2-амин,
К раствору 1,1 г (3,5 ммоль) рац- (4(Х,4ао(, 8р()-4-(диметиламиносульфонил амино)-1-пропилдекагидрохинолин-6-она в 100 мл толуола добавляют 1,3 г (8,7 ммоль) трис(диметиламино)-метана и кипятят с обратным холодильником 45 мин, Толуол удаляют и остаток отбирают в 100 мл этанола. К нему добавляют 250 мл (4,2 ммоль) гуанидина ,и смесь перемешивают в течение ночи |при комнатной температуре. Затем до- бавляют еще 240 мг (4,2 ммоль) гуанидина и смесь нагревают при 50°С в течение 2 ч, после чего ее выливают в воду. Экстрагируют CHCl /изо-РгОН (3:1), сушат сульфатом натрия, упари- вают и получают 1,2 г продукта. Его пропускают через колонку с сидикаге- лем, используя 5% МеОН/СН2С1г, содержащий следы . Объединенные фракции, для которых ТСХ указывает на при сутствие продукта, упаривают с получением 0,9 г вещества, из которого после перекристаллизации из EtOH/EgO получают 380 мг этанолсольвата целевого соединения. УФ-спектр (EtOH): A/waicc 29 6 14,130. Масс-спектр: .
При нагревании при 110°С сольват разлагается и этанол отводят, остав- ляя целевое соединение.
Вычислено, %: С 52,15; Н 7,66; N 22,81.
Найдено, %: С 52,33; Н 7,57; N 22,65.
Т.пл. 201°С (разл.).
Пример 15. рац-(, 8txf, 8арС) 8-Ацетиламино-5-пропил-4,4а,5,6,7,8, 8а,9-октагидро 2Н-пиразол P3, хино- лин.
Целевое соединение получают по методике примера 9 с использованием рац-(4(Х-4а,8а|3)-4-ацетиламино-1-про- пилдекагидрохинолин-6-она в качестве
исходного материала. Т.пл. 190°С. Масс-спектр: .
Вычислено, %: С 46,76; Н 7,85; N 14,54.
Найдено, %: С 46,50; Н 7,12; N 14,78.
Пример 16. рац-(4ар,8а ,8а)- 5-Пропил-4,4а,5,6,7,8,8а,9-октагидро- 2Н-пиразол 3,4-р; |хинолин-8-амин.
Целевой продукт получают гидролизом соединения примера 15. Т.пл. 197- 199°С. Масс-спектр: . УФ- спектр: маке 221;g 5670. ИК-спектр (КВг): 3270, 3245, 2900, 1680 .
Пример 17. рац-(4а|Ь,3(1,8аоО-8 Лцетиламино-5-пропил-4,4а,5,6,7,8,8а, 9-октагидро-2Н-пиразоло 3,4-р,1хинолин
Целевое соединение получают по методике примера 9 при использовании рац-( , 4ао(., 8aft) -4-ацетиламино-1-про- пилдекагидрохннолин- б-она в качестве исходного материала. Затем образуют дигидрохлоридную соль и рекристалли- зуют ее из MeOH/EtOAc. Т.пл. 230°С.
Масс-спектр: . I
Вычислено, %: С 51,58; Н 7,50;
N 16,04.
Найдено, %: С 51,32; Н 7,38; N 15,81.
Пример 18. рац-(, 8|}, 8аЮ 5-Пропил-4,4а,5,6,7,8,8а,9 октагидро- 2Н-пиразолор,4- 1хинолин-8-амин.
Целевой продукт получают кислотным гидролизом соединения примера 17. Затем образуют тригидрохлоридную соль и ее рекристаллизуют из MeOH/EtOAc. Масс-спектр: 235, 215, 149, 80.
Пример 19. 7-(2-Метил-5-пропил -транс -4 ,4а,5,6,8а,9-гексагидро- 2Н-пиразоло Q3,4-р7|хинолинметанол и 7-(1-метил-5-пропил-транс-4,4а,5,6, 8а, 9-гексагидро-1Н-пиразоло 3, хинолин)метанол.
Раствор 650 мг (5,8 ммоль) трет- бутштата калия в 10 мл ТГФ охлажда- ют до О С. К нему добавляют раствор 480 мг (2,1 ммоль) З-гидроксиметил-1- пропил-транс-1,2,4а,5,6,7,8,8а-окта- гидрохинолин-6-она, 600 мг (8,5 ммоль) этилформиата и 15 мл ТГ&. Смесь подогревают до комнатной температуры и перемешивают 5 ч, после чего добавляют 2 мл метилгидразина и концентрацию ионов водорода доводят до рН 9 при поддержании смеси в охлажденном состоянии. Смесь перемешивают в течение ночи при комнатной температуре
111644718 f2
10-октагидропиридо- 2, 3-рЛхинаэолин) метанол.
К раствору 0,5 г (2,2 ммоль) рац- (, 4atf, ) -3-гидроксиметил-1 -про- пилдвкагидррхинолин-6-она в 50 мл толуола добавляют 1,5 мл (5,6 ммоль) трис(диметиламино)метана. Смесь кипятят 2 ч с обратным холодильником. Толуол отгоняют и к раствору остатка в 75 мл этанола добавляют суспензию 130 мг (2,2 ммоль) гуанидина в 50 мл этанола. Смесь кипятят с обратным холодильником в течение 1 ч, переме- 15 шивают при комнатной температуре в
течение ночи, а затем выпивают в воду. Продукт экстрагируют из водной смеси СНС13/изо-РгОН (3:1), экстракт суиат сульфатом натрия и упаривают, полуразолоЈз,4 й1хинолин)метанола, комби- 20 чают 590 мг желтого твердого вещества, нируют и получают гидрохлоридную соль Его пропускают через колонку с силикагелем, используя 7% MeOH/CH Cl, содержащий следы, . Фракции, для ко- (из MeOH/EtOAc),тор ых по данным ТСХ показано присутстПример 20. рац-(4ар, 7о{, 8аоЈЬ25 вие продукта, комбинируют и получают 7-(5-Пропил-4,4а,5,6,7,8,8а,9-окта- 215 мг целевого соединения. Т.пл.
гидро-2Н-пиразоло 3,4-g хинолин) метанол .
К раствору 0,47 г (2,1 ммоль) рац(Зе/,4ао(,8а)-3-гидроксиметил-1-пропил-зо (ДМСО-(16): 7,98 (с, 1Щ 6,21 (с, 2Н), декагидрохинолин-6-она в 50 мл толуо- 0,82 (т, ЗН). ла добавляют 1,4 мл (5,2 ммоль) трис- (диметиламино)метана. Смесь кипятят с обратным холодильником в течение 3 ч. Толуол отгоняют, и к раствору этого материала в 50 мл метанола добавляют 3 Мл гидразина. Смесь перемешивают в течение ночи при комнатной
и затем выливают в воду. Продукт экстрагируют CHClj/изо-РгОН (3:1), затем растворитель отгоняют с получением 560 мг продукта, представленного на ТСХ двумя пятнами. Два изомера разделяют на колонке с силикагелем, используя 7% MeOH/CH Cljj, содержащий следы . Фракции, для которых ТСХ указывает на присутствие 7-(2-метил-5- JQ пропил-тpaне-4,4а,5,6,8а,9-гексагид- ро-2Н-пиразоло 3,4-{Л хинолин)метанола, комбинируют и получают тозилатную соль этого продукта в виде твердого вещества желтого цвета. Т.пл. 232- 233°С (из MeOH/EtOAc).
Фракции, для которых ТСХ указывает на содержание 7-(в1-метил-5-пропил- транс-4,4а,5,6,8а,9-гексагидро-1Н-пиэтого продукта в виде светло-желтого твердого вещества, т.пл. 215-216°С
235°С (из MeOH/EtOAcj. Масс-спектр: 276, 247, 204, 168, 154, 146, 136, 126. Протонный ЯМР-спектр (360 МГц)
35
Пример 22. рац-(4а/3, 7р(, ЗаоО 7-Метоксиметил-5-пропил-4,4а,5,6,7,8, 8а,9-октагидро-2Н-пиразоло 3,4-й хинолин.
Целевой продукт получают по методике примера 20, используя рац- (Зо(, 4ар{, 8аЙ)-3-метилтиометил-1-про- пилдекагидрохинолин-6-он в качестве
Целевой продукт получают по ме тодике примера 20, используя рац- (Зо(, 4ар{, 8аЙ)-3-метилтиометил-1-про- пилдекагидрохинолин-6-он в качестве
температуре и затем выпивают в воду.
Продукт экстрагируют из водной смеси 40 исходного материала«, Его преобразуют
СНС1э/изо-РгОН (3:1), сушат сульфатом натрия и упаривают с получением оранжевого полутвердого продукта, который пропускают через колонку с силикагелем, используя 5-7% МеОН/ , содержащего следы . Фракции, для которых ТСХ указывает на присутствие продукта, комбинируют с получением 300 мг целевого соединения. Его преобразуют в гидрохлорид-50 12,42, ную соль. Т„пл. 224-228°С (из МеОН/ /EtOAc),
в дигидрохлоридную соль и рекристал- лизуют, используя МеОН/СН2С1г, с получением золотисто-коричневого твердого продукта. Т.пл. 229-230°С. 45 , Масс-спектр: 263, 248, 234, 169, 154, 140, 119, 71.
Вычислено,- %: С 53,57; Н 8,09; N 12,49.
Найдено, %: С 53,53; Н 7,90;
П р и м е р 23. рац-(5а/5, Stf, 9аЮ 8-Метоксиметил-1-пропил-5,5а,6,7,8, 9, 9а, 10-октагидропиридо JJ2,3-gJ хиназо- лин-2-амин.
Вычислено, %: С 52,18; Н 7,82; N 13,04.
Найдено, %: С 52,07; Н 7,92;
Целевой продукт получают по мето дике примера 21, используя рац-(3оЈ, 4а#, Яа|5) -З-метоксиметил-1 -пропилN 13,07.
Пример 21. рац-(5а, 8С, 9аЙ) декагидрохинолин-6-он в качестве 8-(2-Амино 6-пропил 5,5а,6,7,8,9,9а,исходного материала. Его рекристал вие продукта, комбинируют и получают 215 мг целевого соединения. Т.пл.
(ДМСО-(16): 7,98 (с, 1Щ 6,21 (с, 2Н), 0,82 (т, ЗН).
235°С (из MeOH/EtOAcj. Масс-спектр: 276, 247, 204, 168, 154, 146, 136, 126. Протонный ЯМР-спектр (360 МГц)
(ДМСО-(16): 7,98 (с, 1Щ 6,21 (с, 2Н), 0,82 (т, ЗН).
Пример 22. рац-(4а/3, 7р(, ЗаоО 7-Метоксиметил-5-пропил-4,4а,5,6,7,8, 8а,9-октагидро-2Н-пиразоло 3,4-й хинолин.
Целевой продукт получают по методике примера 20, используя рац- (Зо(, 4ар{, 8аЙ)-3-метилтиометил-1-про- пилдекагидрохинолин-6-он в качестве
12,42,
в дигидрохлоридную соль и рекристал- лизуют, используя МеОН/СН2С1г, с получением золотисто-коричневого твердого продукта. Т.пл. 229-230°С. , Масс-спектр: 263, 248, 234, 169, 154, 140, 119, 71.
Вычислено,- %: С 53,57; Н 8,09; N 12,49.
Найдено, %: С 53,53; Н 7,90;
12,42,
П р и м е р 23. рац-(5а/5, Stf, 9аЮ- 8-Метоксиметил-1-пропил-5,5а,6,7,8, 9, 9а, 10-октагидропиридо JJ2,3-gJ хиназо- лин-2-амин.
Целевой продукт получают по методике примера 21, используя рац-(3оЈ, 4а#, Яа|5) -З-метоксиметил-1 -пропилдекагидрохинолин-6-он в качестве исходного материала. Его рекристал1J16
лизуют из MeOfl/EtOAc, т.шт. 130°С. Масс-спектр: 290, 275, 261, 245, 218 179, 163, 154, 136, 122, 71.
Вычислено, %: С 66,17; Ч 9,09; N 19,29.
Найдено, %: С 66,41; Н 9,25; N 19,39.
Пример 24. рац-(4а/}, 7с(, 7-Метилтиометил-1-пропил-4 ,4а,5,6, 7, 8,8а,9-ок гагидро-2Н-пира ,4-pQ хинолин.
Целево г продукт получают по методике примера 20 с использованием рац (ЗоЈ, 4ао(, 8а|3)-3-метилтиометил-1-про пил-декагидрохинолин-6-она в качеств исходного материала. Затем получают дигидрохлоридную соль и рекристалли- зуют ее из MeOH/EtOAc, т.пл. 230- 234°С. Масс-спектр: 279, 264, 250, ,232, 185, 170, 119, 87. , П р и м е р 25. рац-(5а|3, 8oi, 9аоО 8-Метилтиометил-6-пропил-5,5а,6,7,8, 9,9а,10-октагидропиридо- 2 , З-fQ хина- золин-2-амин.
Целевое соединение получают по методике примера 21, используя в качестве исходного материала то же соединение, как в примере 24 „
Вычислено, %: С 62,71; Н 8,55;
N 13,28.
Найдено, %: С 62,40; Н 8,73; N 18,38.
Мясс-спектр: 306, 292, 277, 259, 245, 198, 184, 170, 146, 122.
Пример 26. рац-(5а/3, 8(5, 9аоЈ 8-2-Амино-6-пропил-5,5а,6,7,8,9,9а, 10-октагидропиридо-р, 3-р/ хиназолин) метанол.
Целевое соединение получают по ме тодике примера 21, используя рац- (ЗЙ,4аоЈ,8ай)-3-гидроксиметил-1-про- пилдекагидрохинолин-6-он в качестве исходного материала. Затем получают
дигидрохлоридную соль и рекристал- 45 лизуют из MeOH/EtOAc, т.пл. 250 С, Масс-спектр: 276, 247, 204, t68, 154, 146, 136, 126.
Вычислено, %: С 51,59; Н 7,50; N 16,04; О 20,30.50
Найдено, %: С 51,31; Н 7,79; К 15,91; О 20,17.
П р и м е р 27. pan-(5af3,8fj, 9асО- 8-Метоксиметил-6-пропил-5,5а,6,7,8, 9, 9а, 10-октагидропиридо 7., З-pQ хйна- зо лин-2-амин.
Целевой продукт получают по методике примера 21 и в качестве исходно14
го материала используют рац-(ЗГ5, , 8ай) -З-метоксиметил-1 -пропилдекагнд- рохинолнн-6-он.
Вычислено, %: С Н 9,02; N 19,29.
Найдено, %: С 65,89; Н 8,89; N 19,16.
П р и м е р 20. parr(5a/i, 8Д, ) 8-Метилтиометил-t-пропил-5,5а,6,7,8, 9,9а,10-октагидропирндоЈ2,3-р1хиназо- лин-2-амин.
Целевое соединение получают по методике примера 21 из рац-(3|, 4аой 8ай)-3-метилтиометил-1-пропилдекагид- рохинолин-6-она. Масс-спектр: 306, 292, 277, 259, 245, 188, 146. Образуют моногидрохлоридную соль и ее ре- кристаллизуютз Т.пл. более . Вычислено, %: С 56,04; Н 7,94; N 16,34.
Найдено, %: С 56,16; Н 7,73; N 16,09.
Пример 29. ЭтиловьвЧ эфир 4-ок- со-1-пропил-транс-спироГдекагидрохино- лин-6,2 -(1 ,3 -диоксолан)1 -3-карбо- новой кислоты.
К трет-бутилату калия (61,6 г, 0,55 моль) добавляют ТГй (500 мл) и к этой смеси медленно добавляют этиловый эфир 8- (З-этокси-3-оксапропил) пропиламино -1,4-диоксаспиро-4,5-де- кан-7-карбоновой кислоты (98,0 г, 0,27 моль), растворенный в 500 мл ТГФ. Затем смесь выпивают на лед и концентрацию водородных ионов доводят до рН 10. Продукт экстрагируют метилен- хлоридом, сушат сульфатом натрия и упаривают с получением 87,2 г (97,7%) целевого продукта.
Биологические испытания. Взрослых крыс-самцов расы Sprap.ue- Dawley массой около 200 г содержали в кондиционируемом помещении с контролируемым освещением (свет включали с 6 ч утра до 8 ч вечера), кормили и давали пить без ограничений. При про- ,ведении испытаний на резерпинизирован- ных крысах-самцах использовали дозу (Испытуемого соединения 50 мкг/кг, причем каждая крыса получала внутрибрю- пинно инъекцию 2,0 мг резерпина в водной суспензии за 18 ч до введения испытуемого средства. Резерпин вводили с целью однородного повышения уровня содержания пролактина В испытаниях на нерезерпинизированных крысах-самцах, при дозе 1000 мкг/кг испытуемого соединения, предшествую1516
щую процедуру не проводили. Испытуемые соединения растворяли в 10% этаноле, и вводили внутрибрюшинной инъекцией. Каждое соединение вводили при каждом дозировочном уровне группе из 10 крыс, а контрольная группа из 10 интактных самцов получала экви- валентное количество 1 0%-ного этанола. Спустя час после обработки всех крыс убивали обезглавливанием и 150 мкл аликвотные порции сыворотки анализировали на пролактин.
Разность между уровнем пролактина для обработанных крыс и уровнем про- лактина для контрольных животных, поделенная на уровень пролактина для контрольных животных, дает число, которое, будучи умноженным на 100, представляет собой процент угнетения секреции пролактина, характерного для соединений согласно изобретению. Эти показатели процентного угнетения приведены в табл. 1.
Было показано, что агонисты доба- мина влияют на вертячковое поведение пораженных 6-гидроксидофамином крыс в ходе испытаний, предназначенных для выявления соединений, полезных с точки зрения лечения паркинсонизма В этом испытании используются пораженные нитронеостриаталом крысы, подготовленные по методике Ungerstedt Я Arbuthnoff, Brain Res.Соединение, проявляющее дофамин-агонистическую активность и способность проникать через гемато-энцефалический барьер в полосатое тело мозга, заставляет крыс ходить кругами в сторону, противоположную стороне рас- положения раны. По прошествии скрытого периода, длительность которого меняется от соединения к соединению, подсчитывают число оборотов за 15-минутный период.
Показано, что агонисты дофамина, которые проникают через гемато-энцефалический барьер и поступают в мозг, снижают содержание в мозгу метаболитов дофамина, таких как 3,4-ди гидроксифенил-уксусная кислота (ДОФУК) и гомованилиновая кислота (ГВК). Испытания, описанные в работе Perry and Fuller, Soc. Neurosei. Abstr., позволяют оценить влияние соединений на уровень содержания метаболитов дофамина в мозге. Соединения согласно изобретению испытывали согласно этим методикам и резуль18
16
таты для представительных соединений приведены в табл. 2.
Агонисты дофамина, которые поступают в мозг, ведут к повышению уровня кортикостерона в сыворотке. Соединения согласно изобретению испытывали по методике Solem and Brink-Johnsen, Seand. J. Clin, Lab. Invest, для определения их влияния на уровень кортикостерона сыворотки.
Соединения по примерам 1 и 11 являются периферически избирательными агонистами дофамина, Они активны, обеспечивают угнетение секреции пролактина в сыворотку благодаря активированию дофаминовых рецепторов гипофиза, ткани, которая не защищена ге- мато-энцефалическим барьером. Эти соединения ке вызывают вертячкового поведения пораженных 6-гидроксидофамином крыс и не вызывают изменений уровня содержания метаболитов дофамина или кортикостерона в сыворотке, что является видами активности, опосредуемых в участках мозга, которые защищены гёмато-энцефалическим барьером
Соединения согласно изобретению понижают кровяное давление спонтан- но гипертонических крыс,что демонстрируется следующим экспериментом.
Взрослых крыс-самцов спонтанно гипертонических (СГК) массой приблизительно 300 г анестезируют пентобарби- тал-натрием (60 мг/кг, внутрибрюшин- но). Канюлируют трахею и СГК дышат воздухом помещения. Пульсирующее артериальное кровяное давление измеряют по канкшированной сонной артерии с использованием датчика Статхэм (Р23 ID). Среднее артериальное кровяное давление рассчитывают как диастоличес кое кровяное давление плюс 1/3 давления импульса Растворы лекарственного средства вводят внутривенно через катетер, помещенный в бедренную вену. Артериальное кровяное давление измеряют и записывают на многоканальном осциллографе (фирма Бекман, модель R 511A). Для уравновешивания препарата после хирургического вмешательства в течение 15 мин никаких действий не предпринимают.
В табл„ 3 приведены результаты этого испытания для представительных соединений согласно изобретению.
В испытуемых дозах соединения по изобретению признаков токсичности не
проявляли и их можно отнести к категории малотоксичных..
Соединения, полученные согласно изобретению, могут быть использованы для угнетения секреции пролактина, при лечении ненужной лактации, например послеродовой лактации и галакто- реи.
Формула изобретения
Способ получения производных пи- разоло 3,4-рПхинолина или пиридо Ј2,3-g хиназолина формулы
п(I)
R4
I Ко
с)
угде R - атом водорода или Сч-С3-алкил;
кольца С и D транс-конденсированы, R - С(-Сд-алкил, , и R5 определены ниже, если и Rg- - атомы водорода; К.Ј ™ , СНлОСНп, CHrtSCHe,
, -СНг80гСН3,
при условии, что исключены рац-(4ар, 7Й, 8aoi)-4, 4a,5j6,7,8,9-oK rarHflpo- 2Н-пиразоло 3,4- хинолин и рац-(4ай,
7f5, 8аоО-4,4а,5,6,7,3,9-октагидро- 1Н-пиразолор,4 я хинолины; в случае, когда Ъ.. - СНгОСН5, -CH2SCH3 Rg не означает водород; или Rz - СНгОН, -СНгОСН, -CHjjSCH, S-CH3,
8
R-3 водород, a R, и R совмещены с образованием двойной связи, или R2,
4 и % атомы водорода; R, - ОН, -NH2-NHCORT и -NHSOtNR4R8, где Ry и Rg независимо означают С -С алкил, или их солей, отличающийся тем, что производное 7-диметиламинометилен-6-оксо-транс-хинолина формулы
О
(С Н AN -СИ
R, R,
RR4
R.
(ti)
40
, ,
2д где R - RJ. имеют указанные значения, подвергают взаимодействию с гидразином или производным гидразина фор- мулы
NRjNHR
где Rg - водород или С,-С3-алкил, с получением производного пиразоло Р(1хинолина Формулы (I), в котором кольцо В имеет структуру а) или Ь) или с) гуанидином с получением производного пиридоЈ2,З-g хиназолина 35 формулы (I), в котором кольцо В имеет структуру с), и/или, если необходимо, соединение формулы (1),в котором Rg - CH SCH-j окисляют с получением соответствующего соединения формулы (I), в котором Rg - СНг5СН-з, или соедине0
ние формулы (I), где R - NHCOR подч вергают гидролизу и получают соответствующее соединение формулы (I), где RS NH, или переводят соединение формулы (l) в соль о
19
164471820
Продолжение табл.1






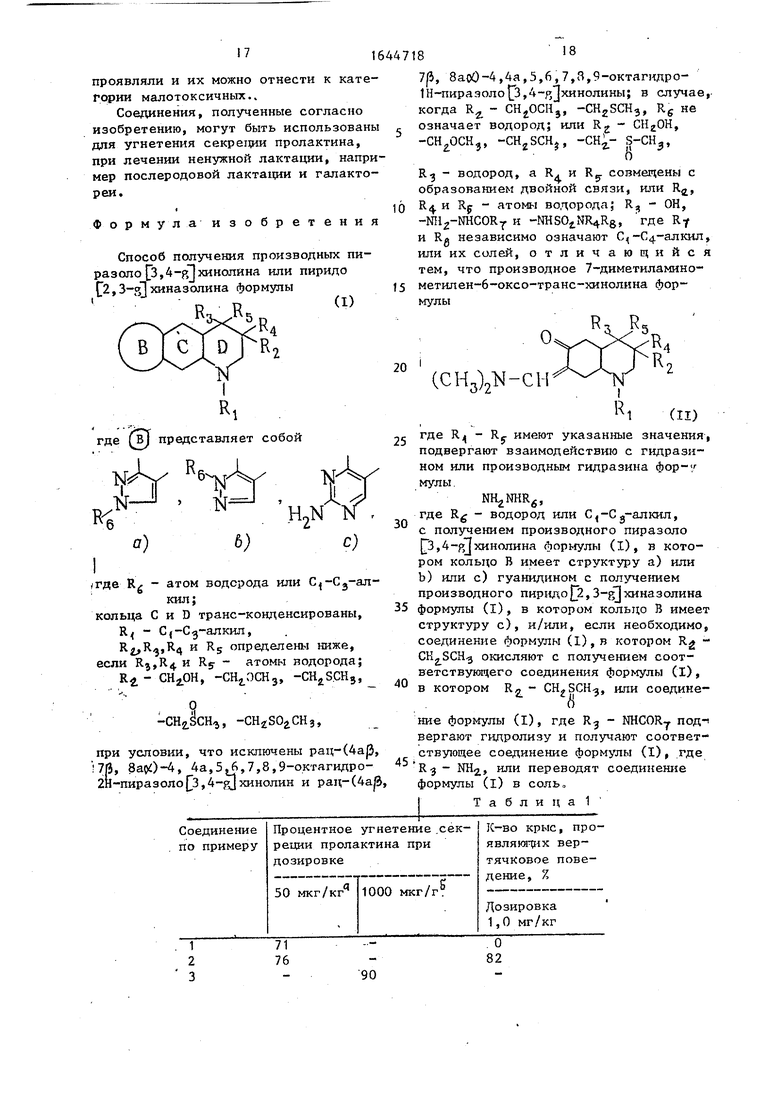


Изобретение относится к гетероциклическим соединениям, в частности к получению производных пиразоло з,4-в хинолина, или пиридо 2,3-gJхина золи на cb-лы JU(1) -R4 Ro 2где Rg - Н или С -Сд-алкил; кольца С и D транс-конденсированы9 RJ - C( алкил, R2,R,,Rn. и R- - определены ниже: 1. R3, . и Rr Н, R2 - СН2ОН,-СН2ОСН}- CH2SCH3, - CH2,S(0)CH3, -СН 50гСНз, при условии, что исключены рац-(4а|3, 7/3, 8аоО -4,4а, 5,6,7,8,9-октагидро-2Н- пиразоло Јз,4-Ј хинолины и рац-(4а/3, 7J5, 8а&) 4,4а, 5, 6, 7, 8, 9-окгагидро-1Н-пн- разоло р,4- хинопины; в случае, когда R - , -CHnSCHg, R8 не означает Н 2. R. - СН2ОН, -СН2ОСН35 , -СНг-5(0)-СНэ, R3- H, a R и - совмещены с образованием двойной связи, или 3. R4, R4 и R Н, R3-OH, -NH2-NHCOR7 и -NHS02NRTR8, где R и R& - независимо -С -С -алкил или их солей, применяемых в качестве аганисюв цоЛамяча. Цель изобретения - разработка способа получения более активных соединений. Получение ведут реакцией соответствующего производного 7-диметиламипометилен-6-ок- со-транс-хинолина с гидразином или производным гидразина ф-лы , где R, - Н JUIH С -Сд-алкип, с получением производного пиразопо 3,4-j хинолина ф-лы (I), где кольцо В-(а) или (Ь) или с гуанидом с получением производного пиридо 2, 3-gJXHHa3onHHa ф-лы (I), где кольцо В -(с) и/или, если необходимо, соединение ф-лы (l), где R 2 - , окисляют с получением соответствующего соединения ф-лы (I), где Кг - (0)CH3, или соединение ф-лы (I), где Кз - NHCOR, подвергают гидролизу и получают соответствующее соединение ф-лы (I), где R - или переводят соединение ф-лы (I) в соль 3 габл с Ј
(1Н) (2Н)
14 62 83 27 7,2
84 84 94
83 84 70 37 89 39 89 92 35
Процентное снижение относительно контроля для уровня пролактина в сыворотке после введения дозы 50 мкг/кг резерпинизированным крысам самцам;
процентное снижение относительно контроля для уровня пролактина в сыворотке после введения дозы 1000 мкг/кг нерезерпинизированным крысам- самцам.
Таблица
ДОФУК 3,4-дигидроксифенилуксусная кислота; ГВК гомованилиновая кислота;
Ь соединение 8-метилтиометил-6-пропил-транс-5,5а, 6,7,9а,10-гексагидропиридо 2,З-R хиназолин- 2-амин.
80
33
О
О
100
| Патент Швейцарии № 641801, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Клупп | 1976 |
|
SU643258A2 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
Авторы
Даты
1991-04-23—Публикация
1987-06-15—Подача