со
Од 00
0д
О1
Изобретение относится к технике получения хромовых соединений, в частности нового соединения - гидроксокарбоната хрома (III) и натрия фор- g основного сульфата хрома. При избыт- мулы NaCr(OH) CO,,lH20, используемого в качестве сырья для получения дубителя и в качестве исходного материала для получения соединений трехвалентного хрома.
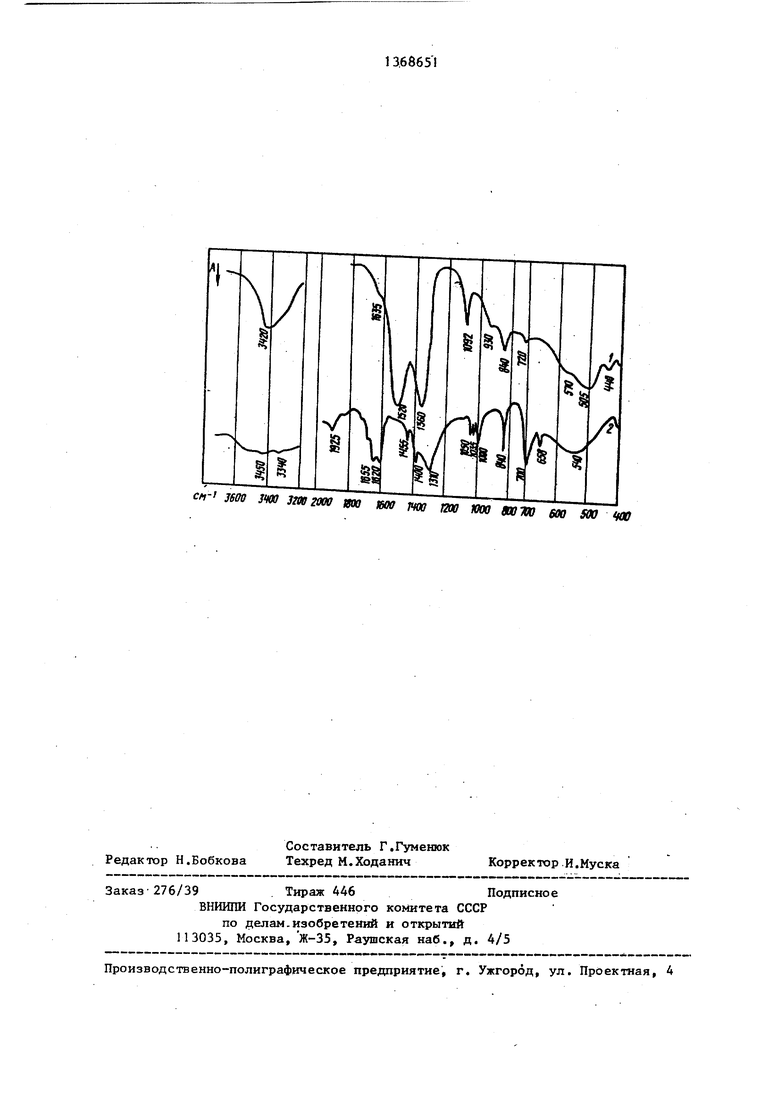
На чертеже приведены полосы поглощения карбонат-иона на ИК-спектре (кривая I) и спектр мехайической смеси NaHCOj и Cr(OH)g Скривая 2). .
Пример 1. К раствору 44,2 г соды () в 300 г воды.добавляют 100 г хромисульфата натрия, содержащего 10,9% Сг (III) и 69-% so,, , пере- мeJливaюT, нагревают до кипения и выдер- живают до достижения рН 7,8., В результате реакции цвет суспензии изменяется от светло-зеленого к серо- зеленому и далее к сиреневому. Целевой продукт отделяют фильтрованием, промываюЧ водой и сушат при 80 С. При этом получают 42,9 г гидроксо карбоната хрома (III).и натрия, содержащего, %: Сг 25,4; СО 28,1; Na 10,9; 17,7; S04 1,0, что соответствует формуле NaCr(OH)COg 2, . Наличие соединения, отвечающего формуле, подтверждается тем, что при промывке большим.избытком воды соотношения между Сг, СОэ и Na в осадке -остается постоянным.
Пример 2. К раствору 45,4 г ; соды () в 250 г воды добавляют 100 г хромисульфата натрия, содержащего 10,9% Сг и 69% 80, перемешивают, нагревают до кипения и вьщер- живают до достижения рН 8,8.
Целевой продукт отделяют фильтрованием, промывают водой и сушат при . При этом получают 42,5 г гид- роксокарбоната хрома (III) и натрия, содержащего, %: Сг 25,6; СО 29,0; Na 11,5; 16,6; ЗОд 0,1, что соответствует формуле NaCr (ОН) (СОР х1,9П20. Фильтрат содержит 0,005% Сг (III).
Количество вводимой в раствор соды натриевой соли хрЬмисерной кислоты влияет на полноту протекания процесса, чистоту получаемого продукта. Молярное соотношение соды и хромисульфата натрия связано с величиной рН. При недостатке соды (избытке натриевой соли хромисерной кислоты, рН - ) разложение происходит не
ке соды (недостатке натриевой соли хромисерной кислоты, ,8) происходит потеря хрома с фильтратом в виде хромита натрия .Целевой продукт за-
10 грязнен примесью соды, которая трудно вымывается, отношение (Na:CO,);Cr 1.
В табл.1 приведены результаты химического анализа полученного соеди15 нения в интервале рН 7,8-8,8.
При ИК-спектроскопическом исследовании гидроксокарбоната хрома (III) и натрия установлено, что представленные образцы являются комплексным
20 соединейием. Роль лигандов выполняют группы , он и возможно ILO.
4- Ч
Комплексообразователь Сг . Карбонат- ион координирован бидентатно, о чем свидетельствзпот полосы поглощения
25 его на ИК-спектре (кривая 1).
В табл.2 приведены результаты ИК- спектроскопического изучения образца гидроксокарбоната хрома (III) и натрия .
30 Расщеплемте , к появление достаточно интенсивной в спектре говорит о присутствии ОН-группы. Полоса поглощения 930 относится к де- ,формациоиному; колебанию ОН-группы. 35 Спектр механической смеси NaHCOj и Cr(OH)j содержит такое же количество Na, Сг и С0з, как и гидроксо- карбонат хрома (III) и натрия. Спектр полностью совпадает со спект40 ром NaHCOj, Полосы поглощения Cr(OH)j на фоне поглощения NaHCO, не видны.
Таким образом, с учетом данных хи. мического анализа и ИК-спектроскопи- ческого исследования подтверждено по45 лучение комплексного соединения гидроксокарбоната хрома (III) и натрия, состав которого может быть выражен формулой ШаСг(ОН)2-СОз-2,0±0, iHjjO. Основным отличительным свойством
50 полученного соединения, отвечающего формуле NaCr(HO)2 COj-2,0±0,1Н20, по сравнению с известным гидроксокарбо- натом хрома, полученным обработкой водорастворимых солей хрома (III)
55 карбонатами, является его устойчивость к окислению кислородом воздуха и парами воды.
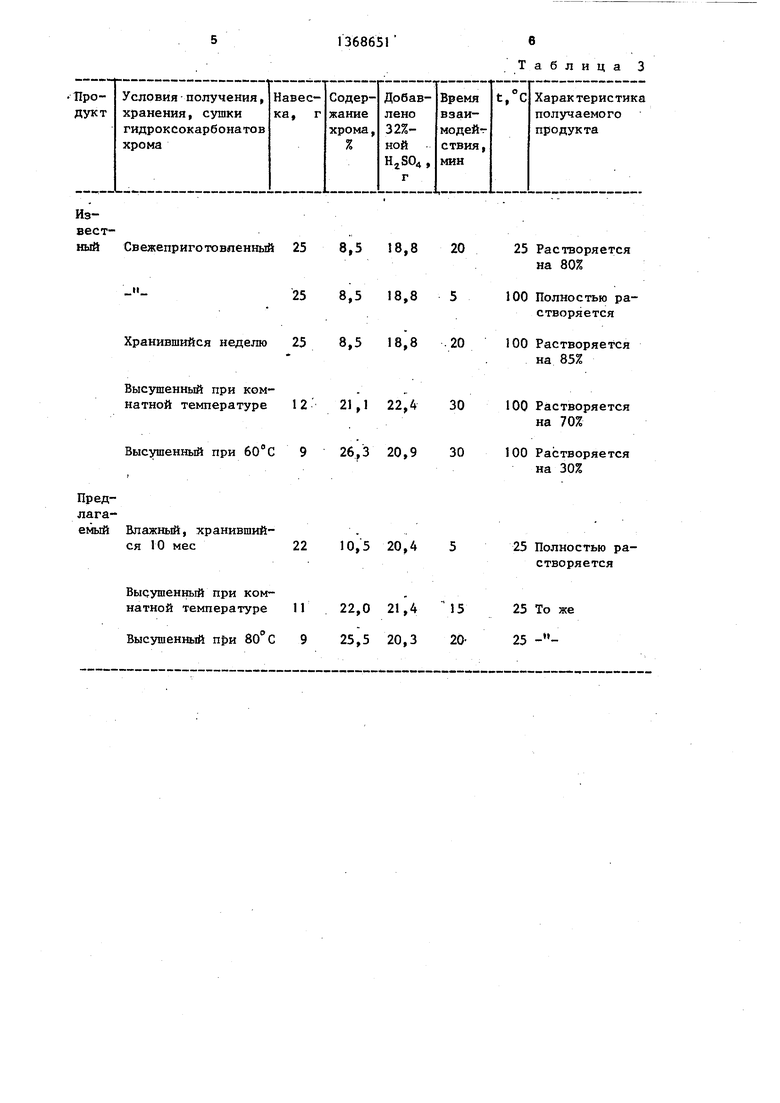
В табл.3 приведены результаты растворимости гидроксокарбонатов хро
3686512
полностью, отношение (Na:COj)Сг 1.
Этот продукт не разлагается полностью серной кислотой с получением раствора
g основного сульфата хрома. При избыт-
ке соды (недостатке натриевой соли хромисерной кислоты, ,8) происходит потеря хрома с фильтратом в виде хромита натрия .Целевой продукт за-
0 грязнен примесью соды, которая трудно вымывается, отношение (Na:CO,);Cr 1.
В табл.1 приведены результаты химического анализа полученного соеди5 нения в интервале рН 7,8-8,8.
При ИК-спектроскопическом исследовании гидроксокарбоната хрома (III) и натрия установлено, что представленные образцы являются комплексным
0 соединейием. Роль лигандов выполняют группы , он и возможно ILO.
4- Ч
Комплексообразователь Сг . Карбонат- ион координирован бидентатно, о чем свидетельствзпот полосы поглощения
5 его на ИК-спектре (кривая 1).
В табл.2 приведены результаты ИК- спектроскопического изучения образца гидроксокарбоната хрома (III) и натрия .
0 Расщеплемте , к появление достаточно интенсивной в спектре говорит о присутствии ОН-группы. Полоса поглощения 930 относится к де- ,формациоиному; колебанию ОН-группы. 5 Спектр механической смеси NaHCOj и Cr(OH)j содержит такое же количество Na, Сг и С0з, как и гидроксо- карбонат хрома (III) и натрия. Спектр полностью совпадает со спект0 ром NaHCOj, Полосы поглощения Cr(OH)j на фоне поглощения NaHCO, не видны.
Таким образом, с учетом данных хи . мического анализа и ИК-спектроскопи- ческого исследования подтверждено по5 лучение комплексного соединения гидроксокарбоната хрома (III) и натрия, состав которого может быть выражен формулой ШаСг(ОН)2-СОз-2,0±0, iHjjO. Основным отличительным свойством
0 полученного соединения, отвечающего формуле NaCr(HO)2 COj-2,0±0,1Н20, по сравнению с известным гидроксокарбо- натом хрома, полученным обработкой водорастворимых солей хрома (III)
55 карбонатами, является его устойчивость к окислению кислородом воздуха и парами воды.
В табл.3 приведены результаты растворимости гидроксокарбонатов хро
ма в серной кислоте в зависимости от условий хранения, получения, сувки
1,5).
/HjSO
(молярное отношение
При температуркой обработке полученного продукта вплоть до 200 С отношение СО, к Сг остается практически постоянным. Полученный продукт в течение 10 мес сохраняет способность растворяться в серной кислоте с получением дубителя.
Присутствие натрия в гидроксокар- бонате хрома в эквимолярном отношении к хрому повьшает устойчивость этого соединения к термической обработке и тем самым способствует сохра- нению его химической активности.
Форь5ула изобретения
Способ получения гндроксокарбоната хрома (III) и натрия формулы
NaCr(OH),0±0,lH20 заключающийся во взаимодействии хромисульфата натрия с раствором соды при температуре кипения реакционной смеси до.рН 7,8- 8,8 с последзлощим отделением, промывкой И сушкой осадка продукта.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гидроксокарбоната хрома (III), алюминия и аммония | 1989 |
|
SU1608126A1 |
| Способ получения дигидроксохром (ш) хромата | 1985 |
|
SU1321682A1 |
| Способ очистки сульфата натрия отСОЕдиНЕНий XPOMA (у1) | 1979 |
|
SU850585A1 |
| Способ определения свободной кислоты в растворах солей хрома /ш/ | 1977 |
|
SU697924A1 |
| Способ определения фосфора (у) в объектах,содержащих примесь хрома ( @ ) | 1985 |
|
SU1394123A1 |
| Способ электролитической регенерации шестивалентного хрома | 1973 |
|
SU583202A1 |
| Способ очистки раствора монохромата натрия | 1980 |
|
SU1225816A1 |
| КАТАЛИЗАТОР ПАРОВОЙ КОНВЕРСИИ МОНОКСИДА УГЛЕРОДА, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2006 |
|
RU2314870C1 |
| Способ получения монохромата натрия | 1976 |
|
SU742381A1 |
| Способ очистки солевых или гидроксидных соединений хрома ( @ ) от железа ( @ ) | 1987 |
|
SU1502471A1 |
Изобретение относится-, к технологии получения хромовых соединений и касается получения нового вещества - гидроксокарбоната хрома (III) и натрия, используемого в качестве сырья для получения дубителя и соединений трехвалентного хрома..Способ получения вещества заключается во взаимодействии хромнсульфата натрия с раствором соды при температуре кипения реакционной смеси до рН 7,8-8,8. 3 табл., I ил.
рН
На
Содержание компонентов СгCOj
Mac.Z I м.д. мас.Х I м.д. мае./С I к.д.
7,810,90,9725,А1,0028,10,9617,72,10НаСг ((), COj-2,
8,211,20,9925,5 ,0028,80,9817,52,00НаСг(Ой)4СО, 2,ОН,0
8,511,31,0025,5 .1,0028,60,9717,32,00КаСг{ОН)СО,,0
8,811,51,0225,6J,0029,00,9916,61,90HaCr(OH)tCO,I,9Н40
Таблица I
Формула соединения
Н,0
мае
1
.1 I м.д.
Т а б л и ц а 2
Известный Свежеприготовленный 25 8,5 8,8 20
25 8,5 18,8 5
Хранившийся неделю 25 8,5 18,8 .20
Высутаенный при комнатной температуре 12 21,1 22,4 30
Высушенный при бО С 9 26,3 20,9 30
Влажный, хранившийся 10 мес
22 10,5 20,4 5
Высушенный при комнатной температуре 11 22,0 21,4 15
Высушенный при 80°С 9 25,5 20,3 20Таблица 3
25 Растворяется на 80%
100 Полностью растворяется
100 Растворяется на 85%
100 Растворяется на 70%
100 Растворяется на 30%
25 Полностью растворяется
25 То же 25 J600 ЛИ 32002000 №Ю «Off тг OOff ЮОО 800140 600 5Ж 400
| Роде Т.В | |||
| Кислородные соединения хрома и хромовые катализаторы | |||
| - М.: Изд-во АН СССР, 1962, с | |||
| Машина для разделения сыпучих материалов и размещения их в приемники | 0 |
|
SU82A1 |
| Encyclopedia of Chem., Techn., 1964, V | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Катодная лампа с внешним подогревом | 1923 |
|
SU493A1 |
Авторы
Даты
1988-01-23—Публикация
1985-11-29—Подача