со
00 9

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО АНАЛИЗА | 1994 |
|
RU2101697C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЛАТИНЫ В ВОДНЫХ РАСТВОРАХ И ТЕХНОЛОГИЧЕСКИХ СЛИВАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2011 |
|
RU2467320C1 |
| Инверсионно-вольтамперометрический способ определения пенициллина G в водных растворах и биологических жидкостях | 1990 |
|
SU1746289A1 |
| СПОСОБ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ИРИДИЯ В НИТРИТНОЙ СРЕДЕ | 2010 |
|
RU2436079C1 |
| СПОСОБ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ РАЗНОВАЛЕНТНЫХ ФОРМ МЫШЬЯКА В ВОДНЫХ РАСТВОРАХ | 1996 |
|
RU2102736C1 |
| СПОСОБ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ БЕНЗИЛПЕНИЦИЛЛИНА | 2010 |
|
RU2425365C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОДНОВРЕМЕННОГО ОПРЕДЕЛЕНИЯ СЕЛЕНА И ЙОДА | 2009 |
|
RU2415411C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РТУТИ КАТОДНО-АНОДНОЙ ВОЛЬТАМПЕРОМЕТРИЕЙ | 2013 |
|
RU2533337C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ИНГИБИТОРОВ КИСЛОТНОЙ КОРРОЗИИ В НЕВОДНЫХ СРЕДАХ | 1997 |
|
RU2145079C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ СЕНСОРОВ НА ОСНОВЕ ЗАМЕЩЕННОГО ПОЛИ(3,4-ЭТИЛЕНДИОКСИТИОФЕНА) | 2021 |
|
RU2781398C1 |
Изобретение относится к области биоэлектрохимии. Цель изобретения - упрощение процесса, улучшение воспроизводимости и сравнимости результатов. Цель достигается тем,что снимают циклические вольт-амперные кривые на золотом электроде,модифицированном ди-(4-пиридил)-дисульфидом, при начальном потенциале (-0,4)-(-0,1)В, потенциале точки поворота (-0,78) - (-0,80)В и скорости развертки потенциала 0,16-0,5 В/с. Концентрация ферредоксина (1,9 -3,8) 10 моль/л. 1 з.п. ф-лы,1 ил., 2 табл. i (Л
со
&0
Изобретение относится к области биозлектрохимии, касается способа идентификации йативного состояния ферредоксина электрохимическим Методом и может Выть использовано для исследований в биохимии, физиологии растений, молекулярной биологии для анализа содержания в гомогенных препаратах ферредоксина нативной формы и его способности участвовать в реакциях, связанных с переносом электронов, включая фотовосстановление НАДФ , фиксацию азота и углекислоты.
Цель изобретения - упрощение анализа и улучшение его воспроизводимости,
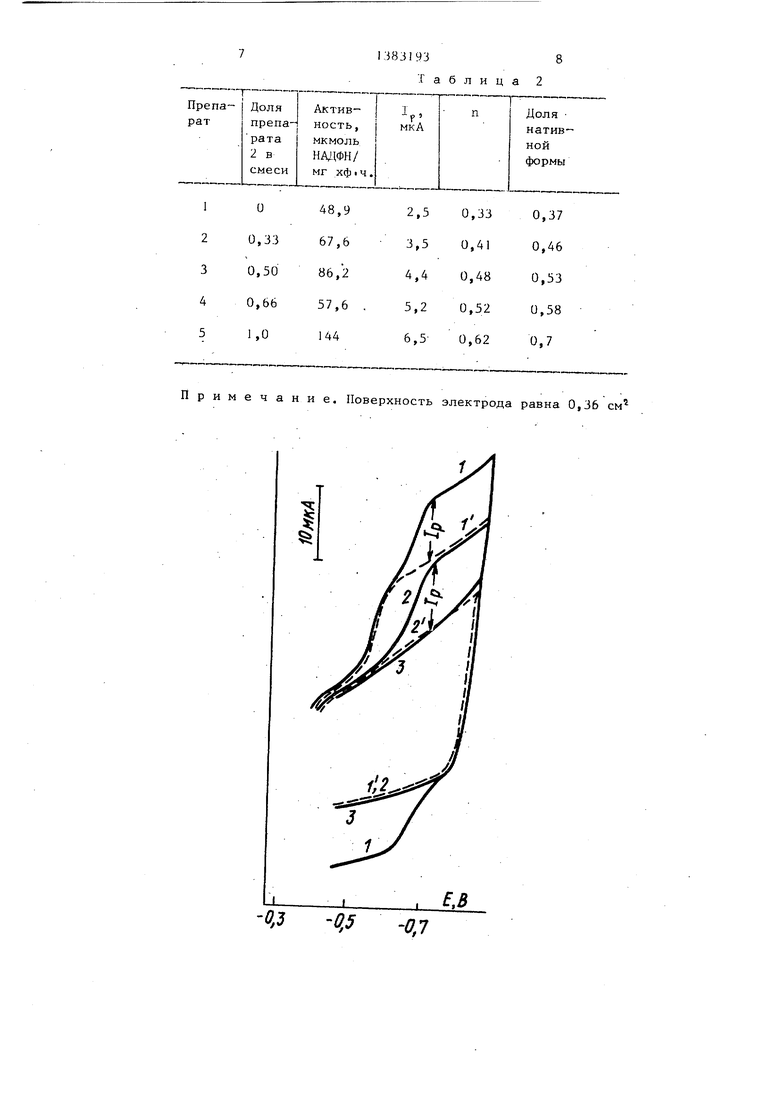
На чертеже представлены вольтампе рограммы 0,31 мМ свежевыделенного ферредоксина и электролита на золото модифицированном (кривые 12 и l ,2 соответственно) и немодифицированном (кривая З) электроде.
Способ осуществляют в несколько стадий: модификация золотого электрода, проведение электрохимическрй реакции и регистрация вольт-амперной кривой, анализ вольт-амперной кривой и расчет числа переносимых электронов- на молекулу ферредоксина.
Модификацию золотого электрода прводят путе;м покрытия поверхности пленкой необратимо адсорбированного ностикрвого переносчика ди-(4-пири- дил)-дисульфида. Необходимо использовать высокоочищенный препарат моди еикатора, например, фирмы Sigma, лектрохимическую реакцию ферредоксина и снятие вольтамперограммы проводят в области потенциалов (-0,4).. (-0,78)В.
Модифицирующее покрытие стабильно в области рН 7...8,2, которая рекомендована для проведения электрохимической реакции ферредоксина (ферре- доксин в этой области рН проявляет максимальную активность в реакции фотовосстановления НАДФ ).
Следующая стадия - проведение электрохимической реакции и снятие вольт-амперной кривой.
Обратимый электродный процесс с диффузионным ограничением для стационарного электрода описывается уравнением512 ,,j, 12
0,272 п
D
, (1)
где I р- пиковое значение тока. А; п - число переносимых, электронов ;
0
5
0
5
0
5
0
5
0
5
q - пло1цадь электрода, см ;
D - коэффициент диффузии, равйый для ферредоксина 1,2 х X
V - скорость развертки потенциала,, Б/с; С - концентрация белка, мМ,
Электрохимическую реакцию ферре- доксина и фиксирование вольтамперо- граммы рекомендуется проводить в следующем оптимальном режиме: кон- .центрация ферредоксина 0,2...0,4 мМ; рН 8,0;ионная сила 0,1 .. .0, 1 7 м; скорость развертки потенциала 0,25 В/с; , начальный потенциал (-0,1)...(-0,4)В. Делают также контрольные измерения: получают вольт-амперную кривую фер- редоксина на немодифицированном золотом электроде и электролита на модифицированном .электроде.
Так как при первом сканировании волна восстановления ферредоксина накладывается на ток восстановления ди-(4-пиридил)-дисульфида, начало волны ферредоксина не всегда хорошо выражено. По вольтамперограмме второго сканирования измерения могут быть сделаны точнее, так как реакция восстановления модифкатора необратима и при повторном сканировании не обнаруживается. Поэтому рекомендует- . ся делать два последующих сканирования потенциала, только потенциал точки поворота прямоугольной развертки не должен превышать (-0,78)... (-0,8)В (относительно насыщенного каломельного электрода).
При электрохимическом анализе могут мешать электрохимически активные низкомолекулярные.соединения, которые искажают вид полярограммы, напри- мер сульфид разложенного кластера. Исследуемый раствор ферредоксина-до анализа необходимо очистить гель-. . фильтрацией на сефадексе С-25 или диализом.
Следующая стадия - анализ вольт- амперной кривой.
Сначала по вольт-амперной кривой- идентифицируют ферредоксин. Для этого находят редокс-потенциал реакции и сравнивают его со стандартным известным редокс-потенциалом. Потенциал катодного пика обратимого процесса смещен относительно редокс- потен- циала на 29 мВ, потенциал анодного пика также смещен в противоположную
сторону. Разность потенциалов между катодным и анодным пиками характеризует обратимость процесса. Для обратимого процесса она равна 58 мВ. Для квазиобратимой электрохимической реакции ферредоксина эта величина составляет 120 мВ, т.е. превьшает теоретическое значение для обратимого одноэлектронного процесса. Редокс-по- тенциал тем не менее может быть определен как средняя точка между потенциалами катодного и анодного пиков .. .
Для определения числа переносимых в реакции электронов находят высоту катодной или анодной волны.Способ расчета высоты представлен на чертеже. Измерйют высоту катодной (или .анодной) волны или пика I от уровня тока контроля. В качестве такого уровня можно взять уровень тока электролита на модифицированном электроде. В этом случае ток восстановления поверхностно связанного ди-(4-пиридил)-дисульфида исключается. Из1мерение катодного пика ферре- доксина делают после второго сканирования, при этом в качестве конт-. рольного, уровня используют ток фер- редоксина на немодифицированном электроде. Высоты волн, найденные этими двумя способами, совпадают.
После того, как найден катодный (или анодный) ,ток, представляют его значение в уравнение (1) и находят число переносимых электронов (п). Отношение найденной величины к 0,9, числу переносимых электронов, характерному для нативного ферредоксйна, характеризует долю нативной формы в препарате. Число п для нативного ферредоксйна меньше 1, по видимому по той причине, что на стадии мёжмолеку лярного электронного обмена в адсорбированном слое электронный обмен несколько заторможен.
Пример 1. Анализируют гомогенный препарат свежевыделенного из двухнедельных проростков гороха ферредоксйна, который характеризуется отношениями пиков оптических плотностей А 2д/А277 Of54; A,,v,/A
J30
277
0,75.
Модификация электрода. Вначале поверхность золотого электрода тщательно полируют водной суспензией А1„0, затем промывают бидистилля- том. Модификацию проводят путем пог-
5
0
5
0
5
0
5
0
5
ружения электрода на. 3 мин в 10 М раствор ди-(А-пиридил)-дисульфида в 0,1 М К-фосфатном буфере, рН 7,0. После этого электрод промьшают в буфере в-течение 1 мин и переносят в электрохимическую ячейку.
Электрохимическая реакция и снятие вольт-амперных кривых. Раствор ферредоксйна предварительно очищают от низкомолекулярных соединений гель- фильтрацией на колонке с сефадексом С-25 (элюируемьй раствор 0,15 М NaCl в 0,02 М трициновом буфере, рН 8), Анализируемый раствор, содержащий 0,307 мМ ферредоксйна, 0,17 М NaCl в 0,02 М трициновом буфере, рН 8,0, помещают в электрохимическую ячейку, предварительно освобожденную от кйсг лорода. Температура в ячейке 20 С. Раствор освобождают от кислорода пропусканием очищенного водорода в течение 1,5 мин. После этого в ячейку помещают модифицированный золотой электрод (q 0,25 см ) и на него подают начальное напряжение 0,3В (относительно насыщенного каломельного электрода). .Далее снимают две. катодно-анодные вольт-амперные кривые со скоростью развертки 0,25 В/с, потенциал точки поворота 0,78 В. В таких же условиях снимают вольтампе- рограмму ферредоксйна на немодифици- рованном золотом электроде.
Анализ вольтамперограммы. Потенциалы пиков: катодного - 0,69В, анодного -0,57В. Потенциал средней точки между потенциалами катодного и анод ного пиков равен -0,63 В и близок к стандартному редокс-потенциалу для растительных фёрредоксинов (-0,62)... (-0,67)В. Катодный и анодный пики одинаковы, а разность потенциалов между ними.составляет 120 мВ.
Высоту волны находят как разность тока в максимуме катодной волны на вольтамперограмме, полученной при втором сканировании на модифицированном электроде, и тока при том же потенциале на катодной ветви вольтамперограммы ф.ёрредоксина, снятой на чистой поверхности электрода. В данном примере эта величина раена 10,0 мкА. Тогда число переносимых электронов, рассчитанное по уравнению (l), равно 0,85. Отсюда доля активной формы ферредоксйна, оцененная этим способом, составляет 0,94.
5 13831
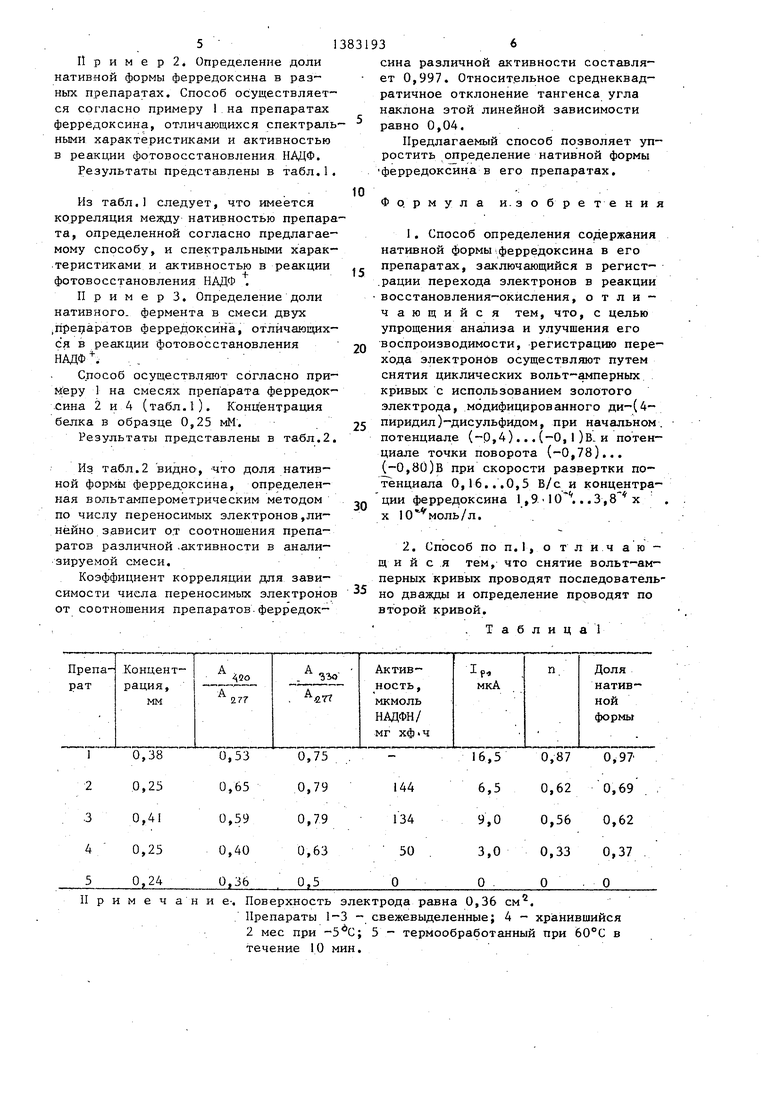
П р и м е р 2. Определение доли нативной формы ферредоксина в раз ных препаратах. Способ осуществляется согласно примеру 1 на препаратах ферредоксина, отличающихся спектраль- ными характеристиками и активностью в реакции фотовосстановления НАДФ. Результаты представлены в табл,1.
Из табл.1 следует, что имеется корреляция между нативностью препарата, определенной согласно предлагаемому способу, и спектральными характеристиками и активностью в реакции фотовосстановления НАДФ .
ПримерЗ. Определение доли нативного. фермента в смеси двух .riperjapaTOB ферредоксина, отличающихся в реакции фотовосстановления НАДФ . , .
Способ осуществляют согласно при- м еру 1 на смесях препарата ферредок- сина 2 и 4 (табл.1). Конг ентрация белка в образце 0,25 мМ.
Результаты представлены в табл.2
Из табл.2 видно, -что доля нативной формы ферредоксина, определенная вольтамперометрическим методом по числу переносимых электронов,линейно зависит от соотнощения препаратов различной .активности в анали- зируемой смеси.
Коэффициент корреляции для зависимости числа переносимых электронов от соотношения препаратов-ферредок-
- ,1 ,1 J-п-гттг-:-г--| - Р И М е Ч а н и е-. Поверхность электрода равна 0,36 см.
Препараты 1-3 - свежевыделенные; 4 - хранившийся 2 мес при 5 - термообработанный при 60°С в течение 10 мин.
0
5
20
5
30
35
936
сина различной активности составляет 0,997. Относительное среднеквадратичное отклонение тангенса угла наклона этой линейной зависимости равно 0,04.
Предлагаемый способ позволяет упростить определение нативной формы ферредоксина в его препаратах.
Формула и-зобретення
I. Способ определения содержания нативной формы ферредоксина в его препаратах, заключающийся в регист- . рации перехода электронов в реакции восстановления-окисления, отличающийся тем, что, с целью упрощения анализа и улучшения его воспроизводимости, регистрацию перехода электронов осуществляют путем снятия циклических вольт-амперных кривых с использованием золотого электрода, модифицированного ди-(4- пиридил)-дисульфидом, при начальном, потенциале (-р,4)...(-0,I)В- и потенциале точки поворота (-0,78)... (-0,80)в при скорости развертки потенциала 0,16...0,5 В/с и концентрации ферредоксина 1,910 ..3,8 х
X 10 МОЛЬ/Л.
Т а б л и ц а 1
Примечание. Поверхность электрода равна 0,36 см 
| Гинс В.К | |||
| и др | |||
| Светозависимое восстановление НАДФ в хлоропластах и активность гликолактоксидазы у яровых пшениц разной продуктивности в онтогенезе | |||
| - Физиология растений, 1985, тТ32, вьт.1, с.53-59 | |||
| Гейровский Я., Кута Я | |||
| Основы полярографии | |||
| - М.: Мир, 1965, с,474. |
Авторы
Даты
1988-03-23—Публикация
1986-06-20—Подача