Изобретение относится к области медицины, а именно к биологическим методам оценки генетической опасности факторов .окружающей среды, и предназначено для повьшения чувствительности индикаторной тест-системы gifin де-кектирования вторичных мута генов, нуждающихся в метаболической активации, и может быть использовано в экспериментальной онкологии, 1гутрициологии, гигиене окружающей среды и токсикологии.
Целью изобретения является повы- . шение чувствительности способа.
Способ осуществляют следукйцим образом.
Используют растущих крыс-саМцов линии ВАГ с исходной массой тела 50- 60 г. Экспериментальных животных содержат на диете, в которой аминокислотный дисбаланс достигался путем замены 83% казеина на пшеничную клейковину которая б.една по содержанию лизина, треонина и метиоиина а витаминную недостаточность моделируют Исключением из состава диеты витаминов А,С и Е. Контрольные группы животных содержат на обще.вивариом рационе и сбалансированном полусинтети- чес15ом рационе.
Перед забоем, после содержания на вышеуказанных рационах в течение 1,5- 2 месяцев, за 24 ч животных лишают корма, В качестве ферментных систем для метаболической активации вторичных м тагенов используют микросо- tta . Экспериментально установ- - лёно, что.оптимальная концентрация
. микросомального белка в инкубационной смеси 1,5-3,0 мг/ьт. В экспериментах использовали концентрацию белка в инкубационной смеси мг/мл. Подготовка бактериальной культуры. Культуру. (Salmonella ЁурЫгаигггпп ТА 1535) с косяка переносят петлей в IО мл мясо- пептонного-бульона и псд. ращивают в термостате при в течение 18 ч. В день постановки эксW
СП
о
оа о а
315103
перимекта 5)0 нп ночной культуры пе- ренос;1т в 100 МП мясо-пептоиного бульона и подравшвшот при до плотности 5-10 клеток при постоянном встряхивании. Содержимое колбы переносят в стерильные центрифужные пробирки и центрифугируют на центри- |)уге, К-23 при при 5000 об/мин fe течение 20 мин. Осадок суспенди- рутот в 30 мл минимальной среды разведенной в четыре раза. Цёнтрифуги- роагние повторяют в том же режиме. Осадок ресуспендяругот в 15 мл 0,15 М хлористого калия.
В иикубацийнную смесь, содержа-- $цую 0,7 мл бактериальной суспензии, О, раствора клористого магния (160мМ 0,2 мл 0,5 fil раствора НАДФН, 0,3 мл суспензии микросом добавляет в слу- чае контрольных вариантов 0,2 мл дистиллированной воды, а в опытные йарианть либо 0,2 мл К-нитрозсмор- фолина до конечной кокцектраи га 200 мкг/мл, либо 0,2 мл вдпслофосфа- на до конечной концентрации 500 мкг/м Инкубационную смесь выдерживают на водяной бане при 37°С в течение 30 мин hpH постоянном встряхиванки. Реакцию останавливает добавлением 2,0 мл холодного М раствора хлористого калия. Затем кнкубациониую смесь цент рифугирутот при 5000,, об/мин в течение 10 мин. Осадок суспендируют в ,5 мл минимальной жидкой среды, раз- веденйЪй в четыре раза.
Для определения количества выживших бактерий 0,5 мл суспензии разводят до 10 и 0,5 мл разведенной суспензии вносят в чашки с мясо-пептон- ным агаром и подращивают в термостате при а течение 18ч,
Для учета количества ревертйнтов О,25 мл цельной суспензии переносят в пробирки с 0,6%-ныи Минимальным ага- ром (предварительно расплавленным при ), перемешивают. Содержимое пробирки разливawT на чашки Петри с. ;1,5%-ным мннимальньпм агаром и инкуби- руют в термостате при в течение лА8 ч... :. Дпя учета выживтш: бактерий подсчитывают количество колоний на чашках, среднее умножают на два и определяют ЧИСЛО жизнеспособнь х клеток в 1 мл при данном разведении. Путем «перемножения этой величины на коэф- фщиент разведения получают число жи неспособгедх .клеток в исходном вариант©
0 5
0
5
5
0
Число ревёртайтов определяют путем перемножения среднего числа колоний на чашках на четыре и получают число мутантов в 1 мл. Расчет частота мутаций производят путем деления числа мутантов в 1 мл число выживших клеток. Статистинескутй обработку полученных данных проводят по критерию Стыодента.
Пример 1. Эксперимент проводят на трех .. iTpynnax крыс линии ВАГ. Первую группу крыс содержат на общевиварном рационе. Вторая группа животных получает сбалансированную полусинтетическую диету (табл.1). Третью группу животных содержат на диете с дефицитом лизина, треонина, метиокина и витаминов А, С и Е (табл.2).
Состав солевой смеси полусинтетических диет приведен в табл. 3. Соо тав витаминов - в табл. 4.В диету жи-| вотных третьей группы витамины А, С и Е не вводя.т.
Животных содержат на вьшеуказанных рационах в течение 1,5-2 месяцев. В течение трех дней перед забоем все группы экспериментальньпс животных п6- лзгчают внутрибрюшинно инъекции фенобарбитала я дозе 80 мг/кг массы тела. Выделение препарата микросом печени крыс проводят общепринятьпч Методом.
Данные по мутагенной метаболической активации N-нитрозоморфрлина и циклофосфана, при описанных выше экспериментальных условиях, приведены в табл. 5 и 6 соответственно.
Как видно из табл.5., частота индуцированных мутаций вследствие метаболической активации Ы-нитрозомор- фолина выше при использовании биоматериала животных, содержащихся на диете с дефицитом лизина треонина, метионина и витамннов А,С и Е, по сравнению с другими rpyirtiaMH животных. Так, количество индуцированных мутаций с биоматериалом третьей группы животных увеличивается в 1,5-6 раз По сравнению с остальными групйамя.
Такая же направленность возрастания частоты .индуцированных мутаций набюдалась при использовании в качестве тестируемого вторичного мутагева циклофосфана (табл.6). Как видно из таблицы,-количество мутаций при использовании биоматериала животных третьей группы достоверно увелк огвапось в 1,5-2 раза по сравнению с другими группами животных.
Таким образом, приведенные вьшё результаты показывают, что прн условии использования биоматериала от животных, содержавшихся на диете с дефицитом лизина, треонина, метно- нина и витаминов А,С и Е, обеспечивается достоверное повыйение чувствительности способа.
Формула изобретения
Способ выявления вторичных мут а- генов путем инкубации исследуемого
10
IS
вещества с микросомами печени в пр сутствии бактериальных Клеток, отд ления бактериальных клеток, посева их на селективную среду и регистра ции числа колоний мутантных клеток в сравнении с контролем, отличающийся тем, что, с целью повьшения чувствительности способа используют микросомы, выделенные и печени животных,содержащихся на дие дефицитной по незаменимым аминокисл там: лизину, треонину, метиоиину и витаминам А,С и Е не менее 1,5 мес цев.
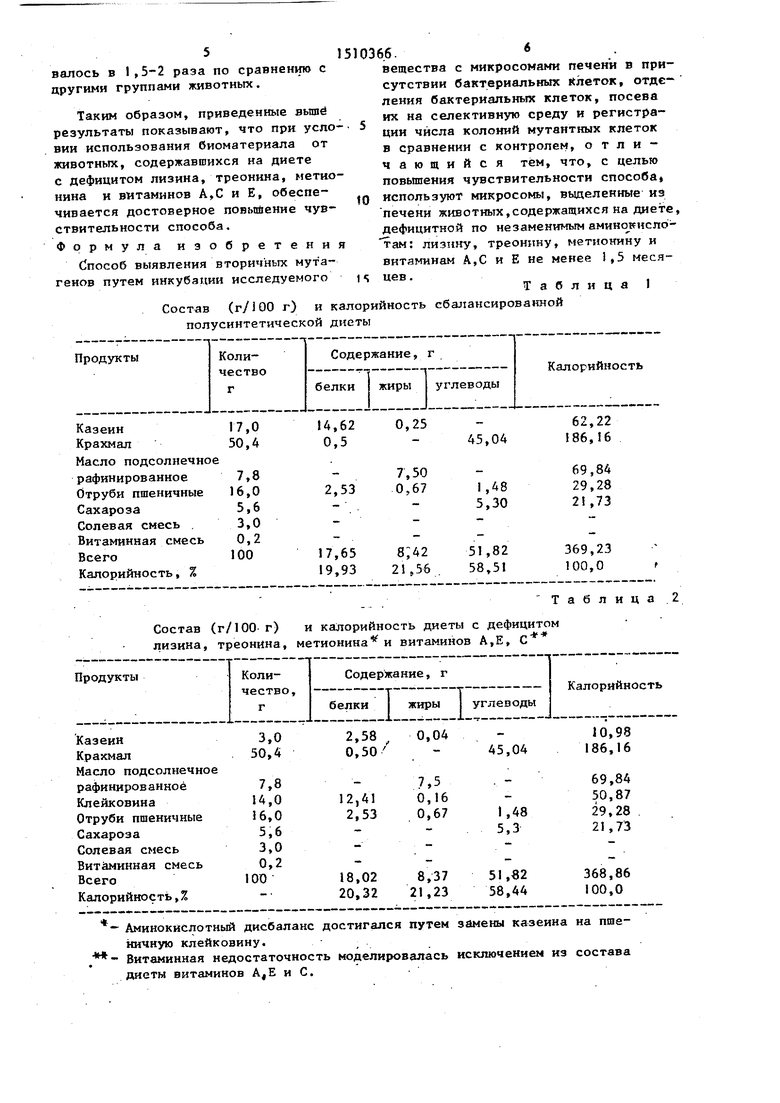
Таблица 1 Состав (г/100 г) и калорийность сбалансированной полусинтетической диеты
1510366.
вещества с микросомами печени в присутствии бактериальных Клеток, отде ления бактериальных клеток, посева их на селективную среду и регистрации числа колоний мутантных клеток в сравнении с контролем, отличающийся тем, что, с целью повьшения чувствительности способа используют микросомы, выделенные из печени животных,содержащихся на диете, дефицитной по незаменимым аминокислотам: лизину, треонину, метиоиину и витаминам А,С и Е не менее 1,5 месяцев.
Таблица 1 йность сбалансированной 


Изобрететте относится к медицине и может быть использовяно для выявления BTOptniHbrx мутагенов. ЦеЛь изобретения - повышение чувствительности способа. Цель достигается за счет использования микросом печени белых крыс, содержащихся на диете с дефицитом лизина, треонина, метионина и витаминов А, Е и С. Способ может быть использован в экспериментальной онкологии, нутрицио- логии, гигиене окружающей среды и токсикологии. 6 таол.
Состав (г/100 г) и калорийность диеты с дефицитом лизина, треонина, метионина и витаминов А,Е, С
- Аминокислотный дисбаланс достигался путем замены казеина на пшеничную клейковину.
- Витаминная недостаточность моделировалась исключением из состава диеты витаминов А,Е и С.
Таблица 2
Состав солевой смеси (мг/)00г)
Сернокислая медь1,6
Сернокислое железо19,А5
Сернокислый марганец4,3
Алгомокалиевые квасцы0,37
Йодистый калий0,16
Фтористый натрий2,03
Углекислый кальций923,7
Фосфорнокислый кальций421,05
Хлористый калий746,9
Фосфорнокислый калий421,69
Хлористый натрий308,4
Углекислый цинк1,36
Хлористый кобальт0,04 Молибденовокислый аммоний 0,01
Углекислый магний124,01
Селенит натрия0,01
Состав литдминов (мг/ЛОО г)
Мутагенная метабол1гческая активация N-нитроэоморфолина микросомами печени крыс, содержавшихся на различных диетах и инду- цированньш фенобарбиталом в дозе 80 мг/кг в течение трёх дней (за 100% принят уровень мутагенной активации Н нитрозомор- фолина при использовании микросом печени крЫс, содержавшихся на общевиварном рационе)
Питание
Частота мутаций Ю , 7,
Мутагенная метаболическая . активация циклофосфана микросомами печени крыс содержавшихся на различных диетах и индуцированных фенобарбиталом в дозе 80 мг/кг в течение трех дней (за 100% принят уровень мутагенной активации цнклофосфана при использовании микросом печени крыс, содержавшихся на общевнварном рационе)
Таблица 3
Таблица А
Таблица 5
Таблица 6
| Mutat Res., 1975, v | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
Авторы
Даты
1991-04-30—Публикация
1987-06-01—Подача