Изобретение относится к медицине, микробиологии, в частности к производству вакцинных препаратов.
Согласно требованию ВОЗ, содержание клеточной ДНК в вакцинах медицинского назначения, приготовленных на основе вирусных сборов с перевиваемых клеточных линий, жестко лимитируется величиной не более 100 пг на дозу, так как нельзя полностью исключить трансформирующей клетки и онкогенной активности такой ДНК.
Цель изобретения - упрощение способа и повышение степени очистки вирусной суспензии от клеточной ДНК путем обработки суспензии протамин сульфатом в концентрагщи 4J1 мг/мл
с последующей ее очисткой ультрацентрифугированием или гельхроматографи- ей.
Способ осуществляют следующим об- разомо
Вирус клещевого энцефалита или гепатита А, размноженный при 37 С в течение 48-72 ч или 14 сут соответственно в перевиваемой культуре клеток, пермессивной для вируса и разрешенной для вакцинного производства, концентрируют и очип(ают от балластных примесей„ Для этого используют обычно следующие последовательные процедуры: осветляющее центрифугирование при 5000-10000 xg или фильтрацию через мембранные фильтры с диаметром пор
СП
со to о СП
200-500 нм и ультрафильтрацию через мег4браны с диаметром пор 5-50 нм К полученному концентрату добавляют протамин сульфат до конечной кон- центрации 41.1 мг/мл и инкубируют в течение получаса при 4 С. Образовав- шийся преципитат удаляют центрифугированием при 4-12 Tbic.xg в течение 30 мин, Остйток клеточной ДНК и про- т-амин сульфат удаляют центрифугированием при 75 тыс о xg в течение 3 ч через 15% сахарозу или гельхроматогра- фией на сорбентах типа Сефароза 6В; 4В; CL-6fi; CL-4B или кремнезем МПС-1000П-МПС-2000П. Количество клеточной ДНК в препаратах на последовательных стадиях очистки измеряют методом точечной гибридизации о Чувствительность метода 2,5 пг/мл. В опыте для вируса клещевого энцефалита при выходе вируса порядка 90% концентрация клеточной ДНК снижается с 1-3 мкг/мл в концентрате до 200- 400 пг/мл в очищенном препарате полу фабриката, а после дополнительного разведения до согласованных уровней иммуногенности эта величина составляет менее 100 пг/мл. В случае суспензии вируса гепатита А при том же выходе антигенного материала количество клеточной ДНК снижается до 1- 90 пг/мл.
Пример 1 о Очистка суспензии вируса клещевого энцефалита от клеточной ДНК с применением протамин сульфата с последующим ультрацентрифгированием. Вакцинный штамм вируса клещевого энцефалита, размноженный в перевиваемой культуре клеток почек зеленой мартышки (4647) при 37 С в течение 72 ч объемом Зле титром инфекционных частиц Ю БОЕ/мл, осветляют центрифугированием при 10 тыс xg в течение 30 мин, фильт- руют через нитроцеллюлозные мембраны Миллипор НА и концентрируют в 20 раз на полиядерных мембранах с диметром пор 50 нм, К вирусному конценрату добавляют протамин сульфат в конечной концентрации 5 мг/мл. После инкубации в течение 30 мин при 4°С преципитат удаляют центрифугированием при 10 тыс, xg в течение 30 мин Надосадок ультрацентрифугируют в 15%-ном растворе сахарозы при 75 тыс X g в течение 3 ч. Осадок, содержащий вирус клещевого энцефалита, ре- суспендируют до исходного объема в
, д
0
5
0,1 М фосфатном буфере рН 7,4 с 0,14 М NaCl. В вирусном концентрате, а также в материале осадка определяют количество клеточной ДНК методом точечной гибридизации с ник-транс- лированной гомологичной ДНК. Содержание ДНК в препарате 200 пг/мл, а после дополнительного разведения до нужного уровня иммуногенности - от 10 до 40 пг в дозе„ Степень очистки от клеточной ДНК около 100 тыс, раз, при высоком выходе вирусного антигена - более 90% (табл,1 и 2),
Пример 2, Очистка суспензии вируса клещевого энцефалита от клеточной ДНК с применением протамин сульфата с последующей гельхроматографи- ей. Надосадок после обработки протамин сульфатом и удаления клеточной ДНК аналогично примеру 1 подвергают гельхроматографии на колонке 5x40 см, заполненной кремнеземом MIIC-2000 П, Для элюции вирусного материала используют среду 199 или 0,1 М фосфатный буфер рН 7,4 с 0,14 М NaCl, Содержание ДНК в конечном препарате 300 пг/мл или 14-57 пг в дозе после дополнительного разведения.
Пример 3, Очистка суспензии вируса клещевого энцефалита от клеточной ДНК с применением протамин сульфата в сниженной концентрации. К вирусному концентрату, полученному аналогично примеру 1, добавляют протамин сульфат в концентрации 0,5 мг/мл. После инкубации в течение 30 мин при 4 С преципитат удаляют центрифугированием при 10 тыс, xg в течение 30 мин, Дальнейщие процедуры очистки вьтолняют аналогично примеру 1. Содержание ДНК в конечном препарате 900 пг/мл или 43-170 пг в дозе после дополнительного разведения.
Пример 4, Очистка суспензии вируса гепатита А с применением протамин сульфата и последующей гельфильт- рации. Вирус гепатита А (щтамм HAS-15/4647 или Л-2424) размножают на монослое перевиваемых клеток 4647 при 37 С в течение 21 сут с еженедельной сменой среды. Суспензию инфицированных клеток (титр инфекционной активности 7,5 Ig ТкИДуд/мл: антигенный титр 1:32-64) в 0,1 М фосфатно- солевом буфере рН 7,4±0,2 (ФСБ) подвергают звуковой Обработке (3x20 с) при 14 кГц и осветляют низкоскоростг ным центрифугированием (5000 xg.
5 мин)„ Супернатант, содержащий вирус, трижды обрабатывают равным объемом охлажденного (0°) фреона-113, интерфазу дополнительно экстрагируют О,1 М ФСБ и объединяют вируссодер- жащие водные фазы. Надклеточнуто жидкость, собранную при сменах среды, концентрируют ультрафильтрацией на мембранах (РТНК фирмы Миллипор, CUiA) и полученный вирусный концентрат объединяют с указанной вируссодержа- щей водной фазой. Объединенную, вирусную суспензию обрабатывают (30 мин, А С) протамин сульфатом в конечной концентрации 3 мг/мл, осадок отделяют низкоскоростным центрифугированием (400 xg, 10 мин, 4 с), а сусперна- тант фракционируют на колонке с Сефа- розой 4В (Фармация, Швеция), Во фрак- циях с колонки определяют содержание вирусного антигена и клеточной ДНК (см, таблоЗ).
Пример 5, Очистка суспензии вируса гепатита А с применением ДНКазы, протамин сульфата и последующей гельфильтрацией. Вирусную суспензию, полученную аналогично примеру
4, обрабатывают хлороформом, продувают газообразным азотом до полного его удаления и обрабатывают (37 С, 60 мин) дезоксирибонуклеазой 1 (Серва, ФРГ) или ДНКазой из поджелудочной железы крупного рогатого скота. Дальнейшую обработку протамин сульфатом и фракционирование осуществляют аналогично примеру 4, используя для хроматографии колонку с сорбентом СМП-1М- 1000.
Формула изобретения
Способ очистки суспензии вируса от клеточной ДКК, включающий его вьфа щивание на клетках перевиваемой клеточной линии, осветление, концентрирование путем ультрафильтрации с последующей хроматографией или центрифугированием в слое сахарозы, отличающийся тем, что,.с целью упрощения способа и повьппения степени очистки вирусной суспензии от клеточной ДНК, полученный концентрат обрабатывают протамин сульфатом в конечной концентрации 4±1 мг/мл„


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ КЛЕЩЕВОГО ИЛИ ЯПОНСКОГО ЭНЦЕФАЛИТА ИЗ ВИРУСНОЙ СУСПЕНЗИИ | 1996 |
|
RU2120804C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА ГЕПАТИТА А | 2006 |
|
RU2314125C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2017 |
|
RU2678431C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2001 |
|
RU2203089C2 |
| ИНАКТИВИРОВАННАЯ ВАКЦИНА ПРОТИВ ВИРУСА ГЕПАТИТА А | 2009 |
|
RU2404804C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ ГЕПАТИТА А | 1989 |
|
SU1672635A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМБИНИРОВАННОЙ БИВАЛЕНТНОЙ, КУЛЬТУРАЛЬНОЙ, ИНАКТИВИРОВАННОЙ, КОНЦЕНТРИРОВАННОЙ, ОЧИЩЕННОЙ ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2009 |
|
RU2445117C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PC-NS3, ОБЕСПЕЧИВАЮЩАЯ ИНТЕГРАЦИЮ КОМПЛЕКСА ГЕНОВ C, PRM, E, NS1, NS2A, NS2B, NS3 ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА (ВКЭ) В ГЕНОМ ВИРУСА ОСПОВАКЦИНЫ (ВОВ) И РЕКОМБИНАНТНЫЙ ШТАММ ВИРУСА ОСПОВАКЦИНЫ, ЭКСПРЕССИРУЮЩИЙ В КЛЕТКАХ ИММУНИЗИРОВАННОГО ОРГАНИЗМА КОМПЛЕКС ГЕНОВ C, PRM, E, NS1, NS2A, NS2B, NS3 ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 1995 |
|
RU2112038C1 |
| КОМПЛЕКСНАЯ ТЕСТ-СИСТЕМА ИММУНОФЕРМЕНТНОГО АНАЛИЗА (ИФА) ДЛЯ ОПРЕДЕЛЕНИЯ УРОВНЯ АНТИТЕЛ К ВИРУСНЫМ РЕСПИРАТОРНЫМ ЗАБОЛЕВАНИЯМ КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2371726C1 |
| Иммунобиологическое средство для профилактики заболеваний, вызванных вирусом клещевого энцефалита на основе рекомбинантного вируса рода Flavivirus | 2022 |
|
RU2795800C1 |
Изобретение относится к медицине, микробиологии, в частности к производству вакцинных препаратов. Цель изобретения - упрощение способа и повышение степени очистки вирусной суспензии от клеточной ДНК. Для этого к суспензии вируса, выращенного на клетках перевиваемой клеточной линии, добавляют протамин сульфат до концентрации 4±1 мг/мл и затем удаляют образовавшийся преципитат центрифугированием, а надосадок подвергают дополнительной очистке хроматографией или ультрацентрифугированием через слой сахарозы. Итоговая концентрация клеточной ДНК в препаратах, пригодных в качестве парэнтеральных вакцин, не превышает 100 пг/мл. 3 табл.
Таблица
Влияние концентрации протамин сульфата на полноту удаления клеточной ДНК из концентрированной суспензии вируса клещевого энцефалита
1,2 1,2
900 600
400
300
т а б л и ц а
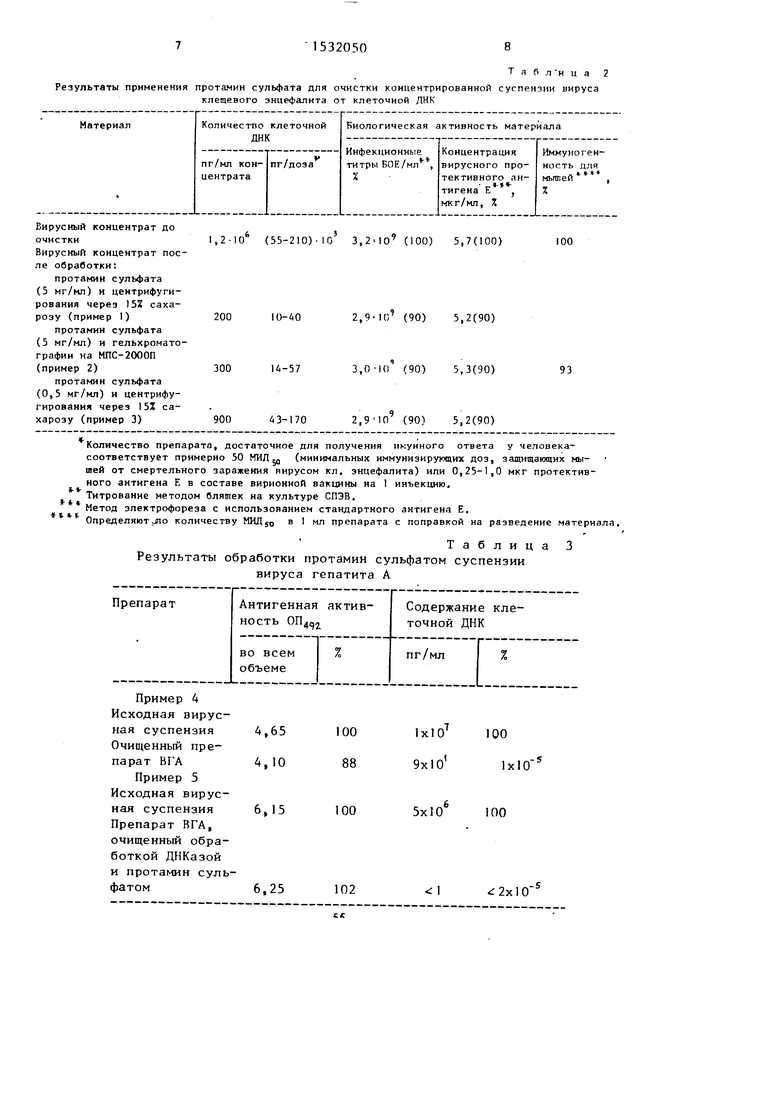
Результаты применения протамин сульфата для очистки коидентрированной суспензии вируса
клещевого энцефалита от клеточной ДНК
Вирусный концентрат до очистки
Вирусный концентрат после обработки:
протамин сульфата (5 мг/мл) и центрифугирования через 15Z сахарозу (пример 1)
протамин сульфата (5 мг/мл) и гельхромато- графии на МПС-2000П (пример 2)
протамин сульфата (0,5 мг/мл) и центрифугирования через 15Z сахарозу (пример 3)
1,2-10 (55-210) 1о 3,210 (100) 5,7(100)
200 10-iiO
300 К-57
2,9- И, (90) 5,2(90)
З.О Ю (90) 5,3(90)
900 43-170 2,910 (90) 5,2(90)
Количество препарата, достаточное для получения икунного ответа у человека- соответствубт примерно 50 МИЛ JQ (минимальных иммунизирующих доз, защищающих мышей от смертельного заражения вирусом кл, энцефалита) или 0,25-1,0 мкг протектив- ного антигена Е в составе вирионной вакцины на I инъекцию. Титрование методом бляшек на культуре СПЭВ.
Метод злектрофореза с использованием стандартного антигена Е. Определяют jjTo количеству MHfljo в 1 мл препарата с поправкой на разведение материала.
Таблица 3
Результаты обработки протамин сульфатом суспензии вируса гепатита А
tn
4,65 100 4, 10 88
6,15 100 6,25 102
100
2,9- И, (90) 5,2(90)
З.О Ю (90) 5,3(90)
93
1x10 100
9x10
1x10
-5
5x10 100
1
«::2х10
-5
| Slavik | |||
| Studies on tick-borne encephalitis virus I, Pastial purification of virus from rat broun suspensions | |||
| Acta virol | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1989-12-30—Публикация
1988-03-24—Подача