Изобретение относится к области микробиологии, медицинской биотехнологии, производству и контролю вирусных вакцин и может быть использовано при получении вакцины клещевого энцефалита (КЭ).
Клещевой энцефалит является трансмиссивным природно-очаговым антропозоонозом. Заражение человека возбудителем - вирусом клещевого энцефалита (семейство Flaviviridae) происходит при присасывании переносчика (клещей рода Ixodes). Очаги КЭ связаны с ареалом обитания иксодовых клещей и эндемичные регионы охватывают широкий пояс хвойных и смешанных лесов умеренной климатической зоны Евразии. Заболевания КЭ регистрируются от Австрии, Швейцарии, Германии, Швеции до Дальнего Востока. В связи с тем, что вирус КЭ поражает нервную ткань, в клинике КЭ в первую очередь выделяют неврологические проявления, которые могут быть очень тяжелыми - вплоть до параличей и поражений ядер ствола мозга. Летальность заболевания может доходить до 30,0% в зависимости от региона.
Для России КЭ является наиболее значимым природно-очаговым заболеванием. Именно на территории РФ циркулируют наиболее вирулентные генотипы вируса. Ежегодно сотни тысяч людей обращаются в медучреждения по поводу присасывания клеща, тысячи заболевают, а для сотен из них заболевание имеет тяжелые исходы - инвалидизация или смерть.
Наиболее эффективным способом специфической профилактики КЭ является вакцинация, которая в десятки раз снижает вероятность заболевания, предотвращает развитие тяжелых форм и осложнений и решает государственную задачу охраны здоровья населения от опасного инфекционного заболевания.
Согласно рекомендациям ВОЗ и требованиям ГФ XIII при производстве вакцин с использованием перевиваемых клеточных культур содержание ДНК клеток-продуцентов не должно превышать 10 нг на 1 дозу вакцины для исключения потенциальной возможности ее онкогенного и трансформирующего действия. Концентрация гетерогенных белков также не должна превышать установленных значений, в частности концентрация белков плазмы крови КРС, используемых при производстве вакцины, не должна превышать 50 нг/доза.
Задача, решаемая изобретением, состоит в получении высокоиммуногенной очищенной вакцины клещевого энцефалита, снижении количества и состава гетерогенных белков, снижении риска контаминации, связанного с использованием куриных эмбрионов, повышении технологичности процесса, повышении стандартности качества препарата, что в конечном итоге позволяет повысить безопасность, эффективность и стабильность препарата, сохранить здоровье населения.
Заявляемый способ получения вакцины клещевого энцефалита включает использование аттестованной культуры клеток Vero, культурального вируса КЭ в качестве посевного, концентрирования ультрафильтрацией в тангенциальном потоке и очистки эксклюзионной хроматографией на полужестких полимерных сорбентах.
Предложенный способ осуществляется следующим образом.
При подготовке посевного вируса проводят двукратное пассирование производственного штамма на культуре клеток Vero с целью удаления компонентов мозга мышей, в котором культивируют производственный штамм. Вирусный сбор (вирусную суспензию) получают путем репродукции вируса в монослойной или псевдосуспензионной культуре клеток Vero. Для увеличения репродукции добавляют глутамин, эмбриональную телячью сыворотку, другие ростовые факторы. Культивирование проводят в роллерных бутылях объемом 2-10 л или многослойных Cell-factory или иных устройствах для монослойного или псевдосуспензионного культивирования в течение 9-10 суток при температуре (37±1)°С при непрерывном перемешивании на роллерной установке со скоростью 1,0-8 об/мин (для роллерных бутылей), в зависимости от объема. Затем вирусную суспензию инактивируют формальдегидом в конечной концентрации 200±20 мкг/мл в течение 3-х суток при температуре (32±1)°С. Концентрацию инфекционного вируса в вирусной суспензии контролируют до инактивации, а инактивированную вирусную суспензию контролируют на отсутствие вирусной активности. Перед объединением культуральную среду, содержащую вирусную взвесь, обрабатывают протаминсульфатом, затем вирусный сбор центрифугируют, объединяя в общую емкость, и фильтруют для освобождения от клеточного субстрата.
Операцию проводят следующим образом.
В инактивированную вирусную суспензию добавляют 4%-ный раствор протаминсульфата до конечной концентрации 50-100 мкг/мл. Оставляют для взаимодействия при температуре (6±2)°С на 0,5-20 часов. Далее преципитат удаляют последовательным центрифугированием полуфабриката из отдельных емкостей на центрифуге при ускорении ~13000 g с последующей фильтрацией объединенного полуфабриката через пакет фильтров с конечным размером пор 0,45 мкм. Полученный таким образом объединенный полуфабрикат концентрируют в 3-30 раз ультрафильтрацией в тангенциальном потоке на мембранных или половолоконных модулях с порогом отсечения 100-300 кДа. Использование ультрафильтрационных модулей обеспечивает удаление значительной части низкомолекулярных примесей. Концентрат дополнительно очищают эксклюзионной хроматографией (гель-фильтрацией) на колонне с полужестким полимерным сорбентом, в качестве которого могут использоваться сорбенты марок Sepharose 4 Fast Flow, Sepharose 6 Fast Flow, WorkBeads 40 SEC, Toyopearl HW 65C, Toyopearl HW 55 F. Использование этого типа сорбентов позволяет повысить скорость процесса, эффективность очистки и стабильность результатов. В собираемой хроматографической фракции контролируют антигенную активность вируса клещевого энцефалита, количество общего белка, ДНК и белков КРС. Затем полученный очищенный концентрат фильтруют через фильтр с размером пор 0,22 мкм, разводят в соответствии с его антигенной активностью и используют для приготовления сорбированной вакцины. Сорбированную вакцину разливают в ампулы или флаконы и при необходимости подвергают сублимации.
Пример 1.
Вирусную суспензию получают путем репродукции вируса в монослойной культуре клеток Vero.
Производственный штамм вируса КЭ (штамм 205), хранящийся в виде мозговой суспензии, вносят в культуру клеток Vero, культивируют в течение 2-4 суток. Культуральную жидкость переносят в новую культуру клеток Vero и также культивируют 2-4 суток. Посевной вирус, прошедший два пассажа через культуру клеток, используют для заражения производственной культуры.
Для увеличения репродукции добавляют глутамин, эмбриональную телячью сыворотку в конечной концентрации 2%. Культивирование вируса проводят в роллерных бутылях объемом 2,0 л в течение 9 суток при температуре (37±1)°С при непрерывном перемешивании на роллерной установке со скоростью вращения 2 об/мин. Затем вирусную суспензию инактивируют формальдегидом в конечной концентрации 200±20 мкг/мл в течение 3-х суток при температуре (32±1)°С. Концентрацию инфекционного вируса в вирусной суспензии контролируют до инактивации. Далее освобождают от клеточного субстрата и объединяют полуфабрикат.
Операцию проводят следующим образом.
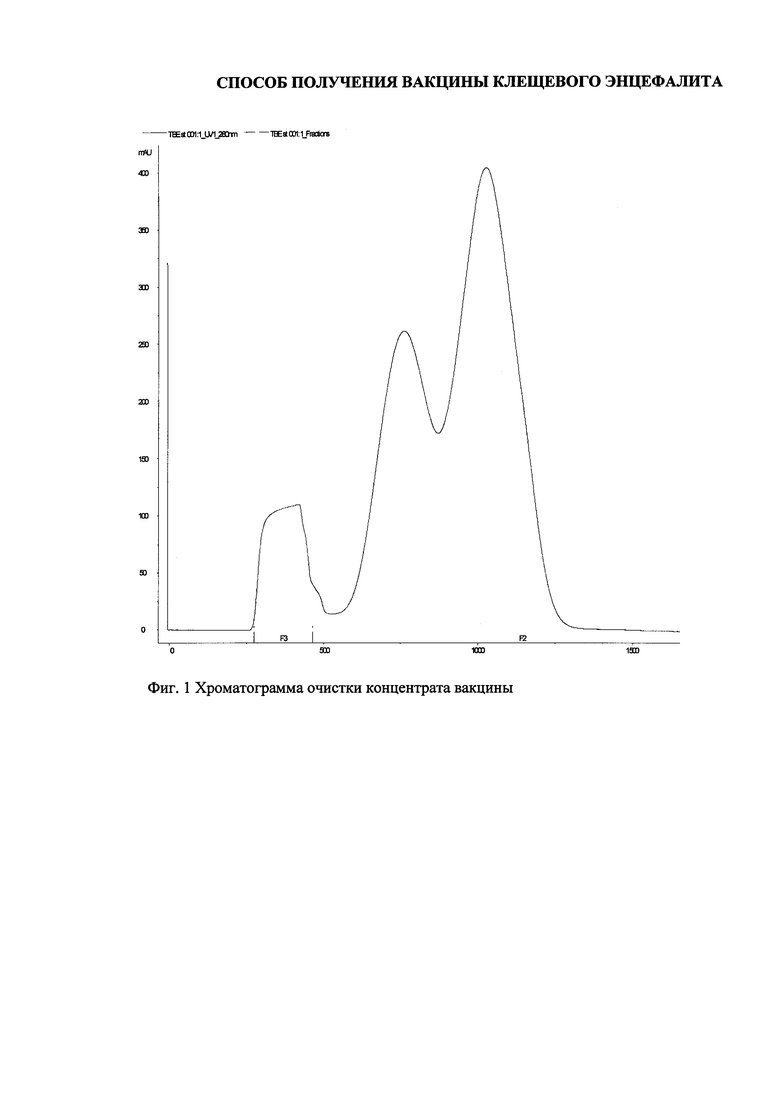
В бутыли с инактивированной культуральной средой, содержащей клеточный дебрис, вирусную взвесь, добавляют протаминсульфат до конечной концентрации 50 мкг/мл. Оставляют для взаимодействия при температуре (6+2)°С на 19 ч. Затем клеточный детрит и образовавшийся преципитат удаляют центрифугированием. Сбор поступающего с центрифуги полуфабриката производят в общую емкость, затем его фильтруют через пакет фильтров с конечным размером пор 0,45 мкм. Полученный таким образом объединенный полуфабрикат концентрируют в 10 раз ультрафильтрацией на половолоконных модулях Xampler UFP-100C- 4×2МА с порогом отсечения 100 кДа. Далее концентрат очищают эксклюзионной хроматографией на колонне с сорбентом Sepharose 6 Fast Flow (Фиг. 1).
В собираемой хроматографической фракции контролируют антигенную активность вируса клещевого энцефалита, остаточные ДНК и белки КРС. Кроме того, контролируется чистота цельновирионной фракции (Фиг. 2).
Затем полученный очищенный концентрат разводят равным количеством буферного раствора, фильтруют через фильтр с размером пор 0,22 мкм и используют для приготовления сорбированной вакцины.
Пример 2.
Вирусную суспензию получают путем репродукции вируса КЭ (штамм 205) в монослойной культуре клеток Vero. Для увеличения репродукции добавляют глутамин, эмбриональную телячью сыворотку в конечной концентрации 2%. Культивирование вируса проводят в 10-слойных Cell-factory (объем среды культивирования 2 л.) в течение 10 суток при температуре (37±1)°С при концентрации углекислоты 5%. Далее инактивацию, очистку и контроль проводят аналогично Примеру 1.
Фиг. 2 Результаты высокоэффективной жидкостной хроматографии исходного концентрата вакцины (А) и очищенного на Sepharose (Б) (колонна Protein Рас 300SW).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2001 |
|
RU2203089C2 |
| Способ получения монослойной перевиваемой линии клеток почки восточноазиатской лесной мыши Apodemus peninsulae для репродукции вируса клещевого энцефалита и производства вирусного антигена для вакцин и диагностических препаратов | 2017 |
|
RU2688327C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМБИНИРОВАННОЙ БИВАЛЕНТНОЙ, КУЛЬТУРАЛЬНОЙ, ИНАКТИВИРОВАННОЙ, КОНЦЕНТРИРОВАННОЙ, ОЧИЩЕННОЙ ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2009 |
|
RU2445117C2 |
| Способ получения четырехкомпонентной культуральной живой вакцины против кори, ветряной оспы, эпидемического паротита, краснухи | 2019 |
|
RU2717769C1 |
| ШТАММ ВИРУСА - ВОЗБУДИТЕЛЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ ПРЕПАРАТОВ (ВАРИАНТЫ) | 2009 |
|
RU2423520C1 |
| ШТАММ ВИРУСА ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ ПРЕПАРАТОВ ПРОТИВ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ (ВАРИАНТЫ) | 2018 |
|
RU2683508C1 |
| Иммунобиологическое средство для профилактики заболеваний, вызванных вирусом клещевого энцефалита на основе рекомбинантного вируса рода Flavivirus | 2022 |
|
RU2795800C1 |
| СПОСОБ ПОЛУЧЕНИЯ И АТТЕСТАЦИИ СТАНДАРТНОГО ОБРАЗЦА АНТИГЕНА ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2017 |
|
RU2667957C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 1993 |
|
RU2082432C1 |
| Штамм вируса лихорадки Синдбис 1383 клон 3 (Sindbis fever virus 1383 clone 3) | 2018 |
|
RU2720518C1 |
Изобретение относится к медицинской биотехнологии, а именно к производству и контролю вирусной вакцины клещевого энцефалита (КЭ). Для этого культуры клеток заражают штаммом 205 культурального вируса клещевого энцефалита 2-го пассажа с последующей репродукцией вируса на перевиваемой линии клеток Vero; для увеличения репродукции вируса добавляют глутамин, эмбриональную телячью сыворотку. Культивирование проводят в роллерных бутылях или клеточных фабриках, после чего вирусную суспензию инактивируют формальдегидом. Далее суспензию концентрируют на половолоконных или мембранных модулях с порогом отсечения 100-300 кДа с последующей хроматографической очисткой на полимерном сорбенте и сорбируют на адъюванте. Концентрация ДНК клеток-продуцентов в вакцине не превышает 10 нг/доза, концентрация белков плазмы крови КРС не превышает 50 нг/доза. Изобретение обеспечивает получение вакцины, которая содержит минимальное количество гетерогенных белков и обладает повышенной безопасностью, эффективностью и стабильностью. 2 з.п. ф-лы, 2 ил., 2 пр.
1. Способ получения вакцины клещевого энцефалита, характеризующийся заражением вирусом культуры клеток с последующей репродукцией и выходом вируса в культуральную среду, его инактивированием, очисткой и сорбцией на адъюванте, включающий репродукцию вируса клещевого энцефалита на перевиваемой линии клеток Vero; использование в качестве посевного вируса культурального вируса штамма 205 вируса клещевого энцефалита 2-го пассажа; добавление глутамина, эмбриональной телячьей сыворотки для увеличения репродукции вируса; культивирование в роллерных бутылях при постоянной скорости вращения 1-8 об/мин; инактивацию вирусной суспензии формальдегидом; концентрирование с использованием половолоконных или мембранных модулей с порогом отсечения 100-300 кДа и очистку концентрированного вируса хроматографией на полимерном сорбенте.
2. Способ по п. 1, отличающийся тем, что культивирование проводят в клеточных фабриках при контролируемом 5% содержании углекислого газа.
3. Способ по пп. 1, 2, отличающийся тем, что для очистки эксклюзионной хроматографией используют сорбенты на основе сефарозы (Sepharose).
| Способ получения вакцины против клещевого энцефалита | 1985 |
|
SU1349757A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2001 |
|
RU2203089C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 1993 |
|
RU2082432C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА НА ОСНОВЕ РАСТВОРИМОГО АНТИГЕНА | 1994 |
|
RU2084242C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВИРИОННОГО АНТИГЕНА ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2009 |
|
RU2402606C1 |
| БИЛАЛОВА Г.П | |||
| и др | |||
| История производства вакцин для профилактики клещевого энцефалита в г | |||
| Томске: от мозговой вакцины до вакцины энцевир, Бюллетень СО РАМН, 2007, 4б 126, стр | |||
| Транспортер для перевозки товарных вагонов по трамвайным путям | 1919 |
|
SU105A1 |
| КОРОЧКИН Р.Б | |||
| Культивирование вирусов в культурах клеток, Витебск, ВГАВМ, 2010, стр | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| LIU Y.-S | |||
| et al | |||
| Preparation of inactivated tick-borne encephalitis vaccine (Vero cells) by using basket bioreactor, Chinese Journal of Biologicals, 2015, 28, 12, pp | |||
| Рельсовая двусторонняя педаль | 1917 |
|
SU1324A1 |
| МОРОЗОВА О.В | |||
| и др | |||
| Динамика репродукции вируса клещевого энцефалита в культурах клеток | |||
| Вопросы вирусологии, 2012, 57, 2 стр | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| SEPHAROSE, INSTRUCTIONS, Amresham Bioscience, 2015, pp | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| МАЙБОРОДА А | |||
| Б | |||
| и др | |||
| Половолоконная мембрана из поливинилиденфторида и ее применение для очистки природных вод, Мембраны и мембранные технологии", 2014, 4, 1, стр | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2019-01-29—Публикация
2017-09-25—Подача