Изобретение относится к химической технологии неорганических веществ и может быть использовано для получения диоксида хлорида в целлюлозно-бумажной промьпиленности в качестве отбеливателя целлюлозы, хлопка, обеззараживания воды.
Цепью изобр етения является упрощение процесса за счет исключения выбросов реакционной смеси, связанных со снижением каталитической активности катализатора.
Пример 1 о В колбу помещают 60 мл хлорат-хлоридного раствора, нагревают до 60-80°С в присутствии
катализатора - соли кобальта (СоС.), взятой в количестве 0,01-1,0% от веса хлората натрия Постепенно приливают 25 мл 65%-ной серной кислоты при давлении 200-250 мм рт. ст. абс. При этом через реакционную смесь бар- ботируют воздух, который удаляет из реактора целевой продукт - диоксид хлора а Время проведения опыта 60 мин, температура 77°С, соотношение хлората натрия к хлориду натрия 1,65:1. Пример 2оВ условиях примера 1 в той же реакционной смеси. Оставшейся от опыта 1, без добавления свежего катализатора проводят
сд со .4
со СП
процесс получения диоксида хлора путем взаимодействия свежей павески NaClOj с Nad. Целевой продукт удал .ют из реактора путем его отдувки воздухом.
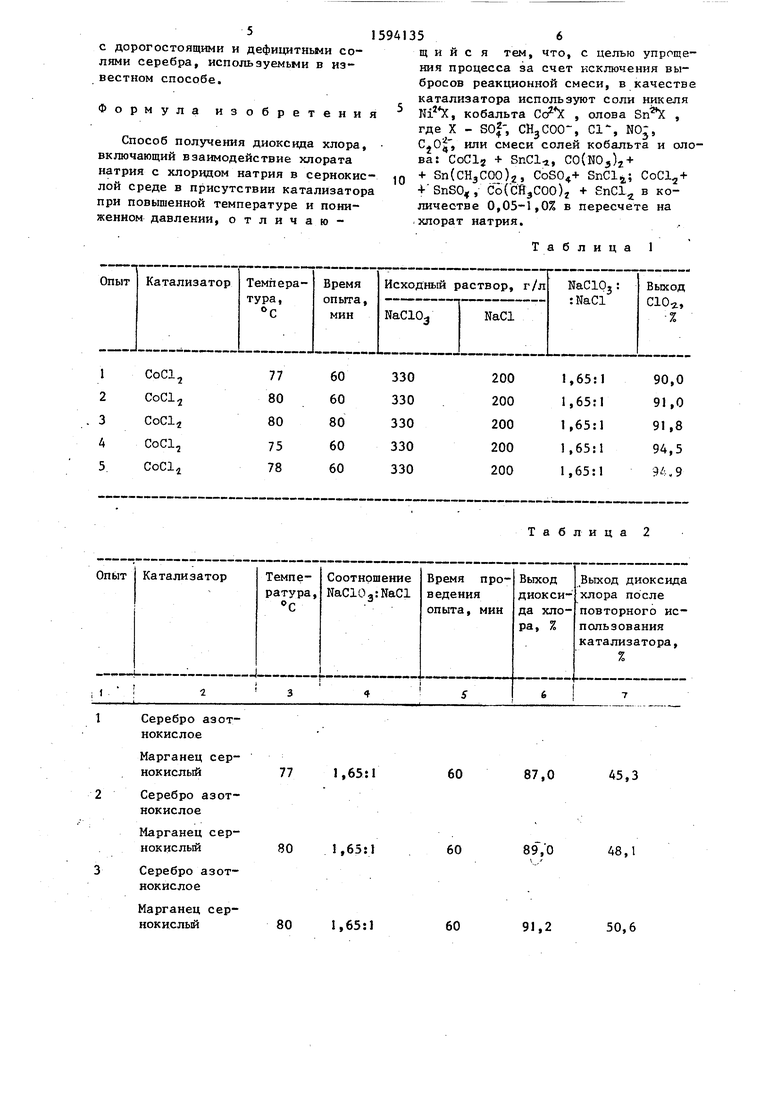
Результаты опыта представлены в табЛо 1.
Из данных, приведенных в табл« 1 видно, что процесс без добавления свежего катализатора протекает так же, как и в опыте 1 о Это свидетельствует об отсутствии снижения каталитической активности солей кобальта в хде их рециркулирования и проведения процесса.
ПримерЗ. В условиях примеров 1,2 проводят процесс получения диоксида хлора в присутствии катализатора - солей серебра и марган- ца, по известному способу.
Под.ачу катализаторов проводят по отдельности растворов азотнокислого серебра и затем сульфата марганца. Рекомендуется никогда не смешивать оба раствора до их ввода в реактор, чтобы не осадить нерастворимую соль серебра. Такое условие вносит определенные трудности в технологию получения диоксида хлора.
После израсходования хлората натрия и хлорида натрия проводят процесс получения диоксида хлора путём добавления свежей навески хлората натрия и хлорида натрия без добавления свежего катализатора - солей серебра и марганца.
Условия примера 3 и результаты опыта приведены в табл. 2,
При повторном проведении реакции путем введения свежих реагентов каталитическая смесь теряет свою активность и выход хлора падает с 87-96,3 до 45,3-58, Uo
Снижение-выхода диоксида хлора до 45% может происходить при проведении одного цикла процесса. Это обусловлено частичной дезактивацией катализатора. -Добавление свежеприготовленного катализатора вызьшает бурное выделение из жидкой реакционной смеси газообразного продукта диоксида хлора и сопровождается силными вскипаниями, выбросами и взрывами в реакторе.
Сущность предлагаемого способа заключается в том, что при получении диоксида хлора в качестве катализатора используют соли никеля , кобальта и олова Sn,
где X - CHjCoo-, CI-;NO;,
или их смеси, взятые в количестве 0,05-1,0% в пересчете на хлорат натрия, которые не снижают своей каталитической активности и могут быть рециркулируемы., Кроме того, смесь указанных катализаторов обладает
Q синергетическим характером и вызывает значительный при использовании в меньшем количестве, чем соли кобальта, никеля или олова, взятых отдельно друг от друга.
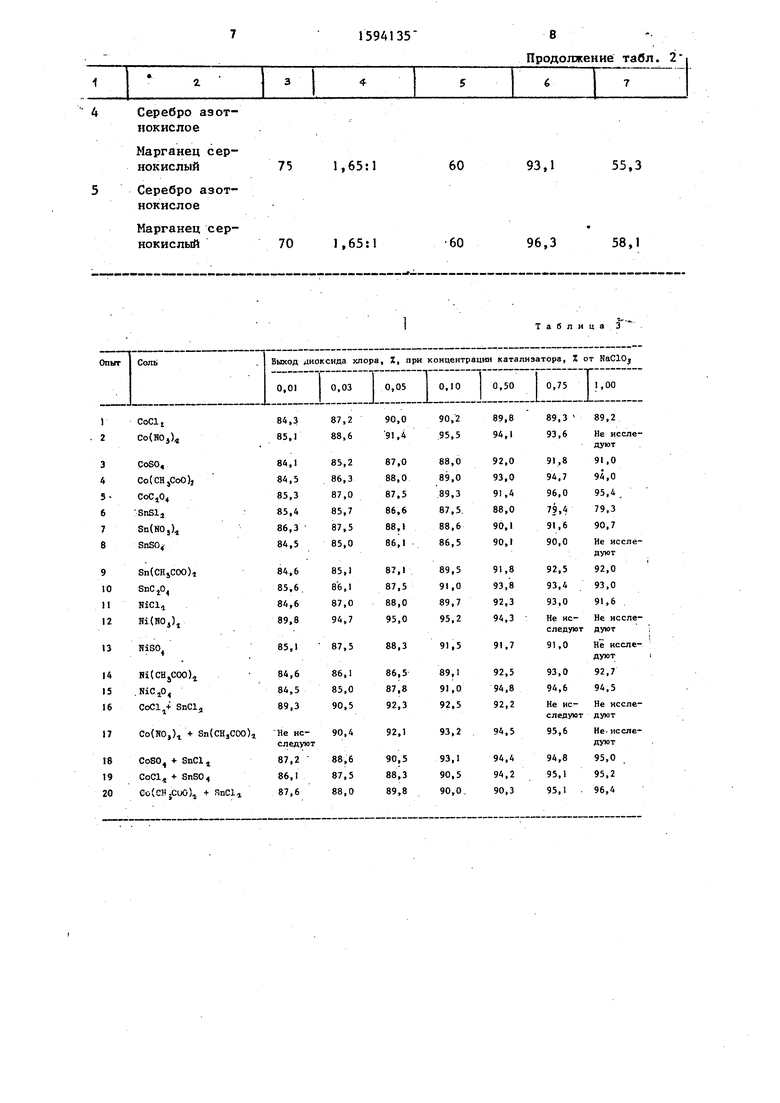
f В табл. 3 представлены данные по выходу диоксида хлора в присутствии предлагаемых катализаторов и их смесей в интервале концентраций 0,01- 1,0% от количества хлората натрия,
Из данных, приведенных в табл. 3, видно, что в присутствии 0,05% катализатора выход диоксида хлорида минимален и составляет 86,1-90,0%. Максимального значения, равного 96,4%,
5 выход диоксида хлора достигает при концентрации катализатора, равной 1%, в присутствии 0,75% катализатора выход продукта составляет 94,7%, что незначительно ниже, чем в присутствии 1% катализатора. Оптимальным количеством следует считать концентрацию катализатора 0,5-0,75%,
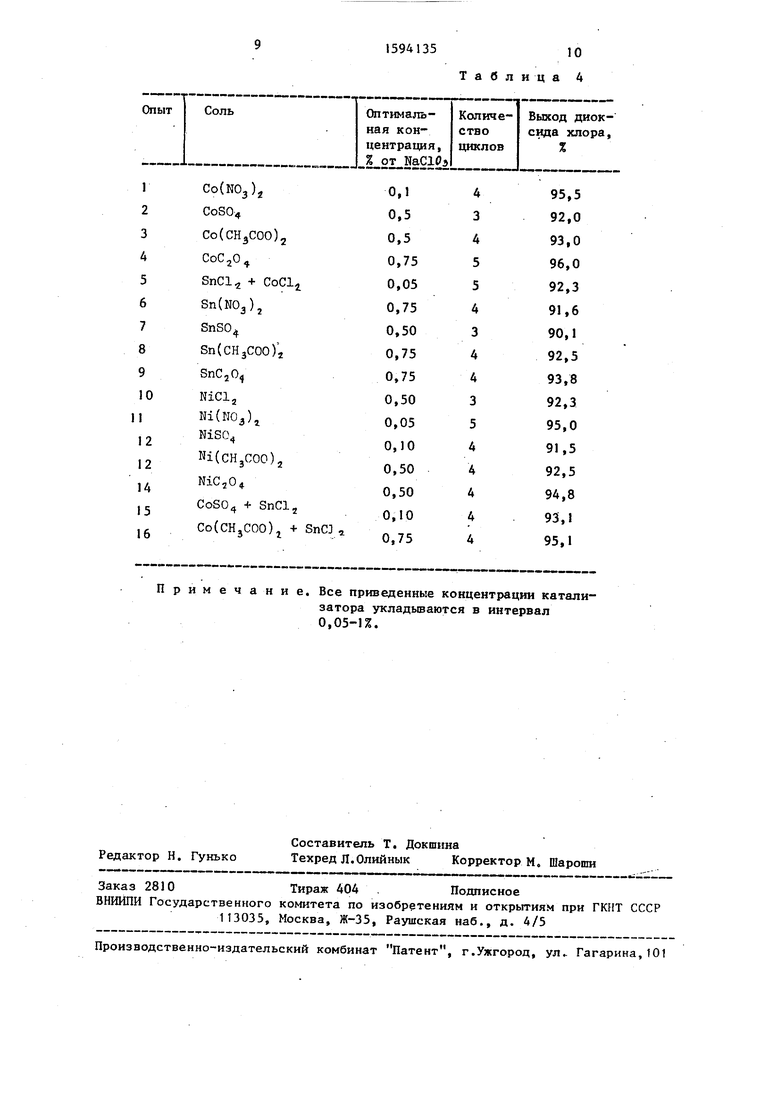
Б табло 4 представлены результаты по выходу диоксида хлора при многократном использовании катализаторов,
5 Таким образом, предлагаемый способ позволяет получать диоксид хлора с выходом 86,6-96,0% при неоднократном использовании катализатора в интервале 0,05-1,0% в пересчете
О на хлорат натрия, в то время как по известному способу выход диоксида, хлора снижается с 87,0-96,3 до 4,5,3- 58,1% при повторном его использовании,
5 Преимуществом предлагаемого способа по сравнению с известным является -упрощение процесса получения диоксида хлора, поскольку применение предлагаемых катализаторов позволяет
0 исключить взрьшы и выбросы реакционной смеси, происходящие в известном способе при добавлении свежих порций катализатора, в то время, когда выход диоксида хлора снижается до 45%.
5 При этом в качестве катализатора в предлагаемом способе иллюстрируются более доступные и дешевые соли никеля, кобальта и олова по сравнению
0
с дорогостоящими и дефицитньми солями серебра, испольэуемьми в известном способе.
Формула изоб
р е т е н и я
Способ получения диоксида хлора, включающий взаимодействие хлората натрия с хлорвдом натрия в сернокислой среде в присутствии катализатора при повышенной температуре и пониженном давлении, отличаю
5941356
щ и и с я тем, что, с целью упрощения процесса за счет исключения выбросов реакционной смеси, в качестве катализатора используют соли никеля , кобальта , олова Sn ,
где X - SOJ-, CHjCOO-, Cl, NO , , или смеси солей кобальта и олова: CoClj + SnCl-i, СО(КОз)2 + Q + 5п(СНзСОО)2, CoS04+ SnClj,; 0001 + t- SnSO, Со(СЙэСОО)г + SnCl, в количестве О,05-1, хлорат натрия.
в пересчете на

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения двуокиси хлора | 1988 |
|
SU1776251A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУОКИСИ ХЛОРА | 1991 |
|
RU2069167C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА ХЛОРА (ВАРИАНТЫ) | 1992 |
|
RU2104247C1 |
| Способ получения диоксида хлора и хлора | 1979 |
|
SU1181527A3 |
| ЭЛЕКТРОД | 2008 |
|
RU2487197C2 |
| Способ очистки раствора от органических примесей | 1982 |
|
SU1112000A1 |
| СПОСОБ ПОЛУЧЕНИЯ УКСУСНОЙ КИСЛОТЫ | 1999 |
|
RU2233832C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ ГЕТЕРОГЕННЫХ РЕАКЦИЙ | 2005 |
|
RU2292950C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА, КАТАЛИЗАТОР И СПОСОБЫ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 1998 |
|
RU2150322C1 |
| КАТАЛИЗАТОР ДЛЯ ПРОИЗВОДСТВА ЭТАНОЛА ПУТЕМ ГИДРОГЕНИЗАЦИИ УКСУСНОЙ КИСЛОТЫ, СОДЕРЖАЩИЙ ПЛАТИНУ-ОЛОВО НА КРЕМНЕЗЕМНОЙ ПОДЛОЖКЕ | 2010 |
|
RU2549893C2 |
Изобретение относится к химической технологии неорганических веществ и может быть использовано для получения диоксида хлора в целлюлозно-бумажной промышленности в качестве отбеливателя целлюлозы, хлопка, обеззараживания воды и позволяет создать возможность для образования диоксида хлора с высоким выходом, исключив выбросы реакционной смеси, связанные с дезактивацией катализатора. Способ осуществляют взаимодействием хлората натрия с хлоридом натрия в сернокислой среде в присутствии катализатора при повышенной температуре и пониженном давлении. В качестве катализатора используют соли никеля NI 2+X, кобальта CO 2+X, олова SN 2+X, где X - SO 2--CH 3COO -,CI -,NO 3,C 2O 2- или смеси солей кобальта и олова: CO/NO 3/ 2+SN/CH 3COO/ 2,CO SO 4+CUCL 2,COCL 2+SNSO 4 CO/CH 3COO/ 2+SNL в количестве 0,05-1,0% в пересчете на хлорат натрия. Предложенный способ позволяет получать диоксид хлора с выходом 86,6-96,0% при неоднократном использовании катализатора. 4 табл.
Серебро азотнокислое
Марганец сернокислый
Серебро азотнокислое
Марганец сер- нокисльй
Серебро азотнокислое
Марганец сернокислый
77
80
1,65:1
1,65:1
80 1,65:1
Таблица 1
Таблица 2
60
87,0
А5,3
60
89,0
48,1
60
91,2
50,6
751,65:1
701,65:1
Опыт Соль
CoCli
Co(HOj)
CoSO,
Co(CHjCoO)j
CoCi04
SnSlj
SntHOj),,
SnSO,:
Sn(CHsCOO),
SnCjO,
HiCl
Hi(HOj)j
NiSO
HKCHjCOO)
.NiCjO,
SnClj
Co(TO,) + Sn(CHjCOO)i
CoSO, SnClt
CoClj + SnS04
Со(С 5СиО)г. + RnCla
60
93,1
55,3
60
96,3
58,1
.
Таблица 3
Примечание. Все приведенные концентрации катализатора укладьшаются в интервал 0,05-1%.
159413510
Таблица 4
| Патент США № 3363702, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1990-09-23—Публикация
1988-02-29—Подача