Изобретение относится к способам биохимического анализа и может быть использовано для определения перекиси водорода в биологических образцах.
Цель изобретения - повышение чувствительности способа при одновременной возможности осуществления способа в присутствии гемсодержащих пигментов.
Способ осуществляется следующим образом.
К исследуемой пробе добавляют буферный раствор, пероксидазу и в качестве хромогена смесь гваякола и п-ами- нодиэтиланилина при концентрации каждого компонента 0,05-0,5 М. Пробу инкубируют до прекращения увеличения
оптической плотности и спектрофото- метрируют против контрольной пробы, не содержащей перекиси водорода. По величине оптической плотности определяют содержание перекиси водорода.
Пример 1. Анализ перекиси водорода в растворах.
К 10-2000 мкл анализируемой пробы, содержащей 10-500 нмоль Н20г, прибавляют 400 мкл 0,5 М фосфатного буфера, рН 7,0-7,5, 400 мкл 2 мМ гваякола и 400 мкл 2 мМ сульфата n-аминодиэтиланилина (или дигидро- хлорида п-аминодиметиланилина). Объем проб доводят до 3,8 мл водой. Реакцию начинают прибавлением 200 мл 0,1%-ного раствора перексидазы хрена и через 5 мин (можно и через
о со оэ i i ю
5-30 мин) измеряют оптическую плотность растворов при 625 нм на спектрофотометре или при 670 нм на фото- электроколориметре КФК-2МП против контроля, содержащего вместо перекиси водорода воду. Содержание в исходной пробе определяют по калибровочному графику по следующей формуле, мМ: ,J
г - , С-,
где п - разведение исходной пробы
перед введением в инкубиру- ему смесьJ
V - объем вносимой пробы, мл;
D - оптическая плотность раствора против контрольного, не содержащего FLO,:
k - коэффициент для , нахо- димый из калибровочного опыта (обычно в описанных условиях для фотоэлектроколоримет- ра КФК-2МП он равен 0,35). Пример 1. Исходную пробу, ,одержащую , развели в 100 раз. Для анализа взяли 0,1 мл. Оптическая плотность фотометрируемого раствора составила 0,210 (ФЭК КФК-2МП, 670 нм , 1 см). Калибровочный коэффициент (т.е количество микромолей Н,0г в 4 мл пробы, соответствующей оптической плотности 1) для данных условий равен 0,35.
Следовательно, исходная концентра- ция равна С 73,5 мМ.
Пример 2. Анализ перекиси водорода, генерируемой в оксидаз- ной реакции (метод определения активности оксидаз).
А. Определение активности алкоголь оксидазы. К анализируемой пробе (5- 100 мкг белка) прибавляют 400 мкл 0,5 М фосфатного буфера, «рН 7,0-7,5, 400 мкл 2 мМ гваякола, 400 мкл 2 мМ сульфата n-аминодиэтиланилина (или дихлоргидрата п-аминодиметиланилина), 400 мкл 100 мМ метанола, объем пробы доводят до 3,8 мл водой. Реакцию начинают прибавлением 200 мкл 0,1%-ной пероксидазы хрена (Реанал RZ 0,6) и через 30 с измеряют приращение оптической плотности за 1 мин при 670 нм фотоэлектрокалориметра КФК-2МП в режиме Активность. Удельную актив- ность фермента (генерируемой перекиси водорода за 1 мин на 1 мг белка) рассчитывают по формуле, мкмоль:
Q
5
5
Л
и О 5
40
0 5
45
А ;&Р/мин . k- n
где ДБ/мин - приращение оптической
плотности за 1 мин; п - разведение раствора
фермента перед прибавлением реагентов; V - объем раствора фермента, вводимого в пробу, мл
Сй - исходная концентрация белка, мг/мл; k - коэффициент для , находимый из калибровочных опытов, (Б описанных условиях он равен 0,35).
Исходную пробу бесклеточного экстракта метилотрофных дрожжей, содержащего алкогольоксидазу, развели в 100 раз. Концентрация белка в исходном экстракте 5,5 мг/мл. Для анализа взяли 0,2 мл. Приращение оптической плотности за 1 мин составило 0,125 (ФЭК КФК-2МП-, 670 нм; 1 см). Калибровочный коэффициент в данных условиях равен 0,35. Следовательно, удельная активность алкогольоксида- зы в исходном экстракте равна А 3,98 мкмоль/мин мг белка.
Б. Определение активности глюкозо- оксидазы. Анализ и расчет проводят точно так же, как в примере 2А с той лишь разницей, что вместо метанола используют 100 мМ глюкозы, а в качестве буфера используют 0,5 М цитрат-NaOH, рН 6,0.
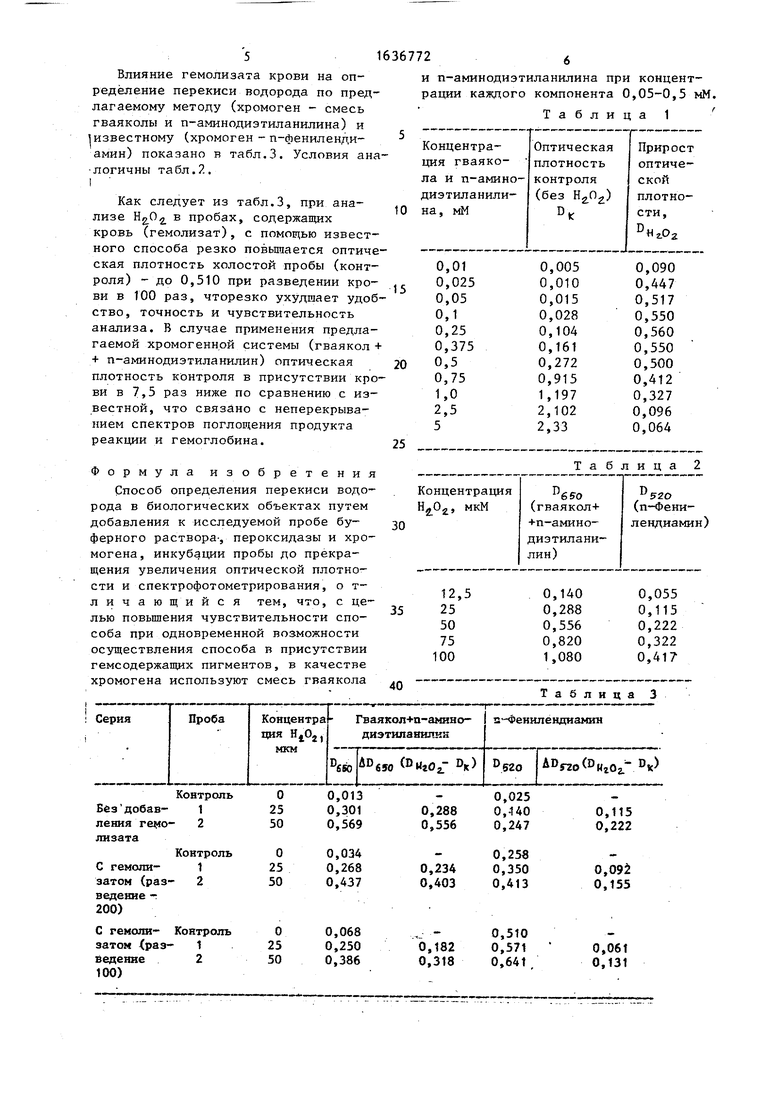
Граничные значения концентрации хромогенов (концентрация HgOj, 50 мкМ) предлагаемого способа сведены в табл.1.
Чувствительность предлагаемого способа повысилась в 2,5 раза.
В табл.2 дано сравнение чувствительности определения перекиси водорода по предлагаемому методу (хромоген - смесь гваяколы и п-аминодиэти- ланилина) и известному (хромоген - п-фенилендиамин). Условия: 50 мМ фосфатный буфер, рН 7,0-, концентрация хромогенов 0,25 мМ$ пероксидазы хрена (RZ 0,6) 0,05 мг/мл. Спектрофотометр СФ-26, 1 см.
Возможно определение перекиси водорода в присутствии гемсодержащих пигментов, в частности гемоглобина крови.
516
Влияние гемолизата крови на определение перекиси водорода по предлагаемому методу (хромоген - смесь гваяколы и n-аминодиэтиланилина) и 1 известному (хромоген - п-фениленди- амин) показано в табл.3. Условия аналогичны табл...
и n-аминодиэтиланилина при концентрации каждого компонента 0,05-0,5 мМ.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения пироксидазной активности биологических объектов | 1988 |
|
SU1636773A1 |
| Способ определения антигена в растворе | 1989 |
|
SU1718119A1 |
| РЕАКТИВ ДЛЯ ОПРЕДЕЛЕНИЯ ГЛЮКОЗЫ В БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1991 |
|
RU2009499C1 |
| СПОСОБ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ НИТРИТОВ В ЖИДКОЙ СРЕДЕ | 2004 |
|
RU2265828C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕМОГЛОБИНА В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2005 |
|
RU2300771C2 |
| НАБОР ДЛЯ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АВЕРМЕКТИНОВ МЕТОДОМ ОДНОСТАДИЙНОГО КОНКУРЕНТНОГО ИММУНОФЕРМЕНТНОГО АНАЛИЗА | 2009 |
|
RU2416094C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ОСНОВНОГО БЕЛКА ТЕПЛОВОГО ШОКА 70 КДА | 2003 |
|
RU2242764C1 |
| Способ определения качества молока с помощью тест-полоски | 2023 |
|
RU2827713C1 |
| РЕКОМБИНАНТНАЯ ДНК pA3, РЕКОМБИНАНТНАЯ ДНК pQE 30-pA3, ОБЕСПЕЧИВАЮЩИЕ ПОЛУЧЕНИЕ ПОЛИПЕПТИДА A3, ШТАММ E. coli М 15-A3, ТРАНСФОРМИРОВАННЫЙ РЕКОМБИНАНТНОЙ ПЛАЗМИДНОЙ ДНК pQE 30-pA3 И ЭКСПРЕССИРУЮЩИЙ РЕКОМБИНАНТНЫЙ ПОЛИПЕПТИД A3, РЕКОМБИНАНТНЫЙ ПОЛИПЕПТИД A3, ОБЛАДАЮЩИЙ СПОСОБНОСТЬЮ СЕЛЕКТИВНО СВЯЗЫВАТЬ ЧСА, И ТЕСТ-СИСТЕМА РФА ДЛЯ КАЧЕСТВЕННОГО ВЫЯВЛЕНИЯ МИКРОАЛЬБУМИНУРИИ, ТЕСТ-СИСТЕМА ДЛЯ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МИКРОАЛЬБУМИНУРИИ | 2013 |
|
RU2550255C2 |
| Способ определения активности пероксидазы | 1983 |
|
SU1167502A1 |
Изобретение относится к способам биохимического анализа и может быть использовано для определения перекиси водорода в биологических образцах и системах, генерирующих . Цель изобретения - повышение чувствительности способа при одновременной возможности осуществления способа в присутствии гемсодержащих пигментов. К исследуемой пробе добавляют буферный раствор, пероксидазу, а также смесь гваякола и п- аминодиэтиланилина при концентрации каждого компонента 0,05-0,5 мМ. Пробу инкубируют до прекращения увеличения оптической плотности и спектро- фотометрируют против контрольной пробы, не содержащей перекиси водорода. По величине оптической плотности определяют содержание перекиси водорода. Способ позволяет повысить чувствительность в 2,5 раза. 2 табл. с 5S (Л
Как следует из табл.3, при анализе в пробах, содержащих кровь (гемолизат), с помощью известного способа резко повышается оптическая плотность холостой пробы (контроля) - до 0,510 при разведении крови в 100 раз, чторезко ухудшает удобство, точность и чувствительность анализа. В случае применения предлагаемой хромогенной системы (гваякол + + n-аминодиэтиланилин) оптическая плотность контроля в присутствии крови в 7,5 раз ниже по сравнению с известной, что связано с неперекрыванием спектров поглощения продукта реакции и гемоглобина.
10
0,01
0,025
0,05
0,1
0,25
0,375
0,5
0,75
1,0
2,5
5
25
| Portsmann В,, Portsmann Т., Nagel Е | |||
| - Clin.Chem | |||
| Clin | |||
| Biochem, 1981, v.19, p.435-439. |
Авторы
Даты
1991-03-23—Публикация
1988-01-13—Подача