С/
с


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выделения сфингомиелина | 1983 |
|
SU1133275A1 |
| СПОСОБ ДИАГНОСТИКИ ОСТРОГО ТОКСИЧЕСКОГО ПОВРЕЖДЕНИЯ ПЕЧЕНИ | 2012 |
|
RU2527770C2 |
| Способ диагностики диффузного гломерулонефрита | 1979 |
|
SU924572A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОПОЛИСАХАРИДНОЙ КОМПОЗИЦИИ, СОДЕРЖАЩЕЙ ЛИПИД А, ЛИПОПОЛИСАХАРИДНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЛИПИД А, 3-O-ДЕЗАКТИВИРОВАННЫЙ 4`-МОНОФОСФОРИЛЛИПИД А | 2002 |
|
RU2302463C2 |
| АДЪЮВАНТНАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ 3-О-ДЕАЦИЛИРОВАННЫЙ 4′-МОНОФОСФОРИЛЛИПИД А | 2006 |
|
RU2427378C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА У НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ | 2005 |
|
RU2291445C1 |
| СПОСОБ ДИАГНОСТИКИ НЕЙРОСИФИЛИСА | 2003 |
|
RU2230323C1 |
| Способ антенатальной диагностики гипотрофии плода | 1981 |
|
SU971274A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЕРОКСИДОВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2005 |
|
RU2293334C2 |
| Способ измерения массовой концентрации метиловых эфиров жирных кислот в биологических средах методом газожидкостной хроматографии | 2020 |
|
RU2758932C1 |
Изобретение относится к биологической химии и медицине. Цель изобретения - упрощение способа. Цель достигается гидролизом упаренного липидного экстракта 0,1 - 0,2 N NAOH в метаноле в течение 0,5 - 4 ч, удалением продуктов гидролиза путем встряхивания с водой и хлороформом с последующим измерением содержания сфингомиелина. Сравнение способа со способом двухмерной тонкослойной хроматографии показало его высокую точность - 98 - 99%. Способ позволяет проводить определение уровня сфингомиелина без использования дорогостоящего оборудования и реактивов, что дает возможность использования его как в биохимической практике, так и в медицине при диагностике респираторного дистресс-синдрома новорожденных. 5 табл.
Изобретение относится к биологической химии, а именно к способам определения концентрации фосфолипида - сфингомиелина, и может быть использовано для,антенатальной диагностики развития респираторного дистресс-синдрома (РДС) у новорожденных, когда для определения степени зрелости легких плода измеряется отношение лецитин (сфингомиелин или гли- церофосфатиды) - сфингомиелин в амнио- тической жидкости. Кроме того, способ может быть использован в биохимических исследованиях, связанных с диагностикой и патогенезом различных нарушений липид- ного обмена.
Цель изобретения -упрощение способа при массовых анализах за счет сокращения стадий.
Цель достигается тем, что упаренный в вакууме липидный экстракт, соответствующий 0,5 мл сыворотки крови или 1,5 мл ам- ниотической жидкости подвергают мягкому щелочному гидролизу 0,1-0,2 н,МаОН в метаноле в течение 0,5-4,0 ч, после чего продукты гидролиза разделяют путем встряхивания в смеси с водой с хлороформом с последующим отстаиванием. При этом в водную фазу уходят продукты гидролиза глицерофосфатидов, а устойчивый к щелочному гидролизу сфингомиелин остается в нижней органической фазе. После разделения фаз количество сфингомиелина определяют с помощью любого метода определения фосфолипидов. Упаривание липидного экстракта осуществляют в вакууме при 40-50°С, гидролиз проводят при концентрации NaOH ( 0,1-0,2 н, вместо 1н.в известном способе), при несколько большей
о о ее сг сг
,ь
температуре, 42-48°С. Для разделения продуктов гидролиза используют хлорофор- мы - метанол - вода в соотношении (2:1:0,6).
Пример 1. Определение содержания сфингомиелина в амниотической жидкости, 1,5 мл амниотической жидкости помещают втриобьема смеси хлороформ:метанол (2:1) и экстрагируют липиды. Экстракт липидов концентрируют путем упаривания в вакууме при 45°С (на роторном испарителе или в колбе с нисходящим холодильником) или в широкой пробирке на водяной бане при 50-60°С небольшими порциями, затем переносят в пробирки, снабженные завинчивающимися крышками с прокладками типа Ругех США и быстро упаривают досуха на водяной бане (гидролиз можно проводить в колбе с обратным холодильником).
Осадок липидов растворяют в 2,0 мл метанола, добавляют 0,2 мл 1н. водного NaOH и инкубируют на водяной бане при 45°С 2 ч с периодическим встряхиванием. После гидролиза в пробирку добавляют4 мл хлороформа и 1,2 мл воды (соотношение хлороформ:метанол:вода взято согласно Фолчу), пробирку энергично встряхивают и после отстаивания отделяют нижнюю фазу. Параллельно равные аликвоты липид- ного экстракта используют для определения сфингомиелина по известному способу, а также при помощи ТСХ (прототип).
Для проверки полноты гидролиза гли- церофосфатидов после гидролиза по предлагаемому способу из содержащей сфингомиелин нижней фазы следовые количества (2-3 мкл) наносят на пластинку с тонким слоем силикагеля и хроматографируют в системе хлороформ:метанол:вода 65:25:4. При этом экстракт после гидролиза по предлагаемому методу содержит только одно пятно сфингомиелина, в то время как после гидролиза по известному способу над пятном сфингомиелина было отчетливое пягно лецитина, составляющее до 50% от исходного его содержания. Это указывало на неполное расщепление лецитина в процессе гидролиза в условиях известного способа.
Для определения количества непрогид- ролизовавшихся фосфолипидов .нижнюю 6aav после гидролиза согласно обоим способам переносят количественно в огнеупорные пробирки, упаривают растворитель досуха на водяной бане и определяют содержание фосфолипидов. Параллельно проводят то же определение для содержащей сфингомиелин зоны силикагеля после ТСХ. Результаты приведены в табл. 1. Как видно из табл. 1, результаты определения сфингоммелинз согласно предлагаемому способу почти совпадают с полученными при помощи классического способа с использованием ТСХ (расхождение 2-5%), в то время как определение согласно извест- ному способу дает грубое завышение (в 1,2-2,2 раза) за счет неполного гидролиза глицерофосфатидов.
С целью расчета точности предлагаемого способа проводят опредение сфингомие- 0 лина согласно этому способу в амниотической жидкости 55 женщин при сроке беременности 28-40 нед.
Результаты приведены в табл. 2. Приведенные результаты статистиче- 5 ски подтверждают отсутствие различий в определении сфингомиелина с. помощью точного, но громоздкого метода, использующего ТСХ, и предлагаемого гидролитическо- 0 го способа.
Пример 2. Определение содержания сфингомиелина в сыворотке крови.
0,05 мл сыворотки крови добавляют к 10 мл хлороформа-метанола (2:1) и экстрагиру- 5 ют липиды.
Экстракт упаривают, подвергают гидролизу и определяют непрогидролизовавшие- ,ся фосфолипиды, как в примере 1, с параллельным определением сфингомиели- 0 на обычным методом с использованием ТСХ.
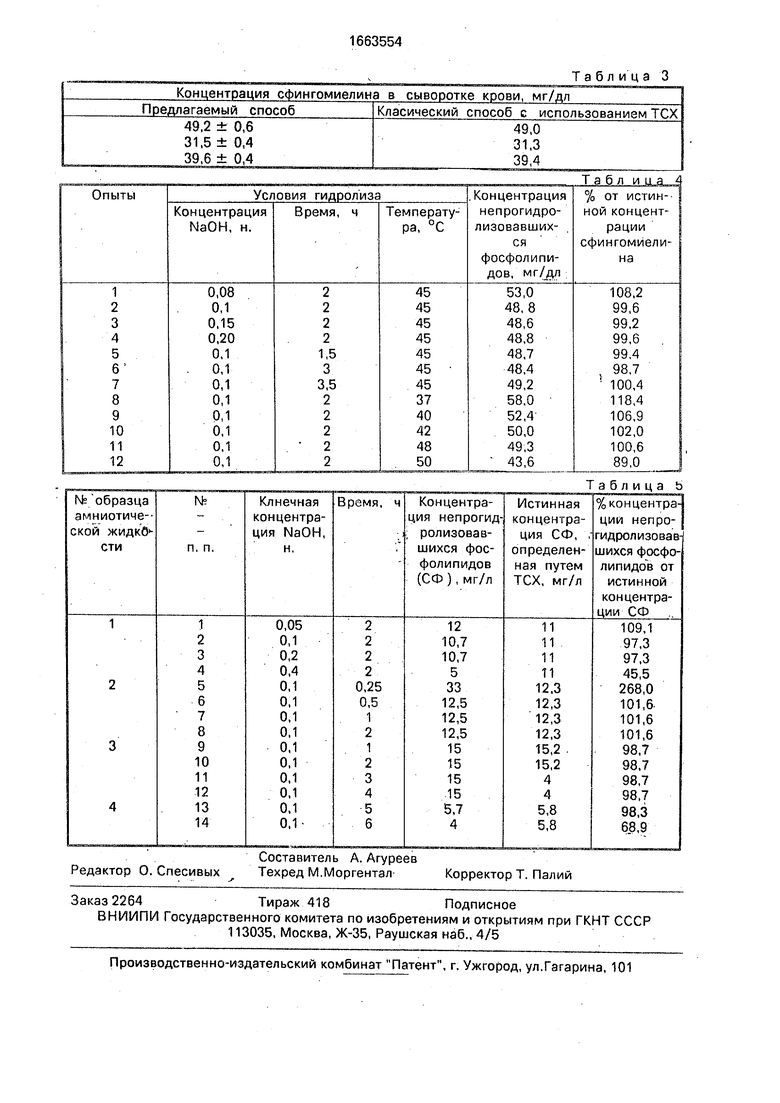
Результаты приведены в табл. 3. Как видно из табл. 3, результаты определения содержания сфингомиелина в сы- 5 воротке крови по предлагаемому способу хорошо воспроизводимы и совпадают с полученными по классическому способу с использованием ТСХ. Таким образом, предлагаемый способ пригоден для определения 0 содержания сфингомиелина и в сыворотке крови.
Пример 3. Изменение условий гидролиза.
Из 0,5 мл сыворотки крови с известным 5 содержанием сфингомиелина (49 мг/дл), определенным предварительно с помощью ТСХ, экстрагируют липиды и обрабатывают экстракт, как в примере 1. Гидролиз.осуществляют, изменяя концентрацию NaOH, 0 время и температуру, после чего в каждом случае проводят обработку реакционной смеси, как в примере 1, с последующим определением непрогидролизовавшихся фосфолипидов известным методом. Результаты 5 обобщены в табл. 4.
Из табл. 4 видно, что правильные результаты, т.е. близкие к результатам, полученным при помощи ТСХ, удается получить при использовании концентрации щелочи в процессе гидролиза не ниже 0,1 н, а температуры гидролиза не ниже 42°С и не выше
48°С. При более низких значениях концентрации NaOH и температуры (опыты 1 и 8) гидролиз глицерофосфатидов неполный, что проявляется в завышении результата определения сфингомиелина. При превышении указанного значения температуры (опыт 12), напротив, результаты занижены вследствие частичного разложения сфингомиелина (С Ф).
Пример 4. Изменение условий гидролиза-смниотической жидкости.
1,5 мл амниотической жидкости экстрагируют, как в примере 1. Проводят гидролиз упаренного экстракта липидов, согласно примеру 1 при 15°С, меняя время гидролиза и повышая концентрацию NaOH. Результаты определения непрогидролизовавшихся фосфолипидов приведены в табл. 5.
Как видно из табл. 5, количество непро- гидролизовавшихся фосфатидов соответствует содержанию сфингомиелина при концентрации NaOH не ниже 0,1 и не выше 0,2 н. При более низкой концентрации NaOH (в более мягких условиях опыт 1) ре- зультаты завышены вследствие неполного гидролиза, а при более высоких занижены (опыт 4) ввиду некоторого разрушения сфингомиелина.
В отношении времени гидролиза из табл. 5 видно, что верные результаты получаются при продолжительности опыта от 0,5 до 4 ч. Увеличение продолжительности гидролиза свыше 5 ч и уменьшение времени (0,5 ч и ниже) также приводят к искажению результатов или ввиду неполного гидролиза (опыт 5) или вследствие некоторого разрушения определяемого вещества - сфингомиелина (опыт 14).
Таким образом, предлагаемый способ позволяет проводить определение уровня сфингомиелина с помощью мягкого щелочного гидролиза в отработанных условиях не только в амниотической жидкости, но также и в сыворотке крови и, возможно, в других биологических препаратах. Метод информативен и точен, в сочетании с простотой выполнения не требует дорогостоящего оборудования и реактивов, что создает возможность для широкого внедрения его в повседневную клиническую практику, в частности для антенатального определения степени зрелости легких плода и прогнозирования развития респираторного дистресс-синдрома у новорожденных.
Формула изобретения Способ определения содержания сфингомиелина в биологических жидкостях путем экстракции липицов лороформ-ме- танольной смесью, вакуумного упаривания экстракта, растворения его в органическом растворителе с последующим фракционированием и измерением, отли чающийся тем, что, с целью упрощения способа при массовых анализах за счет сокращения стадий, экстракт растворяют в метаноле, добавляют к нему 0,1-0,2 H.NaOH и инкубируют 0,5-4 ч при 42-48 С, затем к полученному гидролизату липидов добавляют хлороформ и воду при объемном соотношении хлороформ:метанол в гидро- лизате:вода 2:1:0,6, смесь встряхивают, отбирают нижнюю фазу с последующим нанесением пробы на пластину и измерением.
Таблица 1
Таблица 2
Таблица 3
Таблица Ъ
| Кейтс М | |||
| Техника липидологии | |||
| М., 1979, с | |||
| Ледорезный аппарат | 1921 |
|
SU322A1 |
Авторы
Даты
1991-07-15—Публикация
1988-12-30—Подача