Изобретение относится к перкислотам, в частности, к способу получения алифатических перкарбоновых кислот, которые используют в органическом синтезе.
Целью изобретения является повышение эффективности процесса за счет увеличения срока службы катализатора.
Способ заключается в следующем.
В трехгорлую колбу помещают карбоно- вую кислоту или ее ангидрид, или эфир, пе- рсксид водорода в виде водного или диоксанового раствора при определенном соотношении реагирующих компонентов, хлорсодержащий катионит в Н-форме. Реакционную смесь перемешивают при заданной температуре до установления равновесия. За ходом реакции следят по количеству израсходованной перекиси водорода перманганатометрическим и образовавшейся перкислоты иодометрическим методами титрования. По окончании реакции катализат отделяют от катализатора на фильтре Шотта и получают водный или ди- оксановый раствор перкарбоновых кислот, которые выделяют известными приемами. Статистическую обменную емкость катио- нита до и после реакции определяют по известной методике. Хлорсодержащий катионит КУ-2 х 8 в Н-форме с содержанием хлора 2,2-9,5 мас.% получают обработкой сульфированного сополимера стирола с ди- винилбензолом КУ-2 х 8 смесью соляной кислоты и перекиси водорода (или гипохло- рита натрия) при 20-40°С в течение 4-8 ч и молярном соотношении соляная кислота: окислитель, равном (1-1,5):(0.03-0,25) моль на 10 мас.ч. катионита.
Контрольными опытами определяют стойкость нехлорированного и хлорированного образцов катионита КУ-2 х 8 к действию окислителей, таких как пероксид водорода (Н202) и перуксусная кислота (СНзСОООН).
Os
00
ел ю
со ю
Для этого в колбу загружают определенное количество хлорированного (содержание хлора 2,2-9,5 мае. %) или нехлорированного образца, Затем в колбу добавляют смесь перекиси водорода и уксусной кислоты, реакционную массу перемешивают при 30°С и определяют содержание перекисных компонентов (H2U2 и СНзСОООН) методом титрования. Через каждые 250 ч фильтрованием выделяют катализатор, к которому вновь добавляют свежую исходную смесь перекиси водорода и уксусной кислоты. В результате этих опытов установлено, что нехлорированный катионит КУ-2 х8, использованный в качестве катализатора в реакции синтеза перкислот, годен в течение 1500 ч, после чего происходит деструкция и растворение катионита в среде сильных окислителей (Н202 и СНзСОООН).
Катионит КУ-2 х 8 с содержанием хлора 2,2 мас.%, п отличие от нехлорированного аналога, годен (может катализировать реакции) п течение 2500 ч без потери каталитической активности и первоначальной массы. С увеличением содержания хлора в катио- ните до 9,5 мзс.% его устойчивость к действию окислителей существенно возрастает. Даже после 3500 ч эксплуатации в системе (Н202 + СНзСОООН) катионит не теряет своей первоначальной массы и активности. Обменная емкость воздушно-сухого катионита с содержанием хлора 9,5 мас.% до и после эксплуатации в течение 3500 ч составляет 3,54 и 3,48 мг-экв/г соответственно (см. табл. 1).
Как видно из табл. 1, по сравнению с нехлорированным образцом, у хлорированного катионита КУ-2 х 8 с увеличением содержания хлора (в указанном пределе) увеличивается его стойкость к действиям окислителей и при длительной эксплуатации почти не меняется его активность.
Способ иллюстрируется следующими примерами.
П р и м е р 1 (получение катализатора). Втрехгорлую колбу загружают 10 гкатионо- обменной смолы марки КУ-2 х 8 (обменная емкость 3,56 мг-экв/г) и 152 г (1,5 моль) 36%-ной соляной кислоты. Затем включают мешалку и при 20°С к реакционной смеси в течение 1 ч добавляют 28,5 г (0,25 моль) 30%-ный водный раствор пероксида водорода. Затем реакционную смесь перемешивают 7 ч. После окончания реакции катионит отделяют от водной части фильтрованием, промывают водой и сушат, Получают 11,0 г хлорированного катионита с содержанием хлора 9,5 мас.% (обменная емкость 3,56 мг- экв/г).
П р и м е р 2. Реакцию проводят по примеру 1, но с участием 11,4 г (0,1 моль) 30%-ного пероксида водорода. Получают 11,0 г хлорированного катионита с содержанием хлора 7,5 мас.% (обменная емкость 3,56 мг-экв/г).
ПримерЗ. Реакцию проводят по примеру 1, но с участием 3,5 г (0,03 моль) 30%-ного водного раствора пероксида водорода. Получают 10,5 г хлорированного катионита с содержанием хлора 2,2 мас.% (обменная емкость 3,55 мг-экв/г).
П р и м е р 4. Получение равновесной перуксусной кислоты СНзСОООН. В колбу
при 30 С загружают 0,3 моль (18,0 г) уксусной кислоты, 0,3 моль (34,0 г) 30%-ного ди- оксанового раствора пероксида водорода (при молярном соотношении кислота: Н202 1:1) и 5,1 г катионита КУ-2 х 8 в Н-форме,
катализатор с содержанием хлора 9,5% после 3000 ч эксплуатации (количество катализатора - 10% от реакционной массы). Реакционную массу перемешивают 4. ч, а затем фильтруют через фильтр Шотта и получают 49,4 г катализата, в том числе 12,8 г перуксусной кислоты. Выход перуксусной кислоты на прореагировавшую На02 99,8%. Выход перуксусной кислоты на взятую Н202 56%.
П р и м е р 5. Получение равновесной перпропионовой кислоты. Реакцию проводят по примеру 4, но в реакцию берут 0,3 моль (22,2 г) пропионовой кислоты 0,3 моль(34,0 г)30%-ногодиоксанового раствора перекиси водорода и 5,6 г катионита КУ-2 х 8 в Н-форме с содержанием хлора 7,5% после 3100 ч эксплуатации. Реакционную массу перемешивают при 30°С 4,5 ч. Получают катализат 53,3 г, в том числе 13,8
г перпропионовой кислоты - C2HsCOOOH. Выход перпропионовой кислоты на прореагировавшую Н20299,5%, выход перпропионовой кислоты на взятую Нз02 51,1%,
П р и м е р 6, Получение перуксусной кислоты, свободной от пероксида водорода. Реакцию ведут по примеру 4, но соотношение СНзСОООН:Н202 6:1. Берут 1,2 моль (72 г) уксусной кислоты, С,2 миль (22,6
г) 30%-ного диоксанового раствора пероксида водорода и 9,5 г (10% от реакционной массы) катионита КУ-2 х 8 с содержанием хлора 9,5 мас.% после 3500 ч пероксида содорода полностью расходуется. Выход
СНзСОООН на взятую H2U2 99,3%.
Если взамен уксусной кислоты использовать уксусный ангидрид возможно синтезировать растворы перуксусной кислоты высокой концентрации, не содержащей перекиси водорода.
Пример. Реакцию проводят по примеру 4, но в качестве катализатора используют КУ-2 х 8 с содержанием хлоря 9,5 мас.% после 3500 ч эксплуатации. Взято в реакцию: уксусная кислота 60 г (1,0 моль), 30%-ный водный раствор H2U2 11,4 г (0,1 моль), катализатор 7,1 г, температура 30°С. Получают 71,4 г катализата, в том числе 6,0 г надуксусной кислоты. Выход надуксусной кислоты на взятую HzOz 79,1%, на прореагировавшую Н20а 98,5%.
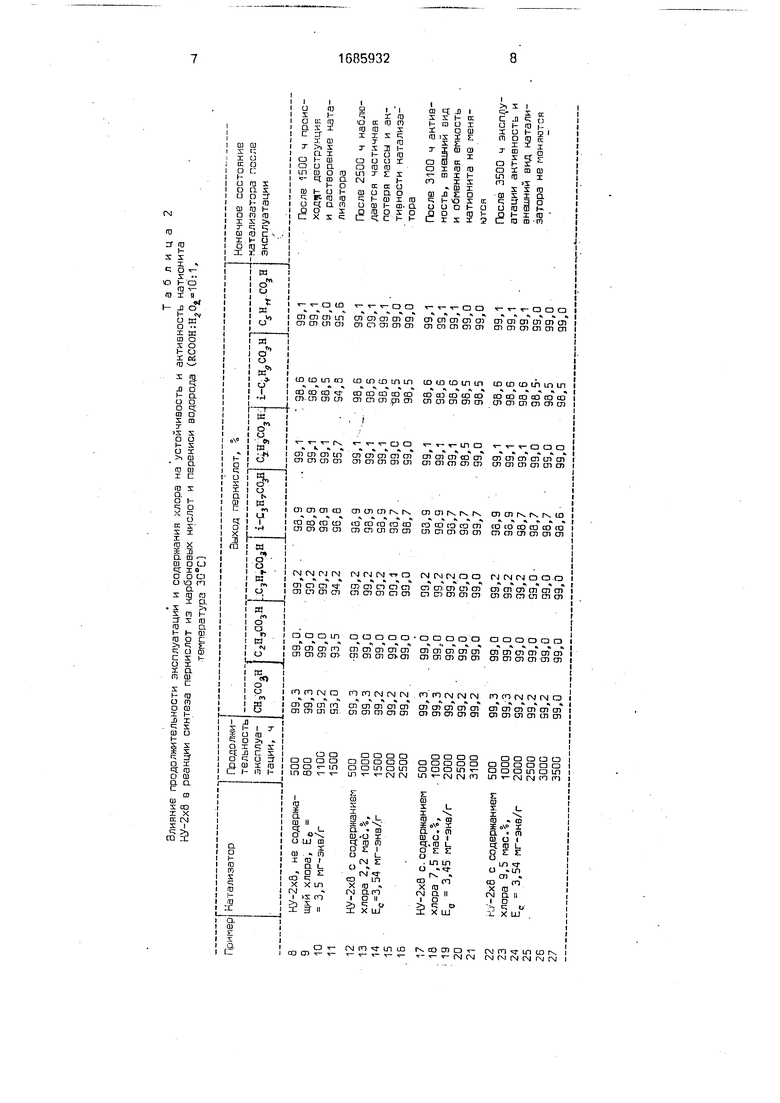
Примеры 8-27 представлены в табл. 2, а примеры 28-47 - в табл. 3.
Примеры 8-27 проводятся аналогично примерам 4 или 7 с водным или диоксано- вым раствором HzC)2. Данные примеров приведены в табл. 2 и 3.
Таким образом, предложенный способ позволяет повысить эффективность процесса за счет увеличения срока службы катализатора с использованием хлорсодержащего
катионита более чем в дпа рлзя (до 3100 3500 против 300-1500 ч в прототипе). Формула изобретения Способ получения алифатических поркарбоновых кислот путем взаимодействии перекиси водорода с соответствующей кяр- боновой кислотой или ее эфиром, или ее ангидридом при 20-40°С и молярном соотношении реагентов к перекиси водорода,
равном 1:1-10:1, в присутствии катализатора - сульфированного сополимера дивинил- бензола со стиролом в водной среде или среде диоксана с.последующим выделением целевого продукта, отличающийся
тем, что, с целью повышения эффективности службы процесса за счет увеличения срока службы катализатора, в качестве катализатора используют предварительно хлорированный раствором соляной кислоты и
перекиси водорода сульфированный сополимер дивинилбензола со стиролом с содержанием хлора 2,2-9,5 мас.%.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения стойкого к окислителям катионита | 1989 |
|
SU1728250A1 |
| Способ получения пирокатехина и гидрохинона | 1977 |
|
SU676159A3 |
| ^^^И&ЛЙОТЕМДЗа'/;«и1тсль Сумгактский филиал Института нефтехимических процессов АНАзербайджанской ССР | 1973 |
|
SU373269A1 |
| Способ получения дибромфенола | 1989 |
|
SU1768574A1 |
| Способ регенерации водород-катионитного фильтра первой ступени химобессоливания воды | 1989 |
|
SU1673207A1 |
| Способ получения циклических диолов | 1989 |
|
SU1712351A1 |
| Способ получения ионитов | 1979 |
|
SU895489A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ПОЛИЭЛЕКТРОЛИТОВ | 1973 |
|
SU384840A1 |
| ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИЯ, ИСПОЛЬЗУЕМАЯ ДЛЯ ДЕЗИНФИЦИРОВАНИЯ МЕДИЦИНСКОГО ОБОРУДОВАНИЯ, ИМЕЮЩЕГО МЕТАЛЛИЧЕСКИЕ ЧАСТИ | 1992 |
|
RU2122434C1 |
| Способ получения карбоксильных катионитов | 1986 |
|
SU1392076A1 |
Изобретение касается производства перкислот, в частности получения алифатических перкарбоновых кислот, используемых в органическом синтезе. Цель - повышение эффективности процесса. Его ведут реакцией перекиси водорода с соответствующей кислотой или ее эфиром, или ее ангидридом при 20-40°С и молярном соотношении 1:1-1:10 в присутствии катализатора - сульфированного сополимера дивинилбензола со стиролом в водной среде или в диоксане с последующим выделением целевого продукта. При зтом катализатор предварительно хлорируют раствором соляной кислоты и перекиси водорода до содержания хлора в нем 2,2- 9,5 мас.%. В этих условиях увеличивается срок службы катализатора с 300 и 1500 до 3100 и 3500 ч. Зтабл.
Влияние продолжительности эксплуатации и содержание хлора на устойчивость и активность в среде Н202 + СНзСОООН при 30°С
Наименование
Продолжительность эксплуатации катионита, ч
КУ-2 х 8 (нехлорированный ) обменная емкость ЕС - 3,56 мг-экв/г КУ-2 х 8 с содержанием хлора в макромолекуле 2,2 мас.%,.обменная емкость
ЕС - 3,54 мг-экв/г КУ-2 х 8 с содержанием хлора 7,5 мас.%, обменная емкость ЕС -3,45 мг-экв/г КУ-2 х 8 с содержанием хлора 9,5 мас.%, обменная емкость ЕС 3,54 мг-экв/г
Конечное состояние катализатора после эксплуатации
Происходят деструкция и растворение катализатора
Наблюдается частичная потеря массы и активности катализатора
Активность и внешний вид
не меняются Ее 3,45 мг-экв/г
Активность и внешний вид
не меняются ЕС 3,48 мг-экв/г
Таблиц
Влияние продолжительности эксплуатации и содержания ллооа на устойчивость и активность натионита НУ-2хб в реакции синтеза пернислот из нарбоновых кислот и перекиси водорода (RCOOH:H Ot 1G:1,
температура ЗО О
Т а
ЙЛИЯНИв ГрОЛГЛ НИТРЛЫ ОСТИ ЭНСПЛуатлцим и CO/JunivJHm X ИД УСТОЙЧИВОСТЬ и ЗНТИВМССТЬ ЛГМ-тиигч Ч
синтнза пео игдат из эфироа и h,G, (моляоное СООГНОШРНИВ R, СООС,Н,:И,о, 10:1, R, . С,Н,.
твмлегитура -UJ С)
1J,
эодолн нтвльнасть i энспяуатлции ка
НУ-2х8 нахлормрояан- мый), обменнан д,,- мость Ес , - 3.56 nr-SMS/r
ИУ-2х8 с сядвцманивм хлора 2,2 мае., Е„- 3.54 «г-эмв/г
НУ-2хв с сцдврканием хлора 7,5 nac.t, Ес- 3,45 fr-эив/г
НУ-2хв с содарианивм хлора 9,5 1-исЛ. Ес- 3,54 мг-э«в/г
500 900 1100 1500
500
1000
1500
2000
2500
500
1000
2000
2500
31DG
500
1СОС 2СОО
2500 3000 3500
-i-
| ^^^И&ЛЙОТЕМДЗа'/;«и1тсль Сумгактский филиал Института нефтехимических процессов АНАзербайджанской ССР | 0 |
|
SU373269A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1991-10-23—Публикация
1989-04-27—Подача