лен-бис-акриламида) суспендируют в 4,0 мл 0,1 М буфера (рН 8), после чего к полученной суспензии добавляют раствор 0,25 моль п- бензохинона в 20%-ном растворе диоксана (1,0 мл) (концентрация п-бензохинона 50 ммоль/л) и выдерживают ее в течение 24 ч при 50°С. Набухший гель отделяют и последовательно промывают 70 мл 20%-ного раствора диоксана в 70 мл дистиллированной воды.
Активированный гель отфильтровывают на вакуумном фильтре и добавляют к нему 2,0 мл 0,01-молярного раствора } -ами- номасляной кислоты. Для растворения у аминомасляной кислбты используют 0,1-молярный раствор калийнатрийфосфат- ного буфера (рН 7,5). Суспензию выдерживают в течение 24 ч при 4°С, гель отделяют, а несвязанную у-аминомасляную кислоту удаляют путем промывкиО,1-молярным рас- твором натрийацетатного буфера (рН 5,0), содержащего 1,0 моль хлористого натрия и 0,1-молярным раствором бикарбоната натрия (рН 8,5). Количество связанной аминомасляной кислоты составляет 4,0 мкмоль, что соответствует 20% от всего ее количества в реакционной смеси.
Пример 3. 0,1 г ксерогеля акрилекс Р-100 (сополимер акриламида и N,N -мети- лен-бис-акриламида) суспендируют в 4,0 мл 0,1-молярного фосфатного буфера (рН 8,0). После добавки к суспензии раствора 0,25 моль п-бензохинона в 20%-ном растворе диоксана (1,0 мл) ее оставляют стоять в течение 24 ч при 50°С. Затем набухший гель отделяют и последовательно промывают 70 мл 20%-ного раствора диоксана и 70 мл дистиллированной воды.
Активированный гель отфильтровывают на вакуумном фильтре и добавляют к нему 2,0 мл раствора альбумина бычьей сыворотки (20 мг/мл). Для растворения альбу- мина бычьей сыворотки используют 0,1-молярный натрийформиатный буферный раствор (рН 3,0). Суспензию выдержи- вают в течение 24 ч при 4°С, после чего гель отделяют и удаляют несвязанный альбумин сыворотки путем последовательной промывки 0,1-молярным раствором натрийацетатного буфера (рН 5,0), содержащего 1,0 моль хлористого натрия и 0,1-молярным раствором бикарбоната натрия (рН 8,5). Количество связанного альбумина бычьей сыворотки составляют 10 мг. Выход 25% в расчете на добавляемый к реакционной смеси альбумин сыворотки.
Пример 4. 0,1 г ксерогеля акрилекс Р-100 (сополимер акриламида и М,М -мети- лен-бис-акриламида) суспендируют в 4,0 мл
0,1-молярного фосфатного буфера (рН 8,0), после чего добавляют к полученной суспензии раствор 0,25 моль n-бенэохинона в 20%- ном растворе диоксана (1,0 мл) и составляют ее состоять в течение 24 ч при 50°С. Затем набухший гель отделяют и последовательно промывают 70 мл 20%-ного раствора диоксана и 70 мл дистиллированной воды.
Активированный гель отфильтровывают на вакуумном фильтре и добавляют к нему 2,0 мл раствора альбумина бычьей сыворотки (20 мг/мл). Для растворения альбумина бычьей сыворотки используют 0,1-молярный калийнатрийфосфатный буфер (рН 6,0). Суспензию выдерживают в течение 24 ч при 4°С, после чего гель отделяют, а несвязанный альбумин сыворотки удаляют путем последовательной промывки 0,1-молярным натрийацетатным буфером (рН 5,0), содержащим 1,0 моль хлористого натрия, и 0,1- молярным раствором бикарбоната натрия (рН 8,5). Количество связанного альбумина сыворотки составляет 4,5 мг, что соответствует 11,25% от всего его количества в реакционной смеси.
Пример 5. 0,1 г ксерогеля акрилекс Р-100 (сополимер акриламида и N.N -мети- лен-бис-акриламида) суспендируют в 4,0 мл 0,1-молярного фосфатного буфера (рН 8,0), после чего к полученной суспензии добавляют раствор 0,25 моль п-бензохинона в 20%- ном растворе диоксана (1,0 мл) и выдерживают ее в течение 24 ч при 50°С. Набухший гель отделяют и последовательно промывают 70 мл 20%-ного раствора диоксана и 70 мл дистиллированной воды.
Активированный гель отфильтровывают на вакуумном фильтре и добавляют к нему 2,0 мл раствора альбумина бычьей сыворотки (20 мг/мл). Для растворения альбумина бычьей сыворотки используют 0,1-молярный буферный раствор карбоната и бикарбоната натрия (рН 9,0). Суспеьзию выдер живают в течение 24 ч при 4°С, после чего гель отделяют и удаляют несвязанный альбумин сыворотки путем последовательной промывки его 0,1-молярным натрийацетатным буфером, содержащим 1,0 моль хлористого натрия (рН 5,0), и 0,1-молярным раствором бикарбоната натрия. Количество связанного альбумина бычьей сыворотки составляет 5,0 мг, что соответствует 12,5% от общего его количества в реакционной смеси.
Пример 6. 0,1 г ксерогеля акрилекс Р-100 (сополимер акриламида и N.N -мети- лен-бис-акриламида) суспендируют в 4,0 мл 0,1-молярного фосфатного буфера (рН 8,0), после чего к полученной суспензии добавляют раствор 0,25 моль п-бензохинона в 20%ном растворе диоксана (1 мл) и выдерживают ее в течение 24 ч при 50°С. Набухший гель отделяют и промывают последовательно 70 мл 20%-ного раствора диоксана и 70 мл дистиллированной воды.
Активированный гель отфильтровывают на вакуумной фильтре и добавляют к нему 2,0 мл раствора глюкозооксидазы (20 мг/мл). Для растворения глюкозооксидазы используют 0,1-молярный калийнат- рийфосфатный буфер (рН 7,5). Суспензию выдерживают в течение 24 ч при 4°С, гель отделяют, а несвязанный блок удаляют путем последовательной промывки 0,1-моляр- ным натрийацетатным буфером, содер- жащим 1,0 моль хлористого натрия (рН 5,0), и 0,1-молярным раствором бикарбоната натрия (рН 8,5).
Количество связанного с гелем белка составляет 4,5 мг. Активность полученного продукта равна 7,2 ед./г ксерогеля. Одна единица активности соответствует тому количеству фермента, которое обеспечивает каталитическое окисление 1,0 мкмоль глюкозы в минуту при рН 7,0 и температуре 25°С. Удельная активность связанного фермента составляет 8% от удельной активности растворенного фермента.
Пример 7. 0,1 г ксерогеля акрилекс Р-100 (сополимер акриламида и Ы,М -метилен-бис-акриламида) суспендируют в 4,0 мл 0,1-молярного фосфатного буфера (рН 8,0), после чего к полученной суспензии добавляют раствор 0,25 моль n-бензохинона в 20%- ном растворе диоксана (1,0 мл) и выдерживают ее в течение 24 ч при 50°С. Набухший гель отделяют и промывают по- следовательно 70 мл 20%-ного раствора диоксана и 70 мл дистиллированной воды.
Активированный гель отфильтровыва- ют на вакуумном фильтре и добавляют к нему 2,0 мл раствора каталазы (20 мг/мл). Для растворения каталазы используют 0,1- молярный раствор калийнатрийфосфатного буфера (рН 7,5). Суспензию выдерживают в течение 24 ч при 4°С, гель отделяют и удаляют несвязанный белок путем последовательной промывки 0,1-молярным натрийацетатным буфером, содержащим 1,0 моль хлористого натрия (рН 5,0) и 0,1-моляр- ным раствором бикарбоната натрия (рН 8.5).
Количество связанного белка составляет 5,3 мг, активность полученного продукта равна 2100 ед./г ксерогеля. Одна единица активности соответствует тому количеству фермента, которое катализирует разложение 1 мкмоль перекиси водорода в минуту при 25°С. Удельная активность связанного
фермента составляет 2% от удельной актин ности раствора фермента.
П р и м е р 8. 0,1 г ксерогеля акрилекс Р-100 (сополимер акриламида и N.N1 -мети- лен-бис-акриламида) суспендируют в 4,0 мл 0,1-молярного фосфатного буфера (рН 8.0) после чего к полученной суспензии добавляют раствор 0,25 моль n-бензохинона в 20%- ном растворе диоксана (1.0 мл) и выдерживают суспензию в течение 24 ч при 50°С Набухший гель отделяют и промывают последовательно 70 мл 20%-ного раствора диоксана и 70 мл дистиллированной воды.
Активированный гель отфильтровывают на вакуумном фильтре и добавляют к нему 2,0 мл 0,01-молярного раствора глюкозы в 0,1-молярном растворе калийнатрийфосфатного буфера (рН 7.5). Суспензию выдерживают в течение 24 ч при 4°С, после чего гель отделяют и удаляют несвязанную глюкозу путем последовательной промывки содержащим 1 моль хлористого натрия 0,1-молярным натрийацетатным буфером (рН 5,0) и 0,1-молярным раствором бикарб- роната натрия (рН 8,5). Количество связанной глюкозы составляет б мкмоль, что соответствует 30% от всего ее количества в реакционной смеси.
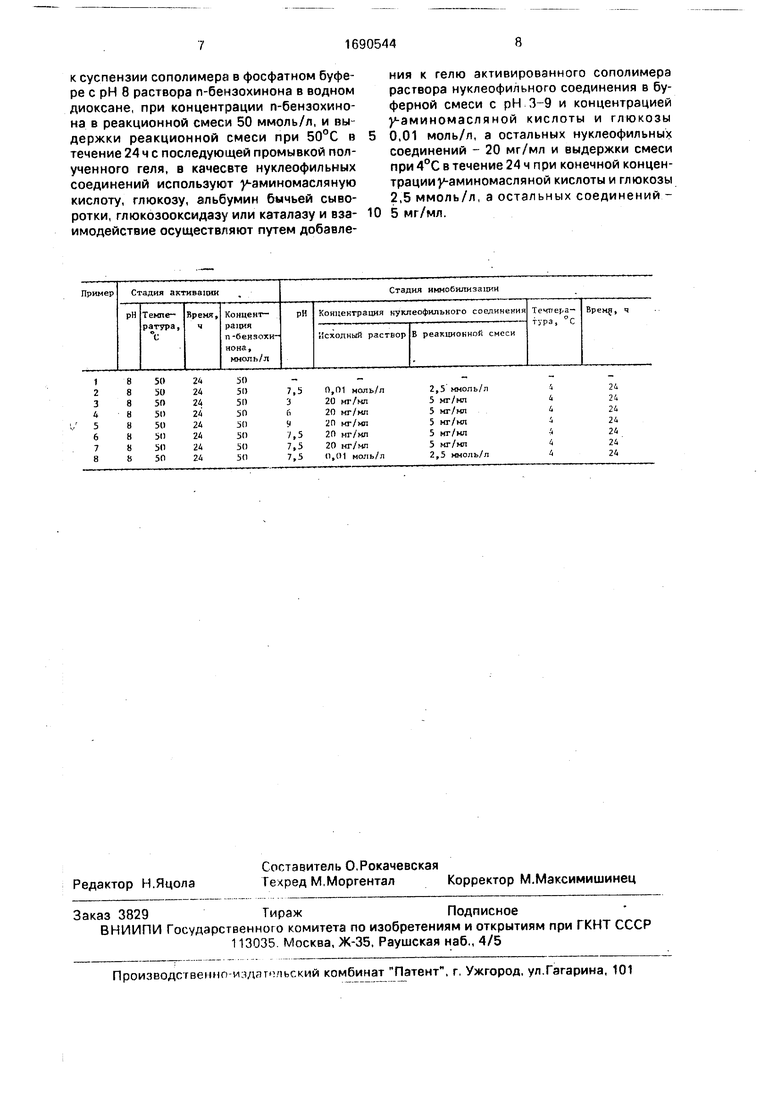
Все данные по примерам 1-8 сведены в таблицу.
П р и м е р 9 (демонстрирует стабильность полученных продуктов), Колонку размером 1,5x10 см заполняют 0,5 г иммобилизованного препарата фермента, полученного согласно примеру 6, активность которого составляла 23 ед.
Через колонку пропускают в условиях промышленного процесса при 25°С и со скоростью 12 мл/ч 0,25-молярный водный раствор глюкозы. Количество продукта в вытекающем потоке оставалось неизменным в течение 51 дня (1224 ч). Это доказывает, что фиксированный препарат фермента сохраняет свою активность.
Применение перепарата инвертазы, полученного известным способом, для процесса гидролиза показало, что активность препарата падает в течение 100 ч работы.
Формула изобретения Способ получения иммобилизованных нуклеофильных соединений, включающий активацию сополимера акриламида с N,N- метиленбис-акриламидом и его взаимодействие с нуклеофильным соединением с последующей промывкой целевого продукта для удаления низкомолекулярных примесей, отличающийся тем, что, с целью повышения стабильности целевых продуктов, активацию проводят путем добавления
к суспензии сополимера в фосфатном буфере с рН 8 раствора n-бензохинона в водном диоксане, при концентрации п-бензохино- на в реакционной смеси 50 ммоль/л, и выдержки реакционной смеси при 50°С в течение 24 ч с последующей промывкой полученного геля, в качесвте нуклеофильных соединений используют у-аминомасляную кислоту, глюкозу, альбумин бычьей сыворотки, глюкозооксидазу или каталазу и взаимодействие осуществляют путем добавления к гелю активированного сополимера раствора нуклеофильного соединения в буферной смеси с рН 3-9 и концентрацией у-аминомасляной кислоты и глюкозы
0,01 моль/л, а остальных нуклеофильных соединений - 20 мг/мл и выдержки смеси при 4°С в течение 24 ч при конечной концентрации у-аминомасляной кислоты и глюкозы 2,5 ммоль/л, а остальных соединений 5 мг/мл.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения иммобилизованной холинэстеразы | 1983 |
|
SU1572418A3 |
| Способ получения иммобилизованной глюкоамилазы | 1983 |
|
SU1461373A3 |
| Способ получения иммобилизованной аминоацилазы | 1982 |
|
SU1228788A3 |
| Способ определения глюкозы в биологических жидкостях | 1984 |
|
SU1505444A3 |
| Способ получения ариламидов аминокислот или пептидов или их солей | 1986 |
|
SU1512484A3 |
| Способ получения полиакриламидного геля | 1984 |
|
SU1393316A3 |
| Способ получения иммобилизованных клеток микроорганизмов или их частей | 1989 |
|
SU1760985A3 |
| Способ получения производных @ -/моно-или дизамещенных /- @ -арилмочевин | 1981 |
|
SU1246891A3 |
| Способ получения конъюгатов полициклических ароматических углеводородов с белками | 1983 |
|
SU1139438A1 |
| Способ получения конъюгированных антигенов | 1983 |
|
SU1109169A1 |
Изобретение относится к способу иммобилизации биологически активных соединений, содержащих нуклеофильные группы - у-аминомасляной кислоты, глюкозы, альбумина бычьей, сыворотки, глюкозооксидазы и каталазы. Изобретение позволяет повысить стабильность полученных продуктов за счет Изобретение относится к способу иммобилизации биологически активных соединений, содержащих нуклеофильные группы, таких как у-аминомасляная кислота, глюкоза, альбумин бычьей сыворотки, глюкозоокси- даза и каталаза. Цель изобретения - повышение стабильности целевых продуктов. Пример1.30г ксерогеля акрилекс Р-100 (сополимер акриламида и N.N -мети- лен-бис-акриламида) суспендируют в 1200 мл 0,1 М фосфатного калиевого буфера (рН 8), того, что активизируют сополимер акриламида с N.N-метиленбисакриламидом путем добавления к суспензии сополимера в фосфатном буфере с рН 8 раствора п-бензохи- нона в водном диоксане при концентрации n-бензохинона в реакционной смеси 50 ммоль/л и реакционную смесь выдерживают при 50°С в течение 24 ч. Полученный гель промывают и подвергают взаимодействию с нуклеофильным соединением - у-ами- номасляной кислотой, глюкозой, альбумином бычьей сыворотки, глюкозооксидазой или каталазой. Взаимодействие проводят путем добавления к гелю активированного сополимера раствора нуклеофильного соединения в буферной смеси с рН 3-9 и концентрацией у-аминомасляной кислоты и глюкозы 0,01 моль/л, а остальных соединений - 20 мг/мл. Смесь выдерживают при 4°С в течение 24 ч при конечной концентрации у-аминомасляной кислоты и глюкозы 2,5 ммоль/л, а остальных нуклеофильных соединений - 5 мг/мл, 1 табл. после чего к полученной суспензии добавляют 0,25 моль n-бензохинона в 20%-ном растворе диоксана (300 мл) и выдерживают ее в течение 24 ч при 50°С. Концентрация п-бен- зохинона в смеси равна 50 ммоль/л. Набухший гель отделяют и последовательно промывают 3 л 20%-ного раствора диоксана и 10 л дистиллированной воды. Отмытый гель лиофилизируют. В результате получают 24,3 г активированного носителя. П р и м е р 2. 0,1 г ксерогеля акрилекс Р-100 (сополимер акиламида и N.N -метиО о о ел fc со

| Способ получения иммобилизованных вполиакриламидном геле ферментов | 1975 |
|
SU530886A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1991-11-07—Публикация
1983-08-23—Подача