Изобретение относится к медицинской микробиологии.
Известна питательная среда для выделения стафилококков, содержащая агар- агар, приготовленный на мясном бульоне, и 10% дефибринированной крови.
Недостатком данной среды являются слабые селективные свойства
Известна питательная среда для выделения стафилококков, содержащая физиологический раствор, мясо-пептонный агар (рН 7,2) 10% хлористого натрия и 10-20% желточной взвеси.
Недостатком данной среды являются также слабые селективные свойства
Известна также питательная среда для выделения стафилококков, содержащая агар-агар, нативный яичный белок хлори стый натрий, бульон Хоттингера
Недостатком данной питательной среды являются ее слабые селективные свойства, сложность и длительность выделения
патогенных стафилококков, так как в связи с широким применением антибиотиков и хи- миотерапевтических препаратов, оказывающих влияние на изменчивость микробов кокковой группы, в этиологии многих гнойно-воспалительных процессов большая роль стала придаваться, наряду с золотистым стафилококком, и другим видам стафилококков, относящимся к группе потенциально-патогенных В соответствии с этим недостатком известной питательной среды является определение только одного вида стафилококков что снижает диагностическую ценность питательной среды
Целью изобретения является повышение селективных свойств среды, упрощение и ускорение выделения патогенных стафилококков.
Эта цель достигается тем что среда дополнительно содержит желток,при этом на тивный белок и желток она содержит в виде яичной взвеси. 0.1 %-ный водный раствор
VI
сл
ю о
кристалвиолета и дефибринированную кровь при следующем соотношении компонентов:
Агар-агар20,0-25,0 г
Натрий хлористый100,0-102,0 г
Яичная взвесь100,0-150,0 г
0,1%-ный водный раствор кристалвиолета3,0-3,5 мл Дефибринированная кровь100,0-150,0 мл Бульон Хоттингера До 1 л Питательную среду готовят, например, следующим образом.
1000 мл агаровой питательной основы, приготовленной из сухого питательного агара по обычной прописи с добавлением 10%- ного хлористого натрия и 3,3 мл 0,1%-ного водного раствора кристалвиолета, стерилизуют, охлаждают до 60-70°С, добавляют в асептических условиях стерильно приготовленную яичную взвесь (куриное яйцо - белок и желток, смешанное с 200 мл стерильного физиологического раствора) в количестве 100 мл и 110 мл дефибриниро- ванной крови. Среду тщательно перемешивают и разливают в чашки Петри. После застывания и подсушивания среду используют для проведения необходимых исследований. Срок хранения среды после приготовления 7-10 дней при температуре +4° С.
Питательная среда используется следующим образом
Для выделения культур стафилококков исследуемый материал (мазки из зева носа, гной, раневое содержимое, вода, смывы с обьектов внешней среды) рассеивают по всей поверхности питательной среды тампоном (лли шпателем, а при дифференциации уже выделенных штаммов стафилококков - штрихами на сектора чашки Петри, Учет результатов проводят через 24-48 ч инкубации в термостате при 37°С
При посеве исследуемого материала на предлагаемую диагностическую среду на ней вырастают, наряду с золотистым стафилококком, и другие виды стафилококков с признаками патогенности (вирулентности) П р и м е р 1. При прямом посеве тампоном мазка из зева ребенка с подозрением на дифтерию были использованы одновременно простой мясо-пептонный агар(МПА), кровяной и желточно-солевой агары, а также предлагаемая диагностическая среда Указанный набор питательных сред применялся как при прямом посеве патологиче- ского материала, так и при проведонии идентификации выделяемых из зева микроорганизмов Через 18-24 ч все культуры с
простого агара подозрительные как стафи лококки (наличие золотистого, желтого или белого пигмента колоний), пересевались вновь на кровяной агар, желточно-солевую
и предлагаемую среды Все колонии с предлагаемой питательной диагностической среды также засевались на кровяной и желточно-солевой агары. После 18 ч инкубации производился учет результатов. Из зева ре0 бенка было выделено 9 штаммов стафилококков (3-е золотистым пигментом, 6 - с белым) Дальнейшая идентификация позволила установить, что все три штамма золотистого стафилококка обладали
5 гемолитической и лецитиназной активностью. Из культур белого стафилококка два штамма дали на кровяном агаре четкую зону гемолиза и один штамм обладал лецитиназной активностью. При посеве этого же мате0 риала на предлагаемую диагностическую среду было выделено 11 штаммов стафилококков (колонии фиолетового или оранжевого цвета), из которых у 4 культур наблюдали одновременно зоны лизиса эритроцитов и
5 помутнения с радужным венчиком у трех колоний отмечалась только зона гемолиза и у одного штамма - только зона помутнения Следовательно, обычными методами выделено б штаммов стафилококков, обладав0 ших факторами агрессии (гемолизин лецитиназа), а при использовании предлагаемой диагностической среды изолировано 8 штаммов патогенных стафилококков Несмотря на несущественное различие в ко5 личестве выделенных штаммов следует подчеркнуть, что исследование с применением предлагаемой диагностической среды продолжалось в течение 18-24 ч, в то время как использование обычной методики по0 требовало не менее 48 ч работы
П р и м е р 2. При параллельном контрольном посеве на МПА, кровяной агар и предлагаемую питательную среду шести смывов и двух проб воздуха в операционной
5 после ее профилактической обработки было обнаружено, что в одном смыве с загубника наркозного аппарата и в одной пробе воздуха присутствовали белые стафилококки обладавшие при последующем исследовании
0 гемолитической активностью, но не имевшие лецитиназы. Применение обычных сред позволило получить окончательный ответ через 48 ч, а при использовании предла5 гаемой диагностической среды ответ был получен через сутки
Пример 3. Готовят среду, как указано, при этом компоненты берут в следующих количествах в бульоне Хоттингера г/л Агар-агар180
Натрий хлооистый99 О
Яичная взвесь 80.0мл
0,1 %-ный водный
раствор кристалвиолета2,75 мл
Дефибринированная
кровь80,0 мл
Золотистый стафилококк дает хороший типичный рост колоний. Зоны гемолиза и помутнения слабо различимы. Колонии белого стафилококка светло-фиолетового цвета, Наблюдается единичный рост колоний кишечной палочки и вульгарного протея, что свидетельствует о недостаточном тормозящем действии хлористого натрия и кристалвиолета в количествах, добавляемых в среду.
Пример 4, Готовят среду, как указано, при этом компоненты берут в следующих количествах в бульоне Хоттингера, г/л:
Агар-агар20
Натрий хлористый100
Яичная взвесь100 мл
0,1 %-ный водный
раствор кристалвиолетэ3 мл
Дефибринированная
кровь100мл
При посеве золотистого стафилококка вырастают колонии оранжево-желтого цвета с явно выраженной зоной гемолиза и зоной помутнения с радужным венчиком, размером на 1 мм более размера зоны гемолиза. Белые стафилококки дают колонии светло-фиолетового цвета с зоной гемолиза и без нее или с зоной помутнения: радужный венчик больше размеров зоны гемолиза на 1 мм, Среда позволяет дифференцировать стафилококки с признаками патогенности от непатогенных видов. Кишечная палочка и протеи роста не дают.
П р и м е р 5. Готовят среду, как указано, при этом компоненты берут в следующих количествах в бульоне Хоттингера, г/л:
Агар-агар23,0
Натрий хлористый101,0
Яичная взвесь130 0 мл
0,1 %-ный водный
раствор кристалвиолета 3,25 мл
Дефибринированная
кровь1300мл
Рост колоний патогенных стафилококков типичный, сопровождается четкой зоной гемолиза вокруг колоний с зоной помутнения и радужным венчиком, превосходящим по размеру зону гемолиза на 3 мм. Колонии стафилококков типичные, оранжевого или фиолетового цвета Некоторые колонии белого стафилококка дают слабый радужный венчик, что позволяет отн ётТГй и х к группе стафилококков с при 5нлкями пато- генносги. Кишечные палочки и протеи не дают роста.
П р и м е р Готовят среду, как указано при этом компоненты берут в следующих количествах в бульоне Хоттингера, г/л
Агар-агар25,0
5Натрий хлористый102,0
Яичная взвесь150,0мл
0,1 %-ный водный раствор кристалвиолета3,5 мл 0 Дефибринированная
кровь.150,0мл
Колонии золотистого и белого стафилококков типичные, оранжевого цвета с зоной гемолиза и зоной помутнения с радужным 5 венчиком по периферии. Зона помутнения превосходит размеры зоны гемолиза на 3 мм; колонии белого стафилококка фиолетового цвета; некоторые колонии дают зону гемолиза и зону помутнения с радужным 0 венчиком, свидетельствующие о наличии факторов агрессии - гемолизина и лецити- назы. Кишечные палочки и протеи не растут. П р и м е р 7, Готовят среду, как указано, при этом компоненты берут в следующих 5 количествах в бульоне Хоттингера, г/л Агар-агар27,0
Натрий хлористый103,0
Яичная взвесь170,0 мл
0,1 %-ный водный 0 раствор кристалвиолета3,75 мл Дефибринированная кровь170,0 мл Колонии золотистого стафилококка вы- 5 растают ярко-оранжевого цвета с нетипичной морфологией (колонии мелкие, слегка морщинистые) со значительным количественным уменьшением числа колоний по сравнению с контрольным высевом, что сви- 0 детельствует о тормозящем действии из- бытка хлористого натрия и кристалвиолета. Зоны гемолиза и помутнения нечеткие, едва различимые из-за слияния по цвету с интенсивно окрашенным фоном среды. Белые 5 стафилококки темно-фиолетового цвета с нетипичной морфологией колоний. Кишечные палочки и протеи роста не дают.
Указанное свидетельствует, что предлагаемая модификация питательной диагно- 0 стической среды позволяет сократить объемы и срок исследований за счет преимущественного выделения стафилококков, одновременной их идентификации и определения признаков из вирулентности, так 5 как наличие в среде раствора кристалвиолета позволяет расти только стафилококкам; присутствие желтка яШТной взвеси в питательной среде дает возможность в этой же чашке визуально наблюдать лецитовителаз- ную реакцию, с помощью которой определятся наличие у исследуемого штамма микрорганизмов фермента лецитиназы; присуттвие в среде дефибринированной крови ает возможность визуально наблюдать гемолитическую активность штаммов. Все отмеченное расширяет диагностические возможности среды.
Положительный эффект достигается олько лишь при строго определенной взаимосвязи существенных признаков. Исклюение любого из них не позволяет достичь положительный эффект.
Проведенные исследования предлагаемой диагностической среды с использованием выделенных и идентифицированных ранее 124 штаммов стафилококков показало, что предлагаемая диагностическая среа четко дифференцирует патогенных микробов этой группы, как и с использованием набора других сред для выделения и идентификации штаммов стафилококков, с той лишь разницей, что выделение и частичная идентификация этих бактерий проводится в одной чашке.
В результате изучения выделяемости патогенных стафилококков с использованием различных питательных сред получены следующие результаты: всего исследовано 124 штамма стафилококков; выделено 97 штаммов стафилококков с признаками вирулентности; в том числе на обычных дифференциальных средах кровяной агар - 81, желточно-солевой агар 74: на предлагаемой диагностической среде 92.
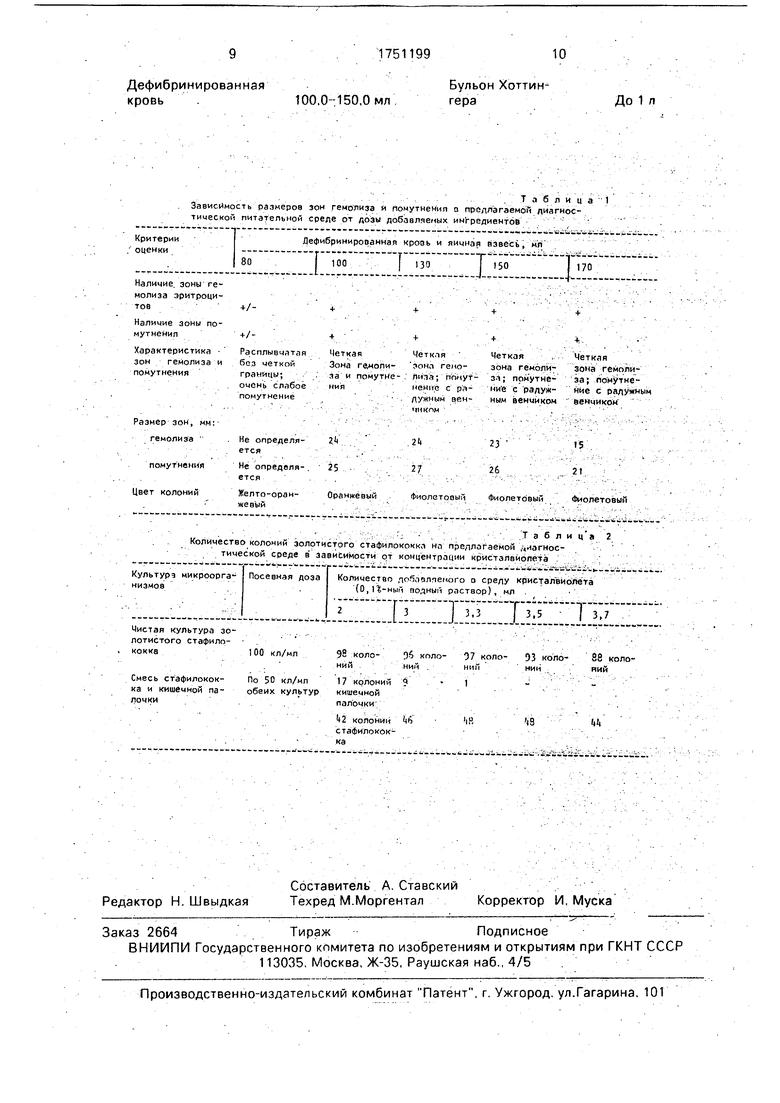
При испытательных исследованиях на предлагаемой диагностической среде вырастали колонии только патогенных стафилококков (колонии фиолетового или оранжевого цвета). Кроме того, при наличии у микробов факторов агрессии (гемолизин и лецитиназа) вокруг колонии наблюдалась зона гемолиза эритроцитов и зона частичного помутнения с радужным венчиком различной интенсивности по периферии зоны гемолиза или несколько ее превосходящая по размерам (на 1-3 мм). В табл. 1 приведены данные, свидетельствующие о различных реакциях микроорганизмов в зависимости от дозы добавляемых в предлагаемую диагностическую среду ингредиентов.
Как свидетельствует табл 1. минимальные количества дефибринированной крови и яичной взвеси, при которых получается довольно четкий результат, определяются на уровне 100-150 мл по показателям четкости зон гемолиза и помутнения с радужным венчиком и величинам размеров зон гемолиза и помутнения.
Зависимость роста стафилококков на предлагаемой питательной среде от количества добавляемого в нее раствора кристалвио- лета представлена в табл. 2.
Как видно из табл. 2, доза добавляемого
в предлагаемую диагностическую среду кристалвиолета существенно не оказывает влияния на культуру стафилококка, в то время как культура кишечной палочки не растет
0 на среде уже в дозе кристалвиолета от 3,5 мл и выше,
Таким образом, как свидетельствуют приведенные примеры, предлагаемая диагностическая питательная среда, приготов5 ленная при строго определенных соотношениях вносимых ингредиентов, позволяет четко дифференцировать патогенных представителей стафилококков от непатогенных с одновременным определе0 нием у них в одной чашке двух ферментов агрессии (гемолизин и лецитиназа). Это позволяет в значительной мере сократить объ- емы и сроки исследования за счет преимущественного выделения только ста5 филококков с одновременной их идентификацией и определением признаков вирулентности. Кроме того, использование предлагаемой диагностической среды позволяет экономить питательные среды, не0 обходимые по обычной методике для аналогичной идентификации (кровяной агар, желточно-солевой агар), а также рабочего времени персонала, необходимого для посева на дополнительные среды (мясо5 пептонный агар, кровяной агар, желточно- солевая среда) по обычной схеме исследования, и времени, требуемого на их раздельное приготовление и подготовку посуды. Все указанное увеличивает произво0 дительность труда персонала бактериологических лабораторий Формула изобретения Питательная среда для выделения патогенных стафилококков, содержащая агар5 агар, нативный яичный белок, хлористый натрий, бульон Хоттингера, отличающаяся тем, что, с целью повышения селективных свойств среды, упрощения и ускорения выделения патогенных стафилококков, она
0 дополнительно содержит желток, при этом нативный яичный белок и желток - в виде яичной взвеси, 0,1%-ный водный раствор кристалвиолета и дефибринированную кровь при следующем соотношении компо5 нентов:
Агар-агар20,0 25.0 г
Хлористый натрий100 0 102 0 (
Яичная взвесь100.0 150 0 i
0,1%-ный водный раствор кристалвиолета 3035 мл
Дефибринированная кровь
100,0-150,0 мл
Бульон Хоттин- гера
До 1 л



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ АССОЦИИРОВАННОЙ ПРОТИВ СТРЕПТОКОККОЗА И СТАФИЛОКОККОЗА КРУПНОГО РОГАТОГО СКОТА | 2009 |
|
RU2406532C1 |
| Способ выделения некультивируемых форм стафилококков | 2020 |
|
RU2738858C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ, АССОЦИИРОВАННОЙ ПРОТИВ ЭШЕРИХИОЗА, СТРЕПТОКОККОЗА И СТАФИЛОКОККОЗА КРУПНОГО РОГАТОГО СКОТА | 2013 |
|
RU2538158C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫЯВЛЕНИЯ ГЕМОЛИТИЧЕСКОЙ АКТИВНОСТИ КУЛЬТУР STAPHYLOCOCCUS AUREUS И CANDIDA ALBICANS | 2013 |
|
RU2536964C1 |
| Набор штаммов бактерий для обучения вопросам микробиологии и методам лабораторной диагностики холеры | 2019 |
|
RU2743454C1 |
| СРЕДА ДЛЯ ОПРЕДЕЛЕНИЯ ГЕМОЛИТИЧЕСКОЙ АКТИВНОСТИ КУЛЬТУР РОДА LISTERIA | 2006 |
|
RU2318022C2 |
| ВАКЦИНА ПРОТИВ МАНХЕЙМИОЗА, БИБЕРШТЕЙНИОЗА И ПАСТЕРЕЛЛЁЗА КРУПНОГО И МЕЛКОГО РОГАТОГО СКОТА АССОЦИИРОВАННАЯ ИНАКТИВИРОВАННАЯ, СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2020 |
|
RU2744744C1 |
| Питательная среда для выявления SтарнYLососсUS aUReUS | 1989 |
|
SU1693060A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ ЭНТЕРОКОККОВОЙ ИНФЕКЦИИ НУТРИЙ | 2005 |
|
RU2288002C1 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЛОР-ОРГАНОВ | 2001 |
|
RU2185190C1 |
Использование медицинская микробиология. Сущность изобретения: питательная среда используется с целью повышения селективных свойств среды, упрощения и ускорения выделения патогенных стафилококков Среда дополнительно содержит желток, при этом нативный яичный белок и желток она содержит в виде яичной взвеси. 0,1 %-ный водный раствор кристалвиолета и дефибринированную кровь при следующем соотношении компонентов агар-агар 20,0 25,0 г, хлористый натрий 100,0-102,0 г, яичная взвесь 100,0-150,0 г; 0.1 %-ный водный раствор кристалвиолета 3,0-3,5 мл, дефиб- ринированная 100,0-150,0 мл, бульон Хоттингера до 1 л. 2 табл. о w Ё
Таблица 1
Зависимость размеров зон гемолиза и помутнения о предлагаемой диагностической питательной среде от дозы добавляемых ингредиентов
Т а б л и ц я 2
Количество колоний золотистого стафилококка нп предлагаемой ,агностической среде в зависимости от концентрации кристзлвиолета
Чистая культура золотистого стафило
| Справочник по микробиологическим и вирусологическим методам исследования, под ред | |||
| Биргера | |||
| (И. | |||
| Медицина, 1973, с 75-76, Авторское свидетельство СССР № 687118, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1992-07-30—Публикация
1990-10-10—Подача