Изобретение относится к органической химии, к классу алифатических соединений карбонильных производных 1,6-гексадиена, а именно к новому способу получения 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов общей формулы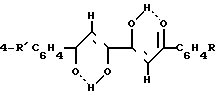 ″-4 где R′ H, R′′ Br (Ia), R′ CH3, R′′ Br (Iб), R′ R′′ Cl (Iв) известные представители которых (с одинаковыми заместителями R' и R'') находят широкое применение в условиях синтеза разнообразных соединений, обладающих значительной бактериостатической [1] и пестицидной активностью [2] фотосенсибилизирующим действием в химии полимеров [3] а также используются для получения термостабильных полимеров и полихелатов металлов [4-6]
″-4 где R′ H, R′′ Br (Ia), R′ CH3, R′′ Br (Iб), R′ R′′ Cl (Iв) известные представители которых (с одинаковыми заместителями R' и R'') находят широкое применение в условиях синтеза разнообразных соединений, обладающих значительной бактериостатической [1] и пестицидной активностью [2] фотосенсибилизирующим действием в химии полимеров [3] а также используются для получения термостабильных полимеров и полихелатов металлов [4-6]
Известен способ получения 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов (1,6-диарил-1,3,4,6-гексантетраонов 1), заключающийся во взаимодействии 5-арил-2,3-дигидро-2,3-фурандионов (2) с этилендинитроамином в среде диоксана при температуре кипения смеси в течение 3 ч [7] по следующей схеме:
4-RC6H
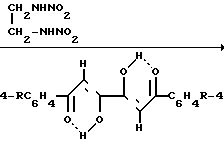
_____→4-RC6H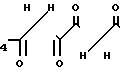 C6H4R-4
C6H4R-4 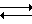 где R H, CH3 (1 и 2). Выходы соединений 1 составляют 95% (RH) и 44% (R CH3) [7] Этот способ-аналог взят за прототип.
где R H, CH3 (1 и 2). Выходы соединений 1 составляют 95% (RH) и 44% (R CH3) [7] Этот способ-аналог взят за прототип.
К недостаткам способа-аналога относятся:
невозможность получения гексадиендионов 1 с различными заместителями R в бензольных кольцах;
длительное нагревание смеси реагентов при температуре более 100оС;
использование токсичного этилендинитроамина [8]
Целью изобретения является разработка простого по выполнению, свободного от указанных недостатков способа, позволяющего с высоким выходом получать 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дио-ны формулы I.
Указанная цель достигается тем, что 5-арил-2,3-дигидро-2,3-фурандионы IIa-IIв подвергают взаимодействию с ароилметилентрифенилфосфоранами (IIIa, IIIб) при мольном соотношении 1:1 в среде бензола при температуре 70-80оС с последующим нагреванием образующихся промежуточных продуктов 5-арил-2-ароилметилен-2,3-дигидро-3-фуранонов (IVa-IVв) с соляной кислотой при мольном соотношении 1:4 в среде ацетона при температуре 40-50оС по следующей схеме: где R′ H (Ia, IIa, IVa), CH3 (Ia, IIб, IVб), Cl (Iв, IIв, IVв);
где R′ H (Ia, IIa, IVa), CH3 (Ia, IIб, IVб), Cl (Iв, IIв, IVв);
R′′ Br (Ia, Iб, IIIa, IVa, IVб), Cl (Iв, IIIб, IVв),
и выделяют целевые продукты Ia-Iв известными приемами.
Полученные соединения Ia-Iв представляют собой желтые кристаллические вещества, растворимые в хлороформе, ацетоне, диметилсульфоксиде и нерастворимые в воде и гексане. Промежуточные продукты соединения IVa-IVв представляют собой желто-оранжевые кристаллические вещества, растворимые в этаноле, ацетоне, хлороформе, бензоле и нерастворимые в воде.
П р и м е р 1. 2-n-Бромбензоилметилен-5-фенил-2,3-дигидро-3-фуранон (IVa).
К раствору 0,87 г (0,005 моль) 5-фенил-2,3-дигидрофуран-2,3-диона (IIa) в 100 мл бензола при температуре 80оС добавляют при перемешивании 2,29 г (0,005 моль) п-бромбензоилметилентрифенилфосфорана (IIIa). Растворитель испаряют и остаток перекристаллизовывают из этанола. Получают 1,45 г (82%) кристаллического соединения IVa с т. пл. 167-168оС.
Найдено, С 60,98; Н 3,04; Br 22,71.
C18H11BrO3 (М 355,18).
Вычислено, С 60,87; Н 3,12; Br 22,50.
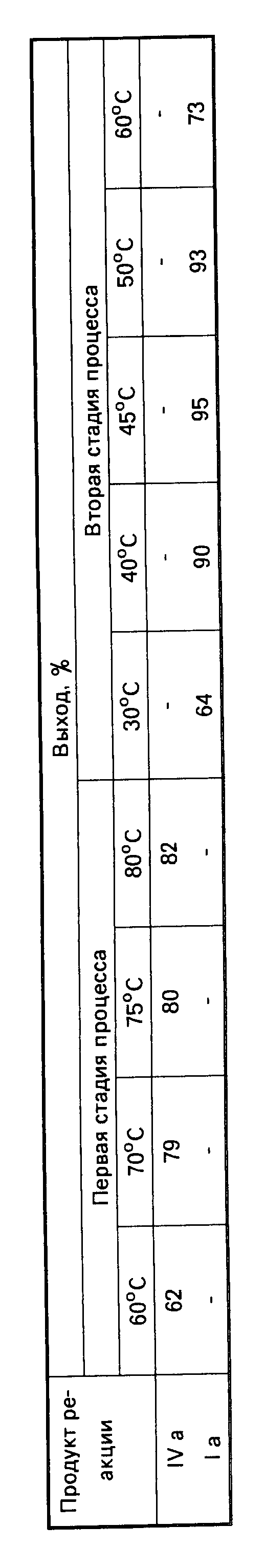
При проведении реакции с темы же количествами реагентов, но при температуре 70оС выход промежуточного продукта IVa составляет 1,40 г (79%), при температуре 60оС выход соединения IVa составляет 1,10 г (62%).
Строение всех полученных веществ доказано спектральными данными, которые соответствуют придаваемой им структуре.
ИК-спектр соединения IVa ν, см-1 (кристаллы): 1690 (С3 0), 1635 (СОС6H4Br-4).
Спектр ПМР, δ, м.д. (СDCl3): 6,30 с (1Н, экзо-СН=), 6,95 с (1Н, С4Н), 7,57-7,99 м (9Н, С6Н5, С6Н4).
П р и м е р 2. 1-n-Бромфенил-6-фенил-2,4-дигидрокси-2,4-гексадиен-1,6-дион (Ia).
К раствору 1,78 г (0,005 моль) 2-п-бромбензоилметилен-5-фенил-2,3-дигидро-3-фу- ранона (IVa) в 150 мл ацетона при температуре 50оС добавляют при перемешивании 2 мл соляной кислоты. Осадок отфильтровывают и перекристаллизовывают из смеси хлороформ-гексан, 1:1. Получают 1,73 г (93%) кристаллического соединения Ia с т. пл. 194-195оС (разложение). Суммарный выход соединения Ia по двум стадиям составляет 76%
Найдено, C 58,11; Н 3,46; Br 21,54.
C18H13BrO4 (М 373,20).
Вычислено, С 57,93; Н 3,51; Br 21,41.
При проведении реакции с теми же количествами реагентов, но при температуре 40оС выход продукта Ia составляет 1,68 г (90%), при температуре 30оС выход соединения Ia составляет 1,20 г (64%), при температуре 60оС выход соединения Ia составляет 1,35 г (73%).
Строение всех полученных веществ (Ia-Iв) доказано спектральными данными, которые соответствуют придаваемой им структуре и согласуются с таковыми известных 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов [7]
ИК-спектр соединения Ia, ν, см-1 (кристаллы): 1595-1585 (СО хелат).
П р и м е р 3. 2-п-Бромбензоилметилен-5-п-толил-2,3-дигидро-3-фураном (IVб).
К раствору 0,94 г (0,005 моль) 5-п-толил-2,3-дигидро-2,3-фурандиона (IIб) в 100 мл бензола при температуре 70оС добавляют при перемешивании 2,29 г (0,005 моль) п-бромбензоилметилентрифенилфосфорана (IIIa). Растворитель испаряют и остаток перекристаллизовывыают из этанола. Получают 1,30 г (71%) кристаллического соединения IVб с т. пл. 160-161оС.
Найдено, С 61,63; Н 3,70; Br 21,52.
C19H13BrO3 (М 369,20).
Вычислено, С 61,81; Н 3,55; Br 21,64.
ИК-спектр, ν, см-1 (кристаллы): 1688 (C30), 1630 (СОС6Н4Br-4), 1585 (С= С).
Спектр ПМР, δ, м. д. (CDCl3): 2,37 с (3Н, СН3), 6,18 с (1Н экзо-СН=), 6,80 с (1Н, С4Н), 7,35-7,80 м (ОН, 2Н6Н4).
В качестве среды для проведения реакции выбран неполярный растворитель бензол. Осуществить реакцию в среде полярного растворителя (вода, спирты, ацетон, диметилформамид) невозможно, так как исходные вещества 5-арил-2,3-дигидро-2,3-фурандионы взаимодействуют с ними уже при комнатной температуре с образованием различных продуктов дециклизации, в то время как ароилметилентрифенилфосфораны подвергаются разложе- нию с образованием трифенилфосфиноксида при кратковременном нагревании с этими растворителями. С другой стороны, исходные вещества нерастворимы или труднорастворимы в эфире, гексане, дихлорэтане или тетрахлорметане.
П р и м е р 4. 1-п-Бромфенил-6-п-толил-3,4-дигидрокси-2,4-гексадиен-1,6-дион (Iб).
К раствору 1,85 г (0,005 моль) 2-п-бромбензоилметилен-5-п-толил-2,3-дигидро-3-фуранона (IIб) в 150 мл ацетона при температуре 40оС добавляют при перемешивании 2 мл (0,02 моль) соляной кислоты. Осадок отфильтровывают и перекристаллизовывают из смеси хлороформ-гексан, 1:1. Получают 1,70 г (88%) кристаллического соединения Iб с т. пл. 230-231оС (разложение).
Найдено, С 59,07; Н 4,01; Br 20,55.
C19H15BrO4 (М 387,22).
Вычислено, С 58,93; Н 3,90; Br 20,63.
ИК-спектр, ν, см-1 (кристаллы): 1587-1600 (СО хелат).
Спектр ПМР, δ, м.д. (ДМСО-Д6): 2,40 с (3Н, СН3), 6,90 с (1Н, СН), 7,05 с (1Н, СН), 7,40-8,10 м (10Н, 2С6Н4, 20Н).
В качестве среды для проведения гидратации в условиях кислотного катализа промежуточных метиленфуранонов IV выбран ацетон. С рядом неполярных и слабополярных растворителей бензолом, толуолом, ксилолом, гексаном, эфиром, дихлорэтаном, хлороформом, тетрахлорметаном не смешивается используемая в реакции соляная кислота, что препятствует осуществлению процесса. В воде нерастворимы исходные соединения для второй стадии 5-арил-2-ароилметилен-2,3-дигид- ро-3-фураноны (IV). Целевые продукты I реакции растворимы в спиртах и полностью не осаждаются, что резко снижает их выход.
П р и м е р 5. 2-п-Хлорбензоилметилен-5-п-хлорфенил-2,3-дигидро-3-фуранон (IVв).
К раствору 1,04 г (0,005 моль) 5-п-хлорфенил-2,3-дигидро-2,3-фурандиона IIв в 100 мл бензола при температуре 75оС добавляют при перемешивании 2,07 г (0,005 моль) п-хлорбензоилметилентрифенилфосфора-на (IIIб). Растворитель испаряют и остаток перекристаллизовывают из хлороформа. Получают 1,62 г (94% ) кристаллического соединения IVв с т. пл. 184-185оС.
Найдено, С 72,70; Н 3,11; Cl 20,43.
C18H10Cl2O3 (М 345,19).
Вычислено, С 62,63; Н 2,92; Cl 20,54.
ИК-спектр, ν, см-1 (кристаллы): 1692 (С3=0), 16345 (СОС6Н4Cl-4), 1590 (С=С).
Спектр ПМР, δ, м.д. (CDCl3): 6,31 с (1Н, экзо-СН=), 6,97 с (1Н, С4Н), 7,60-8,00 м (8Н, 2С6Н4).
П р и м е р 6. 1,6-Бис-(n-хлорфенил)-3,4-дигидрокси-2,4-гексадиен-1,6-дион (Iв).
К раствору 1,72 г (0,005 моль) 2-п-хлорбензоилметилен-5-п-хлорфенил-2,3-дигид- ро-3-фуранона (IVв) 150 мл ацетона при температуре 45оС добавляют при перемешивании 2 мл (0,02 моль) соляной кислоты. Осадок отфильтровывают и перекристализовывают из хлороформа. Получают 1,67 г (92%) кристаллического соединения Iв с т. пл. 246-247оС (разложение).
Найдено, С 59,42; Н 3,49; Cl 19,68.
C18H12Cl2O4 (М 363,21).
Вычислено, С 59,53; Н 3,33; Cl 19,52.
ИК-спектр, ν, см-1 (кристаллы): 1590-1610 (СО хелат).
Спектр ПМР, δ, м.д. (ДМСО-Д6): 6,95 с (1Н, СН), 7,12 с (1Н, СН), 7,30-7,90 м (10Н, 2С6Н4, 20Н).
Выходы продуктов реакции по стадиях в зависимости от температуры процесса представлены в таблице.
Соединения I и IV проявляют противомикробное (бактериостатическое) действие по отношению к эталонным штаммам золотистого стафилококка (гранулоположительные бактерии) и кишечной палочки (грамотрицательные бактерии), что выражается в задержке роста бактериальных культур. Так, соединение Iа проявляет активность при минимальной ингибирующей концентрации (МИК) 1000 мкг/мл по отношению к золотистому стафилококку и 500 мкг/мл по отношению к кишечной палочке, а соединение IV при МИК 125 мкг/мл по отношению к штаммам обеих культур.
Заявляемый способ по сравнению с прототипом имеет следующие преимущества: он простой по выполнению, не длительный, токсичные реагенты отсутствуют, способ предоставляет возможность получения широкого ряда 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов с различными заместителями в бензольных кольцах.
Таким образом, способ получения 1,6-диарил-2,4-дигидрокси-2,4-гексадиен-1,6-дионов может найти применение как в лабораторных, так и промышленных условиях синтеза биологически активных веществ, поскольку эти соединения, а также промежуточные продукты для их синтеза 5-арил-2-ароилметилен-2,3-дигидро-3-фураноны сами являются активными, а также могут служить исходными соединениями для синтеза биологически активных веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5-АРИЛ-2-ГИДРОКСИ-2- (ТРИФЕНИЛФОСФОРАНИЛИДЕН) -МЕТОКСИКАРБОНИЛМЕТИЛ- 2,3-ДИГИДРО-3-ФУРАНОНОВ | 1990 |
|
RU2009144C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-БИС-АРОИЛМЕТИЛЕН-1,2,3,4-ТЕТРАГИДРОХИНОКСАЛИНОВ | 1991 |
|
RU2009136C1 |
| N-ЗАМЕЩЕННЫЕ АМИДЫ 2-ГИДРОКСИ-4-ОКСО-4-(4-ХЛОРФЕНИЛ)2-БУТЕНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОМИКРОБНУЮ АКТИВНОСТЬ | 2009 |
|
RU2429225C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АРИЛ-2,3-ДИГИДРО-2,3-ФУРАНДИОНОВ | 1990 |
|
SU1727378A1 |
| 2-МЕТОКСИКАРБОНИЛМЕТИЛЕН-4-БРОМ-5-АРИЛ-2,3-ДИГИДРОФУРАН-3-ОНЫ, ПРОЯВЛЯЮЩИЕ АНТИСТАФИЛОКОККОВУЮ АКТИВНОСТЬ | 1987 |
|
SU1455617A1 |
| ЭТИЛОВЫЕ ЭФИРЫ 2-АМИНО-1-БЕНЗОИЛАМИНО-4-ОКСО-5-(2-ОКСО-2-АРИЛ-ЭТИЛИДЕН)-4,5-ДИГИДРО-1H-ПИРРОЛИДИН-3-КАРБОНОВЫХ КИСЛОТ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2607920C2 |
| 2-АРОИЛМЕТИЛЕН-2, 4-ДИГИДРО-1Н-3,1-БЕНЗОКСАЗИН-4-ОНЫ, ПРОЯВЛЯЮЩИЕ ФЛУОРЕСЦЕНТНЫЕ СВОЙСТВА, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2276667C1 |
| 2,2,5,5-ТЕТРАБРОМ-1,6-ДИ-(4-МЕТИЛФЕНИЛ)-1,3,4,6-ГЕКСАНТЕТРАОН (I), ОБЛАДАЮЩИЙ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2303025C2 |
| СПОСОБ ПОЛУЧЕНИЯ E-2-АРОИЛМЕТИЛЕН-1-ФЕНИЛ-1,2,3,4-ТЕТРАГИДРОХИНАЗОЛИН-4-ОНОВ | 2006 |
|
RU2306315C1 |
| 1,1'-ДИАРИЛ-3'-АРОИЛ-4'-ГИДРОКСИ-1H-СПИРО[ИНДЕНО[1,2-b]ПИРРОЛ-3,2'-ПИРРОЛ]-2,4,5'-(1'H)-ТРИОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2467011C1 |
Изобретение касается органической химии, в частности способа получения 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов, которые являются полупродуктами для синтеза пестицидов и используются для получения термостабильных полимеров и полихелатов металлов. Цель - упрощение технологии процесса и увеличение выхода целевого продукта. Это достигается способом получения 1,6-диарил-3,4-дигидрокси-2,4-гексадиен-1,6-дионов общей формулы
4-R′C6H4-COOH = C(OH)C(OH) = CHCO-C6H4R″-4
где R′ = H; CH3; R″ = Br; R′ = R ″ = Cl взаимодействием 5-арил-2,3-дигидро-2,3-фурандиона общей формулы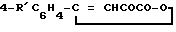
где R1 имеет указанные значения, с органическим реагентом при повышенной температуре в среде органического растворителя. В качестве органического реагента используют ароилдиметилентрифенилфосфоран общей формулы
C6H5)3P = CHCOC6H4R″-4
где R2 имеет указанные значения, который взаимодействует с 5-арил-2,3-дигидро-2,3-фурандионами при мольном соотношении, равном 1 : 1, соответственно при температуре 70 - 80oС с использованием в качестве органического растворителя бензола с получением 5-арил-2-ароилметилен-2,3-дигидро-3-фуранона общей формулы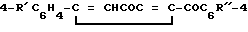
где R1 и R2 имеют указанные значения, который подвергают взаимодействию с соляной кислотой при мольном соотношении 1 : 4, соответственно при температуре 40 - 50oС с использованием в качестве органического растворителя ацетона. Эти условия позволяют получать целевой продукт с выходом до 95% и упрощают технологию за счет отсутствия токсичных реагентов. 1 табл.
СПОСОБ ПОЛУЧЕНИЯ 1,6-ДИАРИЛ-3,4-ДИГИДРОКСИ-2,4-ГЕКСАЛИЕН-1,6-ДИОНОВ общей формулы
где R′ - Н, СН3, R″-Br, R′=R″-Cl,
взаимодействием 5-арил-2,3-дигидро-2,3-фурандиона общей формулы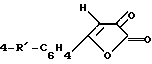
где R′ имеет указанные значения,
с органическим реагентом при повышенной температуре в среде органического растворителя, отличающийся тем, что, с целью упрощения технологии процесса и увеличения выхода целевого продукта, в качестве органического реагента используют ароилметилентрифенилфосфоран общей формулы
(C6H5)3P=CHCOC6H4R″-4,
где R, , имеет указанные значения,
который взаимодействует с 5-арил-2,3-дигидро-2,3-фурандионами при мольном соотношении, равном 1 : 1, при температуре 70 - 80oС с использованием в качестве органического растворителя бензола с получением 5-арил-2-ароилметилен-2,3-дигидро-3-фуранона общей формулы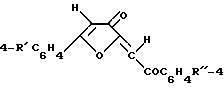
где R′ и R′′ имеют указанные значения,
который подвергают взаимодействию с соляной кислотой при мольном соотношении, равном 1 : 4, при температуре 40 - 50oС с использованием в качестве органического растворителя ацетона.
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Фридман А.Л., Залесов В.С., Конышина Л.О., Плаксина А.Н., Баргтейл Б.А., Кратынская Л.В., Рубинштейн Л.М., Химико-фармацевтический журнал | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
Авторы
Даты
1996-02-27—Публикация
1990-06-14—Подача