Изобретение относится к области технологии химических реактивов, в частности оксид-сульфата ниобия (V), применяемого в радиоэлектронной промышленности при изготовлении конденсаторов, варисторов и других изделий.
Известен способ получения оксид-сульфата ниобия путем взаимодействия оксида серы (VI) с хлоридом ниобия (V), растворенным в хлориде сульфурила. Недостатком способа является сложность и длительность процесса.
Техническим решением наиболее близким к заявляемому, является способ получения оксид-сульфата ниобия (V), заключающийся в обработке оксида ниобия серной кислотой при нагревании, фильтрации, промывке и сушке осадка,
Основным недостатком способа является его большая продолжительность.
Цель изобретения - ускорение процесса.
Поставленная цель достигается тем, что продукт получают взаимодействием оксида ниобия (V) в присутствии пероксида водорода с серной кислотой, с последующей фильтрацией, промывкой и сушкой осадка. Молярное соотношение между оксидом ниобия (V) и пероксидом водорода должно быть равно 1:(81-90).
Отличительным признаком изобретения является то, что процесс взаимодействия оксида ниобия с серной кислотой проходит в присутствии пероксида водорода при мольном соотношении Nb20s:H202 1:81-90.
Пример 1.8 трехгорлую колбу емки- стью 0,5 дм3, снабженную обратным холодильником, капельной воронкой, мешалкой и термометром, вносят 10,0 г оксида ниобия (V) (0,0376 моль) и 160 см3 HzS04 плотностью 1860 кг/м3. Колбу нагревают на песчаной бане, а когда температура содержимого достигает (130± 5)°С включают мешалку и (через один из отростков колбы) медленно
сл С
vj 00 4 СЛ 00 hO
приливают(из капельной воронки)50%-ный раствор пероксида водорода (плотность 1196,6 кг/м. Общее количество пероксида водорода, использованного при проведении процесса, составляет 173 см (3.043 моль). Соотношение между оксидом ниобия (V) и пероксидом водорода равно 1:81. Процесс проводят в течение 16ч. Затем обогрев отключают и дают возможность содержимому колбыЧ ладиться до температуры окружающей среды. Образовавшийся оксидсульфат ниобия (V) оседает на дно колбы.
Непрореагировавшую серную кислоту сливают с осадка, который в дальнейшем промывают холодной (25-30)°С водой-декантацией, затем отсасывают на воронке Бюхнера и вновь промывают. Промывку продолжают до тех пор , пока в промывных водах будет наблюдаться наличие только следов сульфат-ионов (качественная проверка с раствором хлорида бария). Потом осадок выдерживают в сушилке при 100- 120°С до сухого рассыпчатого состояния. Выход продукта (белого порошка) равен 98%.
Рентгенофазовый анализ полученного материала, проведенный при помощи диф- рактометра ДРОН-2,0(Сика -излучение, никелевый фильтр), показал, что он полностью идентичен продукту, получаемому в соответствии с прототипом. Химический анализ данного реактива приведен втабл 1.
Пример 2. В колбу емкостью 0,5 дм , снабженную обратным холодильником и мешалкой, вносят 10,0 г оксида ниобия (V) (0,037 моль Nb20s) и 160 см3 серной кислоты, плотность которой равна 1860 кг/м3. Колбу нагревают на песчаной бане до 130 + 5°С. Процесс проводят (при перемешивании содержимого реакционного сосуда) не менее 630 ч. Затем обогрев отключают и содержимое колбы охлаждают до температуры окружающей среды. Осадок промывают водой (25-30°С) до тех пор, пока в промывной жидкости будут наблюдаться только следы сульфат-ионов (качественная проверка с раствором хлорида бария). Осадок сушат при 100-120°С, Полученный продукт, выход которого равен 96%, удовлетворяет требованиям, предъявляемым к оксид-сульфату ниобия (V) квалификации
чистый.
Последующие опыты проводили в аналогичных условиях, меняя мольные отношения реагентов и продолжительность обработки.
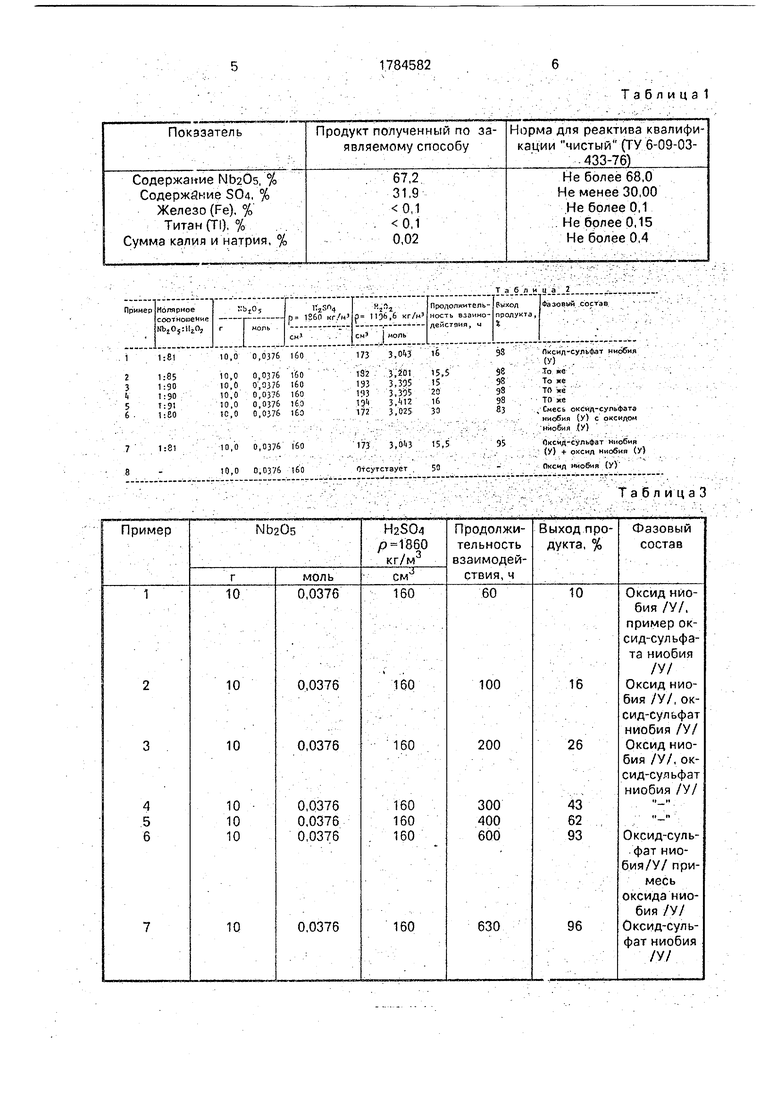
Результаты опытов представлены в табл.2.3.
В табл.2 представлены опыты, проведенные по предлагаемому способу, в табл.3 - по прототипу.
Как показано в табл.2, поставленная цель достигается лишь в том случае, если навеску оксида ниобия (V) обработать НаЗОз в присутствии пероксида водорода, взятом в объеме, обеспечивающем мольное соотношение израсходованных веществ МЬ20б:Н202 1:81-90 ( примеры 1-4). Снижение вышеуказанного количества HteOa в системе Nb20s:H202 1:80 не дает возможности полного завершения процесса и получения качественного продукта (пример 6). Увеличение количества пероксида водорода, поступающего в зону реакции (Nb20s:H202 1:91), не оказывает заметного положительного влияния на процесс получения оксид-сульфата ниобия (V) и связано только лишь с нерациональным расходованием данного реагента (пример 5), При этом следует отметить, что продолжительность 15 ч обработки порошка оксида ниоибя (V)
не сказывается на качестве и выходе конечного продукта.
Предлагаемый способ эффективнее известного, так как синтез оксид-сульфата ниобия (V) осуществляется (в 2 раза) быстрее.
Формулаизобретения
Способ получения оксид-сульфата ниобия (V), включающий обработку оксида ниобия (V) серной кислотой при нагревании, фильтрацию, промывку и сушку образовавшегося осадка, отличающийся тем, что, с целью ускорения процесса, обработку проводят в присутствии пероксида водорода при молярном соотношении оксид ниобия (/):пероксид водорода 1:(81-90).
Т а б л и ц а 1

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НАНОПОРОШКОВ ОКСИДА ИТТРИЯ | 2006 |
|
RU2354610C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АЛКИЛ-5,6,7,8-ТЕТРАГИДРО-9,10-АНТРАХИНОНА | 1992 |
|
RU2080316C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОР-2-МЕТИЛ-3-ОКСАГЕКСАНОИЛПЕРОКСИДА | 2002 |
|
RU2213730C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ЦИНКА | 2011 |
|
RU2467952C1 |
| СТАБИЛЬНЫЙ РАСТВОР ПЕРОКСИДА ЦИКЛОГЕКСАНОНА, НЕ КРИСТАЛЛИЗУЮЩИЙСЯ ДО ТЕМПЕРАТУРЫ МИНУС 20°С И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1993 |
|
RU2046793C1 |
| Способ получения ацетата или оксалата свинца из его оксида (II) | 2023 |
|
RU2807759C1 |
| СПОСОБ ОБЕССЕРИВАНИЯ СЫРОЙ НЕФТИ ПЕРОКСИДОМ ВОДОРОДА С ВЫДЕЛЕНИЕМ ПРОДУКТОВ ОКИСЛЕНИЯ | 2017 |
|
RU2677462C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ХИТОЗАНА | 2010 |
|
RU2417088C1 |
| СПОСОБ ОБРАБОТКИ ГАЗА, СОДЕРЖАЩЕГО ОКСИДЫ АЗОТА (NOx), В КОТОРОМ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ОКСИД ЦЕРИЯ И ОКСИД НИОБИЯ, ПРИМЕНЯЕТСЯ В КАЧЕСТВЕ КАТАЛИЗАТОРА | 2011 |
|
RU2541070C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАНСУЛЬФОКИСЛОТЫ | 2016 |
|
RU2648245C2 |

Показатель
Продукт полученный по заявляемому способу
Содержание Nb20s, %
Содержйкие S04, %
Железо (Fe), %
Титан (TI), %
Сумма калия и натрия, %
Норма для реактива квалификации чистый (ТУ 6-09-03- 433-76)
Не более 68,0 Не менее 30,00
Не более 0,1 Не более 0,15
Не более 0,4
ТаблицаЗ
| ГорощенкоЯ.Г | |||
| Химия ниобия и тантала | |||
| Киев; Иаукова Думка, 1965, с.349 | |||
| Горощенко Я.Г | |||
| Физико-химические исследования переработки редкоземельных титанониобатов сернокислотным методом | |||
| М.-Л.: Изд-во АН СССР, 1960, с.28-30 |
Авторы
Даты
1992-12-30—Публикация
1990-09-05—Подача