Изобретение относится к кормопроизводству.
Цель изобретения - повышение стабильности состава в рубце и сычуге и выделения биологически активного вещества в тонком кишечнике.
Изобретение иллюстрируется следующими примерами.
Пример 1. Используя технику капсу- лирования пульверизацией, получают гранулы из метионина, покрытого оболочкой из композиции, состоящей из зеина 69,2%, этилцеллюлозы № 22 (Геркулес)23% и триа- цетина 7,7%. Содержание метионина в покрытых гранулах 72%.
Для сравнения изготавливают гранулы с метионином, покрытым оболочкой из следующей композиции по прототипу:
Гранулы А: этилцеллюлоза № 100 (Гер кулес) 80%. сополимер стирол-2-винил-пи- ридин (30-70) 20%; содержание метионина в покрытых гранулах 70%.
Гранулы В: этилцеллюлоза № 100 (Геркулес) 58,3%, сополимер стирол-2-винил- пиридин (30-70) 25%, пропиленгликолЬ 16,7%; содержание метионина в покрытых гранулах 73%,
Различные покрытые гранулы, изготовленные подобным образом, подвергаются тестам in vitro и In vivo.
1. Тест In vitro.
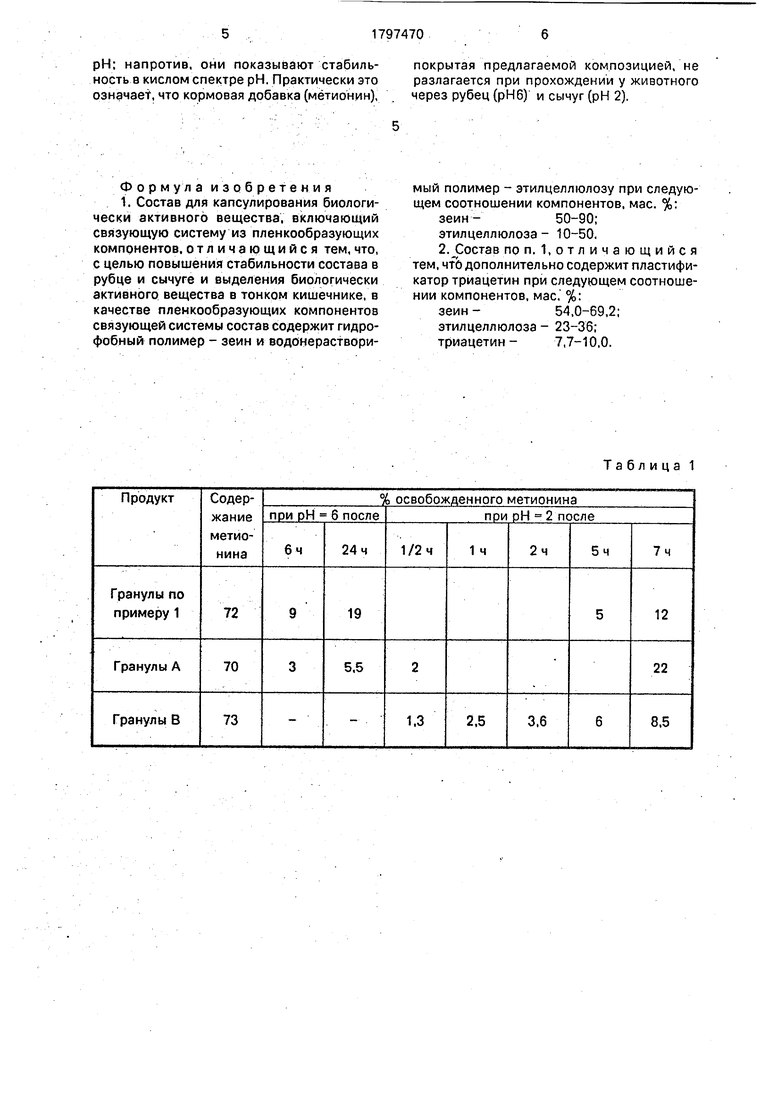
Высаливание метионина, содержащегося в получаемых гранулах, определяют при перемешивании известного количества гранул в буферной среде, поддержания постоянным рН при температуре 40°С.
. Сравнивают скорости высаливания образца при различных рН. Полученные результаты отражены в табл. 1,
2. Тест In vivo.
Определяют стойкость гранул к пребыванию в рубце, в сычуге, затем в тонкой кишке у барана, измеряя количество общего
Х|
Ю
2
3
со
азота, исчезнувшего из мешочков, после каждого из трех последовательных этапов.
2.1. Переваривание в рубце.
Нейлоновые мешочки (квадратная петля 46 микрон), содержащие каждый прибли- ительно 3 г покрытия, точно взвешенные, помещают на 12 ч в рубец двух баранов из расчета два мешочка на продукт и на барана.
После инкубации в рубце мешочки промывают холодной водой, затем сушат в течение 48 ч.
Мешочки развешивают и определяют количество исчезнувших гранул. Остатки затем вынимают из мешочков и отбирают двойную пробу для дозировки общего азота.
Оставшиеся продукты объединяют по видам продуктов и помещают вновь в нейлоновые мешочки.для йнкубации в сычуге.
2.2. Переваривание в сычуге.
Три нейлоновых мешочка (квадратные петли по 46 микрон), размер которых составляет половину ранее использованных мешочков для переваривания в рубце, содержащие приблизительно 0,5 г остатков, применяют для каждой продолжительности инкубации и для каждого исследуемого продукта.
Эти мешочки, закрепленные на веревке, вводят в сычуг 3 баранам с трубкой для размещения в сычуге (внутренний диаметр 28 мм). Устанавливают тот же режим питания из расчета 1 мешочек на барана и на продукт.
После инкубации в течение 0.5 ч, 2 ч и 4 ч мешочки промывают, высушивают и взвешивают.
Остатки, с одной стороны, отбирают в виде проб, для дозировки азота и, с другой стороны, используют для анализа переваривания в тонкой кишке.
2.3. Переваривание в тонкой кишке.
Остатки, полученные выше, объединяют в соответствии со временем инкубации и согласно продуктам. Их помещают в нейлоновые микропакеты (диски диаметром 20 мм; квадратные петли 46 микронов) из расчета 200 мг остатков в пакете и 3 пакета на все время инкубации.
Эти пакеты вводят в начале тонкой кишки (двенадцатиперстная кишка) трем баранам, находящимся на одном и том же режиме питания с простой трубкой на уровне двенадцатиперстной кишки (5 см привратника желудка, 12 мм внутренний диаметр), и повторно вводят трубки (18 мм внутренний диаметр) в конце тонкой кишки (подвздошная кишка).
Остатки каждого типа покрытия изучались 2 по 2 в течение двух циклов измерения, каждое животное получало 1 пакет каждой из 6 обработок (2 покрытия х 3 продолжительности инкубации в сычуге).
Каждое животное получало 6 пакетов с
интервалом 15 мин.
3 ч спустя после начала введения .повторно вводимую трубку открывают и содержимое, относящееся к подвздошной кишке, свободно вытекает наружу из животного.
Пакеты вынимают после продолжительности прохождения от 3,5 до 8 ч. Пакеты собирают и подвергают анализу, как и в предшествующих тестах.
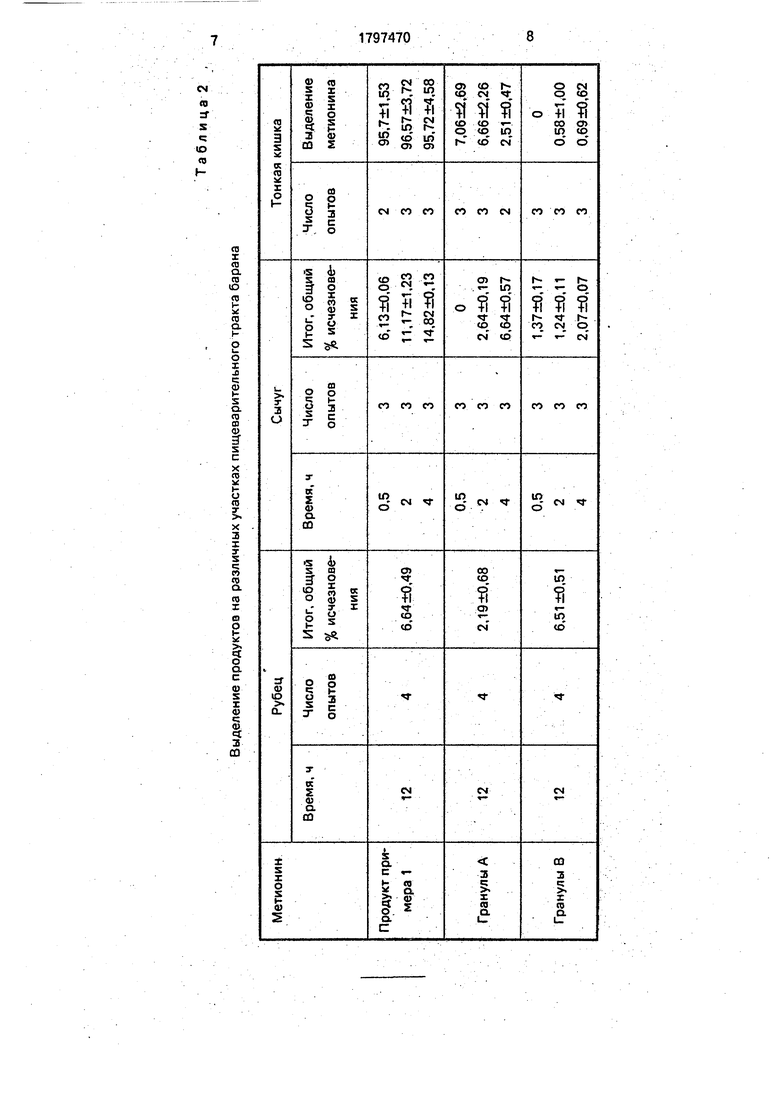
Полученные результаты приведены в
табл.2., Пример- 2. В смеси из 500 см3 дихлорметана и 500 см3 абсолютного этано- ла растворяют 22 г зеина и 88 г стеариновой чистой кислоты.
Полученный раствор напыляют методом аэрозольного напыления на 350 г мёти- онина в виде гранул, средний диаметр которых составляет 0,5-0,63 мм. Получают, таким образом, гранулы в оболочке, где содержание метионина составляет 74,5%.
Количество выделенного метионина из гранул после 24 ч при 40°С в водной буферной среде составляет при рН 6 (рубец) 6% и при рН 2 (сычуг) 7%.
После пребывания в течение 48 ч в рубце овцы содержание остаточного метионина 68,0 ±6%.
Выделение метионина в тонком кишечнике 96% ±4,0.
.Пример 3. В смеси, состоящей из 500 см3 дихлорметана и 500 см3 абсолютного этанола, растворяют 14 г зеина, 88 г чистой стеариновой кислоты и 8 г этилцеллюлозы № 22.
Полученный раствор напыляют методом аэрозольного напыления на 350 г хлор- гидрата лизина в виде гранул, средний диаметр которых близок 0.8 м. Получают, таким образом, гранулы в оболочке, где содержание хлоргидрата лизина составляет
69,4%.:
.Количество хлоргидрата лизина, выделенного из гранул после 24 ч, при 40°С в буферной среде составляет при рН б 2,6% и прирН26%.
После пребывания в течение 48 ч в рубце овцы процент хлоргидрата остаточного лизина 78,0 ±2%,
Результаты примера 4 представлены в табл. 3.
Результаты показывают стойкость.оболочки к среде с рН 6, С учетом примера 1 результаты показывают, что предлагаемые композиции не чувствительны к изменению
рН; напротив, они показывают стабильность в кислом спектре рН. Практически это означает, что кормовая добавка (метионин),
покрытая предлагаемой композицией, не разлагается при прохождении у животного через рубец (рН6) и сычуг (рН 2).


| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ ДЛЯ КАПСУЛИРОВАНИЯ БИОЛОГИЧЕСКИ-АКТИВНОГО ВЕЩЕСТВА | 1992 |
|
RU2038025C1 |
| Способ нанесения покрытия на действующее начало | 1991 |
|
SU1816212A3 |
| Способ получения кормовых гранул для жвачных животных | 1987 |
|
SU1651775A3 |
| Состав для капсулирования биологически-активного вещества | 1990 |
|
SU1809752A3 |
| КОРМОВАЯ ИЛИ МЕДИКАМЕНТОЗНАЯ КОМПОЗИЦИЯ ДЛЯ ЖВАЧНЫХ ЖИВОТНЫХ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2106096C1 |
| Способ получения органорастворимых производных хитозана | 1989 |
|
SU1823878A3 |
| Состав для капсулирования биологически активного вещества | 1987 |
|
SU1748630A3 |
| Способ получения кормовых гранул для жвачных животных | 1989 |
|
SU1809751A3 |
| СПОСОБ НАНЕСЕНИЯ ПОКРЫТИЙ ЛЕКАРСТВЕННЫЙ И/ИЛИ КОРМОВЫХ ВЕЩЕСТВ | 1991 |
|
RU2076701C1 |
| СПОСОБ УЛУЧШЕНИЯ РАЦИОНОВ ОВЕЦ И КОРМОВАЯ ДОБАВКА | 1992 |
|
RU2060682C1 |
Использование: кормопроизводство. Сущность изобретения: состав для капсули- рования биологически активного вещества включает связующую систему из пленкообразующих компонентов, в качестве которых используют гидрофобный полимер - зеин и водонерастворимый полимер - этил- целлюлозу при следующем соотношении компонентов, мае. %: зеин 50,0-90,0; этил- целлюлоза 10,0-50,0, и дополнительно пластификатор - триацетин в количестве 7,7-10,0%.3 табл.
Формула изобретения 1. Состав для капсулирования биологически активного вещества, включающий связующую систему из пленкообразующих компонентов,отличающийся тем,что, с целью повышения стабильности состава в рубце и сычуге и выделения биологически активного вещества в тонком кишечнике, в качестве пленкообразующих компонентов связующей системы состав содержит гидрофобный полимер - зеин и водонерастворимый полимер - этилцеллголозу при следующем соотношении компонентов, мае. %:
зеин-50-90;
этил целлюлоза - 10-50.
зеин -54,0-69,2;
этил целлюлоза - 23-36;
триацетин- 7,7-10,0.
Таблица 1
Выделение продуктов на различных участках пищеварительного тракта барана
Компонент
Зеин Этилцеллюлоза
Триацетин
% метионина в гранулах
Выделение при рН 6 за
6ч
24ч
1797470
10 Таблица 3
Содержание. %
54
36
10
8
14
| СПОСОБ ПРОИЗВОДСТВА ТАБАЧНОГО СЫРЬЯ | 2009 |
|
RU2401621C1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
Авторы
Даты
1993-02-23—Публикация
1988-12-14—Подача