Изобретение относится к области органической химии, конкретно к новым замещенным пиразолам общей формулы I:
Н3С CH2-CH -S-R
Ґси3 н
где: R СбН4Р(а); С3Н7(б); С4Н9(Ь) обладающими антигрибковой активностью.
Целью изобретения является получение новых замещенных пиразолов, обладающих высоковыраженным антигрибковым действием.
Поставленная цель достигается предложенными соединениями (I), полученные взаимодействием 3,5-диметил-4- -бромэ- тил)пиразола с п-фтортиофенолом, пропил- меркаптаном и с бутилмеркаптаном с
выходом 43,4-81,7% в среде пропилового спирта в присутствии едкого натра.
Для лучшего понимания данного изобретения приводятся следующие примеры получения замещенных пиразолов 3,5-ди- метил-4-{2-п-фторфенилтиоэтил)пиразол(1а), 3,5-Диметил-4- 8 - пропилтиоэтил)пиразол (16), 3,5-диметил-4- -бутилтиоэтил)пиразол (1в) и испытания их на антигрибковую активность.
Пример. 3,5-Диметил-4-(2-п-фторфе- нилтиоэтил)пиразол. (la).
HjC-Tj-ji-CHj-CHfS-CgH F
JEJ
N I
Н
сьь
сл
С
00
ю
CJ Ю С
К 3,2 г (0,0025 моль) п-фтортиофенол добавляют 1 г (0,025 моль) едкого натра и 30 мл пропилового спирта. Далее при перемешивании постепенно приливают 5 г (0,025 моль)
спиртовой раствор 3,5-диметил-4- 7-бромэ- тил)пиразола и еще перемешивают 3-4 ч при температуре 80°С, После охлаждения реакционной массы добавляют 50 мл диэтилово- го эфира и промывают водой. Органическую часть перегоняют получают 4 г (67,7%) 3,5- диметил-4-(2-п- фторфенилтиоэтил)пиразо- ла с Т.пл, 69-70°С. Элементный анализ:
Найдено, %: С 61,98; Н 5,74; N 11,03; S 12,54.
Ci3Hi5N2SF
Вычислено, %: С 62,40; Н 6,00; N 11,20; S 12,80
ИГ-спектры: 635 (-CH2-S); 810-1605
N
N Н
ЯМР спектры: 2,04 (6Н, 2СН3С), 2,56 (2Н,т.СН2С), 2,71 (2Н,т.СН25), 6,76 и 7,12 (4Н,СбН4). 12.75 (1H,NH).
3,5-диметил-4-# -пропилтиоэтил)пира- зол. (16).
H3C..CH2-CH2-S-C3H-7
Н
К 1,87 г (0,02 моль) пропилмеркаптана добавляют 0,95 г (0,02 моль) едкого натра и 30 мл пропилового спирта. Далее при перемешивании постепенно приливают 5 г (0,02 мол ь) спи ртовой раствор 3,5-диметил-4-( -бро- мэтил)пиразола и еще перемешивают 3-4 ч при температуре 80°С. После охлаждения реакционной массы добавляют 50 мл диэ- тилового эфира и промывают водой. Органическую часть перегоняют получают 2 г (43,4%) 3,5-диметил-4-( -пропилтиоэтил)пи- разола с Т.кип. 180-183/3-мм, Н20о 1,5280. d 4 1,1128. Элементный анализ:
Найдено, %; С 66.57; Н 9,03: N 13,96; S 15,78.
CioHieN2S.
Вычислено,%: С 60.51; Н 9.09; N 14,14; S 16,16.
ИГ-спектры: 635(), 810-1605
N Н
ЯМР спектры: 0.89 (ЗН,т.СНзСН2); 1,55 (2Н,м. СН2СНз); 2,14 (6Н,2СНзС), 2.382Н,т.СН2С); 2,45(4Н,т.СН25СН2), 12.38 (1H.NH).
3,5-диме1Ил-4- 3 -бутилтиоэтил) зол. (Ib).
Н,ССН9-СН9-5-СлН9
3w 2 2
ЛН3
I Н
К 1.8 г (0,02 моль) бутилмеркаптан добавляют 0,8 г (0,02 моль) едкого натра и 30 мл пропилового спирта. Далее при перемешивании постепенно приливают 4 г (0.02 моль) спиртовой раствор 3,5-диметил-4- (З-бромэтил)пиразола и еще перемешивают 3-4 ч температуре 80°С. После охлаждения реакционной массы добавляют 50 мл диэти- лового эфира и промывают водой. Органическую часть перегоняют получают 3,35 г (81,7%) 3,5-диметил-4- 3 -бутилтиоэтил)пира- золасТкип. 196-200/2 ммрт.ст. Н20о 1,5290, d204 1,0058. Элементный анализ.
Найдено, %: С 61,94; Н 9,13; N 13,11; S 14,58.
CnH20N2S
Вычислено, %: С 62,26; Н 9,43; N 13,21; S 15,09.
ИГ-спектры: 638 (CH2-S), 810-1610
JU
V
Н
ЯМР-спектры:0,82(ЗН,т.СНзСН2), 1,40(4Н,м, (), 2,12 (6Н,2СНзС), 2.36 (2Н,т.СН2С), 2,44(4Н,т.СН25-СН2), 12,23 (1H.NH).
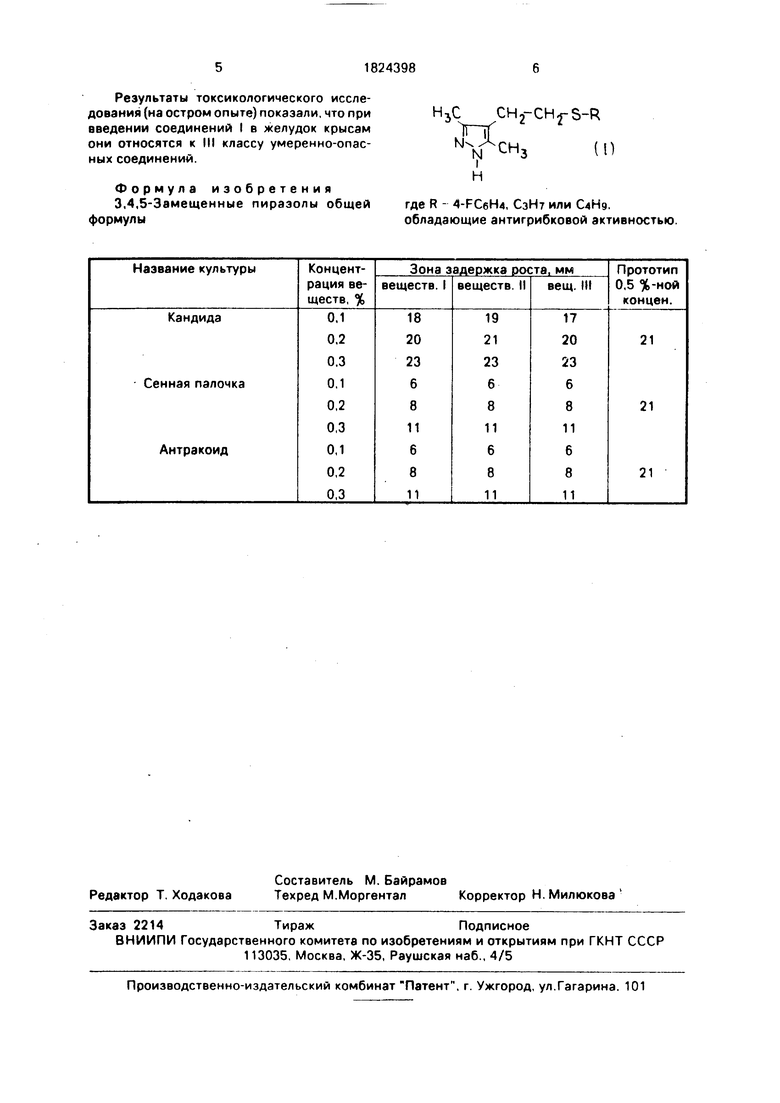
При изучении антигрибковой активности соединений I применен метод диффузии на агаре (дисковый). В качестве растворителя было взят спирто-водный раствор в соотношении с 12,5 мл этилового спирта и 11 мл дистиллированный воды. Результаты испытаний приведены в таблице.
Результаты опытов представленные в таблице, показали, что испытуемые соединения I в 0,1-0,3%-ной концентрации убивают бактерии кандида. сенная палочка и антракоид. Установлено, что 0.3% - концентрации-вещества I дает высокие зоны задержки роста 23 мм только против кан- дида.
Таким образом результаты проведенных испытаний позволяют заключить, что 3,5-диметил-4-(/3 -фторфенилтиоэтил)пира- зол (la), 3,5-диметил-4-(б -бутилтиоэтил)пи- разол (Ib) обладают эффективными антигрибковыми действиями.
Результаты токсикологического исследования (на остром опыте) показали, что при введении соединений I в желудок крысам они относятся к III классу умеренно-опасных соединений.
Формула изобретения 3,4,5-Замещенные пираэолы общей формулы
Н
ЪС CHj-CHj-S-R
N LA у
н
СН:
где R - 4-РСбНл, СзНт или СдНд. обладающие антигрибковой активностью.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения @ , @ -дизамещенных 1,8-диаминонафталинов | 1985 |
|
SU1318587A1 |
| 9,12- ДИНИТРО -14,14- ДИМЕТИЛ -4-ТИО -1,7-ДИАЗАТРИЦИКЛО [5,3,3,1]ТЕТРАДЕКАН | 1981 |
|
SU1025115A1 |
| Способ получения эфиров 2,6-диметил1,4-дигидропиридин-3,5-дикарбоновой кислоты | 1977 |
|
SU740768A1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-СУЛЬФАНИЛМЕТИЛПРОИЗВОДНЫХ 2,4-ПЕНТАНДИОНА, ОБЛАДАЮЩИХ ПРОТИВОГРИБКОВОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ TRICHOPHYTON TERRESTERE | 2015 |
|
RU2654851C2 |
| Способ получения 0,0-диэтил-S-(2-диалкиламиноэтил)тиофосфатов | 1989 |
|
SU1719404A1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АМИНОЗАМЕЩЕННЫХ 1-(1-АДАМАНТИЛ)-3,4-ДИНИТРО-1Н-ПИРАЗОЛОВ | 2013 |
|
RU2533557C1 |
| 2,2-ДИМЕТИЛ-1,2-ДИГИДРО-5-(N-МОРФОЛИНО)-8-ХЛОР- ИЛИ ФЕНИЛГИДРАЗИНО-4Н-ПИРАНО [4′,3′:4,5] ПИРИДО[2,3-B]ТИЕНО[3,2-D]-9,10,11-ТРИАЗИНЫ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВЫМ СВОЙСТВОМ | 1988 |
|
SU1570274A1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛО(3,4-B)ПИРИДИНА | 1989 |
|
RU2022964C1 |
| Производные S-пирролидонметил-цистеина в качестве промежуточных продуктов для синтеза цистинсодержащих пептидов | 1980 |
|
SU876641A1 |
| 5-АМИНОЗАМЕЩЕННЫЕ ТИЕТАНСОДЕРЖАЩИЕ 3-БРОМ-4-НИТРОПИРАЗОЛЫ С АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2801039C1 |
Использование изобретения: в качестве антигрибковых средств в медицине. Сущность изобретения: продукт V 3,4,5-заме- щенные пиразолы СН(СНз) ММНС(СНз) CCH2CH2SR, указано соединение, R, БФ, выход, %, т.пл., °С, или т.кип.: la, 4-F СбН4, Ci3Hi5FN2S, 69.69-70; 16, СзН, CioHi8N2S, 43, 180-183°С/3 мм рт.ст.; 1в, С4Н9, CnH2oN2S, 82, 196-200°С/1 мм рт.ст., соединения умеренно токсичны Реагент I: 3,5- диметил-4-(2-бромэтил)пиразол Реагент 2. 4-фтортиофенол. Условия реакциии: в среде пропилового спирта при 80°С. 1 табл

| Патент ГДР № 228248, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1993-06-30—Публикация
1991-04-29—Подача