Изобретение относится к гидрометаллургии платиновых металлов и может быть использовано в технологии концентрирования для переработки бедных концентратов.
Сущность предлагаемого способа, отличающая его от прототипа, заключается в том, что после химического растворения концентрата на неорганической основе (оксидной, гидроксидной, металлической, сульфидной) с получением солянокислого раствора в полученном растворе создают концентрацию НСl 2-6 моль/л при соотношении 2-3 г НСl/г концентрата, нагревают и поддерживают в состоянии кипения (100-110оС) в течение 1-4 ч для перевода платиновых металлов в анионные комплексы. После этого раствор охлаждают до комнатной температуры и создают в растворе рН (-0,2)-(+0,7) для полного отделения катионов материала сорбента. Затем раствор пропускают через колонку с катионитом, поглощающим катионы металла основы концентрата (Fe3+, Cu2+, Ni2+ и др.) в количестве, достаточном для полного их отделения. Фронтальный раствор, содержащий НСl, соли щелочных металлов и анионные комплексы платиновых металлов, подвергают следующей стадии концентрирования и новый концентрат подвергают повторному обогащению указанным образом и т.д. Каждая операция дает концентрирование по сравнению с предыдущим концентратом в 4-20 раз в зависимости от содержания ценных компонентов в исходном концентрате.
Предлагаемый способ позволяет производить неограниченное количество операций повторного концентрирования с постоянным уменьшением объема растворов и массы сорбента и возрастанием концентрации платиновых металлов в растворах и концентрате, благодаря чему может быть достигнута любая заданная степень концентрирования, причем конечным продуктом будет чистый солянокислый раствор платиновых металлов и NaCl.
Концентрирование платиновых металлов достигается последовательным чередованием операций осаждения последних на гидроксидах и их разделения.
Нижние пределы концентраций и продолжительности нагревания при переводе платиновых металлов в анионные комплексы при нагревании солянокислых растворов обусловлены кинетикой внедрения Сl во внутреннюю сферу и обратной реакции активации, а верхние экономией времени и реагентов (достаточностью) и условиями эффективного поглощения катионов металлов основы концентрата.
Предложенный способ не предусматривает выпаривания раствора, в связи с этим расход электроэнергии на подготовку раствора к разделению цветных и платиновых металлов снижается в 2,5-4,5 раз (от 700-800 до 150-300 ккал/л) и исключаются потери НСl и загрязнение окружающей среды.
Способ обработан в лабораторном масштабе на модельных индивидуальных и коллективных концентратах платиновых металлов на основе гидроксокарбонатов, р.з.э. и железа (III).
П р и м е р 1. Обогащение индивидуального концентрата иридия на основе смешанного гидроксокарбоната La, Ce и Pr. Модельный концентрат иридия получали из 300 мл раствора K2IrCl6 в количестве 1 г, вводя в концентрат 3,47 мг Ir. Концентрат растворили в 2 моль/л НСl, полученный раствор кипятили в течение 1 ч, охладили до комнатной температуры, установили в растворе рН 0,0, довели объем раствора до 50 мл. Для разделения Ir и La, Ce и Pr использовали стеклянную колонку с 8 г воздушно-сухого катионита КУ-2х8 в Н+-форме, длина слоя смолы 15 см, диаметр слоя 0,8 см. Скорость пропускания раствора ≈ 1 мл/мин (0,3 л/м2.с). В последних порциях фронтального раствора появились следы р. з.э. Во фронтальном растворе найдено 2,02 мг Jr, что соответствует степени извлечения 58,2%
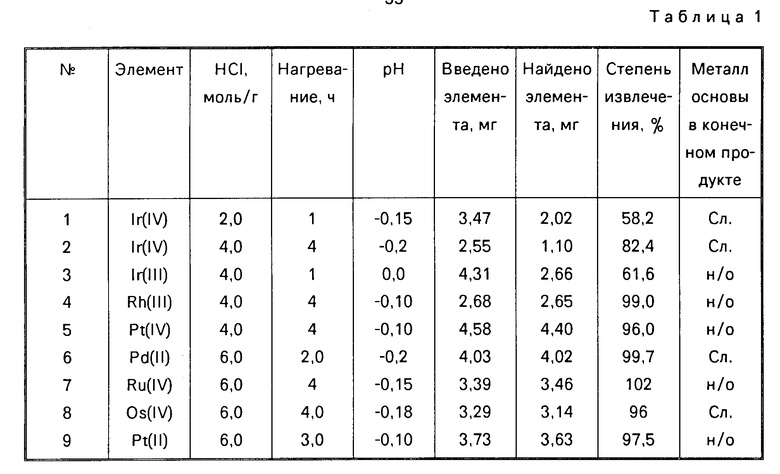
П р и м е р 2-9. Аналогично проведено обогащение модельных концентратов индивидуальных платиновых металлов на основе гидроксокарбоната La, Ce, Pr. Результаты представлены в табл. 1.
П р и м е р 10. Обогащение индивидуального концентрата рутения на основе гидроксида железа (III). Модельный концентрат рутения получали из 200 мл раствора К4Ru2OCl10 в количестве 1 г, введя в концентрат 2,5 мг Ru. Концентрат растворили в 2 моль/л НСl и далее по примеру 1 полученный раствор кипятили в течение 1 ч, охладили до комнатной температуры, установили в растворе рН + 0,1-0,5 и довели объем раствора до 50 мл. Для разделения Ru и Fe использовали стеклянную колонку с катионитом по примерам 1-9, но длина слоя катионита в колонке 50 см, а диаметр слоя 1 см. Скорость пропускания, как в примере 1. В последних порциях фронтального раствора появились следы Fe (III). Во фронтальном растворе найдено 1,6 мг Ru, что соответствует степени извлечения 64%
П р и м е р ы 11-15. Аналогично проведено обогащение модельных концентратов индивидуальных платиновых металлов на основе гидроксида железа (III). Результаты представлены в табл. 2.
П р и м е р 1-15 (табл. 1 и 2) показывают, что оптимумы параметров, обеспечивающих достижение поставленной цели, находятся в следующих областях: концентрации НСl 2-6 моль/л, продолжительности нагревания 1-4 ч, рН раствора для разделения (0,2)-(+0,7) в зависимости от природы платинового металла и металла основы сорбента.
П р и м е р 16. Обогащение коллективного концентрата Ru, Rh и Ir на основе гидроксокарбоната La, Ce, Pr. По примеру 2, 4, 7 рН раствора перед разделением (-0,2).
Ph Ru Ir Введено в концент- рат, мг 1,01 1,10 1,46 Найдено во фрон- тальном раство- ре, мг 1,02 1,07 1,38 Степень извлече- ния, 101 97,3 94,5
П р и м е р 17. Обогащение коллективного концентрата Pd, Pt, Ru, Ir на основе гидроксида железа (III) по примеру 11-15. рН раствора перед разделением (+0,5).
Pd Pt Rh Ru Ir Введено в концент- рат, мг 0,8 1,0 0,83 1,00 1,62 Найдено во фронта- льном раст- воре, мг 0,75 0,75 0,60 0,65 1,00 Степень извле- чения, 93,7 75 72,3 65 89,3
П р и м е р 18. Концентрирование суммы платиновых металлов из сульфидной медноникелевой руды.
70 г руды с содержанием платины, палладия и родия, г/т (по данным пробирного анализа) соответственно: 1,03, 4,0 и 0,13, вскрыто НF и HCl и переведено в солянокислый раствор без остатка (полное растворение). Объем раствора 0,635 л. Содержание цветных металлов, г/л: Fe 45,2; Cu 1,79; Ni 5,03; Al 0,25; Co 0,20. Концентрация НСl 4 моль/л. рН раствора при разделении +0,5. В конечном растворе, не содержащем цветных металлов (объем 50 мл) найдены количества платины, палладия и родия, соответствующие 1,44, 3,85 и 0,25 г/т соответственно.
Таким образом, предлагаемый способ, не снижая степени извлечения и чистоты продукта по сравнению с прототипом, позволяет снизить расход электроэнергии и исключить потери НСl, что имеет важное значение при крупномасштабных технологических процессах и улучшает их экологические показатели.
Процесс подготовки раствора к разделению и самого разделения протекает при атмосферном давлении, не требует сложного оборудования, дорогостоящих реагентов. Единственным отходом процесса является легко утилизируемый NaCl.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗВЛЕЧЕНИЯ И КОНЦЕНТРИРОВАНИЯ ТОРИЯ ИЗ ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ | 2001 |
|
RU2207393C1 |
| СПОСОБ ОТДЕЛЕНИЯ ПЛАТИНЫ (II, IV) И ПАЛЛАДИЯ (II) ОТ СЕРЕБРА (I), ЖЕЛЕЗА (III) И МЕДИ (II) В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 2019 |
|
RU2694855C1 |
| ИНДИКАТОРНЫЙ СОСТАВ ДЛЯ ОПРЕДЕЛЕНИЯ ЗОЛОТА (III) В ВОДНЫХ РАСТВОРАХ | 2004 |
|
RU2256909C1 |
| СПОСОБ СОРБЦИОННОГО ИЗВЛЕЧЕНИЯ И РАЗДЕЛЕНИЯ РОДИЯ И РУТЕНИЯ | 2014 |
|
RU2573853C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ПАЛЛАДИЯ (II) ИЗ ОТРАБОТАННЫХ КАТАЛИЗАТОРОВ | 2010 |
|
RU2442833C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МИКРОКОНЦЕНТРАЦИЙ СУРЬМЫ В ПРИРОДНЫХ ВОДАХ ДЛЯ ЭКОЛОГИЧЕСКОГО МОНИТОРИНГА АКВАТОРИЙ | 2003 |
|
RU2246107C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ПЛАТИНЫ (II, IV), МЕДИ (II) И ЦИНКА (II) В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 2016 |
|
RU2637547C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ПЛАТИНЫ И РОДИЯ В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 1999 |
|
RU2165992C1 |
| СПОСОБ РЕГЕНЕРАЦИИ КАТИОНООБМЕННОЙ СМОЛЫ, ИСПОЛЬЗУЕМОЙ ДЛЯ ОЧИСТКИ ЛИТИЙСОДЕРЖАЩЕГО РАСТВОРА ОТ ПРИМЕСЕЙ | 2024 |
|
RU2838517C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ПЛАТИНОВЫХ МЕТАЛЛОВ ИЗ ВТОРИЧНОГО СЫРЬЯ НА МИНЕРАЛЬНОЙ ОСНОВЕ | 1996 |
|
RU2089636C1 |

Использование: гидрометаллургия платиновых металлов, технология их концентрирования. Сущность изобретения: бедный концентрат платиновых металлов растворяют с переводом в солянокислый раствор 2 6 моль/л (HCl), выдерживают при температуре кипения 1 4 ч, охлаждают раствор до комнатной температуры, создают в нем рН (-0,2) (+0,7) и пропускают через колонку с катионитом для отделения катионов металлов основы (макрокомпонента). Положительный эффект: высокая степень извлечения платиновых металлов со значительным повышением их чистоты. 2 табл.
СПОСОБ ПЕРЕРАБОТКИ БЕДНЫХ КОНЦЕНТРАТОВ ПЛАТИНОВЫХ МЕТАЛЛОВ, включающий химическое растворение концентрата с переводом в солянокислый раствор и разделение компонентов раствора путем пропускания его через катионообменную смолу, отличающийся тем, что обработку ведут до создания концентрации соляной кислоты в растворе 2 6 моль/л с последующим доведением раствора до кипения с последующей выдержкой его при температуре кипения в течение 1 4 ч, охлаждением и установлением рН раствора (-0,2) (+0,7) перед пропусканием раствора через катионообменную смолу.
| Гинзбург С.И | |||
| и др | |||
| Аналитическая химия платиновых металлов | |||
| М.: Наука, 1965, с.257-258. |
Авторы
Даты
1995-08-09—Публикация
1991-05-20—Подача