Изобретение относится к иммуноанализу, а именно к иммунофлуоресцентным методам анализа с временным разрешением.
Цель изобретения повышение чувствительности способа.
Способ осуществляют следующим образом. В качестве меток используют комплексы лантанидов с хелатами общей формулы I или II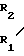 N
N  N
N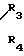 (I)
(I) 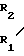 N
N (II) где один из R1-R4-CH2COOH, а остальные три СН2СООН или
(II) где один из R1-R4-CH2COOH, а остальные три СН2СООН или
CH2-COO-NH CO-CH2-CO-CF3 или общей формулы III
CO-CH2-CO-CF3 или общей формулы III N
N  N
N (III) где один из R1-R6-СН2СООН, а остальные четыре СН2СООН или
(III) где один из R1-R6-СН2СООН, а остальные четыре СН2СООН или
CH2-COO-NH CO-CH2-CO-CF3 при этом комплекс обязательно содержит по крайней мере один заместитель
CO-CH2-CO-CF3 при этом комплекс обязательно содержит по крайней мере один заместитель
CH2-COO-NH CO-CH2-CO-CF3
CO-CH2-CO-CF3
Флуоресцентные выходы данных хелатных комплексов с европием равны 106-2,4x x107.
Способ может быть осуществлен в любых вариантах твердофазного анализа, описанных для радиоизотопных, ферментных и флуоресцентных маркеров, а также в гомогенных методах, основанных на тушении и возгорании флуоресценции при связывании меченого соединения. Способ применим к любым соединениям, для которых возможно получение неспецифических антител и с которыми возможно ковалентное связывание маркера (например, поли- и моноклональные антитела, анти-антитела, различные антигены, гормоны, лекарства, вирусные частицы, бактерии, белки, опухолевые маркеры, пептиды, белок А стафилококка).
П р и м е р 1. Синтез 4-аминобензоилтрифторацетона гидрохлорида (АБТФА) (IV).
АБТФА (IV) получают из 4-аминобензофенона (1) в три стадии
CH3- NH2__→ CH3-
NH2__→ CH3-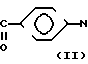 H-
H- H __→
H __→
__→ CF3- H-
H- H __→ CF3-
H __→ CF3- -
-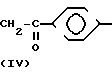 NH2·HCl
NH2·HCl
Cтадия I. К уксусномуравьиному ангидриду, полученному из 7,1 мл (75 ммоль) уксусного ангидрида и 7,1 мл (183 ммоль) 98%-ной муравьиной кислоты, при 0-2оС и перемешивании добавляют в течение 10 мин раствор 6,75 г (50 ммоль) 4-аминобензофенона в 10 мл 98%-ной муравьиной кислоты, полученную смесь перемешивают 1 ч при 60оС. После охлаждения до комнатной температуры добавляют 7,2 мл воды и смесь упаривают досуха на роторном испарителе при 70-80оС. Остаток растворяют в 100 мл хлороформа и промывают последовательно 5% -ной соляной кислотой, водой, 5%-ным карбонатом натрия, сушат над сульфатом магния и упаривают досуха. Твердый остаток перекристаллизовывают из бензола и сушат над фосфорным ангидридом в вакуум-эксикаторе. Получают 4-формиламиноацетофенол (II) в виде белых игольчатых кристаллов с т.пл. 105-106оС (из бензола). Выход 6,99 г (85,7% от теоретического).
Стадия II. К суспензии 1,13 г (21 ммоль) метилата натрия в 40 мл сухого диметилформамида (ДМФА) при перемешивании при 2-5оС добавляют 4,92 г этилового эфира трифторуксусной кислоты (40 ммоль), а затем в течение 10 мин раствор 3,26 г (20 ммоль) 4-формиламиноацетофенола в 20 мл сухого ДМФА. Смесь дополнительно перемешивают 4 ч при комнатной температуре, добавляют 2,28 мл (40 ммоль) уксусной кислоты и упаривают в вакууме на роторном испарителе. Остаток растворяют в 400 мл хлороформа, промывают водой, сушат над сульфатом магния и упаривают досуха. Остаток перекристаллизовывают из бензола с обработкой активированным углем. После высушивания над фосфорным ангидридом получают 3,1 г (60% от теоретического) 4-формиламинобензоилтрифторацетона (III) в виде желтых игольчатых кристаллов с т.пл. 151,5-152,5оС (из бензола).
Стадия III. Смесь 0,52 (2 ммоль) 4-формиламинобензоилтрифторацетона. 8 мл сухого этанола и 0,8 мл концентрированной соляной кислоты греют на кипящей водяной бане 1,5 ч. Затем упаривают досуха на роторном испарителе и сушат в вакууме над фосфорным ангидридом. Получают 0,49 г (92,5% от теоретического) АБТФА в виде желтых мелких кристаллов.
Синтез конъюгата иммуноглобулин мыши 4-аминобензоилтрифторацетон-диэтилентриаминпентауксусная кислота (lgG-АБТФА-ДТПА).
К раствору 10 мг ДТПА в 10 мкл диметилсульфоксида добавляют 4 мкл триэтиламина, а затем при перемешивании по каплям 10 мкл раствора, содержащего 9 мг АБТФА в диметилсульфоксиде и оставляют на 1 ч при комнатной температуре. 10 мкл реакционной смеси добавляют к 200 мкл 0,1 М бикарбонатного буфера (рН 8,5), содержащего 10 мг/мл lgG и оставляют на ночь при 4оС. Очистку конъюгата проводят методом гельфильтрации с использованием колонки 1,5х20 см с носителем Sephadex G-50, собирая фракции белкового пика.
Соотношение lgG/АБТФА, которое определяли по поглощению на длинах волн 280 и 330 нм соответственно, было равно 1/5.
Измерение относительного флуоресцентного выхода лантанидного комплекса.
Относительный флуорецентный выход определяют по формуле
Φотн=  где Iche, Iи интенсивность флуоресценции; Cche, Cεи концентрации; Kche, Kεи константы затухания флуоресценции хелатированного и нехелатированного европия соответственно.
где Iche, Iи интенсивность флуоресценции; Cche, Cεи концентрации; Kche, Kεи константы затухания флуоресценции хелатированного и нехелатированного европия соответственно.
Для определения относительного флуоресцентного выхода европиевого хелата с LgG-АБТФА-ДТПА смешивают в эквимолярном соотношении 10-5 М растворы хлорида европия и lgG-АБТФА-ДТПА в 50 мМ трисгидроксилметиламинометан-НСl (рН 6,6) с 0,15 М NaCl и 0,02% тритона Х-100 и 10-5 М триоктилфосфиноксида. Интенсивность флуоресценции европия измеряют на импульсном люминесцентном спектрометре LS-50 (Perkin Elmer) с временным разрешением на длине волны 615 нм и для свободного, и для хелатированного европия. Длина волны возбуждения для нехелатированного европия 395 нм и для хелата с lgG-АБТФА-ДТПА 330 нм.
Относительный флуоресцентный выход для lgG-АБТФА-ДТПА равен 2˙106.
Проведение конкурентного твердофазного иммуноанализа lgG мыши по измерению остаточного флуоресцентного сигнала в растворе.
5 нг меченых lgG мыши инкубируют в лунках полистирольных стрипов (Eflab, Finkand), покрытых 10 мкг/lgG кролика против мыши, вместе со стандартными растворами, содержащими 0-4000 нг/мл lgG мыши в 0,2 мл буфера для проведения анализа (LKB, Wallac), 0,2% бычьего сывороточного альбумина (BSA) при 37оС в течение 2 ч. Остаточный флуоресцентный сигнал измеряют флуоресцентным спектрометром с временным разрешением. Возбуждение проводят азотным лазером (337 нм) с частотой 50 Гц и полушириной 10 нс. Сигнал измеряют на длине волны 613 нм в режиме счета фотонов в течение 10 с. Время задержки 300 мкс, счет импульсов 1 мс.
П р и м е р 2. "Сэндвич" флуоресцентный иммуноанализ иммуноглобулина человека по измерению остаточного флуоресцентного сигнала в растворе.
lgG кролика против человека метят европиевым комплексом по методике, описанной выше для lgG мыши. Анализ проводят после инкубации стандартных растворов lgG человека (0-4000 нг/мл) в лунках полистирольных стрипов, покрытых lgG кролика против человека (10 мкг/мл), путем добавления 1 нг/мл коньюгата lgG кролика против человека, меченного европием, в буфере для анализа (LKB, Wallac) в течение 2 ч при 37оС.
П р и м е р 3. Способ осуществляют согласно примеру 1, но вместо lgG-АБТФА-ДТПА используют lgG-АБТФА-этилендиаминтетрауксусную кислоту (lgG-АБТФА-ЭДТА). Соотношение АБТФА/lgG составляет 3/1. Относительный флуоресцентный выход 1,06 ˙106.
П р и м е р 4. Способ осуществляют согласно примеру 1, но вместо lgG-АБТФА-ДТПА используют lgG-АБТФА 1,2-диаминоциклогексан N,N,N', N'-тетрауксусную кислоту. Соотношение АБТФА/lgG равно 5/1. Относительный флуоресцентный выход 1,1˙106.
П р и м е р 5. Способ осуществляют согласно примеру 1, но вместо lgG-АБТФА-ДТПА используют lgG-АБТФА-оксисукцинимидный эфир диэтилентриаминпентауксусной кислоты (lgG-АБТФА-ПСЭДТПА), в котором соотношение АБТФА/ПСЭДТПА составляет 1/1. Соотношение АБТФА/lgG равно 5/1. Относительный флуоресцентный выход 2˙106.
П р и м е р 6. Способ осуществляют согласно примеру 1, но вместо lgG-АБТФА-ДТПА используют lgG-АБТФА-ПСЭДТПА, где соотношение АБТФА/ПСЭДТПА составляет 2/1. Соотношение АБТФА/lgG равно 6/1. Относительный флуоресцентный выход 3,2˙106.
П р и м е р 7. Способ осуществляют согласно примеру 1, но вместо lgG-АБТФА-ДТПА используют lgG-АБТФА-ПСЭДТПА, где соотношение АБТФА/ПСЭДТПА составляет 3/1. Соотношение АБТФА/lgG равно 8/1. Относительный флуоресцентный выход 4,2x x106.
П р и м е р 8. Способ осуществляют согласно примеру 1, но вместо lgG-АБТФА-ДТПА используют lgG-АБТФА-ПСЭДТПА, соотношение АБТФА/ПСЭДТПА составляет 4/1. Соотношение АБТФА/lgG равно 8. Относительный флуоресцентный выход 2,4x x107.
Таким образом, описанный способ позволяет повысить чувствительность определения антигенов или антител за счет использования соединений с высоким относительным флуоресцентным выходом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПАРАФЕНИЛБЕНЗОИЛГЕПТАФТОРБУТИРОИЛМЕТАН В КАЧЕСТВЕ РЕАГЕНТА ДЛЯ ФЛУОРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ МАЛЫХ КОЛИЧЕСТВ ЕВРОПИЯ | 1992 |
|
RU2034824C1 |
| КОМПЛЕКСООБРАЗУЮЩИЕ БЕНЗОСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ β-ДИКАРБОНИЛЬНЫЙ ЗАМЕСТИТЕЛЬ С ФТОРИРОВАННЫМИ РАДИКАЛАМИ | 2007 |
|
RU2373200C2 |
| КОМПЛЕКСООБРАЗУЮЩИЕ ДИБЕНЗОСОДЕРЖАЩИЕ ПЯТИЧЛЕННЫЕ ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ДВА СИММЕТРИЧНЫХ БЕТА-ДИКАРБОНИЛЬНЫХ ЗАМЕСТИТЕЛЯ С ФТОРИРОВАННЫМИ РАДИКАЛАМИ | 2005 |
|
RU2296756C2 |
| РАДИОАКТИВНЫЙ ИММУНОРЕАГЕНТ НАПРАВЛЕННОГО ДЕЙСТВИЯ, КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ИЗОБРАЖЕНИЯ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ В ОРГАНИЗМЕ, СПОСОБ ПОЛУЧЕНИЯ ИЗОБРАЖЕНИЯ И КОМПЛЕКСООБРАЗУЮЩИЙ АГЕНТ | 1992 |
|
RU2122431C1 |
| Способ проведения иммуноанализа | 1988 |
|
SU1617381A1 |
| КРИПТАТЫ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ В КАЧЕСТВЕ ФЛУОРЕСЦЕНТНЫХ МАРКЕРОВ БИОЛОГИЧЕСКИХ МОЛЕКУЛ | 1988 |
|
RU2074859C1 |
| КРАСИТЕЛИ НА ОСНОВЕ ДИФТОРИДА ДИПИРРОМЕТЕНБОРА С ДВУХФОТОННЫМ ПОГЛОЩЕНИЕМ И ИХ ПРИМЕНЕНИЕ | 2002 |
|
RU2296333C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ АЛЛЕРГЕНОВ | 1991 |
|
SU1824738A1 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2010 |
|
RU2581367C2 |
| Флуоресцентно-меченые дезоксиуридинтрифосфаты | 2016 |
|
RU2637310C1 |
Изобретение относится к методам проведения иммуноанализа и может быть использовано в медицине, сельском хозяйстве и других областях для определения антигенов, антител или следовых количеств биологически активных соединений. Цель изобретения повышение чувствительности способа. Это обеспечивается использованием специфических хелатирующих агентов, обладающих высокими относительными флуоресцентными выходами.
СПОСОБ ОПРЕДЕЛЕНИЯ АНТИГЕНОВ ИЛИ АНТИТЕЛ, предусматривающий инкубацию иммуносорбента с анализируемыми пробами, добавление коньюгата антигена или антитела с комплексом лантанида и хелатного соединения, отличающийся тем, что, с целью повышения его чувствительности, в качестве хелатного соединения используют соединение общей формулы I или II

где один из R1 R4 CH2COOH,
а остальные три -CH2COOH или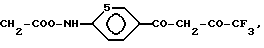
или общей формулы III
где один из R1 R5 CH2COOH,
а остальные четыре -CH2COOH
при этом комплекс содержит по крайней мере один заместитель
| Najafi A., Childs R.L., Hnatovich D.F | |||
| Coupling antibody with DTRA -Au Alternative to the Cyclic Anhydride, int | |||
| G.Appl | |||
| Radiat | |||
| lsotor, 1984, v.35, N 6, p.554-557. |
Авторы
Даты
1995-07-25—Публикация
1989-09-28—Подача