Известно получение γ-полинитрокарбоновых кислот путем присоединения нитроформа к α,β-ненасыщенным кислотам.
Однако получить этим способом α-хлор-γ-полинитрокарбоновые кислоты не удается. Это объясняется уменьшением поляризации двойной связи за счет введения хлора в α-положение к карбоксильной группе.
Авторами предлагается принципиально новый метод получения первого представителя этого ряда по следующей схеме:
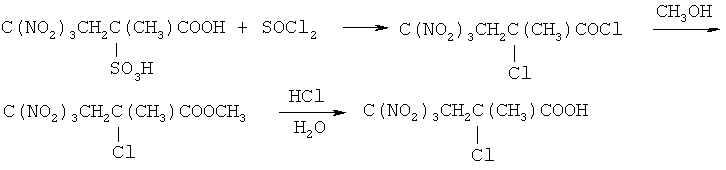
В первой стадии при кипячении исходной α-сульфо-α-метил-γ,γ,γ-тринитромасляной кислоты в хлористом тиониле происходит замещение сульфогруппы на хлор.
В результате реакции образуется хлорангидрид α-метил-α-хлор-γ,γ,γ-тринитромасляной кислоты. Избыток хлористого тионила легко может быть регенерирован путем его отгонки.
Выделение хлорангидрида является процессом опасным и связано с его разложением. В результате выход целевой кислоты (в расчете на α-сульфокислоту) и ее качество резко снижается. Избежать этого можно путем получения из неочищенного хлорангидрида эфира (метилового или этилового), с последующей его очисткой и омылением соляной кислотой.
Пример
Получение эфира
В колбу с обратным холодильником, мешалкой и термометром заливают 119 г (1 моль) свежеперегонного хлористого тионила, и при хорошем перемешивании присыпают 15,85 г (0,05 моля) α-сульфо-α-метил-γ,γ,γ-тринитромасляной кислоты. Реакция протекает бурно с выделением HCl.
Затем реакционную массу нагревают в течение 6 часов при температуре кипения хлористого тионила, после чего хлористый тионил отгоняют. Оставшееся масло растворяют в 150 мл метилового спирта и смесь кипятят в течение 20 часов. По истечении времени выдержки содержимое охлаждают, 2/3 спирта отгоняют, а оставшуюся массу выливают на лед. Выпадает кристаллический осадок, который отфильтровывают, промывают и перекристаллизовывают из этанола. Выход 6,77 г. (47,5%, считая на сульфокислоту).
Температура плавления 71,1°-72,5°C.
Анализ:
Найдено, %: С=25,57; Н=2,90; N=14,70; Cl=12,58
Вычислено C H O C, %: C=25,12; Н=3,14; N=14,65; Cl=12,42
ИК-спектр содержит полосы поглощения тринитрометильной (1593, 1622, 1309, 840 см-1) карбонильной (1173, 1276 см-1) групп и сложноэфирного кислорода (1728 см-1).
Омыление эфира
Полученный метиловый эфир α-метил-α-хлор-γ,γ,γ-тринитромасляной кислоты помещают в колбу с обратным холодильником и мешалкой и заливают сюда же 200 мл соляной кислоты. Массу греют при перемешивании на кипящей водяной бане в течение 6 часов. После чего массу охлаждают и отфильтровывают от неомыленного эфира, а соляную кислоту упаривают под вакуумом водоструйного насоса. В колбе остается α-метил-α-хлор-γ,γ,γ-тринитромасляная кислота. Ее извлекают, промывают водой и сушат. Оставшийся эфир снова заливают соляной кислотой и омыляют. Так повторяют до полного омыления эфира. Подобные операции необходимы для уменьшения потерь за счет декарбоксилирования кислоты. Суммарный выход 4,51 г (70% в пересчете на исходный эфир). В результате омыления получается достаточно чистая кислота с Тпл.=115,7-116,3°C. Перекристаллизация из CCl4 дает Тпл.=119°.
Формула: 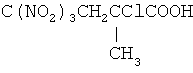 ;
;
Брутто формула: C5H6O8N3Cl;
Анализ: Найдено, %: С=22,71; Н=2,43; N=15,64; Cl=12,61;
Вычислено для C5H6O8N3Cl, %: С=22,10; Н=2,21, N=15,47; Cl=13,07
ИК-спектр содержит полосы поглощения: 1596, 1304, 810 см-1 группа - C(NO2)3; 1715, 1737 см-1 - карбонильная группа.
Титрование в водной среде показало содержание основного вещества 100%. Полученная кислота, а также, получаемые в качестве промежуточных продуктов, эфиры могут быть использованы в следующих областях:
а) как полупродукты в синтезе НМВВ и компонентов ТРТ (при этом могут быть использованы реакционная способность как карбоксильной группы, так и нитрогрупп).
б) в качестве биологически активных веществ и в синтезе фармацевтических препаратов.
Изобретение относится к способу получения α-метил-α-хлор-γ,γ,γ-тринитромасляной кислоты. Способ заключается в том, что α-сульфо-α-метил-γ,γ,γ-тринитромасляную кислоту подвергают взаимодействию с избытком хлористого тионила с последующей обработкой полученного продукта избытком спирта при температуре его кипения и омылением образовавшегося эфира соляной кислотой при t=95-100°C. Предлагаемый способ позволяет получать α-метил-α-хлор-γ,γ,γ-тринитромасляную кислоту с хорошим выходом. Данная кислота может найти применение в качестве полупродукта в органическом синтезе, в том числе биологически активных веществ и фармацевтических препаратов. 1 пр.
Способ получения α-метил-α-хлор-γ,γ,γ-тринитромасляной кислоты, отличающийся тем, что сульфо-α-метил-γ,γ,γ-тринитромасляную кислоту подвергают взаимодействию с избытком хлористого тионила с последующей обработкой полученного продукта избытком спирта при температуре его кипения и омылением образовавшегося эфира соляной кислотой при t=95÷100°C.
Авторы
Даты
2016-06-10—Публикация
1966-12-01—Подача