Предлагаемый способ получения водорода путем разложения воды при помощи щелочно земельных металлов: кальция, стронция и бария состоит в том, что разложение ведется в присутствии растворимой в воде галоидной соли соответственного металла. Изобретение позволяет получать указанные металлы с активированной поверхностью, поскольку действие раствора на металл прекращается ранее полного израсходования металла и может быть применено также и к магнию.
Разложение воды щелочно-земельными металлами достигается на практике лишь в весьма незначительной степени, повидимому, вследствие образования на металле поверхностных слоев, затрудняющих дальнейшее разложение воды металлом. Если вместо воды применять разбавленные кислоты, то реакция протекает необычайно бурно и быстро, что затрудняет контроль расходования металла.
При действии кальция на водный раствор сахара выделяется, как известно, водород, причем сахар действует в качестве восстановителя, однако, скорость реакции при этом незначительна. Магний также реагирует с водою, но крайне медленно, при введении металлического магния в раствор MgClo количество образующегося водорода более значительно, нежели при взаимодействии металлического магния с чистой водой.
Автор установил, что водород энергично выделяется, если ввести какойлибо из щелочно-земельных металлов- кальций, стронций, барий в водный раствор галоидной соли того же самого металла.
Количество выделяющегося при этом водорода во много раз превосходит количество газа, получаемого при прочих равных условиях и в течение того же времени при помощи других известных способов воздействия металлов на растворы.
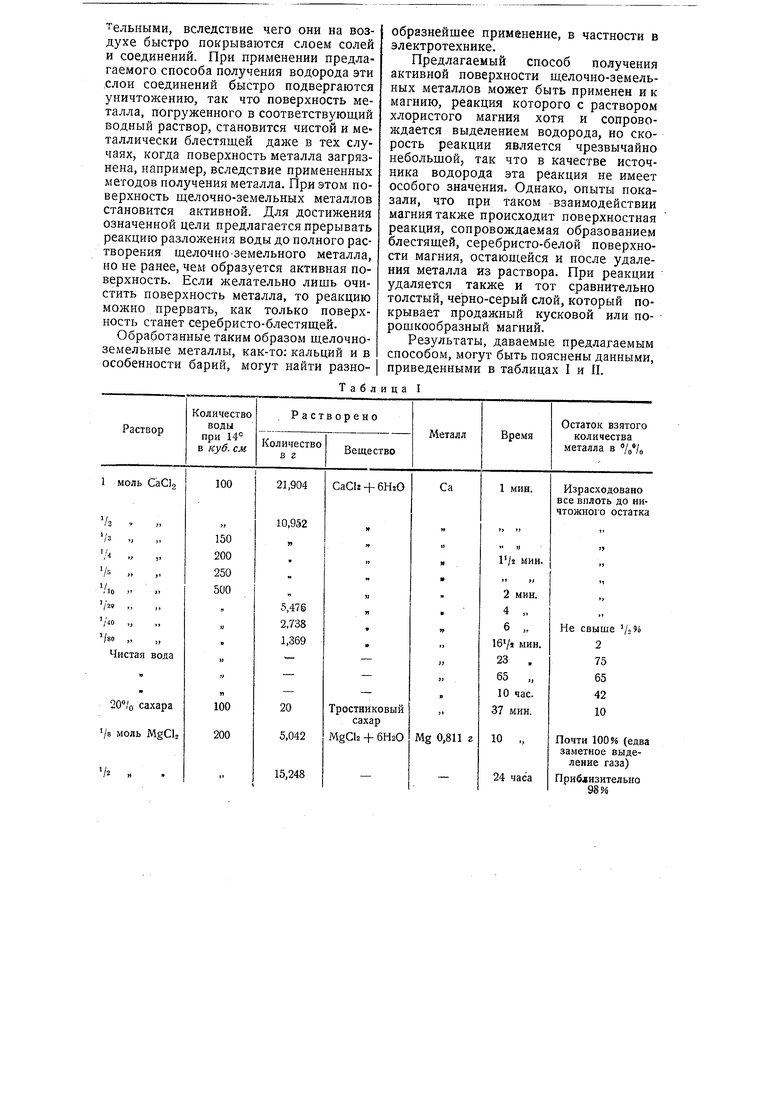
Опыты показали, что например при введении металлического кальция в раствор (1 моль) хлористого кальция, весь металл оказывается израсходованным уже через 1 минуту, так что остается лищь ничтожный остаток, причем выделяется соответствующее количество водорода. Если же вместо кристаллического хлористого кальция растворить в воде то же самое весовое количество тростникового сахара, то через 30 минут все еще остается неизрасходованным 10 % первоначального количества металла. Изменяя концентрацию раствора металлической соли, можно регулировать в щироких пределах скорость реакции.
Щелочно-земельные металлы являются в высокой степени электроположиТельными, вследствие чего они на воздухе быстро покрываются слоем солей и соединений. При применении предлагаемого способа получения водорода эти .слои соединений быстро подвергаются уничтожению, так что поверхность металла, погруженного в соответствующий водный раствор, становится чистой и металлически блестящей даже в тех случаях, когда поверхность металла загрязнена, например, вследствие примененных методов получения металла. При этом поверхность щелочно-земельных металлов становится активной. Для достижения означенной цели предлагается прерывать реакцию разложения воды до полного растворения щелочно-земельного металла, но не ранее, чем образуется активная поверхность. Если желательно лишь очистить поверхность металла, то реакцию можно прервать, как только поверхность станет серебристо-блестящей.
Обработанные таким образом щелочноземельные металлы, как-то: кальций и в особенности барий, могут найти разноТ а б
образнейшее применение, в частности в электротехнике.
Предлагаемый способ получения активной поверхности щелочно-земельных металлов может быть применен и к магнию, реакция которого с раствором хлористого магния хотя и сопровождается выделением водорода, но скорость реакции является чрезвычайно небольщой, так что в качестве источника водорода эта реакция не имеет особого значения. Однако, опыты показали, что при таком взаимодействии магния также происходит поверхностная реакция, сопровождаемая образованием блестящей, серебристо-белой поверхности магния, остающейся и после удаления металла из раствора. При реакции удаляется также и тот сравнительно толстый, черно-серый слой, который покрывает продажный кусковой или порошкообразный магний.
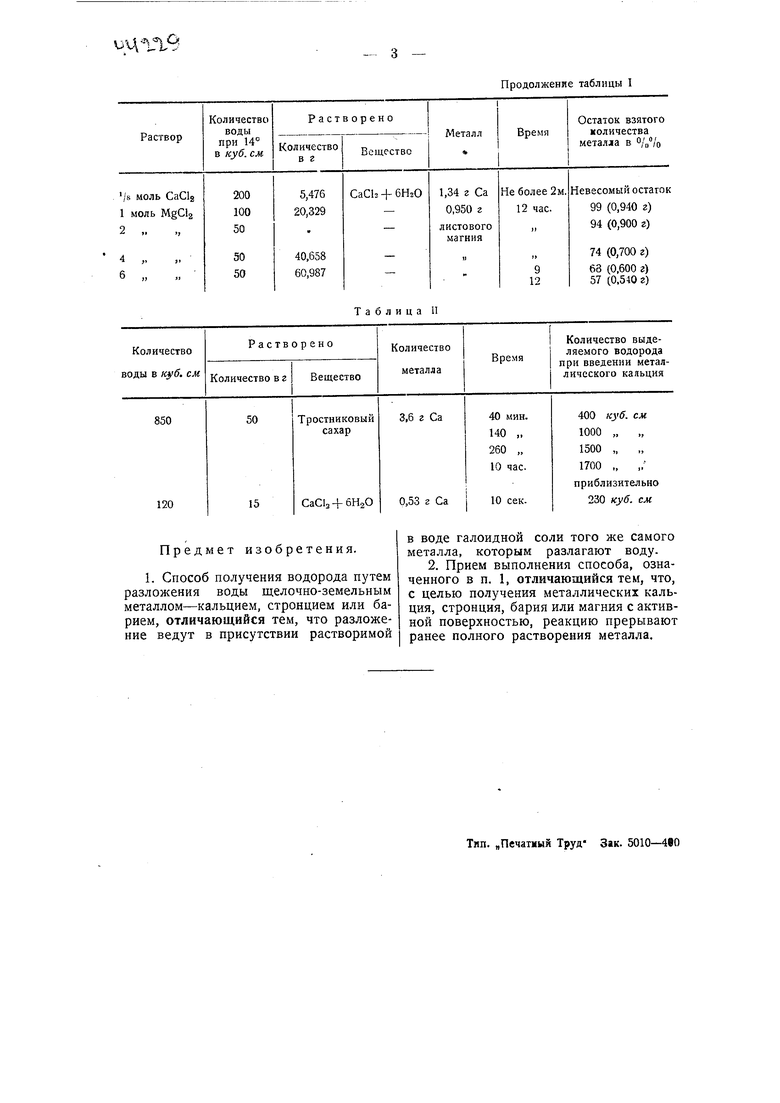
Результаты, даваемые предлагаемым способом, могут быть пояснены данными, приведенными в таблицах I и II,
и ц а I
Продолжение таблицы I
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ УДАЛЕНИЯ СОЛЕЙ ИЗ САХАРНОЙ ПАТОКИ | 1927 |
|
SU38584A1 |
| СПОСОБ КАТАЛИТИЧЕСКОГО ЭПОКСИДИРОВАНИЯ | 2013 |
|
RU2614409C2 |
| Способ получения дианамидов щелочно-земельных металлов или магния | 1927 |
|
SU33032A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРАТОВ ХЛОРИДОВ ЩЕЛОЧНО-ЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 2006 |
|
RU2338689C2 |
| СПОСОБ ПОЛУЧЕНИЯ СПЛАВОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2528919C2 |
| ПРОИЗВОДНЫЕ САХАРИНКАРБОНОВОЙ КИСЛОТЫ И ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1995 |
|
RU2154640C2 |
| Способ гидрогенизации непредельных органических соединений, нитросоединений и фенолов, а также дегидрогенизации гидрированных фенолов | 1927 |
|
SU13214A1 |
| СПОСОБ ПОЛУЧЕНИЯ КАЛЬЦИЙ- ИЛИ МАГНИЙ-ЦИАНАМИДА ИЛИ ИХ СМЕСЕЙ | 1927 |
|
SU38527A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АЛКОКСИАЛКОКСИДОВ ЩЕЛОЧНОЗЕМЕЛЬНЫХ ИЛИ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 1992 |
|
RU2049769C1 |
| Катализатор для конверсии углеводородов | 1990 |
|
SU1780831A1 |

Предмет изобретения.
Таблица II
в воде галоидной соли того же самого металла, которым разлагают воду.

Авторы
Даты
1935-09-30—Публикация
1933-10-03—Подача